方案详情文
智能文字提取功能测试中
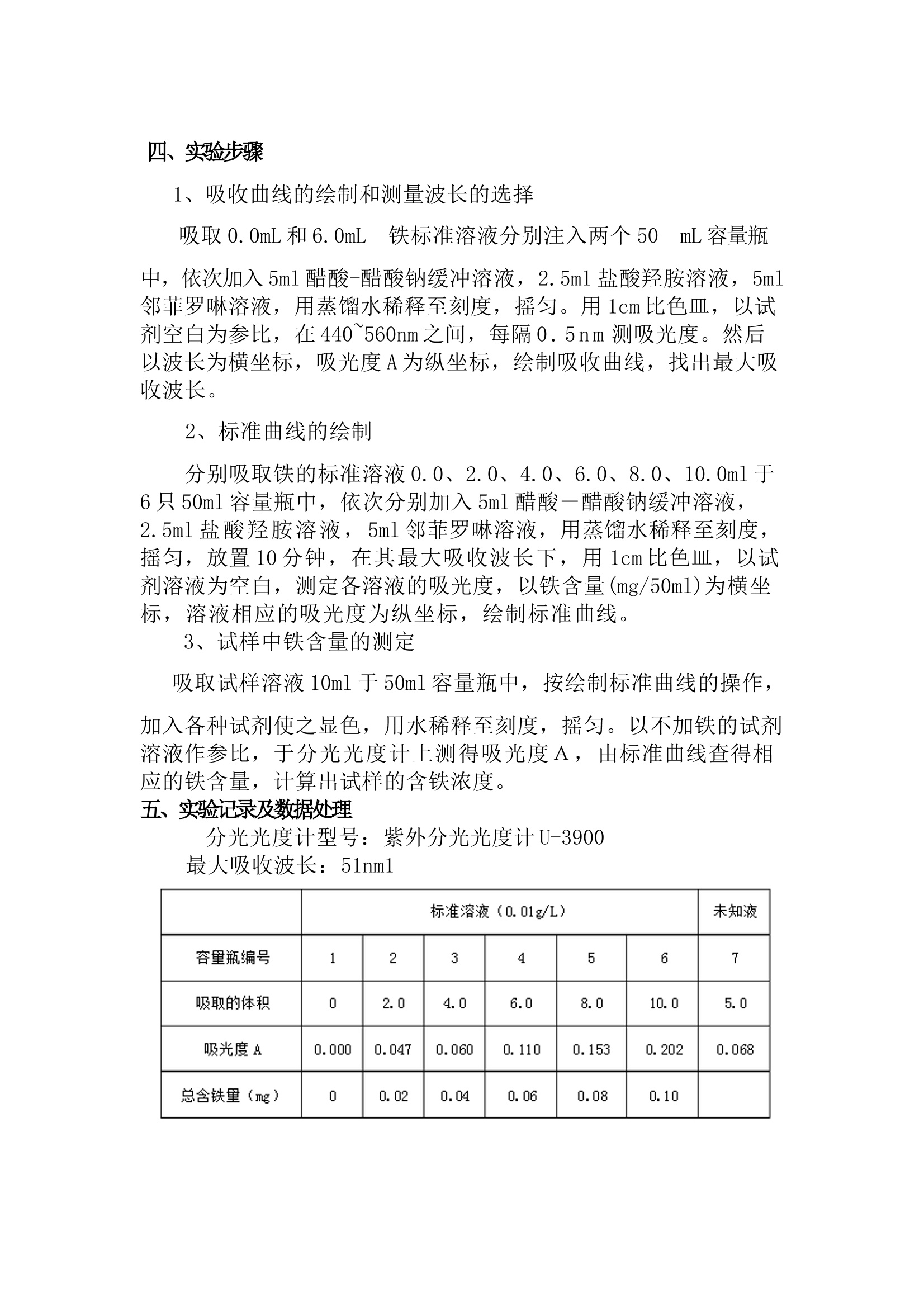
紫外分光光度法测定铁的含量 一、实验目的 1.了解朗伯-比尔定律的应用,掌握分光光度法测定铁的含量的原理; 2.了解紫外分光光度计U-3900的构造; 3.掌握紫外分光光度计U-3900的正确使用; 4.学会吸收曲线的绘制和样品的测定原理。 实验原理 邻菲啰啉是测定微量铁的较好试剂。在pH=2~9 的条件下,邻菲啰啉与Fe2+生成稳定的橙红色配合物,其lgK形=21.3,摩尔吸光系数ε510 = 1.1×104,其反应式如下: 本方法的选择性很高,相当于含铁量40倍的Sn2+、Al3+、Ca2+、Mg2+、Zn2+、SiO32-,20倍Cr3+、Mn2+、V(V)、PO43-,5倍Co2+、Cu2+等均不干扰测定。 显色前首先用盐酸羟胺把Fe3+还原为Fe2+。 4 Fe3+ + 2NH2OH = 4 Fe2+ + N2O + H2O + 4H+ 仪器及试剂 1、紫外分光光度计U-3900; 2、铁标准溶液:含铁0.01mg/mL; 3、0.1%邻菲罗啉水溶液; 4、1%盐酸羟胺水溶液; 5、醋酸-醋酸钠缓冲溶液(pH4.6)。 四、实验步骤 1、吸收曲线的绘制和测量波长的选择 吸取0.0mL和6.0mL 铁标准溶液分别注入两个50 mL容量瓶中,依次加入5ml醋酸-醋酸钠缓冲溶液,2.5ml盐酸羟胺溶液,5ml邻菲罗啉溶液,用蒸馏水稀释至刻度,摇匀。用1cm比色皿,以试剂空白为参比,在440~560nm之间,每隔0.5nm测吸光度。然后以波长为横坐标,吸光度A为纵坐标,绘制吸收曲线,找出最大吸收波长。 2、标准曲线的绘制 分别吸取铁的标准溶液0.0、2.0、4.0、6.0、8.0、10.0ml于6只50ml容量瓶中,依次分别加入5ml醋酸-醋酸钠缓冲溶液,2.5ml盐酸羟胺溶液,5ml邻菲罗啉溶液,用蒸馏水稀释至刻度,摇匀,放置10分钟,在其最大吸收波长下,用1cm比色皿,以试剂溶液为空白,测定各溶液的吸光度,以铁含量(mg/50ml)为横坐标,溶液相应的吸光度为纵坐标,绘制标准曲线。 3、试样中铁含量的测定 吸取试样溶液10ml于50ml容量瓶中,按绘制标准曲线的操作,加入各种试剂使之显色,用水稀释至刻度,摇匀。以不加铁的试剂溶液作参比,于分光光度计上测得吸光度A,由标准曲线查得相应的铁含量,计算出试样的含铁浓度。 五、实验记录及数据处理 分光光度计型号:紫外分光光度计U-3900 最大吸收波长:51nm1 1、绘制邻菲啰啉铁标准曲线图 2、拟合得的邻菲啰啉铁准曲线方程为y=1.9686x-0.0031,x=(y+0.0031)/1.9686=(0.068+0.0031)/1.9686=0.036(mg/ml),则铁的浓度为0.036(mg/ml)。 邻二氮菲(1,10—邻二氮杂菲)是一种有机配位剂,可与Fe2+形成红色配位离子在pH=3~9范围内,该反应能够迅速完成,生成的红色配位离子在510nm波长附近有一吸收峰,摩尔吸收系数为1.1×104,反应十分灵敏,Fe2+ 浓度与吸光度符合光吸收定律,适合于微量铁的测定。实验中,采用pH=4.5-5的缓冲溶液保持标准系列溶液及样品溶液的酸度;采用盐酸羟胺还原标准储备液及样品溶液中的Fe3+并防止测定过程中Fe2+被空气氧化。
关闭-
1/3

-
2/3
还剩1页未读,是否继续阅读?
继续免费阅读全文产品配置单
山东班纳国际贸易有限公司为您提供《铁标准溶液中重金属检测方案(紫外分光光度)》,该方案主要用于环境水(除海水)中(类)金属及其化合物检测,参考标准《暂无》,《铁标准溶液中重金属检测方案(紫外分光光度)》用到的仪器有null。
我要纠错
相关方案


 咨询
咨询




