C/PTFE 气体扩散电极中电合成过氧化氢检测方案(电化学工作站)
检测样品 其他
检测项目 电合成过氧化氢
方案详情文
智能文字提取功能测试中
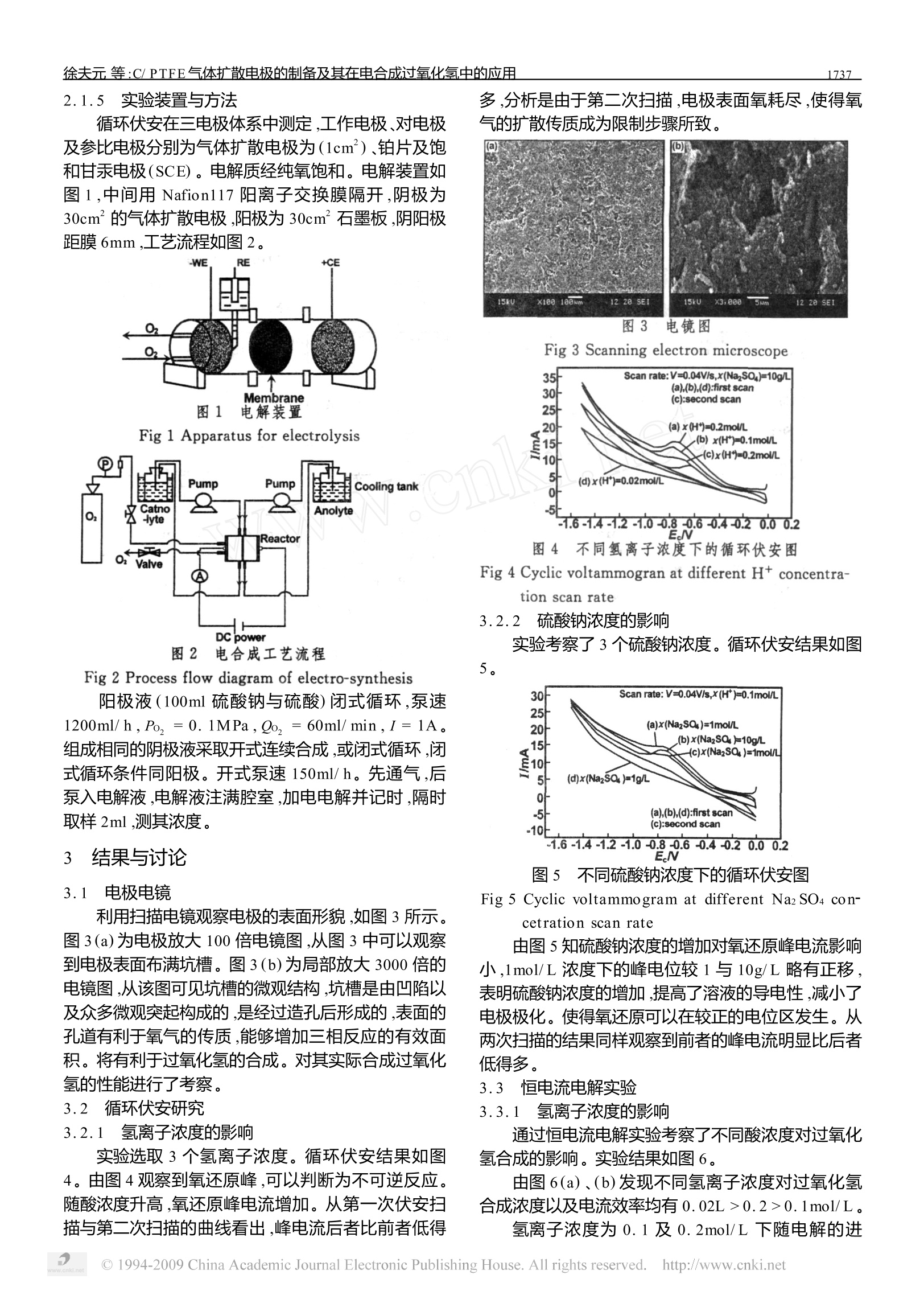
功 能 材 料2008年第10期(39)卷1736 徐夫元等:C/PTFE气体扩散电极的制备及其在电合成过氧化氢中的应用1737 C/PTFE气体扩散电极的制备及其在电合成过氧化氢中的应用 徐夫元,李 星,祝社民,陈英文,宋天顺,沈树宝 (1.南京工业大学国家生化工程技术研究中心,江苏南京210009; 2.南京工业大学材料科学与工程学院,江苏南京210009) 摘 要: 制备了C/PTFE气体扩散电极,在隔膜式反应器中考察了该电极还原氧气合成过氧化氢的性能。通过循环伏安及恒电流电解实验考察了氢离子浓度、硫酸钠浓度对氧还原合成过氧化氢的影响。实验发现,电解液pH急剧上升,导致氧还原机理转变,利于过氧化氢的合成;而过氧化氢的积累对其合成不利。通过开式连续电解获得较高电流效率(>80%)、过氧化氢浓度(>0.3%)及稳定pH值。隔膜能够有效降低阴极产物在阳极的氧化损失。 关键词: 过氧化氢;气体扩散电极:隔膜式反应器:电流效率 文章编号:1001-9731(2008)10-1736-04 引 言 过氧化氢是一种重要的无机化工产品。能无选择地将有机污染物氧化为二氧化碳和水,无二次污染,是公认的高效、绿色、环保的水处理剂,常与臭氧、紫外线等技术联用处理废水1~3。然而,过氧化氢在高温和有杂质存在下易分解,高浓度时易爆炸,传统蒽醌法合成过氧化氢工艺复杂,有氢氧爆炸的隐患,产物杂质多,后步分离难,生产成本高。在线电合成适宜浓度的过氧化氢能很好地解决上述问题,可更安全、方便地为水处理等浓度需求低的应用行业提供廉价的过氧化氢。 国内外对碱性过氧化氢的电合成研究较多14~8]并已有工业化生产及应用的报道。但对需在酸性条件下应用过氧化氢的情况如废水处理中的芬顿氧化19,10]等,还需要耗费大量的酸去调节pH,从而增加了成本和不便。因而探索酸性条件下高效、经济在线电合成过氧化氢的新工艺则具有良好的市场应用前景。 酸性下会发生析氢副反应而导致过氧化氢的电流效率低。国外有报道在电解液中加入蒽醌等物质11,12]来提高氧还原的电流效率,但引入有机物后会带来二次污染。国内对酸性过氧化氢电合成的研究则报道较少13]。目前,酸性条件下过氧化氢的电合成普遍存在浓度低、电流效率不高的缺点。为此,本文借鉴了燃料电池反应器的结构,通过制备新型气体扩散电极,探索 隔膜式反应器中酸性介质条件下过氧化氢合成的最优工艺参数及机理,为进一步工业化放大提供必要的准备和参考。 2 实 验 2.1 实验仪器与材料 2.1.1 实验仪器 超声振荡仪(KQ-400DB,昆山市超声仪器厂)ppH计(PHS-3C,上海精密科学仪器有限公司)、电化学工作站(LK2005,天津市兰力科化学电子高技术有限公司),稳压直流电源(扬州华泰电子有限公司)、平板硫化机(U7011,上海齐才液压机械有限公司)、恒流泵(HL-2,上海青浦沪西仪器厂),扫描电镜JSM-5900(日本电子公司)。 2.1.2 实验材料 碳布(南通森友)、硫酸(广州化学试剂厂)、无水硫酸钠(汕头市西陵化工厂)、XC-72碳黑(卡博特公司)、聚四氟乙烯 PTFE(上海和申化学试剂有限公司)、无水乙醇(上海试剂一厂)。 2.1.3 电极制备 支撑体疏水化处理:取面积为30cm²的碳布于5%的PTFE乳液中反复浸渍至增重一倍,于马弗炉中340℃维持30min ,冷却后取出备用; 电极制备:将XC-72碳黑(过120目筛)、PTFE(20%)、硫酸钠(10%)、无水乙醇按比例混匀,高速搅拌混合30min 后超声分散15min,于烘箱内100℃烘至糊状,涂布于碳布上,上下放2层铝箔,置于模具中于5MPa、340℃下压20min,冷却后取出,于沸水浴中煮至无硫酸钠析出,烘干备用。 2.1.4 分析方法 过氧化氢浓度用高锰酸钾法测定;过氧化氢的法拉第电流效率: 式中n=2;F=96486C/mol,C为产生的过氧化氢质量浓度;V为溶液体积(ml),I为电流强度(A),t为时间(h)。 ( *基金项目:国家高技术研究发展计划(863计划)资助项目(20060102Z2009);江苏省省级污染防治专项资金资助项目(2006-1- W-19);江苏省自然科学基金资助项目(BK2006181,BK2007188) ) 收到初稿日期:2008-03-14 收到修改稿日期:2008-07-07 通讯作者:沈树宝 ( 作者简介:徐夫元 (1982-),男,江苏新沂人,在读博士,师承沈树宝教授,从事环境电化学研究。 ) 2.1.5 实验装置与方法 循环伏安在三电极体系中测定,工作电极、对电极及参比电极分别为气体扩散电极为(1cm)、铂片及饱和甘汞电极(SCE)。电解质经纯氧饱和。电解装置如图1,中间用Nafion117 阳离子交换膜隔开,阴极为30cm²的气体扩散电极,阳极为30cm²石墨板,阴阳极距膜6mm,工艺流程如图2。 Membrane 图1 电解装置 Fig 1 Apparatus for electrolysis 图2 电合成工艺流程 Fig 2 Process flow diagram of electro-synthesis 阳极液(100ml硫酸钠与硫酸)闭式循环,泵速1200ml/h,Po,==0. 1MPa, Qo,,=60ml/ min,I =1A 。组成相同的阴极液采取开式连续合成,或闭式循环,闭式循环条件同阳极。开式泵速150ml/h。先通气,后泵入电解液,电解液注满腔室,加电电解并记时,隔时取样2ml,测其浓度。 3 结果与讨论 3.1 电极电镜 利用扫描电镜观察电极的表面形貌,如图3所示。图3(a)为电极放大100倍电镜图,从图3中可以观察到电极表面布满坑槽。图3(b)为局部放大3000倍的电镜图,从该图可见坑槽的微观结构,坑槽是由凹陷以及众多微观突起构成的,是经过造孔后形成的,表面的孔道有利于氧气的传质,能够增加三相反应的有效面积。将有利于过氧化氢的合成。对其实际合成过氧化氢的性能进行了考察。 3.2 循环伏安研究 3.2. 1 氢离子浓度的影响 实验选取3个氢离子浓度。循环伏安结果如图4。由图4观察到氧还原峰,可以判断为不可逆反应。随酸浓度升高,氧还原峰电流增加。从第一次伏安扫描与第二次扫描的曲线看出,峰电流后者比前者低得 多,分析是由于第二次扫描,电极表面氧耗尽,使得氧气的扩散传质成为限制步骤所致。 图3 电镜图 Fig 3 Scanning electron microscope E.N 图4 不同氢离子浓度下的循环伏安图 Fig 4 Cyclic voltammogran at different H+ concentra-tion scan rate 3.2.2 硫酸钠浓度的影响 实验考察了3个硫酸钠浓度。循环伏安结果如图 5, 图5 不同硫酸钠浓度下的循环伏安图 Fig 5 Cyclic voltammogram at different Na2 SO4 con-cetration scan rate 由图5知硫酸钠浓度的增加对氧还原峰电流影响小,1mol/L浓度下的峰电位较1与10g/L略有正移,表明硫酸钠浓度的增加,提高了溶液的导电性,减小了电极极化。使得氧还原可以在较正的电位区发生。从两次扫描的结果同样观察到前者的峰电流明显比后者低得多。 3.3 恒电流电解实验 3.3.1 氢离子浓度的影响 通过恒电流电解实验考察了不同酸浓度对过氧化氢合成的影响。实验结果如图6. 由图6(a)、(b)发现不同氢离子浓度对过氧化氢合成浓度以及电流效率均有 0.02L>0.2>0.1mol/L. 氢离子浓度为0.1及0.2mol/L下随电解的进 行,电流效率均急剧下降,而0.02mol/L下电流效率不降反升。 分析氧还原的电极反应式: 随电解进行,氢离子被消耗,阳极室的氢离子因离子交换膜的阻隔来不及补充至阴极室,阴极电解液pH升高。氢离子浓度较低时,该影响更显著,使得电解条件改变。实验中在线测定了电解液的pH(如图5(c))。 L,反应初期pH急剧增加,20min 达12.36,之后增加平缓,pH的变化趋势与电流效率的趋势相似,推断该浓度下奇特的结果由pH变化所致,随电解时间的推移,由酸性合成变为碱性合成。 上述分析无法解释0.1、0.2mol/L下电流效率下降的现象,该条件下pH变化小,pH影响小。分析随电解进行,过氧化氢浓度的增加及电解过程中的热效应可能导致上述现象,但由于外部循环设置冷却水槽,热损失影响小;为验证是否产物积累导致电流效率降低。进行3组对照实验,结果如图7. 图6 不同氢离子浓度下过氧化氢积累浓度、电流效率pH Fig 6 Accumulation concentration ,currenct efficiency ,p H of H2 O2 at different H* concentrations 极液与酸性阳极液混合pH值与初始pH近似相等。可通过分室电解获得较高的电流效率,通过混合出液获得稳定的pH值。 3.3.2 硫酸钠浓度的影响 通过恒电流电解考察不同硫酸钠浓度对过氧化氢合成的影响。结果如图8所示。 图7 过氧化氢加入对其合成的影响 Fig 7 Influence of H2O2 on its electro-synthesis 由图7(b)知过氧化氢能在电极上深度还原,通气后图7(a),过氧化氢浓度升高,前20min 过氧化氢浓度增加幅度小,后期变大,表明过氧化氢浓度过高时,过氧化氢深度还原反应明显发生,过氧化氢的绝对合成量减小,当其浓度降至一定值后,过氧化氢合成变成主导反应。过氧化氢的存在不利于其合成。 由图8(a)、(b)知效果 1mol/L明显优于1、10g/L,后两者效果相差不大。从图7(b)发现低硫酸钠浓度下,电流效率下降,1mol/L时不降反升。分析是由于氧还原速度更大,耗酸快 ,pH升高所致。比较图6(c)和图8(c)发现低的氢离子浓度造成的pH效应大于硫酸钠浓度增加所导致的效应,体现在图6(b)较图8(b)中电流效率一直增加,图6(c)在 20min 中pH已为碱性,而图8(c)中在30min 才变为碱性。从图8(b)知1和10g/L下电流效率逐渐降低,则是由于过氧化氢累积所致。 同时发现现 0.02mol/L条件下电解后的碱性阴 图8 不同硫酸钠浓度下过氧化氢积累浓度、电流效率、pH 3.4 恒电流连续合成 开式连续合成产物排出可以减小产物累积的负面 图9 过氧化氢的连续电合成 Fig 9 The continus generation of H202 由图9知连续合成产物浓度先增加后达到稳态,电流效率有相同趋势,最终电流效率稳定在80%以上。且出液pH较稳定。 3.5 隔膜反应器与无隔膜反应器效果对照 为了考察隔膜的效果,与无隔膜反应器的电合成效果进行对照实验,结果图10。 图10 隔膜对过氧化氢合成的影响 Fig 10 Influence of diaphragm on H2O2 generation 由图10知无隔膜过氧化氢易在阳极进一步氧化损失,电流效率急剧下降。隔膜的加入阻止产物向阳极的迁移和扩散,可获得更高的电流效率与过氧化氢浓度。 4 结 论 (1) 氢离子浓度改变了氧还原的峰电流与峰电位、硫酸钠浓度改变峰电位。氢离子浓度过低或硫酸 钠浓度过高,pH剧增,氧还原机理由酸性还原向碱性还原转变。过氧化氢的累积不利于其合成; (2) 连续电合成,1h后电流效率稳定在80%以上,产物浓度高于0.3%,可以直接用于水处理。隔膜反应器较无隔膜反应器能有效防止阴极产物在阳极进一步氧化损失,电流效率比后者大大提高,优势更明显。 实验装置采用先产后用的思路,不受地域限制,体积小巧,移动方便,可操作性强,酸性条件下亦可以获得很高电流效率及过氧化氢浓度。有望用于废水在线处理。不仅适于定点污染源的处理,对散点污染源及突发污染源的处理更加方便快捷、高效。 ( 参考文献: ) ( 11 ( Ormad P , C o rtes S , P u i g A,et al . [ J ]. Water R e s ,1997, 31 : 2387. ) ( [2] Beltr a FJ,Encinar J M , Gonz dez J F . [J ]. Water Res, 1997 ,31:2415. ) ( 31 Beltr { F J,Garc a-Araya J F , et al. [J]. Water Res ,1999 , 33:723. ) ( 4 Gupta N,Oloman C W. [J].J A ppl Electrochem,2006, 36:255. ) ( 51 Gupta N,Oloman C W. [J]. J Ap p l El e ctrochem,2006 ,36:1133. ) ( 61 Oloman C, Watkinson A P . [ J ].J Appl El e ctrochem, 1979,9:117. ) ( 袁志平.[J].中国造纸,1982,1(5):55. ) ( 袁志平,阎德顺.[J].印染,1983,1(6):37. ) ( Kurt U ,Apaydin O , et a l . [J].J Hazard M a ter ,2007 ,143: 1-2. ) ( [101 Gulkaya I ,Surucu G A ,et al.[J].J H a zard Mater ,2006, 13:763-769. ) ( [111 Huissoud A, Tissot P. [ J ].J Appl Electrochem,1999, 28:653-657. ) ( 121 Huissoud A, Tissot P.[J].J Appl Electrochem,1999, 29:11-16. ) ( [131 郁青红,周明华,雷乐成.[J].物理化学学报,2006,22 (7) : 883. ) Preparation of C/ PTFE gas diffusion electrode andits application in electrosynthesis of hydrogen peroxide XU Fu-yuan' ,LI Xing',ZHU She-min’,CHEN Yingwen, SONG Tian shun,SHEN Shu-bao (1.National Engineering Research Centre for Biochemistry,Nanjing University of Technology,Nanjing 210009,China; 2. College of Material Science and Engineering ,Nanjing University of Technology ,Nanjing 210009 ,China)Abstract :C/ PTFE gas diffusion electrode was prepared ,and hydrogen peroxide electro-synthesis by oxygen re-duction was investigated with it in membrane reactor. The influences of H* concentration and Na2 SO4 concen-tration on oxygen reduction for H2O2 generation were studied by cyclic voltammogram and constant current e-lectrolysis.Mechanism transformation was found ,resulting from the sharp increase of pH,which was favorablefor H2O2 generation. On the contrary,H2O2 accumulation was not propitious for its synthesis. High current effi-ciency (>80%) ,high H2O2 concentration (>0.3 %) and stable p H were also achieved simultaneously by openconstant electrolysis. Deep oxidation loss of H2 O2 in anode was effectively reduced by membrane. Key words : hydrogen peroxide;gas diffusion electrode;membrane reactor;current efficiency ◎China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
关闭-
1/4

-
2/4
还剩2页未读,是否继续阅读?
继续免费阅读全文产品配置单
天津市兰力科化学电子高技术有限公司为您提供《C/PTFE 气体扩散电极中电合成过氧化氢检测方案(电化学工作站)》,该方案主要用于其他中电合成过氧化氢检测,参考标准《暂无》,《C/PTFE 气体扩散电极中电合成过氧化氢检测方案(电化学工作站)》用到的仪器有LK2005A电化学工作站。
我要纠错
推荐专场
相关方案






 咨询
咨询