2019年9月24日,清华大学李蓬课题组在Cell Reports上发表了题为“The protein phosphatase 1 complex is a direct target of AKT linking insulin signaling to hepatic glycogen deposition”的研究论文,报道了PP1复合物作为营养感知器,独立于GSK3介导胰岛素刺激下肝脏糖原合成的调节机制。
胰岛素是机体调节血糖吸收、促进合成代谢(anabolic metabolism)最关键的激素,可以促进糖原、脂肪、蛋白质合成。糖原和脂肪可被用于能量贮存;糖原是最先被机体利用的能量储备:比如在运动时,肌肉糖原可以作为快速的能量来源,供肌肉细胞产生ATP;而肝脏中糖原负责在饥饿或能量缺乏时补充血糖,使之维持稳定浓度。但是糖原代谢里一个长期悬而未决的问题,胰岛素是如何激活糖原合成的?甚至在最新版(第七版)的Lehninger生化教科书中,也只是指出需要一个“insulin-sensitive protein kinase”,但不知其身份。虽然胰岛素-AKT可以通过抑制激酶GSK3、降低糖原合成酶GS磷酸化来促进糖原合成,但是这条调节通路的作用非常有限,因为GSK3的磷酸化位点突变后不影响糖原合成。并且,GSK3调控糖原合成是通过双抑制作用而起作用,目前我们的认识里还缺乏一种主动糖原合成调控的机制。虽然已知胰岛素还通过激活磷酸酶PP1,进而调节多个关键糖原代谢酶,然而由于对phosphatase调节研究的困难,领域内只能猜测却难以发现这个调节PP1磷酸酶的“insulin-sensitive protein kinase”。
PP1(protein phosphatase1)对糖代谢具有重要作用,参与调节多个糖原代谢酶活性,包括GS、GP和GPK。PP1全酶由一个催化亚基(PP1c)和一个调节亚基(PPP1R)组成。已知PPP1R3家族作为特殊的一类调节亚基可以把PP1靶向到糖原代谢过程,该家族包括7个成员,PPP1R3a-g。尽管一些研究表明PPP1R3成员参与调节肝脏糖原合成和积累,但是具体的机制究竟是如何呢?
针对这个问题,李蓬团队首先通过生物信息学分析磷酸化蛋白组数据库数据,找到了10个候选蛋白,可能是AKT新的磷酸化底物,同时也参与调节糖脂代谢。随后通过生化实验鉴定出PPP1R3g是AKT一个新的直接底物,同时结合质谱分析发现S79是PPP1R3g的AKT磷酸化位点。其后,课题组发现在胰岛素刺激下PPP1R3g可以直接被AKT磷酸化,更重要的是发现生理和病理条件下的胰岛素信号与PPP1R3g磷酸化水平密切相关。更进一步地,课题组发现在胰岛素刺激下,PPP1R3g介导糖原合成是不依赖于经典的GSK3途径的。接下来,课题组通过敲除和过表达系统在体研究了PPP1R3g磷酸化的生理功能,发现PPP1R3g磷酸化可以加快葡萄糖清除和提高胰岛素敏感性。在机制上,课题组发现PPP1R3g磷酸化可以提升与p-GS的结合,进而加快PP1c对GS的去磷酸化。同时发现了PPP1R3b可作为PPP1R3g的下游,通过结合从PPP1R3g上解离下来的去磷酸化GS,刺激糖原的合成,从而实现对胰岛素信号的传递。
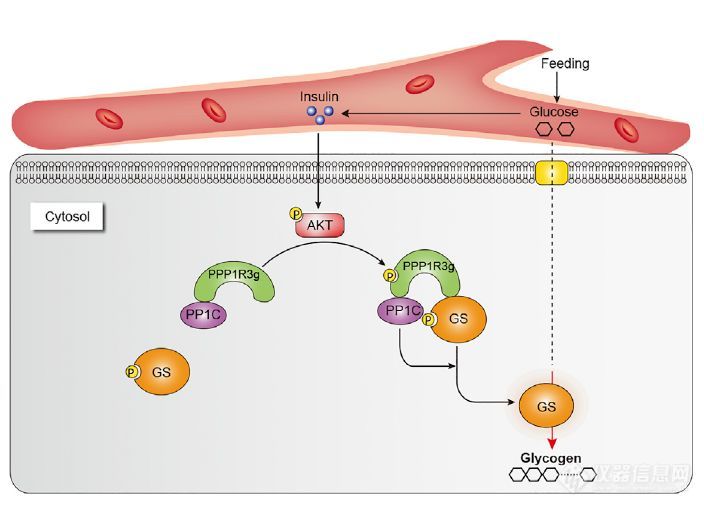
图1. 胰岛素-AKT调控PPP1R3G磷酸化促进糖原合成的新机制
本研究回答了本领域近30年一直未回答的问题,为新版的生物化学书籍完善提供重要的一笔(图2)。
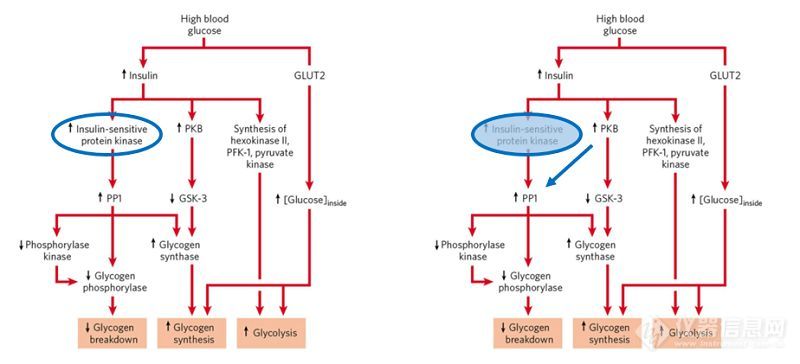
图2. 经典生化教科书中可修改的一笔。左图为Lehninger Principles of Biochemistry(7th Edition)中提出的位置激酶,右图则是该研究提供的改写
该论文中,糖原合成酶和糖原磷酸化酶活性的研究均采用放射性方法,利用放射性标记的葡萄糖作为底物,通过检测放射性活度来计算酶的活性。珀金埃尔默提供了从试剂、耗材到检测仪器的完整解决方案,助力中国科学家取得更大成就。
药典合规性——LAMBDA 365+紫外/可见分光光度计的操作确认
锂行天下 | Avio 200 ICP-OES测定钠离子电池正极材料中元素含量
【转载】公共卫生学院与珀金埃尔默企业管理(上海)有限公司签署关于质谱技术在公共卫生领域应用的合作项目
仪器维护新策略——AVIO 2X0/5X0耗材更换指南

珀金埃尔默热重-红外-气相色谱质谱联用 TG-IR-GC/MS
Avio® 550 Max 珀金埃尔默高性能电感耦合 等离子体发射光谱仪
Avio 550/560 珀金埃尔默高性能电感耦合 等离子体发射光谱仪
珀金埃尔默 PerkinElmer GCMS 2400系统
珀金埃尔默GC 2400™ 平台-带分体式触摸屏 气相色谱质谱平台
珀金埃尔默 PerkinElmer MPS 320™ 微波消解仪
LAMBDA365+ 珀金埃尔默紫外/可见光谱仪
珀金埃尔默 PerkinElmer LC 300 HPLC 超高效液相
珀金埃尔默Spectrum 3™傅立叶变换红外光谱仪
珀金埃尔默 PerkinElmer PinAAcle D 900 原子吸收光谱仪
珀金埃尔默 NexION 5000 多重四极杆ICP-MS
珀金埃尔默环境监测走航系统方案
OilPrep 8 油品稀释器
OilPrep 4 油品稀释器
LPC 500液体颗粒计数器和ICP-OES油品联用系统

关注

拨打电话

留言咨询