
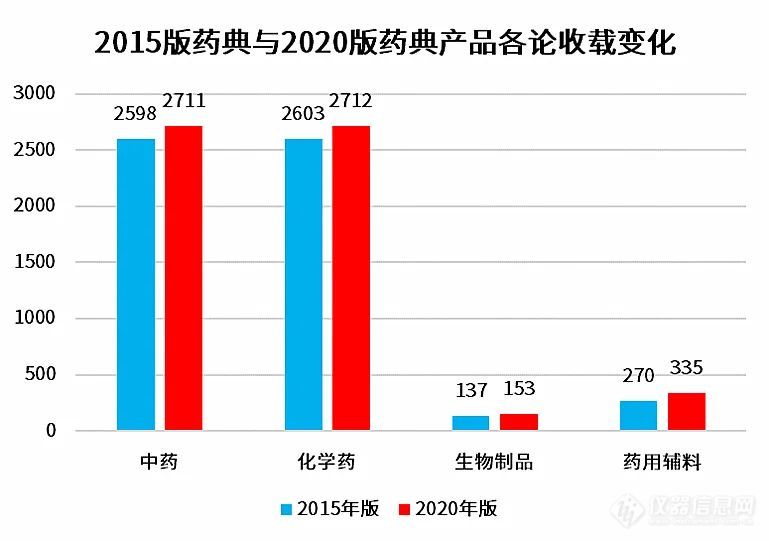
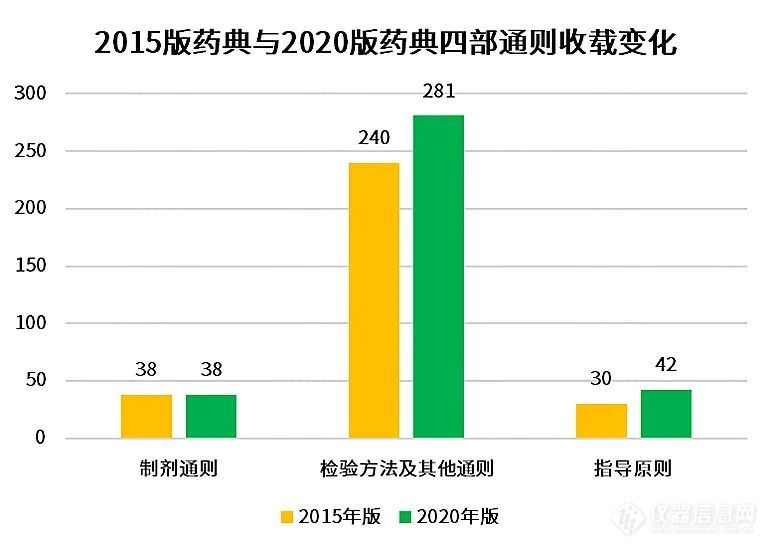


2019年7月26日,国家药典委官网发布关于《预混与共处理药用辅料质量控制指导原则》公示稿,并提到计划收载于《中国药典》四部。
2019年8月26日,国家药典委官网发布关于《9601 药用辅料功能性相关指标指导原则》修订公示稿。
公示稿发布后,岛津积极反馈,针对新增订和修订标准公示稿内容进行了解读,并制定符合通则要求的应对方案,助力我们企业和药检所小伙伴们从容应对新标准。
标准公示稿解读
01增修订变化
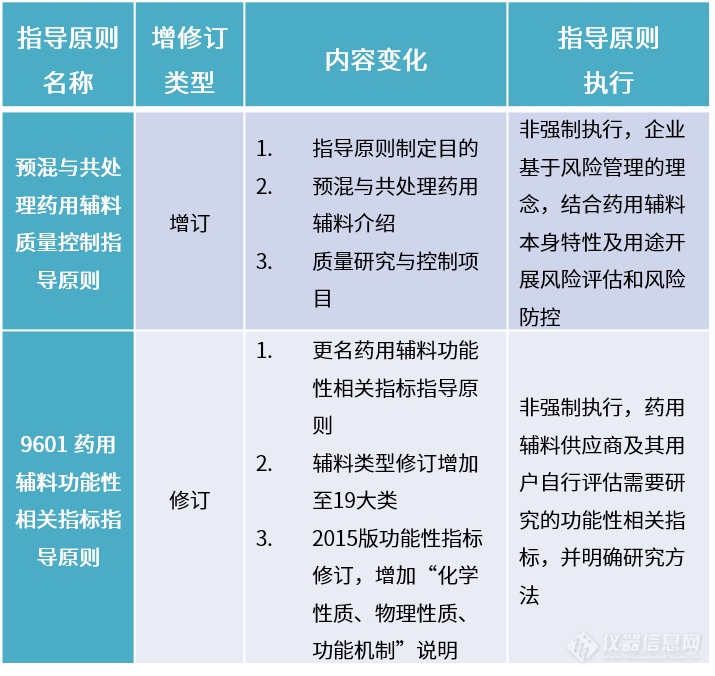
注:执行内容来源于公示稿原文
02粒度项目在指导原则中收载情况
《预混与共处理药用辅料质量控制指导原则》公示稿在功能性指标项目提到:采用适宜的方法,有针对性地建立适合预期功能的关键功能性检查项目,如“粒度与粒度分布”。
《9601 药用辅料功能性相关指标指导原则》公示稿中粒度研究项目在各类辅料功能性相关指标收载情况如下表:
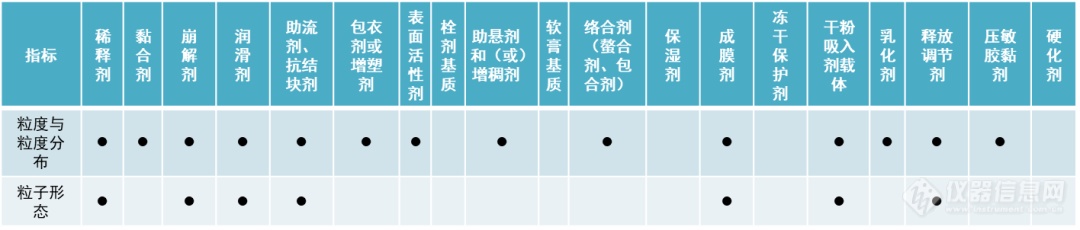
03粉体的颗粒粒度和粒度分布研究必要性
原料药的粒度分布(Particle Size Distribution,PSD),可能会对终产品的性能产生显著的影响,例如溶解度,粒子越小,比表面积越大,溶解性能就好。
原料药和辅料的粒度分布会影响药物可生产性,如流动性、总混均匀度、可压性等。
粉体的粒度分布对口服固体制剂生产过程中的每一步都有很大影响,包括预混合、混合、制粒等。
注:文字来源https://www.americanpharmaceuticalreview.com/featured-articles/36779-particle-size-specifications-for-solid-oral-dosage-forms-a-regulatory-perspective/
04药典中粒度与粒度分布检测方法
2015年版《中国药典》在四部《0982 粒度和粒度分布测定法》中提供方法:
● 第一法:显微镜法
● 第二法:筛分法
● 第三法:光散射法,所用仪器为激光散射粒度分布仪,分为湿法测定和干法测定
解决方案
01粒度分析

SALD-2300干法激光粒度仪
02颗粒形貌分析


EPMA-8050G电子探针显微分析仪
药品粒度与形貌分析应用实例
2019年10月15日,国家药监局综合司发布《化学药品注射剂仿制药质量和疗效一致性评价技术要求(征求意见稿)》,在“质量研究与控制技术要求”明确提出应研究注射用粉末剂型的“复溶时间”。复溶时间的长短与粉末粒度大小和颗粒形貌等因素密切相关。
01注射用头孢曲松钠原研药和仿制药复溶时间测试
原研药20秒时全部溶解,倒置观察未见不溶颗粒,且溶液呈澄清透明状。
仿制药大量不溶,且存在较为明显的团聚颗粒,震荡至60秒仍有部分团聚颗粒存在,震荡至90秒全溶。全部溶解后,两者均呈淡黄色澄清溶液。
02粒度分析
采用SALD-2300干法激光粒度仪分别对原研药和仿制药进行了粒径分布比较研究。
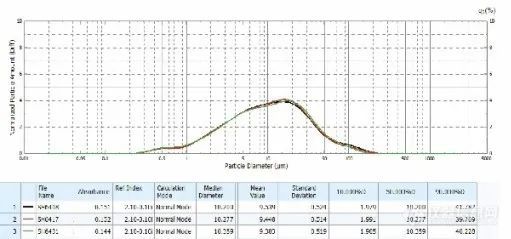
三批原研药测定粒径分布图
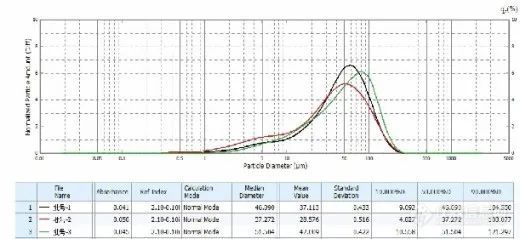
三批仿制药测定粒径分布图
以上结果可见两者存在明显差异:原研药分布范围宽,但呈较好的均匀正态分布,不同生产批次间粒度分布均一稳定、精密度良好;仿制药粒径明显大于原研药,以45μm左右大粒径为主,且不同批次间差异较大。
03颗粒形貌
采用岛津电子探针显微分析仪(EPMA-1720)分别对原研药和仿制药进行了颗粒形貌观察比较研究。

原研药SH6408形貌 某批次仿制药形貌
原研药主要以小的片状颗粒为主,偶尔会有少量松散团聚,比表面积大;而仿制药主要以大的块状结晶颗粒存在,表面存在比较密实的团聚,且不同生产批次间的差异明显。在颗粒形貌方面,两者差异显著,形貌结果与粒径分布结果相吻合。
注射用粉末的粒径、颗粒形貌或可作为指导主成分结晶工艺改进的指标,提升复溶时间的一致性。
参考文献:盖荣银等,注射用粉末剂型仿制药一致性评价关键技术要点解析,中国医药工业杂志,2019,50(2):226-228

岛津祝您中秋节快乐!
岛津原子力显微镜在生物学及生命科学中的应用
岛津特色质谱技术丨SPME-GCMSMS结合气味数据库赋能中药气味鉴别研究
岛津电子探针助力分析含水月壤,发表Nature顶刊!

相关产品

关注

拨打电话

留言咨询