2020年2月28日,国家药监局发布《药品记录与数据要求》征求意见稿,2020年7月1日国家药品监督管理局官网发布关于 “国家药监局关于发布药品记录与数据要求(试行)的公告(2020年第74号)”的通知,明确要求自2020年12月1日起施行。
公告发布后,岛津积极反馈,针对新要求进行解读,并基于在医药行业多年积累的数据完整性经验,结合岛津最新网络版CDS软件LabSolutions CS软件,提出了相应的电子记录和数据解决方案和服务,帮助广大用户从容应对新要求。
要点解读
第一条 为规范药品研制、生产、经营、使用活动的记录与数据管理,根据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《中华人民共和国药品管理法实施条例》等法律、行政法规,制定本要求。
解读
与以往法规不同的是,不仅是数据管理,还增加了记录管理,并强调了药品研制、生产、经营、使用活动的全生命周期记录与数据管理。
第三条 数据是指在药品研制、生产、经营、使用活动中产生的反映活动执行情况的信息,包括:文字、数值、符号、影像、音频、图片、图谱、条码等;记录是指在上述活动中通过一个或多个数据记载形成的,反映相关活动执行过程与结果的凭证。
解读
重新对数据和记录进行了定义,明确了记录与数据的关系,因此不管是数据还是记录都需要进行全面的管理。
电子记录与数据管理要求与解决方案
第二十条 采用电子记录的计算机(化)系统应当满足以下设施与配置:
(一)安装在适当的位置,以防止外来因素干扰;
(二)支持系统正常运行的服务器或主机;
(三)稳定、安全的网络环境和可靠的信息安全平台;
(四)实现相关部门之间、岗位之间信息传输和数据共享的局域网络环境;
(五)符合相关法律要求与管理需求的应用软件与相关数据库;
(六)能够实现记录操作的终端设备及附属装置;
(七)配套系统的操作手册、图纸等技术资料。
解决方案
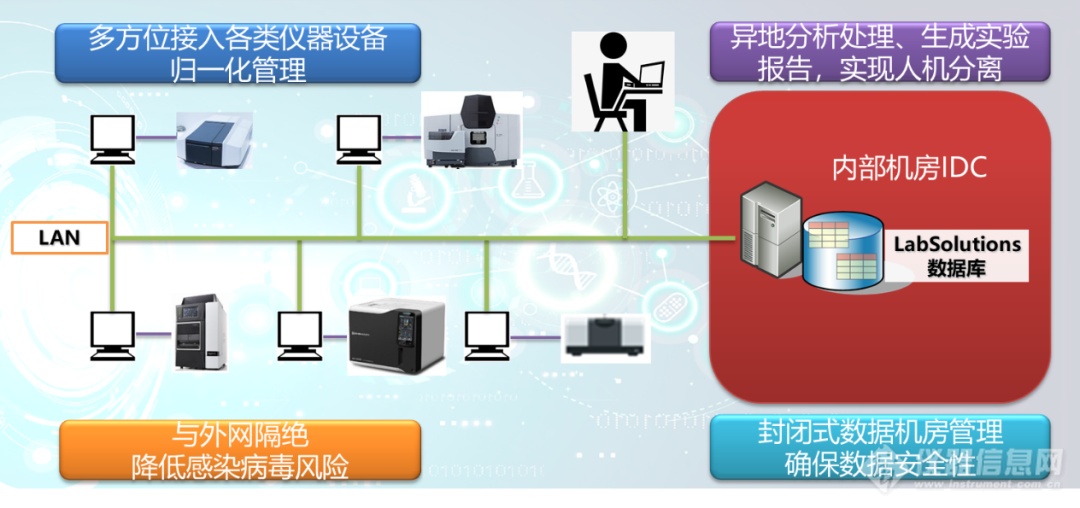
推荐采用网络化方案,即基于网络和数据库技术将存储设备(服务器或主机)存放于专用机房进行安全管理。
岛津LabSolutions 网络版CDS方案示例
第二十一条 采用电子记录的计算机(化)系统至少应当满足以下功能要求:
(一)保证记录时间与系统时间的真实性、准确性和一致性;
(二)能够显示电子记录的所有数据,生成的数据可以阅读并能够打印;
解决方案
推荐使用基于Windows 活动目录(AD: Active Directory)服务管理服务器与计算机客户端,配合正确的多级账户角色设计,实现系统时间的真实性、准确性和一致性。岛津网络版CDS 不仅支持与域账号整合直接登录,还对系统中所有涉及日期和时间的电子记录,均统一以GMT(格林尼治标准时间) 存储于数据库中,确保时间的准确性。
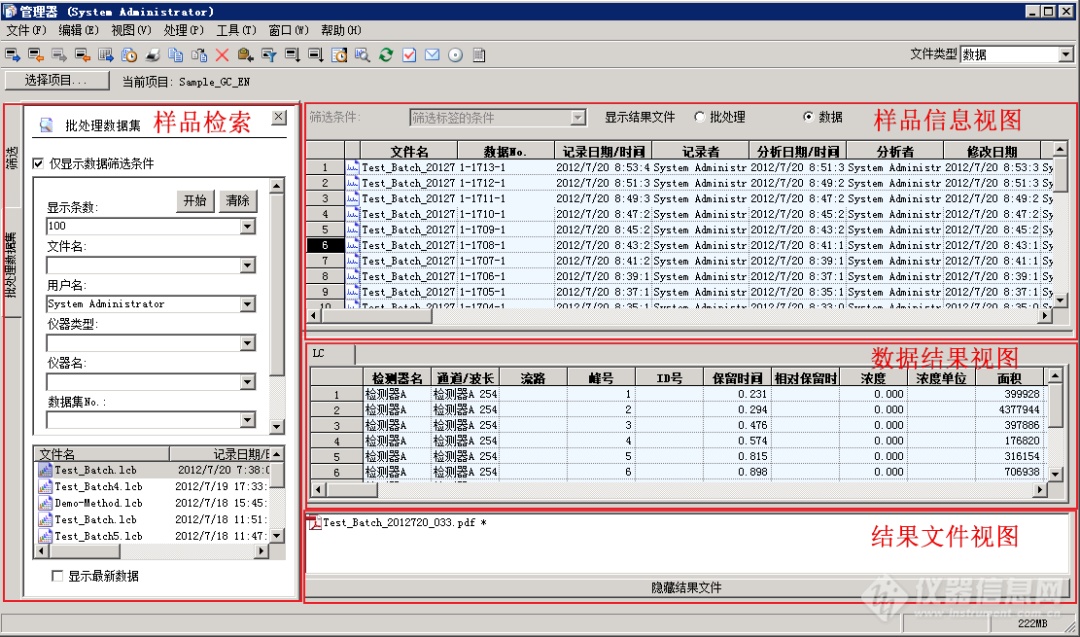
对于电子记录和数据,岛津网络版CDS采用数据库格式进行存储和管理,可以管理所有生成的PDF数据,支持网络化随时阅读、一键打印。
第二十一条 采用电子记录的计算机(化)系统至少应当满足以下功能要求:
(三)系统生成的数据应当定期备份,备份与恢复流程必须经过验证,数据的备份与删除应有相应记录;
(四)系统变更、升级或退役,应当采取措施保证原系统数据在规定的保存期限内能够进行查阅与追溯。
解决方案
仅有数据备份操作已经不够了,还需要对备份/恢复流程进行验证,备份的生成与删除都须有相应记录。
岛津推荐用户定期进行备份与恢复验证,网络版CDS已经自带灾难备份/恢复程序,以及项目备份/恢复程序,所有备份及恢复操作都有日志进行存储 。
另外,岛津也可提供专业的备份与恢复验证服务,由专业资深工程师提供方案及操作,并提供专业的建议方案。
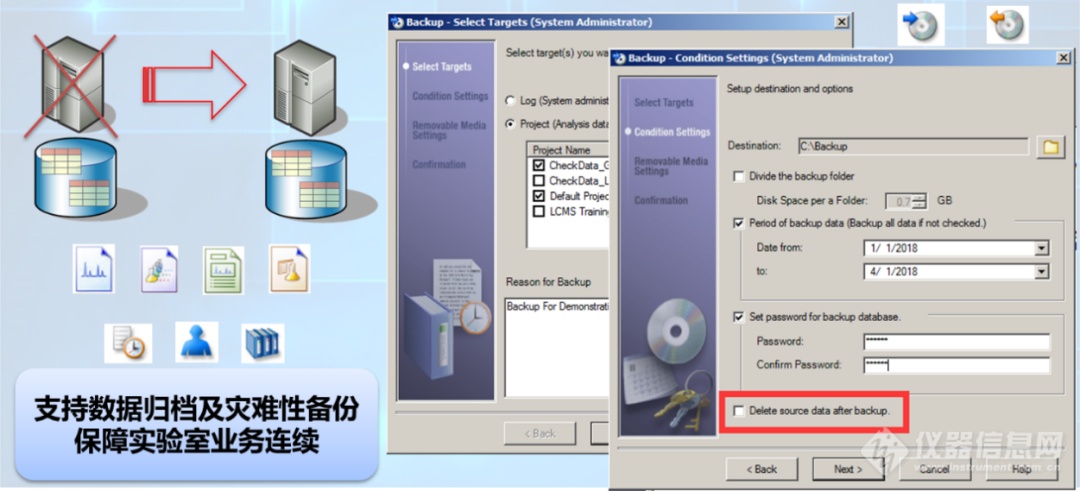
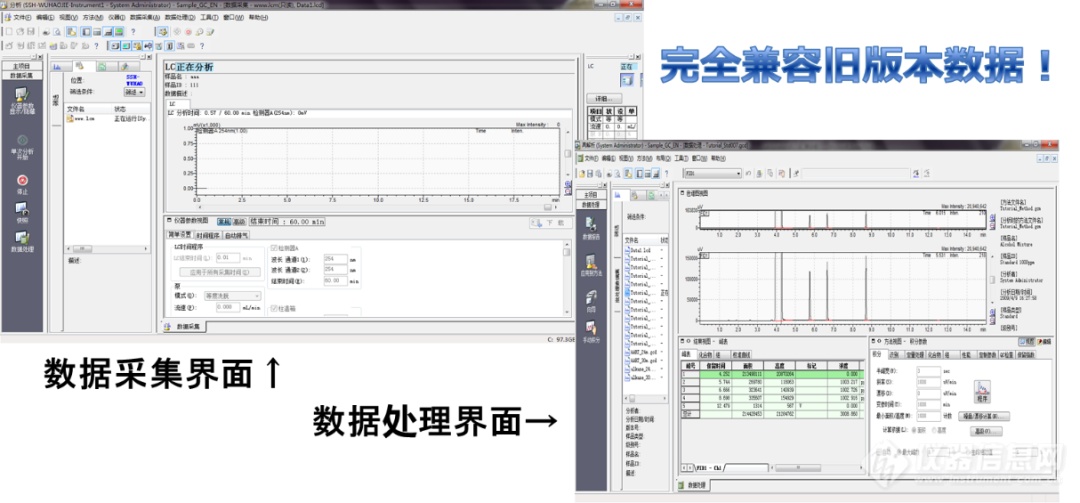
数据查看方面,岛津LabSolutions CS不仅向下兼容所有旧版本工作站数据,以LC数据为例,岛津LabSolutions CS支持LabSolutions单机版(含文件版和DB版)、LCSolution,甚至CLASS-VP工作站生成的数据,可直接打开浏览。
第二十二条 电子记录应当实现操作权限与用户登录管理,至少包括:
(一)建立操作与系统管理的不同权限,业务流程负责人的用户权限应当与承担的职责相匹配,不得赋予其系统(包括操作系统、应用程序、数据库等)管理员的权限;
(二)具备用户权限设置与分配功能,能够对权限修改进行跟踪与查询;
(三)确保登录用户的唯一性与可追溯性,当采用电子签名时,应当符合《中华人民共和国电子签名法》的相关规定;
(四)应当记录对系统操作的相关信息,至少包括操作者、操作时间、操作过程、操作原因;数据的产生、修改、删除、再处理、重新命名、转移;对计算机(化)系统的设置、配置、参数及时间戳的变更或修改。
解决方案
操作与系统管理权限要分开,以后必须独立设置系统管理员,不可由实验室分析员、主管或项目负责人兼任,设定专业的IT专职管理人员成为必需。
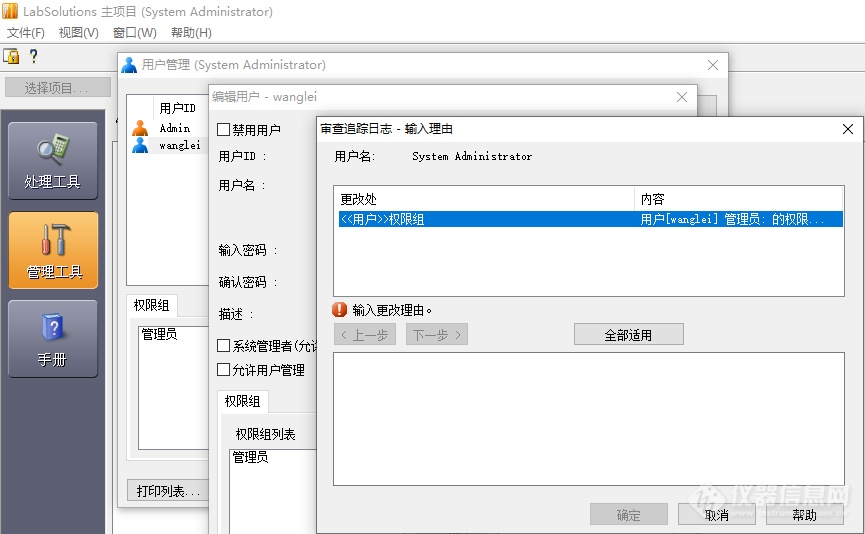
岛津LabSolutions CS支持多个机种近1000条权限选项,以权限组方式进行管理。软件支持各权限项自由组合,只有拥有权限组管理权限的人员,才可进行变更修改,且修改时必须要输入相应审计追踪理由。
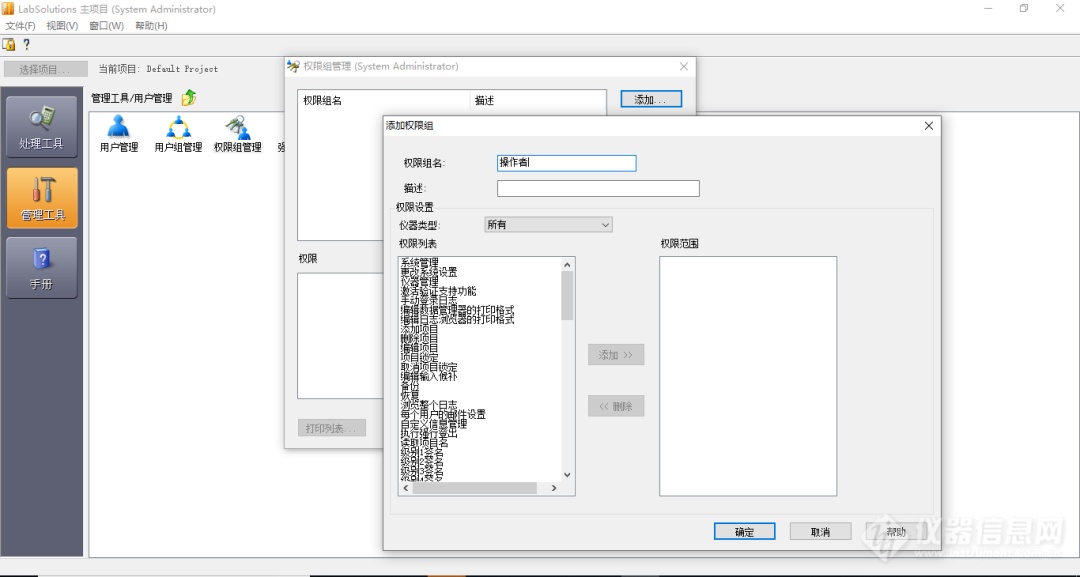
岛津LabSolutions CS 根据FDA 21 CFR Part 11法规进行设计,支持电子签名操作。
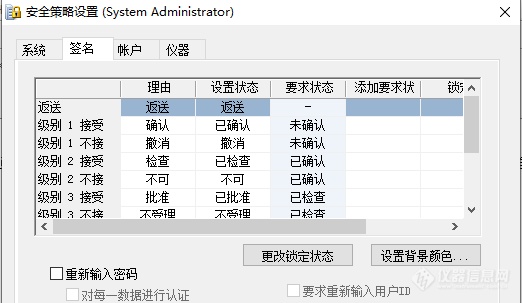
岛津LabSolutions CS拥有的审计追踪系统,含数据文件修改审计追踪系统配置审计追踪、用户与权限变更审计追踪,对任何变更均需输入理由,并以标准时间戳进行记录。
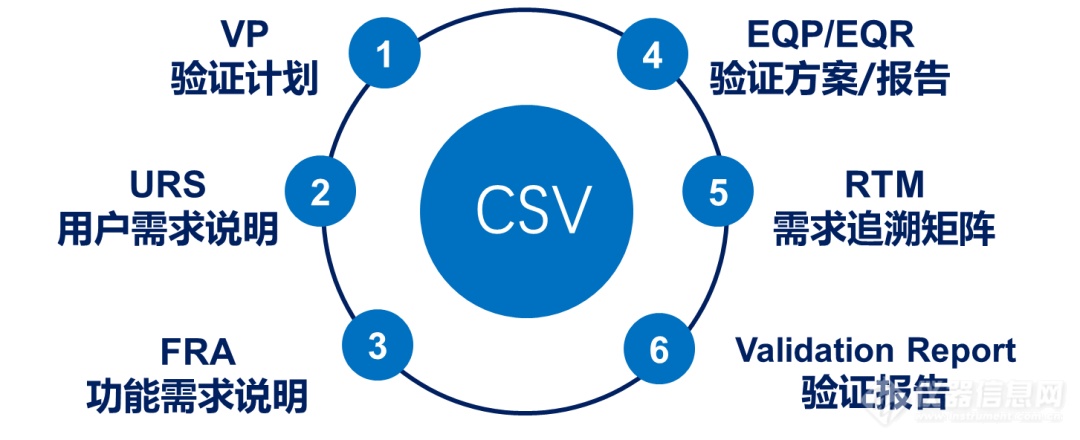
第二十三条 采用电子记录的计算机(化)系统验证项目应当根据系统的基础架构、系统功能与业务功能,综合系统成熟程度与复杂程度等多重因素,确定验证的范围与程度,确保系统功能符合预定用途。
解决方案
岛津LabTotal可根据用户需求,提供全套计算机化系统验证服务(CSV),基于用户需求及系统复杂性,为用户提供专属定制化验证服务,以符合预期需求。
以上就是本次《药品记录与数据管理要求》解读的全部内容了,更多岛津实验室数据管理软件功能,请登录岛津官网进行了解。
岛津试验机丨夹具世界系列之金属材料
夏日亲子溯溪:一场清凉的聚会
【国家列管】7月1日起,这类“上头电子烟”替代物被列管!
岛津祝您中秋节快乐!

相关产品

关注

拨打电话

留言咨询