
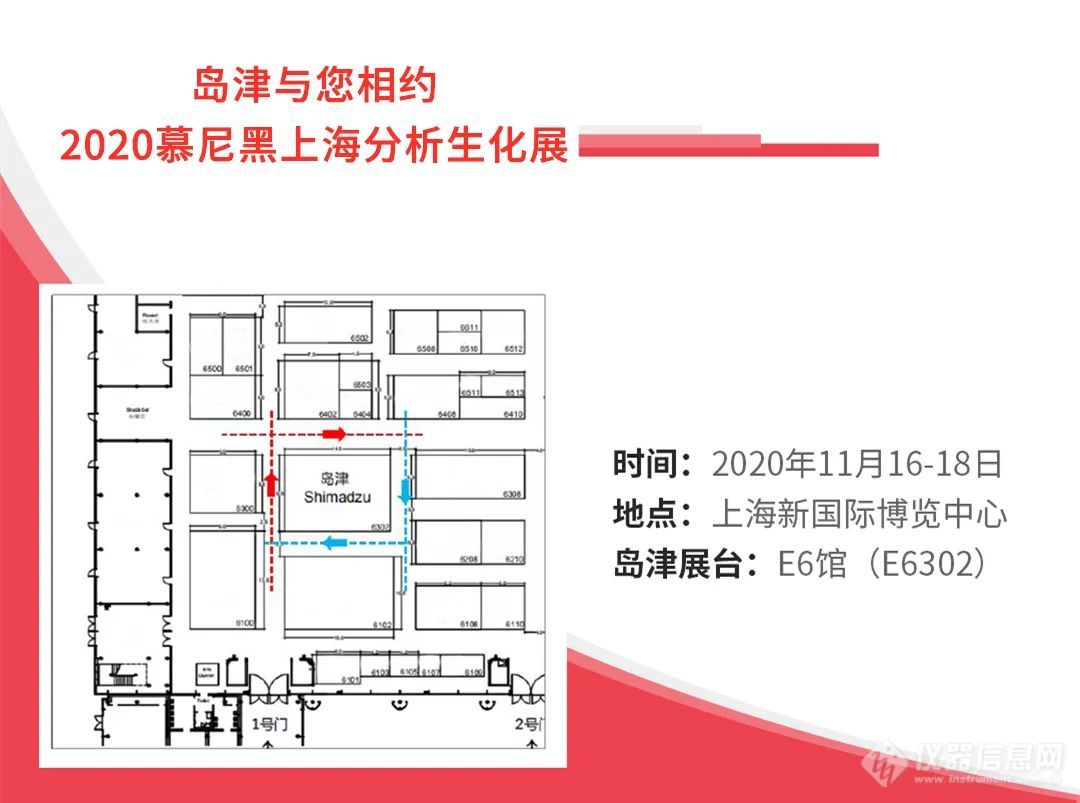
2020年11月16-18日,岛津以“Celebrating 50 Years of MS Innovation (1970-2020)”为主题,亮相“慕尼黑上海分析生化展”。
岛津长期致力于推动中国的医药/临床行业的发展,积极支持生命科学和生物技术、新药研究和仿制药评价等领域的多种分析检测工作,比如中药安全与评价、遗传(基因)毒性杂质、包材相容性、蛋白质组学、基因组学和代谢组学等。
在医药/临床展区将为您呈现:2020年版《中国药典》、中药检测、疫苗、TDM以及生物药解决方案,除解决方案外还将为您呈现LC-40、LCMS-8045、GCMS-TQ8040NX、LCMS-8050CL和Nexera UC Pre等产品介绍。
解决方案介绍
Part 01 2020年版《中国药典》
我国是天然药物之乡,随着对中药资源的开发和研究,我国对中药的用药理论和临床应用积累了丰富的经验,对于很多慢性病的治疗,中药的疗效越来越被国人所认可,被世人所熟知。然而阻挡中药走出国门的壁垒不仅包括中药有效成分难以确认,而且还包括中药中有害残留物超标,如农药残留和重金属等,致使中药在世界上的声誉受到影响。
2020版药典四部增订《第五法药材及饮片(植物类)中禁用农药多残留测定法》和修订《0212 药材和饮片检定通则》。首次收载禁用农药残留检测项目、限量要求、检测方法进入四部通则,形成整体检验标准,对中药安全性控制提出了更高的要求。
针对2020年版《中国药典》,将介绍以下解决方案:
《中国药典》2020年版通则与各论解读
《中国药典》2020年版中药禁用农残和重金属检测解决方案
Part 02 生物药
生物药在许多威胁生命的疾病治疗方面已显示出明显的临床优势,国内外各大医药企业都大力介入生物药物研发,并在某些领域有所收获。
国家食品药品监督管理总局药品评审中心(CDE)于2014年10月和2014年12月连续发布两个指导原则—生物类似药研发与评价技术指导原则(征求意见稿)和《生物制品稳定性研究技术指导原则》,并于2015年3月发布《生物类似药研发与评价技术指导原则(试行)》进入实施,旨在为生物药物的研发和质量控制提供更官方的、完备的指导原则。参考国内外重要机构的指导原则(如NMPA、ICH、PIC/S),岛津能够为生物药品的研发、生产和质量控制提供完整的解决方案。
针对生物药,将介绍以下解决方案:
《岛津蛋白类生物药开发和临床试验解决方案》
Part 03 疫苗行业
疫苗,作为预防性药物,在患病之前给予人体抵御疾病的能力,比治疗性药物意义更加重大。生产优质的疫苗、严把疫苗质量关是关乎民族存亡和国家兴衰的大事。然而,疫苗现存的大多数问题已无法依靠传统理化检测方法(如液相色谱和紫外分光光度计)进行应对。现代化、先进理化技术的参与,为解决疫苗现存问题提供了方向。
岛津自2017年开始,先后与中国食品药品检定研究院和国内知名疫苗企业开展合作。在合作中,除采用传统理化检测方法(如液相色谱和紫外分光光度计)以外,还以液相色谱质谱、聚集体分析、痕量元素分析、电子探针和MALDI-TOF等先进技术为支撑,开发了从疫苗生产到质量评价的全过程疫苗检测方法,覆盖蛋白类疫苗(如百白破)、多糖类疫苗(23价肺炎多糖疫苗等)、病毒类疫苗(如流感疫苗)和多糖蛋白结合疫苗(13价肺炎多糖疫苗、脑膜炎疫苗、Hib疫苗)等疫苗品种。
针对疫苗行业,将介绍以下解决方案:
《岛津疫苗质量评价新技术方案》
产品信息介绍





为了更好、更直观地了解各产品应用,届时我们会进行现场的技术交流会,诚邀您来参观与交流。

携手中科院广州地化所,揭示轮胎磨损与水源污染“蝴蝶效应”
生物惰性液相质谱联用系统直接进样法分析食品中草甘膦和氨甲基膦酸
从分析到制备的无缝工作流程(一) 岛津分析制备双流路系统鼎力相助
Nexis视角丨十问十答助您高效应对氢能新国标


关注

拨打电话

留言咨询