今年 2 月,国家药品监督管理局发布了《中国医疗器械标准管理年报(2023 年度)》,截至 2023 年 12 月 31 日,现行有效医疗器械标准共计 1974 项。自新修订的《医疗器械监督管理条例》出台以来,医疗器械各类标准不断推陈出新,以《医疗器械生物学评价》(GB/T16886) 为例,近两年来多个分项陆续更新,在医疗器械材料的化学表征、降解分析、生物相容性和生物安全性方面做了更细致科学的规定,这也给医疗器械分析技术带来了更高要求。
从产品研发到生产质控,医疗器械的整个周期都离不开各种分析技术的保驾护航。安捷伦作为生命科学和化学分析领域的领军者,为医疗器械行业提供了全方位的整体解决方案,助力医疗器械行业蓬勃发展。

医疗器械的材料表征与分析
《医疗器械生物学评价 第 18 部分 风险管理过程中医疗器械材料的化学表征》(GB/T16886.18) 中对材料表征提出了指导和要求。通过材料表征,可以全面了解医疗器械材料的物理、化学和机械性能,以及材料对环境因素的耐受性,对于确保医疗器械的安全性、有效性和质量可控性具有至关重要的意义。
针对不同材料所需的研究项目和分析技术不尽相同。下图是由安捷伦液相色谱+多角度光散射检测器(MALLs)系统进行的透明质酸样品检测,涉及摩尔质量分布与累积分布等结果。
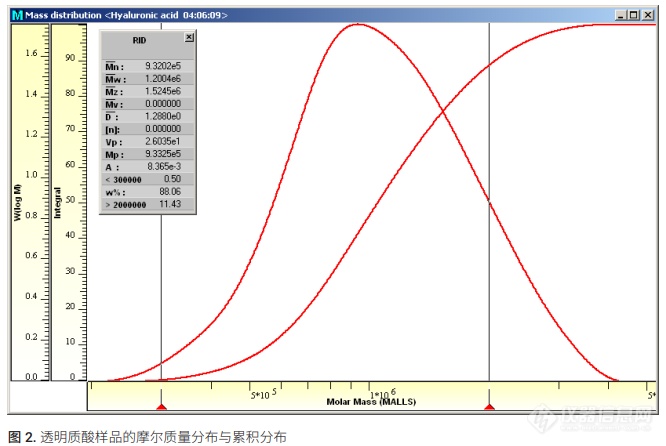

由于医疗器械材料的类型各异,相关的分析项目和技术手段也不胜枚举。例如金属材料或生物活性陶瓷等无机非金属材料的表征,则离不开原子吸收光谱仪(AAS)、电感耦合等离子体质谱仪(ICP-MS)等元素分析仪器,高分子聚合物材料则需通过液相色谱/体积排阻色谱进行分子量和残留单体的检测等。更详细的分析技术及案例分享,请关注后续安捷伦医疗器械方案的系列推文。
医疗器械的研发
有了合适的材料,下一步我们就步入医疗器械产品的研发了。这一环节中广受行业关注的,就是众多医疗器械报批时都需要的可沥滤物与可浸提物(Extractables and Leachables, E&L)分析。
国家药品监督管理局医疗器械技术审批中心发布了《医疗器械未知可沥滤物评价方法建立及表征技术审查指导原则》和《医疗器械已知可沥滤物测定方法验证及确认注册技术审查指导原则》,以帮助指导 E&L 实验室的工作。安捷伦也根据国标与指导原则的要求,整合了 E&L 分析多平台综合解决方案,使您“拿来即用”,快速获得针对 2000 种风险有机化合物及无机元素的高效筛查和快速定性定量分析能力。

在生物相容性与生物安全性方面,安捷伦可提供酶标仪、成像系统、流式细胞仪、实时抗阻分析系统等多款仪器,为遗传毒性、致癌性和生殖毒性等方面的研究提供多维度多视角的组合分析方法。
医疗器械的生产制造与质量控制
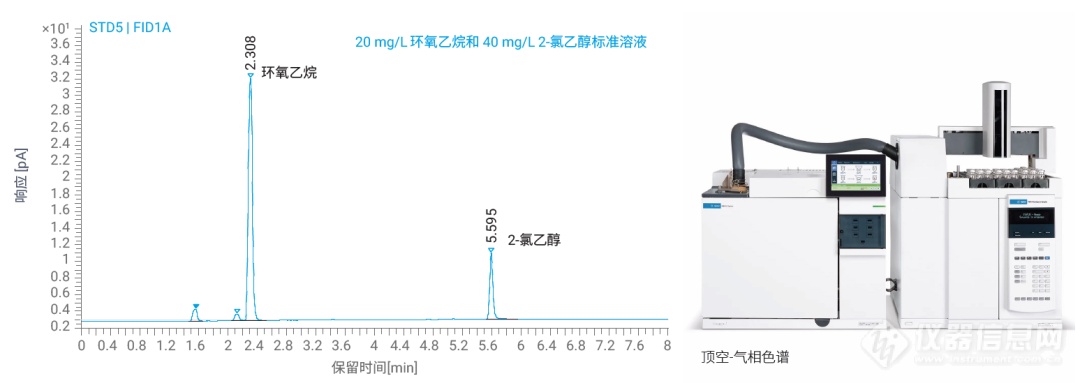
产品研发成功,进入生产环节,我们的关注点也转移到了如何进行质量控制,以保障产品的安全性和有效性。环氧乙烷残留量的测定,是众多使用环氧乙烷灭菌的医疗器械产品必备的质控环节。按照《医用输液、输血、注射器具检验方法 第 1 部分:化学分析方法》(GB/T14233.2-2022) 及《医疗器械生物学评价 第 7 部分:环氧乙烷灭菌残留》(GB/T 16886.7-2015),需要使用气相色谱技术对环氧乙烷和 2- 氯乙醇残留量进行测定。
代谢组学,妙手何来?|迈理奥,开拓代谢组学新科技的先锋
星光不负开学人丨安捷伦点亮开学季网络讲座
专业之选丨水中短链氯化石蜡分析解决方案
单光子后电离质谱成像方案:分子影像革新者
相关产品
CrossLab企业资产管理服务
Agilent GC 8890 气相色谱系统
Agilent Cary 3500 紫外可见分光光度计
Agilent Resolve 手持拉曼系统
Agilent TRS100 激光拉曼系统
Agilent 1290 Infinity II 二维液相色谱解决方案
Agilent 1290 Infinity II 液相色谱系统
Agilent 1260 Infinity II 液相色谱系统
Agilent 7900 电感耦合等离子体质谱仪
Agilent Bravo 自动液体处理平台
Agilent 7010C 三重四极杆气质联用系统
Agilent 7000E 三重四极杆气质联用系统
Agilent 5977C GC/MSD 单四极杆气质联用仪
Agilent 1290 Infinity II 高通量系统
Agilent 1290 Infinity II 方法转移系统

关注

拨打电话

留言咨询