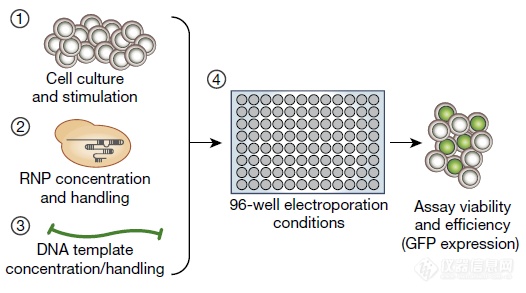
此次分享的是一种新的技术组合,将人们熟知的技术:电穿孔、同源介导修复、CRISPR Cas9放到一起编辑T细胞,具体如下:
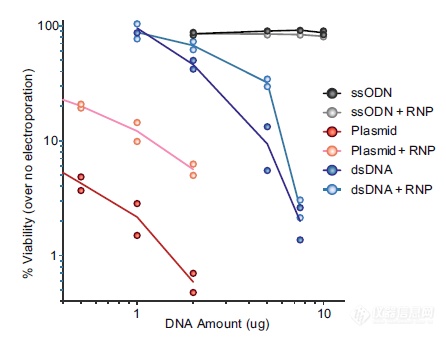
DNA链对于细胞是有毒性的,会降低细胞活力,不同类型的DNA链毒性不同:ssODN-寡聚脱氧核苷酸、RNP-CRISPR Cas9核糖核蛋白、Plasmid-质粒、dsDNA-线性双链DNA
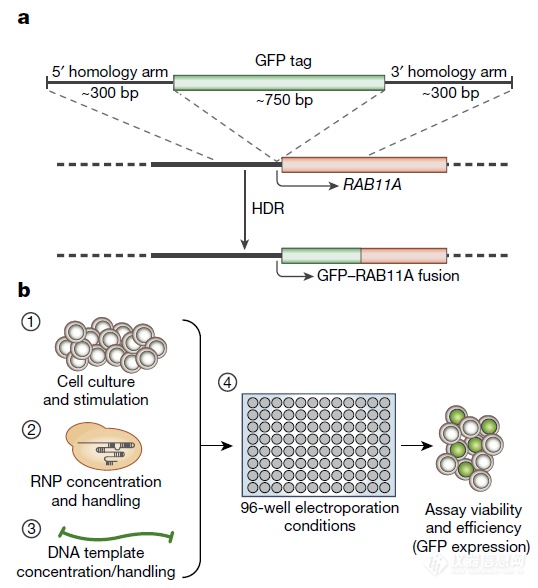
作者的策略是在要导入的序列两端加入与整合位点同源的序列,利用细胞自带的同源介导修复机制(HDR-用于修复细胞内偶发的DNA损伤)将新片段定点整合到基因组中以降低毒性
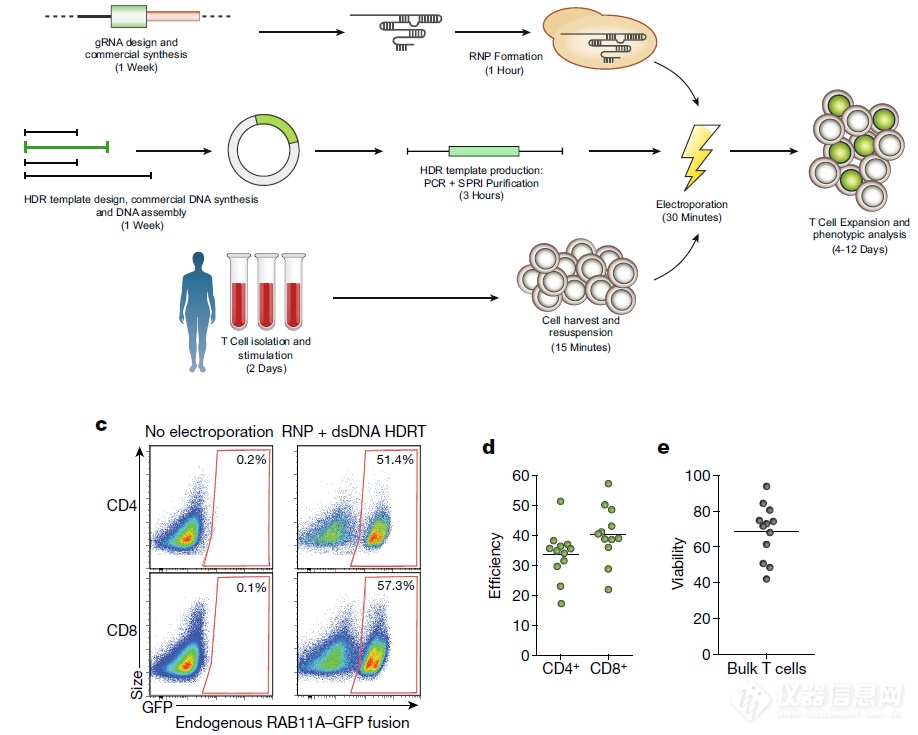
RNP + dsDNA HDR + 电穿孔的方法能够高效、安全的把GFP序列导入并表达
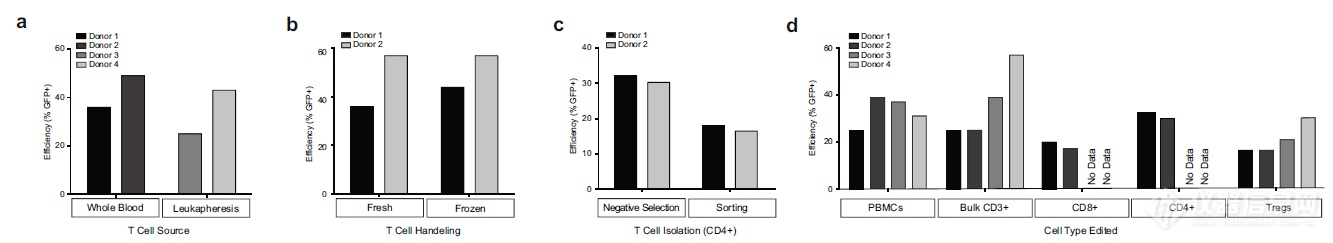
验证通用性:新方法能有效用于各种类型的样品
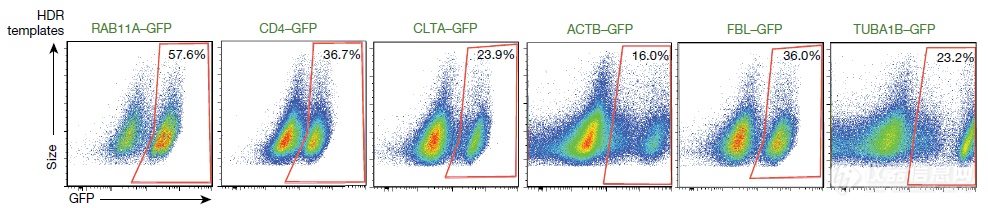
验证通用性:设置不同的位点,导入GFP,细胞层面没问题,可以表达GFP
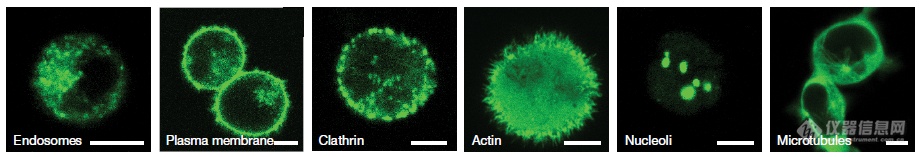
验证通用性:设置不同的位点,导入GFP,不同位点对应的亚细胞定位不同,显微镜空间角度验证-GFP的表达位置和靶序列对应蛋白亚细胞定位一致
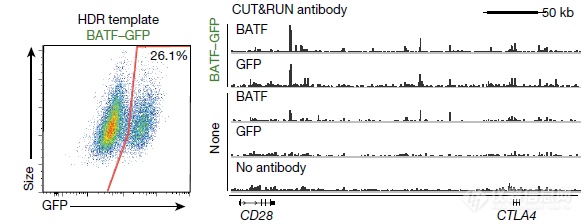
BATF是个转录因子,会结合到特定的DNA位点,CUT&RUN法(类似CHIP的方法)验证GFP和BATF一起定位到了BATF结合的DNA位点,暗示新方法准确的将GFP基因整合到了BATP基因
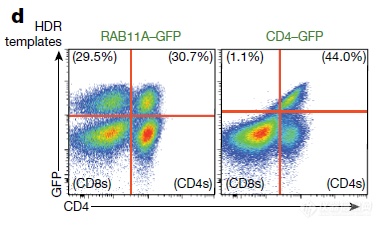
选取匹配的同源序列,如上图,用CD4同源序列新方法可以“靶向”编辑混合细胞中的特定细胞亚群CD4 T细胞,不影响CD8 T细胞(RAB11A两种细胞都表达,用它的同源序列转CD4和CD8都会表达GFP)
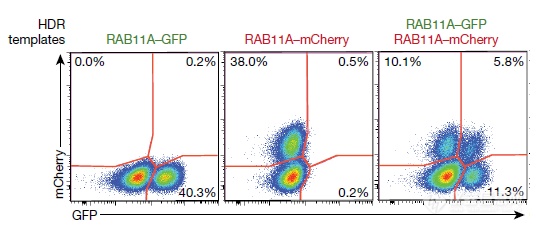
可将两个不同基因同时导入一个位点
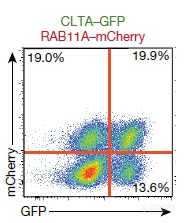
可将两个不同基因同时导入同一个细胞的不同位点
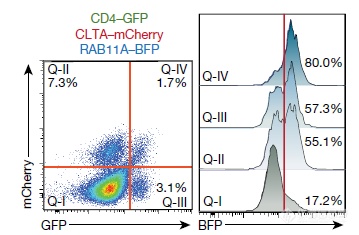
可将3个不同基因同时导入同一个细胞的不同位点

前面只是单方面的看到了可把目的序列靶向整合,但是否存在脱靶不知道,用targeted locus amplification (TLA) sequencing看是否会脱靶-无脱靶
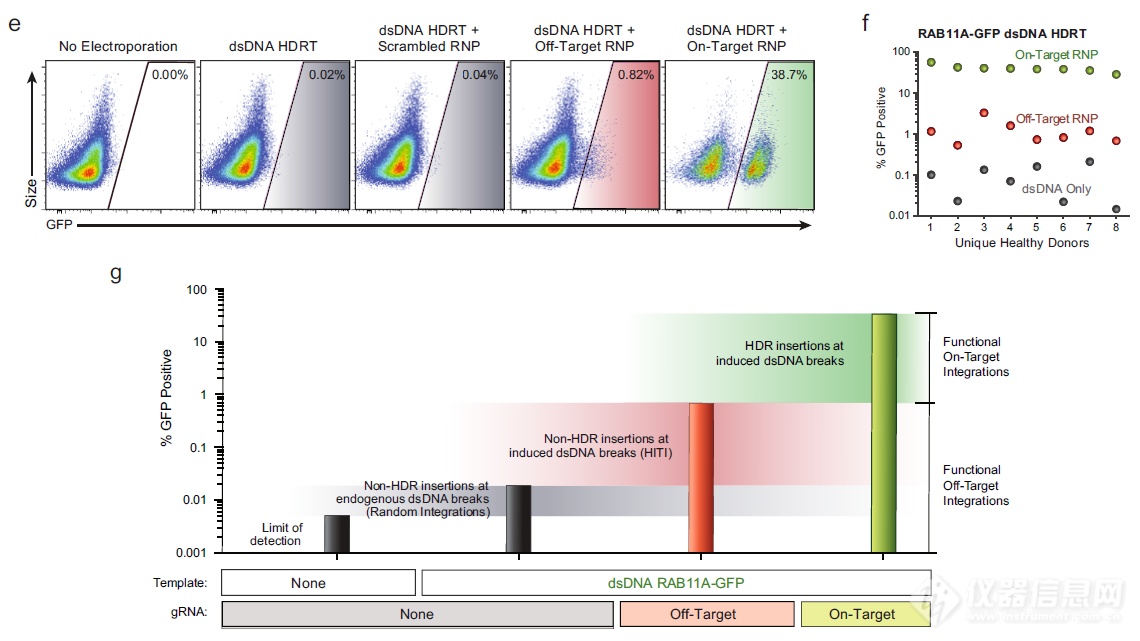
RNP(CRISPR Cas9)的作用是切开靶序列,做了“脱靶”的RNP,发现即便切开了错误的位点,但由于同源介导修复模板(HDRT)的存在也不会发生脱靶
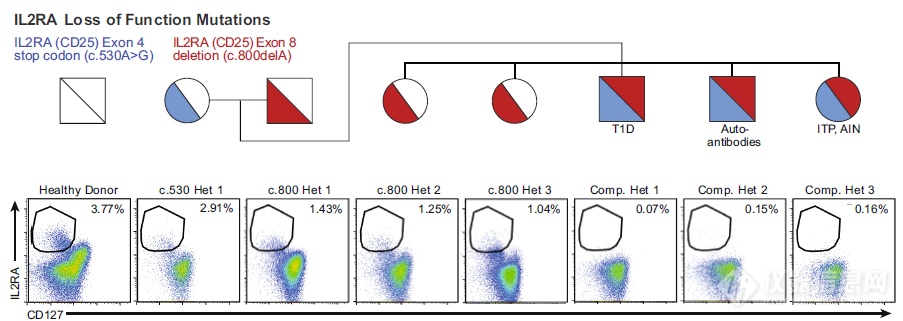
前面是以GFP为模型从各个角度证明方法的有效性,可用于编辑基因,开始在别的模型上看该方法用用于治疗疾病的可能:关注IL2受体突变,这个突变会造成IL2受体表达降低,IL2功能受限
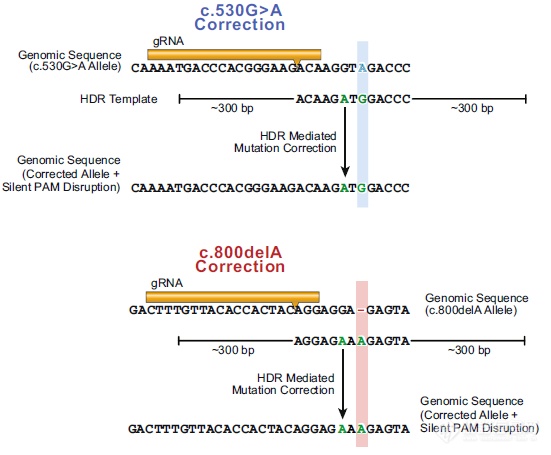
设计HDR
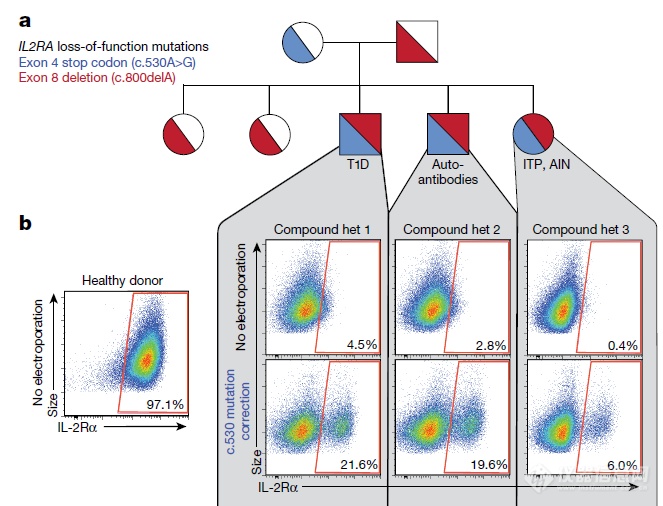
能够校正IL2受体表达缺陷
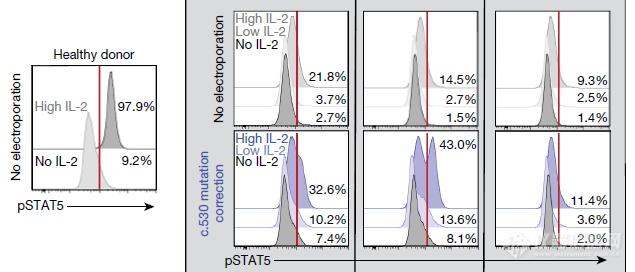
校正IL2受体后,IL2信号得到恢复
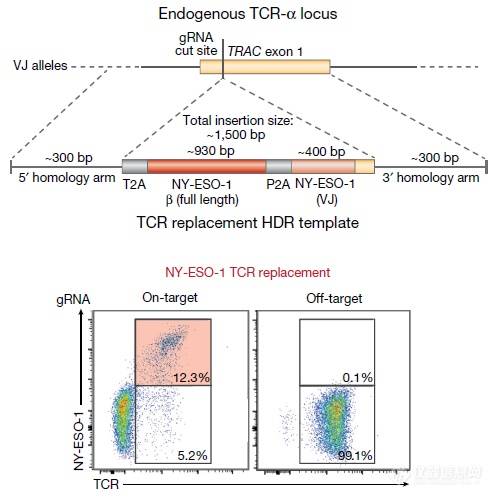
换一个模型看该方法的能用于治疗:让T细胞表达识别特异抗原的TCR
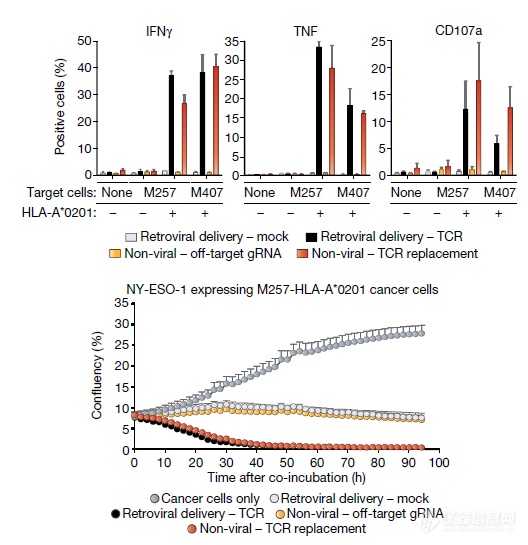
In vitro,编辑出的TCR-T能够响应肿瘤细胞刺激分泌细胞因子、杀死肿瘤细胞
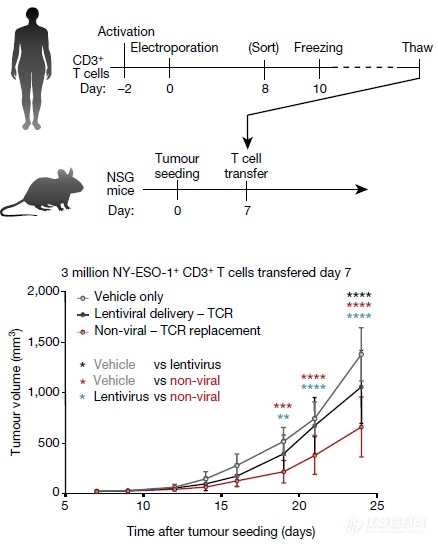
In vivo,编辑出的TCR-T能够抑制肿瘤生长
没有什么新的点,只是把旧有技术做了一个组合(同源介导修复、CRISPR Cas9、电穿孔),但故事讲的好 - 以病毒介导整合的随机性、DNA的“毒性”为起点,接着多个角度证明方法的有效性,最后将方法和实际结合,落脚在当下的热点肿瘤免疫!技术和发现就在那里,决定高度的是你能看多远......
Theodore L. Roth, Cristina Puig-Saus, Ruby Yu, Eric Shifrut, Alexander Marson et al. Reprogramming human T cell function and specificity with non-viral genome targeting.[J] .Nature, 2018.
想了解更多CNS级期刊最新内容,请关注我们的公众号,常有更新哦,也可加笔者微信交流:qianle522568!
酶标仪科普专栏丨第二期:荧光偏振(FP)介绍及应用
从分子到疾病:线粒体动力学研究取得新突破
【会议预告】第三届 3D 细胞类器官应用与高内涵成像技术研讨会邀您参加
开学啦|新学期,“心”守护实验室仪器免费巡检报名名额领取中
相关产品
上海美谱达UV-3200扫描型紫外/可见分光光度计
Leica徕卡DM750M正置显微镜
希森美康ExoCounter 全自动外泌体分析仪
智能化共聚焦高内涵成像分析系统
比利时 Bioruptor plus非接触式全自动超声破碎仪
DM3000德国徕卡leica生物显微镜
徕卡生物倒置显微镜LeicaDMi1
希森美康ExoCounter 全自动外泌体分析仪
梅特勒托利多pH 复合电极 LE438
Diagenode全自动核酸剪切仪Megaruptor ®3
化学发光成像仪Amersham ImageQuant 800
BIORUPTOR超声波细胞破碎仪new pico比利时Diagenode
美国博勒飞AMETEK Brookfield CTX质构仪
美国思拓凡 cytiva go蛋白纯化系统
ATS超高压均质机AH-D400

关注

拨打电话

留言咨询