外泌体是一类细胞产生的细胞外囊泡 (EVs) ,直径约40~160 nm,它们携带核酸、蛋白质、脂质和代谢物,是细胞间的通讯介质,影响细胞生物学的各个方面[1]。人体几乎所有类型的细胞在正常及病理状态下均可分泌外泌体,外泌体广泛分布在如血液、唾液、尿液、脑脊液和乳汁等。
由于外泌体等EVs具有高生物利用度、生物稳定性、靶向特异性、低毒性和低免疫原性,其在疾病诊断、治疗及药物递送中极具潜力。Biacore作为分子互作“金标准”,研究EVs当然也离不开ta。
免疫检查点疗法通过调节T细胞中的免疫检查点信号通路来增强抗癌免疫应答,取得了重要的临床进展,然而由于免疫衰竭,超过一半的癌症患者对这种治疗没有反应。北京大学吕万良教授团队针对肿瘤免疫检查点治疗中免疫衰竭与免疫逃逸的问题,重组构建了一种基因工程外泌体PD1 - Imi Exo,用于逆转肿瘤免疫治疗中的T细胞衰竭。相关研究于今年初在线发表在Bioactive Materials杂志[2]。
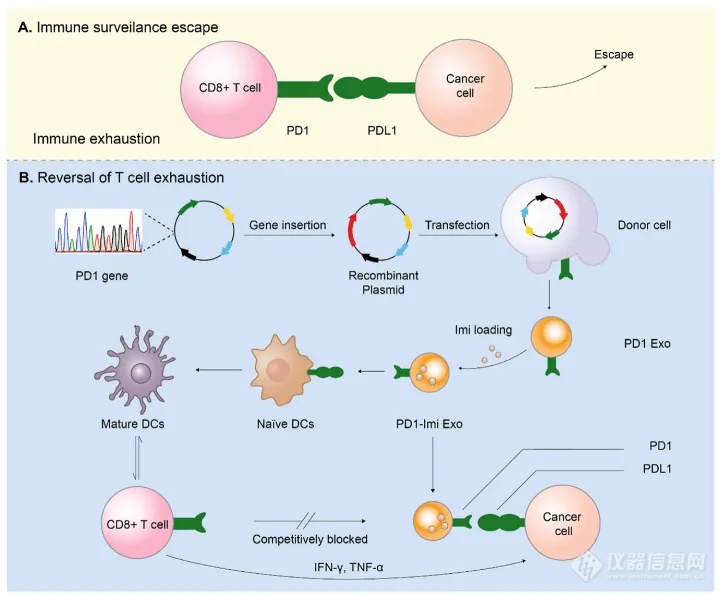
图1:工程化外泌体PD1 - Imi Exo研究路线及作用机制
PD1- Imi Exo通过基因工程设计PD1,同时包裹一种免疫佐剂Imiquimod,可以首先阻断CD8+ T细胞与肿瘤细胞的结合,表现出PD1/PDL1免疫检查点阻断作用,并通过释放Imiquimod促进未成熟树突状细胞成熟,激活和恢复CD8+ T细胞的功能,逆转免疫衰竭(图1)。
为了验证PD1 Exo与PDL1的直接结合,作者使用Biacore分别测定了PDL1与PD1蛋白及与PD1 Exo的结合(图2)。作者首先将PDL1蛋白偶联在CM5芯片上,PD1蛋白或PD1 Exo作为分析物,测定结合变化。结果表明,相较于PD1蛋白,PD1 Exo与PDL1的亲和力提高了数百倍。而除了亲和力信息外,Biacore实时检测的特点可以获得二者的结合速率和解离速率信息,相较于PD1蛋白,PD1 Exo与PDL1的解离明显变慢,说明其与PDL1的结合更加稳定,预示着其可能具有较长的药效。
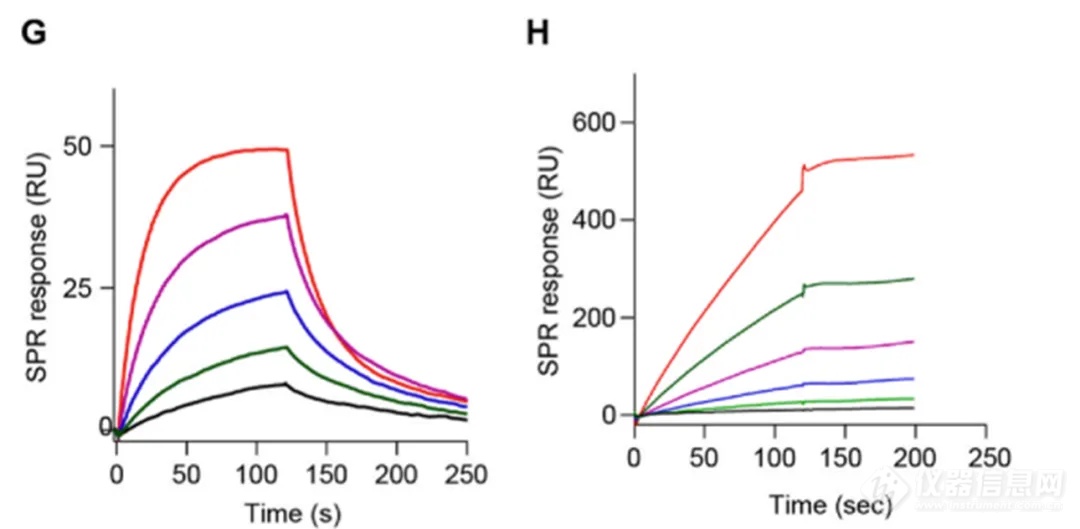
图2:Biacore检测PDL1与PD1蛋白 (G) 与PD1 Exo (H) 的结合
文中实验还表明,PD1 - Imi Exo呈水泡状圆形(约139 nm),对肿瘤细胞和树突状细胞均有明显的靶向作用和较强的结合作用,对黑色素瘤小鼠和乳腺癌小鼠均有显著的治疗效果。本研究也为提高PD1/PDL1的治疗效果,通过重建患者的免疫功能来预防术后肿瘤复发或转移,从而巩固整体预后提供了一种有希望的新策略。
除了通过基因工程化改造外,胞外对已分离的细胞外囊泡 (EV) 表面进行工程化改造的方法不受细胞活性影响,还可以引入非天然的分子。意大利布雷西亚大学的研究团队2023年在Nanoscale Advances发表的封面文章中,分别利用物理吸附与化学吸附(利用点击化学共价结合)两种方法将Cetuximab (CTX) 修饰在Red blood cell EV表面,并使用Biacore检测两种方法制备的REV与靶点EGFR结合的差异[3]。
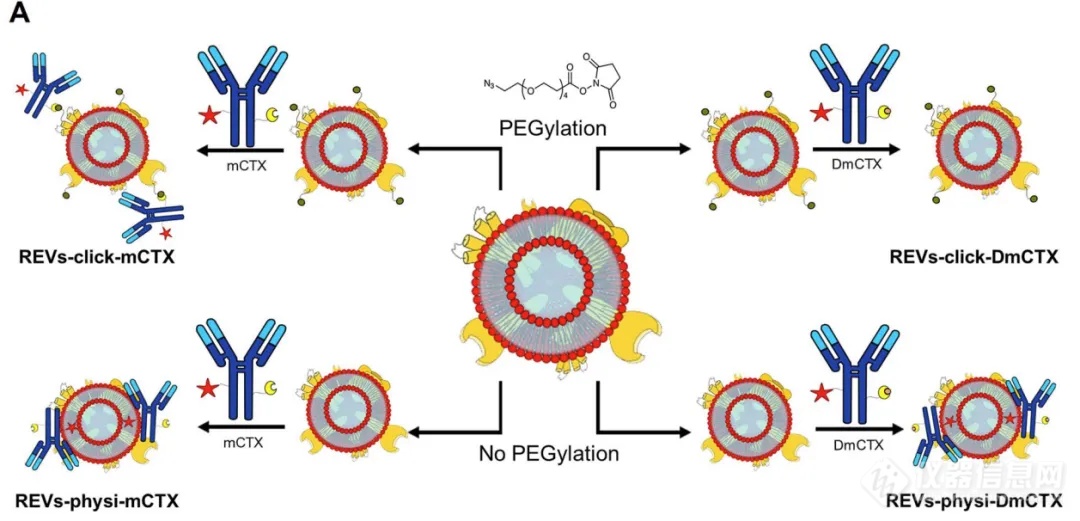
图3:抗体EV组装方法示意图
作者使用Biacore X100,将EGFR偶联在CM5芯片上,分别检测了EGFR与EGF、CTX、mCTX (modfied CTX) 、天然REVs、四种工程化REVs的亲和力。EGF、CTX与EGFR的亲和力均与文献报道相符 (67.3nM、1.8nM) ,而化学修饰则使CTX的亲和力降低,mCTX亲和力为3.6nM。在检测EGFR与外泌体的结合时,首先天然的REVs未观察到结合信号,化学吸附的REVs-click-mCTX的亲和力为0.17nM,高于mCTX十倍,且呈现典型的慢解离过程,物理吸附的外泌体REVs-physi-mCTX亲和力与REVs-click-mCTX相当。
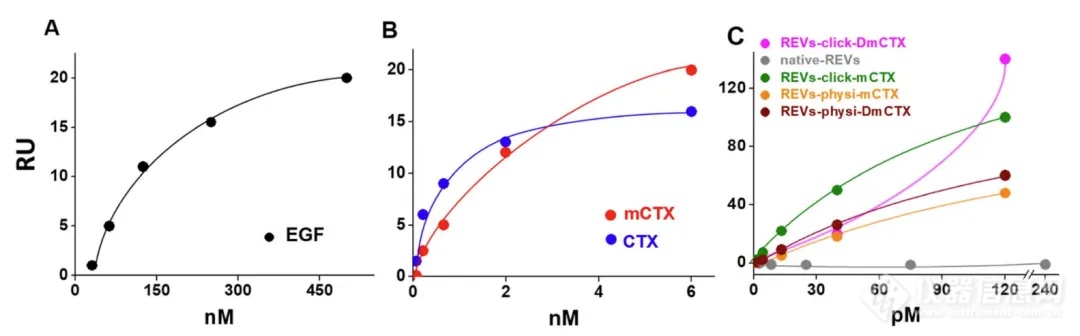
图4:Biacore X100检测EGFR与蛋白或REVs的亲和力
此外,作者还发现,同一张EGFR芯片检测中,REVs-click-mCTX的饱和结合信号Rmax比REVs-physi-mCTX高4倍,推测可能时由于物理吸附较弱,当mCTX与芯片表面的EGFR结合更强时,mCTX从REVs上脱落下来,牢牢地结合在芯片表面地EGFR上,并与REVs-physi-mCTX竞争性结合EGFR,最终导致芯片表面的最大结合量Rmax降低。而工程化的REVs-mCTX稳定性可能对体外囊泡摄取及其实际治疗应用具有重要意义,细胞实验发现REVs-click-mCTX对靶细胞表现出更好的结合和摄取能力。
外泌体广泛分布在血液与体液等液态标本中,通过检测其内容物或表面生物标志物等,可以进行精准的疾病诊断。锡耶纳大学研究团队发现黑色素瘤细胞在常氧和缺氧条件下都释放小细胞外囊泡sEV,但只有缺氧诱导的sEV表达CA-IX mRNA和CA-IX蛋白,据此开发一种ELISA检测方法,相关成果于2023年发表在International Journal Of Molecular Sciences[4]。
缺氧处理HEK293pRTS-CA9 cells获得sEVs后,为了鉴定其表面是否有CA-IX蛋白,作者使用Biacore分别检测了anti-CA-IX 抗体与CA-IX蛋白及sEVs的结合,确定了sEVs表面的CA-IX蛋白。
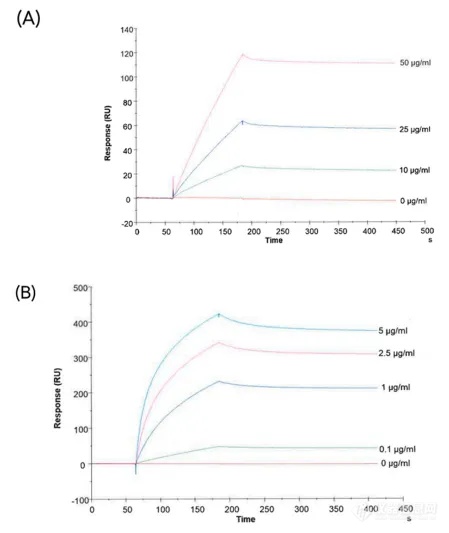
图5:Biacore检测anti-CA-IX抗体与CA-IX蛋白及sEVs的结合
外泌体等细胞外囊泡的功能研究,及其在在治疗、诊断领域的开发愈加火热,持续的技术和实验进展将会揭示更多其异质性和生物学功能的信息,促进其用于治疗和诊断疾病。Biacore作为高灵敏、高精准的分子互作技术,可以为各类型分子间的相互作用提供高质量的结合动力学、亲和力、浓度等数据,期待与广大用户共同发现更多新疗法,新应用。
参考文献

声明:本文为作者原创首发,严禁私自转发或抄袭,如需转载请联系并注明转载来源,否则将追究法律责任

检测病毒
分离纯化

灵活省时
广泛应用
咨询德泉兴业,即可获取相关产品信息和报价。
【Webinar 预告】肝脏类器官研究进展及应用分享
【邀请函】第七届酶标仪应用及软件操作高级培训班北京站开班,邀您报名!
【订购有礼】限时狂欢!电商专享商品上线,每单必得惊喜好礼!
酶标仪科普专栏丨第二期:荧光偏振(FP)介绍及应用
相关产品
上海美谱达UV-3200扫描型紫外/可见分光光度计
Leica徕卡DM750M正置显微镜
希森美康ExoCounter 全自动外泌体分析仪
智能化共聚焦高内涵成像分析系统
比利时 Bioruptor plus非接触式全自动超声破碎仪
DM3000德国徕卡leica生物显微镜
徕卡生物倒置显微镜LeicaDMi1
希森美康ExoCounter 全自动外泌体分析仪
梅特勒托利多pH 复合电极 LE438
Diagenode全自动核酸剪切仪Megaruptor ®3
化学发光成像仪Amersham ImageQuant 800
BIORUPTOR超声波细胞破碎仪new pico比利时Diagenode
美国博勒飞AMETEK Brookfield CTX质构仪
美国思拓凡 cytiva go蛋白纯化系统
ATS超高压均质机AH-D400

关注

拨打电话

留言咨询