表面等离子体共振 (SPR) 是一种广泛使用的无标记互作检测技术,用于研究生物分子的结合行为。自 20 世纪 90 年代商业化 [1] 以来,SPR 在技术开发和应用方面都取得了巨大进步。它已成为生物医学研究、生物传感器开发和药物发现的核心工具。在过去十年中,SPR 还与其他技术结合联用,例如电化学 (EC-SPR) [2]、液相色谱 (HPLC) 和质谱 (SPR-MS) [3],并已用于气相痕量检测(SPR-气相检测)。近年来最重要的发展之一是 SPR Microscopy (SPRM),这是一种将高分辨率光学显微镜与表面等离子共振相结合的技术。SPRM 兼具两种技术的优势,可直接对样品进行空间可视化定位分析,并实时测量结合亲和力和动力学。利用传统的(基于通道的)SPR技术,研究细胞膜蛋白与候选药物或其他配体的结合一直具有挑战性,因为从细胞中提取蛋白并将纯化的蛋白固定在 SPR 传感器上不仅耗时费力,而且改变了蛋白质的天然微环境。SPRM 通过将细胞直接固定在 SPR 传感器上,从而保持了蛋白质的天然状态,显著改善了此类测量的结果 [4]。此外,还可以确定和绘制每个细胞中膜蛋白的分布和局部结合活性。
在本技术说明中,着重介绍 SPRM 技术及其与传统 SPR 技术的比较。
1 传统(基于通道)SPR
基于流体通道的SPR检测模式是最常见的分子结合研究方法(图 1)。传感器顶部安装有多个通道的微流控模块,样品通过泵系统传输送到每个通道。配体分子被固定在每个通道的传感区域上,随后分析物分子被传输到每个通道中与特定配体结合。对每个通道的传感区域(紫色区域)的数据进行平均,以产生 SPR 传感图(如图 1 右侧所示)。每个通道在一次测量循环中都会生成一个传感图(或表面再生后的多个传感图),结合亲和力和动力学参数可从这些传感图中分析得出。

图 1 传统(基于通道)SPR模式
2 SPRM(高分辨率显微镜)
SPRM 是一种基于高分辨率成像的 SPR 模式。它提供明场光学图像和传感区域的 SPR 数据(亲和力和动力学常数)(图 2)。SPRM(例如 SPRm200)在图像的每个像素处生成一个 SPR 传感图,提供任何给定传感区域上结合事件的空间映射,并提供比传统 SPR 模式更多的信息。SPRM 不仅可用于传统的 SPR 结合分析测量,还可用于细胞对候选药物反应的异质性研究。由于其高空间分辨率(~ 1 µm),它可以监测和测量病毒、细菌的结合事件,而这些无法通过传统 SPR 模式直接测量。SPRM 在测量药物与天然状态下的膜蛋白相互作用方面尤其有效,因为蛋白质分子位于活细胞膜内。
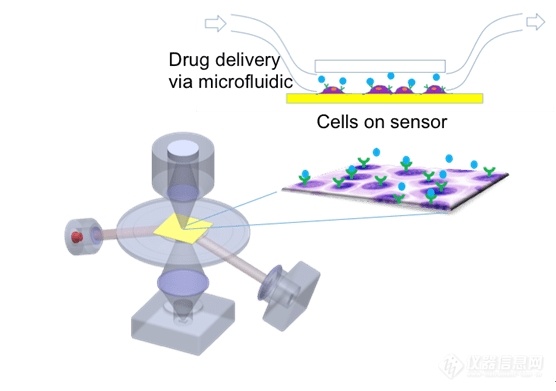
图 2 基于高分辨率成像的SPR模式
细胞在传感器表面孵育或固定,分析物或药物分子被传输到传感区域。图 3 显示了传感器上药物分子与细胞之间相互作用的示例。实时 SPR 图像 (3B,蓝色图像) 表示细胞受体与药物分子的相互作用或结合反应 (粉红色区域)。通过明场图像 (3A,绿色图像) 选择感兴趣的区域,生成传感图 (3C) 并分析得出结合信息。当选择许多不同的细胞区域时,可以用具有统计意义的数据确定细胞和细胞膜的异质性。
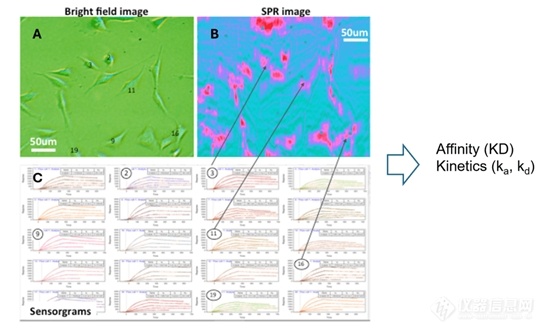
图 3 SPRM 同时提供明场图像 (A) 和 SPR 图像 (B)。结合参数由传感图 (C) 得出
总之,SPRM 提供了一种独特的功能来可视化细胞膜的结合活性。与传统的基于通道的 SPR 模式相比,SPRM 还具有额外的优势,即可以通过空间映射细胞膜蛋白天然状态下的结合亲和力和动力学,从而提供更多生物学相关信息。由于其高空间分辨率,SPRM 可用于监测其他表面发生过程,例如标记有生物分子的纳米颗粒的结合或纳米颗粒包被药物的递送。
3 SPRM与SPR要点比较
_ | SPR | SPRM(SPRm200) |
检测技术 | SPR | SPR显微镜、光学成像 |
传感器区域 | 平均通道面积 | 每个像素 |
样品递送 | 基于通道的微流控传输 | 微流控传输 |
样品类型 | 药物分子 蛋白质 脂质 DNA | 药物分子 蛋白质 脂质 DNA 细胞 病毒 细菌 纳米粒子 |
数据类型 | 每个通道的传感图曲线 | 每个像素的传感图曲线 明场光学图像与实时SPR图像 |
实际测量 | 亲和力 动力学常数 | 亲和力 动力学常数 细胞响应的异质性研究 纳米颗粒活性 明场图像 |
4 SPRM 200介绍
SPRM 200是美国BI公司细胞原位分子互作动态分析系统
应用
小分子药物或抗体药物与细胞膜蛋白(受体、离子通道等)原位结合分析;抗体药物与单细胞或多细胞的结合筛选;细胞结合统计学分布分析,开展细胞异质性研究;细菌或病毒与抗性药物的相互作用;其他分子与细胞/活细胞层面原位相互作用研究。
功能
亲和力测定;动力学分析;同步于SPR测量的光学成像;药物对多细胞或单细胞作用的研究;细菌或病毒与抗性药物相互作用的纳米级观察。
特点无标记
实时定量
细胞膜蛋白原位分析
细胞膜上指定区域分析
细胞或细胞膜异质性研究
电化学联合分析
参考文献
1. Liedberg, B et al, Biosens. Bioelectron. 10, i-ix, 1995
2. Patskovsky, S et al, Analyst, 139, 596-602, 2014
3. Nedelkov, D and Nelson, R, Trends in Biotechnology, 21, 7, 301-305, 2004
4. Wang, W et al, Nature Chemistry, 3, 249-255, 2011
CASY细胞计数:精准测量,助力糖尿病研究
CERO创新—微流控3D肠道肿瘤模型为纳米药物递送开辟新路径
类器官构建
无标记3D细胞分析系统:提升iPSC与类器官研究的精准性与可靠性

关注

拨打电话

留言咨询