对于正相Flash纯化而言,由于Biotage独家的上样杯技术,保证了上样方式的多种多样,每一种的上样方式都会产生不同的柱效表现。
对于flash而言,反相的应用在过去的十年时间里,有着非常快速稳健的成长和发展。而反相受制于上样方式的单一性,进样溶剂的选择变成了反相flash纯化的一个非常关键的要素,值得探讨。
本文主要就一些现在数据的基础上对进样溶剂对反相Flash纯化对了阐述和讨论。
在液相色谱分离中,反相色谱技术经常被用来分离大极性分子或者容易与正相硅胶形成死吸附的分子。如果你最近正在进行制备级的反相分离纯化,那么不管是水,甲醇还是乙腈,都会存在一些流动相的限制,和正相体系一样,每一次的纯化分离都希望通过极性最弱的流动相体系来达到最可能高的浓度。但是很多情况下,反相体系中样品在流动相体系中的溶解度一直是一个非常大的挑战。
如何选择呢?反相体系中水是最常用的流动相体系之一,但是溶解性并不好。
Weak solvent | Strong solvent | Strong solvent strength |
Water | Methanol | 1.0 |
Water | Acetonitrile | 3.1 |
Water | Tetrahydrofuran | 3.7 |
通常情况下,我们都是通过流动相来溶解样品,流动相比例的选择至关重要,极性太高,影响分离效果,极性太低,溶解性不好。那么这是否就意味着不能直接使用纯甲醇,纯乙腈,那么丙酮呢?我们发现,在1g/mL的高样品浓度的条件下,如果使用0.5%柱体积的进样量进行分离的话,可以得到一个比较好的分离结果。
但是,当进样量溶剂比例增加的时候,样品溶剂的增多会影响色谱的动力学分配,降低分离效果,同时减少色谱柱载样量。
为了突出溶剂选择的重要性,我们对五种不同极性化合物进行反相分离实验对比(methyl paraben, butyl paraben, naphthalene, 1-nitronaphthalene, 3,5-dibenzyloxyacetophenone)。分别称取1g样品(各五种)合在一起溶于5mL所选溶剂(methanol, acetonitrile, acetone, DMF, and DMSO)中,得到五种不同溶剂的样品,在使用之前再通过相同溶剂以1:1的比例对各个样品进行稀释,得到五种相同浓度的溶剂样品。进样量为0.1mL,使用色谱柱型号为12 g Biotage® Ultra C18,梯度方法从起始的55%甲醇升至结束时候的100%甲醇。
Test mix component | Amount |
Methyl paraben | 1 gram |
Butyl paraben | 1 gram |
Naphthalene | 1 gram |
1-Nitronaphthalene | 1 gram |
3,5-Dibenzyloxyacetophenone | 1 gram |
Dissolution solvent | Stock concentration | 1:1 dilution concentration | Injection volume |
Methanol | 1 g/ mL of each component | 1 mL methanol stock diluted in 1 mL of methanol | 0.1 mL |
Acetonitrile | 1 g/ mL of each component | 1 mL acetonitrile stock diluted in 1 mL of acetonitrile | 0.1 mL |
Acetone | 1 g/ mL of each component | 1 mL acetone stock diluted in 1 mL of acetone | 0.1 mL |
DMF | 1 g/ mL of each component | 1 mL DMF stock diluted in 1 mL of DMF | 0.1 mL |
DMSO | 1 g/ mL of each component | 1 mL DMSO stock diluted in 1 mL of DMSO | 0.1 mL |
实验一:使用甲醇作为进样溶剂,结果令我们很吃惊,对于甲醇而言,样品的溶解性很好,同时0.1mL的进样体积只占到0.6%的柱体积,但是结果并不和我们预想的一样,产生了拖尾现象,同时峰3和峰4 之间也没有得到很好的分离。
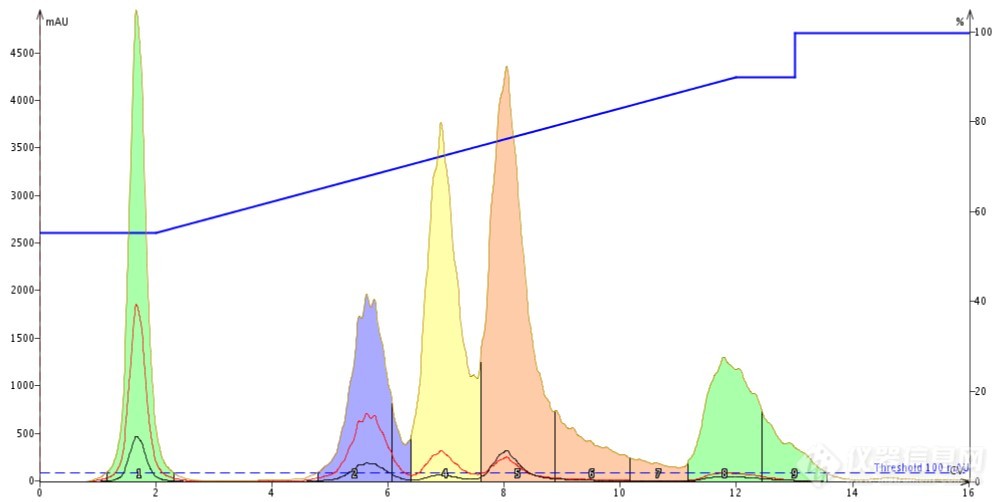
Figure 1. 50mg混合样品反相分离梯度,流动相:水-甲醇;进样量0.1mL;分离度不够,伴有拖尾现象。
实验二:使用乙腈作为进样溶剂,由于乙腈更加强的极性,正如我们预期的一样,分离效果比甲醇条件更好,如Figure 2,峰型更尖,但是不如意的地方就是峰之间较低的分离度仍然没有改善。
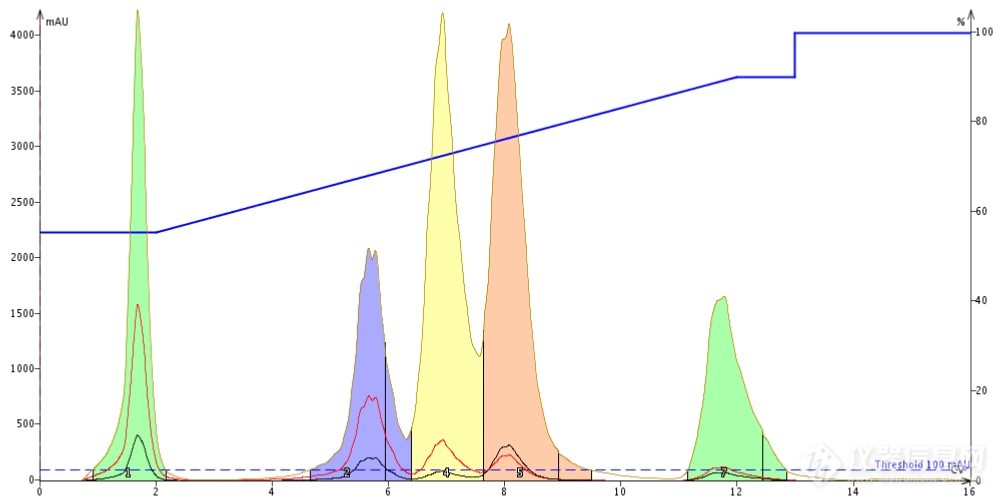
Figure 2. 50mg混合样品反相分离梯度,流动相:水-甲醇;进样量0.1mL;进样溶剂:乙腈;峰3和峰4 之间的分离度仍然较低。
在以前的实验中,我们讨论过,对于丙酮是一个非常好的溶剂选择,不管是在水相还是在有机相中,它都有着非常好的兼容性,所有在正相和反相应用中都可以进行广泛使用。
从实验结果可以发现,丙酮的分离效果也是明显优于甲醇的,但是丙酮也带有比较明显的拖尾现象。
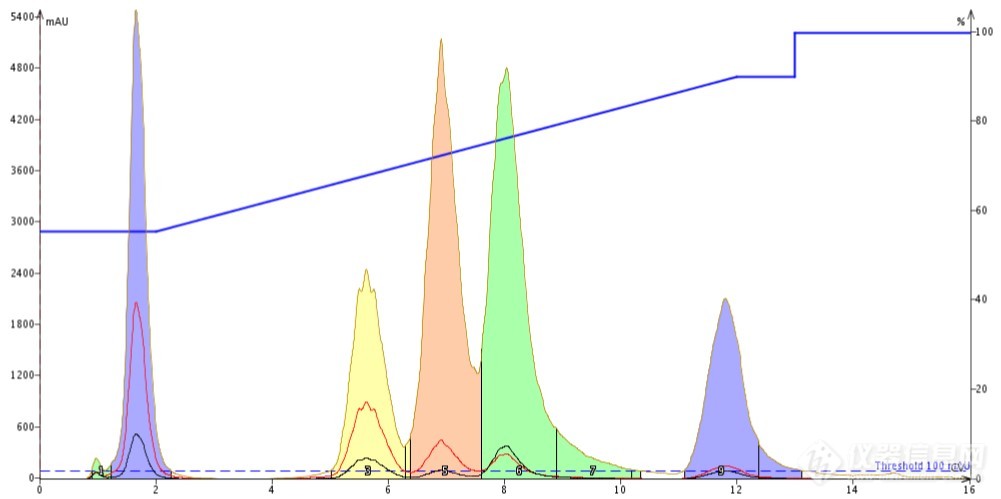
Figure 3. 50mg混合样品反相分离梯度,流动相:水-甲醇;进样量0.1mL;进样溶剂:丙酮。优于甲醇,但仍旧有拖尾。
最后我们将DMF和DMSO作为进样溶剂进行了测试,这两种溶剂的极性都很大,样品的兼容性都非常广泛,它们自身的很多特性都促成了其在多肽和有机合成当中的广泛应用。但是很多化学家都认为直接用DMF和DMSO作为进样溶剂进行注射,会对样品的分离产生负面的影响,所以我们将这两种溶剂加入大我们的实验当中来检测这一说法是否真的如此。
有趣的是,DMF和DMSO的加入都促进了样品的更好的分离,峰型更好,同时拖尾现象被有效抑制!
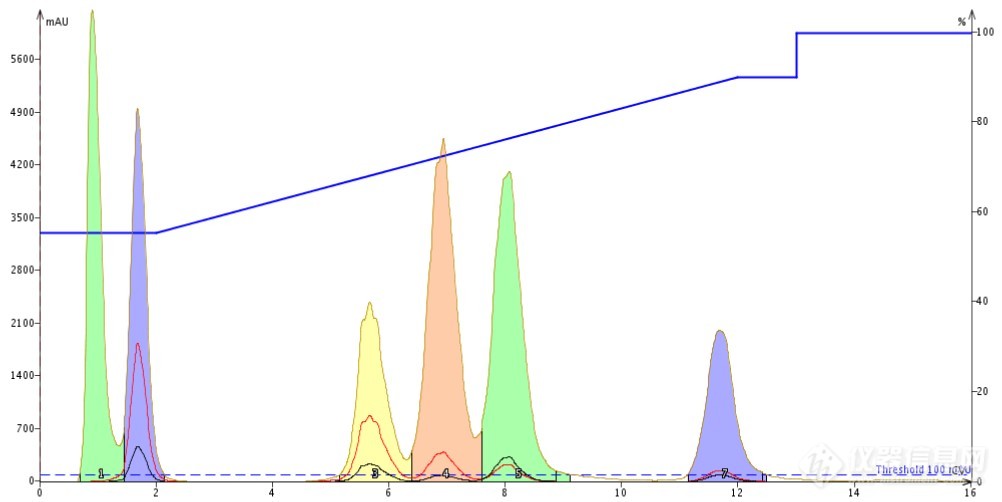
Figure 4. DMF 使得峰型和分离度都取得了较大的改善。
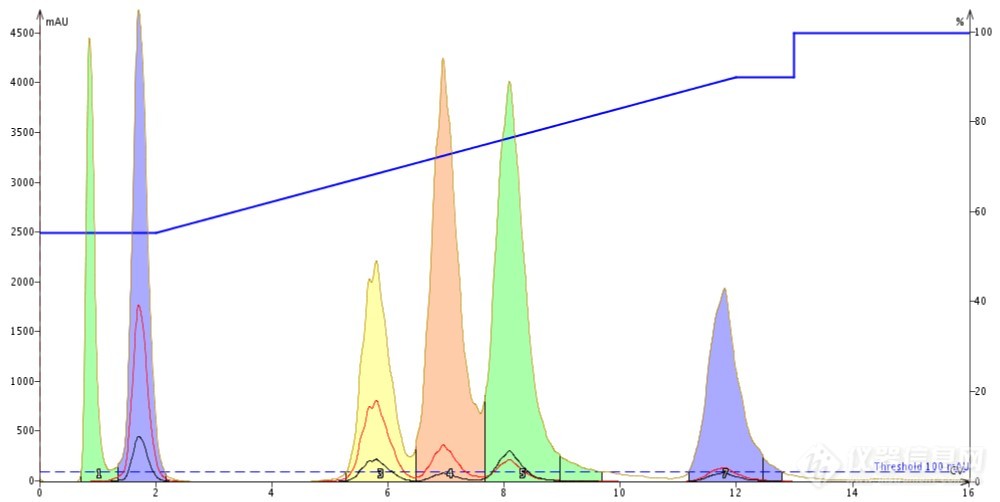
Figure 5. DMSO 使得峰型和分离度都取得了较大的改善。
那么为什么会产生这么多不同的结果呢?我们来看看每一个溶剂本身。
甲醇:质子型溶剂,布朗斯特Bronsted酸,流动相的一部分,分离效果最差。
乙腈:非质子型溶剂,路易斯Lewis碱,可以将峰型塑造得更尖。
根据这些信息,我们还不知道溶剂极性以及相对酸度是否在分离过程中起到一定的作用,继续往下看。
丙酮是非质子型溶剂,路易斯Lewis酸,它的色谱分离结果明显优于甲醇,但是不如乙腈。
但是对于DMF和DMSO 呢?这两种溶剂的分离效果都明显优于另外三种,这两种都是非质子型溶剂,与乙腈和丙酮一致,但这并不能解释为什么DMF和DMSO得到了更好的分离效果。或者我们可以解释为这两种溶剂可以使得样品和C18能够更充分的接触和交换。由于溶解样品溶剂的高极性,使得样品更愿意和C18接触,而不是DMF或者DMSO,从而使得分离更加完全而充分。
在我们的研究中,我们发现DMSO和DMF都有着非常高的负值LogP酯水性分配系数,数值越大,溶剂的极性越强。对于DMF,Log P 是 -2.03;对DMSO,Log P 是 -1.01,而甲醇,乙腈和丙酮(MeOH, MeCN, acetone),他们的Log P分别为:-0.77,-0.54,-0.24,都比DMF和DMSO有着更强的亲脂性。
Dissolution solvent | Log P | Protic/Aprotic | Acid/Base |
Methanol | -0.77 | Protic | Acid |
Acetonitrile | -0.54 | Aprotic | Base |
Acetone | -0.24 | Aprotic | Acid |
DMF | -1.01 | Aprotic | Base |
DMSO | -2.03 | Aprotic | Base |
因此,基于我们的数据分析,在起始谱带展开的阶段,Log P对分离结果起着至关重要的作用,溶解样品溶剂的选择在色谱分离中,至关重要。
通过我们实验的结果与讨论,或许可以给您在反相色谱分离中,提供一个全新的视角和改善方法。
Biotage助力药物分子开发全流程 ——访美国贝勒医学院贾斯汀·安林(Justin Anglin)博士
瑞典Biotage AB公司与山东英盛生物技术有限公司签署针对中国临床质谱应用市场的战略合作协议
拜泰齐完成对PhyNexus的收购
拜泰齐收购PhyNexus 加强实验室分子生物纯化领域
相关产品
Selekt Enkel 快速色谱仪
Biotage Selekt 快速制备液相色谱
Syro II 全自动多肽及有机合成平行工作站
TurboVap 多功能全自动样品浓缩仪
Biotage V10 Touch超高速溶剂蒸发工作站
Biotage Alstra 全自动微波多肽合成系统
Biotage Extrahera 全自动样品前处理系统
Biotage Isolera Dalton 2000制备液相
Biotage Isolera LS高通量快速纯化系统
Biotage Isolera Prime快速制备液相色谱
Biotage Isolera One 快速色谱仪
Biotage Initiator+微波合成仪
Biotage 全自动氮吹浓缩仪LV型
Biotage 全自动氮吹浓缩仪96型
Biotage 全自动氮吹浓缩仪II型

关注

拨打电话

留言咨询