
方案摘要
方案下载| 应用领域 | 其他 |
| 检测样本 | 其他 |
| 检测项目 | |
| 参考标准 | 【预约试拍】超高分辨显微镜在神经科学中的应用(一) |
本文译自Werner等科学家在美国化学学会会刊(ACS)上发表的一篇综述,比较详实系统介绍了超高分辨率显微技术在神经科学上的最新应用进展。我们在此文基础上进行了编译整理。因文章较长,我们将分期陆续介绍。本期介绍第一部分。
本文译自Werner等科学家在美国化学学会会刊(ACS)上发表的一篇综述,比较详实系统介绍了超高分辨率显微技术在神经科学上的最新应用进展。我们在此文基础上进行了编译整理。因文章较长,我们将分期陆续介绍。本期介绍第一部分。
 《Super-resolving Microscopy in Neuroscience》
《Super-resolving Microscopy in Neuroscience》
荧光成像技术在我们理解神经系统中起着关键作用。各种超分辨率显微镜方法和专用荧光探针的出现使得能够以迄今为止无与伦比的分辨率直接洞察细胞亚区室中的神经元结构和蛋白质排列。

成像技术是推动生命科学几乎所有学科基础研究的核心平台。在神经科学中,共聚焦显微镜在过去的几十年中构成了用于分析神经元组织的标准荧光成像技术。固定神经元样本的激光扫描共聚焦显微镜提供了单个细胞水平上的三维和多色图像,直到树突结构的分辨率。作为补充,电子显微镜(EM)可用于获得神经元和亚室超微结构的信息,并用于脑内的连通性分析。EM非常适用于神经元突触和囊泡、细胞器和膜构象的结构分析。然而,由于靶特异性标记的方法限制,基于EM的复杂样品中的蛋白质和特异性电子密度签名的识别是有限的。作为理解神经元功能的进步,包括双光子显微镜在内的几种活体视频显微镜应用的发展使得神经元细胞培养物、器官型切片培养物的活细胞成像和动物模型的活体成像成为可能。同时,新的荧光染料、功能探针和荧光蛋白以及光遗传学方法和光学致动器(如笼状化合物)不仅允许表征,而且允许从单分子水平到整个神经系统操纵神经元及其相互作用。然而,荧光显微图像中可见细节的水平,即图像分辨率,仍然受到衍射极限的限制。
一个多世纪以来,阿贝衍射极限(定义为λ/2NA,其中λ为波长,NA为显微镜物镜的数值孔径)决定了光学显微镜的分辨率极限,并禁止分离距离小于200 nm的两个光斑。在过去二十年中,超分辨显微术(Super Resolution,SR,下文中出现SR均指超高分辨率显微成像技术)已经发展成为细胞亚衍射分辨率荧光成像和细胞器结构研究的一种非常强大的方法。SRM方法现在可以提供远低于光学显微镜衍射极限的空间分辨率,使人们能够深入了解固定的和活的神经元细胞培养制备物和组织中蛋白质的空间组织和相互作用。

2.1.衍射屏障及其对神经科学的影响
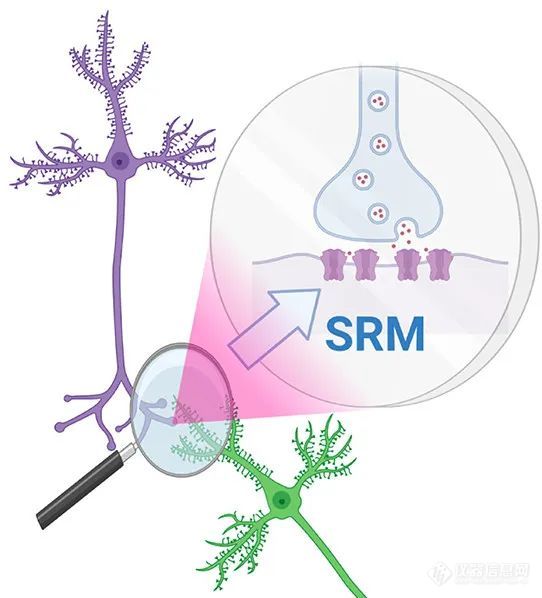
人类大脑包含800多亿个神经元,每个神经元由数千个突触连接。因此,它构成了复杂神经元网络最突出的例子。这些网络的主要组成部分,如突触神经末梢,其空间维度接近于由约200 nm的衍射势垒所施加的分辨率限制。例如,突触活性区(释放递质的突触前细胞基质的特化区)的直径通常约为300 ± 150 nm。10突触囊泡作为运输和释放递质的关键元件,其直径甚至要小约10倍。直径为40− 50 nm。递质被释放到宽度为20−50 nm的突触间隙中,与突触后受体结合。因此,胞吐机制和跨突触信号传导的组织结构在传统光学显微镜下仍然很大程度上是隐藏的,因此需要分辨率提高约10倍(图1)。此外,位于小尺寸突触区室内的突触信号传导所涉及的大量不同分子产生了对显微镜研究具有挑战性的分子密度分布。例如,对于较小的突触,兴奋性突触可以包含几百个小泡,对于大的苔藓状纤维结,兴奋性突触可以包含多达几千个小泡,每个小泡含有多达104 - 105个递质分子。在这些小泡中,约10 ± 5个与释放位点对接,释放的递质平均遇到0−20 N-甲基-D-天冬氨酸和0−200 α-氨基-3-羟基-5-甲基-4-异恶唑丙酸受体(分别为NMDA-Rs和AMPA-Rs)在突触后侧被320 ± 130个突触后密度蛋白95(PSD-95)分子包围。

由于加速电子的波长要短得多,因此EM是唯一能够解析突触纳米级特征的方法。然而,传统EM创建了具有优异超微结构分辨率的电子密度图像,但所需的组织制备和固定以及靶向特异性标记的方法限制极大地限制了蛋白质鉴定和神经元示踪。荧光显微镜可以很容易地进行蛋白质选择性标记,但可见光(400 - 700 nm)的衍射会使所得图像模糊,并妨碍对底层纳米结构的分析。
2.2.1. 确定性集合超高分辨率成像方法(Deterministic Ensemble SR-Imaging Methods)
用探测器阵列代替单点探测器并打开针孔,可以将CLSM的空间分辨率提高 2倍。CLSM测量每个扫描位置探测器每个点的荧光信号。在应用适当的算法后,生成分辨率提升的图像。这些所谓的像素重分配方法包括图像扫描显微镜(ISM)、重扫描共聚焦(RSC)、光学光子重分配(OPRA)、AiryScan和即时结构照明显微镜(iSIM)。对于信号检测,使用了诸如CCD相机、光电倍增管阵列、单光子雪崩二极管阵列和六角光纤束等探测器阵列。
结构照明显微镜(SIM)在光路中插入光栅,产生相干光束与样品发生干涉,从而产生横向和轴向不同的新照明模式。然后可以使用傅里叶变换提取这种新类型的信息,从而在所有三维空间中实现空间频率解混和分辨率加倍。SIM对样品制备的要求最低,并且与所有传统的荧光探针兼容,这些探针表现出最低的光稳定性,并且可以容易地扩展到多色成像。
然而,当记录三维叠层或用于长时间成像时,强烈建议荧光团的光稳定性。此外,SIM需要的辐照强度显著较低,因此是活细胞SR实验的首选方法。为了实现更高的分辨率,非线性SIM(NL-SIM)已经引入了通过图案化饱和或荧光激发或图案化耗尽的光可切换染料。然而,对染料的开关特性的苛刻要求限制了NL-SIM对于常规生命科学实验的适用性。非线性SIM还需要更多的图像,因此实际上仅限于2D成像。另一方面,掠入射(GI)-SIM显示出高达每秒266帧的快速超分辨率成像以及100 nm的分辨率,揭示了细胞器动态的前所未有的细节。结构化照明的局限性在于其对波长的普遍依赖性、与其他SR成像技术相比的低分辨率增益,以及对系统稳定校准的需要。最后,后处理需要先验质量检查,以避免伪影,例如由于高背景信号或低效标记导致的低对比度图像而产生的人造蜂窝图案。
一种实现高得多的空间分辨率的成像方法是通过受激发射耗尽(STED)显微镜进行的超分辨率成像。在此,具有高斯分布的激发激光束被至少保留一个局部强度最小值的耗尽激光束覆盖,并用于通过扫描点外围的受激发射使荧光团返回基态。这导致了纳米级的焦点,其尺寸与耗尽光束的强度成反比,这直接转化为STED显微镜的分辨率能力,遵循:
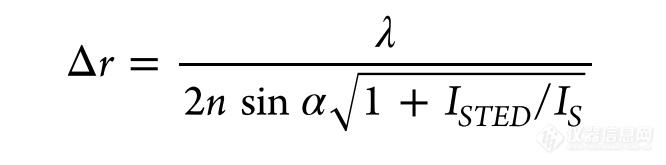
其中λ为波长,n为折射率,α为物镜的收集角,ISTED为STED光束的辐照强度,IS为饱和强度。因此,可以通过调整耗尽激光强度来调节分辨率,在定制设计的STED显微镜中,分辨率可达到30 − 80 nm。STED显微镜模式可通过应用连续波、脉冲激发或时间门控方法来区分。采用脉冲激光的STED显微镜可降低激发能量,从而减少实时成像中的光毒性效应。通过提取隐藏在荧光团的光子到达时间中的空间信息,STED显微术中的时间选通检测也可以在较低的平均功率下操作。STED在使用商业系统时提供用户友好的高分辨率成像,无需进一步的数据后处理。实时成像(如体内脊柱动态)已得到广泛认可,但快速动态成像仍是一种点扫描方法,因此仅限于小帧尺寸。40高激光强度可能导致光损伤,但Dymin扫描和救援STED等实施方案可减少光损伤。在Dymin STED中,在共焦模式下扫描时确定最低可能的STED光束强度。根据样品的标记密度,这产生20至100倍的低STED光束强度。救援STED通过减少荧光团状态跃迁到需要分离相邻特征的区域的实施,同样减少了光漂白,因此光漂白效应减少了8倍。STED的另一个限制是其对光稳定荧光团的依赖性,因为在高激光强度下光漂白会成为问题。这对于长期动力学研究和三维叠加的获取尤其具有挑战性。值得注意的是,最近的发展通过使用荧光团标记的寡核苷酸(与连接到靶蛋白结合探针的互补寡核苷酸短暂结合)或非结合荧光团产生细胞结构的清晰负像,从而避免STED光漂白问题。两种方法,基于DNA的STED成像和超分辨阴影成像(SUSHI)分别通过荧光团标记的寡核苷酸的恒定交换和高浓度的非结合和自由扩散荧光团来防止光漂白。SUSHI已成功用于活体器官型脑切片细胞外间隙和神经纤维网结构和动力学的STED成像。
如果代替标准荧光团而使用具有毫秒寿命或更长的两个稳定状态的可逆可切换荧光团,则照明强度可显著降低。可逆可饱和/可切换光学线性荧光跃迁(RESOLFT)已通过可逆可切换荧光蛋白(reFP)实现,并成功应用于活器官型海马脑切片中树突棘的超分辨率成像。
2.2.2. 随机单分子SR成像方法(Stochastic Single-Molecule SR-Imaging Methods)
2.2.3. SMLM-点累计纳米成像技术(PAINT,Point Accumulation for Imaging Nanoscale Topography)
图2.原代神经元中几个神经元靶点的多重交换-PAINT
2.2.4.定量SMLM
与所有其他超分辨成像技术相比,如果每个靶分子都可以被单独标记和定位,则SMLM还可以提供关于分子分布和分子绝对数量的单分子信息。然而,内源性蛋白质的定量免疫标记仍然是一个挑战,并且多种标记抗体的不同数量的定位可能使数据解释复杂化。另一方面,实现内源表达水平的困难以及FPs的缓慢成熟同样会使定量PALM成像恶化。然而,可以进行特别设计的对照实验以支持拷贝数估计并提取关于生物学靶结构的分子组织的真实信息。在适当算法的帮助下,SMLM可以提供关于拷贝数、聚类、共定位和复杂化学计量的数据,用于生成定量模型和模拟。此外,通过结构信息与功能突触参数的相关性也可以实现定量,例如通过生物细胞素标记膜片钳神经元。在这方面,内源性大麻素信号传导已经通过修补神经元的链霉亲和素后标记的STORM成像结合CB1受体的免疫标记,随后在GABA能海马轴突末梢内对其进行定量来研究。本研究发现,与树突投射中间神经元相比,体周投射中间神经元的CB1受体密度更高,活动区更复杂。
在黑腹果蝇中,神经肌肉接头处内源性Bruchpilot(Brp)分子的数量已经89使用抗体滴定参考实验,野生型神经肌肉接头活性区细胞基质中存在的Brp蛋白数量已被确定为约137,其中四分之三组织在约15个七聚体簇中。结合从相同组织样本记录的电生理学数据,这些数据提供了关于Brp组织如何控制活动区功能的见解。每个活动区Brp蛋白的估计数量已通过定量DNA-PAINT(qPAINT)实验得到确认,其中DNA纳米结构已用作校准参考。此外,定量dSTORM实验证明,每个活动区Brp蛋白的数量和分布受突触结合蛋白-1,的影响,突出了活动区递质释放的复杂性。在最近的一项研究中,使用Alexa Fluor 532和Alexa Fluor 647进行免疫标记的双色dSTORM已被用于量化小鼠小脑平行纤维活性区的4型代谢型谷氨酸受体(mGluR 4)的纳米级组织(图3)。本研究还使用了抗体滴定参考实验,以估计每个活性区平均含有约35个排列在小纳米域中的mGluR 4分子。此外,mGluR 4经常被发现与munc-18-1和CaV2.1通道非常接近,这支持了mGluR 4与这些蛋白质相互作用以调节突触传递的观点。这些研究显示了神经科学中定量SMLM研究的潜力,而作者没有声明其完整性。可以预见,定量SMLM的进一步发展将为突触前和突触后蛋白的组织和结构-功能关系提供有价值的信息。
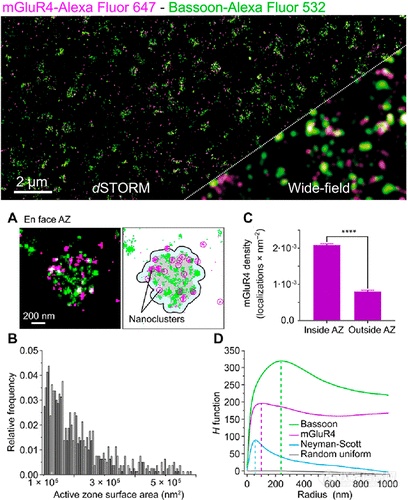
图3.在小鼠小脑切片中使用双色dSTORM记录定量代谢型mGluR4受体定位
2.2.5. 组织三维(3D)SMLM
力显智能现已发布的超高分辨率显微成像系统 iSTORM,成功实现了光学显微镜对衍射极限的突破,使得在20纳米的分辨率尺度上从事生物大分子的单分子定位与计数、亚细胞及大分子复合物结构解析、生物大分子生物动力学等的研究成为现实,从而给生命科学、医学等领域带来重大突破。

关于我们
About us
宁波力显智能科技有限公司(INVIEW)是专业从事超高分辨率显微技术和产品研发的科技企业,依托复旦大学的自动控制、新一代信息技术及香港科技大学的生物、光学、图像处理等的技术,拥有光学、生物、自控、机械、信息技术等多领域交叉学科技术团队,将2014年诺贝尔化学奖技术产业化,推出了超高分辨率显微成像系统iSTORM、细胞智能监控助手赛乐微等一系列产品,帮助人们以前所未有的视角观察微观世界,突破极限,见所未见。


【应用实例】使用随机光学重建显微镜STORM对皮质下白质进行超分辨率成像
【应用实例】超分辨率显微镜在观察革兰氏阳性菌的细胞外囊泡生物中的应用
用STORM成像揭示细胞间隧道纳米管(TNTs)的结构和组织
相关产品

关注

拨打电话

留言咨询