一、 艾玮得生物 创新科技守护心脏健康
在医疗科技日新月异的今天,心脏器官芯片作为一项前沿技术,正逐步成为守护人类心脏健康的“秘密武器”。艾玮得这项技术不仅为药物研发提供了更为精准、高效的平台,还极大地推动了心血管疾病研究方法的进步。
二、 心脏器官芯片: 模拟真实心脏的“微缩版”
心脏器官芯片利用微流控技术,将多种心脏细胞类型(如心室肌细胞、心房肌细胞、成纤维细胞和内皮细胞等)集成在芯片上,模拟心脏的三维结构和细胞间相互作用。提供比传统2D细胞培养更真实的生理环境,同时能够精确控制营养物质和废物的流动以及氧气浓度和剪切应力,模拟体内的血液循环和不同条件下心脏状态。这种高度仿真的环境,使得心脏器官芯片能够精准模拟心脏在生理和病理条件下的反应,为药物筛选和疾病模型开发提供了强大的工具。
三、药物研发的新利器
在药物研发过程中,心脏毒性是一个不容忽视的问题。传统的动物模型由于存在种间差异,往往难以准确预测药物在人类中的心脏毒性反应。动物心肌细胞和人类心脏在离子通道和特征蛋白方面存在巨大差异,影响其在药物心脏毒性预测中的有效性和准确性。此外,2D心肌细胞培养无法重现心脏组织的复杂三维结构和细胞间相互作用,无法模拟且表现出功能特性,如钙处理能力和收缩力,同样影响药物心脏毒性和药效学评估。而心脏器官芯片则能够克服这一难题,它能够在体外模拟人类心脏的反应,从而帮助科学家在药物研发的早期阶段就识别出潜在的心脏毒性风险,大大节省了研发成本和时间。
四、艾玮得生物 心脏器官芯片相关模型
01 心脏类器官模型
艾玮得已建立高效、稳定的心肌类器官分化平台,明场观察可见心肌类器官具有空腔结构(图1),这些腔室类似心脏在人体中发育过程中形成的心管腔和早期左心室腔结构。
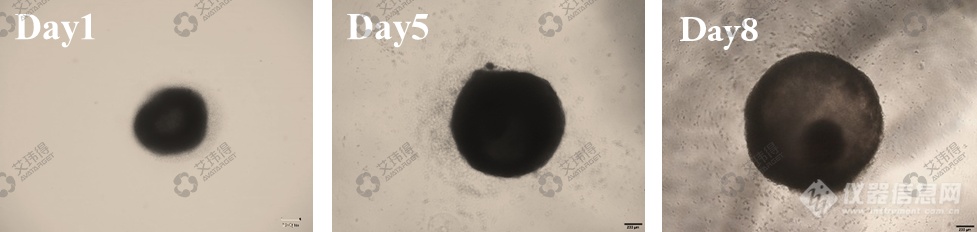
图1 心肌类器官明场影像
通过免疫荧光染色可观察到α-actinin、cx-43高表达,并且α-actinin成极性排列结构。表明心肌类器官内部连接紧密、结构完整(图2,图3)。
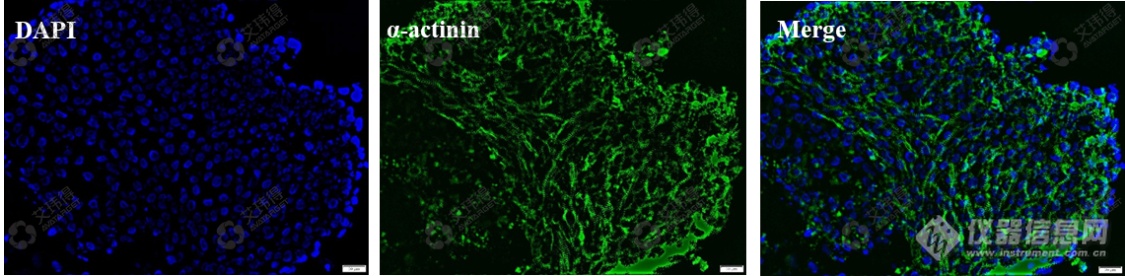
图2 心肌标志物α-actinin免疫荧光鉴定
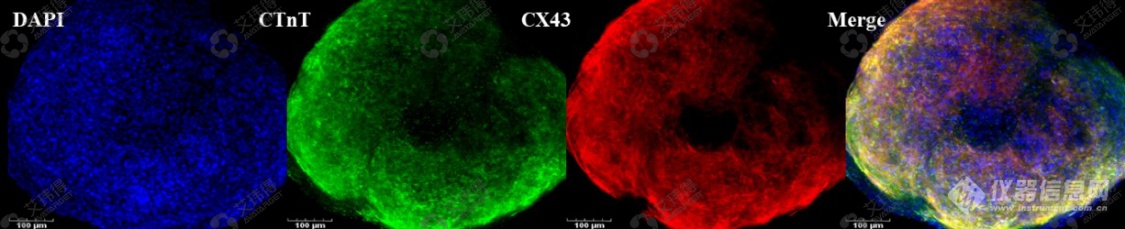
图3 心肌标志物cx-43免疫荧光鉴定
通过心肌RNAseq和scRNAseq结果显示,人体心脏中关键离子通道基因、主要心脏细胞基因均有表达。本体系获得的心肌类器官同时包含心房肌细胞、心室肌细胞、心脏成纤维细胞(图4)。
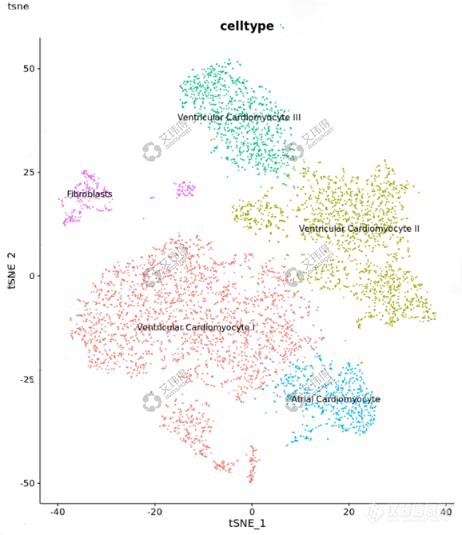
图4 心肌类器官细胞类型及关键基因鉴定
02 心衰模型
通过化合物诱导和低氧诱导两种方案,艾玮得成功构建两种心肌类器官心衰模型,结果显示,在两类心衰模型中均出现了心肌收缩力下降及心衰标志物NPPB上升,证明了两类心衰构建成功(图5、6)。
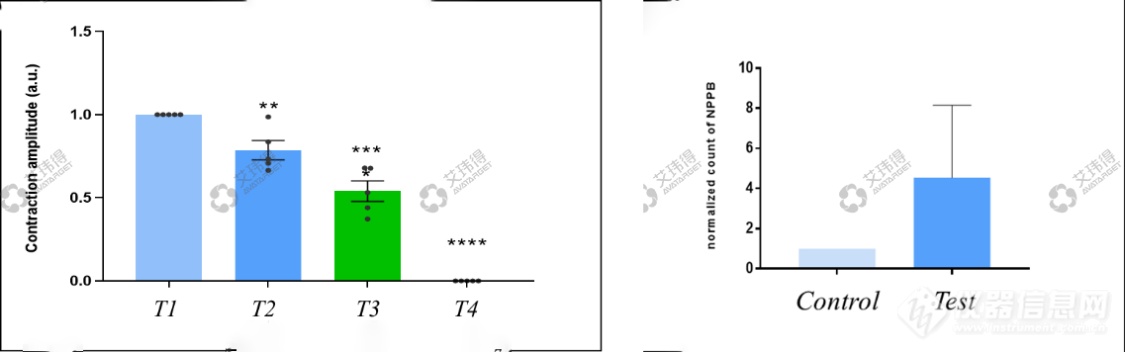
图5 低氧心衰模型构建
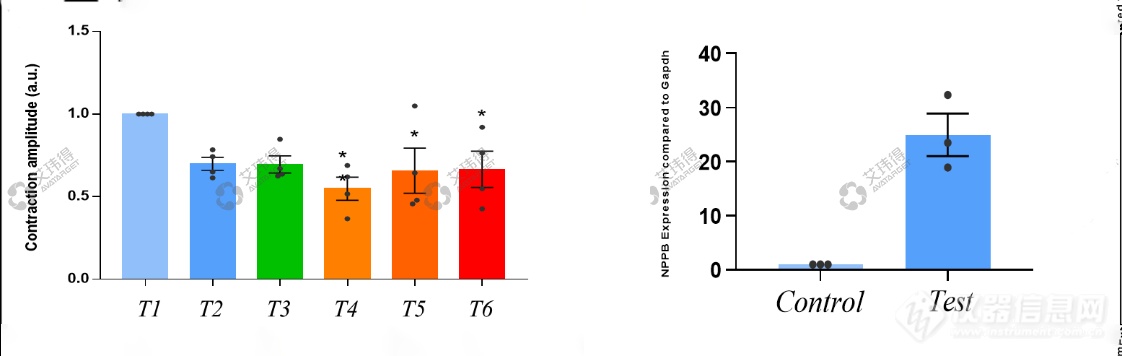
图6 化合物诱导心衰模型构建
03 心肌类器官模型
选取单腔膜式芯片或高通量膜式芯片,在芯片上层加入水凝胶,心肌类器官固定于水凝胶上,在上层通道加入心肌类器官培养基,培养24 h;在芯片下层加入血管内皮细胞,贴壁24 h,在下层通道加入血管内皮细胞培养基,流动培养3-7天。所构建的心肌类器官芯片可用于药物测试,或疾病模型开发。
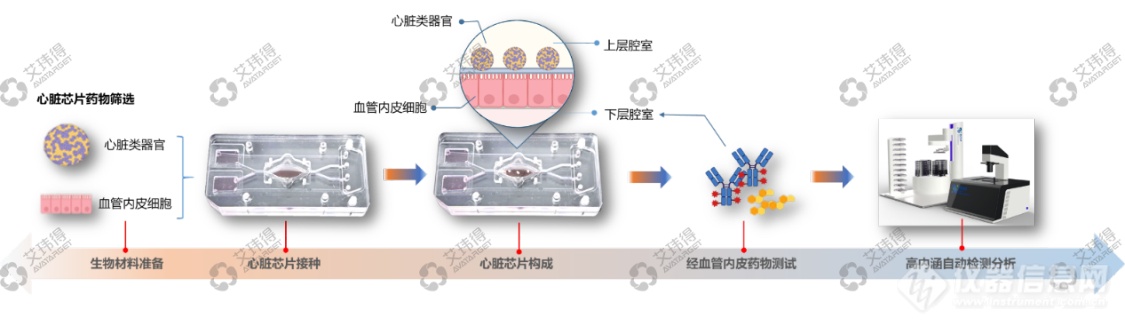
心肌类器官芯片应用于离子通道及功能性药物检测、钙信号检测如图7、8所示。
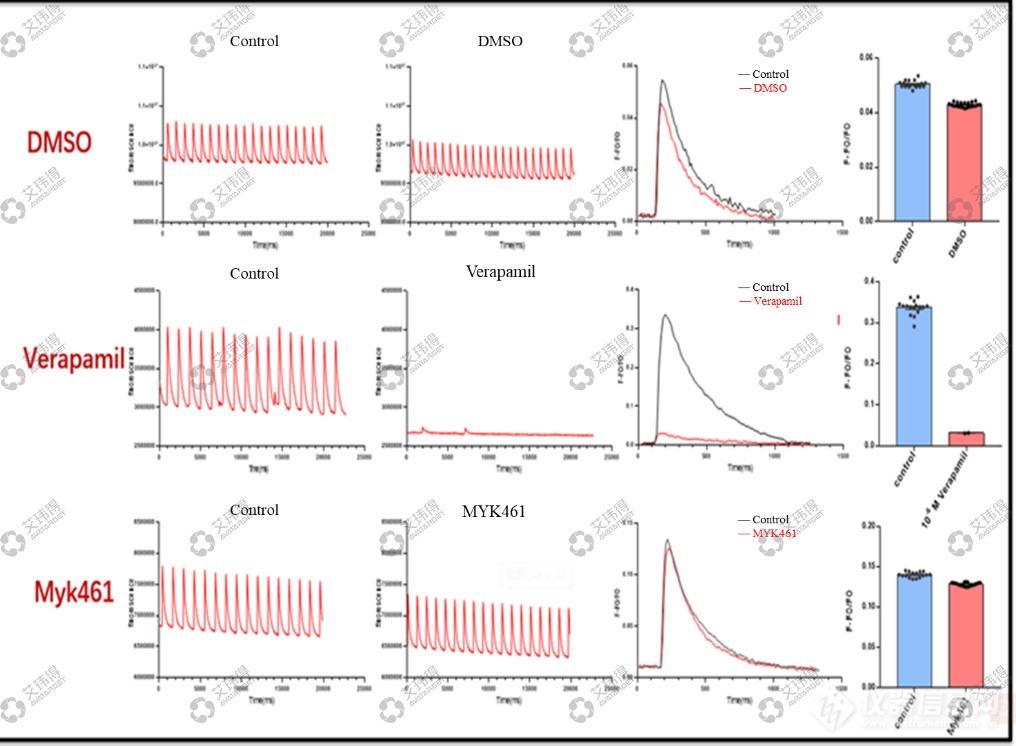
图8 心肌类器官芯片应用于钙信号检测
五、 成功案例
01 心脏相关药物高通量筛选
艾玮得心肌类器官芯片在国内首次应用于药企药效筛选,为恒瑞研发心肌肥大治疗药物提供了一个理想的试验平台。2023年5月,恒瑞医药HRS-1893片获批开展临床试验,HRS-1893通过特殊机制抑制心肌过度收缩,拟用于治疗肥厚型心肌病以及心肌肥厚导致的心力衰竭,首次将类器官芯片数据突破到CGT药物以外领域。
02 药物心脏毒性检测
艾玮得心肌类器官芯片也可以用于心脏毒性检测,在针对几种临床不良率高的肿瘤药物检测中,如图9所示在一定的药物浓度下,心肌类器官芯片均检测到了显著的收缩抑制,符合临床病人用药后出现的心衰不良反应。
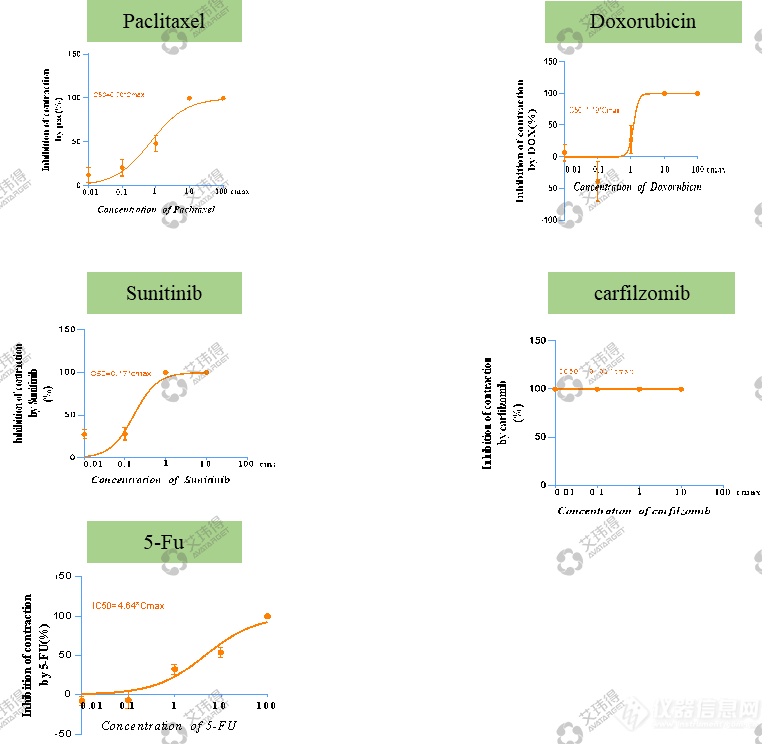
图9 心肌类器官芯片应用于药物心脏毒性检测
六 、心脏器官芯片无限可能
艾玮得心脏器官芯片已与国内知名高校包括西安交通大学、上海交通大学、上海微系统研究所等用于基础科研项目。同时,艾玮得还为国内知名药企恒瑞、齐鲁制药等提供了体外心肌的安全性、功能性评价服务。随着技术的不断进步,心脏器官芯片的应用前景将更加广阔。它不仅将在药物研发和精准医疗领域发挥重要作用,还将为心脏疾病的早期诊断、治疗监测以及康复评估等方面提供有力支持。我们有理由相信,在不久的将来,心脏器官芯片将成为守护人类心脏健康的“心脏守护者”。
关注艾玮得生物,了解更多关于器官芯片的新动态和研究成果!一起见证生命健康科技的未来吧!
参考文献
1. Fermini, B., Fossa, A. A., & Pollard, C. E.** (2018). Cardiovascular safety pharmacology: current practices and future directions. *Journal of Pharmacological and Toxicological Methods, 94*, 24-34. doi:10.1016/j.vascn.2018.01.004
2.Gintant, G. A., Sager, P. T., & Stockbridge, N. (2016). Evolution of strategies to improve preclinical cardiac safety testing. Nature Reviews Drug Discovery, 15(7), 457-471. doi:10.1038/nrd.2015.34
3.Weber, C., Bogdan, R., & Heinke, S. (2020). Human cardiac organoids for the modelling of myocardial infarction and drug cardiotoxicity. Nature Reviews Cardiology, 17(6), 387-401. doi:10.1038/s41569-019-0308-5
4.Zhao, Y., Rafatian, N., Feric, N. T., Cox, B. J., Aschar-Sobbi, R., Wang, E. Y., ... & Radisic, M. (2019). A Platform for Generation of Chamber-Specific Cardiac Tissues and Disease Modeling. Cell, 176(4), 913-927. doi:10.1016/j.cell.2018.11.042
5.Zhang, D., Shadrin, I. Y., Lam, J., Xian, H. Q., Snodgrass, H. R., & Bursac, N.** (2013). Tissue-engineered cardiac patch for advanced functional maturation of human ESC-derived cardiomyocytes. *Biomaterials, 34*(23), 5813-5820. doi:10.1016/j.biomaterials.2013.04.026
日程会场更新!2024微生理系统国际研讨会暨第七届类器官与器官芯片学术会议通知
预热9月 | 艾玮得生物市场活动日历大公开,精彩连连,邀您同行!
艾玮得生物血管芯片:用“芯”出发,探索血管奥秘
光子晶体生物力显微镜揭示银屑病患者皮肤杨氏模量异常:机械力-化学级联信号在发病过程中的关键作用

相关产品

关注

拨打电话

留言咨询