MFI专注蛋白聚集分析,助力药物稳定性研究
近日,美国明尼苏达大学药学院药理学科学家,利用MFI,在权威杂志Journal of ControlledRelease(IF:7.901)发表文章:Freezing-induced Protein Aggregation - Role of pH Shift and Potential Mitigation Strategies, J Control Release. 2020 Jul 10;323:591-599.
--研究背景--
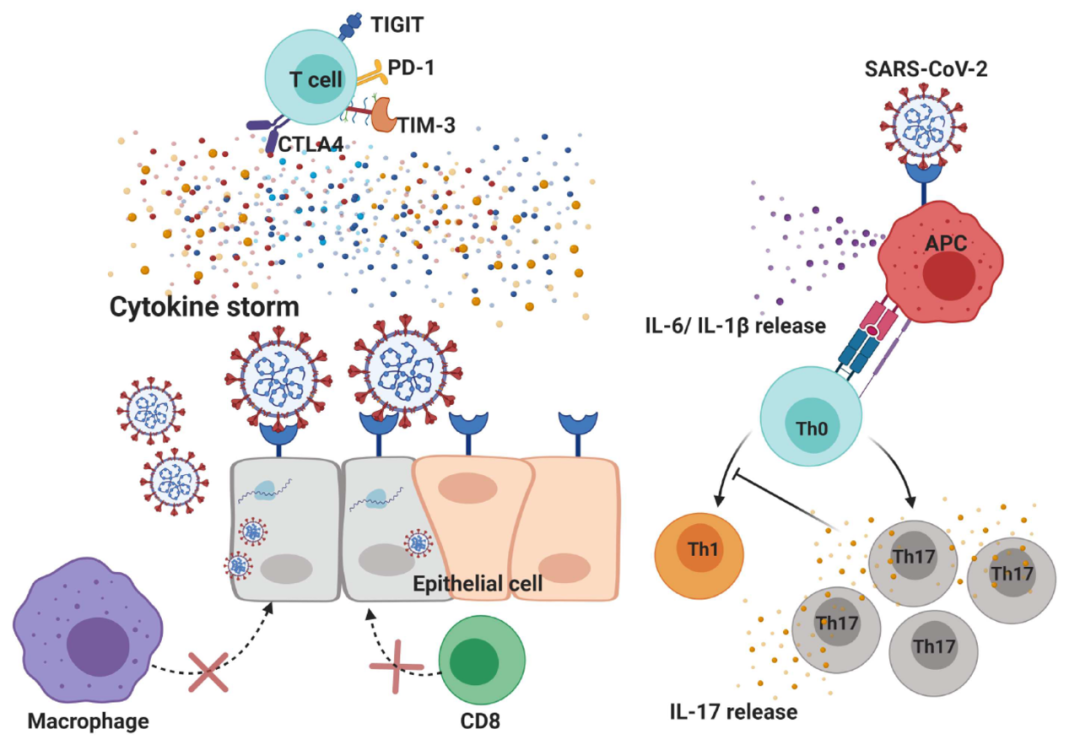
在设计用于肠胃外给药的蛋白质药物产品中,聚集体的产生,除了在外观上引起不适之外,最重要的是它们具有细胞毒性作用,或是引起机体免疫原性应答。美国和欧洲药典对肠胃外药物产品中的不溶性聚集物有规定:对于小剂量的肠胃外药物,通过光阻法测量的小颗粒(≥10μm)和大颗粒(≥25μm)的推荐药典规范分别为≤6000/container和≤600/container。

因此,预防和减轻蛋白质聚集对于维持蛋白质药物产品的安全性,功效和质量至关重要。药品加工步骤中,如纯化,搅动,冻融,填充,冻干,制剂成分,运输压力,都有可能将天然蛋白质转化为聚集体。而蛋白质溶液在配制为药物产品之前,通常以冷冻状态保存很长一段时间,所以,因反复冻融而产生的蛋白聚集体更应引起关注。
蛋白质制剂如缓冲液可确保制剂的pH值在整个保质期内都保持在所需范围内。但在低温过程中,某些缓冲区的有效性可能会受到影响。例如,当冷冻含有磷酸二氢钠和磷酸二钠的水溶液(即磷酸钠缓冲液)时,磷酸氢二钠的选择性结晶导致冷冻浓缩液的pH降低,从而引起蛋白聚集体的产生。
因此,本文旨在研究,在不同缓冲溶液的冻融循环过程中,两种模型蛋白质(牛血清白蛋白(BSA)和β-半乳糖苷酶(β-gal))聚集体的产生,以及这两种蛋白对缓冲液pH值变化的影响。同时,评价了添加的非结晶溶质对pH值变化的影响,以及pH改变对蛋白质聚集行为的影响。
--研究结果--
使用MFI表征冷冻和解冻后蛋白颗粒的形成
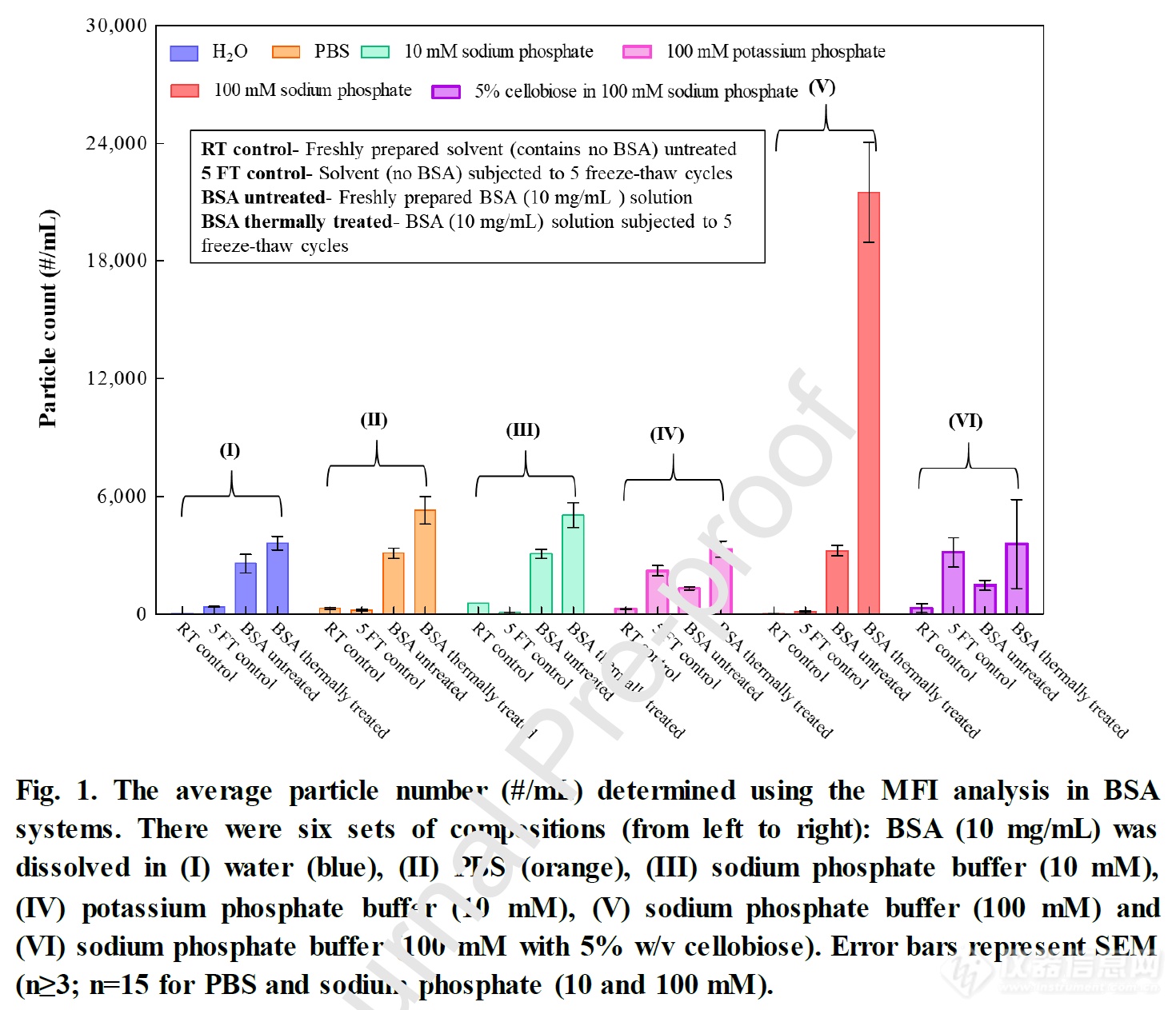
利用MFI检测发现,无论何种缓冲液,BSA(10mg/mL)在制备和立即分析时均显示出较低的颗粒数。当这些溶液经受五个冻融循环时,在许多系统中颗粒数量都有小幅增加。但冻融循环在磷酸钠缓冲液(100mM)中导致的颗粒计数增加显著。加入纤维二糖(纤维二糖(一种还原糖)被用作模型非结晶溶质,一种冷冻保护剂)后,在磷酸钠缓冲液(100mM)中导致的颗粒数有明显缓解。
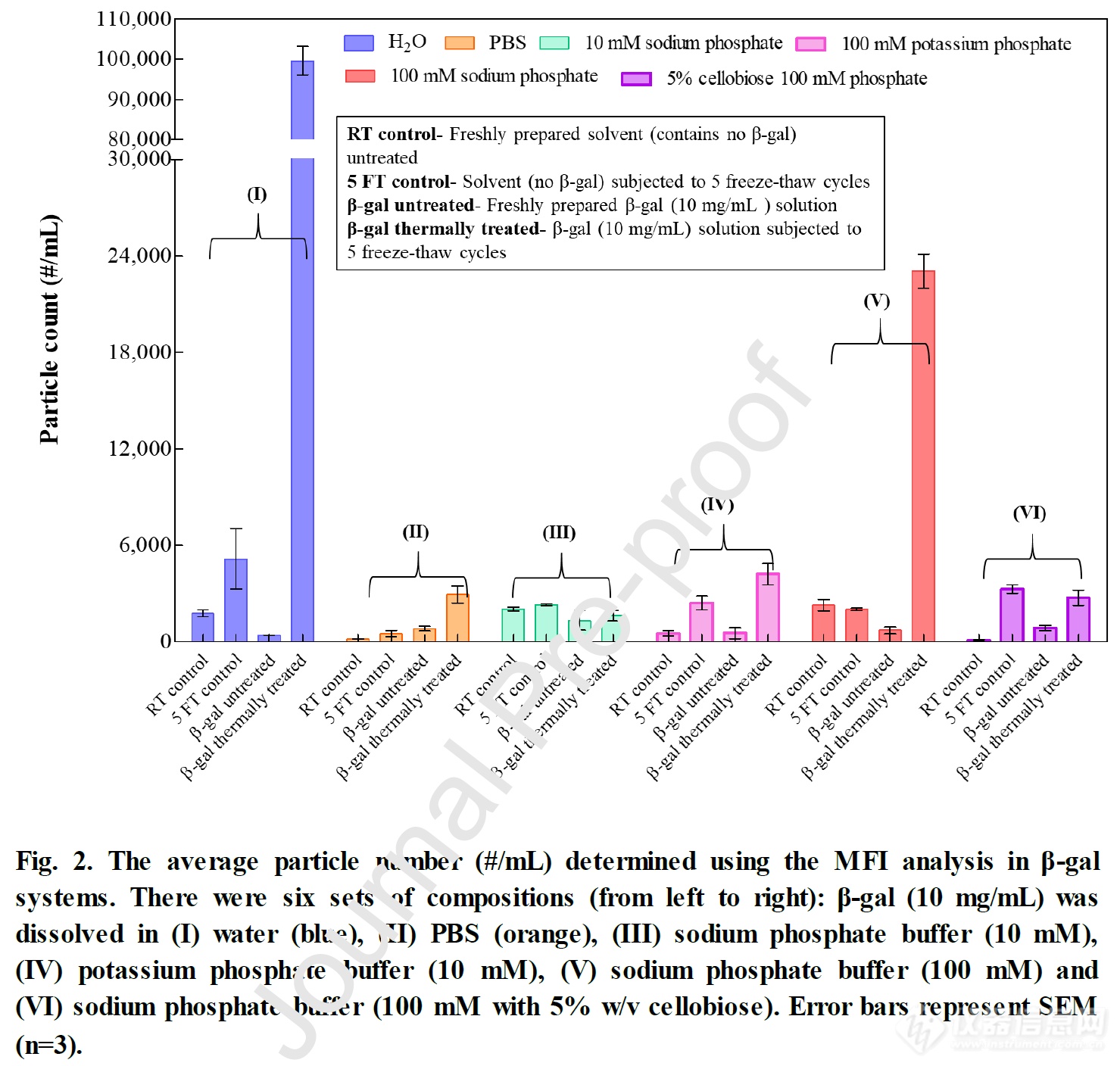
利用MFI检测发现,β-gal(10mg/mL)在水中冻融后的颗粒数(?100,000)急剧增加,表明该蛋白质对PH值的极端敏感性。同样,β-gal在磷酸钠缓冲液(100mM)中导致的颗粒计数增加显著。加入纤维二糖后,在磷酸钠缓冲液(100mM)中导致的颗粒数有明显缓解。
低温pH测定
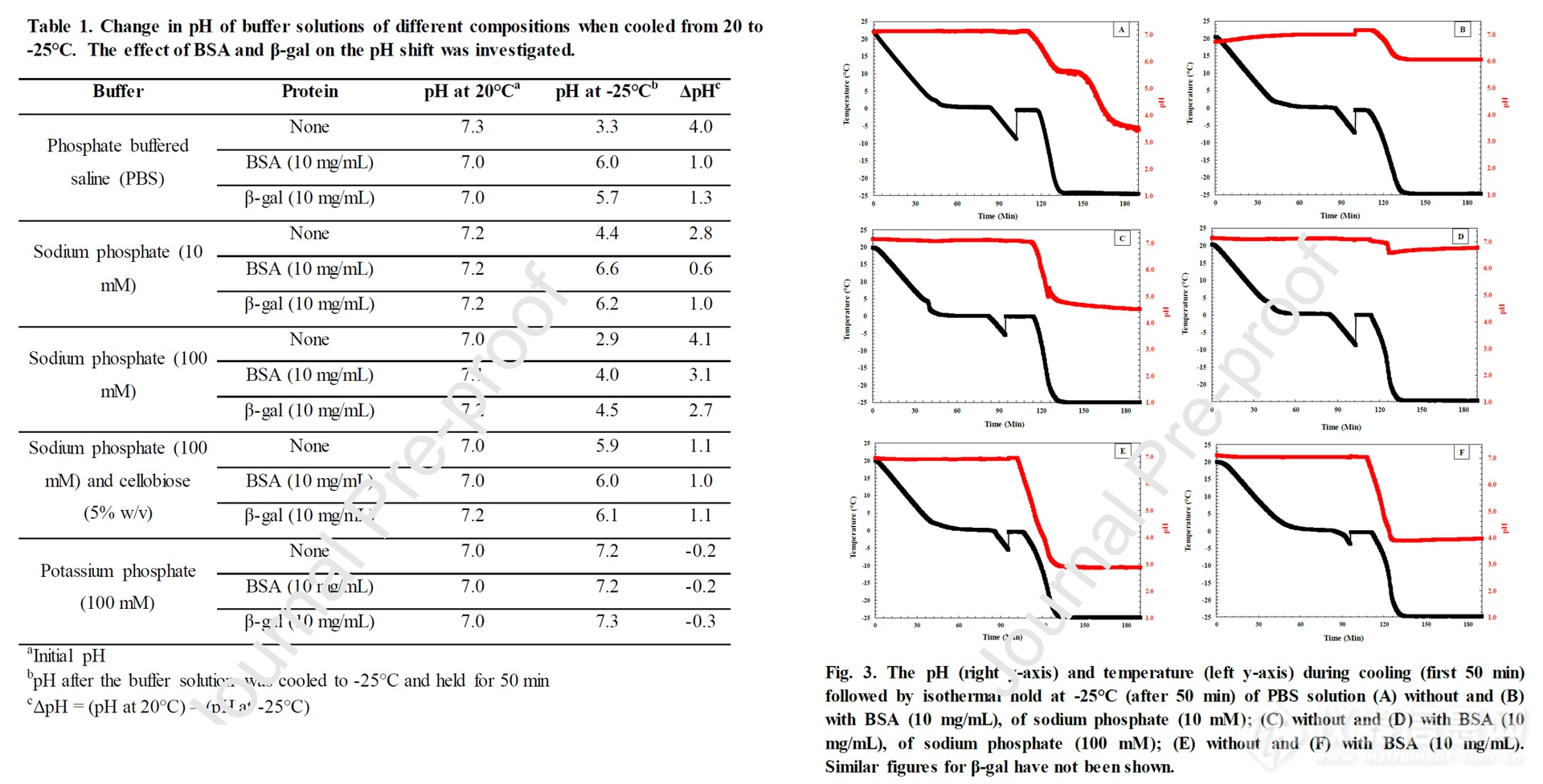
将PBS和磷酸钠(100mM)冷却后,发现pH值变化幅度相似。当磷酸钠浓度为10mM时,冷却时的pH值变化不明显。而蛋白质的添加(10mg/mL)可以降低了PBS和磷酸钠(10mM)中pH值变化的幅度。当磷酸钠浓度很高(100mM)时,蛋白质的作用就不那么明显了,这表明,低蛋白浓度(10mg/mL)似乎不足以抑制缓冲盐的结晶和随之而来的pH偏移。
低温XRD测定
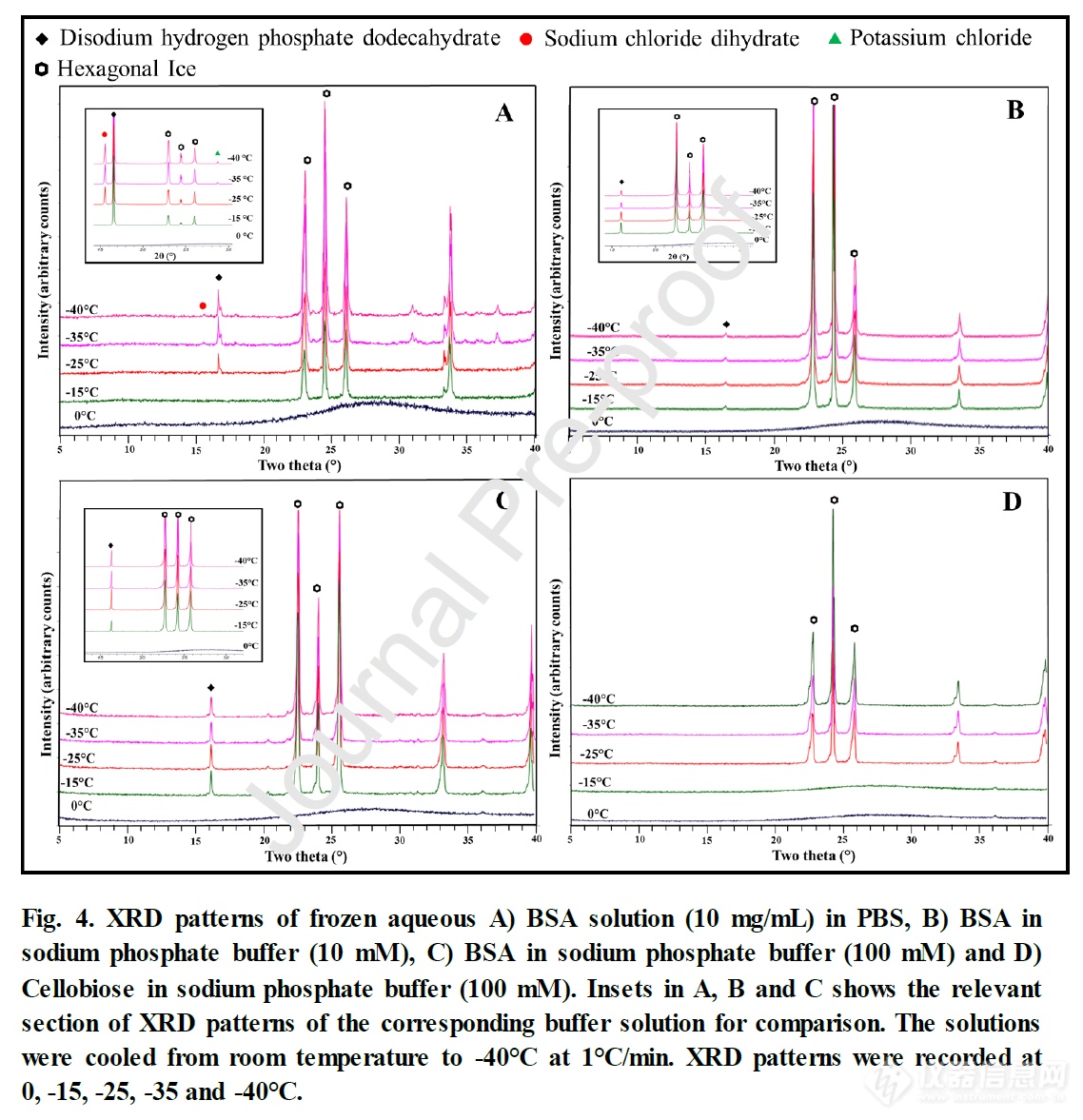
研究结果发现,当将磷酸钠缓冲溶液(10和100mM)冷却时,在-15°C时Na2HPO4•12H2O结晶明显(分别参见图4B和4C)。而BSA的添加,可以使Na2HPO4•12H2O的峰强度降低,特别是在较低的缓冲液浓度(10mM)下更为明显。这与观察到的BSA对缓冲溶液pH值变化幅度的影响密切相关。此外,纤维二糖的添加完全抑制了缓冲盐的结晶(图4D),以及冰峰的强度也受到了抑制。这些结果揭示了非结晶溶质在蛋白质制剂中的附加作用。通过抑制缓冲盐的结晶和随之而来的pH值变化,这些赋形剂可防止蛋白质不稳定性。
热分析
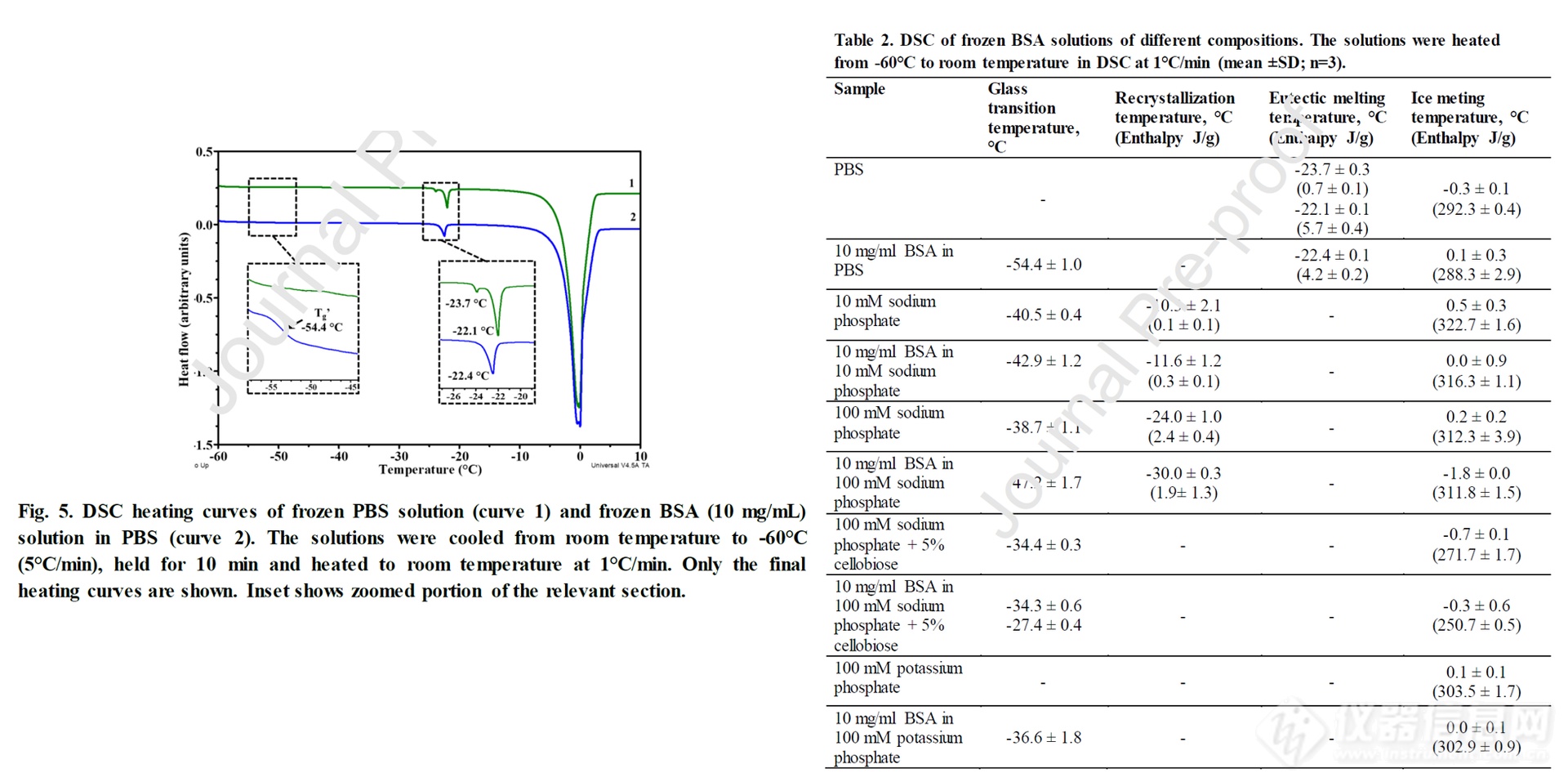
结果显示,当将BSA添加到PBS中时,在-54.4℃出现玻璃化转变温度(Tg′),随后在-22.4和0.1℃出现两个吸热峰。玻璃化转变温度反映了冷冻浓缩物组成发生了改变。BSA仅对100mM缓冲液的热行为有明显影响,导致Tg’(-47°C)和结晶温度(-30°C)降低。同时,纤维二糖的添加有望改变冷冻浓缩物的成分,这在Tg’(-34°C)中有所体现。
结论:
磷酸盐缓冲液被广泛用于肠胃外蛋白质制剂中。但在冷冻过程中,磷酸氢二钠(十二水合物)的选择性结晶会降低冷冻浓缩液的pH值,从而导致蛋白质聚集。可以通过降低缓冲液浓度来减小pH偏移。同时,BSA和β-gal可以通过对缓冲液结晶的抑制,减少pH的变化,但其作用程度要取决于缓冲液浓度。其它非结晶性赋形剂(纤维二糖)的添加,可通过抑制缓冲盐结晶,来提高蛋白质的稳定性。

来源于:美国ProteinSimple公司
热门评论
最新资讯
厂商动态
新闻专题
更多推荐