水活度对口服固体制剂化学和物理稳定性的影响
水活度对口服固体制剂化学和物理稳定性的影响
在整个产品生命周期内,需要对口服固体制剂的多种化学和物理特性,进行测试评估。本文将介绍三个案例研究,以表明通过水分活度评估水分对效价和溶解的影响。
国际药物开发创新与质量联合会(IQ)报告,“自十年前ICH Q1A稳定性方案首次发表以来,稳定性方面研究已经得到完善和发展”。例如《加速预测稳定性(APS):基础知识和制药行业实践》一书,其中包括总共22章详细的技术细节供开发和执行稳定性研究的科学家参考。此书中大量描述的概念之一就是水活度(Aw)。
最初稳定性试验通常在敞口烧杯或小瓶中进行,将口服固体制剂暴露在高温和一定的相对湿度(RH)下,且没有保护性包装,在一定时间后从稳定性试验箱中取出样品分析化学和物理稳定性。
虽然每种药物都会吸附水分,但每种药物水分吸收速率以及药物在稳定性试验箱中达到平衡湿度所需的时间有很大差异。
通过最初测量产品的水活度,以及测量记录水活度在暴露和吸湿期间随时间的变化,可以确定口服固体制剂的游离水与环境湿度达到平衡的速度。
在平衡状态下,稳定性实验箱的相对湿度相当于当时状态下产品的水活度。绘制的曲线是水活度对温度的函数,水活度这一数值代表了药物产品中游离水所占的比例;或者换句话说,游离的水可以参与我们不想发生的反应,因此产品稳定性可以根据水活度来定义,将水活度测试添加到稳定性试验中是一个重要的质量控制方法。
除了定义产品化学稳定性外,即使化学稳定性在允许的范围内,也可以通过水活度识别水分对口服固体制剂物理稳定性的影响。本文描述了三个案例研究,其中高水活度对不同产品的效价和/或溶出度产生了负面影响。尽管这些研究根据相对湿度条件进行描述的,但我们也可以通过直接测量产品水分活度的方法来表述。
水活度会影响降解速率指数
对水分敏感的药物会与水发生化学反应,破坏原料药中的化学键。这既降低了效价,又增加了杂质含量。多项研究表明,在低湿度条件下本具有长达几年稳定性终点的化合物在RH从40%变成75%储存时有明显变化。他们的稳定性终点从几年减少到了几个月。
在下面的例子中,研究人员定量测定了温度和湿度对硝西泮固体制剂分解的影响。硝西泮在双分子酸碱催化反应中降解,游离水分的多少会显著影响这一反应。因此,水活度值的大小决定了两种主要分解产物所占的比例。强制破坏试验的结果如图1所示,样品在四种温度(40、55、70和85℃)和六种相对湿度条件(30、40、50、60、70和80%相对湿度)下储存在开放的杯子中。图1A描述了硝西泮降解常数(K)与温度和相对湿度之间的明显指数相关性;在对数标度上绘制时,观察到线性相关性(图1B)。在高相对湿度(80%相对湿度及更高)下,分解化合物变得不稳定,因此无法轻易建立降解曲线。如前所述,平衡相对湿度相当于产品的水活度——因此,以下数据可以直接与水活度相关,硝西泮的后续水活度测量将决定产品的稳定性。
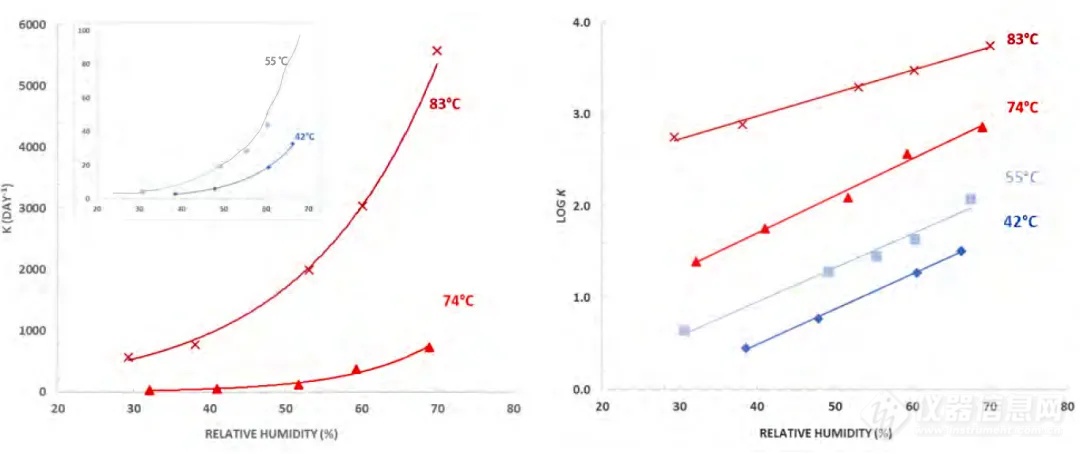
图1 硝西泮在不同相对湿度和温度下的降解速率
A)指数关系 B)对数关系
水活度会影响溶出速率
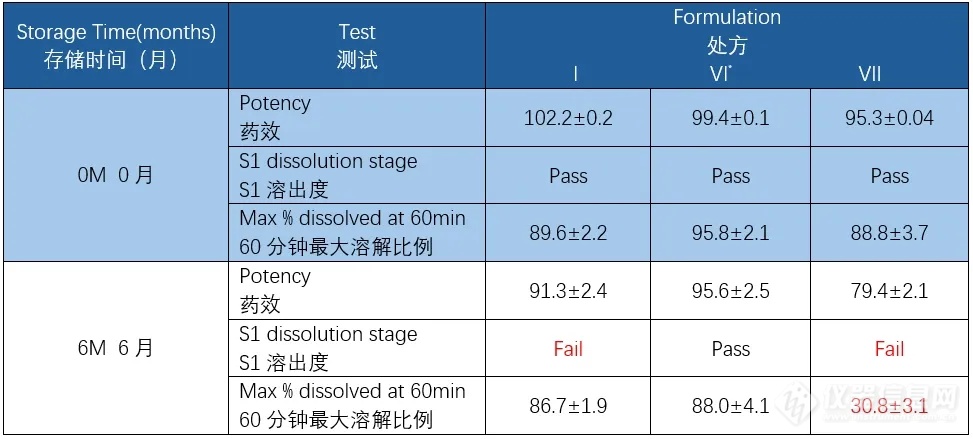
在进行化学稳定性测试的同时还应进行物理稳定性测试,以确定产品是否保持了其他关键质量属性。即使原料药本身对水分不敏感,高水分活度也会导致产品某些配方的溶解速率、硬度或易碎性发生改变。在下面的例子中,研究人员通过研究体外溶出度和效价(化学稳定性),评估了不同商品化环丙沙星(CIP)片剂在加速变性条件下(40℃/75%相对湿度)初级包装的稳定性。结果显示,配方VII未通过体外溶出度试验和效价试验;60分钟后,只有30.8%的药物溶解,储存6个月后,只有79.4%的原料药残留(表1)。仅6个月后,配方I未通过溶出试验,而效价仍在规范范围内。
表1 环丙沙星的加速稳定性试验
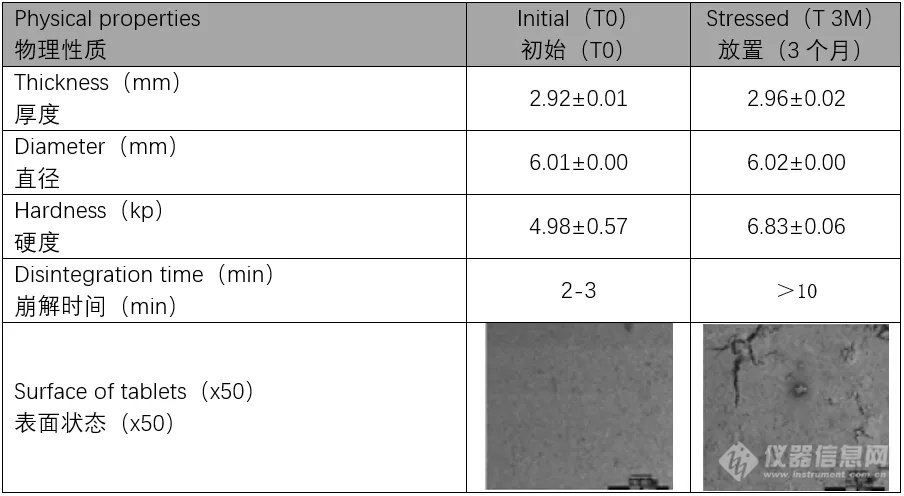
在另一项已发表的研究中,研究人员使用热分析和X射线分析来研究盐酸贝那普利的溶解稳定性。结果显示,当片剂在40℃/75%相对湿度下储存3个月时,即使原料药本身也没有变化,制剂物理结构也会发生改变。当含水量增加到临界水平以上时,溶解速率呈线性下降。崩解剂的“预激活”导致片剂的结构变化,是溶出速率降低的根本原因(表2)。
表2 盐酸贝那普利的加速稳定性试验
通过这两个溶解稳定性示例,我们发现实验结果可直接与平衡相对湿度(即水活度)相关。一旦溶解和水活度之间的相关性已知,产品水活度测量也可用于确定产品溶解质量。
通过测定水活度来确定干燥药品的稳定性和质量非常重要,美国药典USP-水活度通则的导言指出,“一些水分子可能与API或药物辅料紧密结合,无法参与化学、生物化学或物理化学反应(例如,作为水合物),而有些水分子可以自由地参与水解等反应,或者参与到支持微生物生长的中。确定可用(游离)水所占比例很重要,而水活度(aw)的测定可以为我们提供这一信息。”USP中描述的水活度方法之一是可调谐二极管激光吸收光谱法,这是唯一能够准确测量含有挥发性物质样品水活度的技术。

Aqualab TDL激光法测定水活度
美国药典USP优先推荐镜面露点法,该方法可高精度测量所有样品,测量时间小于5min。可以对生产过程中微生物限度进行全流程控制。是业内公认具有潜力的微生物检测新方法。

Aqualab 4TE 镜面冷凝露点法水活度仪
产品特点:
·国际公认水活度金标准镜面冷凝露点法。
·全球用户量第一的品牌Aqualab水活度仪。
来源于:北京合邦兴业科学仪器有限公司
热门评论
最新资讯
厂商动态
新闻专题















