
产品详情
果胶酶活性检测试剂盒说明书
可见分光光度法
规格:50T/24S
产品组成:使用前请认真核对试剂体积与瓶内体积是否一致
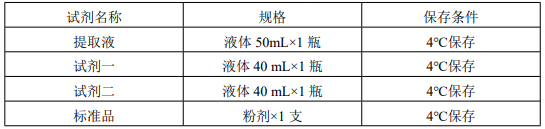
溶液的配制:
1、试剂一:若溶液中有不溶解物质,可以 50℃水浴溶解。
2、标准品:10mg 半乳糖醛酸。临用前加入 0.943mL 蒸馏水,配成 50μmol/mL 的标准液。
产品说明:
果胶酶(pectinase)是分解果胶的酶类,包括原果胶酶,果胶酯酶,多聚半乳糖醛酸酶和果胶裂解酶四大类,广泛存在于高等植物果实和微生物中,是水果加工中最重要的酶。
果胶酶水解果胶生成半乳糖醛酸,半乳糖醛酸与 DNS 试剂反应生成在 540nm 有特征吸收峰的棕红色物质,测定 540nm 处吸光值变化可计算得果胶酶活性。
注意:实验之前建议选择 2-3 个预期差异大的样本做预实验。如果样本吸光值不在测量范围内建议稀释或者增加样本量进行检测。
需自备的仪器和用品:
可见分光光度计、台式离心机、水浴锅、1mL 玻璃比色皿、可调式移液枪、研钵/匀浆器、冰和蒸馏水。
操作步骤:
一、样本处理(可适当调整待测样本量,具体比例可以参考文献)
1、组织:按照组织质量(g):提取液体积(mL)为 1:5~10 的比例(建议称取约 0.1g 组织,加入 1mL 提取液)进行冰浴匀浆,然后 10000g,4℃,离心 10min,取上清置于冰上待测。
2、菌类:按照细菌数量(104个):提取液体积(mL)为 500~1000:1 的比例(建议 500 万细菌加入 1mL提取液),冰浴超声波破碎细菌(功率 300w,超声 3 秒,间隔 7 秒,总时间 3min);然后 10000g,4℃,离心 10min,取上清置于冰上待测。
3、液体:直接检测。
二、测定步骤
1、 可见分光光度计预热30min 以上,调节波长至540nm,蒸馏水调零。
2、 将 50μmol/mL 标准液用蒸馏水稀释为 6、5、4、3、2、1 μmol/mL 的标准溶液备用。
3、 取 125μL 样本沸水浴 10min 备用。
4、 样本测定(在1.5mL离心管中):
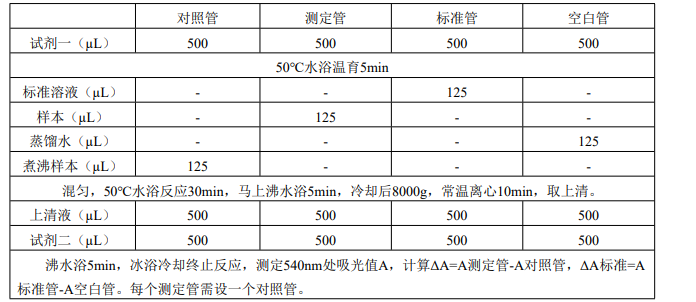
三、果胶酶活性计算
1、 标准曲线的绘制:
以各个标准溶液的浓度为 x 轴,其对应的△A 标准为 y 轴,绘制标准曲线,得到标准方程 y=kx+b,将 ΔA 带入方程得到 x(μmol/mL)。
2、 果胶酶活性的计算:
(1)按蛋白浓度计算
酶活定义:在 50℃,pH3.5 条件下,每毫克蛋白每小时分解果胶产生 1μmol 半乳糖醛酸为 1 个酶活力单位。
果胶酶活性(U/mg prot)=x×V 提取÷(V 提取×Cpr)÷T= 2x÷Cpr
(2)按样本质量计算
酶活定义:在 50℃,pH3.5 条件下,每克样本每小时分解果胶产生 1μmol 半乳糖醛酸为 1 个酶活力单位。
果胶酶活性(U/g 质量)= x×V 提取÷W÷T=2x÷W
(3)按照细菌数量计算
酶活定义:在 50℃,pH3.5 条件下,每 104个细菌每小时分解果胶产生 1μmol 半乳糖醛酸为 1 个酶活力单位。
果胶酶活性(U/104 cell)= x×V 提取÷T÷细菌数量(万个)=2x÷细菌数量(万个)
(4)按液体体积计算
酶活定义:在 50℃,pH3.5 条件下,每 mL 样本每小时分解果胶产生 1μmol 半乳糖醛酸为 1 个酶活力单位。
果胶酶活性(U/mL)= x×V 样÷V 样÷T= 2x
V 提取:提取液体积,1mL; V 样:加入的样本体积,0.125mL;Cpr:样本蛋白浓度,mg/mL;W:样本质量,g;T:反应时间:0.5h。
注意事项:
1、 A 大于 1.5 时,建议将样本用提取液稀释后再进行测定。
2、 植物果实组织建议将样本稀释 10 倍或 20 倍后再测定。
实验实例:
0.1g 猕猴桃加入 1mL 提取液进行冰浴匀浆,然后 10000g,4℃,离心 10min,取上清置于冰上稀释 10 倍后按照测定步骤操作,测得计算 ΔA= A 测定管-A 对照管=1.465-1.45=0.015,依据标准曲线 y=0.2575x-0.2214,计算得 x=0.918μmol/mL,按样本质量计算酶活得:
果胶酶活性(U/g 质量)=2x÷W×10(稀释倍数)= 183.6 U/g 质量。
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!




