
产品详情
谷胱甘肽过氧化物酶(GSH-Px/GPX)活性检测试剂盒说明书
微量法
注意:本产品试剂有所变动,请注意并严格按照该说明书操作。
规格:100T/48S
产品组成:使用前请认真核对试剂体积与瓶内体积是否一致
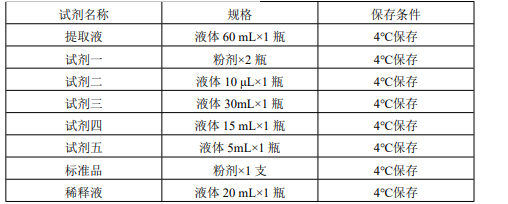
溶液的配制:
1、 试剂一:临用前加入 3.3 mL 稀释液,充分溶解;
2、 试剂二:临用前按 2 μL 试剂二:10 mL 蒸馏水的比例稀释试剂二,现用现配;
3、 试剂三:瓶底若有结晶可 50℃水浴溶解,此溶液为饱和溶液,若底部最终还有结晶,吸取上清使用即可;
4、 标准品:10 mg 还原型谷胱甘肽。临用前加入 0.405 mL 稀释液溶解为 80 μmol/mL 的标准溶液备用。
产品说明:
谷胱甘肽过氧化物酶(glutathione peroxidase, GSH-Px 或 GPX)是机体内广泛存在的一种重要的过氧化物分解酶。GPX 能够催化还原型谷胱甘肽(GSH)生成氧化型谷胱甘肽(GSSG),使有毒的过氧化氢还原成无毒的羟基化合物。
GPX 催化 H2O2氧化 GSH,产生 GSSG,GSH 能与 DTNB 生成在 412nm 处有特征吸收峰的化合物,412nm 下吸光度的下降即可反应 GPX 的活性。
注意:实验之前建议选择 2-3 个预期差异大的样本做预实验。如果样本吸光值不在测量范围内建议稀释或者增加样本量进行检测。
需自备的仪器和用品:
可见分光光度计/酶标仪、天平、台式离心机、微量玻璃比色皿/96 孔板、可调式移液枪、研钵/匀浆器、EP 管。
操作步骤:
一、样本处理(可适当调整待测样本量,具体比例可以参考文献)
1、组织:按照组织质量(g):提取液体积(mL)为 1:5~10 的比例(建议称取 0.05 g 组织,加入 1 mL 提取液)进行冰浴匀浆。5000 rpm,4℃离心 10 min,取上清置冰上待测 (如上清不清澈可以离心更长时间)。
2、细菌、细胞:按照细胞数量 104个:提取液体积(mL)500~1000:1 的比例(建议 500 万细胞加入 1 mL 提取液),冰浴超声波破碎细胞(功率 300w,超声 3s,间隔 7s,总时间 3 min)然后 5000 rpm,4℃,离心 10min,取上清置冰上待测 (如上清不清澈可以离心更长时间)。
3、血清(浆)等液体:直接测定。
二、测定步骤
1、 分光光度计/酶标仪预热 30min 以上,调节波长至 412 nm,蒸馏水调零。
2、 将 80 μmol/mL 标准液用稀释液稀释为 0.08 μmol/mL 的标准溶液,现用现配。
3、 操作表:(在 1.5 mL 离心管中依次加入下列试剂)
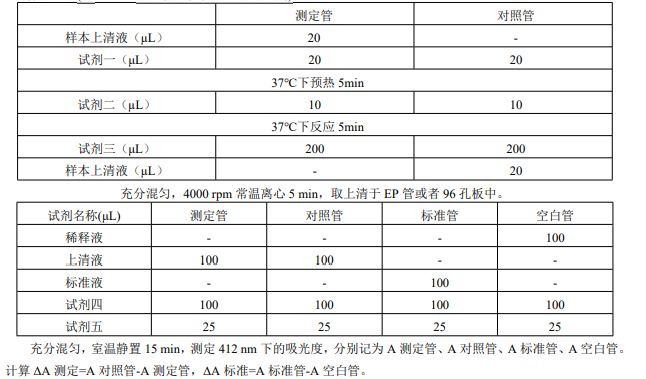
三、GPX 活性计算
1、 抑制百分率的计算
抑制百分率=(A 对照管-A 测定管) ÷(A 对照管-A 空白管)× 100%
尽量使样本的抑制百分率在 30-70%范围内,越靠近 50%越准确。如果计算出来的抑制百分率小于 30%或大于70%,则通常需要调整加样量后重新测定。如果测定出来的抑制百分率偏高,则需适当稀释样本;如果测定出来的抑制百分率偏低,则需重新准备浓度比较高的待测样本。
2、 GPX 活性计算
(1)按蛋白浓度计算
活力单位定义:每 mg 蛋白在反应体系中每分钟催化 1 nmol GSH 氧化定义为一个酶活力单位。
GPX (U/mg prot) =ΔA 测定÷(ΔA 标准÷C 标)×1000×V 酶促÷(Cpr×V 样)÷T
=200×ΔA 测定÷ΔA 标准÷Cpr
(2)按样本质量计算
活力单位定义:每 g 样本在反应体系中每分钟催化 1 nmol GSH 氧化定义为一个酶活力单位。
GPX (U/g 质量)= ΔA 测定÷(ΔA 标准÷C 标)×1000×V 酶促÷(V 样÷V 样总×W)÷T
=200×ΔA 测定÷ΔA 标准÷W
(3)按细胞数量计算
活力单位定义:每 104 个细胞在反应体系中每分钟催化 1 nmol GSH 氧化定义为一个酶活力单位。
GPX (U/104 cell)=ΔA 测定÷(ΔA 标准÷C 标)×1000×V 酶促÷(细胞数量×V 样÷V 样总)÷T
=200×ΔA 测定÷ΔA 标准÷细胞数量
(4)按液体体积计算
活力单位定义:每 mL 液体在反应体系中每分钟催化 1 nmol GSH 氧化定义为一个酶活力单位。
GPX (U/mL)= ΔA 测定÷(ΔA 标准÷C 标)×1000×V 酶促÷V 样÷T=200×ΔA 测定÷ΔA 标准
C 标:标准液混合物的浓度:0.08 μmol/mL;V 酶促:酶促反应体系体积,0.25 mL;V 样:酶促反应中加入样本体积,0.02 mL;V 样总:提取液体积,1 mL;Cpr:上清液蛋白浓度,mg/mL;T:反应时间,5 min;细胞数量:以万计;W:样本质量,g;1000:换算系数,1 μmol=1000 nmol。
注意事项:
1、 吸光度若大于 1.5 时,建议将样本用提取液稀释后进行测定。
2、 建议一次不要做过多样本以免检测时间过长影响显色,使测定不准确。
实验实例:
1. 取 0.1 g 小鼠肝脏组织加入 1 mL 提取液进行匀浆研磨,取上清稀释 40 倍后再按照测定步骤操作,用 96 孔板测得 A 测定管=0.152,A 对照管=0.278,A 标准管=0.370,A 空白管=0.064,计算?A 测定=A 对照管-A 测定管=0.126,?A 标准=A 标准管-A 空白管=0.306,按样本质量计算酶活得:
GPX (U/g 质量)=200×ΔA 测定÷ΔA 标准÷W×40(稀释倍数)=32941 U/g 质量。
2. 取 0.1 g 杨树叶片加入 1 mL 提取液进行匀浆研磨,用 96 孔板测得 A 测定管=0.199,A 对照管=0.259,A 标准管=0.370,A 空白管=0.064,计算?A 测定=A 对照管-A 测定管=0.060,?A 标准=A 标准管-A 空白管=0.306,按样本质量计算酶活得:
GPX (U/g 质量)=200×ΔA 测定÷ΔA 标准÷W=392 U/g 质量。
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!




