摘 要 本文以去离子水为萃取剂,通过加电膜萃取装置萃取了乙酸丁酯中的无机阴离子。在600V直流电压的作用下,8 ml乙酸丁酯中的四种无机阴离子通过聚丙烯中空纤维膜孔内的有机液膜进入膜内的100 μl 去离子水中。萃取完成后,使用离子色谱对萃取液进行分析。本文优化了影响萃取过程的因素,如施加电压、搅拌速度以及萃取时间。最佳萃取条件为:施加电压为600V,搅拌速度为600rpm,萃取时间为5分钟。该方法成功应用于乙酸丁酯实际样品的测定,无机阴离子的线性范围为0.01 mg/L-1mg/L,加标回收率为97-102%。实验结果表明,该方法快速有效,并可应用于其他微溶性有机物中无机阴离子的测定。关键词 无机阴离子;乙酸丁酯;加电中空纤维膜萃取;离子色谱 最近15年来,中空纤维膜萃取技术作为一种样品前处理方法,被广泛应用于环境分析、药物分析以及食品和饮料检测等重要领域。中空纤维膜萃取技术具有样品无需处理即可直接进样,对分析物具有预富集作用,基体消除,成本低廉,易与气相色谱、高效液相色谱、毛细管电流和离子色谱联用等优点。但分析物穿透中空纤维膜壁上的支撑液膜的运输机理是基于被动扩散,因此,常常需要花费超过30分钟甚至长达一小时的时间才能达到萃取平衡。为了克服传统的中空纤维膜萃取技术耗时的缺点,2005年挪威的Pedersen-Bjergaard和Rasmussen首次提出了一种称为加电中空纤维膜萃取的新型样品前处理方法。短短5分钟内,碱性药物在300V直流电压的作用下能够成功地穿过一层薄薄的有机液膜进入到300 μl 接收相中。与传统基于被动扩散的膜萃取技术相比,电动力迁移在加电中空纤维膜萃取中起到了主导作用,因此在很短的时间内就能取得良好的萃取效果。随后,Pedersen-Bjergaar小组又将这种新型的加电中空纤维膜萃取方法应用于更多种类的碱性药物、酸性药物、肽类和氯酚类物质的萃取 。他们建立了加电中空纤维膜萃取过程的理论模型并考察了影响加电中空纤维膜萃取效率的参数 。此外,新加坡的Lee小组使用加电中空纤维膜萃取技术从羊水、血清、口红和尿样中萃取了铅离子。目前为止,加电中空纤维膜萃取技术一直应用于液-液-液三相萃取体系,而本实验首次将加电中空纤维膜萃取应用于液-液两相萃取体系。我们曾经使用在线中空纤维膜萃取-离子色谱法测定了乙酯乙酯的无机阴离子,但该方法的萃取时间长达半小时,并且使用了柱切换技术,装置复杂,操作繁琐,仪器成本高。而本实验使用加电中空纤维膜萃取技术仅需要短短5分钟就能完成萃取,并且装置简单,操作简便,成功应用于乙酸丁酯中无机阴离子的测定。
想求购一款能够滴定微量氯离子含量的电位滴定仪,因为产品是一种深色的多糖,想控制氯离子使其不咸,查资料得出氯离子含量要控在在百分之零点零一左右,想求购一款电位滴定仪能够满足这分析,满足GB 5009.44食品中氯离子的检验中电位滴定,求知道的推荐下,最好带上价格
[font='Times New Roman'][font=黑体][b]问题描述:[/b][/font][/font][font=宋体]在用氯离子选择性电极测定氯时,标液都是定容到[/font][font='Times New Roman']100[/font][font=宋体] [font=Times New Roman]mL[/font][font=宋体],样品是否也一定要定容到[/font][font=Times New Roman]100 mL[/font][font=宋体]?定容到小于[/font][font=Times New Roman]100 mL[/font][font=宋体]行不行?[/font][/font][font='Times New Roman'][font=黑体][b]解答:[/b][/font][/font][font=宋体]样品的定容体积与标液尽量一致,这样操作目的是最大程度使样品基质、干扰离子、各组分浓度等方面与标液接近,也可以使分析组分的浓度在标准曲线范围内,减少分析过程中误差。但样品的定容体积与标液也不一定必须相同,配制时也可以灵活些,比如取样量少些定容体积就可小些,甚至分析组分浓度较高也可以定容体积大些,但在结果计算中也要根据实际样品定容体积进行换算。[/font]
新安装了一台梅特勒的T50电位滴定仪。用来检测我们某乳剂营养品中氯离子的含量。(详见http://bbs.instrument.com.cn/shtml/20131029/5032928/电位滴定法测定某乳剂营养品中氯离子的含量)http://ng1.17img.cn/bbsfiles/images/2013/10/201310310955_474365_1609327_3.jpg配套用的电极是DM141-SC银环电极,主要就是用来滴定氯离子含量的。新机装好后,按照《中国药典》2010年版二部附录的方法配制和标定0.1mol/L的硝酸银滴定液。然后用标定好的硝酸银滴定液滴定我们的样品。然后就是清理善后。清洗电极(因为是沉淀反应,在电极部位是有沉淀吸附的),清洗滴定杯。电极的清洗是直接用蒸馏水冲洗,然后用滤纸轻轻擦拭可能吸附的沉淀。滴定杯现用大量的自来水冲洗,然后蒸馏水涮洗干净,最后反扣晾干。在清洗自来水的时候,突发奇想:自来水厂一般都会用氯气消毒,氯气消毒的同时,肯定要发生这样的化学反应:http://ng1.17img.cn/bbsfiles/images/2013/10/201310291721_473897_1609327_3.jpg因此,自来水中不可避免的会有氯离子存在。可不可以用硝酸银滴定液滴定自来水中的氯离子呢?能不能测的出来呢?第二天,再测样品的时候,就称量了约50g的自来水,用硝酸银滴定液进行了滴定。并把从家里取的自来水进行对比。结果如下:http://ng1.17img.cn/bbsfiles/images/2013/10/201310291720_473896_1609327_3.jpgGB 5749-2006要求氯含量的限值不能超过250mg/L。从数据上来看,都在合格范围内。
电 导 率 的 定 义 电导率是物质传送电流的能力,是电阻率的倒数。在液体中常以电阻的倒数——电导来衡量其导电能力的大小。水的电导是衡量水质的一个很重要的指标。它能反映出水中存在的电解质的程度。根据水溶液中电解质的浓度不同,则溶液导电的程度也不同。通过测定溶液的导电度来分析电解质在溶解中的溶解度。这就是电导仪的基本分析方法。 溶液的电导率与离子的种类有关。同样浓度电解质,它们的电导率也不一样。通常是强酸的电导率最大,强碱和它与强酸生成的盐类次之,而弱酸和弱碱的电导率最小。因此,通过对水的电导的测定,对水质的概况就有了初步的了解。电导率 电阻率的倒数即称之为电导率L。在液体中常以电阻的倒数——电导来衡量其导电能力的大小。电导L的计算式如下式所示: L=l/R=S/l电导的单位用姆欧又称西门子。用S表示,由于S单位太大。常采用毫西门子,微西门子单位1S=103mS=106μS。 当量电导 液体的电导仅说明溶液的导电性能与几何尺寸间的关系,未体现出溶液浓度与电性能的关系。为了能区分各种介质组成溶液的导电性能,必须在电导率的要领 引入浓度的关系,这就提出了当量电导的概念。所谓的当量电导就是指把1g当量电解质的溶液全部置于相距为1cm的两板间的溶液的电导,符号“λ”。由于在电导率的基础上引入了浓度的概念。因此各种水溶液的导电来表示和比较了。在水质监测中,一般通过对溶液电导的测量可掌握水中所溶解的总无机盐类的浓度指标。温度对电导的影响 溶液的电阻是随温度升高而减小,即溶液的浓度一定时,它的电导率随着温度的升高而增加,其增加的幅度约为2%℃-1。另外同一类的电解质,当浓度不同时,它的温度系数也不一样。在低浓度时,电导率的温度之间的关系用下式表示: L1=L0[1+α(t-t0)+β(t-t0)2]由于第二项β(t-t0)2之值较小,可忽略不计。在低温时的电导率与温度的关系可用以下近似值L1=L0[1+α(t-t0)]表示,因此实际测量时必须加入温度补偿。 电导的温度系数 对于大多数离子,电导率的温度系数大约为+1.4%℃-1~3%℃-1对于H+和OH-离子,电导率温度系数分别为1.5%℃-1和 1.8%℃-1,这个数值相对于电导率测量的准确度要求,一般为1%或优于1%,是不容忽视的。纯水的电导率 即使在纯水中也存在着H+和OH-两种离子,经常说,纯水是电的不良导体,但是严格地说水仍是一种很弱的电解质,它存在如下的电离平衡:H2O←→H++OH或2H2O←→H3+O+OH-其平衡常数:KW=[H+].[OH-]/H2O=10-14式中KW称为水的离子积[H+]2=[OH-]2=10-14∴[H+]2=[OH-]2=10-7lH2O,0=λOH-,0=349.82+198.6=548.42S/cm.mol2已知水的密度d25℃/H2O=0.9970781cm3 故原有假设为1的水分离子浓度只能达到0.99707。实际上是仅0.99707份额的水离解成0.99707.10-7的[H+]和[OH-],那么离解后的[H+]和[OH-]电导率的总和KH2O用下式求出:KH2O=CM/1000λH2O=(0.99707.10-7/1000).548.42=0.05468μS.cm-1≈0.054μS.cm-1∴ρH2O=1/KH2O=1/0.05468×10-9=18.29(MΩ.cm)≈18.3(MΩ.cm) 由水的离子积为10-14可推算出理论上的高纯水的极限电导为0.0547μS.cm-1,电阻为18.3MΩ.cm(25℃)。 水的电导率的温度系数在不同电导率范围有不同的温度系数。对于常用的1μS.cm-1的蒸馏水而言大约为+2.5%-1。
电位滴定法测定氯离子和碘离子 1.实验目的 (1)用电位滴定法测定氯离子和碘离子的含量。 (2)掌握电位滴定法终点的确定方法和实验技术。2.实验原理电位滴定法利用电极电位的“突跃”指示滴定终点。电位滴定终点的确定,不必知道终点电位的确定值。只要测得电位值的变化,就可通过作图法或二阶微商法确定滴定终点。氯化银、碘化银的溶度积分别为AgCl: Ksp = 1×10-10 mol2.L-2 AgI: Ksp = 1×10-16 mol2.L-2用硝酸银进行滴定含氯离子和碘离子的试液时,先生成碘化银沉淀,当碘化银沉淀完全后,开始生成氯化银沉淀。本实验以硝酸银为滴定剂,基于银离子与碘离子和银离子分步沉淀原理进行测定。以银-氯化银电极为指示电极,玻璃电极为参比电极,通过测量滴定过程中电位的变化,测定待测溶液中碘离子和银离子的浓度。滴定过程中,溶液pH不发生变化,pH玻璃电极可作为参比电极。滴定过程中,有两个电位“突跃”。每次滴定下1.0 mL;在终点附近的量,电位值变化较大时,每次可滴下0.10 mL,以便于微商法的计算和获得准确的测定结果。3.仪器与试剂高输入阻抗电位计(或pH记,或离子计,或ZD-2型自动电位滴定仪),银-氯化银电极;pH玻璃电极。200 mL烧杯;10 mL移液管。0.10 mol.L-1AgNO3标准溶液:准确称取110℃干燥的AgNO3(GR)8.6 g于500 mL烧杯中,用约200 mL不含Cl-的蒸馏水溶解,转入500 mL容量瓶中,再用不含Cl-的蒸馏水定容。计算其浓度。配制的溶液装入棕色瓶中暗处保存。电位滴定时,稀释成0.050 mol.L-1 AgNO3标准溶液。含氯离子和碘离子的试液(各含约0.01 mol.L-1)。4.实验步骤移取10.00 mL含氯离子和碘离子的试液于200 mL烧杯中,放入搅拌子,加入80 mL蒸馏水,将电极浸入试液中,以银-氯化银电极为指示电极,pH玻璃电极为参比电极①,用0.050 mol.L-1 AgNO3标准溶液进行滴定,大概估计滴定终点。记录消耗AgNO3标准溶液的体积和电位测定值。平行测定三次。5.数据处理(1)以消耗AgNO3标准溶液的体积(V)为横坐标,以测得的电位(E)为纵坐标,绘制E-V曲线,再绘制一次微分 曲线和 曲线,确定终点体积。(2)计算试液中氯离子和碘离子的浓度和测定结果的相对平均偏差。注释①参比电极也可使用双盐桥电极(外套管内装1 mol.L-1 KNO3溶液)或用内含1 mol.L-1 KNO3溶液的盐桥连接的饱和甘汞电极。思考题1.银电极、银离子选择电极或氯离子选择电极可否用作指示电极?为什么?2.pH玻璃电极为什么可用作参比电极?3.用本实验的方法可否连续测定氯离子、溴离子和碘离子? 陕西师范大学分析化学研究所
测大气中的氟化物,用离子选择电极法,我们用的雷磁的离子计,用之前用两点校定,检定溶液就是氟化钠的标准溶液吗?还是做标准系列就是对离子计校定?

你好!我想问下 卡尔费休(恒流测电压)滴定水到终点,碘分子过量的时候,极化电流是把过量的碘分子极化为碘离子了么? 然后有了碘离子/碘分子的电对,于是溶液导电性增强,电压下降到我们设定的值指示终点么?碘离子是电流极化出来的 还是溶液反应生成的呢?这里的极化电流怎么工作的?您、能给解答下么?还有一个小问题:在滴定水的为什么电压是在一点点的下降,溶液中的碘分子不都是去滴定水了么,为什么电压会一点点的降低,我的意思是说电压突降前的那段;而不是保持一个恒定的值,当到达终点过量一点点碘的时候电压突降呢?http://ng1.17img.cn/bbsfiles/images/2012/06/201206282223_374857_1966297_3.jpg
各位大侠,我需要检测产品溶液中的氯离子含量,看了很多文献,但是还是不大清楚。我现在又一台 奥立龙 的 501的电位计(国外带回来的,很老的机子了好像,没有说明书...)有:E-201pH复合电极一个,502型铂环ORP复合电极一个,银离子电极一个。我的这个产品,根据药典测氯离子是说,用银-玻璃电极测。请问:1.我的502型铂环ORP复合电极能不能测氯离子?2.如果不能,要用电位滴定法测银离子含量,是不是还要买一个玻璃参比电极?价格大约多少?3.银离子电极,接线端是那种U型的金属片,可是现在的酸度计不都是那种圆形的直接卡上的孔,要怎么接?4.我实在不会用现有的这台电位计啊,所以如果要买一台,是不是普通酸度计就可以,就是也可以pH ,也可以测氯离子?价格大约多少?5.自动电位滴定仪,是不是比较好用?价格大约多少?6.是不是有那种银-玻璃复合电极,可以直接测的,价格大约多少?还有,我还想问一下,电导率仪和酸度计有什么差别? 电导率仪可以测ORP吗?谢谢!!!
【篇名】 紫外分光光度法测电活性物质的稳定常数 【作者】 张金昌. 赵文凯. 薛斌. 【刊名】 沈阳工业大学学报 2005年06期【机构】 沈阳工业大学石油化工学院. 辽宁辽阳111003. 【关键词】 乙基紫. 缔合物. 紫外分光光度法. 稳定常数. 电活性物质. 【摘要】 乙基紫是碱性染料,它是一种阳离子载体,与阴离子形成缔合物可作为PVC膜电极的电活性物质,电活性物质的溶度积(KSP)影响电极的响应性能.用紫外分光光度法测定了乙基紫与SCN-反应生成用于离子选择性电极缔合物的稳定常数,建立了测定缔合物稳定常数的方法,用紫外分光光度法测得该缔合物的稳定常数为2.6367×106,检测方法的相对标准偏差为2.28%.
使用氯离子自动电位滴定仪检测试样中氯离子时,其电势是负值,结果显示也是负数,这时读数是0呢还是负负得正?
[电化学专题]:电 动 势 测 定 背景知识一、关于电池、电极和盐桥 电化学是研究电现象与化学现象之间内在联系的一门学科,其最基本的要素是电极和溶液。电极能传导电子,常为金属,也可以是半导体。电池是原电池和电解池的通称,电池由至少两个电极及相应的电解质组成,它依靠离子导电,通常是水溶液,也可以是非水溶液、熔盐或固体电解质。1、电极反应:在电极-溶液界面上产生的伴有电子得失的氧化或还原反应。2、电池反应:电池中各个电极反应、其它界面上的变化以及由离子迁移所引起的变化的总合。其中必进行氧化还原反应。3、阳极:负离子趋向或正离子离开的电极。在阳极上产生失电子的氧化反应,电流由电极进入溶液。4、阴极:正离子趋向或负离子离开的电极。在阴极上产生得电子的还原反应,电流由溶液进入电极。5、正极:电势高的电极。6、负极:电势低的电极。7、原电池:将化学能转变为电能的装置,池内发生 0的自发反应,运行时两电极间产生的电势差形成了对外做功(输出电能)的本领。又称之为伽伐尼电池。8、电解池:将电能转化为化学能的装置,池内发生 0的非自发反应,运行时电池消耗从外界输入的电能。当通过电极的电流为零,电池达到电化学平衡时,原电池与电解池也就没有区别。9、可逆电池:满足热力学可逆条件的电池,其两端的电势差为该可逆电池的电动势。形象地说,电动势是促使电荷流动的势头。可逆电池须满足以下三个条件:(1)电极和电池反应本身须可逆,这样在电池充电时,可使放电反应的物质得到复原。(2)在充或放电过程中,通过电极的电流须无限小,此时电极反应在接近电化学平衡的状态下进行,电池能作最大的非体积功。这样在电池充电时,可使原放电时的能量得到复原。(3)电池工作时,无其他不可逆过程(如扩散)存在。10、可逆电极:可逆电池要求其各个相界面上发生的变化都是可逆的,亦即电极/溶液界面上的电极反应同样须是可逆的,此即可逆电极。11、标准电池:作为电动势测定时校验之用,它具有稳定的电动势,且其温度系数很小。韦斯顿发明的镉汞电池常作为标准电池,这种电池具有高度可逆性。韦斯顿标准电池多为饱和式,有H管型和单管型两种,如图1所示。对于H型标准电池,负极为镉汞齐(含12.5%Cd),上部铺以CdSO4∙ H2O(s),正极为纯Hg上铺盖糊体状的Hg2SO4(s)和少量CdSO4∙ H2O(s),两极之间盛以CdSO4的饱和溶液,管的顶端须密封,并留一定空间以供热膨胀之用,两极的底部各接一铂丝与电极相连。做标准电池所用的各种物质须极纯。 [img]http://ng1.17img.cn/bbsfiles/images/2005/11/200511181830_10378_1604910_3.gif[/img]
[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱压力一直升高,不稳定。第一次出现的时候依次排查发现保护住有问题。换了保护柱,第一天做样都正常压力在4.9-5.2之间。第二天再开机做样时,压力由4.9上升到12点多。单接保护住20分钟压力变化从2.8-4.1还在上升,单结保护住压力在5.2-6.0之间。两者都接压力从9.8上升到12.0还有上升趋势。还有废液管排水不是一节一节的,而是连续的这个有问题吗?仪器是青岛盛翰[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],型号:CIC-D120。请大神们帮忙解决一下是什么问题。
[align=center]离子计检定规程修订说明[/align]一、任务来源离子计检定规程修订任务由全国物理化学计量技术委员会下达。归口单位:全国物理化学计量技术委员会。由中国测试技术研究院承担制定任务。二、修订本规程的目的意义 离子计是广泛应用于[s]工矿企业[/s]工业、农业、国防、科研、[s]商品检验、卫生防疫、食品检验、[/s]医[s]药[/s]疗卫生、环境保护等多个[s]领域[/s]领域的常用仪器[s],是计量法规定强制检定的项目之一[/s]。JJG 757-2007 离子计检定规程是检定时所依据的法规性文件。[s]。[/s]由于离子计仪器的更新发展,[s]不断有新的要求出现,而原离子计检定规程制订于2007年,[/s]部分检定方法及要求也[s]发生了变化,原规程也出现了[/s]应适应新的仪器发展要求[s]的条款,[/s]。为了确保量值的准确传递及数据的可靠使用,有必要修订该检定规程,以便更为贴切地开展这项检定工作。三、修订本规程的技术依据JJF 1001-2011 通用计量术语及定义JJF 1002-2010 国家计量检定规程编写规则JJG757-2007离子计GB/T 26812—2011 离子选择电极校准溶液制备方法四、修订内容说明 与JJG757- 2007 《离子计》相比,除编辑性修改外,在主要技术内容有如下变化:删除了0.02级和0.05级实验室离子计的计量性能要求;删除了指针式模拟调整的斜率调节器范围、等电位调节器调节范围、定位调节器调节范围等检定项目;删除了输出误差、稳定性、电源电压适应性等检定项目;删除了附录C;修改了术语,按照JJF 1001-2011 通用计量术语及定义的要求将原规程中的“示值误差”修改为“电计示值偏移”;将原规程中的“重复性”修改为“电计测量不确定度”;将原规程中的“温度补偿器误差”修改为“温度补偿器偏移”;将原规程中的“温度示值误差”修改为“温度示值偏移”;修改了检定环境条件,将原规程中的相对湿度由小于某湿度修改为具体范围;修改了标准器的准确度等级要求;修改了输入电流、输入阻抗试验方法;减少了后续检定项目:所有实验室离子计的后续检定都取消了输入阻抗、输入电流两个检定项目;后续检定的电计示值偏移和电计测量不确定度两项,都只进行电位示值偏移和电位测量不确定度的检定;增加了电计部分活度的测量不确定度试验方法和计量要求(见第6.3.6.3和表1);增加了仪器示值偏移和仪器测量重复性试验方法和计量要求(见第6.3.9、6.3.10及表1);增加了附录C 离子活度标准溶液的制备方法。
觉得理解起来没有四极杆马修稳定图容易。图上横坐标不是RF电压,而是离子喷射点qz ,这个,用比较形象的解释,是代表什么呢?水平线上下的网状部分,又该怎么理解呢(因为离子从不会经过这些区域)?欢迎大家用通俗易懂的语言赐教啊!
当绝缘样品经过长时间的氩离子轰击后,可能会导致样品表面累积大量的正电荷,荷电位移可以高达一百多电子伏特。累积的正电荷会随时间逐渐转移走,荷电位移因此逐渐减少,但很长时间都不能够稳定。例如窄扫过程中扫第一个元素时位移50eV,扫最后一个元素时位移40eV。使得荷电校正非常困难。请教你们在实践中是否曾经遇到这个问题?如何避免该问题的发生?我们的离子枪型号时EX05。曾经尝试在样品表面覆盖金属网以提高样品的导电性,但是效果不明显。
谁有固定污染源 氟化物 离子选择电极法HJ/67-2001 标准曲线 最好全点 各点的毫伏值
如题,离子选择电极可以配到自动电位滴定仪上吗?离子选择电极在测量的时候是不是还需要配一个参比电极?有复合好参比电极的离子选择电极吗?请大家帮忙
我想请教各位:四极杆与离子阱质谱仪的优缺点各是什么?是不是离子阱质谱的质谱仪没有标准谱库,在定分子式时有一定的难度?
硫代硫酸钠标准滴定溶液的标定,用硫代硫酸钠标准滴定溶液测定食盐中碘离子含量。有谁做过啊?怎么做有那些标准参考?做的过程中要注意那些事项.如果有的发一份给我谢谢:308775746@qq.com
谁给个用自动电位滴定仪测溴离子浓度的方法,检测中所需溶液的配制,啥都没有,谁有这个方法啊,仪器是雷磁的自动滴定仪
请问大家有做过用CuSO4做滴定剂,去滴定几种螯合剂,比较他们的对铜离子的螯合性能。是不是每种螯合剂都要加入特定的PH缓冲溶液下下才会出现EP点?
最近公司要扩项,涉及到水质碘离子的测定,求各位大神告知一下,需要哪些硬件(备注:已有一台瑞士万通883离子色谱)?色谱柱、抑制器、检测器这些直接在883基础上加装还是得重新买一台离子色谱?另外做工业循环冷却水中钠、铵、钾、镁和钙离子的测定离子色谱法GB/T15454-2009这个标准时需要哪些设备!!!
用氯仿做溶剂,碘分子,碘离子,三碘离子,五碘离子的紫外吸收各在什么位置呢?好心人帮帮忙~~
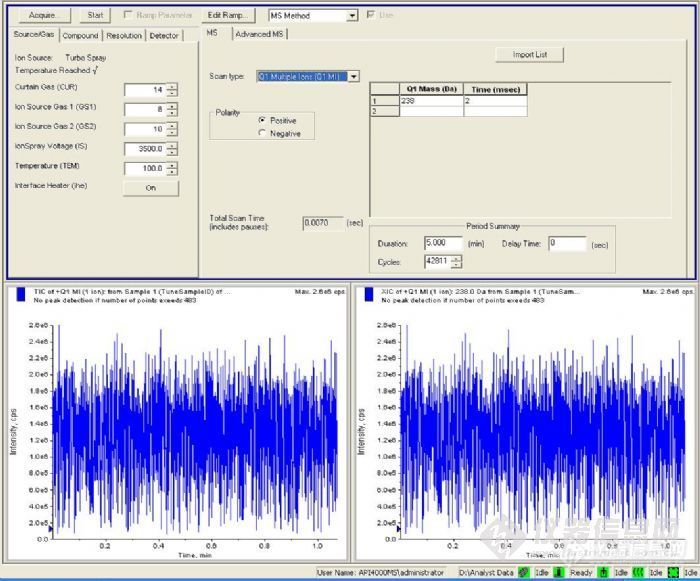
请问战友, 在Tune时, MAC具体是什么含义,on和off在调谐时有何区别?刚开始使用AP14000做定量分析。今天用流动注射法对目标化合物进行优化, 发现化合物离子化非常的不稳定,母离子离子强度变化太大 (如图)。用MRM检测子离子也是同样的不稳定。优化了sourece gas 和compound选项,也没见起色!请有经验的战友帮忙看看是什么问题啊?[img]http://ng1.17img.cn/bbsfiles/images/2010/05/201005220529_220067_1636522_3.jpg[/img]
各位老师,你们好!最近在做一个药品的含量测定是通过破坏其结构获得游离的氯离子来测的,药典规定是用电位滴定指示终点,0.1N硝酸银滴定,做了好几天了,除了第一次做有电位突跃以外,后面怎么做都没有突跃,我用的是国产的PHS-3C型酸度计,电极是216型银电极和217型饱和甘汞电极,双盐桥,外面盐桥为饱和硫酸钾(药典规定)。有用过这个的老师们帮忙分析一下原因,很着急啊
用Y溶液检查等离子体状态;进 1000 ppm Y 溶液观察等离子体 ,对于垂直炬管,红色弹头区应当刚好在炬管顶端。水平炬管应当刚好在右边一点。兰色分析区应当清楚地见到。您觉得做法有道理吗?
各位大虾,小弟这厢有礼了小弟现在遇到一个非常让人头痛的问题[em09509]实验是采用NH4SCN反滴定硝酸银的办法来测定总氯离子的含量的实验,实验中的指示剂为硫酸亚铁铵,从理论上来讲溶液滴定至淡红色即为实验的滴定终点,但实际上小弟感觉非常困难。1.首先是一直有氯化银的白色沉淀,其次还有硫氰化银的沉淀,小弟还发觉一个问题,在认为是接近终点的时候,经过一个剧烈的晃动,溶液的颜色又出现变浅的迹象2.还有一个小弟的滴定溶液中有部分的Fe2O3粉末,这本身就会使沉淀显示一定的红色,小弟不能确定这淡红色是来自于溶液还是来自于沉淀中的Fe2O3粉?请各位有经验的哥哥姐姐给予指导,谢谢
谢谢各位老师的指点,但我还想请教一个问题,在测定硫酸中是否有氯离子时,如果加入硝酸银溶液,不也会产生硫酸银沉淀吗,是否影响我的判定??
本人用的是上海精科的离子计 pxsj-226,用的是雷磁的PF-1-01的氟离子选择电极,232参比电极,都是新买没多久的,可是在测氟化物的时候电位数一直在变化,都是到了最低点以后又往上升,等了很久都不稳定,想问一下有没有老师指点一下这是什么原因造成的呢,又该如何解决。麻烦大家了。