药品研发注册杂质研究与控制专题研讨会会议通知
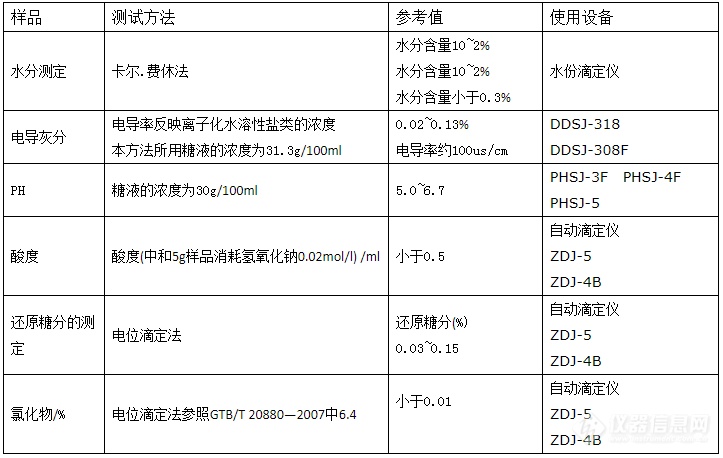
关于举办“药品研发注册杂质研究与控制专题研讨会”的通知 各有关单位: 随着《国家药品安全规划(2011—2015年)》的出台,对全面提高药品安全保障能力,降低药品安全风险提出了更高的要求 而在药品安全研究中,杂质问题一直是国内注册和国际注册的难点和重点,控制药物中杂质已成为控制药品质量的关键因素之一,也是困扰着广大药物分析工作者的难题之一。由于药物杂质的来源广泛,已知的杂质可以通过现有的分析手段进行定性定量,未知的杂质则成为分析的难题,为了让广大药物分析工作者能实现有效地药品杂质控制,更深刻的理解安全性对于药品的关键影响,经研究,全国医药技术市场协会定于2013年3月15日-17日在北京市举办“药品研发注册杂质研究与控制专题研讨会”。请各有关单位积极选派人员参加。现将有关事项通知如下: 一、会议时间地点: 时间:2013年3月15日-17日(15日全天报到) 地点: 北京市 (地点确定直接通知报名者) 二、会议主要内容 详见课程安排(附件一) 三、参会对象 制药企业和新药研究机构的研发人员,各级药品检验所(院)和口岸药品检验所人员,药品生产企业研发技术与质量管理负责人,新药研发CRO实验室人员及高管。各药品分析仪器设备研发生产、代理商 各高等院校、科研院所、医疗机构等相关专业人员。 四、会议说明 1、理论讲解,实例分析,模拟审计,互动答疑. 2、主讲嘉宾均为药典委委员和行业内资深专家、欢迎来电咨询 3、本次会议将征集与会议主题和研讨内容有关的论文。来稿应具有科学性、实用性,且论点鲜明、数据可靠、文字精练通顺。截稿日期:2013年3月9日。 五、会议费用 会务费:1980元/人。会务费包括:培训、研讨、证书、资料及论文集。食宿统一安排,费用自理。 六、联系方式 电 话:13121666780 传 真:010-52226401 联 系 人:陈海涛 邮 箱:yyxhpx2012@126.com 会议质量监督电话:010-51606480 张 岚 附件一 日 程 安 排 表 3月16日 (星期六) 09:00-12:00 14:00-17:00 药品杂质分析指导原则 1、创新药物杂质研究的思路、仿制药物杂质研究的思路、原料药物杂质研究的思路 2、仿制药与原研有关物质的对比研究 3、.新药注册申请资料的质量要求、药物杂质研究案例分析(对注册批件中生产工艺内容要求的思考) 4、针对质量标准中已规定的已知杂质和未知杂质的研究思路 5、药物研发中杂质分离、分析、控制策略与去除策略 6、有关物质研究中的液相使用技巧与注意事项 7、起始原料质量对终产品的重要影响:杂质超标等问题 8、原料药杂质控制的相关法规:Q3A, Q3B, Q3C 9、原料药申报中采用HPLC方法测定有关物质存在的问题 10、原料药与成品药中的残留溶剂 11、主药与辅料相容性研究时出现的杂质问题 12、案例分析 主讲人:谢沐风 资深专家、上海市食品药品检验所及国家药典委中检所相关专家等。 3月17日 (星期日) 09:00-12:00 14:00-17:00 FDA对药物杂质的控制要求 1、原料药与成品药中的有机杂质 2、有机杂质来源和控制 3、有机杂质控制限度的论证 4、案例分析:有机杂质控制限度的设置和论证 5、原料药与成品药中的残留溶剂 6、残留溶剂的指导原则和控制限额的建立 7、案例分析:如何建立残留溶剂的控制限额 8、具有基因毒性杂质的控制 9、多晶型药物质量控制、异构体杂质控制等。 主讲人:沈新华博士 上海安必生技术有限公司研发副总裁,首席科学家,主要负责药物分析研发。曾在国外工作20 多年,具有药物研发、药物合成、药物分析的丰富实践经验及其深厚的理论知识,以及国际仿制药公司工作的经验。曾在TEVA 药业(全球著名的跨国仿制药集团)加拿大分公司任高级研发科学家,以及在加拿大最大的制药公司Apotex 任研发部门经理,负责和参与了数十种非专利药ANDA 的分析研发、药物申报和质量监控等工作。曾获中国药科大学有机合成硕士学位和瑞典皇家理工大学 化学博士学位 兼任北京大学药物信息与工程研究中心授课教师。 备注 每天除专家报告外,还安排了约1小时的代表发言和提问时间。 附件二: 药品研发注册杂质研究与控制专题研讨会回执表 (此表复制有效) 单位名称 联系人 地 址 邮 编 姓 名 性别 职务 电 话 传真/E-mail 手 机住宿是否需要单间:是○ 否○ 是否参加企业推广: 是○ 否○ 是否参加会议发言:是○ 否○ 是否提交论文: 想学习的内容: 论文题目: 联系人: 陈海涛 电话/传真:010-52226401 邮箱:yyxhpx2012@126.com