高分辨SID-EMR Orbitrap仪器研制及大蛋白复合物结构测定
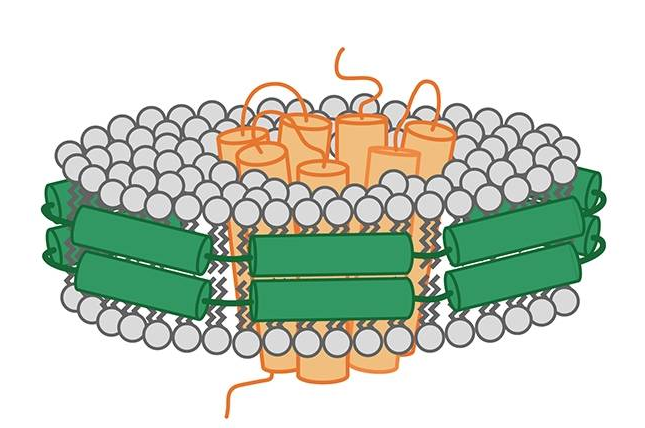
p style=" text-align: justify " 近日俄亥俄州立大学化学和生物化学系的 span style=" font-family: times new roman " VickiH. Wysocki /span 教授课题组在AC上发表了一篇文章,题目为 span style=" font-family: times new roman " Surface-InducedDissociation of Noncovalent Protein Complexes in an Extended Mass RangeOrbitrap Mass Spectrometer /span 。 /p p style=" text-align: justify " 获取蛋白质复合物的四级结构信息,对于理解其生物功能来说至关重要。与传统的CID/HCD通过多次碰撞沉积能量以实现解离相比, strong 表面诱导解离 /strong ( span style=" font-family: times new roman " Surface induceddissociation,SID /span )是通过使复合物离子撞击一个具有化学惰性、刚性的表面,经过单次高能撞击后,产生相比于CID和HCD技术电荷更均匀分布的蛋白亚基(如图1),从而提供化学计量比和互作网络等信息。此外,相比于CID常常导致小分子配体丢失,SID可以产生保留小分子配体的复合物亚基。 /p p style=" text-align: justify " & nbsp /p p style=" text-align: center " img width=" 600" height=" 253" title=" SID.webp.jpg" style=" width: 600px height: 253px " alt=" SID.webp.jpg" src=" https://img1.17img.cn/17img/images/201903/uepic/671db102-c3a5-4bc3-ad7d-5e07248fc1a3.jpg" border=" 0" vspace=" 0" / /p p style=" text-align: center " 图1. SID示意图 /p p style=" text-align: justify " 目前,SID技术在蛋白复合物方面的工作主要是在飞行时间质谱( span style=" font-family: times new roman " TOF MS /span )上完成,但随着蛋白复合物的分子量越来越大,结构解析深度越来越深入,对质谱仪器的分辨率也提出了更高的要求。每一种类型的质量分析器( span style=" font-family: times new roman " TOF、FTICR或者Orbitrap /span )都有它们的优劣势,而仪器的选择主要依赖于待解决的问题本质。为此,Vicki H. Wysocki课题组与赛默飞公司Alexander A. Makarov博士合作, strong 首次将SID解离源装配到Exactive Plus Extended Mass Range(EMR)Orbitrap仪器上 /strong (如图2)。这套SID即可用来传输离子又可用来进行SID。值得一提的是,SID装置并未影响离子进入HCD池和一级质谱分析。 /p p style=" text-align: center " img title=" EMR-orbitrap.jpg" alt=" EMR-orbitrap.jpg" src=" https://img1.17img.cn/17img/images/201903/uepic/97acf2a9-f158-474e-bef1-ca2f3c2deea8.jpg" / /p p style=" text-align: center " img width=" 600" height=" 498" title=" 2.webp.jpg" style=" width: 600px height: 498px " alt=" 2.webp.jpg" src=" https://img1.17img.cn/17img/images/201903/uepic/7c134afb-82fa-472e-8848-062123d511f0.jpg" border=" 0" vspace=" 0" / /p p style=" text-align: justify " 图2. a)SID装置3D设计图,b)SID模式下离子轨迹图,c)SID改造后EMR Orbitrap仪器图。 /p p style=" text-align: justify " 随后,作者 strong 利用该仪器对Streptavidin和L-GlutamateDehydrogenase蛋白复合物进行了质谱分析 /strong 。其中,前者是具有D2对称性的同源四聚体,后者是具有D3对称性的同源六聚体。图3为Streptavidin的一级谱及其SID谱图。先前的文献表明,通过CID主要产生的是streptavidin复合物的去折叠单聚体和三聚体,但这一结果显然不能支持streptavidin是由同源二聚体组成的结构。而11+的母体streptavidin复合物经过SID会解离成两个二聚体,分别为5+和6+,证明SID更能反映他们真实的拓扑结构(图3a-c)。值得一提的是,之前对于谱图中出现的3+单聚体和6+同源二聚体,由于TOF MS分辨率不高所以要依靠IMS才能进行分辨3,但现在EMR Orbitrap在高分辨率模式(R=140,000 at m/z 200)下就可直接对它们二者进行分辨(图3d),甚至盐加和离子或者N末端Met修饰与否都可以在高分辨谱图中完全获得(图3e)。 /p p style=" text-align: center " img width=" 600" height=" 466" title=" 3.webp.jpg" style=" width: 600px height: 466px " alt=" 3.webp.jpg" src=" https://img1.17img.cn/17img/images/201903/uepic/335862ab-316e-4d66-8193-777c95b0aa48.jpg" border=" 0" vspace=" 0" / /p p style=" text-align: justify " 图3. a)Streptavidin四聚体拓扑结构(PDB ID:1SWB),b)Streptavidin四聚体一级质谱图,c)11+价态Streptavidin四聚体的SID谱图( span style=" font-family: times new roman " 45 V,495 eV /span ),d)高分辨率模式下3+价态Streptavidin单聚体和6+价态的二聚体,e)3+价态单聚体和6+价态二聚体的N末端蛋氨酸修饰和Na离子加和谱图。 /p p style=" text-align: justify " 此外,作者还考察了 span style=" font-family: times new roman " L-Glutamate Dehydrogenase /span 同源六聚体的拓扑结构。HCD结果表明,该六聚体很难在气相中发生解离,需要较高HCD能量和高电荷态,常常导致先失去一个去折叠单体,无法真实反映亚基组成。而通过SID可以获得比较稳定的三聚体信号,反映出 span style=" font-family: times new roman " L-GlutamateDehydrogenase /span 同源六聚体的拓扑结构主要为三聚体-三聚体界面,在低能量下主要断裂较弱的三聚体界面(图4a),当能量逐渐升高单体会从三聚体亚基中解离出来(图4b)。 /p p style=" text-align: center " img width=" 600" height=" 461" title=" 4.webp.jpg" style=" width: 600px height: 461px " alt=" 4.webp.jpg" src=" https://img1.17img.cn/17img/images/201903/uepic/f1e97f6c-ca94-485b-825b-e918eeceb873.jpg" border=" 0" vspace=" 0" / /p p style=" text-align: justify " 图4. 28+价态L-Glutamate Dehydrogenase同源六聚体在a)175 eV和b)235 eV能量下的SID谱图。 /p p style=" text-align: justify " 综上所述,相比于SID-TOF MS仪器,具有更高质谱分辨率的SID–EMR Orbitrap仪器后续将为大蛋白复合物提供更丰富的四级结构信息。此外,Vicki H. Wysocki课题组先前还报道了将SID装载到FTICR-MS仪器,在SID谱图中可对霍乱毒素(Cholera toxin B,CTB)多种亚基进行同位素分辨(R=210,000 at m/z 5803.7),例如8+四聚体、6+三聚体、4+二聚体和2+单聚体4,感兴趣的学者们可进一步了解。得益于Orbitrap和FTICR的超高质量分辨率,相信SID源将在蛋白-蛋白、蛋白-金属离子、蛋白-小分子配体复合物体系中发挥越来越重要的作用。 /p p style=" text-align: justify text-indent: 2em " 参考文献: /p p style=" text-align: justify " span style=" font-family: times new roman " [1] VanAernum, Z. Gilbert, J. Belov, M. Makarov, A. A. Horning, S. Wysocki, V. Anal. Chem., 2019, DOI: 10.1021/acs.analchem.8b05605. /span /p p style=" text-align: justify " span style=" font-family: times new roman " [2] Zhou, M. Wysocki, V. H. Acc. Chem. Res., 2014, 47, 1010-1018. /span /p p style=" text-align: justify " span style=" font-family: times new roman " [3] Quintyn,Royston S. Yan, J. Wysocki, Vicki H. Chem. Biol., 2015, 22, 583-592. /span /p p style=" text-align: justify " span style=" font-family: times new roman " [4] Yan, J. Zhou, M. Gilbert, J. D. Wolff, J. J. Somogyi, Á . Pedder, R. E. Quintyn, R.S. Morrison, L. J. Easterling, M. L. Pa?a-Toli?, L. Wysocki, V. H. Anal. Chem., 2017, 89,895-901. /span /p p style=" text-align: justify text-indent: 2em " strong 文献链接: /strong /p p style=" text-align: justify text-indent: 2em " a style=" color: rgb(0, 32, 96) text-decoration: underline " href=" https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.analchem.8b05605" target=" _blank" span style=" color: rgb(0, 32, 96) " https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.analchem.8b05605 /span /a /p p style=" text-align: justify text-indent: 2em " (文献原文可联系仪器信息网编辑部提供,联系电话:010-5165-4077-8223) /p p style=" text-align: justify text-indent: 2em " 文中提及的赛默飞 span style=" font-family: times new roman " ExactivePlus(EMR)Orbitrap /span 相关信息可点击链接:& nbsp /p p style=" text-align: justify text-indent: 2em " a style=" color: rgb(0, 32, 96) text-decoration: underline " href=" https://www.instrument.com.cn/netshow/sh100244/C152611.htm" target=" _blank" span style=" color: rgb(0, 32, 96) " https://www.instrument.com.cn/netshow/sh100244/C152611.htm /span /a /p