【新品上市】核电领域专用卧式力学测试系统问世
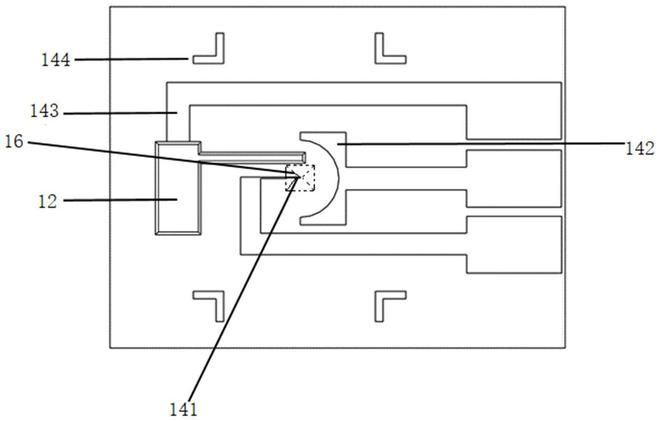
随着全球核能发展趋势,国际上将核电站的发展分为四代。第一代核电站,是指上世纪50、60年代初期开发的核电站。第二代核电站,是指从60年代后期到90年代前期进一步开发和建造的发电功率达30万千瓦的大型商用核 电站。第三代核电站,是从上世纪90年代中后期到2010年开始运行的具有更高安全指标的先进核电站。正在开发中的第四代核电站,具有经济性好、安全性高、产生废物少、核资源可持续、核扩散可防止等优点。其中铅基反应堆(LFR)由于其突出的优点成为第四代反应堆系统具有发展潜力的两种堆型之一。铅基反应堆使用铅或者铅铋共晶合金(LBE)作为冷却剂材料,且最早在前苏联开发用于阿尔法级核潜艇,但由于LBE是一种腐蚀材料,结构钢材在LBE环境会发生液态金属腐蚀(LMC)和液态金属脆化(LME),LMC和LME以及氧浓度成为影响铅基反应堆性能的关键问题。因此为了研究液态铅铋环境下结构材料的力学特性,亟需开发一种可模拟不同氧浓度高温液态铅铋环境的力学试验系统。图1 一到四代核反应堆发展及代表堆型氧控方案 液态LBE控氧技术主要包括气态控氧和固态控氧,其中气态控氧技术又分为两种。如图2所示,第一种是将Ar/H2还原性混合气体或Ar/O2氧化性混合气体通入液态LBE内部或覆盖在表面,通过化学反应实现对氧浓度的控制。如图3所示,另一种气态控氧方式为在液态LBE表面通入Ar/H2/H2O三元混合气体,通过控制H2和H2O的组分比例来使液态LBE氧浓度达到目标值并稳定。第一种气态控氧方式控氧速率较快,但是控氧精度较差且容易失控,第一种气态控氧方式可以获得稳定的氧浓度且波动较小,但时控氧时间较长。图2 第一种气态控氧方式及控氧曲线图3 第二种气态控氧方式及控氧曲线氧传感器及氧浓度测量原理 氧传感器是氧控系统中的关键部件,要求其在低浓度的氧含量范围内准确地、稳定地测量,同时具有长期的运行稳定性。用于液态金属中溶解氧的电化学氧传感器利用了固体电解质的离子导体性质,可以用于测量极低的氧含量。目前,一般采用氧化锆基固体电解质为主要材料,利用电化学浓差式电池原理制作氧传感器。其原理如图4所示,根据 Nernst原理,当固态电解质两端有氧浓度梯度时,氧离子会从高浓度的一侧穿过固态电解质到低浓度的一侧,于是会在固态电解质的阴阳两极之间形成一个可以反映两边氧浓度差值的电动势(EMF)。在一定的温度下,这个EMF的理论值可以通过公式算出: E为理论电动势EMF,单位为V;R=8.31441J/(molK),为理想气体常数;F=96484.6C/mol,为法拉第常数;T为温度,单位是K;PO2,ref为参比电极氧分压;PO2是被测介质中的氧分压。在一定的温度下,参比电极中的氧分压是一定的,那么被测介质中的氧分压就可以通过测量电动势E的值获得。图4 氧传感器原理图 根据参比电极的不同类型,可将氧传感器分为两种,一种是金属-空气氧传感器,如Pt-空气氧传感器,另一种是金属-金属氧化物传感器如Bi-Bi2O3、Cu-CuO2氧传感器。国内外均有多家机构研发了LBE氧传感器,考虑到金属-空气参比电极传感器需要和空气连通,电解质破裂可能会造成回路泄漏,优先开发金属-金属氧化物参比电极氧传感器。且Bi-Bi2O3在应用温度范围、准确性、响应速度、稳定性等方面综合性能优异,基于以上原因,优先开发 Bi-Bi2O3参比电极传感器。 自行设计的Bi-Bi2O3氧传感器结构图如图5-a所示,实物图如图5-b所示,图6为不同温度下氧传感器的稳定性测试结果,测试结果误差稳定在2mV以内。图5 Bi-Bi2O3型氧传感器结构图(1) BNC 接头;(2) 密封法兰;(3) 氟胶圈;(4) 密封陶瓷片;(5) 螺纹压紧件;(6) 锥形环;(7) 散热片;(8) CF法兰;(9) 氧化铝陶瓷管;(10) 电极引线;(11) YSZ陶瓷锥管图6 不同温度下氧传感器稳定性测试结果(a) 500 ℃;(b) 450 ℃;(c) 400 ℃;(d) 350 ℃试验装置 主要构成包括:凯尔测控力学测试系统(卧式/立式),高温液态LBE储液系统,高温液态铅铋试验腔,氧控系统,高温引伸计(卧式)/LVDT位移传感器(立式),保温系统以及支撑台架。其中凯尔测控力学测试系统为测试主体,最大载荷50kN,最大试验频率15Hz。高温液态LBE储液系统储液温度可达550℃,最大储液量15L,可进行液态铅铋氧浓度的预控制。高温液态铅铋试验腔单次试验仅需1.5L液态铅铋,氧控系统包含氧传感器及配套气瓶以及控制系统,可实现动态精确控氧气,误差可控制在2mV以内。根据氧浓度需求,高温液态铅铋试验腔可分为氧饱和液态铅铋试验腔体、贫氧液态铅铋试验腔以及控氧液态铅铋试验腔体。保温系统控温550℃及以上,温差±1℃,隔热效果良好。 高温引伸计/LVDT位移传感器可在550℃氧饱和液态铅铋试验环境下使用,精度达到0.002mm,且配套有特制的固定移动装置,图7为高温液态铅铋环境卧式单轴疲劳试验系机结构图,展示了高温引伸计的安装方式及安装实物图。贫氧液态铅铋试验腔以及控氧液态铅铋试验腔体通过数字图像技术(DIC)进行应变测量。 卧式试验装置方便装夹高温引伸计且节省铅铋,立式试验装置节省占地面积,集成度较高,可根据需要设计卧式或立式结构。图7高温液态金属环境卧式单轴疲劳试验系机结(a) 主机结构;(b) 引伸计安装示意图;(c) 引伸计安装实物图参考文献[1]Rivai A K , Kumagai T , Takahashi M . Performance of oxygen sensor in lead-bismuth at high temperature[J]. Progress in Nuclear Energy, 2008, 50(2-6):575-581.[2]秦博,付晓刚,马浩然,等.铅铋合金气相氧含量控制初步实验研究[J].材料导报, 2019, 33(11):4.DOI:CNKI:SUN:CLDB.0.2019-11-010.凯尔测控公司介绍 凯尔测控是一家专业从事开发、生产、销售各类力学试验系统的国家高新技术企业,自2008年成立以来一直致力于发展新的测试方法。先后与清华大学、北京大学、中科院金属所、中国工程物理研究院等国内著名高校、科研院所建立密切合作,持续在航空、航天、核电等关键领域进行技术研发与投入。公司拥有各类力学性能试验机四个系列四十余个品种,主导产品电磁式疲劳试验系统、原位力学试验系统、原位双轴力学试验系统、拉扭多轴疲劳试验机等测试系统打破国外设备的垄断。凭借着过硬的技术、性能优良的产品和专业妥善的服务,凯尔测控赢得了众多用户的信赖。 凯尔测控是一家专业从事开发、生产、销售各类力学试验系统的国家高新技术企业,自2008年成立以来一直致力于发展新的测试方法。先后与清华大学、北京大学、中科院金属所、中国工程物理研究院等国内著名高校、科研院所建立密切合作,持续在航空、航天、核电等关键领域进行技术研发与投入。公司拥有各类力学性能试验机四个系列四十余个品种,主导产品电磁式疲劳试验系统、原位力学试验系统、原位双轴力学试验系统、拉扭多轴疲劳试验机等测试系统打破国外设备的垄断。凭借着过硬的技术、性能优良的产品和专业妥善的服务,凯尔测控赢得了众多用户的信赖。