生物发光技术在细胞学检测中的应用摘要:本文就生物发光技术的种类、机理、及其技术特点进行了综述,并就其在细胞学检测中的应用与研究进展展开了讨论。关键词:生物发光; ATP;荧光素酶;细胞凋亡;细胞内游离Ca2+自从20多年前,Marlene A DeLuca’s第一个成功的获得表达萤火虫荧光素酶基因(luc基因)的转基因烟草以来,生物发光(Bioluminescenc,BL)作为一个古老而又年轻的技术, 近年来得到了很大的发展和广泛的应用。而近几年来,随着分子生物学的进展以及一些新生物技术工具的出现,尤其在某些关键技术如生物传感器、基因序列分析、活体细胞ATP 测定]等方面取得了一些突破,使生物发光的应用进入了一个新时代,极大提高了生物发光的检测和快速应用,其应用范围更进一步扩大[1]。1 生物发光的种类和特点尽管自然界中的生物体普遍存在发光现象,它们的发光机理、强度和光谱范围存在着很大差异。目前,国际上根据发光的机理不同将生物发光分为:受激荧光,发光生物发光,化学发光和生物的超微弱发光[3,4]。1.1 受激荧光受激荧光是指生物体在受到外界光辐射的作用时,体内固有的荧光物质或吸收的荧光标记物发光的现象。在生物学领域中,由于分析物质荧光的方法敏感性极高,而且几乎所有的有机分子都能够直接或经过适当的化学处理后发生荧光,故很早就受到重视,并逐渐发展成为生物学和医学中的荧光分析。在生物医学领域应用荧光分析最多的是荧光显微技术,基本工具为荧光显微镜。但一般的荧光显微镜某些情况下荧光的亮度不足,使观察困难随着光电技术和计算机技术的进步,已经发展出的激光共聚焦显微镜,操作更加方便,实验可重复性提高,使受激荧光的应用更加广泛[5]。1.2 发光生物发光在生物发光领域中最容易被人们所接受的发光现象就是以萤火虫的闪光为代表的发光生物发光[3]。现在,已了解各种发光生物发光的基本反应,在这个领域中也取得了一些新的进展,例如在体外重组虫荧光素酶,用基因工程技术在大肠杆菌中表达;人工合成荧光素;体外模拟细菌发光体系已获成功;细菌的发光基因已被提出,同样也已用基因工程方法在大肠杆菌中表达。水母发光蛋白已经分离纯化,一级结构已经清楚。由于生物发光的量子效率极高,所以研究生物发光能量的转化具有重要的理论与实际意义。近年来被广泛应用的发光蛋白,如GFP、YFP、CFP 等,其发光原理就是源自动物的自发发光,从而为生物医学研究提供了新的手段[6]。1.3 化学发光化学发光是在化学反应过程中(主要为氧化还原反应)发出可见光的现象[6]。化学发光反应是由两个关键步骤组成:激发和发射。许多化学反应进行时能释放足够的自由能而把参加反应的物质之一激发到能发射光的电子激发态,生成一种激发态产物,在它回到基态时,剩余能量转变成光子能量产生发光现象。随着化学发光物质合成技术的进步,化学发光在生物医学及其它领域的应用越来越广泛[7,8],将化学发光与免疫反应结合起来建立的化学发光免疫测定法和化学发光标记是继荧光标记,放射性核素标记,酶标记三大标记技术之后,发展起来的最新检测技术[8]。1.4 生物超微弱发光 随着生物发光研究的进一步深入,发现人体的器官、组织、细胞、乃至大分子都在发光,不过发光强度更弱。这些有关生物超微弱发光(ultra-weak bioluminescence)的研究课题,构成了当前生命科学发展前沿中的一个极其重要的研究领域——生命系统的超微弱光子辐射(ultra-weak photon emission from living system) [8]。20世纪60~70 年代以来,各国先后出现了一些研究小组专门进行这方面的探讨,如日本的稻场文男小组(1991)研究了鼠肝核的超微弱天然光子发射;德国F.A. Popp小组提出了“生物光子”概念和一系列的相干理论[9]。目前研究已涉及到细胞、亚细胞乃至生物大分子的层次[ 9,10]。越来越多的实验表明,DNA 是生物超微弱发光的一个辐射源。1.5 生物发光特点研究发现生物发光有以下几个特点:① 生物发光的颜色范围很宽,可从红光到深蓝光;② 氧是几乎所有生物发光系统中必须的因素;③ 生物发光是由“荧光素酶”与“荧光素”的化学反应所引起的;④ 所有的生物发光反应似乎都是酶-底物类型的反应,但复杂程度不同,某些生物发光反应涉及3 种或4种底物,而另一些生物发光反应甚至需要3个或4个酶的体系[8]。[/size]
德国WITec公司网络报告:生物细胞组织和医药学的3D共聚焦拉曼成像检测报告内容:着重介绍高分辨3D共聚焦拉曼成像在生物细胞组织和医药学的重要应用,例如生物细胞组织的表征,癌化细胞的鉴定,细胞对药物吞噬过程及药物反应过程的监测。。。报告时间:2014 年3月 26日晚上11:00(北京时间)具体内容请查看以下网址:http://www.witec.de/events/onlineseminars请登录以下网页注册:http://www.microscopy-analysis.com/witecwebinars期待与大家见面!
[font=宋体]流式细胞术,作为一种先进的生物技术,已经在生物医学研究中占据了举足轻重的地位。这种技术以其高精度、高速度以及多参数同时检测的能力,广泛应用于细胞生物学、免疫学、肿瘤学等多个领域。流式细胞术不仅可以对单个细胞进行多参数定量分析和分选,还能够对细胞内部的蛋白质、核酸、细胞受体以及细胞表面抗原等进行检测。因此,它在疾病诊断、药物筛选、细胞功能研究等方面具有广泛的应用前景。本文将对流式细胞术的检测原理、应用领域以及发展前景进行详细介绍,旨在为读者提供对这一技术全面而深入的了解。流式细胞术可以检测什么?下面是具体检测信息及应用:[/font][font=宋体] [/font][b][font=宋体][font=Calibri]1.[/font][font=宋体]细胞表型检测[/font][/font][/b][font=宋体]免疫细胞表型是流式细胞术最突出应用。[/font][font=宋体][font=宋体]通过检测免疫细胞群的表面或细胞内标志物,对其进行鉴定和表征。流式细胞术能够精确鉴定和分类免疫细胞群,例如[/font] [font=Calibri]T [/font][font=宋体]细胞、[/font][font=Calibri]B [/font][font=宋体]细胞、[/font][font=Calibri]NK [/font][font=宋体]细胞、树突状细胞、单核细胞、巨噬细胞、血小板和粒细胞等。[/font][/font][font=宋体] [/font][font=宋体]研究人员可以识别和量化异质群体中的各种免疫细胞亚群。[/font][font=宋体] [/font][font=宋体][font=宋体]临床医生可以诊断和监测各种血液系统疾病、进行免疫免疫评估([/font][font=Calibri]8[/font][font=宋体]大类免疫细胞构成与肿瘤预后)。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体][font=Calibri]2.[/font][font=宋体]细胞活力检测[/font][/font][/b][font=宋体] [/font][font=宋体]流式细胞术能够定量测量群体内和体外培养的活细胞和非活细胞。[/font][font=宋体] [/font][font=宋体]通过使用选择性标记活细胞或死细胞的荧光染料,流式细胞术可以提供精确可靠的活力测定,有助于确定细胞活力百分比。[/font][font=宋体] [/font][font=宋体]流式细胞术可以根据特定的标志物或染料区分活细胞、凋亡细胞和坏死细胞,从而更详细地了解细胞的健康和状态。通过将活力染料与细胞表面抗原、细胞内蛋白或功能测定的标记物相结合,研究人员可以在特定细胞类型或实验条件下获得有关细胞活力及其发生机制的全面信息。[/font][font=宋体] [/font][font=宋体]最常用的活性检测染料[/font][font=宋体] [/font][font=宋体][font=宋体]死细胞:碘化丙啶([/font] [font=Calibri]propidium iodide[/font][font=宋体],[/font][font=Calibri]PI[/font][font=宋体])和[/font][font=Calibri]7-AAD[/font][font=宋体],与[/font][font=Calibri]DNA[/font][font=宋体]结合,但只能进入膜受损的细胞,使死细胞发出荧光。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]凋亡细胞:[/font][font=Calibri]annexin V[/font][font=宋体]:对磷脂酰丝氨酸具有强结合亲和力的蛋白质,在细胞凋亡的早期阶段暴露在质膜的外表面[/font][font=Calibri]annexin V+PI[/font][font=宋体]是常用区分凋亡细胞和坏死细胞的组合。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]活细胞:[/font][font=Calibri]calcein AM[/font][font=宋体]、[/font][font=Calibri]CFDA[/font][font=宋体]([/font][font=Calibri]carboxyfluorescein diacetate[/font][font=宋体])、[/font][font=Calibri]FDA [/font][font=宋体]([/font][font=Calibri]fluorescein diacetate[/font][font=宋体]) :进入活细胞,但只有在与细胞内酶相互作用时才会发出荧光[/font][/font][font=宋体] [/font][font=宋体][font=宋体]细胞体内增殖:[/font][font=Calibri]CFSE(CFDA-SE)[/font][font=宋体]穿透细胞膜,在活细胞内与胞内蛋白共价结合,水解后释放出绿色荧光。在细胞分裂增殖过程中,它的荧光强度会随着细胞的分裂而逐级递减,标记荧光可平均分配至两个子代细胞中,因此其荧光强度是亲代细胞的一半,根据这一特性,它可被用于检测细胞增殖,细胞周期的估算及细胞分裂等方面。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]3.[/font][font=宋体]细胞周期分析[/font][/font][/b][font=宋体] [/font][font=宋体]从流式细胞术的早期开始,细胞周期分析就成为有价值的应用。[/font][font=宋体] [/font][font=宋体]原理是基于荧光和核酸的量之间的关系。[/font][font=宋体] [/font][font=宋体][font=宋体]常用核酸结合染料:碘化丙啶([/font][font=Calibri]PI[/font][font=宋体]),[/font][font=Calibri]Hoechst[/font][font=宋体],[/font][font=Calibri]DAPI[/font][font=宋体],[/font][font=Calibri]7-AAD[/font][font=宋体],溴化乙锭等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]流式细胞术细胞周期分可以有很多方面的应用,例如,[/font][font=Calibri]DNA/Ki67[/font][font=宋体]测定可以将表型选择与细胞周期分析相结合,用于监测[/font][font=Calibri]p53[/font][font=宋体]细胞周期停滞,评估抗癌活,多药耐药性等。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]4.[/font][font=宋体]离子通道测定[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]钙作为关键的第二信使,在许多细胞信号通路中起着至关重要的作用。它在免疫细胞活化中尤为重要,包括[/font][font=Calibri]T[/font][font=宋体]细胞、[/font][font=Calibri]B[/font][font=宋体]细胞和[/font][font=Calibri]NK[/font][font=宋体]细胞。[/font][/font][font=宋体]此外,钙信号传导还参与肥大细胞脱颗粒、神经元兴奋性、突触传递和神经递质释放至关重要。[/font][font=宋体] [/font][font=宋体][font=宋体]细胞脱颗粒的早期测量值是通过使用钙离子载体[/font][font=Calibri]A23187[/font][font=宋体]的流式细胞术确定的。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]常用荧光染料:[/font][font=Calibri]fluo-3 [/font][font=宋体]和[/font][font=Calibri]indo-1[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]虽然[/font][font=Calibri]Ca2+[/font][font=宋体]通道测量是最常见的应用之一,但其他离子如镁、钾、钠和氢也可以使用流式细胞术进行监测。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]5.[/font][font=宋体]细胞功能检测[/font][/font][/b][font=宋体]最早的检测是细胞酯酶。[/font][font=宋体] [/font][font=宋体][font=宋体]使用响应氧化态变化的活性染料检测粒细胞的氧化电位。例如,氢乙啶([/font][font=Calibri]hydroethidine[/font][font=宋体])用于中性粒细胞呼吸爆发。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]二乙酸二氯荧光素([/font][font=Calibri]dichlorofluorescein diacetate[/font][font=宋体]),已被用于吞噬细胞功能研究。[/font][/font][font=宋体] [/font][font=宋体]效应细胞杀伤功能,是流式细胞术的另外一个重要应用。[/font][font=宋体] [/font][font=宋体]细胞因子是免疫细胞功能的重要执行分子,对科学研究,免疫细胞治疗,临床诊疗都及其关键。基于流式细胞术开发的多重细胞因子检测,已经有广泛应用。[/font][font=宋体] [/font][b][font=宋体][font=Calibri]6.[/font][font=宋体]蛋白质工程[/font][/font][/b][font=宋体] [/font][font=宋体]流式细胞术和分选传统上不是蛋白质工程中最常用的技术之一。然而,近年来,在该领域的应用越来越多。[/font][font=宋体] [/font][font=宋体][font=宋体]流式细胞术被用于酶学蛋白质研究,包括细胞色素[/font][font=Calibri]P450[/font][font=宋体]、葡萄糖氧化酶、几丁质酶、纤维素酶、过氧化物酶、酯酶、转移酶、β半乳糖苷酶、硫代内酯酶等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]蛋白质工程,包括在基因水平上引入突变(随机或特异性),以创建由数千到数百万个单个蛋白质变体组成的文库(如上图),使用流式细胞术[/font] [font=宋体]每天能够分析多达[/font] [font=Calibri]10^8[/font][font=宋体]–[/font][font=Calibri]10^9 [/font][font=宋体]个克隆,并对具有所需特性的克隆进行分类。[/font][/font][b][font=宋体] [/font][font=宋体][font=Calibri]7.[/font][font=宋体]哺乳动物细胞和细菌细胞分选[/font][/font][/b][font=宋体] [/font][font=宋体]细胞分选是流式细胞的重要应用之一,哺乳动物细胞相对成熟,不做赘述。细菌细胞方面的应用,也逐渐开始建立。[/font][font=宋体] [/font][font=宋体]与耗时的传统琼脂铺板检测方法相比,流式分选可以快速检测和分选悬浮液中的单个细菌细胞。[/font][font=宋体] [/font][font=宋体]尽管细胞分选仪具有高性能,但它们在微生物学中的应用一直受到限制。[/font][font=宋体] [/font][font=宋体]这主要是由于微生物体积小,因此很难将它们与培养基中的细胞碎片或背景颗粒区分开来。另一个潜在的问题是,通常没有细菌菌株特有的抗体。[/font][font=宋体] [/font][font=宋体][font=宋体]限制细胞分选仪在细菌检测和分选中的适用性的其他因素主要与分选仪硬件功能本身有关,在流式细胞术仪器的早期,数量有限的激光器和检测器,限制一次只能使用一种或两种荧光染料。随着最新仪器的发展,多激光器和检测起的仪器被开发:包括赛默飞世尔的[/font][font=Calibri]Bigfoot[/font][font=宋体]光谱细胞分选仪,[/font][font=Calibri]BD FACSAria III[/font][font=宋体]分选仪,索尼[/font][font=Calibri]MA900[/font][font=宋体]细胞分选仪和贝克曼库尔特的[/font][font=Calibri]MoFlo Astrios EQ[/font][font=宋体]等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]此外,部分致病性细菌,需要在[/font][font=Calibri]BSL2[/font][font=宋体]以上的实验环境下进行,现在部分流式细胞术带有[/font][font=Calibri]BSL 2 hood[/font][font=宋体]。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]8.[/font][font=宋体]液滴微流体[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]液滴微流体是一个相对较新的领域,专注于皮升体积中含有细胞或[/font][font=Calibri]DNA[/font][font=宋体]的离散液滴的形成,操作和分析,应用于生物学、化学、材料科学和医学。[/font][/font][font=宋体] [/font][font=宋体]在生物学中,液滴微流体可实现单细胞分析、生物分子的高通量筛选、细胞异质性研究和药物发现。[/font][font=宋体] [/font][font=宋体][font=宋体]流式细胞术分析是研究单细胞的强大技术,可提供有关各种参数的宝贵信息。然而,它的测量仅限于直接连接到细胞的分子,例如表面或细胞内标记物,限制研究由细胞分泌或由[/font][font=Calibri]DNA[/font][font=宋体]分子产生但不物理附的分子。液滴微流体提供了一种克服这一限制的新方法。将细胞或[/font][font=Calibri]DNA[/font][font=宋体]封装在单个液滴中会产生离散的区室,从而能够分析由封装实体释放或产生的化合物。[/font][/font][b][font=宋体] [/font][font=宋体][font=Calibri]9.[/font][font=宋体]下一代生物制剂[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]生物制药已经占据了药物市场的重要份额,包括治疗性蛋白质([/font][font=Calibri]65%[/font][font=宋体]),疫苗([/font][font=Calibri]20%[/font][font=宋体])等。通过测序([/font][font=Calibri]NGS[/font][font=宋体])进行单[/font][font=Calibri]B[/font][font=宋体]细胞库分析和克隆扩增鉴定,直接从人类幸存者克隆免疫球蛋白基因,分离出高亲和力中和抗体,加快了单克隆抗体药物的研发,然而,这种方法比较昂贵,且依旧需要后续的功能验证等。新策略可使用流式细胞术、[/font][font=Calibri]MACS[/font][font=宋体]或微流体将单细胞分离与功能筛选相结合,降低开发成本并消除失败的候选药物,是流式细胞术新的应用开发方向。[/font][/font][font=宋体] [/font][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/flow-cytometry-service][b]流式细胞检测技术服务[/b][/url],拥有[/font][font=宋体][font=宋体]①具有 [/font][font=Calibri]20,000 [/font][font=宋体]次以上流式抗体筛选鉴定经验及多年流式诊断抗体研发经验,在实验方案设计、样品制备、数据分析等方面确保科学性、准确性和可靠性[/font][font=Calibri] [/font][/font][font=宋体][font=宋体]②拥有 [/font][font=Calibri]1,000 [/font][font=宋体]余株自产精品流式抗体,覆盖细胞膜、胞内、核内及分泌抗原;[/font][/font][font=宋体][font=宋体]③自产 [/font][font=Calibri]Annexin V/7-AAD [/font][font=宋体]凋亡检测试剂盒,并储备多种流式检测常用试剂,大大节约购买试剂的等待时间和实际费用;[/font][/font][font=宋体][font=宋体]④可以提供近 [/font][font=Calibri]200 [/font][font=宋体]种细胞系选择,省去细胞样本寄送过程中的风险,并可以免费提供健康人外周血细胞对照品。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/flow-cytometry-service[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b][font=宋体] [/font][font=Calibri] [/font]
摘要:细胞凋亡与坏死是两种完全不同的细胞凋亡形式,根据死亡细胞在形态学、生物化学和分子生物学上的差别,可以将二者区别开来。细胞凋亡的检测方法有很多,下面介绍几种常用的测定方法。一、细胞凋亡的形态学检测根据凋亡细胞固有的形态特征,人们已经设计了许多不同的细胞凋亡形态学检测方法。1. 光学显微镜和倒置显微镜(1) 未染色细胞:凋亡细胞的体积变小、变形,细胞膜完整但出现发泡现象,细胞凋亡晚期可见凋亡小体。贴壁细胞出现皱缩、变圆、脱落。(2) 染色细胞:常用姬姆萨染色、瑞氏染色等。凋亡细胞的染色质浓缩、边缘化,核膜裂解、染色质分割成块状和凋亡小体等典型的凋亡形态。2. 荧光显微镜和共聚焦激光扫描显微镜一般以细胞核染色质的形态学改变为指标来评判细胞凋亡的进展情况。常用的DNA特异性染料有:HO 33342 (Hoechst 33342),HO 33258 (Hoechst 33258), DAPI。三种染料与 DNA的结合是非嵌入式的,主要结合在DNA的A-T碱基区。紫外光激发时发射明亮的蓝色荧光。Hoechst是与DNA特异结合的活性染料,储存液用蒸馏水配成1mg/ml的浓度,使用时用PBS稀释成终浓度为2~5mg/ml。DAPI为半通透性,用于常规固定细胞的染色。储存液用蒸馏水配成1mg/ml的浓度,使用终浓度一般为0.5 ~1mg/ml。结果评判:细胞凋亡过程中细胞核染色质的形态学改变分为三期:Ⅰ期的细胞核呈波纹状(rippled)或呈折缝样(creased),部分染色质出现浓缩状态;Ⅱa期细胞核的染色质高度凝聚、边缘化;Ⅱb期的细胞核裂解为碎块,产生凋亡小体(图1)。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376278_small.jpg3 透射电子显微镜观察结果评判:凋亡细胞体积变小,细胞质浓缩。凋亡Ⅰ期(pro-apoptosis nuclei)的细胞核内染色质高度盘绕,出现许多称为气穴现象(cavitations)的空泡结构(图2);Ⅱa期细胞核的染色质高度凝聚、边缘化;细胞凋亡的晚期,细胞核裂解为碎块,产生凋亡小体。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376295_small.jpg二、磷脂酰丝氨酸外翻分析(Annexin V法)磷脂酰丝氨酸(Phosphatidylserine, PS)正常位于细胞膜的内侧,但在细胞凋亡的早期,PS可从细胞膜的内侧翻转到细胞膜的表面,暴露在细胞外环境中(图3)。Annexin-V是一种分子量为35~36KD的Ca2+依赖性磷脂结合蛋白,能与PS高亲和力特异性结合。将Annexin-V进行荧光素(FITC、PE)或biotin标记,以标记了的Annexin-V作为荧光探针,利用流式细胞仪或荧光显微镜可检测细胞凋亡的发生。碘化丙啶(propidine iodide, PI)是一种核酸染料,它不能透过完整的细胞膜,但在凋亡中晚期的细胞和死细胞,PI能够透过细胞膜而使细胞核红染。因此将Annexin-V与PI匹配使用,就可以将凋亡早晚期的细胞以及死细胞区分开来。http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376296_small.jpg方法1. 悬浮细胞的染色:将正常培养和诱导凋亡的悬浮细胞(0.5~1×106)用PBS洗2次,加入100 ul Binding Buffer和FITC标记的Annexin-V(20ug/ml)10 ul,室温避光30 min,再加入PI(50 ug/ml)5 ul,避光反应5 min后,加入400 ul Binding Buffer,立即用FACScan进行流式细胞术定量检测(一般不超过1 h), 同时以不加AnnexinV-FITC及PI的一管作为阴性对照。2. 贴壁培养的细胞染色:先用0.25%的胰酶消化,洗涤、染色和分析同悬浮细胞。3. 爬片细胞染色:同上,最后用荧光显微镜和共聚焦激光扫描显微镜进行观察。结果 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376298_small.jpg http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376300_small.jpg
[font=宋体][font=宋体]在生物学和医学研究中,细胞增殖是一个关键过程,对于理解生命活动的基本规律以及疾病的发病机理具有重要意义。随着科技的发展,流式细胞仪作为一种高效、灵敏的分析工具,广泛应用于细胞增殖的检测。流式细胞仪通过快速分析单个细胞,可以对细胞周期、细胞增殖活性、细胞凋亡等多个方面进行研究。本文将探讨流式细胞仪在检测细胞增殖方面的主要方法,包括但不限于溴脱氧尿苷([/font][font=Calibri]BrdU[/font][font=宋体])掺入法、细胞周期蛋白检测法以及细胞大小分析法等,以期为读者提供全面的技术应用概览。流式细胞仪检测细胞增殖方法:[/font][/font][b][font=宋体][font=Calibri]1[/font][font=宋体]、[/font][font=Calibri]3H[/font][font=宋体](氚离子)掺入法[/font][/font][/b][font=宋体][font=宋体]原理:是在细胞[/font][font=Calibri]DNA[/font][font=宋体]合成时,用[/font][font=Calibri]3H[/font][font=宋体]脱氧胸腺嘧啶核苷代替普通的脱氧胸腺嘧啶核苷掺入新合成的[/font][font=Calibri]DNA[/font][font=宋体]中,增殖的细胞因为掺入[/font][font=Calibri]3H[/font][font=宋体]而具有放射性,通过定量检测样品细胞的放射性大小而反映细胞的增值活性[/font][/font][font=宋体][font=宋体]缺点:[/font][font=Calibri]1[/font][font=宋体])使用的是具有放射性的同位素,操作较为复杂,同时需要采取放射性保护措施 [/font][font=Calibri]2[/font][font=宋体])低比例高活跃增殖和高比例低活跃增殖可能得到的是相同的结果,用此方法无法进行鉴别 [/font][font=Calibri]3[/font][font=宋体])此方法无法进一步得到具有活性的增值细胞用于下一步的研究 [/font][font=Calibri]4[/font][font=宋体]) 此方法时间较短,无法检测加入前细胞的增殖情况,而且检测到放射性只能说明细胞[/font][font=Calibri]DNA[/font][font=宋体]合成,而不能提供合成[/font][font=Calibri]DNA[/font][font=宋体]的细胞是否进入增殖阶段的信息[/font][/font][b][font=宋体][font=Calibri]2[/font][font=宋体]、相对计数法[/font][/font][/b][font=宋体]原理:将对照组和各实验组控制在相同条件下直接计数然后比较计数结果得到增殖结论[/font][font=宋体]注意点:[/font][font=宋体][font=宋体]对照组与实验组每种细胞所加浓度必须相同,每组至少设置[/font][font=Calibri]3[/font][font=宋体]个复孔,这样每个孔可以得到[/font][font=Calibri]1[/font][font=宋体]个细胞数,将[/font][font=Calibri]3[/font][font=宋体]个复孔取平均值后就是这个组的结果。如果同时需要得到每孔目标细胞增殖后的绝对参数,在每孔细胞中加入[/font][font=Calibri]1*105PE[/font][font=宋体]标记的人工微球作为内参[/font][/font][font=宋体] [/font][font=宋体][font=宋体]收集各组的细胞于[/font][font=Calibri]EP[/font][font=宋体]管中,注意必须尽量将各组的所有细胞都收集起来。标记需要计数细胞的标志表型的荧光素偶联抗体,[/font][font=Calibri]4[/font][font=宋体]℃静置[/font][font=Calibri]30min[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]PBS[/font][font=宋体]洗涤一次,洗去游离的抗体[/font][/font][b][font=宋体][font=Calibri]3[/font][font=宋体]、示踪染料标记法[/font][/font][/b][font=宋体][font=宋体]示踪染料与细胞结合的方式:[/font][font=Calibri]1[/font][font=宋体])能够与细胞内的蛋白质上的氨基发生非特异性的共价结合 [/font][font=Calibri]2[/font][font=宋体])能够非特异性地嵌入细胞膜的脂质双分子层中与细胞发生非共价性结合[/font][/font][font=宋体] [/font][font=宋体][font=宋体]原理:示踪染料的荧光信号都很强,当细胞分裂时,母细胞内的染料会被平均分配到子细胞中,细胞荧光信号会被减弱一半,所以通过检测减弱的、发射示踪染料荧光信号的细胞比例就可以判断细胞增殖的强弱。当荧光强度减弱到标记时的[/font][font=Calibri]1/2[/font][font=宋体]以及以下的细胞都是增殖后的细胞,这些细胞所占比例越高则代表细胞增殖越活跃[/font][/font][font=宋体] [/font][font=宋体]标记方法:[/font][font=宋体][font=宋体]①纯化增殖反应的目标细胞,将细胞的浓度调整为[/font][font=Calibri]1*106/ml[/font][font=宋体],加入[/font][font=Calibri]CFSE[/font][font=宋体],其标记浓度为[/font][font=Calibri]5[/font][font=宋体]微摩尔[/font][font=Calibri]/[/font][font=宋体]升。置于[/font][font=Calibri]37[/font][font=宋体]℃水浴中标记[/font][font=Calibri]15min[/font][font=宋体],在标记过程中每隔一段时间混匀细胞一次[/font][/font][font=宋体] [/font][font=宋体][font=宋体]②加入预冷、含有血清的培养基终止标记,在[/font][font=Calibri]4[/font][font=宋体]℃冰箱中静置[/font][font=Calibri]5min[/font][font=宋体],离心沉淀[/font][/font][font=宋体] [/font][font=宋体][font=宋体]③用培养基再洗涤一次,尽量洗净未结合的游离的[/font][font=Calibri]CFSE[/font][font=宋体],然后将目标细胞静置在增殖体系中[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]4[/font][font=宋体]、[/font][font=Calibri]BrdU[/font][font=宋体]和[/font][font=Calibri]EdU[/font][font=宋体]掺入法[/font][/font][/b][font=宋体][font=Calibri]BrdU[/font][font=宋体]:[/font][font=Calibri]5-[/font][font=宋体]溴脱氧尿嘧啶核苷是胸腺嘧啶核苷的类似物,其特点是胸腺嘧啶环上[/font][font=Calibri]5[/font][font=宋体]位[/font][font=Calibri]C[/font][font=宋体]连接的甲基被溴取代,在细胞增殖[/font][font=Calibri]DNA[/font][font=宋体]合成时可以与内源性的胸腺嘧啶核苷竞争掺入到新合成的[/font][font=Calibri]DNA[/font][font=宋体]中,而[/font][font=Calibri]BrdU[/font][font=宋体]抗体可以特异性的识别[/font][font=Calibri]BrdU[/font][font=宋体],不与胸腺嘧啶核苷结合,所以可以用于检测细胞增殖[/font][/font][font=宋体][font=宋体]适用范围:适用于体内检测目标细胞的增殖,一般将[/font][font=Calibri]BrdU[/font][font=宋体]掺入小鼠的应用水中或经腹腔注射,经过一段时间后,取出目标细胞制成单细胞悬液然后用多聚甲醛固定细胞,后用打孔剂皂苷在细胞膜上打孔,最后标记荧光素偶联抗[/font][font=Calibri]BrdU[/font][font=宋体]抗体,目标细胞的[/font][font=Calibri]BrdU[/font][font=宋体]阳性细胞就是增殖的细胞,阳性比例越高,增殖越活跃。[/font][/font][font=宋体] [/font][b][font=宋体][font=Calibri]5[/font][font=宋体]、其他方法[/font][/font][/b][font=宋体][font=宋体]细胞周期法检测细胞增殖:流式细胞术能够检测细胞内[/font][font=Calibri]DNA[/font][font=宋体]的含量,所以可以检测细胞周期。处于[/font][font=Calibri]S[/font][font=宋体]期的细胞,[/font][font=Calibri]DNA[/font][font=宋体]的量处于二倍体和四倍体之间[/font][font=Calibri] [/font][font=宋体]处于[/font][font=Calibri]G2/M[/font][font=宋体]期时,[/font][font=Calibri]DNA[/font][font=宋体]量为四倍体。处于[/font][font=Calibri]S[/font][font=宋体]期和[/font][font=Calibri]G2/M[/font][font=宋体]期的细胞比例越高说明细胞增殖越活跃[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]PCNA[/font][font=宋体]检测细胞增殖:[/font][font=Calibri]PCNA[/font][font=宋体](增殖细胞核抗原),在细胞核合成且只存在于细胞核内,是[/font][font=Calibri]DNA[/font][font=宋体]聚合酶的辅助蛋白,所以与细胞[/font][font=Calibri]DNA[/font][font=宋体]的合成关系密切,是反映细胞增殖状态的良好指标[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]Ki-67[/font][font=宋体]检测细胞增殖:是一种与细胞增殖特异相关的核抗原[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]CD71[/font][font=宋体]检测细胞增殖:是转铁蛋白受体,表达于细胞的表面,该受体广泛表达于各种恶性肿瘤细胞表面,正常细胞表达较少,与肿瘤细胞的增殖密切相关[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/flow-cytometry-service][b]流式细胞检测技术服务[/b][/url],更多关于流式细胞仪检测细胞增殖详情欢迎咨询,详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/flow-cytometry-service[/font][/font][b][font=宋体] [/font][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
近日来自哈佛大学、麻省理工学院以及瑞士苏黎世联邦高等工业学院的研究人员在新研究中成功地将生物“计算机”诊断网络导入到人类细胞中,这种生物网络通过对5种肿瘤特异性分子进行逻辑组合分析识别出了特异的癌细胞,并触发了这些癌细胞的毁灭过程。这一研究成果在线发表在9月2日的《科学》(Science)杂志上。文章的通讯作者是哈佛大学系统生物学中心的生物工程学家Yaakov Benenson及麻省理工大学的Ron Weiss教授。Benenson长期致力于开发在活体细胞内运作的生物计算机。生物计算机是一种完全由DNA、RNA及蛋白质构成的分子自动机(molecular automata),它们的“输入”是细胞质中的RNA、蛋白质以及其他化学物质,“输出”的则是很容易辨别的分子信号。由于生物计算机能够探测和监控基因突变等细胞内一切活动的特征信息,因此它们可以确定癌细胞等病变细胞。此外,它们还能够自动激发微小剂量的治疗行为。利用这些“分子医生”将有望引发人类医学的重大变革——明确地对人体病变细胞或组织进行治疗,而健康的细胞完全不会受到干扰。不过,要最终实现这一目标,还有很长的路要走。科学家近期进行的一些相关研究,大都是尝试以不同方式开发具有多种用途的生物计算机。在这篇文章中,研究人员成功构建了一个多基因合成“电路”,此电路负责鉴别肿瘤细胞与正常细胞,进而靶向性摧毁识别的肿瘤细胞。其具体工作原理是:对细胞内5种肿瘤特异性分子及出现频率进行抽样及综合分析。是由当5种因子同时在细胞内出现时,该电路才做出正识别响应。这使得肿瘤检测的精确性大大增高。研究人员希望这一成果能为开发出特异的抗癌治疗奠定基础。随后科学家们用这一多基因合成网络对实验室中培养的两种人类细胞Hela细胞(一种子宫颈癌细胞)和正常细胞进行了检测。当遗传生物计算机被导入到这两种不同的细胞类型中时,只有Hela细胞被摧毁,而正常细胞则安然无恙。获得这一结果并非易事,研究人员为之投入了大量的基础工作。Benenson及同时首先针对正常健康细胞和Hela细胞中的miRNA分子进行了高通量筛查,最终确定了能将Hela细胞从健康细胞中鉴别出的5种特定的miRNA组合。“这些miRNA分子被导入到细胞中进行检测。新型的生物计算机利用诸如‘是’与‘非’的逻辑运算对这五种miRNA分子进行组合。只有当对所有分子的整体运算结果为逻辑‘真’时才会生成需要的结果——即促使细胞死亡,”Benenson说。目前研究人员已确定这一生物计算机网络在活细胞中能够非常稳定地工作,准确组合所有细胞内因子并生成正确答案,这代表着研究者们在该领域又向前迈进了重要的一步。 http://www.bioon.com/biology/UploadFiles/201109/2011090911135106.jpgdoi:10.1126/science.1205527 PMC:PMID:Multi-Input RNAi-Based Logic Circuit for Identification of Specific Cancer CellsZhen Xie, Liliana Wroblewska, Laura Prochazka, Ron Weiss, Yaakov BenensonEngineered biological systems that integrate multi-input sensing, sophisticated information processing, and precisely regulated actuation in living cells could be useful in a variety of applications. For example, anticancer therapies could be engineered to detect and respond to complex cellular conditions in individual cells with high specificity. Here, we show a scalable transcriptional/posttranscriptional synthetic regulatory circuit—a cell-type “classifier”—that senses expression levels of a customizable set of endogenous microRNAs and triggers a cellular response only if the expression levels match a predetermined profile of interest. We demonstrate that a HeLa cancer cell classifier selectively identifies HeLa cells and triggers apoptosis without affecting non-HeLa cell types. This approach also provides a general platform for programmed responses to other complex cell states.
http://gene.bjmu.edu.cn/news/ap1.gif 细胞凋亡与坏死是两种完全不同的细胞凋亡形式,根据死亡细胞在形态学、生物化学和分子生物学上的差别,可以将二者区别开来。细胞凋亡的检测方法有很多,下面介绍几种常用的测定方法。 一、细胞凋亡的形态学检测 根据凋亡细胞固有的形态特征,人们已经设计了许多不同的细胞凋亡形态学检测方法。 1 光学显微镜和倒置显微镜 (1) 未染色细胞:凋亡细胞的体积变小、变形,细胞膜完整但出现发泡现象,细胞凋亡晚期可见凋亡小体。 贴壁细胞出现皱缩、变圆、脱落。 (2) 染色细胞:常用姬姆萨染色、瑞氏染色等。凋亡细胞的染色质浓缩、边缘化,核膜裂解、染色质分割 成块状和凋亡小体等典型的凋亡形态。 2 荧光显微镜和共聚焦激光扫描显微镜 一般以细胞核染色质的形态学改变为指标来评判细胞凋亡的进展情况。 常用的DNA特异性染料有:HO 33342 (Hoechst 33342),HO 33258 (Hoechst 33258), DAPI。三种染料与 DNA的结合是非嵌入式的,主要结合在DNA的A-T碱基区。紫外光激发时发射明亮的蓝色荧光。 Hoechst是与DNA特异结合的活性染料,储存液用蒸馏水配成1mg/ml的浓度,使用时用PBS稀释成终浓度为2~5mg/ml。 DAPI为半通透性,用于常规固定细胞的染色。储存液用蒸馏水配成1mg/ml的浓度,使用终浓度一般为0.5 ~1mg/ml。 结果评判:细胞凋亡过程中细胞核染色质的形态学改变分为三期:Ⅰ期的细胞核呈波纹状(rippled)或呈折缝样(creased),部分染色质出现浓缩状态;Ⅱa期细胞核的染色质高度凝聚、边缘化;Ⅱb期的细胞核裂解为碎块,产生凋亡小体(图1)。 3 透射电子显微镜观察 结果评判:凋亡细胞体积变小,细胞质浓缩。凋亡Ⅰ期(pro-apoptosis nuclei)的细胞核内染色质高度盘绕,出现许多称为气穴现象(cavitations)的空泡结构(图2);Ⅱa期细胞核的染色质高度凝聚、边缘化;细胞凋亡的晚期,细胞核裂解为碎块,产生凋亡小体。
人神经干细胞染色体是否有异常的检测的检测方法微生物检测,还是诺禾测序方法,那种比较好呢?
发酵过程中,细胞浓度是一个非常重要的生理参数,不但可以计算比生长速率,底物消耗速率、生物量产率和维持系数等参数,还可以及时判断是否有染菌等异常情况发生。目前测量细胞浓度的方法主要有化学法(DNA/RNA分析)和物理法(干重、光密度、呼吸商等)两大类。一般来说,与物理法相比,化学法能较准确的测量有代谢活性的生物量,缺点是花费时间长,而利用物理法测量,无法区分区分处于悬浮状态的颗粒和微生物,也无法分别活死细胞。 实现在线活细胞浓度一直是发酵领域的热门话题,仅些年来出现了不少的测量方法,依据的工作原理也是五花八门,其中最具代表性的有声学,激光散色、荧光、核磁、量热或电容。 其中法国fogale公司的测量仪器,以电容法为工作原理,直接将传感器安装与发酵罐上,可承受121℃高温灭菌,理论技术也比较成熟,是目前最为理想的适合工业级别的在线活细胞传感器。工作原理:电容传感器采用活细胞的介电特性,实时连续测量活细胞的生物体积,可应用于实验室桌面型的反应器或者是工业规模的大型反应器两对对电极位于传感器的顶部,一对用于在培养基中产生交变的电场,在电场范围内,带有完整细胞膜的细胞会在培养基中发生极化现象,发生极化的细胞可以认为是极小的电容,死细胞或者其他粒子没有完整的细胞膜,所以不能形成电容型号。另一对电极用于检测培养基中的介电信号,培养基中的介电信号和细胞的浓度是精确关联的。细胞的极化率和电场的频率纯在函数关系,当频率增加时,培养基中细胞的介电常数由低频峰(最大极化)降低到高频峰(最小极化)。这种随频率增加极化率降低的现象称为β-散射。传感器采用双频测量模式:培养基的基线在10MHz左右得到,细胞的信号在临界频率区域获得,在曲线的拐点,(动物细胞和细菌在1MHz,酵母在2MHz)我们获得了最佳的信号线性。应用:这项技术可广泛应用于各种细胞培养,生物发酵过程。已被文献证实可应用的细胞如下:动物细胞:CHO, BHK, MDCK, PERC6, NSO, HEK, Hela,Hybridoma, Vero细 菌:E.Coli, Bacillus Thuringensis, Salmonella,Streptomyces, Lactic Bacteria酵 母:Pichia Pastoris, Saccharomyces Cervisiae, PolymorphaHasenula昆虫细胞:sf9, Hi-5真 菌:Absidia
流式细胞仪可以检测哪些细胞
[b][font=宋体][font=宋体]细胞周期[/font][font=Calibri]cell cycle [/font][/font][/b][font=宋体]是指从一次细胞分裂形成子细胞开始到下一次细胞分裂形成子细胞为止所经历的过程,它反映了细胞增殖的速度。在临床上,有很多研究证明,细胞周期分析对人肿瘤的诊断预后具有很高的价值。[/font][font=宋体] [/font][font=宋体][font=宋体]一个完整的细胞周期包含间期和分裂期([/font][font=Calibri]M[/font][font=宋体]期)两个阶段,间期又分为[/font][font=Calibri]DNA[/font][font=宋体]合成前期([/font][font=Calibri]G1[/font][font=宋体]期)、[/font][font=Calibri]DNA[/font][font=宋体]合成期([/font][font=Calibri]S[/font][font=宋体]期)和[/font][font=Calibri]DNA[/font][font=宋体]合成后期([/font][font=Calibri]G2[/font][font=宋体]期),处于不同时期的细胞的[/font][font=Calibri]DNA [/font][font=宋体]含量存在差异。一般认为,[/font][font=Calibri]G 1 [/font][font=宋体]期细胞具有增殖活性,参与细胞周期循环,是二倍体细胞;[/font][font=Calibri]S [/font][font=宋体]期细胞,[/font][font=Calibri]DNA [/font][font=宋体]含量逐渐增加,从二倍体变成四倍体,随后进入 [/font][font=Calibri]G 2 [/font][font=宋体]期,最终进入 [/font][font=Calibri]M [/font][font=宋体]期。检测细胞周期常用的方法是检测[/font][font=Calibri]DNA[/font][font=宋体]含量,可以选择能与[/font][font=Calibri]DNA[/font][font=宋体]结合的荧光染料(如[/font][font=Calibri]PI[/font][font=宋体]等),再根据细胞各个时期[/font][font=Calibri]DNA[/font][font=宋体]含量不同从而荧光强度不同的方法,分析各个阶段的细胞比例。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体][font=宋体]流式细胞仪[/font][font=Calibri]PI[/font][font=宋体]染色法检测细胞周期的原理[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]由于细胞周期各时相的[/font][font=Calibri]DNA[/font][font=宋体]不同[/font][font=Calibri],[/font][font=宋体]通常正常细胞的[/font][font=Calibri]G1/G0[/font][font=宋体]期具有二倍体细胞的[/font][font=Calibri]DNA[/font][font=宋体]含量[/font][font=Calibri](2N),[/font][font=宋体]而[/font][font=Calibri]G2/M[/font][font=宋体]期具有四倍体细胞[/font][font=Calibri]DNA[/font][font=宋体]含量[/font][font=Calibri](4N),[/font][font=宋体]而[/font][font=Calibri]S[/font][font=宋体]期的[/font][font=Calibri]DNA [/font][font=宋体]含量介于二倍体和四倍体之间。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]PI[/font][font=宋体](碘化丙啶)为插入性核酸荧光染料,能选择性嵌入核酸[/font][font=Calibri]DNA[/font][font=宋体]和[/font][font=Calibri]RNA[/font][font=宋体]双螺旋的碱基之间与之结合,结合量与[/font][font=Calibri]DNA[/font][font=宋体]的含量成正比关系,其荧光强度直接能反映细胞内[/font][font=Calibri]DNA[/font][font=宋体]含量。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]因此[/font][font=Calibri],[/font][font=宋体]通过流式细胞仪[/font][font=Calibri]PI[/font][font=宋体]染色法对细胞内[/font][font=Calibri]DNA[/font][font=宋体]含量进行检测时[/font][font=Calibri],[/font][font=宋体]可以将细胞周期各时相区分为[/font][font=Calibri]G1/G0 [/font][font=宋体]期[/font][font=Calibri],S [/font][font=宋体]期和[/font][font=Calibri]G2/M [/font][font=宋体]期[/font][font=Calibri],[/font][font=宋体]获得的流式直方图对应的各细胞周期可通过特殊软件计算各时相的细胞百分率。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]通过定量测定[/font] [font=Calibri]DNA [/font][font=宋体]含量来分析细胞周期是流式细胞术最早的应用之一。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]流式细胞周期([/font][font=Calibri]cell cycle[/font][font=宋体])检测结果分析常用的流式细胞术分析细胞周期的方法是依据细胞[/font][font=Calibri]DNA[/font][font=宋体]含量(横坐标)来分析的:[/font][font=Calibri]G0[/font][font=宋体]期:静止期,有丝分裂完成后,脱离细胞周期暂时停止分裂的一个阶段,胞内[/font][font=Calibri]DNA[/font][font=宋体]含量保持二倍体;[/font][font=Calibri]G1[/font][font=宋体]期:[/font][font=Calibri]DNA[/font][font=宋体]合成前期,从有丝分裂到[/font][font=Calibri]DNA[/font][font=宋体]复制前的一段时期,此期主要合成[/font][font=Calibri]RNA[/font][font=宋体]和核糖体,胞内[/font][font=Calibri]DNA[/font][font=宋体]含量保持二倍体;[/font][font=Calibri]S[/font][font=宋体]期:[/font][font=Calibri]DNA[/font][font=宋体]合成期,在此期,合成[/font][font=Calibri]DNA[/font][font=宋体]及组蛋白,胞内[/font][font=Calibri]DNA[/font][font=宋体]含量介于[/font][font=Calibri]G1[/font][font=宋体]期与[/font][font=Calibri]G2[/font][font=宋体]期之间;[/font][font=Calibri]G2[/font][font=宋体]期:[/font][font=Calibri]DNA[/font][font=宋体]合成后期,是有丝分裂的准备期,合成[/font][font=Calibri]RNA[/font][font=宋体]及蛋白质,[/font][font=Calibri]DNA[/font][font=宋体]合成终止,胞内[/font][font=Calibri]DNA[/font][font=宋体]含量为四倍体;[/font][font=Calibri]M[/font][font=宋体]期:细胞分裂期,胞内[/font][font=Calibri]DNA[/font][font=宋体]含量为四倍体;[/font][/font][font=宋体] [/font][b][font=宋体]流式细胞检测正常范围[/font][/b][font=宋体]流式细胞检测的正常范围通常依赖于被检测细胞或生物粒子的类型以及所测参数的性质。一般而言,正常的细胞数量、细胞大小、细胞形态、细胞内物质的浓度和分布等参数都在一定的范围内。这些正常范围通常是通过对比大量健康个体或样本的流式细胞检测结果而得出的。例如,正常血细胞的计数和比例,各种免疫细胞的分布,以及细胞内的荧光强度等,都有相应的正常范围。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/flow-cytometry-service][b]流式细胞检测技术服务[/b][/url],同时还提供完善的[url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]流式单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]细胞分选平台[/b][/url],详情关注:[/font][font=Calibri]https://cn.sinobiological.com/services/flow-cytometry-service[/font][/font][font=宋体][font=Calibri]https://cn.sinobiological.com/services/platform/facs-b-cell-sorting[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
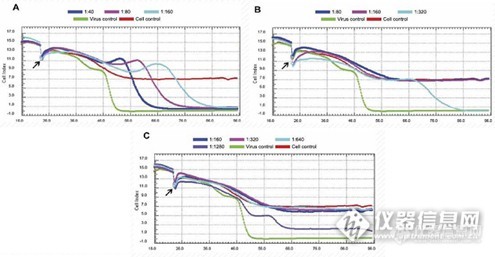
【线上讲座233期】实时细胞分析技术在肿瘤研究和病毒抗体疫苗检测中的应用 主讲人:周尧 活动时间:2013年10月9日-10月19日 热烈欢迎 周尧 老师光临生命科学仪器版面进行讲座!http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647975_2685866_3.gif引言实时无标记细胞分析技术(RTCA, Real Time cell Analysis)是艾森生物全球独有的专利核心技术,该技术采用特殊工艺,将微电极列阵整合在细胞培养板的每个细胞生长孔底部,用以构建实时、动态、定量跟踪细胞形态和增殖分化改变的细胞阻抗检测传感系统。该技术可广泛应用于生物活性因子测定、细胞增殖检测、大规模抗肿瘤药物筛选、细胞毒性检测等研究。http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647975_2685866_3.gif提要一、 实时细胞分析技术原理 1.传统终点检测与实时无标记动态检测 2. 实时细胞分析技术原理 3. 实时细胞分析技术优势二、 实时细胞分析技术平台产品简介三、 实时细胞分析技术在肿瘤、药物细胞毒性检测领域的应用 1.RTCA实时动态细胞毒性检测 2.肿瘤与微环境之间的相互作用RTCA实时动态检测 四、 实时细胞分析技术在病毒、细胞毒素、中和抗体及疫苗检测与评估领域的应用 1.RTCA实时动态检测病毒Cytopathic Eff ect效应 2.RTCA实时定量检测病毒侵染效力及评估中和抗体效价http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647975_2685866_3.gif提问时间:2013年10月09日--10月19日答疑时间: 2013年10月09日--10月19日特邀佳宾:生命科学仪器版面版主、专家以及同行们参与人员:仪器论坛全体注册用户活动细则:1、请大家就ATR技术知识的相关问题进行提问,直接回复本帖子即可,自即日起提问截至日期2013年10月19日2、凡积极参与且有自己的观点或言论的都有积分奖励(1-50分不等),提问的也有奖励在活动期间我们将评选出20名积极参与奖和5名精彩问答奖。3、提问格式:为了规范大家的提问格式,请按下面的规则来提问 :周尧老师您好!我有以下问题想请教,http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647975_2685866_3.gif说明:本讲座内容仅用于个人学习,请勿用于商业用途,由此引发的法律纠纷本人概不负责。虽然讲座的内容主要是对知识与经验的讲解、整理和总结,但是也凝聚着笔者大量心血,版权归tianzhen老师和仪器信息网所有。本讲座是根据笔者对资料的理解写的,理解片面、错误之处肯定是有,欢迎大家指正。http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_647975_2685866_3.gif
原标题 “纳米生物间谍”技术能进入活细胞取样 可用于深入揭示线粒体基因组变异的重要性 科技日报讯 据物理学家组织网近日报道,美国加利福尼亚大学圣克鲁兹分校(UCSC)研究人员开发出一种机器人式的“纳米生物间谍”系统,能从单个活细胞内提取出微量样本,进行RNA或DNA测序,而不会杀死细胞。研究人员表示,这种单细胞“纳米生物间谍”技术是一种了解活细胞内部动态过程的有力工具。相关论文发表在最近出版的美国化学协会《纳米》杂志上。 “我们能从活细胞中拿走一个‘生物间谍’,再把它送回该细胞,在几天内这样重复多次而不会杀死细胞。如果用其他技术,你不得不牺牲这个细胞才能分析它。”该生物传感与生物电技术小组负责人、UCSC巴斯金工程学院生物分子工程教授内德·波曼德说。 “纳米生物间谍”平台是研究小组用纳米吸液管开发的最新设备。纳米吸液管是一种小玻璃管,取液端越来越细,至尖端直径仅50到100纳米。波曼德说:“我能在实验室造出纳米吸液管,这不需要昂贵的纳米制造设备。但要进入一个细胞,问题是即使在高倍显微镜下,你也看不见吸液管尖端,不知道它偏离了细胞有多远。” 实验室博士后研究员亚当·赛格尔解决了这一问题。他基于在一台改造过的扫描离子电导显微镜(SICM),开发出一种反馈控制系统。该系统能利用通过纳米吸液管尖端的离子流作为反馈信号,在尖端接近细胞表面时探测其中的液滴。在尖端进入细胞之前,一种自动控制系统能定位它在细胞上面的位置,然后尖端很快插入穿透细胞膜,通过操控电压有控制地提取一小点细胞内物质。由于吸液管尖端极精细,对细胞造成的损害极微小。 研究小组用这种系统从活细胞中提取的微量细胞物质,估计只有50毫微微升(千万亿分之一升),约一个人体细胞百分之一的量。他们从单个人体癌细胞中提取物质并进行RNA测序,还从人类成纤维细胞中提取了线粒体并对其进行了DNA测序。“人们已经知道,线粒体和多种神经退化疾病有关。该技术可用于深入揭示线粒体基因组变异的重要性。”波曼德说。 该技术应用前景广阔。波曼德希望能与其他研究人员合作,探索其更多用途。“对于癌症生物学家、干细胞生物学家等想要了解细胞内部情况的科学家来说,这是一种多功能的平台。”(常丽君)来源:中国科技网-科技日报 2014年01月20日
[align=center][font='calibri'][size=13px]生乳体细胞检测[/size][/font][/align]1、 [size=18px]生乳体细胞检测目的及意义[/size][size=18px]体细胞数的英文是Somatic Cell Count , 缩写为SCC是指出现在正常牛奶中少量的动物身体细胞。以每毫升牛奶中的体细胞数表示,通常以千个计数。体细胞( scc ) 的组成,白细胞 (即巨噬细胞、嗜中性白细胞和淋巴细胞)和上皮细胞。[/size][size=18px]体细胞(SCC)越低牛奶质量越高SCC越高对原奶质量的影响越大,并对牛奶的保质期和乳制品如酸奶、奶酪等的产量、质量、风味等产生极大的不利影响。因此各国都将体细胞数作为牛奶质量标准中最重要的指标之一。[/size]2、 [size=18px]检测原理[/size][size=18px]采用荧光染色自动镜检原理,染色剂外无需额外的化学试剂;干粉式染色剂无需要样品稀释液。排除液体染色剂挥发的影响;体细胞检测范围1-1000万,建议有效计数范围为5万以上。[/size]3、 [size=18px]操作过程[/size][align=left][size=18px]第一步:充分搅拌后在取样瓶中用 100ul 的[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]抽取 [/size][size=18px]100ul [/size][size=18px]奶[/size][size=18px],[/size][size=18px]加入到染色瓶中;第二步:把加入奶样后的染色剂瓶放置在搅拌器上,按 2 秒,松 [/size][size=18px]2 [/size][size=18px]秒,共搅拌 [/size][size=18px]10 [/size][size=18px]次, 静止 [/size][size=18px]2 [/size][size=18px]分钟让它充分染色,然后再放在搅拌器上按压搅拌 [/size][size=18px]3 [/size][size=18px]次。第三步:打开盖子,用另外一个[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]取样出 8ul 奶样在检测板半圆孔处缓慢排出,无需排气, 让样品慢慢渗过去,然后静置 [/size][size=18px]30 [/size][size=18px]秒,直至对面直线处充满样品。[/size][/align][align=left]4、 [size=18px]注意事项[/size][/align][align=left][size=18px]1、开机时,先接电源,打开机器,最后开平板,避免第二步自检不成功[/size][/align][align=left][size=18px]2、在进行检测时,若点击按钮没有反应,则机器可能进入了仿真模式,若出现 [/size][/align][align=left][size=18px]这种情况,可返回自检界面,调整箭头所指模式即可。[/size][/align][align=left]3、 [size=18px]仪器使用较长时间后,会出现卡顿现象,这种情况下可以清除以往检测数据,点击参数选项,进入页面。[/size][/align][align=left][size=18px]4、仪器使用时,请勿在平板上下载游戏,视频等占内存的软件,避免出现卡顿现象。 [/size][/align][align=left][size=18px]5[/size][size=18px]、仪器使用结束后,关机时请先关闭平板,再关闭机器,最后拔下电源。[/size][/align]
目前血细胞分析仪检测原理包括电学和光学两种,电学包括电阻抗法和射频电导法,光法包括激光散射法和分光光度法。电阻抗法根据Coulter原理及血细胞非传导的性质,以电解质溶液中悬浮的血细胞在通过计数小孔时引起的电阻变化进行检测为基础,进行血细胞计数和体积测定。当有细胞通过小孔时,由于电阻增加,于瞬间引起电压变化及通过脉冲。细胞体积越大,脉冲振幅越高,细胞数量越多,脉冲数量也越多。脉冲信号经过:放大、阈值调节、甄别、整形、计数而得出细胞技术结果。电阻抗法可准确量出细胞(或类似颗粒)的大小,是三分类血液分析仪的主要应用原理,并与光学检测原理组合应用于五分类血液分析仪中。激光散射法应用了流式细胞术检测原理及细胞通过激光束被照射时,产生与细胞特征相应的各种角度的散射光。对经信号检测器接受的散射光信息进行综合分析,即可准确区分正常类型的细胞。激光散射法在区别体积相同而类型不同的细胞特征时,比电阻抗法分群更加准确。故激光散射法已成为现代五分类血液分析仪的主要检测原理之一。射频电导法是用高频电磁探针渗入细胞膜脂质可测定细胞的导电性,提供细胞内部化学成分、细胞核和细胞质、颗粒成分等特征信息。射频电流是每秒变化大于10000次的高频交流电磁波,能够通过细胞壁。分光光度法是所有类型的血细胞分析仪检测血红蛋白的原理,它利用血红蛋白与溶血剂在特定波长下比色,吸光度的变化与液体中血红蛋白含量成比例。
生物质谱技术在细胞生物学中的应用桑志红 王红霞 综述 概 论 蛋白分离与显色 蛋白质鉴定 数据库查寻 灵敏度 具体示例 展望未来(相关文献)摘 要 基因组计划的飞速发展使我们提早进入"后基因组时代",而质谱技术的重要进展使得通过酶解、质量分析、序列分析及其数据库检索对蛋白质进行高通量快速鉴定的技术方法应运而生,并成为"后基因组时代"的关键核心技术。这种技术的应用范围已经从细胞,组织以及整个有机体中蛋白质的表达到蛋白质翻译后修饰等等方面。本文简要综述生物质谱技术在细胞生物学等学科中的应用。 过去的十年经历并见证了生命科学革命性的变化. 大规模基因组测序技术的问世使人类基因组计划最终目标的实现比预期一再提前。与此同时,近几年间已有10余种模式生物的基因组序列测定告罄,3年内还将有40种左右生物的基因组全序列问世。因此大多数人同意我们现在已经提早进入"后基因组时代"(post-genome era), 目前我们所面临的挑战是如何破解基因组计划已获得的大量序列信息并加以应用。这个问题的关键是基因的生物学功能不能只通过对核酸一级结构(序列)的检测来确定。研判一个未知基因的功能、与其他基因产物及其亚细胞结构之间的功能联系, 最终都必须通过在蛋白水平对基因产物的研究才能确定。蛋白质组这个名词是近几年才提出来的,它用来描述一个细胞的全部蛋白质,而在蛋白水平上进行大规模的研究引出了新的术语蛋白质组学。蛋白质表达图谱是依靠蛋白质显示技术和精确定量技术对细胞或组织中蛋白质表达总况进行比较(2), 这个领域最近已有综述(11)。细胞图谱蛋白质组学是指应用生物质谱技术鉴定蛋白质及其相互作用并确定在亚细胞中的定位。本文的目的是 简要综述生物质谱技术在细胞生物学领域中越来越多的应用,并为该领域正考虑应用这种技术的研究者提供一些的有用的信息。 作为一个新的研究领域,蛋白质组学发展的关键是近年来质谱技术的革新。这种革新极大地促进了质谱技术在生命科学研究中的应用。质谱现在可以作为将各种蛋白质与序列数据库联系起来的桥梁。生物质谱根据质量数和所载电荷数不同的多肽片断在磁场中产生不同轨道而以质荷比(m/z)方式来分离它们。80年代末,随着两种崭新的尤其适合蛋白质研究的软电离方式ESI(电喷雾电离)和MALDI(基质辅助激光解吸附电离)的出现,质谱成为现代蛋白质科学中最重要和不可缺少的组成部分。 生物质谱最强大的应用功能之一是能够鉴定蛋白质复合物的组成成分(19)。细胞中一些最重要的生命过程都是通过多蛋白质复合体来执行和调节的,但由于蛋白质鉴定的困难,大多数上述蛋白复合体都是未知的。生物质谱灵敏度的不断提高显著地促进了对具有生物学功能和治疗潜力的蛋白复合体的鉴定,例如,NF-k B信号通路,CD95(FAS/APO-1)介导的细胞死亡途径,和核受体介导的转录信号传导过程中形成的蛋白复合体。在某些情况下,复合物可通过常规蛋白纯化的方法进行纯化,如剪接体复合(25),酵母纺锤体复合物(29)及VHL肿瘤抑制复合物(18)。然而,更常见的是,复合物中的组成成分通过一步免疫沉淀或免疫亲和步骤后就可纯化,这种方法甚至可以用于鉴定那些用常规蛋白纯化和鉴定技术所不及的一些过渡态或不稳定的复合物。因为生物质谱技术的介入,现在已经不再需要通过抗体进行免疫印迹实验,而是通过生物质谱技术对免疫沉淀获得的蛋白复合体组分直接进行蛋白序列分析。以酵母P24复合物鉴定为例,应用上游表位标签策略有可能不需制备抗目标蛋白的抗体就能对蛋白质复合物进行鉴定(13)。这种方法(36)对于基因组序列已完全清楚和遗传稳定的生物(如芽殖酵母,啤酒酵母)尤为简便, 例如对RENT复合物和促有丝分裂后期复合物(49)。因为这种方法的成功应用,使人们对上游表位标签策略-蛋白纯化-生物质谱分析的方法兴趣倍增。值得一提的是,将能被特殊蛋白酶切除的连接子(接头)掺入表位标签是尤为有利的(如下所述)。 上述方法是通过识别蛋白复合物中相互作用和配对的各组分而达到对蛋白鉴定的目的,另一种策略则是通过对分离纯化的细胞器蛋白组成进行鉴定而在亚细胞水平对蛋白质定位. 用这种方法确定蛋白质位置, 对评价蛋白质潜在的功能将是大有帮助的. 应用这种方法,我们称为细胞器蛋白质组学, 已经发现正常工作状态下的细胞器含有比我们以前所知道的数量多得多的蛋白种类。然而实际上,由于质谱极高的分辨率和灵敏度,纯化后的细胞器组分即使只有微量的混杂,也能被质谱分辨并误认为是细胞器的组成部分。因此,如何充分的纯化以保证至少绝大多数被鉴定的蛋白质都来自同一种细胞器,成为制约上述工作的瓶颈。 蛋白质翻译后修饰也是蛋白鉴定工作中的一个重要方面。根据DNA序列信息并不能可靠预测或推导出蛋白质翻译后的修饰。而质谱技术已经被证明对研究蛋白质翻译后的修饰(例如磷酸化和糖基化)是极为有用的,特别是对序列已知的蛋白的鉴定。例如:Betts等人(1a)用这种方法成功地鉴定了从小鼠大脑中分离的神经纤维蛋白体内磷酸化位点。同样方法, Wong等人(45)确定了钙联蛋白质(calnexin)C未端的磷酸化位点。在糖基化的例子中, Carr等人(5)采用液相色谱与质谱联用技术选择性地鉴定了糖蛋白中N- 和O-联接的寡糖. 稍后, 本文将会通过对E-选择素中糖基化位点的鉴定来进一步说明这种方法.
非特异性的硅珠黏附细胞法检测宫颈癌美国克拉克森大学纳米工程和生物技术实验室中心Igor Sokolov课题组开发出一种新的宫颈癌检测方法——非特异性的硅珠黏附细胞法(nonspecific adhesion of silica beads to cells)。这篇研究报告发表在Small杂志上。这项研究是基于课题组之前发表在Nature Nanotechnology杂志的研究报告,他们观察到,正常的和发生癌变的宫颈上皮细胞表面存在着某些之前未发现的差异。在这项研究中,研究人员将硅珠连接到原子力显微镜(atomic force microscopy,AFM)的旋臂上,从而使硅珠黏附在细胞表面,硅珠和细胞分离所需的的黏附力的大小可以通过测量得到。黏附能力越高的细胞表面黏住的硅珠越多。根据细胞表面的荧光硅珠粒子的数目以及荧光的亮度轻易区别出癌细胞和正常细胞。试验中所使用的超亮的荧光硅珠(ultrabright fluorescent silica particles)也是Sokolov课题组开发出来的。(
作者:丁香园网友Docofsoul《每日科学》2011年9月1日报道——由瑞士联邦理工学院(ETH)Yaakov Benenson教授与麻省理工Ron Weiss教授率领的研究小组成功地将生物“计算机”诊断网络导入人类细胞。该网络有识别某些肿瘤细胞的能力,利用五种肿瘤特异性分子因子的逻辑组合,进而触发肿瘤细胞毁灭过程。http://img1.jiansuo.net/cms/upload/userfiles/image/2011/09/04/1315042501_small.jpg细胞微机布线图:所有五种因子必须处于相应的正确状态,由此触发细胞死亡(图片来源:y Benenson Y. 教授 R. Weis教授)开发活体细胞内运作的生物电脑,是ETH苏黎世分院合成生物学教授Yaakov (Kobi) Benenson孜孜以求的目标,其职业生涯的大部分时间都倾注于此。他想建立既能侦测细胞生存状况、又能在细胞异常时对相应信息进行处理以提供合适的治疗响应的生物微机。目前,通过与麻省理工教授Ron Weiss以及团队成员(包括博士后学者Zhen Xie 与 Liliana Wroblewska、博士生Laura Prochazka)合作,他向这一目标迈出了重大一步。这一研究成果已发表于《Science》(见本文所附参考文献),论文介绍了一种多基因合成“电路”;此电路负责鉴别正常细胞与肿瘤细胞、继而进一步摧毁肿瘤细胞。其工作方式是:对细胞内五种肿瘤特异性分子因子及其出现频率进行抽样与综合;只有当所有这些因子在细胞内同时出现时,该电路才会作出正识别响应。这种方式使得侦测肿瘤的准确率非常高。研究者希望这一成果能够为高特异性抗癌治疗奠定基础。对肿瘤细胞的选择性破坏本研究对实验室培养的两种类型人类细胞进行了基因网络测试:海拉细胞(子宫颈癌细胞)与正常细胞。当基因生物微机被导入这两种不同的细胞类型时,只有海拉细胞被摧毁,而正常细胞则安然无恙。当然,取得这一结果需要做大量的基础工作。首先必须找出海拉细胞特有的分子组合。Benenson及其他小组成员在属于小RNA分子(MicroRNA或miRNA)这一类化合物的分子中找,终于确认其中一个miRNA组合(或者说“可识别属性”)只有海拉细胞才有,其它健康细胞类型内则不存在。发现这种可识别属性是一项颇具挑战性的任务。人体内既存在250种不同的健康细胞类型,此外也存在为数众多的肿瘤细胞的变异型(其中数百种可作实验室培养)。但miRNA多样性则更是不让须眉花样繁多,人类细胞中已得以描述的即达500到1000不同种类。Benenson指出:“每种健康或病损细胞类型都有其不同的miRNA分子处于开放或关闭状态。”可识别肿瘤属性中的五种因子确立一种miRNA“可识别属性”与发现一组症状以可靠诊断一种疾病有所不同。教授说:“一种症状,比如说发热吧,不可能由此概括出一种疾病。医生获得的信息越多,其诊断才越可靠。” 一年半前他从哈佛大学到ETH后,研究小组找到了几种因子,可由此可靠地将海拉细胞从所有其它健康细胞中鉴别出;结果表明,仅仅五种特定miRNA的组合(其中某些以高水平出现,某些则以极低水平出现)就足以将海拉细胞从其混迹的健康细胞中揪出来。与微机运作相似的网络Benenson介绍说:“这些miRNA因子在细胞内进行逻辑代数运算;该生物微机运用诸如‘与’与‘非’等逻辑操作将这些因子进行组合,并且,当全部因子的整体运算结果为逻辑‘真’值时,只产生所需要的结果——那就是细胞死亡。” 确实,研究者已经能够显示该网络在活体细胞内可以非常稳定地运作,可正确组合所有细胞内因子并给出正确的诊断。Benenson认为,这一成果代表该领域的一项重大成就。动物模型与基因疗法该研究小组想在下一步在合适的动物模型上测试该细胞计算方法,以期在未来创建诊断与治疗工具。这听起来可能象科幻小说,但Benenson相信其可行性;不过,仍有不少棘手的问题需要解决。比如,如何有效、安全地将外源基因导入细胞?这种DNA递送在目前情况下颇具挑战性。尤其是,该方法需要将外源基因暂时而不是永久导入细胞。现有的病毒导入法或化学导入法均未充分开发,需要进一步完善。Benenson说:“为人类提供一种功能完善的治疗方法还非常遥远。不过这一工作是重要的第一步,显示了单一细胞水平上这样一种选择性诊断方法具有可行性。”参考文献:1. Z. Xie, L. Wroblewska, L. Prochazka, R. Weiss, Y. Benenson. Multi-Input RNAi-Based Logic Circuit for Identification of Specific Cancer Cells. Science, 2011; 333 (6047): 1307 DOI: 10.1126/science.1205527
[em03] [em03] [em04] [em04] [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=52163]流式细胞仪检测凋亡2[/url]把一 二放在一个文件夹下然后打开就行!!!
大神们,帮忙推荐台主要针对小鼠骨髓细胞数检测的仪器,再一个就是能对小鼠血细胞的种类分类,计数。要求不高。。但是这种针对性的仪器还这难找。。
将在药物开发进程中发挥重要作用2011年03月26日 来源: 科技日报 作者: 常丽君 本报讯 据每日科学网近日报道,美国范德堡大学研究人员开发出一种新型激光技术,可检测细胞膜上的蛋白质和其它多种生物分子之间的相互反应。这种检测将在药物开发进程中发挥重要作用。 人类细胞中约有7000种蛋白质,其中30%在细胞膜上,控制细胞分子运作机制的信号有60%—70%由这些膜蛋白产生,因此当前市场上约一半的药物都是瞄准细胞膜蛋白。但因为膜蛋白很难提纯,科学家在研究它们的结构时面临很多困难。现有的检测膜手段大多是将膜蛋白从其所处环境中分离,或用不同方式如荧光标签加以修改,以分析它们的活性。这些方法不仅昂贵耗时,还可能会影响目标膜蛋白的功能。 范德堡大学化学生物研究院化学教授达里尔·波恩霍普领导的研究小组和斯克里普斯研究院合作,开发了一种名为“后向散射干涉仪”(BSI)的新型激光技术,能精确检测出膜蛋白和自然界中各种分子之间的结合力。 BSI操作起来很简单,只要把两种分子混合装入一个充满液体的显微镜小盒中,用一束类似于条形码扫描仪的红色激光照射,就能测出它们之间的结合力。小盒的几何形状调整合适后,激光就会产生干涉图案,而这种干涉图案对分子之间的反应非常敏感。如果分子开始互相作用,图案就开始变换。 为了检验BSI的准确性,研究人员制造了一种含有GM1小蛋白质的合成膜,霍乱毒素要进入细胞,主要结合对象就是这种小蛋白质。他们把霍乱毒素B和这些膜混合,检测出的结合力结果与用其他方法所得到的结果一致。为了进一步确认,他们还用了一种和胸腺癌相关的天然分离膜和3种分别与疼痛、发炎和神经传导素GABA(用于放松、睡眠和调节紧张)相关的蛋白质膜进行检验,把包含这些蛋白质的膜和对应结合分子相混合,用BSI技术测得的值也和用其他方法得到的结果一样。 此外,该技术进入商业化也前景广阔,范德堡大学对新型激光检测技术已申请了专利,并已获得3项批准。他们还专门成立了一家分子传感公司对新技术进行独家开发。
[font=宋体]流式细胞分析是一种在生物学和医学领域广泛应用的实验技术,它可以实现对细胞群体的快速、准确分析和分类。本文将详细介绍流式细胞分析的步骤和流式免疫检测的应用,帮助读者全面了解这一技术的原理、方法和应用。[/font][font=宋体] [/font][b][font=宋体][font=宋体]流式细胞分析方案主要分为[/font][font=Calibri]4[/font][font=宋体]个步骤: [/font][/font][/b][font=宋体] [/font][font=宋体]①样品制备:应通过机械分离方法或化学解离技术制备单细胞悬液,如采用酶溶液或钙螯合试剂。[/font][font=宋体] [/font][font=宋体][font=宋体]②封闭:通常采用抗[/font][font=Calibri]Fc[/font][font=宋体]抗体稀释液悬浮细胞,防止一抗非特异性结合。[/font][/font][font=宋体] [/font][font=宋体]③抗体孵育:流式细胞分析的孵育步骤涉及多种组分,包括一抗、二抗、链霉亲和素和荧光染料。[/font][font=宋体] [/font][font=宋体]④流式细胞仪检测:将处理后的细胞通过流式细胞仪进行检测和分析,获取细胞的各项指标数据。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]适当的对照[/b][/font][font=宋体]除了目标细胞之外,每次进行流式细胞实验还应包含以下对照:[/font][font=宋体] [/font][font=宋体]至少一份未染色样品,与试样同时进行每一步的缓冲液孵育,以优化实验的流速和电压。[/font][font=宋体] [/font][font=宋体]一份适当的阴性对照样品,与试样基本相同,但用在一抗的宿主种属中生产的同型对照替代试样中的一抗。该对照用于非特异性结合二抗。[/font][font=宋体] [/font][font=宋体]如有需要也可准备一份已知表达所有目标抗原的细胞组成的阳性对照,并与试样共同孵育,但仅用单色检测。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]流式免疫检测方法与应用[/b][/font][font=宋体]同其他免疫检测应用一样,流式细胞分析也可通过多种方法利用抗体探测特定的细胞基元。两大常用方法为:直接检测法和间接检测法。[/font][font=宋体] [/font][font=宋体]直接检测法[/font][font=宋体][font=宋体]直接检测法采用一步染色工艺,仅需一抗即能特异性结合目标抗原,无需额外步骤,可直接与支持成像或其他结合状态检测的分子结合。在探测细胞表面抗原时,应避免固定细胞,因为固定可能导致抗体探针无法与目标抗原充分接触。因此,保持细胞活力对于数据采集至关重要。若需查找适用于直接检测法的抗体,推荐使用[/font][font=Calibri]Antibody Explorer[/font][font=宋体]抗体搜索工具,将搜索范围限定为“仅限一抗”,并将应用选择为“流式细胞分析”。这样,您将能够快速找到适合您实验需求的抗体。[/font][/font][font=宋体] [/font][font=宋体]间接检测法[/font][font=宋体] [/font][font=宋体][font=宋体]间接检测法首先使用纯化抗体与目标抗原进行结合,然后使用荧光染料标记的二抗(能够特异性靶向一抗的宿主同型)与一抗进行特异性结合,形成一抗[/font][font=Calibri]-[/font][font=宋体]荧光二抗复合物。通过将纯化的一抗与各种波长(或颜色)的荧光染料标记的二抗(特异性针对产生一抗的宿主同型)进行搭配,可以增强抗体库的模块化程度。这种方法能够提高实验的灵敏度和特异性,同时减少背景干扰和误差。[/font][/font][font=宋体] [/font][font=宋体][b]义翘神州提供[url=https://cn.sinobiological.com/services/flow-cytometry-service]流式细胞检测技术服务[/url],其优势:[/b][/font][font=宋体][font=宋体]①具有 [/font][font=Calibri]20,000 [/font][font=宋体]次以上流式抗体筛选鉴定经验及多年流式诊断抗体研发经验,在实验方案设计、样品制备、数据分析等方面确保科学性、准确性和可靠性[/font][font=Calibri] [/font][/font][font=宋体][font=宋体]②拥有 [/font][font=Calibri]1,000 [/font][font=宋体]余株自产精品流式抗体,覆盖细胞膜、胞内、核内及分泌抗原;[/font][/font][font=宋体][font=宋体]③自产 [/font][font=Calibri]Annexin V/7-AAD [/font][font=宋体]凋亡检测试剂盒,并储备多种流式检测常用试剂,大大节约购买试剂的等待时间和实际费用;[/font][/font][font=宋体][font=宋体]④可以提供近 [/font][font=Calibri]200 [/font][font=宋体]种细胞系选择,省去细胞样本寄送过程中的风险,并可以免费提供健康人外周血细胞对照品。[/font][/font][font=宋体][font=宋体]详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/services/flow-cytometry-service[/font][/font]
新华社华盛顿11月20日电 (记者林小春)美国研究人员20日在美国《科学转化医学》杂志上报告说,他们开发出的一种微芯片可简单、快速地检测人体体液中是否存在癌细胞,这一成果将有助于早期的癌症诊断。 癌变细胞的变形能力要比正常细胞大得多。研究人员利用癌变细胞的这一特征开发出一种有多个小孔的微芯片,从胸水提取的细胞进入这些小孔后会撞上芯片的“墙壁”弹回而发生变形,变形程度会被高速成像设备记录下来,以每秒100个细胞的速度分析,从而判断是否存在癌细胞。 领导研究的美国加利福尼亚大学洛杉矶分校教授饶建宇对新华社记者说,他们利用微芯片检测了100多个样本,结果100%地找出了癌变样本。而现有的癌症检查方法通常只能检测出80%到90%。下一步,他们将开展更大规模的临床试验。 饶建宇说,目前的癌症检查往往是间接地判断癌变细胞的一些行为特征,如浸润性和转移能力、对药物的敏感性等,一般要先对细胞进行固定处理再染色,或提取DNA及蛋白成分等进行分析,程序多而复杂,但所得结果往往是片面和间接的。 而微芯片技术则是直接判断癌变细胞的物理及行为特征,无需对细胞处理或染色,因此简单而快速,也更加精确。饶建宇说:“这就好像判断一个人的角斗能力,光看高矮胖瘦或家庭背景等也许有一些帮助但不够,而直接的比赛是最管用的。” 他说:“人们谈癌色变往往是由于癌细胞具有浸润和转移的共性,同时又有千变万化的个性,因此以直接的方法来判断癌细胞的物理及行为特征尤为重要,这使得我们对癌细胞的认识更直接、全面和准确,对癌症的诊断由此上了一个新平台。”
关于生乳中体细胞检测,目前主流的有流式细胞仪法,电子显微镜法,粘度测定法,电导率法等技术,你用的哪种方法?
大神们,帮忙推荐台主要针对小鼠骨髓细胞数检测的仪器,再一个就是能对小鼠血细胞的种类分类,计数。要求不高。。但是这种针对性的仪器还这难找。。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=52162]流式细胞仪检测凋亡[/url][em03] [em03] [em04] [em04]
你检测体细胞了吗,用的啥仪器,啥方法???
2015年3月底,第一个中国科学院和中国食品药品检定研究院联合开发的试剂盒出现在中国食品药品检定研究院网站的国家药品标准物质目录中:CHO宿主细胞DNA残留检测试剂盒(PCR-荧光探针法)。在2016年7月举办的生物制品研讨会上,中检院吕萍主任对这个试剂盒做了精彩的说明。这个由中检院与中科院联合研发,由生物制药企业参与标定的试剂盒与现行美国药典(USP)建议的检测方法同步,但与2010版药典附录中外源性 DNA 残留量测定法有所不同,将是国内生物制品的研发和生产的上下游企业检测宿主细胞DNA残留的第一选择,其后又联合开发了宿主细胞DNA残留样本前处理试剂盒,E.coli宿主细胞DNA残留检测试剂盒,Vero宿主细胞DNA残留检测试剂盒,毕赤酵母DNA残留检测试剂盒,大大的方便的广大厂商的选择。产品优势:1:中检所参与开发并认可其质量2:灵敏度高,稳定性好3:高效回收微量dna,回收率70-130%4:操作快捷,整个过程只要4小时5:满足自动化操作要求,可以高通量检测 ,6:参考品溯源至中检所DNA国家标准品7:价格便宜,基本价格都在ABI公司价格的一半以下,大大节约了企业成本订货信息货号 品名 包装SK030203D100 宿主细胞DNA残留样本前处理试剂盒 100TSK030201c100 CHO宿主细胞DNA残留检测试剂盒 100TSK030202e100 E.coli宿主细胞DNA残留检测试剂盒 100TSK030204v100 Vero宿主细胞DNA残留检测试剂盒 100TSK030205p100 毕赤酵母DNA残留检测试剂盒 100T生物制品中宿主细胞残留DNA具有潜在致瘤和传染风险,所以各国药品监管部门对DNA杂质的限量要求非常严格。美国药典在General Chapter 介绍了三种常用技术,但将在2015年颁布的新版(USP38-NF33)中增加全新章节(General Chapter )来进一步规范残留DNA检测的方法和标准物质。与1000号以上的章节不同的是,USP编号1000以内的章节详细规定了检测技术、系统适应性标准和标准物质。新版USP中将唯一推荐qPCR法作为生物制品中宿主残留DNA的标准方法。qPCR法的技术优势在于序列特异性高、灵敏度高、重现性好,可以为生物制药工业在工艺研究和成品质量控制方面提供可靠的检测手段。我国参照WHO、FDA和欧盟的标准,很早以前开始就对生物制品中残余DNA含量进行限制。从卫生部颁布的《人用重组DNA制品质量控制要点》到近年的《中国生物制品规程》都对DNA含量做了严格要求,部分标准高于国际标准。2010年版中国药典附录收录了DAN探针杂交法和荧光染料法,这两种方法都存在技术缺陷,很难达到杂质限量检测的灵敏度,已经被欧美药典摒弃。目前,仍有很多国内企业沿用这两种方法检测残留DNA,致使生产工艺和产品质量很难达到国际一流水平。根据残余DNA检测技术的发展趋势,小编预计我国2015版药典或增补版本中将出现qPCR方法。企业在生产与研发中采用中检院标准物质目录中提供的成套试剂盒,可以大幅度减少费时、耗力、成本高昂的方法学考察,只需开展少量方法适应性实验,就可以在生产工艺和质控体系的优化方面发挥实际作用,同时满足美国FDA相关标准的要求。同时,联合研发单位中科院湖州营养中心提供免费技术咨询和培训,帮助企业解决试剂盒应用中的各种技术问题。生物制品可用于治疗和预防疾病,关系到患者和健康人的用药安全,产品质量必须得到保障。我国药品监管部门对生物制品中残留DNA的限量标准制订的非常严格,但药典修订存在一定滞后性,附录中的检测技术与先进国家尚存在差距,企业在研发和生产中应具有一定前瞻性,否则会使改进工艺、提高质量、保障安全的努力大打折扣。为什么要检测残余DNA?生物制剂是制药行业中发展最快的领域,2014年全球十大畅销药中7个是生物制剂。这些销售在临床上疗效确切,但研发成本高,生产和质量控制要求非常严格。绝大部分生物制剂是不经过胃肠道直接进入体内,所以除了生物活性外,监管部门对药品中杂质的限量要求非常严格。其中,宿主细胞残留DNA因为具有特别的潜在安全风险,一直是国内外药品监管机构关注的重点。美国药典会从2011年开始就组织专门小组讨论修订生物制品中残留DNA检测方法,并在2014年Prescription/Non-Prescription Stakeholder Forum Meeting#5上宣布将在2015年药典修订版中增加新的章节(General Chapter )来规范检测方法和标准物质。为什么美国药典会的专家组花几年时间讨论一个微量成分(100pg/剂量)的检测方法?还要专门增加章节来规范化?回答这些问题,先要了解它的来源和潜在危害性。生物制品中的重组蛋白药、抗体药、疫苗等产品是用连续传代的动物细胞株表达生产,虽然经过严格的纯化工艺,但产品中仍有可能残余宿主细胞的DNA片段。这些残余DNA可能带来传染性或致瘤性风险,比如残留DNA可能携带HIV病毒或Ras癌基因。分布在哺乳动物细胞基因组的LINE-1序列可能发挥逆转录转座子作用插入到染色体中,这种插入可能影响关键基因功能的发挥,比如激活癌基因或抑制抑癌基因。此外,由于微生物来源的基因组DNA富含CpG和非甲基化序列,增加了重组蛋白药物在体内的免疫源性风险。目前的研究结果显示,残留DNA的致瘤性相比传染性风险要低,但考虑到致瘤性实验是动物实验,传染性实验是在细胞水平做的,或许对两方面的风险都不能掉以轻心。众所周知,外源蛋白可能引起严重免疫反应,但关于残留DNA诱导的免疫反应的研究还不多。在一些临床前和临床研究中报道了高剂量的核酸样品,比如DNA疫苗或佐剂中的CpG寡聚核苷酸,可以诱导免疫反应,还诱导产生DNA抗体。生物制品中宿主残余DNA既是是生产中带来的杂质,还存在一定安全隐患。因此,WHO和各国药物注册监管机构一般只允许生物制剂中存在100pg/剂量以下的残留DNA。根据杂质来源和工艺,特殊情况下最高允许10ng/剂量。各种残余核酸检测技术的优劣正如前面讲过,2015年版的美国药典将新增章节对残余DNA检测进行规范化,那究竟和现有方法有什么不同?为什么最后只确定了一种方法?我们来看看现行美国药典对于残余DNA检测的总体要求。"因为残留DNA涉及到潜在来源(传染性病毒DNA)、管理规程等关键问题,药品监管部门建议必须建立产品的DNA残留检测方法。不论是否成品的常规检测包含DNA残留含量检测,还是工艺开发中已经证实了DNA清除率,残留DNA技术指标和定量分析监测规程都必须确立。分析方法包括杂交法、基于DNA结合蛋白的免疫色谱法(阀值法)、定量PCR(Q-PCR)或其他DNA扩增方法。理想的定量检测方法的灵敏度应该能够检测到约10pg/剂量的残留DNA。杂交法、阀值法和定量PCR方法因为灵敏度可以达到检测要求,所以属于经典方法。"下面我们引用美国药典(USP)的内容分别介绍一下这三种方法。杂交法(Hybridization-based):在这种方法中,根据宿主DNA序列设计DNA探针用于测定产品中配对DNA的数量。双链DNA被变性成单链后固定在尼龙膜或硝化纤维膜上,DNA探针被放射或荧光随机掺入标记以后,与膜上固定的样品宿主DNA杂交结合,并在胶片或成像仪对应位置中显现斑点。对于荧光标记的探针,斑点的光密度结果可以在仪器中定量分析。斑点光密度对应结合在目标DNA上的探针数,进而推测出残留DNA的数量。通过目测方法可以半定量地检测样品中残留DNA,仪器读片可以对应斑点光密度绘制标准曲线,对应检测结果更加准确。DNA结合蛋白免疫阈值法(DNA-BINDING PROTEIN-BASED):这种方法使用DNA结合蛋白和DNA抗体,分四步检测。第一步,通过加热把DNA变性成单链DNA,变性后DNA与偶联了亲和素的DNA结合蛋白以及偶联了尿素酶的DNA单克隆抗体混合反应,液相中的单链DNA、DNA结合蛋白、DNA抗体共同形成序列非特异的复合物。第二步,样品混合液通过生物素标记的膜,亲和素-生物素结合把DNA复合物固定在膜上,洗去非特异吸附。第三步,膜放入检测仪器中与尿素溶液反应,反应产物氨改变溶液pH值并被仪器记录变化。这种pH值的变化直接与样品中的DNA数目相关。第四步,仪器软件自动分析原始数据确定样品中残留DNA数量。定量PCR法(QUANTITATION PCR-BASED):qPCR方法以其快速、高通量的特点已经被应用于生物制药的一些领域(拷贝数检测与病毒检测)。这项技术能够确定各种样品中目标DNA序列的准确数量。DNA探针的设计非常关键,这种DNA探针包含一端染料分子和另一端淬灭分子。当特殊设计的DNA引物引导DNA聚合酶沿着模板序列复制合成另一条对应序列时,DNA聚合酶切断结合在目标DNA上的探针染料端,释放到反应液里的染料信号被仪器测量。经过数十个循环的DNA扩增,荧光信号与起始DNA模板成对应关系,对应标准曲线可以准确计算出样品中残留DNA的数量。美国药典附录进一步对三种方法进行了应用评价。杂交法可以序列特异性地检测目标DNA,但32P标记的探针因为存在半衰期短、放射等问题,实际应用并不广泛。
Nature:转基因酵母细胞制造出能互相交流的“生物电路”生物电路, 转基因, Nature, 酵母, 细胞典和西班牙科学家使用转基因酵母细胞制造出了能够互相交流的“生物电路”,未来,科学家有望使用人体细胞构建出更复杂的系统,来检测人体健康状况。相关研究发表在12月9日出版的Nature杂志上。作为欧盟“分子计算机”项目的一部分,瑞典哥德堡大学和西班牙巴塞罗那庞培法布拉大学的科学家在哥德堡大学施特芬·霍曼教授的领导下进行了该项研究。哥德堡大学细胞和分子生物学系肯塔罗·弗瑞卡瓦表示,尽管经过重新编程的细胞不能像真正的计算机做同样的工作,但该研究为使用这样的细胞建立复杂的系统铺平了道路。未来人体健康状况有望通过这种“分子对分子”的交流系统来探测,将疾病消灭在萌芽阶段;或者将其作为生物传感器来探测污染物,分解环境中的有毒物质等。合成生物学是一个方兴未艾的研究领域,其中的一个应用是设计出自然界中不存在的生物系统。例如,研究人员已经成功地使用转基因细胞构建出许多不同的人工连接装置,诸如电路断路器、振荡器和传感器等。尽管这些人工连接器具有很大的潜力,但迄今为止还存在很多技术限制,主要原因是,分处不同细胞中的人工系统很少能按科学家的期望来工作,因此影响了最终结果。
求助各位大侠,有没有测过细胞的拉曼光谱。我们用的雷尼绍的仪器,785nm激发光,背景信号太强,一点细胞的信号都测不出,怀疑激光没有聚焦在细胞上。1. 细胞测量前要怎么处理?2. 细胞放在什么样的载玻片上测量,怎样减小背景影响?3. 仪器参数设置上有什么需要注意的么?怎样确定把光聚焦到细胞上?老板逼得紧,谢谢各位啊!