目前来说,最常用的[url=https://www.thermofisher.com/cn/zh/home/life-science/antibodies.html]抗体检测[/url]方法应该是ELISA,既可以检测抗体的存在又可以对其定量。此方法用到的仪器主要有离心机,自动洗板机和酶标仪;用到的主要试剂有PBS溶液,吐温20,BSA,一抗,二抗和显色液。其他的抗体检测方法还有免疫扩散和免疫电泳,但是大多是定性或者半定量,而好处是操作简单,所需试剂少。
印度首都第五轮抗体检测超一半人阳性。
[font='calibri'][size=13px]什么是中和抗体?如何检测[/size][/font][font='calibri'][size=13px]假病毒[/size][/font][font='calibri'][size=13px]中和抗体?[/size][/font]什么是中和抗体?中和抗体是一类与病毒结合并使病毒失去传染性的抗体。当病毒侵入人体时,浆细胞会产生病毒特异性抗体,但只有少数是中和抗体。中和机制如下:(1)改变病毒表面的构象;(2)与吸附相关的病毒表位结合,阻断其与宿主细胞受体的相互作用;(3)与病毒形成免疫复合物,易于被巨噬细胞清除;(4)当病毒表面抗原与中和抗体结合时会激活补体,从而导致病毒裂解。S蛋白(spike protein)是SARS-CoV-2病毒的主要包膜蛋白,由S1和S2亚基组成的三聚体跨膜糖蛋白,负责识别宿主细胞受体即血管紧张素转换酶2(ACE2)并介导膜融合。S1亚基上的受体结合域(RBD)直接参与宿主受体识别并介导病毒入侵。S蛋白上的受体结合结构域(RBD),被认为是病毒感染宿主细胞的关键位点和大多数中和抗体的靶标。中和抗体可阻止S1或RBD与ACE2结合,从而防止病毒侵入宿主细胞并最终阻止病毒感染(图1)。因此,S1或RBD的突变可能会导致SARS-CoV-2有较强的传染性。如何检测假病毒中和抗体?中和抗体检测试验包括病毒中和试验、假病毒中和试验和替代病毒中和试验。病毒中和试验中和抗体检测的金标准是病毒中和试验,主要包括空斑减少中和试验和微量中和试验。两种方法都使用定量的活病毒与不同稀释度的等量血清混合,并接种预先准备好的单层细胞。最后,根据空斑形成单位或细胞病变效应来评估中和抗体的效价。由于涉及到活病毒的操作,这些检测只能在生物安全三级实验室进行,极大地限制了空斑减少中和试验和微量中和试验的使用。假病毒中和试验目前,越来越多的实验室使用假病毒中和试验进行中和抗体检测。SARS-CoV-2假病毒以非致病性病毒(如复制缺陷型HIV-1)为载体,将载体病毒的包膜蛋白替换为SARS-CoV-2的S蛋白,并引入检测信号分子,例如GFP和荧光素酶。假病毒利用S蛋白的RBD结构域与ACE2结合,模拟病毒入侵的过程。中和抗体可有效抑制SARS-CoV-2假病毒感染宿主细胞(图2),并通过信号检测评估中和抗体效价。由于假病毒为一次性感染病毒,不具备自我复制能力,无生物安全危险,所以这种方法可以在生物安全二级实验室进行。替代病毒中和试验替代病毒中和试验是基于竞争性酶联免疫吸附试验(ELISA)的原理,利用重组RBD蛋白与重组ACE2蛋白的结合作用来模拟病毒-细胞相互作用。样品中的中和抗体可有效阻断RBD蛋白与ACE2蛋白的结合。与病毒和假病毒中和试验相比,替代病毒中和试验更安全、更容易执行且耗时更少。中和检测服务信息由北京义翘神州科技股份有限公司(Sino Biological Inc.)为您提供,如您想了解更多关于SARS-CoV-2 (2019-nCoV) Spike假病毒中和检测服务报价、型号、参数等信息,欢迎来电或留言咨询。具体详情可点击:https://cn.sinobiological.com/services/pseudovirus-neutralization-assay-service
GB/T 18089-2008 蓝舌病病毒分离、鉴定及血清中和抗体检测技术
实验室常用的ELISA方法可以用来测定抗体,也可以用来测定抗原。我们可以根据试剂的来源和标本的情况以及检测的具体条件,可设计出各种不同类型的检测方法。下面就让上海劲马ELISA试剂盒为您分享其中关于双抗体夹心法检测抗原的操作步骤。双抗体夹心法是检测抗原最常用的方法,操作步骤如下:1) 将特异性抗体与固相载体联结,形成固相抗体。洗涤除去未结合的抗体及杂质。2) 加受检标本,保温反应。标本中的抗原与固相抗体结合,形成固相抗原抗体复合物。洗涤除去其他未结合物质。3) 加酶标抗体,保温反应。固相免疫复合物上的抗原与酶标抗体结合。彻底洗涤未结合的酶标抗体。此时固相载体上带有的酶量与标本中受检抗原的量相关。4) 加底物显色。固相上的酶催化底物成为有色产物。通过比色,测知标本中抗原的量。只要获得针对受检抗原的异性抗体,就可用于包被固相载体和制备酶结合物而建立此法。如抗体的来源为抗血清,包被和酶标用的抗体最好分别取自不同种属的动物。如应用单克隆抗体,一般选择两个针对抗原上不同决定簇的单抗,分别用于包被固相载体和制备酶结合物。这种双位点夹心法具有很高的特异性,而且可以将受检标本和酶标抗体一起保温反应,作一步检测。劲马ELISA试剂盒小提示:双抗体夹心法适用于测定二价或二价以上的大分子抗原,但不适用于测定半抗原及小分子单价抗原,因其不能形成两位点夹心。
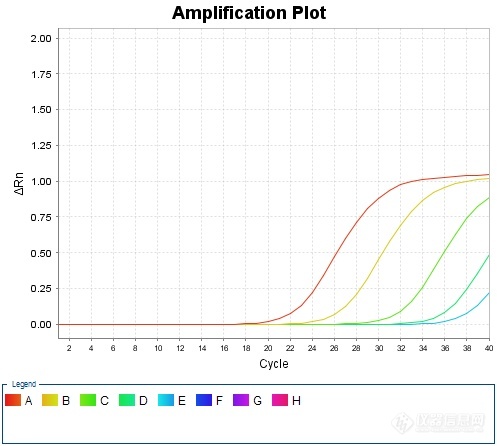
[color=black]猪圆环病毒荧光定量[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法的模块化构建及实践[/color][color=black]1 前言[/color][color=black]猪圆环病毒(porcine circovirus,PCV)在分类学上属圆环病毒科圆环病毒属,为已知的最小的动物病毒之一。病毒粒子直径14~17nm,呈20面体对称结构,无囊膜,含有共价闭合的单股环状负链DNA,基因组大小约为1.76kb。[/color][color=black]PCV对外界理化因子的抵抗力相当强,即便在PH3的酸性环境及72℃的高温环境中也能存活一段时间,氯仿作用不失活,无血凝活性。现已知PCV有两个血清型,即PCV1和PCV2。PCV1为非致病性的病毒,PCV2为致病性的病毒,是断奶仔猪多系统衰竭综合征(Postweaning Multisystemic Wasting Syndrome,PMWS)、皮炎与肾病综合征(Porcine Dermatitis and Nephropathy Syndrome,PDNS)的主要病原。猪对PCV2具有较强的易感性,感染猪可自鼻液、粪便等废物中排出病毒,经口腔、呼吸道途径感染不同年龄的猪。[/color][color=black]在病猪鼻黏膜、支气管、肺脏、扁桃体、肾脏、脾脏和小肠中有PCV2粒子存在。胸腺、脾、肠系膜、支气管等处的淋巴组织中均有该病毒,其中肺脏及淋巴结中检出率较高。表明PCV2严重侵害猪的免疫系统:病毒与巨噬细胞/单核细胞、组织细胞和胸腺巨噬细胞相伴随,导致患猪体况下降,形成免疫抑制。因此,有必要对猪圆环病毒进行检测,对感染PCV2的商品猪进行疫苗免疫,对PCV2长期阳性的种猪予以淘汰。[/color][color=black]2 模块化检测方法思路[/color][color=black]总体思路是:将动物疫病荧光定量[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测分为三个模块,核酸提取采用DNA/RNA共提试剂,核酸扩增采用预混液+引物探针方式,质控品利用抗原或商品化疫苗自制。具体思路如下:[/color][color=black]——核酸提取采用DNA/RNA共提试剂;[/color][color=black]——引物探针严格按照标准方法,委托生物工程公司合成;[/color][color=black]——反应体系中其他成分,采购商品化q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液;[/color][color=black]——质控品:阳性对照采用商品化疫苗,测定结果后按一定比例稀释,保存备用。[/color][color=black]——反应体系:设为20μL,其中包含:预混液(2×)10μL、ROX 0.4μL为固定量,引物探针加入量根据检测标准中的终浓度予以换算,加灭菌水补足18μL,RNA模板为2μL;[/color][color=black]——反应条件首先按照标准中的条件开展摸索,如达到预期效果则予以固定;如效果不佳则参照预混液及引物探针推荐条件进行适当调整。[/color][color=black]3 材料和方法[/color][color=black]3.1 病毒[/color][color=black]猪圆环病毒疫苗。[/color][color=black]3.2 试剂[/color][color=black]DNA/RNA共提试剂盒:FastPure Viral DNA/RNA Mini Kit试剂盒,南京诺维赞生产;[/color][color=black]q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液:AceQ Universal U+ Probe Master Mix V2,南京诺维赞生产。[/color][color=black]3.3 引物探针[/color][color=black]按照GB/T 35901-2018 《猪圆环病毒2型荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》提供的序列,委托上海生工合成,引物稀释成10μmol/L、探针稀释成5μmol/L,分装成小包装冷冻保存备用。具体序列如下:[/color][color=black]正向引物:5’-GGAGTCTGGTGACCGTTGC-3’[/color][color=black]反向引物:5’-CCAATCACGCTTCTGCATTTT-3’[/color][color=black]探 针:5’-FAM-CCGCTCACTTTCAAAAGTTCAGCCA-BHQ1 -3’[/color][color=black]3.4 反应体系[/color][color=black]根据GB/T 35901-2018 《猪圆环病毒2型荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》所载反应体系,按照终浓度一致原则予以转化。具体转换方法:[/color][color=black]——反应体系总体积设定为20μL;[/color][color=black]——将标准中反应体系的10×[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] Buffer、MgCl2、dNTPs、Taq酶等成分转换为q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液10μL(推荐量);[/color][color=black]——因使用ABI7500荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]仪,故在体系中加入ROX 0.4μL;[/color][color=black]——标准中正向引物、反向引物、探针的终浓度分别为0.2μmol/L、0.2μmol/L和0.12μmol/L,故在修改后的体系中加入量为0.4μL、0.4μL和0.48μL;[/color][color=black]——总DNA加入量修改为2μL(根据经验该加入量已经足够);[/color][color=black]——根据上述各成分用量,补充体积的无核酸酶水修改为6.32μL。[/color][table][tr][td][color=black]标准方法[/color][/td][td][/td][td][/td][td][color=black]修改方法[/color][/td][td][/td][/tr][tr][td][color=black]10Χ [url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] Buffer[/color][/td][td][align=center][color=black]5.0[/color][/align][/td][td][/td][td][color=black]2Χ q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液[/color][/td][td][align=center][color=black]10[/color][/align][/td][/tr][tr][td][color=black]Taq酶(5U/μL)[/color][/td][td][align=center][color=black]2.0[/color][/align][/td][td][/td][td][color=black]ROX[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]dNTPs(100mmol/L)[/color][/td][td][align=center][color=black]1.5[/color][/align][/td][td][/td][td][color=black]正向引物(10μmol/L)[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]MgCl2[/color][/td][td][align=center][color=black]0.25[/color][/align][/td][td][/td][td][color=black]反向引物(10μmol/L)[/color][/td][td][align=center][color=black]0.4[/color][/align][/td][/tr][tr][td][color=black]正向引物(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]探针(5μmol/L)[/color][/td][td][align=center][color=black]0.48[/color][/align][/td][/tr][tr][td][color=black]反向引物(10μmol/L)[/color][/td][td][align=center][color=black]1.0[/color][/align][/td][td][/td][td][color=black]无核酸酶水[/color][/td][td][align=center][color=black]6.32[/color][/align][/td][/tr][tr][td][color=black]探针(10μmol/L)[/color][/td][td][align=center][color=black]0.6[/color][/align][/td][td][/td][td][color=black]总DNA[/color][/td][td][align=center][color=black]2.0[/color][/align][/td][/tr][tr][td][color=black]无核酸酶水[/color][/td][td][align=center][color=black]26.95[/color][/align][/td][td][/td][td][color=black]总体积[/color][/td][td][align=center][color=black]20[/color][/align][/td][/tr][tr][td][color=black]内参质粒[/color][/td][td][align=center][color=black]0.2[/color][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][color=black]总DNA[/color][/td][td][align=center][color=black]10[/color][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][color=black]总体积[/color][/td][td][align=center][color=black]50[/color][/align][/td][td][/td][td][/td][td][/td][/tr][/table][color=black]3.5 反应条件[/color][color=black]参照GB/T 35901-2018 《猪圆环病毒2型荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》推荐的扩增程序,结合ABI7500荧光采集时间不能少于34s的要求,进行预试验。扩增程序如下:[/color][color=black]50℃2min →95℃2min →(95℃15s → 60℃34s)*40[/color][color=black]如扩增结果理想,则不做修改直接采纳,否则进行适当调整。[/color][color=black]4 试验结果[/color][color=black]对猪圆环病毒疫苗(SH株)进行核酸检测,结果较理想。扩增曲线如下:[/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009251444312083_9380_1627156_3.jpg[/img][/align][color=black]5 阳性质控的制备[/color][color=black]根据GB/T 35901-2018 《猪圆环病毒2型荧光[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测方法》规定,阳性对照应Ct≤30。对猪圆环病毒疫苗(SH株)适当稀释后进行再次检测,结果如下:[/color][table][tr][td][align=center][color=black]稀释倍数[/color][/align][/td][td][align=center][color=black]1:10^0[/color][/align][/td][td][align=center][color=black]1:10^1[/color][/align][/td][td][align=center][color=black]1:10^2[/color][/align][/td][td][align=center][color=black]1:10^3[/color][/align][/td][/tr][tr][td][align=center][color=black]PCV-2疫苗[/color][/align][/td][td][align=center][color=black]20.99[/color][/align][/td][td][align=center][color=black]25.17[/color][/align][/td][td][align=center][color=black]30.68[/color][/align][/td][td][align=center][color=black]34.80[/color][/align][/td][/tr][/table][color=black]经综合判定,最后采用猪圆环病毒疫苗(SH株)作1: 10^1稀释,分装为200μL/管作为阳性质控,Ct值约25,-70℃冻存备用。[/color][color=black]6 讨论[/color][color=black]6.1 检测工作更加方便高效[/color][color=black]一是在核酸提取环节采用了DNA/RNA共提试剂,待检样品经一次提取核酸,除可应用于圆环病毒、非洲猪瘟等DNA病毒项目检测外,还可应用于口蹄疫、蓝耳病等RNA病毒项目检测;[/color][color=black]二是由于实验室储备了足够量的q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液,在开展检测时,不必担心部分检测量较少的项目由于试剂组分不足而罢工事件的发生;[/color][color=black]三是由于q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]预混液适用于多数DNA病毒项目的检测,在检测任务发生重大变化时,可以方便地调整检测项目,不必担心试剂不足或浪费情况的发生。[/color][color=black]6.2 阳性质控品制备方便[/color][color=black]猪圆环病毒疫苗是较常用的动物免疫用疫苗,只需对疫苗进行含量测定,进行一定比例的稀释即可作为实验室内部的阳性质控品。[/color][color=black]6.3 适用性有待进一步验证[/color][color=black]尽管在构建新方法时,对适用性进行了验证,但对于其他毒株,尤其是较新型的变异株是否有效,尚有待进一步观察和验证。[/color][color=black]6.4 严格依法依规操作[/color][color=black]如果有关法律法规或上级有关部门出台政策,要求采用获批准的成品试剂盒用于检测,则实验室必须及时停止自建方法的使用。[/color]
国家卫健委5月29日通报,全国新冠病毒疫苗接种超过6亿剂次。自3月27日超过1亿剂次以来,每亿剂次所需时间为25天、16天、9天、7天、5天,间隔不断缩短,这就是疫苗接种的中国速度。接种新冠病毒疫苗后,理论上体内会产生IgM、IgG及中和抗体,这些抗体与新冠病毒结合后将使病毒失去感染性。因此新冠病毒疫苗接种后,检测IgM、IgG及中和抗体水平,对于评价疫苗的免疫效果至关重要,同时为常态化新冠疫情防护政策调整提供基础性的数据参考。
国家卫健委5月29日通报,全国新冠病毒疫苗接种超过6亿剂次。自3月27日超过1亿剂次以来,每亿剂次所需时间为25天、16天、9天、7天、5天,间隔不断缩短,这就是疫苗接种的中国速度。接种新冠病毒疫苗后,理论上体内会产生IgM、IgG及中和抗体,这些抗体与新冠病毒结合后将使病毒失去感染性。因此新冠病毒疫苗接种后,检测IgM、IgG及中和抗体水平,对于评价疫苗的免疫效果至关重要,同时为常态化新冠疫情防护政策调整提供基础性的数据参考。
一 抗体选择指南:检测任何目的靶蛋白都有不止一种抗体可供选择,为缩小抗体的选择范围选中合适的抗体,需要考虑如下几种因素:1. 分析或应用的类型2. 样本蛋白的结构性质3. 样本的种属4. 抗体宿主的种类5. 抗体的标记和检测1 分析试验的应用类型一般抗体说明书都列出该抗体经试验验证过适用于何种分析类型,如:可以应用于WB IHC ICC ELASA 分析等,如果抗体说明书没有提及的应用类型,并不意味着该抗体不适用于此种分析应用类型,而仅是说明尚未经过此种分析试验验证,如果抗体不适用某些分析试验,则会在抗体说明书上标注出来不适于某分析试验。2 样本蛋白的结构性质了解样本蛋白的结构性质有助于选择最合适的抗体,至少两方面因素需要考虑(1)..待测样本蛋白的结构域:抗体是由各种不同免疫原免疫宿主而制备得来,其中的免疫原包括:全长蛋白、蛋白片断、多肽、全有机体(如:细菌)或细胞,抗体说明书一般都有免疫原的描述,如果打算检测的是蛋白片断或一种特殊的同型物或蛋白全长的某一区域,则必须选择用含此片段域的免疫原制备出的抗体。如果打算用FACS 流式检测活细胞的表面蛋白,则需要选择含该表面蛋白的胞外域来免疫制备的抗体。(2)样本的提取或处理过程:某些抗体要求样本经过某些特殊处理,例如:许多抗体只识别还原和变性的、表位已暴露不受二级四级结构阻碍的蛋白样本,另一方面,某些抗体仅识别天然折叠状态的蛋白。当选择免疫组化的抗体时,应注意某些抗体只识别未固定的冷冻的组织,而另一些抗体则适用于无需抗原修复解交联步聚的甲醛固定石蜡包埋的组织,这些都会在抗体说明书上应用部分标示出来3 样本的物种 应选择物种相同或有交叉反应的抗体,抗体可能与不同物种的同种靶蛋白有交叉反应,因其氨基酸序列同源性较高,如果样本的种类未列入抗体说明书上的交叉反应种属表中,并不意味着该抗体不适用于检测该物种的蛋白,而只是表示该物种尚未用此抗体检测验证过,应通过序列比对的方法来预测交叉反应,可应用Expasy 和 NCBI BLAST 来进行不同物种蛋白同源性比对。4 一抗宿主物种的选择一般说来,在使用偶联二抗结合无偶联物的一抗时,一抗宿主动物的物种选择较为重要,对于免疫组化而言,尽可能选择与样本不同种系物种的一抗,从而避免二抗与样本内源性免疫球蛋白产生交叉反应,例如:检测小鼠样本蛋白,则不应选择小鼠或大鼠源的一抗,最好选兔源的一抗,则二抗则可选择偶联了检测分子(酶、荧光素、生物素等)的抗兔IgG。如果选择有偶联物的一抗则不适用上述情况,除免疫组化外的其它对不含内源性免疫球蛋白样本的检测方法,则抗体宿主物种的影响不大,如对不含IgG 的细胞裂解物样本的western blotting检测,尽管如此,含有血清的组织裂解物和组织培养上清中含有免疫球蛋白,还原变性样本中含IgG,在western blot 检测中则结合出现IgG 分子50 and 25 kDa 的重链和轻链条带。5 二抗的选择 二抗应选用与使用的一抗相同的物种来源,例如:如果你的一抗是小鼠的单克隆抗体,二抗则选抗小鼠的二抗anti-mouse secondary。建议检查二抗说明书确保该抗体适用于你的检测应用, 二抗一般连接荧光素FITC 或发光团。6 双重染色抗体的选择用未偶联一抗进行细胞培养物或组织切片的双重免疫染色要求一抗来源于不同物种并且二抗分别识别其中之一,二抗说明书应描述其与其它物种来源的免疫球蛋有否有交叉吸附。
[font='calibri'][size=13px]人源化抗体和全人源抗体区别[/size][/font][font='calibri'][size=13px]?[/size][/font][font='calibri'][size=13px]义翘[/size][/font][font='calibri'][size=13px]抗体人源化[/size][/font][font='calibri'][size=13px]服务内容[/size][/font][font='宋体']人源化抗体和全人源抗体区别:[/font][font='宋体']根据单克隆抗体的来源不同,可分为鼠源抗体、嵌合体抗体、人源化抗体和全人源抗体。[/font][font='宋体']所谓的全人源单抗,就是基因来源100%都是人源的。不过,事实上全人源单抗也是在小鼠身上产生的,通过把产生抗体相关的人类基因转移到小鼠,此后小鼠体内的抗体结构可以跟人类抗体结构一样。所以全人源抗体直接用人体[/font][font='宋体']细胞制作的抗体,只是抗体结构100%按照人类基因编码而成。[/font][font='宋体']人源化单抗则是大部分来源是人源,同时融合了鼠源成分。近年来,科学家通过基因工程特意将鼠抗的关键有利基因结构保留在人源框架上,起到特殊的作用,就像优化再加工(2l。例如,依奇珠单抗(人源化单抗)中保留了1.8%的鼠源成分,这部分整合了优势有利的基因,成就了依奇珠单抗的高亲和力,其起效速度快可能也和其亲和力高有关。[/font][font='宋体'] [/font][font='宋体'] [/font][font='宋体']义翘神州[url=https://cn.sinobiological.com/services/antibody-humanization-service][b]抗体人源化服务[/b][/url]:[/font][font='宋体']抗体人源化[/font][font='宋体']非人源性抗体进入人体内会引起严重的机体排异反应,进而影响抗体在临床应用时的安全性和治疗效果。抗体人源化通过基因改造,使鼠源抗体具有与人体内抗体类似的结构,从而逃避免疫系统的识别。抗体人源化经历了从嵌合抗体到CDR移植、SDR移植等技术演变,力求在保持高亲和力、高特异性结合能力的同时克服传统鼠源抗体的免疫原性,在肿瘤治疗等领域具有极为广泛的应用前景。[/font][font='宋体']义翘神州利用CDR置换技术及计算机辅助结构模拟设计可对鼠源单抗等进行人源化改造,保证人源化程度 95%,为客户提供优质的单克隆抗体人源化服务。[/font]
猪瘟抗体金标快速检测卡使用说明书【产品用途】本检测卡采用免疫原理和胶体金免疫层析技术制成,用于快速检测猪血液或猪血清中的猪瘟抗体,为国内最新检测试剂。检测时间仅需20 分钟,操作简便、快速、结果准确、直观、灵敏度高、容易判定。当猪瘟抗体滴度达到能抵御猪瘟强毒攻击时,在检测区和对照区各形成一条色线,则视为阳性,抗体滴度越高,检测线颜色越深;当猪瘟抗体滴度达不到抵御猪瘟强毒攻击的抗体滴度时,只在对照区形成一条色线,则视为阴性。本卡附带一张金标试纸与正相间接血凝试验实物参照图,将检测线的颜色深浅与参照图对照,便可粗略估计样品抗体的滴度。【操作步骤】1.打开包装袋,取出检测卡平放在桌面上,并做好标记;2.在检测卡的加样孔内加入2 滴(50-100ul)血液或血清样品;3.在20 分钟内观察和记录结果,超过20 分钟的结果只能作为参考。【结果判定】见右图阳性:在检测区(T)和对照区(C) 各出现一条紫红色线。检测线颜色越深,表明猪瘟抗体滴度越高。弱阳性:在检测区(T)和对照区(C)各出现一条紫红色线,但检测线颜色很浅。阴性:只在对照区(C)出现一条紫红色线。无效:都不出现紫红色线或只在检测区(T)出现紫红色线,对照区(C)不出现紫红色线。【结果参考意义】1.强阳性结果说明猪瘟抗体滴度较高,暂时不必进行猪瘟疫苗的接种免疫;2.弱阳性结果说明猪瘟抗体滴度只达到抵抗猪瘟强毒攻击的最低保护水平,这时应该及时进行猪瘟疫苗接种,此时也是猪瘟疫苗接种的最佳时间;3.阴性结果说明机体内无猪瘟抗体或抗体水平低于抵抗猪瘟强毒攻击的最低保护水平,如果动物群体健康,应该及时进行猪瘟疫苗接种。如果动物群体已有个别动物出现疑似猪瘟病时,则可作为诊断猪瘟病的一个参考依据。【注意事项】1.请严格按照说明书要求进行操作和结果判定。2.检测样品可以是猪血液或血清。3.检测卡从铝箔袋取出后应尽快使用,尽量避免长时间放置在空气中,否则吸潮后将失效。4.检测环境应保持一定的湿度,避风和避免在过高温度下进行操作。5.检测卡在室温下保存,如在2-8℃冷藏,使用时需平衡至室温后方可打开包装进行检测操作。【包装规格】单头份铝箔袋包装(内含检测卡、吸管和干燥剂);50 头份/盒【贮藏和有效期】密封,在干燥处保存;在3-30℃下贮存,有效期为12 个月。
[quote]项目概况绵阳高新区疾病预防控制中心人类免疫缺陷病毒抗体检测试剂采购项目 采购项目的潜在供应商应在绵阳高新区绵兴东路55号中沅广场世爵假日18楼获取采购文件,并于2023年08月14日 14点00分(北京时间)前提交响应文件。[/quote][font=inherit]一、项目基本情况[/font]项目编号:ZDSF(2023)0801号项目名称:绵阳高新区疾病预防控制中心人类免疫缺陷病毒抗体检测试剂采购项目采购方式:竞争性磋商预算金额:20.0000000 万元(人民币)最高限价(如有):20.0000000 万元(人民币)采购需求:详见采购需求附件合同履行期限:签订合同后5个工作日内交清货物。本项目( 不接受 )联合体投标。[font=inherit]二、申请人的资格要求:[/font]1.满足《中华人民共和国政府采购法》第二十二条规定;2.落实政府采购政策需满足的资格要求:无3.本项目的特定资格要求:(1)供应商须符合《医疗器械监督管理条例》要求,若供应商是制造厂家的须具有《医疗器械生产许可证》或有效备案凭证;若供应商为经销商或代理商的须具有《医疗器械经营许可证》或有效备案凭证。(仅限医疗器械适用)(2)投标产品须符合《医疗器械注册与备案管理办法》要求并提供产品的注册/备案证明材料。(仅限医疗器械适用)[font=inherit]三、获取采购文件[/font]时间:2023年08月04日 至 2023年08月10日,每天上午9:00至12:00,下午14:00至17:00。(北京时间,法定节假日除外)地点:绵阳高新区绵兴东路55号中沅广场世爵假日18楼方式:获取磋商文件时,经办人员当场提交以下资料:供应商为法人或者其他组织的,只需提供单位介绍信(原件)、经办人身份证明(查验原件收复印件);供应商为自然人的,只需提供本人身份证明。以上资料均盖单位鲜章。售价:¥300.0 元(人民币)[font=inherit]四、响应文件提交[/font]截止时间:2023年08月14日 14点00分(北京时间)地点:绵阳高新区绵兴东路55号中沅广场世爵假日18楼[font=inherit]五、开启[/font]时间:2023年08月14日 14点00分(北京时间)地点:绵阳高新区绵兴东路55号中沅广场世爵假日18楼[font=inherit]六、公告期限[/font]自本公告发布之日起3个工作日。[font=inherit]七、其他补充事宜[/font][font=inherit]八、凡对本次采购提出询问,请按以下方式联系。[/font]1.采购人信息名 称:绵阳高新区疾病预防控制中心地址:绵阳高新区石桥铺东路创意联邦6栋1单元302联系方式:赵金华 0816- 25306052.采购代理机构信息名 称:四川中达盛丰工程项目管理有限公司地 址:绵阳高新区绵兴东路55号中沅广场世爵假日18楼联系方式:蒋骐羽 0816-21997273.项目联系方式项目联系人:蒋骐羽电 话: 0816-2199727
[font=宋体]抗体是生物体内重要的免疫分子,它们能够识别并攻击外部入侵者,如病毒和细菌。在医学、生物学和免疫学等领域,抗体标记与检测技术广泛应用于疾病诊断、治疗监测、药物研发等方面。本文将详细介绍[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-conjugation][b]抗体标记[/b][/url]与检测的种类和方法,包括直接标记、间接标记、免疫荧光、酶联免疫吸附试验等。通过对这些技术的了解和应用,我们可以更好地利用抗体进行疾病诊断和治疗监测,提高医疗水平和治疗效果。[/font][font=宋体] [/font][font=宋体][b][font=Calibri]1.[/font][font=宋体]抗体与标记物[/font][/b][/font][font=宋体] [/font][font=宋体][font=宋体]抗体广泛应用于多种免疫分析中,用于检测和定量抗原。直接识别抗原的抗体被称为一抗([/font][font=Calibri]primary antibody[/font][font=宋体]),赋予检测的特异性。同时,在检测中还需加入标记物(详见后文“间接标记法 [/font][font=Calibri]Vs.[/font][font=宋体]直接标记法”),标记物的加入赋予可检测性。表[/font][font=Calibri]1[/font][font=宋体]中列出了一些常用的免疫分析技术,及可能使用到的标记物。[/font][/font][font=宋体] [/font][font=宋体] [/font][table][tr][td][b][font=微软雅黑]免疫分析方法[/font][/b][/td][td][b][font=微软雅黑]标记物[/font][/b][/td][/tr][tr][td][font=微软雅黑][font=微软雅黑]免疫印迹[/font][font=微软雅黑](WB)[/font][/font][/td][td][font=微软雅黑][font=微软雅黑]酶[/font][font=微软雅黑](通常为辣根过氧化物酶HRP或碱性磷酸酶AP)[/font][/font][/td][/tr][tr][td][font=微软雅黑][font=微软雅黑]酶联免疫吸附试验[/font][font=微软雅黑](ELISA)[/font][/font][/td][td][font=微软雅黑][font=微软雅黑]酶、生物素[/font][font=微软雅黑]/链亲和素[/font][/font][/td][/tr][tr][td][font=微软雅黑][font=微软雅黑]免疫荧光[/font][font=微软雅黑](Immunofluorescence)[/font][/font][/td][td][font=微软雅黑]荧光染料[/font][/td][/tr][tr][td][font=微软雅黑][font=微软雅黑]免疫组化[/font][font=微软雅黑](Immunohistochemistry)[/font][/font][/td][td][font=微软雅黑][font=微软雅黑]酶、生物素[/font][font=微软雅黑]/链亲和素[/font][/font][/td][/tr][tr][td][font=微软雅黑][font=微软雅黑]流式细胞术[/font][font=微软雅黑](Flow Cytometry)[/font][/font][/td][td][font=微软雅黑]荧光蛋白或染料、串联染料[/font][/td][/tr][/table][font=宋体] [/font][font=宋体] [/font][font=宋体][b][font=Calibri]2.[/font][font=宋体]直接检测法 [/font][font=Calibri]Vs.[/font][font=宋体]间接检测法[/font][/b][/font][font=宋体] [/font][font=宋体]检测技术可分为两大类:直接法和间接法。对于直接检测法,标记物通过共价键连接到一抗上。而对于间接检测法,标记物则是共价连接到与一抗特异性结合的二抗上。[/font][font=宋体] [/font][font=宋体][font=宋体]在间接法中,检测由两个部分组成:第一步,用未标记的一抗进行孵育(通常[/font][font=Calibri]1[/font][font=宋体]小时),[/font][font=Calibri]([/font][font=宋体]若存在抗原[/font][font=Calibri])[/font][font=宋体]部分抗体与抗原结合,未结合的抗体则通过洗涤去掉,然后加入标记二抗。再次孵育(通常[/font][font=Calibri]1[/font][font=宋体]小时),洗涤去掉未结合的二抗。然后对结合在抗体上的标记物进行量化。若有抗原存在时,标记物通常导致有色物质的生成或某一个波长的发射光量增加。当无抗原存在时,则无一抗的结合,也无二抗试剂的结合,因此无信号产生。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]在直接法中,标记物直接与一抗共价结合,因此仅需一轮孵育及洗涤步骤,而间接法则需要两轮孵育及洗涤步骤。直接法简化了试验的流程,但检测的灵活性降低。下表列举出了直接法[/font][font=Calibri]/[/font][font=宋体]间接法的主要利弊。[/font][/font][table][tr][td][b][font=微软雅黑]方法[/font][/b][/td][td][b][font=微软雅黑]优点[/font][/b][/td][td][b][font=微软雅黑]缺点[/font][/b][/td][/tr][tr][td][font=微软雅黑]直接法[/font][/td][td][font=微软雅黑]仅需使用一抗,检测快速[/font][font=微软雅黑][/font][font=微软雅黑]无二抗的非特异性结合[/font][/td][td][font=微软雅黑][font=微软雅黑]由于标记可能导致一抗的免疫反应性降低[/font][font=微软雅黑] [/font][/font][font=微软雅黑][/font][font=微软雅黑]信号放大作用较弱[/font][/td][/tr][tr][td][font=微软雅黑]间接法[/font][/td][td][font=微软雅黑]一抗含有多个标记,二抗可结合的表位,因而灵敏度升高,信号放大作用较强。[/font][/td][td][font=微软雅黑][font=微软雅黑]二抗可能发生非特异性结合[/font][font=微软雅黑] [/font][/font][font=微软雅黑][/font][font=微软雅黑]孵育及洗涤步骤增多[/font][/td][/tr][/table][font=宋体] [/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]尽管直接标记法具有诸多潜在的优点,但为何如今众多的免疫分析仍采用间接法原理呢[/font][font=Calibri]?[/font][/font][font=宋体] [/font][font=宋体]无疑,最主要的原因就是直接标记一抗相对较复杂,确实从历来经验看,抗体标记都是由那些具有化学修饰技术的专业人员来完成的。在间接法中二抗试剂所起的信号放大效应究竟如何呢?是否直接标记法所产生的信号就很弱?其实在很多情况下,间接法的放大效应是让人产生错觉的。在与二抗试剂的孵育过程及洗涤过程中,一些一抗会与抗原发生解离,因此真正被放大的只是逐渐减少的一抗的量。其实在很多情况下,直接法也可获得与间接法相同甚至更好的结果。[/font][font=宋体] [/font][font=宋体][b][font=Calibri]3.[/font][font=宋体]常见的抗体标记方法[/font][/b][/font][font=宋体]和所有蛋白质一样,抗体也是由氨基酸组成的。理论上,通过大多数氨基酸可以实现生物偶联。以下内容介绍了几种基于赖氨酸残基的抗体偶联和标记技术。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]①[/font][font=Calibri]NHS[/font][font=宋体](琥珀酰亚胺)酯法[/font][/font][font=宋体]应用广泛的荧光染料(如罗丹明衍生物)是采用这种方法对抗体进行偶联。通常在磷酸盐缓冲液中进行,随后与未标记的染料在柱上进行分离。该方法的主要缺点是,由于酯类对水分敏感,酯类的稳定性差。因此,反应结束后,标记抗体应立即使用。[/font][font=宋体] [/font][font=宋体][font=宋体]吉妥珠单抗([/font][font=Calibri]Gemtuzumab ozogamicin, Mylotarg[/font][font=宋体])是全球范围内首个获批上市的抗体偶联药物([/font][font=Calibri]ADC[/font][font=宋体])。半合成的卡奇霉素衍生物具有[/font][font=Calibri]NHS[/font][font=宋体]酯,以便将卡奇霉素与人源化[/font][font=Calibri]IgG4[/font][font=宋体]的赖氨酸残基偶联。然而,由于患者的临床获益不足,[/font][font=Calibri]Mylotarg[/font][font=宋体]已于[/font][font=Calibri]2010[/font][font=宋体]年退市。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]②异硫氰酸盐法[/font][font=宋体][font=宋体]这种方法主要用于异硫氰酸荧光素([/font][font=Calibri]FITC[/font][font=宋体])染料的偶联,广泛用于荧光标记蛋白和抗体的制备。异硫氰酸盐比[/font][font=Calibri]NHS[/font][font=宋体]更稳定,但也更难制备,而且利用该方法,标记的反应效率可能会降低。与[/font][font=Calibri]NHS[/font][font=宋体]法一样,应在反应结束后通过层析法去除多余染料。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]③碳二亚胺法[/font][font=宋体][font=宋体]碳二亚胺衍生化合物将蛋白质上的羧基转换为反应中间体,可与赖氨酸发生反应。碳二亚胺的高反应性意味着它们可用于使用相对惰性的材料(如磁性或金颗粒)标记抗体。最常用的碳二亚胺为[/font][font=Calibri]EDC[/font][font=宋体]。[/font][font=Calibri]NHS[/font][font=宋体]有时可被添加至反应中,以辅助产生相对稳定的中间体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]该方法操作简单,但与[/font][font=Calibri]NHS[/font][font=宋体]一样,[/font][font=Calibri]EDS[/font][font=宋体]具有吸水性,因此,标记后抗体需立即使用。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]④高碘酸盐法[/font][font=宋体][font=宋体]这种方法可用于制备特异性的[/font][font=Calibri]HRP[/font][font=宋体]标记抗体。高碘酸盐通过产生与赖氨酸残基相互作用的醛分子来激活[/font][font=Calibri]HRP[/font][font=宋体]。[/font][font=Calibri]HRP[/font][font=宋体]本身只有少量的赖氨酸残基,因此酶聚合的影响不大。[/font][font=Calibri]HRP[/font][font=宋体]和抗体之间的键是可逆的,可通过添加氰基硼氢化钠使其保持稳定。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-conjugation[/font][/font]
[font=宋体][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/anti-idiotype-antibody][b]抗独特型抗体[/b][/url]是一种能够特异性结合另一抗体独特位的抗体。独特型由多个抗原决定簇([/font][font=Calibri]Antigenic determinant[/font][font=宋体])组成,每个抗原决定簇都是一个独特位。抗原决定簇或独特位可存在于重链可变区,也可存在于轻链可变区,或者存在于两条链组成的表面。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗独特型抗体在治疗性抗体药物开发过程中有着非常广泛的应用。由于抗独特型抗体与抗药抗体([/font][font=Calibri]Anti-drug antibody, ADA[/font][font=宋体])之间的相似性,抗独特型抗体在免疫原性([/font][font=Calibri]Immunogenicity[/font][font=宋体])分析中可作为阳性对照用于抗药物抗体总量的测定。另外,在抗体药的药代动力学([/font][font=Calibri]PK[/font][font=宋体])和药效学([/font][font=Calibri]PD[/font][font=宋体])分析中,抗独特型抗体可用于检测血液中抗体药物的含量(游离型、结合型和总量)。[/font][/font][font=宋体] [/font][font=宋体][b]抗独特型抗体的不同应用[/b][/font][font=宋体] [/font][font=宋体][font=宋体]①药代动力学([/font][font=Calibri]PK[/font][font=宋体])分析[/font][/font][font=宋体][font=宋体]药代动力学([/font][font=Calibri]PK[/font][font=宋体])描述并表征了药物在人或动物体内的四个不同阶段:吸收、分布、代谢和排泄(也称为[/font][font=Calibri]ADME[/font][font=宋体])。在药物开发中,[/font][font=Calibri]PK[/font][font=宋体]分析提供了药物与身体相互作用以及疗效强度和疗效持续时间的基本信息。在开发生物仿制药时,需要通过比较[/font][font=Calibri]PK[/font][font=宋体]分析来评价与原研药在生物活性的潜在差异。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]根据结合模式和性质的不同,抗独特型抗体可分为三种类型:抗原阻断型、抗原非阻断型和药物靶标复合物型。基于这些特点,可以建立不同形式的[/font][font=Calibri]PK[/font][font=宋体]检测,以测量血清中的抗体药物含量,包括游离型、结合型或总量。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗独特型抗体可用于定量检测动物或人血清中的抗体药物水平,是[/font][font=Calibri]PK[/font][font=宋体]研究的关键检测试剂。抗体药物定量分析有多种分析方法,其中[/font][font=Calibri]ELISA[/font][font=宋体]为最常用的形式。在抗独特型抗体捕获[/font][font=Calibri]ELISA[/font][font=宋体]中,将抗独特型抗体包被在平板上,再将含有抗体药物的样本加入系统中,然后用特异性结合药物的标记抗独特型抗体定量抗体药物。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]②免疫原性[/font][font=Calibri]/[/font][font=宋体]抗药抗体([/font][font=Calibri]ADA[/font][font=宋体])检测[/font][/font][font=宋体][font=宋体]免疫原性评价主要采用抗药抗体([/font][font=Calibri]anti-drug antibody, ADA[/font][font=宋体])分析的方法进行,这是治疗性蛋白药物(如单克隆抗体、[/font][font=Calibri]ADC[/font][font=宋体]和融合蛋白)开发过程中的关键步骤。在这些情况下,通常采用多层次递进式进行(图[/font][font=Calibri]3[/font][font=宋体])。该方法首先采用高灵敏的筛选试验鉴别阳性抗体样本,使用验证性试验尽量减少假阳性结果,然后使用表征试验评估抗体的中和能力。[/font][/font][font=宋体][font=宋体]在整个过程中,抗独特型抗体是必要的试剂。检测[/font][font=Calibri]ADA[/font][font=宋体]的检测方法有多种,包括[/font][font=Calibri]ELISA[/font][font=宋体]、放射免疫沉淀法([/font][font=Calibri]RIPA[/font][font=宋体])、表面等离子体共振([/font][font=Calibri]SPR[/font][font=宋体])和电化学发光检测([/font][font=Calibri]ECL[/font][font=宋体])。其中,桥联[/font][font=Calibri]ELISA[/font][font=宋体]是最常用方法,可用于检测所有[/font][font=Calibri]ADA[/font][font=宋体]同种型([/font][font=Calibri]IgG[/font][font=宋体]、[/font][font=Calibri]IgM[/font][font=宋体]、[/font][font=Calibri]IgA[/font][font=宋体]等)。在典型的桥联[/font][font=Calibri]ELISA[/font][font=宋体]中,将抗体药物预包被在平板上,并将标记的抗体药物与患者样本一起孵育,以检测是否存在[/font][font=Calibri]ADA[/font][font=宋体](图[/font][font=Calibri]4[/font][font=宋体])。抗独特型抗体将用作阳性对照或参比标准品,用于样本中[/font][font=Calibri]ADA[/font][font=宋体]的定性分析。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][url=https://cn.sinobiological.com/services/anti-idiotype-antibody-service][b]抗独特型抗体制备[/b][/url][b]套餐[/b][/font][font=宋体][font=宋体]为支持药物开发,义翘神州为客户提供了从抗原制备、抗独特型抗体开发到检测方法建立和试剂盒开发的全方位、一站式的定制抗独特型抗体生产服务。我们拥有丰富的开发经验,包括不同抗体类型如全长[/font][font=Calibri]mAb[/font][font=宋体]、[/font][font=Calibri]F(ab')2[/font][font=宋体]、[/font][font=Calibri]Fab[/font][font=宋体]、[/font][font=Calibri]scFv[/font][font=宋体]、[/font][font=Calibri]VHH[/font][font=宋体]、[/font][font=Calibri]ADC[/font][font=宋体]、[/font][font=Calibri]bsAb[/font][font=宋体]和[/font][font=Calibri]Fc[/font][font=宋体]融合蛋白等。定制的抗独特型抗体可用于建立药代动力学([/font][font=Calibri]PK[/font][font=宋体])[/font][font=Calibri]/ADA[/font][font=宋体]检测方法,以测定样本中的特异性抗体药物或[/font][font=Calibri]ADA[/font][font=宋体]水平。[/font][/font][font=宋体] [/font][font=宋体]服务:[/font][font=宋体]①抗独特型兔多抗制备服务[/font][font=宋体]交付内容:[/font][font=宋体]? 纯化抗体[/font][font=宋体][font=宋体]? [/font][font=Calibri]CoA[/font][/font][font=宋体][font=宋体]周期:[/font][font=Calibri]2-3[/font][font=宋体]个月[/font][/font][font=宋体] [/font][font=宋体]②抗独特型鼠单抗制备服务[/font][font=宋体]交付内容[/font][font=宋体][font=宋体]? 阳性克隆,[/font][font=Calibri]2[/font][font=宋体]管细胞[/font][font=Calibri]/[/font][font=宋体]克隆[/font][/font][font=宋体][font=宋体]? 纯化抗体,[/font][font=Calibri]10 mg/[/font][font=宋体]克隆[/font][/font][font=宋体][font=宋体]? [/font][font=Calibri]ELISA[/font][font=宋体]抗体对(可选)[/font][/font][font=宋体][font=宋体]? [/font][font=Calibri]CoA[/font][/font][font=宋体][font=宋体]周期:[/font][font=Calibri]4~6[/font][font=宋体]个月[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/anti-idiotype-antibody[/font][/font]
猪瘟抗体金标快速检测卡使用说明书【产品用途】本检测卡采用免疫原理和胶体金免疫层析技术制成,用于快速检测猪血液或猪血清中的猪瘟抗体,为国内最新检测试剂。检测时间仅需20 分钟,操作简便、快速、结果准确、直观、灵敏度高、容易判定。当猪瘟抗体滴度达到能抵御猪瘟强毒攻击时,在检测区和对照区各形成一条色线,则视为阳性,抗体滴度越高,检测线颜色越深;当猪瘟抗体滴度达不到抵御猪瘟强毒攻击的抗体滴度时,只在对照区形成一条色线,则视为阴性。本卡附带一张金标试纸与正相间接血凝试验实物参照图,将检测线的颜色深浅与参照图对照,便可粗略估计样品抗体的滴度。【操作步骤】1.打开包装袋,取出检测卡平放在桌面上,并做好标记;2.在检测卡的加样孔内加入2 滴(50-100ul)血液或血清样品;3.在20 分钟内观察和记录结果,超过20 分钟的结果只能作为参考。【结果判定】见右图阳性:在检测区(T)和对照区(C) 各出现一条紫红色线。检测线颜色越深,表明猪瘟抗体滴度越高。弱阳性:在检测区(T)和对照区(C)各出现一条紫红色线,但检测线颜色很浅。阴性:只在对照区(C)出现一条紫红色线。无效:都不出现紫红色线或只在检测区(T)出现紫红色线,对照区(C)不出现紫红色线。【结果参考意义】1.强阳性结果说明猪瘟抗体滴度较高,暂时不必进行猪瘟疫苗的接种免疫;2.弱阳性结果说明猪瘟抗体滴度只达到抵抗猪瘟强毒攻击的最低保护水平,这时应该及时进行猪瘟疫苗接种,此时也是猪瘟疫苗接种的最佳时间;3.阴性结果说明机体内无猪瘟抗体或抗体水平低于抵抗猪瘟强毒攻击的最低保护水平,如果动物群体健康,应该及时进行猪瘟疫苗接种。如果动物群体已有个别动物出现疑似猪瘟病时,则可作为诊断猪瘟病的一个参考依据。【注意事项】1.请严格按照说明书要求进行操作和结果判定。2.检测样品可以是猪血液或血清。3.检测卡从铝箔袋取出后应尽快使用,尽量避免长时间放置在空气中,否则吸潮后将失效。4.检测环境应保持一定的湿度,避风和避免在过高温度下进行操作。5.检测卡在室温下保存,如在2-8℃冷藏,使用时需平衡至室温后方可打开包装进行检测操作。【包装规格】单头份铝箔袋包装(内含检测卡、吸管和干燥剂);50 头份/盒【贮藏和有效期】密封,在干燥处保存;在3-30℃下贮存,有效期为12 个月。
抗核抗体(antinuclear antibody,ANA)又称抗核酸抗原抗体,是一组将自身真核细胞的各种成分脱氧核糖核蛋白(DNP)、DNA、可提取的核抗原(ENA)和RNA等作为靶抗原的自身抗体的总称,能与所有动物的细胞核发生反应,主要存在于血清中,也可存在于胸水、关节滑膜液和尿液中。抗核抗体识别是各种细胞核组分(细胞核生化成分),可特征地出现于许多疾病中。ANA鉴别诊断对于一些特定疾病的确认十分必要,而且对自身免疫性疾病的进一步诊断也很有价值。为了确保检测结果的准确性,对此相关部门对抗核抗体谱(IgG)检测制定了标准操作规程。在规程中,对于样品的要求写到,患者样本用样本缓冲液1:101稀释,如可取15μl血清用1.5ml样本缓冲液稀释并用漩涡混匀器进行充分混匀,不可用加样器混匀。选择一款稳定、高效的漩涡混匀器备显重要。化验室样品处理量大,选择一款快捷、省力的漩涡混匀器十分必要。意大利VELP推出了创新性红外感应漩涡混匀器,红外传感是VELP创新性的专利产品。VELP红外感应漩涡混匀器,一旦检测到试管,VELP漩涡混匀器自动开始震动,不需要施加任何外力,而且相比于传统的接触模式,VELP红外传感漩涡混匀器能确保在震动减少过程的急剧变化。VELP漩涡混匀器确保了样品的稳定性。VELP漩涡混匀器最大转速可以达到3000rpm,VELP漩涡混匀器可以满足大部分实验室的需求。VELP漩涡混匀器在实验中解放您的双手,让实验更快捷、更准确!
[font=宋体][font=宋体]抗体已成为治疗和诊断人类疾病的有效工具。非人源抗体会诱导人类免疫反应,使用非人源抗体产生的中和反应会限制此类抗体在治疗人类疾病的应用。为了克服这个问题,抗体人源化技术应运而生。抗体人源化经历了从嵌合抗体到[/font][font=Calibri]CDR[/font][font=宋体]移植、[/font][font=Calibri]SDR[/font][font=宋体]移植等技术演变,力求在保持高亲和力、高特异性结合能力的同时克服传统鼠源抗体的免疫原性。[/font][/font][font=宋体] [/font][font=宋体][b]现阶段,常用抗体人源化方法包括以下几种:[/b][/font][font=宋体] [/font][font=宋体][font=宋体]①基于框架区同源性的[/font][font=Calibri]CDR[/font][font=宋体]移植与回复突变[/font][/font][font=宋体] [/font][font=宋体][font=宋体]非人源化抗体人源化的常用方法是互补决定区([/font][font=Calibri]CDR[/font][font=宋体])移植,即非人源抗体的[/font][font=Calibri]CDR[/font][font=宋体]区移植到人源抗体框架区上。通常,会选择与非人源抗体框架区同源性最高的人源抗体框架区作为[/font][font=Calibri]CDR[/font][font=宋体]移植的受体。这种方法最主要问题是与特定靶标结合的亲和力会降低乃至丧失。将小鼠抗体的[/font][font=Calibri]CDR[/font][font=宋体]环直接移植到人源抗体框架上在某些情况下不会影响抗体亲和力,然而在多数情况下,它会显著降低亲和力。鼠源抗体框架区的一些残基已被证明会影响[/font][font=Calibri]CDR[/font][font=宋体]环的构象以及抗体的亲和力,我们称其为游标区残基。这些残基位于靠近[/font][font=Calibri]CDR[/font][font=宋体]区的β折叠。因此,在选择所需的人源抗体框架区后,需要对这些残基进行回复突变,使其保留在人源化抗体中。除此之外,可变区外氨基酸残基的突变也已被用于赋予人源化抗体新的特性。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]②基于胚系基因的[/font][font=Calibri]CDR[/font][font=宋体]移植[/font][/font][font=宋体] [/font][font=宋体][font=宋体]人类胚系基因可作为鼠源抗体人源化框架区的替代来源。与来源于[/font][font=Calibri]IgG[/font][font=宋体]的框架区相比,胚系基因具有较少的克隆内体细胞超突变。因此,人们认为利用胚系框架的人源化抗体比[/font][font=Calibri]IgG[/font][font=宋体]框架的人源化抗体表现出更低的免疫原性。尽管胚系基因的免疫原性可能较低,但事实上[/font][font=Calibri]IgG[/font][font=宋体]的衍生框架有时更有利。复数研究反映,人源化抗体[/font][font=Calibri]Fc[/font][font=宋体]区的变化会影响抗体活性与亲和力。如有研究证实,将鼠抗可变区融合到[/font][font=Calibri]IgG[/font][font=宋体]恒定区构建的嵌合抗体对黄热病感染的预防和治疗有效,而具有[/font][font=Calibri]IgM[/font][font=宋体]恒定区的嵌合抗体则不然。[/font][/font][font=宋体] [/font][font=宋体]③抗体表面重塑[/font][font=宋体] [/font][font=宋体]抗体表面重塑是非人源抗体人源化的另一种策略。表面重塑是指对非人源抗体的表面氨基酸残基进行抗体人源化改造。该策略的原则是确定鼠源抗体表面残基的位置,在维持抗体活性并兼顾减少抗体免疫原性的基础上,选用与人源抗体表面残基相似的氨基酸进行替换。通过这种方法人源化的抗体通常表现出稳定性和亲和力的变化很小。[/font][font=宋体] [/font][font=宋体][font=宋体]④基于[/font][font=Calibri]CDR[/font][font=宋体]同源性的[/font][font=Calibri]CDR[/font][font=宋体]移植[/font][/font][font=宋体] [/font][font=宋体][font=宋体]以往的[/font][font=Calibri]CDR[/font][font=宋体]移植通常会选择与非人源抗体框架区同源性最高的人源抗体框架区作为[/font][font=Calibri]CDR[/font][font=宋体]移植的受体。[/font][font=Calibri]Hwang[/font][font=宋体]及其同事首次设计了一种基于[/font][font=Calibri]CDR[/font][font=宋体]区域同源性的抗体人源化新方法。该方法不使用框架区的同源性来选择人源化抗体框架,关键的鼠源残基也不进行回复突变。使用这种方法可以减少被识别为外源物质的可能性。比起基于框架区同源性的[/font][font=Calibri]CDR[/font][font=宋体]移植,通过该方法改造的抗体亲和力维持更好。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]⑤[/font][font=Calibri]SDR[/font][font=宋体]移植[/font][/font][font=宋体] [/font][font=宋体][font=宋体]通过[/font][font=Calibri]CDR[/font][font=宋体]移植获得的人源化抗体仍可能在患者中引发免疫性抗独特型([/font][font=Calibri]anti-Id[/font][font=宋体])反应。为了最大限度地减少抗[/font][font=Calibri]V[/font][font=宋体]区免疫反应,可以通过仅将[/font][font=Calibri]CDR[/font][font=宋体]序列中抗原结合活性所必需的特异性决定残基([/font][font=Calibri]SDR[/font][font=宋体])移植到人源抗体框架区上来实现抗体人源化。[/font][font=Calibri]SDR[/font][font=宋体]移植的方法更进一步地提升了抗体人源化程度,并尽可能地减少了鼠源[/font][font=Calibri]CDR[/font][font=宋体]中效应[/font][font=Calibri]T[/font][font=宋体]细胞表位的数量,从而将抗体可变区潜在的免疫原性风险做到最小化。[/font][/font][font=宋体] [/font][font=宋体]⑥其他抗体人源化方法[/font][font=宋体] [/font][font=宋体][font=宋体]定向筛选或链替换抗体库技术,是利用噬菌体展示的方法,将鼠源抗体重轻链[/font][font=Calibri]V[/font][font=宋体]区结构域分别顺序或平行地替换为人源化的。该方法为人源化提供了一个强大的工具,可以最大限度地减少人体的免疫原性。值得注意的是,通过噬菌体展示技术产生人源化抗体,即使是全人源抗体,也无法消除全部的免疫原性。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州利用[/font][font=Calibri]CDR[/font][font=宋体]置换技术及计算机辅助结构模拟设计可对羊驼纳米抗体、鼠源单抗进行人源化改造,保证人源化程度 [/font][font=Calibri]95%[/font][font=宋体],为客户提供优质的单克隆[url=https://cn.sinobiological.com/services/antibody-humanization-service][b]抗体人源化服务[/b][/url]。更多抗体人源化改造详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/antibody-humanization-service[/font][/font]
[font=宋体][font=宋体]目前,用细胞工程制备人单抗在技术上和伦理上都存在一些难题,治疗性抗体的开发就集中在具有治疗前景的鼠源单抗上。但是鼠源单抗对人体具有异源性反应,可诱发人抗鼠抗体效应[/font][font=Calibri](Humananti-mouseantibodies,HAMA[/font][font=宋体]反应[/font][font=Calibri])[/font][font=宋体],使得单抗的治疗效果明显滞后。随着基因重组技术的发展和人们对抗体结构认识的深入,研究者们尝试对鼠源性抗体进行改造,致力于在保留与抗原结合的高亲和力的基础上,减少异源性抗体的免疫原性,推动抗体人源化研发的进程。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]人源化抗体主要指以用基因克隆及[/font][font=Calibri]DNA[/font][font=宋体]重组技术对鼠源单克隆抗体改造,重新表达产生的抗体。其大部分氨基酸序列被人源序列取代,基本保留亲本鼠单克隆抗体的亲和力和特异性,又降低了其异源性,有利应用于人体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]根据人源化程度不同,单抗又可分为[url=https://cn.sinobiological.com/resource/antibody-technical/chimeric-monoclonal-antibody][b]嵌合抗体[/b][/url][/font][font=Calibri](60%-70%[/font][font=宋体]人源化氨基酸序列[/font][font=Calibri])[/font][font=宋体]和[/font][font=Calibri]CDR(complementarity-determiningregion)[/font][font=宋体]移植抗体[/font][font=Calibri](90%-95%[/font][font=宋体]人源化氨基酸序列[/font][font=Calibri])[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]1[/font][font=宋体]、人[/font][font=Calibri]-[/font][font=宋体]鼠嵌合抗体:[/font][/b][/font][font=宋体][font=宋体]人[/font][font=Calibri]-[/font][font=宋体]鼠嵌合抗体[/font][font=Calibri](chimericantibody)[/font][font=宋体]:第一代人源化抗体。其是在基因水平上将鼠源单克隆抗体的[/font][font=Calibri]V[/font][font=宋体]区和人抗体的[/font][font=Calibri]C[/font][font=宋体]区[/font][font=Calibri](variableregion,[/font][font=宋体]可变区[/font][font=Calibri])[/font][font=宋体]连接,在合适的宿主细胞内表达可得到人[/font][font=Calibri]-[/font][font=宋体]鼠嵌合抗体。嵌合抗体用于人体所产生的[/font][font=Calibri]HAMA[/font][font=宋体]反应比鼠源单抗明显减弱[/font][font=Calibri] [/font][font=宋体]另外,人源[/font][font=Calibri]C[/font][font=宋体]区[/font][font=Calibri](constantregion[/font][font=宋体],恒定区[/font][font=Calibri])[/font][font=宋体]可更有效地介导人体一些免疫反应,如[/font][font=Calibri]CDC(complement-dependentcytotoxicity,CDC,[/font][font=宋体]依赖补体的细胞毒性作用[/font][font=Calibri])[/font][font=宋体],[/font][font=Calibri]ADCC(antibodydependentcellmediatedcytotoxicity,[/font][font=宋体]抗体依赖的细胞介导的细胞毒性作用[/font][font=Calibri])[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]2[/font][font=宋体]、[/font][font=Calibri]CDR[/font][font=宋体]移植抗体[/font][/b][/font][font=宋体][font=宋体]嵌合抗体虽然可以部分解决异种蛋白的排斥问题,但由于其还含有鼠源[/font][font=Calibri]V[/font][font=宋体]区,依然有可能会诱发[/font][font=Calibri]HAMA[/font][font=宋体]反应,干扰抗体疗效,诱发超敏反应,在临床上其应用会受到一定限制。因此人们进一步研究鼠源可变区的改造,研发出了[/font][font=Calibri]CDR[/font][font=宋体]移植的人源化抗体,即第二代人源化抗体也是现在普遍所说的人源化抗体[/font][font=Calibri](humanizedantibody)[/font][font=宋体]。[/font][/font][font=宋体][font=Calibri]CDR[/font][font=宋体]移植抗体是研究者们在嵌合抗体的基础上进一步用人源框架区[/font][font=Calibri](Frameworkregion,FR)[/font][font=宋体]替代鼠源框架区[/font][font=Calibri](FR)[/font][font=宋体],仅保留了[/font][font=Calibri]3[/font][font=宋体]个鼠源性[/font][font=Calibri]CDR[/font][font=宋体],其他全部为人源结构,人源性可达[/font][font=Calibri]90%[/font][font=宋体]以上。但对于特定的抗原分子,[/font][font=Calibri]FR[/font][font=宋体]并不能随意替换。多方面研究均证实,具有支持作用的[/font][font=Calibri]FR[/font][font=宋体]不仅为[/font][font=Calibri]CDR[/font][font=宋体]的构象提供了环境,有时还参与抗体结合。因此简单的[/font][font=Calibri]CDR[/font][font=宋体]移植往往明显降低抗原[/font][font=Calibri]-[/font][font=宋体]抗体结合的亲和力,甚至是丧失抗原抗体结合的能力。[/font][/font][font=宋体] [/font][font=宋体]针对这种状况,目前主要有四种策略:[/font][font=宋体][font=宋体]①同源替换,使用与鼠源对应部分具有较大同源性的[/font][font=Calibri]FR[/font][font=宋体]进行替换[/font][font=Calibri] [/font][/font][font=宋体][font=宋体]②表面重塑,对鼠源[/font][font=Calibri]CDR[/font][font=宋体]和[/font][font=Calibri]FR[/font][font=宋体]表面氨基酸残基进行重塑,以使其类似于人抗体[/font][font=Calibri]CDR[/font][font=宋体]的轮廓或者[/font][font=Calibri]FR[/font][font=宋体]型式[/font][font=Calibri] [/font][/font][font=宋体][font=宋体]③补偿变化,改编关键位置氨基酸残基,以补偿完全的[/font][font=Calibri]CDR[/font][font=宋体]移植[/font][font=Calibri] [/font][/font][font=宋体][font=宋体]④定位保守,人源化单抗以[/font][font=Calibri]FR[/font][font=宋体]保守序列为模板进行人源化,但保留鼠源单抗可变区的关键氨基酸残基。[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]3[/font][font=宋体]、全人源抗体[/font][/b][/font][font=宋体][font=宋体]为了彻底消除异源性抗体的不良影响,[/font][font=Calibri]90[/font][font=宋体]年代以后,人们将噬菌体展示技术应用到抗体的表达和克隆上,产生了噬菌体抗体库技术。由此,抗体工程技术进入到了一个新的发展阶段,全人源化抗体的生产和应用也逐渐走向成熟。[/font][/font][font=宋体][font=宋体]全人源化抗体是指将人类抗体基因通过转基因或转染色体技术,将人类编码抗体的基因全部转移至基因工程改造的抗体基因缺失动物中,使动物表达人类抗体,达到抗体全人源化的目的。目前已建立多种方法生产完全人源性抗体,主要有噬菌体展示技术、转基因小鼠技术、核糖体展示技术和[/font][font=Calibri]RNA-[/font][font=宋体]多肽技术。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]人源化抗体的应用[/b][/font][font=宋体]目前,人源化抗体在肿瘤,器官移植排斥反应,病毒感染,血液性疾病,自身免疫性疾病等方面的治疗和临床诊断中显示出越来越大的应用前景。[/font][font=宋体][font=Calibri]1[/font][font=宋体]、在肿瘤治疗中的应用[/font][/font][font=宋体]近年来,兴起的分子靶向治疗,是根本意义上的肿瘤特异性治疗手段,是以肿瘤抗原特异性结合的单抗为载体,连接放射性核素,化疗药物等对肿瘤有杀伤作用的负载而成的抗体导向疗法。其靶向性好,毒性小等特点,非常适合肿瘤的内放射治疗。采用该技术用于临床的人源性抗体有治疗转移性乳腺癌的赫赛汀,用于治疗结直肠癌的西妥昔单抗等。[/font][font=宋体][font=Calibri]2[/font][font=宋体]、自身免疫性疾病治疗[/font][/font][font=宋体]自身免疫疾病多于自身抗体异常增多有关。很多临床研究发现,一些具有免疫疾病的病毒感染患者,体内病毒水平常伴随某些免疫分子水平的升高而升高,因此很多免疫分子的人源化抗体在此类病毒的治疗中显示出很好的效果。[/font][font=宋体][font=Calibri]3[/font][font=宋体]、病毒感染中的应用[/font][/font][font=宋体]病毒感染几乎无特效药,现有的核苷酸类抗病毒药物效果并不理想,且毒副作用大,单抗治疗因其针对性强,和相对比较安全,已越来越多研究者将其应用于抗病毒的治疗中。[/font][font=宋体] [/font][font=宋体][font=宋体]目前义翘神州提供[url=https://cn.sinobiological.com/services/antibody-humanization-service][b]抗体人源化服务[/b][/url],详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/antibody-humanization-service[/font][/font]
[font=宋体]在生物学和医学领域,抗原与抗体之间的结合反应是极为重要且复杂的过程。这种反应不仅关乎免疫系统的正常运作,而且在诊断、治疗等多个领域具有广泛的应用。本文将详细探讨抗原抗体结合反应的原理及其背后的生物学意义。[/font][font=宋体] [/font][font=宋体]一、抗原与抗体的基本概念[/font][font=宋体] [/font][font=宋体]抗原,通常是指能够刺激机体产生特异性免疫应答的物质。它们可能是外来的微生物、毒素,也可能是机体自身的异常成分。抗体,则是免疫系统在受到抗原刺激后产生的特异性免疫球蛋白,能够与抗原发生特异性结合。[/font][font=宋体] [/font][font=宋体]二、抗原抗体结合的结构基础[/font][font=宋体] [/font][font=宋体]抗原抗体之间的结合,依赖于它们分子间的结构互补性和亲和性。这种互补性主要源于抗原的表位和抗体的结合部位之间的匹配。抗原的表位,即其表面能够与抗体结合的区域,通常是特定的化学基团或空间构象。而抗体的结合部位,即其能够与抗原结合的区域,由重链和轻链上的可变区组成,形成了特定的空间结构,能够与抗原表位进行精确的结合。[/font][font=宋体] [/font][font=宋体]三、抗原抗体结合的动力学过程[/font][font=宋体] [/font][font=宋体]抗原抗体结合反应通常可以分为两个阶段。第一阶段是抗原与抗体发生特异性结合的阶段,此阶段反应速度极快,仅需几秒钟即可完成。这是因为抗原抗体之间的结合是高度特异性的,一旦找到合适的配对,它们会迅速结合形成抗原抗体复合物。第二阶段是可见反应阶段,此时抗原抗体复合物在环境因素的影响下,进一步交联和聚集,表现为凝集、沉淀、溶解等肉眼可见的反应。这一阶段的反应速度较慢,往往需要数分钟至数小时。[/font][font=宋体] [/font][font=宋体]四、抗原抗体结合反应的意义[/font][font=宋体] [/font][font=宋体]抗原抗体结合反应在生物学和医学领域具有广泛的应用。在免疫学中,它是机体免疫系统识别和清除外来抗原的基础。在医学诊断中,利用抗原抗体反应可以进行疾病的快速、准确诊断。例如,利用单克隆抗体技术可以检测乙型肝炎等病毒。此外,抗原抗体反应还被广泛应用于治疗领域,如利用载药单克隆抗体进行肿瘤的靶向治疗等。[/font][font=宋体] [/font][font=宋体]五、总结[/font][font=宋体] [/font][font=宋体]抗原抗体结合反应是生物学和医学领域的重要反应之一,其原理涉及到分子间的结构互补性和亲和性、反应动力学等多个方面。对这一反应的研究不仅有助于我们深入理解免疫系统的运作机制,也为疾病的诊断和治疗提供了新的方法和手段。[/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以查看义翘神州[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function][b]抗体的结构和功能[/b][/url]:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-structure-function[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b][font=Calibri] [/font]
该如何选择健康体检项目?目前健康体检项目很多,人们应根据自己家庭病史、年龄、性别、身体状况等方面,有针对性地选择体检“套餐”。1、一般人群常规检查 对于身体没有症状、工作压力不太大以及生活、作息、饮食较为规律的中青年人,只需接受常规性体检即可。主要体检项目包括:内科、外科、胸部透视、腹部B超、心电图和化验血、尿常规以及肝肾功能、血脂两项、血糖等。2、白领筛查“亚健康” 公司白领、从事脑力劳动强度较高的机关工作人员,因工作压力大、生活节奏快,并且作息不规律、应酬多、平时锻炼时间少,多坐少动,身体不同程度地存在“亚健康”状态,甚至有人已经患有高血压、脂肪肝等常见病。所以,建议这一人群在接受上述常规体检的基础上,再增加乙肝六项、血脂全项、血尿酸、胸部拍片和五官科、口腔科等项目;40岁以上人群应加查肛门指诊,以及早发现直肠肿物;中年女性还应增加妇科、宫颈涂片检验、乳腺扫描、B超检查。3、老年人体检应全面 高血压、冠心病、糖尿病、恶性肿瘤以及慢性呼吸道疾病等是老年人的常见病,并且由于老年人各脏器功能减退,对躯体疼痛、发热等症状反应迟钝,极易因延误治疗而损伤脏器功能。老年人定期体检有利于早期发现病情,应把内科、神经内科作为必查项目,同时接受B超、心电图、经颅多普勒、脑电图、眼底照相,以及血尿常规、血糖、血流变和肝、肾功能检查,然后再根据医生临床观察,视情增加CT等相关检查项目。此外,老年男性还应检查前列腺,老年女性应增加妇科检查及宫颈涂片检测。
[b][font=宋体]一、引言[/font][/b][font=宋体] [/font][font=宋体]荧光标记技术是生物学和医学领域中常用的可视化技术,其中荧光标记抗体凭借其独特的应用优势,在许多研究方向中发挥了重要作用。本文将详细介绍荧光标记抗体的原理、应用及最新进展。[/font][font=宋体] [/font][b][font=宋体]二、荧光标记抗体的原理[/font][/b][font=宋体] [/font][font=宋体]荧光标记技术是一种利用荧光物质对目标进行标记,通过特定波长的光激发后发出荧光,从而实现可视化检测的方法。荧光标记抗体则是将荧光物质与特异性抗体结合,形成荧光标记抗体,用于对目标抗原进行特异性结合和荧光标记。常见的荧光物质有荧光素、量子点、上转换纳米颗粒等。[/font][b][font=宋体] [/font][font=宋体]三、荧光标记抗体的应用[/font][/b][font=宋体] [/font][font=宋体][font=宋体]免疫分析:荧光标记抗体在免疫分析中具有广泛的应用,如酶联免疫吸附试验([/font][font=Calibri]ELISA[/font][font=宋体])、流式细胞术、免疫荧光染色等。通过荧光标记抗体与抗原的特异性结合,可以实现对目标抗原的高灵敏度、高特异性检测。例如,利用荧光标记抗体检测肿瘤标志物,有助于肿瘤的早期诊断和治疗监测。[/font][/font][font=宋体]细胞成像:荧光标记抗体在细胞成像中具有重要作用,可以用于观察细胞内特定抗原的表达情况,了解细胞的功能和行为。例如,利用荧光标记抗体对细胞膜抗原进行标记,可以观察细胞迁移、侵袭等行为。[/font][font=宋体]组织切片染色:荧光标记抗体也可用于组织切片染色,对病理组织中的特定抗原进行标记,有助于病理诊断和组织学研究。例如,利用荧光标记抗体对肿瘤组织进行染色,有助于肿瘤类型的鉴别和恶性程度的评估。[/font][font=宋体]药物筛选:荧光标记抗体在药物筛选中具有重要应用,可以用于药物作用靶点的检测和药物作用机制的研究。例如,利用荧光标记抗体对药物作用靶点进行标记,可以观察药物对靶点的影响,评估药物的疗效和安全性。[/font][font=宋体] [/font][b][font=宋体]四、展望[/font][/b][font=宋体] [/font][font=宋体]随着荧光标记技术的不断发展,荧光标记抗体在灵敏度、特异性和可视化效果等方面得到了显著提升。同时,新型荧光物质的开发和制备也为荧光标记抗体的应用提供了更多选择。未来,随着荧光标记技术的进一步优化和多色荧光标记技术的发展,荧光标记抗体将在更多领域发挥重要作用,为生物学、医学和其他相关领域的研究提供有力支持。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/immunofluorescence-service][b]免疫荧光检测服务[/b][/url]:[/font][font=Calibri]https://cn.sinobiological.com/services/immunofluorescence-service[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体][font=Calibri]EB[/font][font=宋体]病毒衣壳抗原[/font][font=Calibri]IGG[/font][font=宋体]高可能是有过感染史或者现症感染,还需综合其他数据分析。[/font][/font][font=宋体][font=Calibri]EB[/font][font=宋体]病毒是一种很常见的疱疹病毒,多见于不明原因发烧患者,[/font][font=Calibri]EB[/font][font=宋体]病毒衣壳抗原可刺激人体产生两种抗体,一种是[/font][font=Calibri]IGG[/font][font=宋体],还有一种是[/font][font=Calibri]IGM[/font][font=宋体]。一般如果只是[/font][font=Calibri]EB[/font][font=宋体]病毒衣壳抗原[/font][font=Calibri]IGG[/font][font=宋体]指标上升,[/font][font=Calibri]IGM[/font][font=宋体]保持在正常范围内,则表示患者有过[/font][font=Calibri]EB[/font][font=宋体]病毒感染病史,现已康复 ;如[/font][font=Calibri]EB[/font][font=宋体]病毒衣壳抗原[/font][font=Calibri]IGG[/font][font=宋体]、[/font][font=Calibri]IMG[/font][font=宋体]都处于升高范围,则表示患者近期感染[/font][font=Calibri]EB[/font][font=宋体]病毒,可能还会伴随有发热、淋巴结肿大、皮疹等症状表现。下面对几个常见概念进行科普:[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]1[/font][font=宋体]、[/font][font=Calibri]igG[/font][font=宋体]阳性[/font][/b][/font][font=宋体][font=Calibri]igG[/font][font=宋体]阳性并不是[/font][font=Calibri]EB[/font][font=宋体]病毒检测专有的检测,如单纯疱疹病毒、风疹病毒等多种疾病,都需要进行[/font][font=Calibri]igG[/font][font=宋体]的检测。[/font][/font][font=宋体][font=宋体]当病原体等感染机体后,免疫系统会产生[/font][font=Calibri]igM[/font][font=宋体]与[/font][font=Calibri]igG[/font][font=宋体]等不同的抗体。[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]2[/font][font=宋体]、[/font][font=Calibri]igM[/font][font=宋体]抗体:[/font][/b][/font][font=宋体] [/font][font=宋体][font=宋体]免疫应答中首先分泌的具有保护性的抗体;一般在机体收到感染时快速产生,经过一段时间[/font][font=Calibri]igM[/font][font=宋体]抗体量逐渐减少而消失;[/font][/font][font=宋体][font=宋体]所以检测[/font][font=Calibri]igM[/font][font=宋体]抗体阳性,在临床上是提示为目前体内存在感染的情况。[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]3[/font][font=宋体]、[/font][font=Calibri]igG[/font][font=宋体]抗体:[/font][/b][/font][font=宋体] [/font][font=宋体][font=宋体]当[/font][font=Calibri]igM[/font][font=宋体]抗体出现后,随后会出现[/font][font=Calibri]igG[/font][font=宋体]抗体;但[/font][font=Calibri]igG[/font][font=宋体]抗体在机体内持续的时间会比较长;[/font][/font][font=宋体][font=宋体]所以检测[/font][font=Calibri]igG[/font][font=宋体]抗体检测阳性,在临床上是提示患者存在既往感染等的情况。[/font][/font][font=宋体] [/font][font=宋体][b][font=Calibri]4[/font][font=宋体]、[/font][font=Calibri]EB[/font][font=宋体]病毒[/font][/b][/font][font=宋体][font=Calibri]EB[/font][font=宋体]病毒[/font][font=Calibri](EBV)[/font][font=宋体]是一种嗜人类淋巴细胞的疱疹病毒[/font][font=Calibri],[/font][font=宋体]又称人类疱疹病毒[/font][font=Calibri]4(HHV-4)[/font][font=宋体];主要通过唾液等传染,是传染性单核细胞增多症的病原体;因[/font][font=Calibri]EBV[/font][font=宋体]一旦入侵机体,可能会对[/font][font=Calibri]B[/font][font=宋体]细胞进行诱导,使其转化为恶性肿瘤细胞,所以[/font][font=Calibri]EBV[/font][font=宋体]感染与鼻咽癌、胃癌、淋巴瘤等疾病的发生、发展有密切关系。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]EBV[/font][font=宋体]编码多种结构抗原,如病毒衣壳抗原([/font][font=Calibri]VCA[/font][font=宋体])、早期抗原([/font][font=Calibri]EA[/font][font=宋体])、膜抗原([/font][font=Calibri]MA[/font][font=宋体])、核抗原([/font][font=Calibri]NA[/font][font=宋体])等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]在机体感染[/font][font=Calibri]EBV[/font][font=宋体]后针对不同的抗原会产生相应的抗体,如抗[/font][font=Calibri]VCA[/font][font=宋体]—[/font][font=Calibri]igG[/font][font=宋体]、抗[/font][font=Calibri]VCA[/font][font=宋体]—[/font][font=Calibri]igG[/font][font=宋体]、抗 [/font][font=Calibri]EBNA[/font][font=宋体]—[/font][font=Calibri]igG[/font][font=宋体]等。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]通过对这些[/font][font=Calibri]EBV[/font][font=宋体]特异性抗体进行检测,可以明确目前机体的情况,如对帮助判断是否是原发性[/font][font=Calibri]EBV[/font][font=宋体]感染、或是既往感染等的情况。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]EB[/font][font=宋体]病毒衣壳抗原[/font][font=Calibri](igG)[/font][font=宋体]、抗[/font][font=Calibri]EBV[/font][font=宋体]核抗原[/font][font=Calibri](EBVNA[/font][font=宋体]一[/font][font=Calibri]igG)[/font][font=宋体]呈阳性,即提示存在既往有[/font][font=Calibri]EB[/font][font=宋体]病毒感染,但要明确目前的身体的情况,需要配合[/font][font=Calibri],igM[/font][font=宋体]等其他的结果分析,以明确后续的方向。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]目前利用[url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]细胞分选平台[/b][/url],义翘神州可向全球客户提供[url=https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology][b]细胞抗体制备服务[/b][/url],整个过程涉及单[/font][font=Calibri]B[/font][font=宋体]细胞分离、测序、克隆和单[/font][font=Calibri]B[/font][font=宋体]细胞抗体筛选等步骤。详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology[/font][/font][b][font=宋体] [/font][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体][font=宋体]抗独特型抗体是一种能够特异性结合另一抗体独特位的抗体。独特型由多个抗原决定簇([/font][font=Calibri]Antigenic determinant[/font][font=宋体])组成,每个抗原决定簇都是一个独特位。抗原决定簇或独特位可存在于重链可变区,也可存在于轻链可变区,或者存在于两条链组成的表面。[/font][/font][font=宋体] [/font][font=宋体][b]抗独特型抗体三种类型:[/b][/font][font=宋体] [/font][font=宋体]①抗原非中和型[/font][font=宋体]不具有抗体结合区特异性,治疗性抗体仍可与其目标抗原相结合。这种类型的抗独特型抗体可用于检测抗体药物总量。[/font][font=宋体]②抗原中和型[/font][font=宋体]具有抗体结合区特异性,与其目标抗原相互竞争,因此,此类型可用于检测游离型抗体药物。[/font][font=宋体]③药物靶标复合物型[/font][font=宋体][font=宋体]仅特异性地识别抗体[/font][font=Calibri]-[/font][font=宋体]靶标复合物,不与未结合的抗体或未结合的目标抗原相结合。这种类型的抗独特型抗体仅能检测结合型抗体药物。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]抗独特型抗体的不同应用[/b][/font][font=宋体]①免疫原性分析[/font][font=宋体][font=宋体]免疫原性分析对于生物药物开发具有重要的意义。几乎所有的生物制药产品(如蛋白、抗体、多肽偶联药物或寡核苷酸等)都会诱导机体内免疫应答,从而导致抗药抗体([/font][font=Calibri]ADA[/font][font=宋体])的产生。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗独特型抗体属于高度特异性[/font][font=Calibri]ADA[/font][font=宋体]。多克隆抗体能较大限度地模拟血样中的真实情况,还具有制备周期较短和成本低的优势。因此,大多数情况下,在分析患者样本中是否存在[/font][font=Calibri]ADA[/font][font=宋体]时,抗独特型多克隆抗体通常用作阳性对照。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]②药代动力学([/font][font=Calibri]PK[/font][font=宋体])分析[/font][/font][font=宋体][font=宋体]抗独特型抗体也是药代动力学([/font][font=Calibri]PK[/font][font=宋体])分析的关键工具试剂之一。 在临床前研究和临床研究中,[/font][font=Calibri]PK[/font][font=宋体]分析可用于评估抗体药物的用药剂量和毒性。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗独特型单克隆抗体特异性强,可作为[/font][font=Calibri]PK[/font][font=宋体]分析的检测试剂,用于检测人或动物血清中的抗体药物含量。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/anti-idiotype-antibody-service][b]抗独特型抗体制备服务[/b][/url],同时拥有综合性的抗独特型抗体开发平台,涵盖兔多抗、杂交瘤、噬菌体、流式单[/font][font=Calibri]B[/font][font=宋体]细胞和[/font][font=Calibri]Beacon[/font][font=宋体]单[/font][font=Calibri]B[/font][font=宋体]细胞技术,为客户提供更多选择。详情可以关注抗独特型抗体制备服务[/font][font=Calibri]https://cn.sinobiological.com/services/anti-idiotype-antibody-service[/font][/font]
[font=宋体][font=宋体]第一代人源化抗体是通过将鼠源[/font][font=Calibri]McAb[/font][font=宋体]的可变区与人抗体的恒定区相结合,形成了一种[url=https://cn.sinobiological.com/resource/antibody-technical/chimeric-monoclonal-antibody][b]嵌合抗体[/b][/url]。尽管这两部分在空间结构上相对独立,使得其独特的抗原亲和力得以保持,但由于嵌合抗体中仍然包含鼠源[/font][font=Calibri]McAb[/font][font=宋体]的可变区,因此在应用时仍可能引发强烈的[/font][font=Calibri]HAMA[/font][font=宋体]反应。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]为了克服这一问题,科学家们进一步进行了改进,将鼠源[/font][font=Calibri]McAb[/font][font=宋体]可变区中的相对保守的骨架区([/font][font=Calibri]Framework region, FR[/font][font=宋体])替换为人的[/font][font=Calibri]FR[/font][font=宋体],而仅保留抗原结合部位的互补决定区([/font][font=Calibri]Complementarity-Determining region, CDR[/font][font=宋体])。这种改进使得抗体真正实现了人源化。然而,[/font][font=Calibri]FR[/font][font=宋体]作为抗体的脚手架,不仅为[/font][font=Calibri]CDR[/font][font=宋体]提供了空间构象环境,有时还参与抗体结合位点正确构象的形成,甚至与抗原的结合。因此,简单的[/font][font=Calibri]CDR[/font][font=宋体]移植往往会导致原抗体亲和力的丧失或降低。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]为了解决这一问题,目前科学家们已经探索出了四种策略,旨在优化[/font][font=Calibri]FR[/font][font=宋体]和[/font][font=Calibri]CDR[/font][font=宋体]之间的相互作用,以恢复或提高人源化抗体的亲和力。这些策略的实施将有助于进一步提升抗体人源化的效果,为医学研究和治疗提供更多的可能性。[/font][/font][font=宋体] [/font][b][font=宋体]人源化抗体构建原则与策略[/font][/b][font=宋体][font=Calibri]1.[/font][font=宋体]模板替换[/font][/font][font=宋体][font=宋体]在使用与鼠对应部分有较大同源性的人抗体[/font][font=Calibri]FR[/font][font=宋体]替换鼠[/font][font=Calibri]FR[/font][font=宋体]时,通常有两种途径可供选择。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]第一种途径是采用同一个(或少数几个)具有已知晶体结构数据的人源抗体可变区框架(如[/font][font=Calibri]VH[/font][font=宋体]中的[/font][font=Calibri]NEW[/font][font=宋体]、[/font][font=Calibri]KOL[/font][font=宋体],[/font][font=Calibri]VL[/font][font=宋体]中的[/font][font=Calibri]REI[/font][font=宋体]等)作为基本模板,通过序列比较与分子模建,确定人、鼠间存在种源差异的氨基酸残基,特别是与鼠[/font][font=Calibri]CDR[/font][font=宋体]密切作用的氨基酸残基,在替换过程中予以保留。为了确保[/font][font=Calibri]CDR[/font][font=宋体]的空间构象得以维持,需要特别关注原来抗体[/font][font=Calibri]CDR[/font][font=宋体]下方的堆积残基以及周围的残基。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]这种方法的优势在于,已知的人源[/font][font=Calibri]FR[/font][font=宋体]晶体结构为残基替换提供了明确的信息。然而,其不足之处在于可能难以保持鼠[/font][font=Calibri]CDR[/font][font=宋体]的天然构象,从而可能导致抗体亲和力的降低或丧失。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]第二条途径是在已有的抗体序列库中搜索与鼠[/font][font=Calibri]McAb FR[/font][font=宋体]具有最大同源性的人源[/font][font=Calibri]FR[/font][font=宋体]进行替换。在选择同源的人[/font][font=Calibri]FR[/font][font=宋体]时,早期的研究者倾向于将[/font][font=Calibri]VL[/font][font=宋体]和[/font][font=Calibri]VH[/font][font=宋体]作为一个整体来考虑,以寻找最高同源的人[/font][font=Calibri]FR[/font][font=宋体],理由是同一个抗体的[/font][font=Calibri]VL[/font][font=宋体]和[/font][font=Calibri]VH[/font][font=宋体]在折叠上更能匹配。然而,后来的研究者则认为将[/font][font=Calibri]VL[/font][font=宋体]和[/font][font=Calibri]VH[/font][font=宋体]分开考虑,分别寻找最高同源的对应序列,可以更好地保持[/font][font=Calibri]FR[/font][font=宋体]原来的框架,为鼠[/font][font=Calibri]CDR[/font][font=宋体]提供整体上最类似的环境。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]同源替换的主要考虑因素是确保鼠[/font][font=Calibri]CDR[/font][font=宋体]在此背景下具有类似的折叠环境,从而维持其原来的构象。同样需要借助分子模建来提供[/font][font=Calibri]CDR[/font][font=宋体]移植后可能缺失的[/font][font=Calibri]FR[/font][font=宋体]关键残基的信息。这种方法的优点在于能够减少需要更改的氨基酸数目,更好地保持[/font][font=Calibri]CDR[/font][font=宋体]所需的空间环境。然而,其不足之处在于选择的人源[/font][font=Calibri]FR[/font][font=宋体]可能并无结构数据可供参考,因此无法提供有效的关键残基信息。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]表面重塑[/font][/font][font=宋体][font=宋体]对鼠[/font][font=Calibri]CDR[/font][font=宋体]及[/font][font=Calibri]FR[/font][font=宋体]的表面残基进行镶饰([/font][font=Calibri]veneering[/font][font=宋体])或重塑([/font][font=Calibri]resurfacing[/font][font=宋体]),以使其轮廓([/font][font=Calibri]profile[/font][font=宋体])或型式([/font][font=Calibri]pattern[/font][font=宋体])更加类似于人抗体的[/font][font=Calibri]CDR[/font][font=宋体]或[/font][font=Calibri]FR[/font][font=宋体]。这一策略的前提是,鼠[/font][font=Calibri]McAb[/font][font=宋体]可变区的免疫原性主要源自其表面残基。由于残基的运动性和溶液可及性是成为抗原决定簇的关键因素,因此表面残基很可能携带全部或绝大部分的抗原表位。在定义溶液可及性表面残基时,我们采用的标准是:构成该残基的全部原子的[/font][font=Calibri]30%[/font][font=宋体]以上是溶剂可及的。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]尽管人、鼠间抗体可变区表面暴露残基的精确型式存在差别,但大多数表面位置的残基类别具有强烈的倾向性。仅仅考虑这种表面型式,我们就可以区分抗体可变区的不同组别。这表明抗体可变区的表面至少与框架区核心一样保守,而表面型式的差异则是人鼠间抗体的主要区别。根据对现有抗体晶体结构数据的分析结果统计,人、鼠间抗体可变区残基在序列配对位置上的相对溶剂可及性分布保真度高达[/font][font=Calibri]98%[/font][font=宋体]。这意味着在异种间诱导免疫反应的残基是由其余的种特异性溶液可及表面残基引起的。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]通过将鼠特异性表面残基替换为人源性的残基,我们可以模拟人源抗体的表面轮廓,从而逃避人体免疫系统的识别,达到人源化的目的。这种策略可以在不进行同源模建的情况下,基于序列同源分析,选择与鼠表面残基暴露类型最相匹配的人源型式进行。然而,需要注意的是,如果要改变的残基在侧链大小、电荷、疏水性或有可能形成氢键从而影响到[/font][font=Calibri]CDR[/font][font=宋体]的构象时,则不应进行改变。这是因为改变的残基较少,有助于减少[/font][font=Calibri]CDR-FR[/font][font=宋体]之间的不相容性。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]作为一种较新的人源化途径,该策略仍在逐步成熟阶段。关于鼠源[/font][font=Calibri]McAb[/font][font=宋体]在人体引起的[/font][font=Calibri]HAMA[/font][font=宋体]反应是否完全由其表面暴露残基引起,还是由表面残基与内部残基的共同贡献所致,这涉及到抗体产生最基本的免疫学机制,目前仍是研究的热点。通过深入探索这一策略,我们有望为抗体人源化提供更多有效的解决方案。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]补偿变换[/font][/font][font=宋体][font=宋体]在选择人[/font][font=Calibri]FR[/font][font=宋体]进行改变时,我们重点关注那些与[/font][font=Calibri]CDR[/font][font=宋体]有相互作用、与抗体的亲和力有密切关系或对[/font][font=Calibri]FR[/font][font=宋体]空间结构折叠起关键作用的残基。这些改变旨在补偿完全的[/font][font=Calibri]CDR[/font][font=宋体]移植可能带来的影响。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]根据立体结构数据和同源性分析,我们了解到在抗原结合、稳定[/font][font=Calibri]CDR[/font][font=宋体]构象和[/font][font=Calibri]FR[/font][font=宋体]折叠方面,构成抗体[/font][font=Calibri]FR[/font][font=宋体]的残基并不具有相同的重要性。基于这一点,我们可以将这些残基分为三类:低风险性残基,这些残基暴露于溶剂中,对抗原结合和抗体结构的贡献较少。替换这些位置的残基可以降低免疫原性,而几乎不影响抗体的亲和力;高风险性残基,这些残基直接参与抗原结合、稳定[/font][font=Calibri]CDR[/font][font=宋体]构象或[/font][font=Calibri]FR[/font][font=宋体]折叠。为了保持人源化抗体的活性,我们应尽量避免在这些位置进行替换;中度风险性残基,对于这类残基,我们需要谨慎处理。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]FR[/font][font=宋体]中的高风险性残基和某些中度风险性残基,统称为非[/font][font=Calibri]CDR[/font][font=宋体]区补充调控残基。它们分布于线性序列的不同位置,为每个[/font][font=Calibri]CDR[/font][font=宋体]回折提供了合适的“平台”。这些残基的形状和侧链大小协同决定了[/font][font=Calibri]CDR[/font][font=宋体]的基本构象,并影响其抗原结合的特异性。因此,在将[/font][font=Calibri]CDR[/font][font=宋体]移植到人源[/font][font=Calibri]FR[/font][font=宋体]后,我们必须将人[/font][font=Calibri]FR[/font][font=宋体]中的这些位置替换成鼠源非[/font][font=Calibri]CDR[/font][font=宋体]区补充调控残基,以补偿完全的[/font][font=Calibri]CDR[/font][font=宋体]移植带来的影响。[/font][/font][font=宋体] [/font][font=宋体]这种分析方法使我们能够制定具有选择性和针对性的人源化突变方案,避免了盲目的、可能导致失败的探索。此外,通过在中度风险性残基中进行变化,我们还有可能提高人源化抗体的亲和力。然而,需要注意的是,对残基的分类需要基于晶体数据和三维结构,以确保提供准确的标准。[/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]定位保留[/font][font=Calibri](positional consensus method)[/font][/font][font=宋体][font=宋体]人源化[/font][font=Calibri]McAb[/font][font=宋体]保留了鼠源[/font][font=Calibri]McAb[/font][font=宋体]可变区中参与抗原结合的关键氨基酸残基,这包括了[/font][font=Calibri]CDR[/font][font=宋体]以及[/font][font=Calibri]FR[/font][font=宋体]中的一些至关重要的残基。尽管我们可以将鼠框架区的其余部分从某个人[/font][font=Calibri]FR[/font][font=宋体]中移植过来,但无可避免的是,这样得到的人源化抗体序列与人抗体的保守序列([/font][font=Calibri]consensus sequences[/font][font=宋体])在某些位置上仍会存在差异。这些非典型残基,源自个体型抗体在亲和力成熟过程中的体细胞突变,应用于病人后可能会诱导免疫反应。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]因此,一个更为理想的途径是,以人[/font][font=Calibri]FR[/font][font=宋体]的保守序列为模板进行人源化设计。由于人抗体轻、重链可变区不同亚类的保守序列存在差异,我们需要寻找一种合适的方法来确定最适合的保守序列。最简位置模板([/font][font=Calibri]minimal positional template[/font][font=宋体])为我们提供了确定这些关键位置的方法,它揭示了抗体可变区中哪些位置对于维持抗原结合结构域的完整性是绝对必要的。[/font][/font][font=宋体] [/font][font=宋体]在选择人框架区时,我们首先会从现有的人源抗体保守序列中搜寻与鼠框架区最为类似的序列。接着,根据最简位置模板,我们确定鼠可变区的关键位置残基。最后,我们将保留所有这些关键位置,而将其余部分进行人源化改造。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]上述人源化的四种策略,均以保持抗体的亲和力为核心目标,以降低免疫原性为最终目的,各具特色。总的来说,抗体人源化设计的关键步骤包括:[/font][font=宋体] [/font][font=宋体][font=宋体]①从同源抗体或共同序列抗体中选择适合的人源[/font][font=Calibri]FR[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]②根据已发布的研究信息,确定[/font][font=Calibri]FR[/font][font=宋体]中起关键作用的氨基酸残基。[/font][/font][font=宋体][font=宋体]③以鼠[/font][font=Calibri]McAb[/font][font=宋体]可变区的立体模型为指导,进行精确的设计和改造。[/font][/font][font=宋体][font=宋体]在设计过程中,同源分析和分子模建提供了必要的辅助手段。尽管存在一些一般性原则,但在对某一具体的鼠[/font][font=Calibri]McAb[/font][font=宋体]进行人源化时,仍需进行具体的分析和调整。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以关注[url=https://cn.sinobiological.com/services/antibody-humanization-service][b]抗体人源化服务[/b][/url]:[/font][font=Calibri]https://cn.sinobiological.com/services/antibody-humanization-service[/font][/font][font=宋体][font=宋体]嵌合抗体:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/chimeric-monoclonal-antibody[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
[font=宋体][font=宋体]传统意义上,抗核抗体([/font][font=Calibri]antinuclear antibodies[/font][font=宋体],[/font][font=Calibri]ANA[/font][font=宋体])是所有抗细胞核抗原成分的自身抗体的总称,包括一大类抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]然而,随着[/font][font=Calibri]ANA[/font][font=宋体]检测技术的改进、尤其是培养细胞抗原基质(如[/font][font=Calibri]HEp-2[/font][font=宋体]细胞,即人喉癌上皮样细胞系)的广泛运用,[/font][font=Calibri]ANA[/font][font=宋体]针对的靶抗原成分已由细胞核扩展到整个细胞成分,包括细胞核、细胞浆、细胞骨架及细胞分裂周期蛋白等。目前对[/font][font=Calibri]ANA[/font][font=宋体]的定义为:以真核细胞的各种成分为靶抗原的自身抗体的总称。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]ANA[/font][font=宋体]的检测方法,目前国际及国内指南或共识推荐的均是间接免疫荧光法([/font][font=Calibri]indirect immunofluorescence[/font][font=宋体],[/font][font=Calibri]IIF[/font][font=宋体]),而且是以[/font][font=Calibri]HEp-2[/font][font=宋体]细胞为实验基质的[/font][font=Calibri]IIF[/font][font=宋体]。此外还有[/font][font=Calibri]ELISA[/font][font=宋体]、线性免疫印迹法、化学发光免疫分析法等,各有优缺点。瑞金医院检验科实验室、皮肤科实验室均采用[/font][font=Calibri]IIF[/font][font=宋体]法检测[/font][font=Calibri]ANA[/font][font=宋体]。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]IIF-ANA[/font][font=宋体]规范的结果报告内容应包括:检测方法、定性结果(阳性[/font][font=Calibri]/[/font][font=宋体]阴性)、荧光模型、滴度、临床建议。[/font][font=Calibri]IIF-ANA[/font][font=宋体]荧光模型分[/font][font=Calibri]3[/font][font=宋体]类:细胞核荧光模型([/font][font=Calibri]14[/font][font=宋体]种)、细胞浆荧光模型([/font][font=Calibri]9[/font][font=宋体]种)、细胞有丝分裂荧光模型([/font][font=Calibri]5[/font][font=宋体]种);国内共识建议必报的荧光模型有[/font][font=Calibri]13[/font][font=宋体]种,细胞核类的有均质型、斑点型(需区分致密斑点型)、着丝点型、核点型、核仁型、核膜型,细胞浆类的有胞浆纤维型、胞浆颗粒型、胞浆网状[/font][font=Calibri]/[/font][font=宋体]线粒体型、胞浆极型[/font][font=Calibri]/[/font][font=宋体]高尔基体型、胞浆棒状环状型、胞浆线性[/font][font=Calibri]/[/font][font=宋体]肌动蛋白型。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]抗核抗体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体阳性通常指的是抗核糖体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体阳性,它可能意味着身体存在结缔组织疾病,尤其是系统性红斑狼疮([/font][font=Calibri]SLE[/font][font=宋体])。[/font][/font][/b][font=宋体][font=宋体]包括类风湿关节炎、干燥综合征的患者等,阳性率并不是很高,特异性也不是很好。系统性红斑狼疮是一种自身免疫性疾病,可能会对皮肤黏膜、肝功能、中枢神经系统等造成损伤。抗核糖体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体对系统性红斑狼疮具有高度特异性,尤其是在伴有典型神经系统症状的中枢神经系统损害型红斑狼疮中,出现抗核糖体[/font][font=Calibri]P[/font][font=宋体]蛋白抗体阳性的几率比较高。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]所以出现抗体阳性后,一定要到医院请专科大夫来进行诊断,并来进行合理的解释,再进行其他实验室检查,包括血沉、[/font][font=Calibri]C[/font][font=宋体]反应蛋白 、血尿常规、肝肾功能、类风湿因子,以及相关其他,如[/font][font=Calibri]SM[/font][font=宋体]抗体、核小体抗体、[/font][font=Calibri]SSA[/font][font=宋体]抗体、[/font][font=Calibri]SSB[/font][font=宋体]抗体等自身抗体检查。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/platform/facs-b-cell-sorting][b]细胞分选平台[/b][/url],可向全球客户提供[url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]单[/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]B[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/single-b-cell-antibody-service][b]细胞抗体制备服务[/b][/url],整个过程涉及单[/font][font=Calibri]B[/font][font=宋体]细胞分离、测序、克隆和单[/font][font=Calibri]B[/font][font=宋体]细胞抗体筛选等步骤。更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/single-b-cell-technology[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]义翘神州:蛋白与抗体的专业引领者,欢迎通过百度搜索[/font][font=宋体]“义翘神州”与我们取得联系。[/font][/font][/b]
随着生命科学的发展,围绕蛋白进行的研究越来越多,抗体试剂在实验中的重要性越来越举足轻重。面临着纷呈复杂的抗体试剂市场,如何选择到适合自己实验的抗体就变得尤为重要。一、关于特异性的选择:特异性的选择主要需要考虑四个方面:蛋白特异性、种属特异性、实验方法特异性、标记物的特异性。1、蛋白特异性:针对需要检测的蛋白查找抗体,几个细节要区分,重组表达的蛋白和内源性蛋白的检测,对抗体的要求是不一样的,注意查看抗体说明书的检测说明。如果重组蛋白不是全长表达,则需要注意抗体的免疫原区域是否在重组蛋白区域内。内源性蛋白最好能清楚其剪切与修饰的方式,特殊表型的蛋白需要进行序列比对,并结合抗体免疫原序列,查看交叉反应的情况。磷酸化蛋白检测需要确定具体位点,不同位点的磷酸化意味着可能有不同的机制存在,不宜一概而论。2、种属特异性:同种蛋白不同物种,有着或大或小的差异。目前大部分商品化抗体都是以人源蛋白序列为模板重组蛋白或设计多肽抗原的,根据蛋白的同源性情况与其他种属发生交叉反应。需要参照说明书注明的可反应种属信息。一些稀有种属很难找到抗体,可以通过蛋白的序列比对,选择同源序列免疫的抗体,不过一般这种情况生产商不会受理其关于质量的申诉,如果可以申请到免费的抗体样品,则利于抗体选择。3、实验方法特异性:目前使用抗体的实验方法有很多,不同的使用方法过程中,因为对蛋白样品的处理方式不一样,蛋白的含量有差异,对抗体的识别表位和效价要求都是不一样的。具体的根据说明书注明的产品应用方法进行选择。但是生产商一般不会将每个抗体都进行各种实验的检测,目前检测比较多的只是WB、IHC、IF等,如果针对具体的实验方法没有找到合适的抗体的,可以结合蛋白序列分析和抗体的抗原信息,选择尽可能有效果的抗体。同样,申请到免费的抗体样品是个很好的途径。4、标记物的特异性一般基于实验操作的实验方法不会使用带有标记的一抗,比如WB、IHC等,都是通过二抗类的试剂标记达到结果呈现的目的。但是基于仪器分析的一些实验,可能就会使用到直接标记的一抗,比如流式实验。那么需要了解到自己将要使用的仪器能检测到的荧光范围,针对不通的参数要求选择对应的标记物。在免疫荧光双标实验中,需要选配不同的荧光标记物。
[font=宋体]在生物医学研究和治疗领域,[/font][url=https://cn.sinobiological.com/resource/antibody-technical/monoclonal-antibody-production][u][font=宋体][color=#0000ff][b][font=宋体]单克隆抗体([/font][font=Calibri]mAbs[/font][font=宋体])[/font][/b][/color][/font][/u][/url][font=宋体][font=宋体]扮演着越来越重要的角色。特别是在癌症和慢性疾病的治疗中,抗体的亲和力[/font][font=宋体]——即其与目标抗原结合的紧密程度[/font][/font][font=宋体],[/font][font=宋体]直接影响[/font][font=宋体]抗体药物的[/font][font=宋体]治疗效果。因此,开发一种既准确又可靠的抗体亲和力测定方法,对于提高治疗效率和开发新型抗体药物至关重要。[/font][b][font=宋体]传统[/font][font=宋体]的亲和力测定[/font][font=宋体]技术[/font][/b][font=宋体]目前存在多种测[/font][font=宋体]定[/font][font=宋体]抗体亲和力的方法,如放射免疫[/font][font=宋体]分析[/font][font=宋体][font=宋体]、表面等离子共振([/font][font=Calibri]SPR[/font][font=宋体])、流式细胞术[/font][/font][font=宋体]、酶联免疫吸附分析和动力学排阻分析[/font][font=宋体]等[/font][font=宋体]。作为一种成功的候选治疗药物,[/font][font=宋体][font=Calibri]mAbs[/font][font=宋体]必须能识别目标抗原上的天然表位,因此需要一种更加快速灵敏、直观简便的测定方法。[/font][/font][b][font=宋体]基于细胞的荧光法:一种新的[/font][font=宋体]检测[/font][font=宋体]技术[/font][/b][font=宋体][font=Calibri]Yu[/font][font=宋体]等人在杜克大学医学中心的研究中,开发了一种基于细胞的荧光[/font][/font][font=宋体]检测[/font][font=宋体]法[/font][font=宋体](如基于细胞的[/font][font=宋体][font=Calibri]ELISA[/font][font=宋体]法[/font][/font][font=宋体])[/font][font=宋体],用于测[/font][font=宋体]定[/font][font=宋体][font=宋体]抗体亲和力。这种方法通过使用荧光标记的抗体,并将其加入到固定在[/font][font=Calibri]96[/font][font=宋体]孔板上的抗原阳性和抗原阴性的细胞系中,通过计算特异性结合和非特异性结合的差值来测量抗体的亲和力。[/font][/font][font=宋体][font=宋体]研究者通过与传统的流式细胞术和放射性([/font][font=Calibri]I[/font][/font][sup][font=宋体][font=Calibri]125[/font][/font][/sup][font=宋体][font=宋体])[/font][font=Calibri]Scatchard[/font][font=宋体]分析方法进行比较,验证了基于细胞的荧光法的有效性。结果显示,新方法得到的解离常数[/font][font=Calibri]KD[/font][font=宋体]值与传统方法相当,证明了这一新技术的准确性和可靠性。[/font][/font][font=宋体]此外,研究还展示了如何使用这种荧光法进行竞争性结合分析,进一步验证了抗体与抗原的特异性结合。这一功能对于研究抗体的结合表位和选择高亲和力抗体具有重要意义。[/font][b][font=宋体]基于细胞的荧光法的优势[/font][/b][font=宋体]与[/font][font=宋体]流式细胞术和[/font][font=宋体][font=Calibri]I[/font][/font][sup][font=宋体][font=Calibri]125[/font][/font][/sup][font=宋体]比色法等[/font][font=宋体]传统方法相比,基于细胞的荧光法具有多项优势。首先,该方法不使用放射性同位素,减少了实验的安全风险。其次,使用完整的细胞而非纯化的蛋白质,能够更真实地模拟抗体与天然抗原的相互作用。此外,该方法操作简便,成本低廉,适合高通量筛选,且能够在短时间内完成大量样本的分析。[/font][font=宋体] [/font][font=宋体]尽管基于细胞的荧光法具有诸多优势,但也存在一些局限性。例如,对于复杂样品的处理可能会产生非特异性结合,导致结果的误判。然而,随着技术的不断优化和发展,这些问题有望得到解决。[/font][font=宋体]尽管目前还未有人利用[/font][font=宋体]基于细胞的荧光法[/font][font=宋体]来评估抗体亲和力,但是其自身具备的优势[/font][font=宋体][color=#182026]表明[/color][/font][font='Segoe UI'][color=#182026]该方法具有作为抗体亲和力检测方法的潜力[/color][/font][font=宋体],为抗体药物的开发和研究提供强有力的支持。[/font][font=宋体] [/font][font=宋体][/font][font=宋体]本篇[/font][font=宋体]文章[/font][font=宋体]由[/font][font=宋体]义翘神州[/font][font=宋体]编辑[/font][font=宋体]整理[/font][font=宋体],[/font][font=宋体]同时[/font][font=宋体]义翘[/font][font=宋体]神州[/font][font=宋体]提供[/font][url=https://cn.sinobiological.com/services/spr-bli-assay-services][u][font=宋体][color=#0000ff][b][font=Calibri]SPR/BLI[/font][font=宋体]亲和力测定服务[/font][/b][/color][/font][/u][/url][font=宋体],[/font][font=宋体]详情[/font][font=宋体]请[/font][font=宋体]点击[/font][font=宋体]![/font][font=宋体][/font][font=宋体] [/font][font=宋体]参考文献:[/font][font=宋体][font=Calibri]Yu X, Pegram CN, Bigner DD, Chandramohan V. Development and validation of a cell-based fluorescent method for measuring antibody affinity. J Immunol Methods. 2017 442:49-53. doi:10.1016/j.jim.2016.12.004[/font][/font][font=Calibri] [/font]
[font=宋体][font=宋体]免疫组化法([/font][font=Calibri]IHC[/font][font=宋体])是使用抗体检测组织切片(例如肝脏、胰腺或心脏)中细胞蛋白质(抗原)的过程。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]当组织样本被送到实验室进行疾病检查时,有几个细节不易确定。几种疾病或疾病亚型在显微镜下可能看起来相似或看起来具有相似大小的细胞,但具有不同的行为和必要的治疗,区分它们的最佳方法是检测这些细胞上作为标记的特定分子。免疫组化法([/font][font=Calibri]IHC[/font][font=宋体])是一种使用抗体(匹配分子)的技术,用于寻找、识别附着在细胞上的标记物。在显微镜下可以看到抗体本身,这有助于技术人员进行精确识别。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]免疫组化法([/font][font=Calibri]IHC[/font][font=宋体])已广泛应用于医学中,特别是癌症诊断。淋巴瘤是依赖于[/font][font=Calibri]IHC[/font][font=宋体]进行正确诊断和治疗决策的癌症之一。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]免疫组化常见问题:[/font][font=宋体][font=宋体]问题一:我应该使用[/font][font=Calibri]PIER[/font][font=宋体]还是[/font][font=Calibri]HIER[/font][font=宋体]进行抗原修复?[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]固定过程可能会掩盖抗原,导致抗体结合无法进行。这种掩盖可以通过一种称为抗原修复[/font][font=Calibri]/[/font][font=宋体]抗原去掩蔽的技术来逆转,该技术可以通过加热([/font][font=Calibri]HIER[/font][font=宋体];热诱导抗原修复)或蛋白酶([/font][font=Calibri]PIER[/font][font=宋体];蛋白水解诱导抗原修复)介导。后者使用蛋白酶[/font][font=Calibri]K[/font][font=宋体]、胰蛋白酶和胃蛋白酶等酶。[/font][font=Calibri]PIER[/font][font=宋体]方法通过降解掩盖表位的肽而起作用。然而,[/font][font=Calibri]PIER[/font][font=宋体]也可能导致样品形态或抗原本身的改变。因此,[/font][font=Calibri]PIER[/font][font=宋体]的使用频率低于[/font][font=Calibri]HIER[/font][font=宋体],后者通过恢复表位的二级和三级结构而起作用。[/font][/font][font=宋体]为了确定是否应该进行抗原修复以及采用哪种方法,应遵循以下指南:[/font][font=宋体]进行文献检索,以确定其他研究人员如何可视化您感兴趣的抗原。[/font][font=宋体]检查抗体供应商是否推荐了特定的抗原修复方案。[/font][font=宋体][font=宋体]如果没有特定的协议可用,我们建议使用[/font][font=Calibri]HIER[/font][font=宋体]而不是[/font][font=Calibri]PIER[/font][font=宋体]协议。[/font][/font][font=宋体][font=宋体]对于[/font][font=Calibri]HIER[/font][font=宋体],总是使用中性抗原修复缓冲液,如[/font][font=Calibri]AbD Serotec[/font][font=宋体]的[/font][font=Calibri]BUF025A[/font][font=宋体],并与未进行抗原修复的样品进行比较。[/font][/font][font=宋体][font=宋体]如果中性染色溶液没有产生良好的染色效果,则应测试碱性或酸性抗原修复缓冲液。除了[/font][font=Calibri]pH[/font][font=宋体]值外,其他需要优化的参数是温度和持续时间。理想情况下,尝试各种[/font][font=Calibri]pH[/font][font=宋体]值、温度和时间组合。[/font][/font][font=宋体][font=宋体]为了排除由[/font][font=Calibri]HIER[/font][font=宋体]过程引起的伪影,始终包括一个控制样品,该样品在没有[/font][font=Calibri]HIER[/font][font=宋体]步骤的情况下进行染色。[/font][/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体][font=宋体]问题二:如何选择[/font][font=Calibri]IHC[/font][font=宋体]实验的抗体,单克隆抗体还是多克隆抗体?[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]单克隆抗体和多克隆抗体的抗体特性决定了其优缺点。单克隆抗体是针对单个表位的同种免疫球蛋白。抗体是由一个动物的单个[/font][font=Calibri]B[/font][font=宋体]细胞克隆产生的,因此在免疫化学上相似。多克隆抗体是针对同一抗原的各种表位的异质抗体混合物。抗体是由动物的不同[/font][font=Calibri]B[/font][font=宋体]细胞克隆产生的,因此在免疫化学上不同。多克隆混合物中的抗体可能具有略微不同的特异性和亲和力。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]如果蛋白质靶标具有相同的氨基酸序列,单克隆抗体更合适。一旦抗原因各种原因发生构象变化,如蛋白质相互作用、翻译后修饰、温度、[/font][font=Calibri]pH[/font][font=宋体]值、固定、盐浓度等,单克隆抗体和抗原的联合作用将受到严重影响。由于多克隆抗体具有多个表位,不受蛋白质构象变化的影响,一般来说,在一定范围内的[/font][font=Calibri]pH[/font][font=宋体]和盐浓度内,多克隆抗体之间的抗原结合比单克隆抗体更稳定。[/font][/font][font=宋体] [/font][b][font=宋体]问题三:一抗的孵育时间多久?[/font][/b][font=宋体][font=宋体]一抗的孵育时间与温度[/font][font=Calibri],[/font][font=宋体]抗体浓度有关。一般情况下[/font][font=Calibri],[/font][font=宋体]在[/font][font=Calibri]37[/font][font=宋体]℃的条件下[/font][font=Calibri],[/font][font=宋体]孵育[/font][font=Calibri]1-2[/font][font=宋体]小时左右。在室温的条件下[/font][font=Calibri],[/font][font=宋体]孵育[/font][font=Calibri]3[/font][font=宋体]小时左右。在[/font][font=Calibri]4[/font][font=宋体]℃的条件下[/font][font=Calibri],[/font][font=宋体]孵育[/font][font=Calibri]18-24[/font][font=宋体]小时左右。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州提供[url=https://cn.sinobiological.com/services/immunohistochemistry-service][b]石蜡切片免疫组化([/b][/url][/font][font=Calibri][url=https://cn.sinobiological.com/services/immunohistochemistry-service][b]IHC[/b][/url][/font][font=宋体][url=https://cn.sinobiological.com/services/immunohistochemistry-service][b])检测服务[/b][/url],更多免疫组化的问题可以上义翘神州网咨询![/font][font=Calibri]https://cn.sinobiological.com/services/immunohistochemistry-service[/font][/font][font=宋体] [/font][font=Calibri] [/font]
影响抗原[url=https://www.tw-reagent.com/category.php?id=34]抗体[/url]反应的因素有两方面,一是反应物自身的因素;二是反应环境条件。 (一)反应物自身的因素 1.抗体:不同来源的抗体,反应性各有差异,抗体的浓度、特异性和亲和力都影响抗体抗原反应,为提高试验的可靠性,应选择高特异性、高亲和力的抗体作诊断试剂。等价带的宽窄也影响抗原抗体复合物的形成,单克隆抗体不适用于沉淀反应。 2.抗原:抗原的理化性状、分子量、抗原决定簇的种类及数目均可影响反应结果。颗粒性抗原出现凝集反应,可溶性抗原出现沉淀反应,单价抗原与相应抗体结合不出现沉淀现象。 (二)反应环境条件 1.电解质:抗原与抗体发生特异性结合后,虽由亲水胶体变为疏水胶体,若溶液中无电解质参加,仍不出现可见反应。为了促成沉淀物或凝集物的形成,常用0.85%NaCl或各种缓冲液作为抗原及抗体的稀释液。 2.酸碱度:抗原抗体反应必须在合适的pH环境中进行。蛋白质具有两性电离性质,因此每种蛋白质都有固定的等电点。抗原抗体反应一般在pH6~9进行,有补体参与的反应pH为7.2~7.4,pH过高或过低都将影响抗原与抗体反应。 3.温度:在一定范围内,温度升高可加速分子运动,抗原与抗体碰撞机会增多,使反应加速。一般为15℃~40℃,常用的抗原抗体反应温度为37℃,温度如高于56℃,可导致已结合的抗原抗体再解离,甚至变性或破坏。此外,适当振荡也可促进抗原抗体分子的接触,加速反应。
[font=宋体][b]什么是纳米抗体?[/b][/font][font=宋体][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/nanobody][b]纳米抗体[/b][/url]([/font][font=Calibri]nanobody, Nb[/font][font=宋体])是一种人工设计的抗体分子,又称为单域抗体([/font][font=Calibri]single-domain antibodies, sdAbs[/font][font=宋体])、[/font][font=Calibri]VHH[/font][font=宋体]抗体或[/font][font=Calibri]camelid[/font][font=宋体]抗体,是发现于羊驼、单峰驼等驼科以及鲨鱼、鳐鱼等软骨鱼中的一种天然缺失轻链的重链抗体([/font][font=Calibri]heavy-chain antibodies, HCAbs)[/font][font=宋体]。[/font][font=Calibri]1993[/font][font=宋体]年,比利时的科学家在骆驼的血清中发现了一种天然轻链缺失的重链抗体,分子量约[/font][font=Calibri]95 kDa[/font][font=宋体],其中包括两个恒定区([/font][font=Calibri]CH2[/font][font=宋体]和[/font][font=Calibri]CH3[/font][font=宋体])、一个铰链区和一个重链可变区([/font][font=Calibri]variable heavy chain domain, VHH[/font][font=宋体]),接着克隆得到只包含一个重链可变区的单域抗体,即[/font][font=Calibri]VHH[/font][font=宋体]抗体。[/font][font=Calibri]VHH[/font][font=宋体]抗体的晶体结构为[/font][font=Calibri]4 nm[/font][font=宋体]×[/font][font=Calibri]2.5 nm[/font][font=宋体]×[/font][font=Calibri]3 nm[/font][font=宋体]的椭圆形,分子量大小仅普通抗体的[/font][font=Calibri]1/10[/font][font=宋体],约[/font][font=Calibri]12-14 kDa[/font][font=宋体],是最小的完整抗原结合片段,因此又被称为纳米抗体。纳米抗体可用于肿瘤等疾病的治疗、疾病的检测、疫苗的研发等。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]纳米抗体特性:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]高耐热性和稳定性[/font][/font][font=宋体] [/font][font=宋体][font=宋体]将不同的纳米抗体在[/font][font=Calibri]37[/font][font=宋体]℃放置[/font][font=Calibri]1[/font][font=宋体]周,结果其抗原结合活性均在[/font][font=Calibri]80%[/font][font=宋体]以上,表明纳米抗体在室温下保存相当稳定,这使其比常规抗体更易于储藏和运输。[/font][/font][font=宋体][font=宋体]比较了鼠单抗和纳米抗体在高达[/font][font=Calibri]90[/font][font=宋体]℃高温长时间处理的抗原结合活性,发现纳米抗体都保持了较高的活性仍能重新获得抗原结合能力,而所有常规抗体在[/font][font=Calibri]90[/font][font=宋体]℃处理后都丧失了活性,发生了不可逆的聚合。[/font][/font][font=宋体][font=宋体]在恶劣条件,如在高热、离液剂、存在蛋白酶和极度[/font][font=Calibri]pH[/font][font=宋体]值变性的条件下(如胃液和内脏中),正常抗体会失效或分解,而纳米抗体仍具有高度的稳定性。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]高抗原结合性:[/font][/font][font=宋体] [/font][font=宋体][font=宋体]纳米抗体独特的结构决定了其高抗原结合特性:纳米抗体较长的[/font][font=Calibri]CDR3[/font][font=宋体],可形成一稳定的暴露的凸环结构(凸环中具有稳定结构的二硫键),能够深入抗原内部以更好的结合抗原从而提高了其抗原特异性和亲和力。[/font][/font][font=宋体][font=宋体]而传统抗体[/font][font=Calibri]Fab[/font][font=宋体]片段及单链抗体[/font][font=Calibri]scFv[/font][font=宋体]的抗原结合表面常形成凹形拓扑结构[/font][font=Calibri], [/font][font=宋体]通常只能识别位于抗原表面的位点,因此纳米抗体[/font][font=Calibri]VHH[/font][font=宋体]单域具有更加广泛的抗原结合力,甚至当靶蛋白紧密包裹隐藏了普通抗体识别的位点时[/font][font=Calibri],[/font][font=宋体]纳米抗体也可以对其进行表位识别。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]较强的组织穿透力:[/font][/font][font=宋体] [/font][font=宋体]纳米抗体具有强而快的组织穿透能力,可以进入致密的组织如实体瘤发挥作用;并且多余未结合的纳米抗体能够很快的被清除,这相对于单克隆抗体组织穿透力差,不易被清除的不足,更有利于疾病的诊断。另外,纳米抗体能够有效的穿透血脑屏障,这样的特性为脑部给药提供了新方法,有望成为治疗老年痴呆症的新药。[/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]高水溶性、高表达性[/font][/font][font=宋体] [/font][font=宋体][font=宋体]正常抗体[/font][font=Calibri]VH[/font][font=宋体]结构域单独表达时通常形成包涵体,或者暴露的疏水域相互黏附;而纳米抗体[/font][font=Calibri]VHH[/font][font=宋体]由于其[/font][font=Calibri]FR2[/font][font=宋体]中的疏水残基被亲水残基所取代,使得纳米抗体的水溶性增加,聚合性减少;而且即使以包涵体形式表达,也很容易复性,这样可以大大提高作为药物的利用率。[/font][/font][font=宋体][font=宋体]因纳米抗体分子量小、结构简单,由单一的基因编码,所以它很容易在微生物中合成,能在噬菌体、酵母等微生物中大量的表达,而且其相对价格低廉、可进行大规模生产,易于普及和应用。有报道,可通过酵母反应器酿造将纳米抗体的产量提高,每公升可达[/font][font=Calibri]1[/font][font=宋体]克的产量。[/font][/font][font=宋体] [/font][font=宋体][b]纳米抗体的应用优势[/b][/font][font=宋体] [/font][font=宋体][font=宋体]①用于生物医药研发(基因工程药物研发、[/font][font=Calibri]ADC[/font][font=宋体]药物研发);[/font][/font][font=宋体]②用于临床体外诊断(胶体金法、酶联免疫吸附法、电化学发光法);[/font][font=宋体]③用于肿瘤研究、免疫学研究等基础研究;申请具有自主知识产权的发明专利及科研奖项;[/font][font=宋体]④拓展研究思路、发表国际知名学术刊物。[/font][font=宋体] [/font][font=宋体][font=宋体]纳米抗体是一种非常有前景的下一代治疗性抗体技术,受到越来越多的研究机构和制药公司的关注。为支持纳米抗体药物的早期发现,义翘神州利用噬菌体抗体库技术自主研发了纳米抗体开发平台,已成功开发了多个纳米抗体候选分子。另外,我们的高通量纳米抗体表达平台,已成功表达和生产了多种纳米抗体形式,包括单价、多价或多特异性[/font][font=Calibri]VHH[/font][font=宋体],满足客户的各种定制需求。[/font][/font][font=宋体][font=宋体]更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/nanobody[/font][/font][font=Calibri] [/font]