推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-858-8867
400-858-8867
 留言咨询
留言咨询

 400-860-5586
400-860-5586
 留言咨询
留言咨询
 400-860-5168转6004
400-860-5168转6004
 留言咨询
留言咨询






在糖果工业中,折光仪和旋光仪有着非常广泛的应用。软糖 – 应用折光仪检测浓度:绝大多数企业都利用折光仪来控制巧克力制品、硬糖和其他糖果制品中混合糖的浓度。当产品本身参数范围较宽(例如从76 到78 °Brix)时,在很多时候,仪器的再现性比准确度更重要。为了能在合适的阶段/时间停止熬煮过程,也要求仪器能够快速读数。过去,光学“发射折光仪” (又称为 ‘Queen Mary’ 或 ‘battleships’) 已经应用在这些领域。它们操作简单,使用起来不需要技巧性,但在检测粘性样品时灵敏度不高。现在这些仪器已经基本上被RFM730数字折光仪所取代。手持式折光仪和阿贝折光仪也同样应用在这些方面,但考虑到样品的熬煮温度,在选择合适的仪器类型时需要特别小心。有时,为了使高浓度的样品保持在液体状态,适当提高仪器温度,及减少冷却时间以加快读数速度也是同样必要的。Abbe 折光仪可以通过连接恒温水浴可以实现在60°C条件下测量,而新的RFM300+系列由于内置了帕尔贴 (Peltier) 电子精确温控元件,可以支持高达70°C条件下的样品检测。过程折光仪也有相同的应用,能够取得实时的 °Brix 值,而无需将样品从容器中移出,从而消除样品表层的蒸发的影响,也无需等待样品冷却的时间。过程折光仪安装到罐体外部的旁通循环回路上作为“出口部分”时,仪器能够实时提供控制信号,以便在到达熬煮终点时自动将产品移入缓冲罐中。硬糖和“口香糖”:在糖果的熬煮过程中,Eclipse 手持式折光仪、阿贝折光仪及数字式仪器都可以用来检测样品。与软糖的类似,在选择合适的折光仪时,产品的温度是一个关键参数。而产成品的质量管理检验则有些困难,因为样品通常都是固态的(例如有的浓度高达 90 °Brix)。有些生产商将样品切成薄片,并在棱镜中心位置滴加接触液,再将切片后的样品放置在棱镜上测量。测量结果可以精确到一位小数。巧克力:粗品巧克力中的脂肪含量的测定是QC的一个重要指标。但折光仪测定的是可溶性固体,因此若不能事先将某些不溶性固体(脂肪)转化为溶液,仪器将无法作出分析。此时,可以添加化学物质“单溴代萘”来解决这一问题。这一混合溶液的折光率常在1.60 RI附近,可以使用阿贝折光仪或数字式折光仪(如RFM960或RFM970)进行检测。软糖 – 各种糖类混合物的调和控制:糖果中心馅的质感和风味依赖于添加到糖果中的各种糖类的精确混合。通常转化糖 与蔗糖 按照一定比例混合可以得到一个乳脂状的中心(如餐后薄荷糖)。由于蔗糖的RI值与转化糖的RI值相近,因此虽然可以检测该混合物的总浓度,但却无法控制混合物中各种糖类的混合比例。然而,不同种类的糖(如蔗糖/转化糖)具有不同的比旋光度,因此可以利用旋光仪来检测糖类混合物是否与预选设定的混合比例相符。ADP410和ADP440旋光仪就可以满足此类应用。食品添加剂及原料:折光仪和旋光仪都可以用于检测制备糖果产品的原材料。例如,在糖果中添加的阿拉伯胶是起到了增稠剂的作用,可以用旋光仪来检测。此外,明胶可用折光仪检测,风味剂,如薄荷油,则可以用旋光仪来检测。废液: 监控糖果厂排出的废液可有助于保护污水处理厂(的反渗透系统设备)免受高糖溶液的损害。在线过程折光仪就适合实现废液的监测,在某些情况下还可对废液流进行控制,帮助企业免受环保机构的处罚。
请教一下各位:测葡萄糖浆的固形物含量,用手提式折光仪测如何操作呢?有没有相关标准?
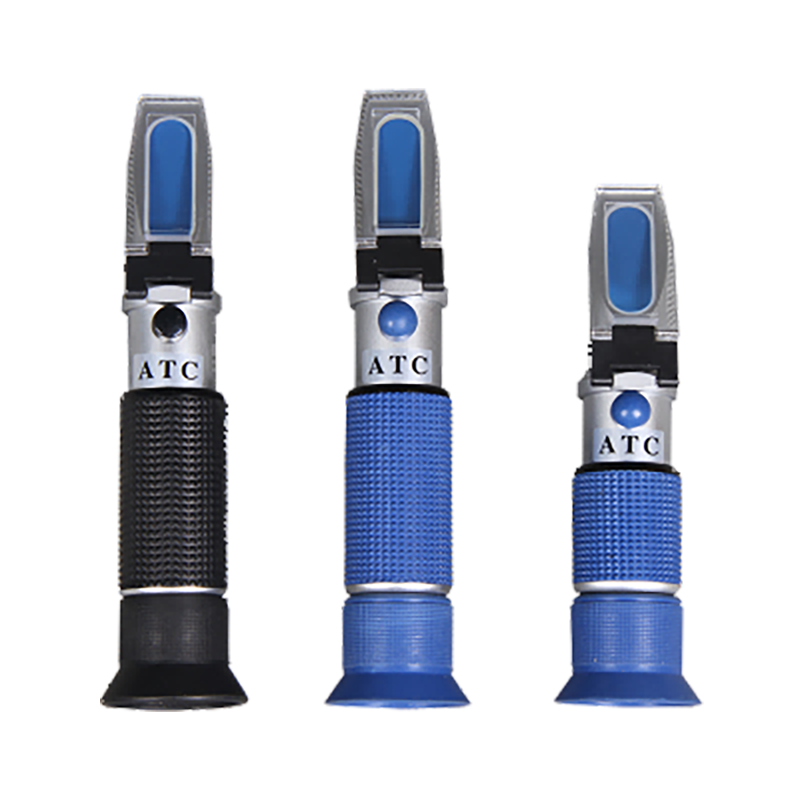
一、总可溶性固形物含量的测定(折光仪法)一、目的及原理 利用手持式折光仪测定果蔬中的总可溶性固形物(Total Soluble Solid,TSS)含量,可大致表示果蔬的含糖量。 光线从一种介质进入另一种介质时会产生折射现象,且入射角正弦之比恒为定值,此比值称为折光率。果蔬汁液中可溶性固形物含量与折光率在一定条件下(同一温度、压力)成正比例,故测定果蔬汁液的折光率,可求出果蔬汁液的浓度(含糖量的多少)。 常用仪器是手持式折光仪,也称糖镜、手持式糖度计,该仪器的构造如下图所示。 通过测定果蔬可溶性固形物含量(含糖量),可了解果蔬的品质,大约估计果实的成熟度。 二、药品与器材 番茄、柑桔、菠萝 蒸馏水 烧杯、滴管、卷纸、手持式折光仪三、操作步骤 打开手持式折光仪盖板(a),用干净的纱布或卷纸小心擦干棱镜玻璃面。在棱镜玻璃面上滴2滴蒸馏水,盖上盖板。于水平状态,从接眼部(b)处观察,检查视野中明暗交界线是否处在刻度的零线上。若与零线不重合,则旋动刻度调节螺旋,使分界线面刚好落在零线上。打开盖板,用纱布或卷纸将水擦干,然后如上法在棱镜玻璃面上滴2滴果蔬汁,进行观测,读取视野中明暗交界线上的刻度,即为果蔬汁中可溶性固形物含量(%)(糖的大致含量)。重复三次。 四、结果与计算 汁液种类 总可溶性固形物含量(%) 平均(%) 读数1 读数2 读数3 二、含酸量的测定(中和法)一、目的及原理 果蔬中含有各种有机酸,主要的有苹果酸、柠檬酸、酒石酸、草酸等。果品品种种类不同,含有有机酸的种类和数量也不同 。果蔬含酸量测定是根据酸碱中和原理,即用已知浓度的氢氧化钠溶液滴定,故测出来的酸量又称为总酸或可滴定酸。计算时以该果蔬所含主要的算来表示,如苹果、梨、桃、杏、李、番茄、莴苣主要含苹果酸,以苹果酸计算,其毫克当量为0.067g;柑橘类以柠檬酸计算,其毫克当量为0.064g;葡萄以酒石酸计算,其毫克当量为0.075g。二、药品与器材 桃、杏、葡萄、番茄、莴苣等; 0.1N氢氧化钠、1%酚酞指示剂; 50ml或10ml滴定管、200ml容量瓶、20ml移液管、100ml烧杯、研钵、分析天平、漏斗、棉花或滤纸、小刀、白瓷板、滴定管。三、操作与步骤 称取均匀样品20g,置研钵中研碎,注入200ml容量瓶中,加蒸馏水至刻度。混合均匀后,用棉花或滤纸过滤。 吸取滤液20ml放入烧杯中,加酚酞指示剂2滴,用0.1N NaOH滴定,直至成淡红色为止。记下NaOH液用量。重复滴定三次,取其平均值。 某些果蔬容易榨汁,而其汁液含酸量能代表果蔬含酸量,可以榨汁,取定量汁液(10ml)稀释后(加蒸馏水20ml),直接用0.1N NaOH液滴定。 计算: VxNx折算系数 B 果蔬含酸量%= ――――――― x ― x100 b A V = NaOH液用量(毫升) N = NaOH液当量浓度(N) A = 样品克数 B = 样品液制成的总毫升数 b = 滴定时用的样品液毫升数 折算系数 = 以果蔬主要含酸种类计算,如苹果或番茄用0.067四、结果与计算 1.将测定数据填入下表中 样品名称 NaOH浓度(N) NaOH用量(ml) 含酸量(%) 以何酸计 2.列出计算式并计算结果三、维生素C的含量的测定(2.6―二氯靛酚法)一、目的及原理 天然的抗坏血酸有还原型和脱氢型两种,还原型抗坏血酸分子结构中有烯醇(COH=COH)存在,故为一种极敏感的还原剂,它可失去两原子氢而氧化为脱氢型抗坏血酸。染料2.6―二氯靛酚钠盐(C12H6O2NCl2Na)作为氧化剂,可以氧化抗坏血酸而其体身亦被还原成无色的衍生物。 2.6―二氯靛酚钠盐易溶于水,其碱性或中性水溶液呈蓝色,在酸性溶液中成桃红色,这个变化用来鉴别滴定的终点。 由于抗坏血酸在许多因素影响下都易发生变化,因此,取样品时应尽量减少操作时间,并避免与铜、铁等金属接触以防止氧化。 对带为颜色的样品液,可用中性的白陶土脱色,吸取澄清滤液进行测定二、药品与器材 番茄(青色、红色),辣椒、甘蓝、洋葱、柑橘、蜜枣、鲜枣、柿子、苹果等。 抗坏血酸(纯),2.6―二氯靛酚钠盐,2%草酸,白陶土。 微量滴定管,100ml容量瓶,10ml移液管,烧杯,研钵(或打碎机),铝盒,漏斗,分析天平,离心机。三、操作与步骤 1.试剂制备 (1)标准抗坏血酸溶液:精确称取抗坏血酸50mg(±0.1毫克),用2%草酸溶解,小心地移入250ml容量瓶中,并加草酸稀释至刻度,算出每毫升溶液中抗坏血酸的毫克数。 (2)2.6―二氯靛酚溶液标定。称取2.6―二氯靛酚钠盐50mg,溶于50ml热水中,冷后加水稀释至250ml,过滤后盛于棕色药瓶内,保存在冰箱中,同时用刚配好的标准抗坏血酸标定。 吸取标准抗坏血酸溶液2ml,加2%草酸5ml,以2.6―二氯靛酚染料溶液滴定,至桃红色15秒钟不褪即为终点,根据已知标准抗坏血酸和染料的用量,计算出每1毫升染料溶液相当的抗坏血酸毫克数。 2.样品液的准备与测定 称取切碎的果蔬样品20g(或蜜枣5g),放在研钵中加2%草酸溶液少许研碎(或称取100g±0.1g样品加2%草酸100g倒入打碎机中打成浆,然后称取40g),注入200ml容量瓶中,加2%草酸溶液稀释至刻度,过滤备用。如果滤液有颜色,在滴定时不易辨别终点,可先用白陶土脱色,过滤或用离心机沉淀备用。 吸取滤液10毫升与烧杯中,用已标定过的2.6―二氯靛酚钠盐溶液滴定,至桃红色15秒不褪为止,记下染料的用量。 吸取2%草酸溶液10ml,用染料作空白滴定记下用量。 计算公式: (V-V1) X A b W = ―――――――― X — X 100 B a W = 100克样品含的抗坏血酸毫克数。 V = 滴定样品所用的染料毫升数。 V1 = 空白滴定所用的染料毫升数。 A = 1毫升染料溶液相当的抗坏血酸毫克数。 B = 滴定时吸取的样品溶液毫升数。 b = 样品液稀释后总毫升数。 a = 样品的克数。 附注:经过熏硫或亚硫酸及其盐类处理的样品,在配置样品液时,应加甲醛(纯)5毫升以除去二氧化硫的影响,以后再定容量。四、结果与计算 1.将测定的数据填入下列表中 (1)染料的标定 标准抗坏血酸溶液的浓度(mg/ml) 滴定时所消耗的染料溶液(ml) 每1毫升染料溶液所相当的抗坏血酸(mg) 第一次 第二次 第三次 平均 (2)样品中抗坏血酸含量的计算 样品名称 样品数量(g) 样品液的总体积(ml) 滴定时所用样品液的量(ml) 滴定样品所用染料量(ml) 空白滴定所用染料量(ml) 维生素C含量(mg/100g) 1 2 3 平均 1 2 3 4 2.列出计算式并计算结果四、果蔬呼吸强度测定(气流法)一、目的及原理 呼吸作用是果蔬采收后进行的重要生理活动,是影响贮运效果的重要因素。测定呼吸强度可衡量呼吸作用的强弱,了解果蔬采后生理状态,为低温和气调贮运以及呼吸热计算提供必要的数据。因此,在研究或处理果蔬贮藏问题时,测定呼吸强度是经常采用的手段。 呼吸强度的测定通常是采用定量碱液吸收果蔬在一定时间内呼吸所释放出来的CO2,再用酸滴定剩余的碱,即可计算出呼吸所释放出的CO2量,求出其呼吸强度。其单位为每公斤每小时释放出CO2毫克数。 反应如下: 2NaOH + CO2→Na2CO3 + H2O Na


