1、色谱长度色谱长度与分离度通常成正比。色谱柱越长,组分之间分辩效果越好,但色谱柱越长压降越大,而输入的压力是有限的。色谱柱过长会增大进出口压力比,相反会降低分离度。通常采用的柱长2m~4m,内径2mm,毛细管柱长度可达20m~150m,内径为0.2mm。2、色谱柱填料颗粒大小填料的粒子越细,由于表面积增加,分辩效果越好,分离度就越高。但是颗粒极细时可能会增大柱压降,也会起反作用。一般采用惰性、多孔的固体颗粒。多由硅藻土或玻璃珠制成,分析不同极性的微生物化合物,为了获得最适的分离条件,要求有不同固定相的载体。3、柱温气体在液体中的溶解度或在固体表面的吸附程度都随温度增高而降低,在气液色谱分析中,当超过一定温度时,静态的液体通常会从色谱柱中挥发掉,所以选择柱温时应考虑到样品的沸点。一般是略低于样品沸点的平均值。4、载气种类常用的载气有 氮气、氢气等。其中氢气、氦气的分子量较小,有利于提高分析速度,但浓度较高的介质易在其间形成扩散,影响分离度,所以在实际测量中氢气、氦气一般都用在介质浓度较低的区域并提高其流速,减少扩散的影响。5、载气流速介质在固定相上的滞留时间,主要取决于介质自身的特性(挥发性,极性等)和载气的流速。所以流速快慢直接影响分离度。
影响色谱分离度的因素有哪些?各位大侠支招!
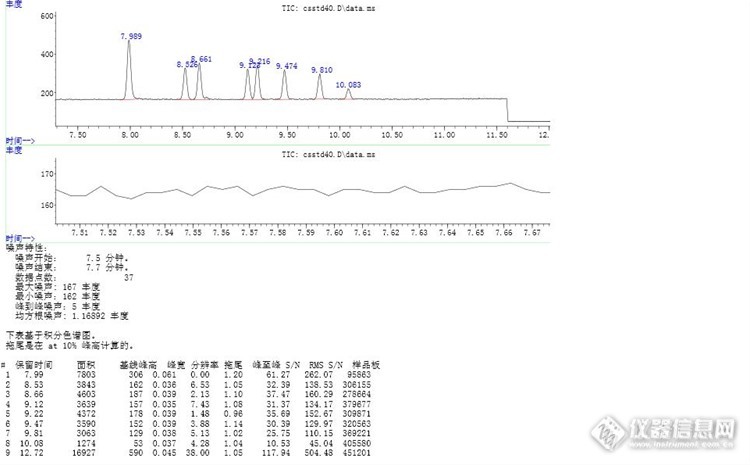
使用安捷伦GCMS新的软件计算色谱峰的分离度,但是不知道如何看懂报告,请老师指点!请老师指出各个色谱峰的分离度,其中Rthttp://ng1.17img.cn/bbsfiles/images/2017/03/201703221726_01_1794257_3.jpg12.7min的峰没有截图出来。
我[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离度老是不好,能通过调节气体流速和温度或其他条件来提高分离度吗?具体可以调节哪些条件啊? 谢谢了啊
做中药产品,有什么好推荐的液相色谱柱,250 的那种,要分离度好点的有没有推荐下做中药分离度大点的色谱柱?有的告诉我下!
[size=18px][url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]中影响分离度的因素有哪些?提高分离度的途径有哪些?这看似是两个问题,其实质是相同的。影响[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]分离度的因素有:1、色谱柱的固定相,也就是色谱柱的型号;2、色谱柱的规格,也就是色谱柱的柱长、内径、固定液的液膜厚度等因素;3、载气的种类;4、载气的流速,不同流速柱效都不一样;5、柱温;6、进样室的结构;7、检测器的结构。后面两个因素6、7都是属于仪器方面的问题,主要是柱外因素。提高分离的途径也就是从以上几方面入手。[/size]
各位,请教下如何计算色谱峰的分离度,我用的是戴安的ICS-3000/5000,软件上能实现吗?还有,分离度R大于多少时说明两峰完全分离?
同一根色谱柱,在不同的色谱仪器上,采用相同的色谱条件,但是杂质的分离度差异太大
色谱柱污染冲洗后,检测有主峰,峰面积比之前的,是不是分离度下降,或掺杂杂志峰,对检测含量有影响,如何看出有杂峰混合呢
某色谱柱长1m时,其分离度为1.0,问要完全分离时,色谱柱应为多少
色谱中分离度的计算公式有哪些?

怎样提高液相色谱的分离度(梯度)
下式为分离度计算公式http://www.dikma.com.cn/Public/Uploads/images/R.JPGN:柱效(Efficiency)反映色谱柱性能,柱效越高,分离度越好。在其他条件恒定的情况下,塔板数增加一倍,分离度仅提高40%。操作中,可通过下面两种方式增加塔板数进而提高分离度:其一,使用长柱或双柱串联,但也会使分离时间大大延长;其二,使用细粒径填料的色谱柱,但这需要耐更高压力的液相色谱系统。相比之下后者更为可取。α:选择性(selectivity)是指色谱柱-流动相体系分离两个化合物的能力。选择性主要与固定相、流动相组成以及柱温等因素有关,与保留值也密切相关,其中固定相和流动相组成影响较大。以最常见的反相模式为例,反相柱(包括C18、C8、PH等)是以分配作用对化合物进行保留的,不同化合物的分离是基于它们在键合相与流动相中分配系数的差异,如果两种化合物的水溶性、在烷烃-水体系的分配系数等方面存在明显差异,那么这些化合物通常是能够利用反相柱达到分离;PH柱对具有苯环的化合物具有特殊保留。正相模式下,硅胶柱、胺基柱、氰基柱与带有极性基团的化合物之间存在极性相互作用,对化合物的基团具有选择性,常常用于结构类似物、异构体化合物的分离。流动相方面,降低流动相的洗脱强度通常可以增大分离度;而有机溶剂类型也会影响分离,比如反相条件下,乙腈和甲醇的选择性就存在很大差异,这种差异需要在实践中摸索,但无论如何,多种溶剂类型带给我们更多的实现分离的可能。k:随着容量因子k的增大,分离度也随之增加,这种影响在k值较低时非常明显,当k值大于10时,k值增加对分离度的影响就不再显著,这就告诫无原则地提高k值以增大分离度是没有意义的。增加键合相密度能够提高k值;另外改变键合基团类型也能改变k值,比如在反相色谱中,随着键合相碳链长度的增加,k值逐渐增大。

其他讲座资料看[url=http://www.instrument.com.cn/bbs/detail.asp/threadid/1679222/forumid/25/year/2009/query/search] 学习[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]跟yuen72老师入门[/url]前面很多地方谈到了分离度R。分离度R是评价两个相邻色谱峰的关键参数。它的定义是这样的:[img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903231359_140112_1641581_3.jpg[/img]百度百科如此定义分离度R:又称分辨率,为了判断分离物质对色谱柱在色谱柱中的分离情况,常用分离度作为柱的总分离效能指标.用R表示.R等于相邻色谱峰保留时间之差的两倍与两色谱峰峰基宽之和的比值.resolution,R相邻两峰的保留时间之差与平均峰宽的比值。也叫分辨率,表示相邻两峰的分离程度。R=。当W1=W2时,R=。当R=1时,称为4σ分离,两峰基本分离,裸露峰面积为95.4%,内侧峰基重叠约2%。R=1.5时,称为6σ分离,裸露峰面积为99.7%。R≥1.5称为完全分离。《中国药典》规定R应大于1.5。事实上,如果色谱峰是等腰三角形,则R=1就完全达到了基线分离。由于峰型是高斯分布的扣钟形,因此当两个色谱峰间的距离是6σ时,两个色谱峰大小相当时,每个色谱峰各占有其中的一半3σ,重叠部分即3σ之外的部分,不足0.3%。由于色谱方法的正常分析误差为3%,因此色谱峰重叠所带来的误差已经比正常误差低一个数量级,已经可以忽略不计,因此认为R=1.5时,达到了基线分离。
[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]抑制电导检测器、氢氧根系统,请问怎么改善乙酸和乙酰丙酸的分离度流速、梯度、浓度方面已经尝试过了,都没有什么效果。还有没有其他的方法,比如加入改良剂,请大佬帮忙指点一下
为什么可用分离度R作为色谱柱的总分离效能指标?
我对仪器挺感兴趣的,在上网浏览各厂家的仪器介绍时,都看到说明时,说此款仪器对分离度有何改善,分离度提高多少倍。而我却认为,无论是什么色谱,分离的部件在色谱柱,应该是色谱柱起作用,或起主要作用,无非仪器在设计时,柱外死体积小,流通池的设计更趋合理,等,至于仪器起主要作用,我觉得是不是厂家的宣传啊?我是一个初学者,可能理解有偏差,请各位专家请教!!
前一段时间,我在做GPC时,由于柱子的问题,该物质分子量分布虽然正常,但是不同的分子量的物质的分离度并不理想。比如做聚砜分子量分布,流动相为DMF-氯仿,分离度不佳。在反相色谱中,为了增加分离度,可以向流动相中加水。那么,GPC方法如何改变流动相,才能使不同分子量的聚合物分离度提高呢?多谢指教!
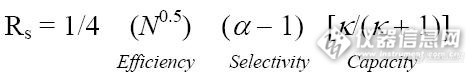
今天有客户咨询,他在做产品有关物质时,它的色谱峰分离度有时好,有时不好。流动相的比例我也做了适当调整。到底还有什么因素会导致它分离度不好呢?关于这个问题,我们首先要看影响分离度的因素有哪些?各个因素起到的作用分别是?哪一个因素是主导的?根据这些我们在来想办法,改善分离度。下面俺就为大家分析分析一下哈~~,供参考~~下式为分离度计算公式http://ng1.17img.cn/bbsfiles/images/2015/05/201505051000_544743_2452211_3.jpgN:柱效(Efficiency)反映色谱柱性能,柱效越高,分离度越好。在其他条件恒定的情况下,塔板数增加一倍,分离度仅提高40%。操作中,可通过下面两种方式增加塔板数进而提高分离度:其一,使用长柱或双柱串联,但也会使分离时间大大延长;其二,使用细粒径填料的色谱柱,但这需要耐更高压力的液相色谱系统。相比之下后者更为可取。α:选择性(selectivity)是指色谱柱-流动相体系分离两个化合物的能力。选择性主要与固定相、流动相组成以及柱温等因素有关,与保留值也密切相关,其中固定相和流动相组成影响较大。以最常见的反相模式为例,反相柱(包括C18、C8、PH等)是以分配作用对化合物进行保留的,不同化合物的分离是基于它们在键合相与流动相中分配系数的差异,如果两种化合物的水溶性、在烷烃-水体系的分配系数等方面存在明显差异,那么这些化合物通常是能够利用反相柱达到分离;PH柱对具有苯环的化合物具有特殊保留。正相模式下,硅胶柱、胺基柱、氰基柱与带有极性基团的化合物之间存在极性相互作用,对化合物的基团具有选择性,常常用于结构类似物、异构体化合物的分离。流动相方面,降低流动相的洗脱强度通常可以增大分离度;而有机溶剂类型也会影响分离,比如反相条件下,乙腈和甲醇的选择性就存在很大差异,这种差异需要在实践中摸索,但无论如何,多种溶剂类型带给我们更多的实现分离的可能。k:容量因子随着容量因子k的增大,分离度也随之增加,这种影响在k值较低时非常明显,当k值大于10时,k值增加对分离度的影响就不再显著,这就告诫无原则地提高k值以增大分离度是没有意义的。增加键合相密度能够提高k值;另外改变键合基团类型也能改变k值,比如在反相色谱中,随着键合相碳链长度的增加,k值逐渐增大。
你模式过色谱条件吗?你测定过多个组分吗?来分享下你使用离子色谱时改善分离度方法的方法吧,看看你都是怎么改善的!!!!
[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱可以进行老化,可以调节流速、升温速度等提高分离度,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]可以调节什么来提高色谱柱的分离度呢?
体积排阻色谱分离蛋白质,分子量范围100万~1万,其中有分子量47000的组份,要分析分子量68000的杂蛋白含量,采用TSK4000SW,长度为60厘米的色谱柱,分离分子量68000与47000的2个组份,分离度在0.9~1.0左右,分离度达不到1.5,有什么方法解决?

在很多色谱专著里,对色谱分离度的表示方法中有峰宽分离度和半峰宽分离度(计算式见附件)。它们的表示方法如下: 峰宽分离度定义为相邻二峰保留值之差与其各自峰底宽总和之半的比值。 半峰宽分离度定义为相邻二峰保留值之差与其各自半峰宽总和之半的比值。 在这两种计算分离度的方法中,两者的差别一个是用峰底宽而另一个是用半峰宽,其它部分均相同。由于峰底宽大约比半峰宽大一倍,这样用这两种方法计算出的分离度也要相差一倍。按理不同的计算方法得到的结果应该大致相等才对,有誰知道这是怎么回事? [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=110700]分离度计算式[/url][img]http://ng1.17img.cn/bbsfiles/images/2008/09/200809291725_110713_1605035_3.jpg[/img]
[color=#444444]我做液相色谱的分离度实验。药典要求将样品酸化2小时后,加碱回调ph,这样能得到主峰的水解产物并且RRT=0.9。但是最后得出的结果并没有这个峰。并且,其他杂质反而变大了,主峰也没有降解的迹象。希望老师能帮忙解答我的难题。[/color]
色谱学理论中,如何计算分离度?
想请教各位一个问题,我在做产品有关物质时,它的色谱峰分离度有时好,有时不好。流动相的比例我也做了适当调整。到底还有什么因素会导致它分离度不好呢?我的流动相是甲醇,正己烷,氨水组成。是不是我可以通过多加一点氨水来增大它的极性,从而提高它的分离度?
想请教各位一个问题,我在做产品有关物质时,它的色谱峰分离度有时好,有时不好。流动相的比例我也做了适当调整。到底还有什么因素会导致它分离度不好呢?我的流动相是甲醇,正己烷,氨水组成。是不是我可以通过多加一点氨水来增大它的极性,从而提高它的分离度?
对于定性分析,色谱峰的分离度应至少达到多少呢?
反相色谱中, 流动相极性↑,洗脱能力↓,k↑,组分tR↑,分离度R↑? 对吗?
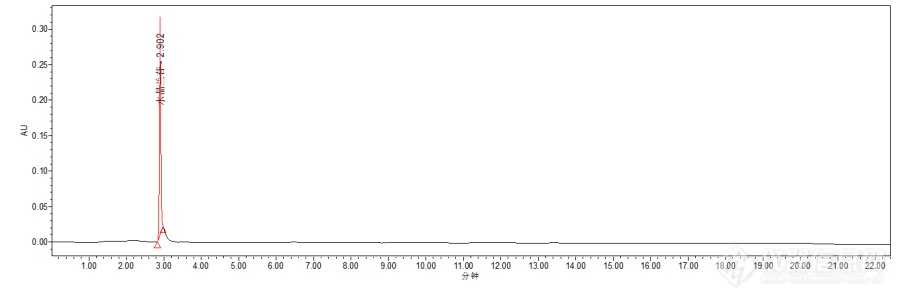
使用样品为胶囊提取样,标品为水晶兰苷,waters2996检测器,X-bridge C18柱,流动相:甲醇、0.05%磷酸水,等度洗脱,甲醇0.1 磷酸水0.9,色谱图如下。请问,如何提高分离度?(甲醇流速0.05、0.03试过,效果不佳)[img=,690,230]https://ng1.17img.cn/bbsfiles/images/2019/07/201907051306109623_250_1777483_3.png!w690x230.jpg[/img][img=,690,268]https://ng1.17img.cn/bbsfiles/images/2019/07/201907051306211145_9031_1777483_3.png!w690x268.jpg[/img]