作为一个新人,要开始做实验了。仪器是waters的XEVO TQD,实验是液质联用来做三种药物的检测方法。很迷茫啊!听说液质方法先确定质谱方法,怎么确定,怎么进样。求教各位的经验啊。
http://simg.instrument.com.cn/bbs/images/default/emyc1010.gif当你拿到一个标准后,里面的液相条件和质谱条件你还会进行摸索吗?还是只按照上面的条件设置?还有就是,前处理按照标准的方法做多少次你会判定此方法回收率做得好与坏?曾经做过一个兴奋剂的标准,质谱条件是别人摸索好的方法,前处理是自己优化出来的,大概做了十几次回收率还是50---60%,最后判断这方法如果不加内标绝对做不到像标准上说的那样1ng/ml回收率在70%---120%
质谱方法(Mass Spectroscope,MS)是通过正确测定蛋白质分子的质量而进行蛋白质分子鉴定、蛋白质分子的修饰和蛋白质分子相互作用的研究。质谱仪通过测定离子化生物分子的质荷比便可得到相关分子的质量。但长期以来,质谱方法仅限于小分子和中等分子的研究,因为要将质谱应用于生物大分子需要将之制备成气相带电分子,然后在真空中物理分解成离子。但如何使蛋白分子经受住离子化过程转成气相带电的离子而又不丧失其结构形状是个难题。20世纪70年代,解吸技术的出现成功地将蛋白分子转化成气相离子。尔后快原子轰击与其紧密相关的溶液基质二次离子质谱法使得具有极性的、热不稳定的蛋白分子可经受住电离过程。但这些方法仅限于10kD以下蛋白分子的研究。80年代电喷雾电离(ESI)和软激光解吸(SLD)电离技术的发展则使得质谱方法应用于高分子量蛋白分子的研究。 电喷雾电离(ESI)原理可按电荷残留模型予以描述,带电液滴蒸发,液滴变小,液滴表面相斥的静电荷密度增大。当液滴蒸发到某一程度,液滴表面的库仑斥力使液滴爆炸。产生的小带电液滴继续此过程。随着液滴的水分子逐渐蒸发,就可获得自由徘徊的质子化和去质子化的蛋白分子。针对电喷雾电离所产生的多电荷状态,Fenn将多电荷状态理解为对分子质量进行多次独立的测量,并基于联立方程解的平均方法,获得对分子质量的正确估量,解决了多电荷离子信息的问题,使蛋白分子质量测量精度获得极大的提高,并于1988年首次成功地测量了分子量为40 kD的蛋白质分子,精确度达到99.99%。
2003年人类基因组精细图绘制完成,是人类科学史上一个里程碑式的事件。后基因组时代的研究重点自然落在了蛋白质头上。为啥?因为中心法则告诉我们,基因的产物——蛋白质,是生命活动的最终执行者。与基因组类比,研究生物体内全套蛋白质的科学,就是蛋白质组学。基因组计划完成的同年,人类蛋白质组计划启动,令人激动的是,2014年人类蛋白质组的草图也完成了。而蛋白质组学能够飞速发展的最大功臣非质谱莫属。质谱的应用范围非常广泛,但这里只讨论蛋白质组学中的质谱。简单地说,质谱法(mass spectrometry)就是对肽段离子的重量(质荷比,m/z)进行测量的分析方法。样品经质谱仪(mass spectrometer)检测得到质谱图(mass spectrum),通过对质谱图的分析就可以对样品中的蛋白进行鉴定、定量。亲,图1的这种典型的蛋白质组学流程都很熟悉吧。蛋白首先都要被特异性的酶(通常为Trypsin)切割为肽段,再进行后续分析,这在蛋白质组学中被称为“自下而上”的研究策略(Bottom-up proteomics)。我们平时见到的质谱分析基本都是这种类型。提到蛋白质组,即会联想到一系列高大上的名词,iTRAQ、SWATH、SILAC、Shotgun、Label-free等等。很多概念容易弄混淆,下面我们就来理理清楚。图1. 典型的蛋白质组学流程大体上,质谱研究蛋白主要是鉴定和定量。通过二级质谱图(MS2或者MS/MS)进行数据库搜索匹配鉴定蛋白。通过各种标记或非标记的手段对不同样品中的蛋白进行比较就是定量。蛋白定量比较是质谱最重要的用途,图2是对定量方法的一个简单总结。非标定量(Label-free)不需要标记,不同样品分别处理、分别进质谱检测;优点是处理简单、无需标记、价格便宜、可以比较很多组样品,缺点是对操作步骤、LC、质谱稳定性要求严格。SILAC是在细胞培养基中加入稳定同位素标记的氨基酸,在代谢水平标记蛋白,一级质谱图进行定量,可以做到三组样品混合后进行比较,定量准确,但是不能标记组织样本,养细胞成本也较贵。双甲基化标记是通过化学反应的办法在肽段水平进行标记,一级质谱定量,也可以三组对比,标记试剂都比较便宜,而且可以标记任何来源的样品。iTRAQ和TMT是商品化的试剂盒,肽段水平标记,二级质谱定量;分别可以做到最多8组和10组样品间蛋白质组的比较。图2. 质谱定量方法以上这几个是一家的,还有几个名词是属于另外一家,比如Shotgun (DDA)、SWATH/DIA、SRM (MRM)、MRMHR/PRM。质谱进行数据采集的方式大致分为三种:鸟枪法(Shotgun)、选择反应监控(SRM)和全景式的SWATH/DIA。下面对照图3再来简单介绍一下。图3. 质谱扫描方式DDA、IDA、Shotgun和鸟枪法说的是相同的东西,意思是质谱在每个循环的中从一级里挑选丰度高的TopN个肽段去打碎做二级扫描,得到的结果通过与已知数据库中的理论蛋白进行匹配。DDA简单有效,分析流程比较成熟,也是目前质谱分析的主流方式。DDA也有其固有的缺陷,即具有一定的随机性,偏向于检测丰度较高的肽段,而抑制了低丰度肽段的检测。靶向策略被称为质谱领域的Western blot。质谱只去采集目标肽段大小的离子信息,因而提高了灵敏度和特异性。这种方法用来研究感兴趣的特定蛋白,定量准确,但是通量很有限。SWATH/DIA这种全景式的数据采集方式在最近几年突然火了起来,被认为在不远的未来可能会取代DDA的主流位置。该方法采取的策略是将扫描范围内的所有肽段按照质荷比分为若干个窗口,再对每个窗口里所有的肽段一起打碎,采二级,数据分析时通过抽提蛋白的子离子信息进行定量。SWATH/DIA解决了DDA中随机性选择肽段的缺陷,所以重复性更好,定量的准确性基本达到了SRM的水平,而且可以实现大规模定量。借用听来的一个比喻来说明:DDA就像机关枪扫射,数量多、体积大的目标命中的概率要大一些。靶向扫描(SRM或PRM)就像精准狙击,排除干扰,目标明确,每一枪直指目标,但是难以大规模消灭敌人。SWATH/DIA就是地毯式轰炸,只要暴露在我方攻击范围内的敌人,不管三七二十一,全部炸完。图4. 定量方法与采集方式结合如果将上述的定量方法(图2)和质谱数据采集方式(图3)结合起来,就得到了现在基于质谱的蛋白质组学研究的各种策略(图4)。再打个比方,保证吃货们一听就懂:鸡、鱼、肉、蛋、蔬菜要通过炒锅、烤箱、高压锅、微波炉等烹调之后才能变为美食,填饱肚子。同样的,各种定量方法(非标的和标记的)处理的样品,要通过质谱各种采集方式变为电脑中的数据,才能分析并从中得到蛋白的信息。本次的介绍就先到这里了,如果其中有什么问题,欢迎您批评和建议,我们会努力变得更好;如果需要跟我们进行技术交流和讨论,欢迎大家联系武汉金开瑞。后续我们还会继续推出对质谱技术各方面进行解析的文章,敬请期待。ReferencesA draft map of the human proteome. Nature 509: 575–581 (2014)Mass-spectrometry-based draft of the human proteome. Nature 509: 582–587 (2014)A review: Annu. Rev. Biochem. 80: 273–99 (2011)SILAC: Molecular & Cellular Proteomics 1: 376-386 (2002)iTRAQ: Molecular & Cellular Proteomics 343: 91–99 (2010)SRM: Nature Methods 9: 555–566 (2012)SWATH: Molecular & Cellular Proteomics 11: 1–17 (2012)
MV_RR_CNJ_0003有机质谱分析方法通则1. 有机质谱分析方法通则说明编号JY/T 003—1996名称(中文) 有机质谱分析方法通则(英文) General principles for organic mass spectrometry归口单位国家教育委员会起草单位国家教育委员会主要起草人郑思定批准日期1997年1月22日实施日期1997年4月1日替代规程号无适用范围本通则规定了有机质谱法分析方法,适用于带有计算机数据处理及控制的质谱仪器。本通则适用于所用仪器规定质量范围内的有机化合物定性和定量分析。本标准包括:有机磁质谱法通则;四极质谱法通则;[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]—离子阱质谱联机方法通则。共三部分。本通则规定了四极质谱法分析方法,适用于带有计算机数据处理及控制的四极质谱及与[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]、液相色谱联机仪器。应具备进样器,色谱与质谱联用所需的接口,离子源,质量分析器,检测器,计算机控制与数据处理系统,真空系统等。本通则适用于仪器规定质量范围的有机化合物定性和定量分析。本通则规定了有机质谱法对离子阱质谱仪的要求和分析方法,本通则适用于仪器规定质量范围内的有机化合物定性和定量分析。主要技术要求1. 定义2. 方法原理3. 试剂和材料4. 仪器5. 样品6. 操作步骤7. 分析结果的表述是否分级无检定周期(年)附录数目无出版单位科学技术文献出版社检定用标准物质相关技术文件备注2. 有机质谱分析方法通则的摘要本通则规定了有机质谱法分析方法,适用于带有计算机数据处理及控制的质谱仪器。本通则适用于所用仪器规定质量范围内的有机化合物定性和定量分析。本标准包括:有机磁质谱法通则;四极质谱法通则;[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]—离子阱质谱联机方法通则。共三部分。3 定义本通则采用下列定义3.1 原子质量单位 Atomic Mass Unit定义C原子质量的1/12为一个质量单位,简写为amu或u。3.2 毫原子质量单位 Milli Mass Unit千分之一的原子质量单位,简写为 mmu,lmmu=1/1000u。3.3 质荷比 Mass to Charge Ratio离子的质量和所带电荷的比值,简写为m/z。3.4 质谱图 Mass Spectrum质谱分析中以质荷比为横坐标,离子的相对强度为纵坐标所作的谱图。3.5 分子离子 Molecular Ion试样分子失去或得到一个电子而形成的离子。它在正离子场合下表示为M+。它的质荷比即表明试样分子所对应的分子量数值。在分子中含不同同位素时,以天然丰度最大者作分子离子。3.6 亚稳离子 Metastable Ion是指离子在质谱仪的离子源中产生,在达到检测器前分解的离子。其表观质量记为m※。3.7 母离子 Parent Ion是指产生某一碎片的前体离子,母离子不一定是分子离子。3.8 子离子 Daughter Ion是指由母子离子裂解后形成的离子。3.9 碎片离子 Fragment Ion分子离子经过裂解后形成的离子。3.10 重排离子 Rearrangement Ion是指质谱过程中产生的与前体离子中原子排列不同的离子。3.11 电子轰击电离 Electron Impact Ionization试样分子在离子源内经电子流轰击电离成离子的方法,简写为EI。3.12 化学电离 Chemical Ionization在离子源内电子流首先使反应气如 甲烷、异丁烷、氨等离子化,然后再与试样分子发生分子离子反应,使试样分子离子化,这种方法称化学电离,简写为CI。3.13 解吸电离 Desorption Ionization通以电流使涂在金属线圈上的试样分子迅速解吸下发生电子电离或化学电离,简写为DEI或DCI。3.14 场致电离和场解吸电离 Field Ionization and Field Desorption Ionization经过活化处理的发射丝,尖端的曲率半径可达微米级,加上高电压后,其附近的场强可达108V/cm,高场强使挥发性的试样分子产生离子化称为场致电离,简写为FI;而把试样涂在发射丝上并通以加热电流在高场强下使样品离子化称为场解吸电离,简写为FD。3.15 快原子轰击电离和二次离子质谱 Fast Atom Bombardment and Secondary Ion Mass Spectrometry快速Ar原子(或Xe原子)轰击涂敷有某种底物靶面上的试样,使试样分子离子化,这种方法称为快原子轰击电离,简写FAB;如用高能量的一次离子如Xe+、Ar+、Cs+来轰击涂敷在靶面上的试样而溅射出试样分子的二次离子来进行质谱分析,称为二次离子质谱法,简写SIMS。3.16 磁式质谱仪 Magnetic Sector Mass Spectrometer是一种使试样分子电离成离子,并通过扫描磁场,使它们按质荷比不同进行分离,并依次检测它们的强度,对它们进行定性和定量分析的一种仪器。3.17 双聚焦质谱仪 Double Focussing Mass Spectrometer是由静电场(E)和磁场(H)所组成的质量和能量分析器的有机磁质谱仪。如静电场排列在前,称为正置式(EH)双聚焦质谱仪,反之,如磁场排列在前,称为反置式(HE)双聚焦质谱仪。3.18 联动扫描 Linked Scanning是在双聚焦磁质谱仪中,加速电压(V)固定,将磁场强度H和静电场强度E的比值保持不变,来扫描不同质荷比的离子,由母离子来找到各种子离子的测定方法以及将H2/E的比值保持不变来扫描,由于离子来找母离子的测定方法,皆称为联动扫描。3.19 碰撞诱导解离或碰撞诱导活化 Collision Induced Dissociation & Collision Induced Activation在电场和磁场中间的无场区,具有较高动能的离子与中性原子或分子(一般为惰性气体如N2,He)发生非弹性碰撞,离子的一部分动能转化为内能,结果导致离子的解离,这种由离子与中性原子或分子碰撞而引起的解离称为碰撞诱导解离或碰撞诱导活化,简写为CID或CIA。3.20 色质联机 Chromatography Mass Spectrometer由色谱仪与质谱仪通过接口构成为整体的一种联用仪器。3.21 色质联用法 Chromatography Mass Spectrometry通过色质联机对物质进行分析的方法,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]与质谱联用分析简写为GC/MS,液相色谱与质谱联用分析简写为LC/MS。3.22 质谱/质谱联用法 Mass Spectrometry/Mass Spectrometry在第一质谱仪中进行离子的质量分离,选择感兴趣的离子在碰撞室中进行解离,得到所选离子的各种裂解碎片谱图。这一过程等于获得一个质谱中某一离子的质谱,称为质谱/质谱法,此类仪器称为串联质谱仪,简写为MS/MS。3.23 总离子流色谱图 Total Ion Chromatogram是未经质量分离的各种质荷比离子,所产生的总电流强度信号与时间相对应的关系图。在色质联用分析时,TIC与色谱分析时各种检测器所得到的色谱图相对应,各峰的面积可作为GC/MS定量分析的依据,简写为TIC。
色谱方法与质谱方法还是有很大区别,除了质谱参数外,就色谱分离这一步,方法转换需要修改哪些内容呢?
[color=#444444]做了两次TOF,有4个杂质没有质谱响应,只有一个杂质有响应,最开始怀疑是浓度太低,增高浓度后,仍检测不出来,目前怀疑是杂质极性太低,用的是ESI源,流动相PH6,弱极性药物。请问下有什么方法可以改善质谱响应???[color=#444444]流动相是醋酸铵10毫摩,药品是个弱碱性的,但是做成了盐酸盐,不知道我应该换酸性还是碱性的流动相。[/color][/color]
仪器名称:气相色谱质谱联用仪 仪器型号:Agilent GC6890-5975I MS 生产厂家:美国Agilent 公司 使用方法: 气相配有顶空进样器、FID检测器;质谱为最新四极杆质量分析器;具体使用方法: 一、开、关机顺序: 开机:通氮气 开电源 设置温度 (柱箱、汽化) 加热 通空气、氢气 点火 调准基线 进样 关机:关氢气、空气 关掉加热器 通者氮气降温至室温 关电源 关氮气 二、温度设定 1、柱温设定(范围:-99℃~399℃) 例如:设置温度为50℃,命令如下 COL/AUX.1 I.TEMP 50 ENT 进样器温度设定(范围:0~99℃) 例如:设置温度为120℃,命令如下 INJ/AUX.2 120 ENT 2、了解温度设定情况 柱温: COL/AUX.1 I.TEMP ENT 进样器: INJ/AUX.2 ENT 3、监测实际温度 柱箱: MONI COL/AUX.1 进样器: MONI INJ/AUX.2 4、设定温度的启动和停止 柱箱温度和汽化室温度设定好后,按START键,开始升温。(要执行程序升温,接着按START键。) 要设定温度控制自动停止,命令如下: 如设定STOPTIME 为5小时 (单位:分钟) SHIFT.D 2/STOP.T 300 ENT
前几天写了个液相的简易流程,朋友看到让我写个质谱方面。那就写吧,因为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]用的多点,拿[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]来说吧。我们已经放假了,长假期该如何操作,保证仪器不受损伤。第一,关机。[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]频繁开关机很不好,我们的仪器只有在维护的时候才关机。关机首先在真空控制中卸真空,降温到合适的温度后关掉工作站,MS,GC依次关,氦气电脑打印机随意。我培训新人经常说的是,开机先开便宜的,后开贵的,关机先关贵的,后关便宜的。关机燃气助燃在仪器前,载气保护气在仪器后,开机反过来。很容易记住。第二,维护,由于日常仪器都是处在运行之中,年前要进行下维护保养,平常不容易碰到的离子源,经常碰到的进样口检测器等,该清洗清洗,好像网上也有很多视频。我的建议是,拆的时候录像或者拆一个拍一张,装的时候就有参照了。另外提前拿一干净盘子在旁边,零件什么的及时放里面,防止掉落。顺便还可以除除尘,如果有仪器套膜可以罩上防尘。曾经有人问我,进实验室为什么要换鞋?你买的又不是防酸碱鞋,咱们又不是洁净室。其中一个原因是,灰尘是很多仪器的天敌,鞋底带入的灰尘相对比较多,所以最好换鞋。色谱和质谱类进样按照说明书都能操作,但是再解析有人就很懵了。怎么那么多方法,那么多文件。我这里有一个简单易懂的程序。质谱和色谱都可用的第一种,先走一个高浓度的标准物质,这时的方法是你设置的方法,没有带任何信息的方法。走完之后定性,不管是质谱离子对定性还是色谱保留时间定性,可另存一个定性方法。这时色谱质谱设置标准物质点数,浓度,质谱设置SIM方法,我们称之为定量方法,然后拿定量方法去走序列,可直接得出曲线和样品浓度。第二种,色谱的,可以先设置方法,不带信息的那种,走序列,走完之后拿其中一个点保留时间定性,浓度点定量,保存为定量方法,在再解析里用定量方法处理一遍序列,可得曲线和浓度。有时需要走完标准曲线确定定性方法,建立标准曲线,然后根据处理标准曲线得到的定量方法,用它去处理样品。根据不同的工作站和仪器进行操作。OK。任务完成,都是基本操作,有不同意见或者有更好的处理方法请留言,多谢。
用于研究蛋白,核苷酸还是小分子,这里也许有理想的答案 正如其它先进的技术一样,质谱技术冲击带来了市场的膨胀,造成了多选择性的产品,专业性的术语,这也就无形中增加了研究人员选择合适于他们的系统的困难性。正如西雅图Fred Hutchinson癌症研究中心蛋白组主任Philip Gafken所说的那样,“无论大家相信与否,这种技术并没有如它们所被应用的那样被逐渐的了解,研究人员没有认识到利用这种技术的真正目的。”比如说三级四极质谱仪(Triple Quadrupole Mass Spectrom)是一种相对便宜一点,但扫描速率(scan rate)也相对比较慢的质谱仪,而目前精良的傅立叶变换离子回旋共振质谱仪(Fourier transform ion cyclotron resonance,FTICR)则在精确性和分辨率都是首屈一指的,当然价钱也会比较贵。Gafken说道,“人们总是倾向于购买一些顶级的产品,但是事实上,这些应用中很大一部分都能由一些相对便宜一点的仪器来完成”,所以我们需要购买适用于各自需要的正确仪器。1.Protein Chemist级分析对于protein chemist而言,需要得到的仅仅就是知道他在研究的是什么。通过分析一种蛋白的免疫共沉淀的成份,或者利用二维电泳识别特殊的蛋白斑点,protein chemist就可以了解这种蛋白质的生物学特性了。对于这种应用,快速而并不需要太精确的方法就可以满足需要了。[color=#DC143C]推荐系统:MALDI+TOF[/color]理由:肽指纹图谱(PePtide Mass Fingerprinting,PMF)和基质辅助激光解析电离飞行时间(matrix-assisted laser desorption ionization-time of flight,MALDI-TOF)质谱是可以考虑的首选方法。TOF是一种简单的质谱分析系统,灵敏度高,能进行从10原子质量单位到上百上千单位的片段分析。另一个TOF的优点就是分析的速度,伊利诺斯大学的化学副教授Neil Kelleher就表示“这就是它为什么能与MALDI配合工作的原因,你可以以一种高重复率在激光上操作,每秒获得许多光谱。” 而MALDI则是一种首先就可以考虑的方法,但是并不适合如何人,来自华盛顿大学的化学教授,Journal of the American Society for Mass Spectrometry杂志的编辑Michael Gross就说,“如果你的免疫共沉淀中有20或30个蛋白,每一个有50条特殊带,那么你就有1000条带,利用MALDI并不能在[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中打到全部的”,为了得到更多的信息,必需要考虑一个可以提供序列详细信息的任意构造,比如MALDI-TOF-TOF,或者一个更加灵敏的仪器——离子捕获。 2. 灵敏级 难题总是出在事实本质的详细内容当中,对于蛋白而言,那就是指翻译后修饰了。比如说,假设你正在研究包含有乙酰化和三甲基化修饰的组蛋白,但是一个标准的质谱也许无法区别出这两种修饰,这时就需要高精度的仪器了,这种仪器能获得二位或者四位小数位的报告。 推荐系统:[size=4]LC+ESI+FTICR with ECD[/size]理由:准确度高的仪器可以区别对于所谓的正常(nominal-mass)仪器而言相同的分子,一般认为选择液相色谱(liquid chromatography,LC)与电喷雾电离化(electrospray ionization,ESI),以及傅立叶变换离子回旋共振质谱仪(Fourier transform ion cyclotron resonance,FTICR)相结合能达到高精度和高灵敏度的要求。也许还需要电子捕获解离技术(electron capture dissociation,ECD)来获得可重复的结果。虽然经典的碰撞诱导解离技术(collision induced dissociation,CID)介导的串联质谱方法可以进行斑点修饰(spot modifications),但是对于识别包含了修饰的蛋白残基而言,这并不是一种理想的方法,这主要是由于解离蛋白的时候常常会降解多肽的蛋白修饰,然而ECD则可以保持这种修饰的完整性。不过来自辛辛那提大学的Patrick Limbach提出一个忠告:这些仪器偏差范围小,因此可能会丢失掉一些未预期到的情况,比如天冬酰胺残基的脱酰胺,或者磷酸化。 3.边缘分析级 并不是每一人都对蛋白质感兴趣的,比如说,也许你想知道的是一种特殊的核酸是否包含了不同寻常的或是修饰了的残基(比如methyl-C),以及这些序列定位在那儿。回到这两个问题也许就需要利用到LC-ESI串联质谱(LC-ESI-tandem mass spec),对于前面那个问题需要在负电荷模式里——因为核苷酸是带负电荷的,而后者则需要正电荷模式。 推荐系统:[color=#00008B]LC+ESI+ION TRAP 或 QUAD+TOF [/color]推荐理由:Limbach博士在进行其核酸实验的时候使用的是LC-ESI线性离子阱(LC-ESI-linear ion trap),LC-ESI-QTOf(quadrupole time of flight hybrid,杂交四矩飞行时间) 质谱两种技术,他指出,“你有哪种特殊的串联质谱并不是关键问题,关键是你需要哪种串联MS功能”,比如要想完成能识别修饰,以及确定多聚核苷酸链中修饰定位在哪儿这两项任务。在这种串联质谱模式中,可以检测离子,降解(比如CID或ECD),然后获得序列以及结构的信息,但是串联质谱并不是都一样的。来自Scripps研究院的细胞生物学家John Yates表示,线性离子阱速度很快,“要比QTOf快许多,但是分辨率和质谱精度要低一些”。但这两种相对于FTICR仪器而言,都是比较便宜的选择。这些都是值得推荐的质谱方法,当然也要考虑相对慢和灵敏度低的缺点,因此需要一个超导磁(superconducting magnet)和有经验的操作人员。4.混合分析级 对小分子代谢物(比如糖类,脂质)进行详细的分析需要一套不同的仪器设备,也许你就在这个探索的过程中——寻找一种特殊疾病或者药物有效性的生物标记,那么你需要的是能明确得到化学结构的串联质谱分析能力,可供选择的就是LC-ESI-triple quad。但更重要的是,你还要借助多离子方法撒开更广的网,因此我们可以考虑两种选择:APPI(大气压光离子,atmospheric pressure photoionization),和APCI(大气压化学电离,atmospheric pressure chemical ionization)。 推荐系统:[color=#DC143C]LC+ESI+triple quad with multiple ionization sources [/color]推荐理由:APCI可以利用溶剂中的化学成份使样品电离,Limbach表示,“比如说我有一个样品在甲醇/水的溶液中,(APCI)就可以利用甲醇或者水分子发生化学反应电离样品,这样透射入光,光化学产生离子”,当然正如MALDI和电喷雾不能精确电离同样的分子,APCI和APPI也不行。 5. 计算分析级 一旦你识别了所需的生物标记,也许就需要在成百上千的生物样品中对其进行评估计算,可以考虑的定量应用分析仪器就是triple quad——与液相色谱和电喷雾离子化串联使用。Gafken就认为,“triple quads的关键用途就是真实定量,虽然有许多对蛋白和多肽进行定量,但是如果你需要的是绝对定量,那么最好的方法就是triple-quad仪器。” 推荐系统:[color=#00008B]LC+ESI+triple quad with single or multiple reaction monitoring [/color]推荐理由:Limbach认为,“Quadrupoles(四极)实际上是滤波器,就像是无线电装置一样运转:你调出一个频率,就会有一个特殊的离子传出,这样你就可以扫过这些无线电转盘(radio dial)获得离子,其它的一切都会被剔除”。这些仪器的优势就在于可以进行一个或两个离子频率的扫描(即质荷比(mass-to-charge),m/z),缺点就是对于在许多研发模式工作中需要的高m/z扫描而言太慢了。 但是怎么知道所观测到的离子就是你想要的呢?在任何生物样品中,几个离子也许有相同的m/z值,这就需要single-reaction monitoring介入,Gross认为,“这就能克服第一quad和扫描的慢速问题,因为你知道什么是你想要的”,比如说你的特异分子有m/z1000,m/z300片段离子,你就可以设置第一quad为m/z1000滤波器离子,在第二个quad中将其断裂,然后在第三个quad中对其进行计算(m/z300)。而在multiple reaction monitoring,则可以将仪器设置成“hop”——从一个m/z值到另一个,因此可以同时计算2个,或者3个分析组。
质谱方法(Mass Spectroscope,MS)是通过正确测定蛋白质分子的质量而进行蛋白质分子鉴定、蛋白质分子的修饰和蛋白质分子相互作用的研究。质谱仪通过测定离子化生物分子的质荷比便可得到相关分子的质量。但长期以来,质谱方法仅限于小分子和中等分子的研究,因为要将质谱应用于生物大分子需要将之制备成[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]带电分子,然后在真空中物理分解成离子。但如何使蛋白分子经受住离子化过程转成[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]带电的离子而又不丧失其结构形状是个难题。20世纪70年代,解吸技术的出现成功地将蛋白分子转化成[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]离子。尔后快原子轰击与其紧密相关的溶液基质二次离子质谱法使得具有极性的、热不稳定的蛋白分子可经受住电离过程。但这些方法仅限于10kD以下蛋白分子的研究。80年代电喷雾电离(ESI)和软激光解吸(SLD)电离技术的发展则使得质谱方法应用于高分子量蛋白分子的研究。 GtqA@&5& ueJ_F#y 电喷雾电离(ESI)原理可按电荷残留模型予以描述,带电液滴蒸发,液滴变小,液滴表面相斥的静电荷密度增大。当液滴蒸发到某一程度,液滴表面的库仑斥力使液滴爆炸。产生的小带电液滴继续此过程。随着液滴的水分子逐渐蒸发,就可获得自由徘徊的质子化和去质子化的蛋白分子。针对电喷雾电离所产生的多电荷状态,Fenn将多电荷状态理解为对分子质量进行多次独立的测量,并基于联立方程解的平均方法,获得对分子质量的正确估量,解决了多电荷离子信息的问题,使蛋白分子质量测量精度获得极大的提高,并于1988年首次成功地测量了分子量为40 kD的蛋白质分子,精确度达到99.99%。 {0} Q5 p@=B\A] 软激光解吸(SLD)是指从激光脉冲中获得能量后,样品分子以完整的低电荷分子离子释放,然后由电场加速。运用激光解吸电离蛋白分子时,激光的能量和波长、化学/物理基质的吸收和热传递特性,与基质中分析物的分子结构之间需要作合理的选择调配。Tanaka选用了低能量氮激光和含有胶状颗粒的甘油作基质,成功地测定了高分子量的糜蛋白酶原、梭肤酶-A以及细胞色素。由于Tanaka成功的开创性工作,SLD技术迅速发展。目前占主导的方法是基质辅助激光解吸电离(MALDI)。这一方法是将样品掺入一种低分子量的结晶基质,基质的最大吸收与激光脉冲波长匹配。由于MALDI产生的是低电荷的完整[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]大分子,可用于检测纯度不高的生物分子。MALDI与飞行时间(TOF)联合已经成为鉴别大分子的重要方法,成为鉴定细胞内蛋白组分不可或缺的研究手段。
请问各位大佬,我目前只用过thermo的QE与obitrap 480质谱测蛋白,发现两个质谱软件的方法界面与调谐软件的界面很不一样。然后我要开始学QE HFX的界面,想请教各位大佬,HFX的界面与QE一样吗?有没有什么区别呀?跪谢大家
液相色谱-质谱同时对242种化合物的定性筛查方法 作者倪春芳,耀 刘,叶海英,张润生,张玉荣,...本发明公开了一种可同时对242种化合物(药物或毒物)进行定性筛查的方法。采用液相色谱-质谱联用(LC-MS/MS)多反应监测(multiple reaction monitoring,MRM)方式以两对母离子-子离子对和保留时间对目标物进行定性。242种药毒物包括阿片类、苯丙胺类、可卡因...这篇文献我搜不到 现在想向诸位求助
[align=center]API质谱仪MRM定量方法的建立方法[/align] 质谱仪凭借其高灵敏度和选择性,定量小分子化合物越来越受到重视。MRM:Multi Reaction Monitor,指多反应监测。针对二级质谱或多级质谱的某两级之间,即母离子选一个离子,碰撞后,从形成的子离子中也只选一个离子。因为两次都只选单离子,所以噪音和干扰被排除得更多,灵敏度信噪比会更高,尤其对于复杂的、基质背景高的样品。那么我们今天来分享一下API质谱仪MRM定量方法的建立方法。 首先选择Q1 FULLSCAN:用SYRINGE PUMP 5ul/min,样品浓度约1-10pmol/u,根据待测化合物性质选择+- ESI/APCI/APPI。根据待测化合物分子量选择扫描范围:在分子量上下各100Da足够,TIME不要小于1秒。通过调节DP,使得分子离子峰明显高于噪音峰,确定分子离子。如果分子离子峰不明显,可能需要增加样品浓度,如果仍然不能确定分子离子,考虑改变离子化方式或样品前处理方法,例如POS方式可酸化溶液,NEG方式碱化溶液。对于某些化合物,POS方式[sup]+[/sup]不明显,可考虑[M+NH[sub]4[/sub]][sup]+[/sup],尽量避免采用[sup]+[/sup],[sup]+[/sup]。 第二步选择Q1 MI SCAN:TIME 100ms,用SYRINGEPUMP 5ul/min,根据第1步选择的母离子,EDIT RAMP优化DP,CXP及EP,存储此参数。 第三步选择PRODUCT ION SCAN,用SYRINGE PUMP5ul/min,扫描范围:上限比母离子高10-50 Da,下限50-100 Da,TIME 不小于1s。通过调节CE等参数得到高质量的MS2图,母离子相对峰高在1/4-1/2即可。Acquire命名 MCA20次,平滑后选择特征子离子。 第四步选择MRM优化,用SYRINGE PUMP5ul/min。根据特征子离子强度选择MRM离子对,母离子M/Z值由第1步确定,子离子M/Z值由第3步确定,精确到小数点后1位。可选择多个MRM离子对,同时优化,对较弱离子对可适当多分配TIME例如200 ms,强离子对可40-50 ms。同时EDIT RAMP优化COMPOUND项下参数先根据第3步的CE优化CXP,然后再优化CE,在质量扫描范围窗口点右键对各离子参数分别设定。CAD参数可手动优化,值不要太高,通常4-6。初步建立METHOD,存储为*.dam文件。 第五步不接色谱柱进行FIA定量优化。首先接通LC系统,检查工作是否正常,有无气泡,否则先排气。激活CONFIGURE中[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]配置。在ACQURE栏内调出第3步初步建立的METHOD,若已经有LC条件,则可参考,若无根据拟选用的色谱柱内径确定LC流速(2mm典型流速200-300ul/min,3mm典型流速400-500ul/min,4.6 mm典型流速800-1000ul/min)以及流动相组成,设定MS初始温度和气流,加上LC PUMP和AUTOSAMPLER,并设定同步方式为LC SYNC。 第六步使用4mm以上内径色谱柱时先设定分流比,使进入MS的流量在200-400ul/min最佳。MS与LC的period都设为0.5-1min,进样体积2-5ul,浓度0.01-0.1pmol/ul,按照FIA教程操作,优化CUR,GAS1,GAS2(API3000AUX要手动优化),TEMP,IS。平衡5 min后开始进行FIA定量优化,完成最后方法的质谱条件优化。 第七步接好并平衡色谱柱,至少20min,用适当浓度标准品检验峰型等分离情况。根据色谱分离情况,可设定梯度洗脱。MRM可以不必所有峰都基线分离,但要避开基质的离子抑制干扰(出峰时间不能太早,要在溶剂峰后)。 第八步空白基质添加标准品,稀释成不同浓度,通常可2倍等比稀释,5-7级。根据LC流动相选择溶剂体系一致的稀释液,配制实际样品。编辑批处理文件,排列进样顺序,最好第一针先做空白,然后由稀到浓。平衡MS离子源和色谱柱后开始正式采样。 以上是一种化合物的定量方法,如果多种物质同时定量(包括内标),分别用纯标样重复第2-4步,记录各参数,然后合并到第5步最后的METHOD,再进行第6-8步。完成上述所有步骤后,即可制做标准曲线。如果不能自动正确积分色谱图,可手工修改。有内标和无内标的计算方法分别演示。最后结果的打印和存贮,复制。 今天的分享到此结束,感谢仪器信息网提供原创大赛让我们有机会互相分享学习!
请教电喷雾质谱的解谱方法
赛默飞多款质谱新品闪耀2012美国质谱大会中国上海,2012年6月12日 – 5月20-24日,第60届美国质谱会(ASMS 2012)在加拿大温哥华举行,来自全世界各地的从事与质谱领域相关的科研人员、专家学者以及业内人士参加了此次盛会。作为全球服务科学的领导者,赛默飞世尔科技(以下简称:赛默飞)在此次大会上展示了出众的质谱系列产品。除了在业内久负盛名的仪器及耗材外,赛默飞此次还展示了有助于大大提高仪器性能以及实验室效率的系列软件系统。“我们领先的质谱技术不仅帮助客户在医学研究方面不断取得重要发现,还能够满足环境和消费者安全测试领域不断增长的需求,”赛默飞总裁及首席执行官Marc N. Casper说道,“正如我们的客户一样,我们从未停止创新,质谱大会上新软件的发布将会把赛默飞Orbitrap平台带入新的水平,尤其是Elite和Q Exactive系统。在如今的经济环境下,许多实验室面临资金压力,但是更需要优质的实验结果。赛默飞将利用我们业内领先的仪器及软件系统,致力于帮助客户解决分析结果及成本控制的双重挑战!”赛默飞在2012美国质谱大会(ASMS)上发布的产品、技术、软件及解决方案包括: TargetQuan 3数据处理软件:该软件专为实验室对持久性有机污染物(POPs)的数据分析和报告设计。TargetQuan 3数据处理软件只需进行样品批处理的简单操作,并整合至日常POPs的实验室流程中,省时并减少得到报告的时间。除了应用于传统的高分辨率技术,该软件还可用于分析三重四极杆仪器得出的数据,对同位素稀释进行定量。 Thermo Scientific HiPPR 去污剂去除树脂:这是一款可高效去除蛋白质和多肽中去污剂的工具,特别适用于处理浓度介于10-150微克之间的蛋白样品。这款高性能 HiPPR 树脂的去污剂去除率高达95%,可去除浓度范围在0.5%到1%的离子型、非离子型或两性离子型去污剂。 Thermo Scientific 一步法重标蛋白体外表达试剂盒:该试剂盒可快速实现蛋白的无细胞表达,并在新合成的蛋白中掺入带有稳定同位素标记(如重同位素)的氨基酸。用此试剂盒表达出的重标蛋白可用作质谱分析中的对照,以确定蛋白水解效率、样品制备过程的差异和蛋白富集程度,8 小时内便能完成同位素掺入率达90-95%的蛋白质的合成。 Thermo Scientific SILAC蛋白定量产品线扩充产品:此次,赛默飞推出了新款氨基酸和培养基产品,进一步扩充了Thermo Scientific SILAC蛋白定量产品线。在细胞培养中, SILAC是一种对复杂蛋白样品进行差异定量的有力工具。SILAC方法通过体内代谢将“重同位素”(13C-或15N-)标记的氨基酸整合到蛋白中,再通过质谱(MS)分析以加快对蛋白的鉴定、分析和定量。 Thermo Scientific EASY-Spray 解决方案:该方案实现了对EASY-SprayTM 柱与EASY-Spray 离子源的整合,可轻松获得“即插即喷”纳升级液相色谱-质谱联用(LC-MS)的出色性能。不同于其他类型的整合纳升级 LC-MS 解决方案,易于使用且高度可靠的 EASY-Spray在柱装载方面没有限制,能够在高达1000巴的情况下展现最佳性能。 新款 Accucore™ C8 HPLC色谱柱:采用最先进的Core Enhanced Technology™ 技术制作,新款 Accucore™ C8 HPLC色谱柱不仅提供了比同等C18反相柱更低的疏水保留功能,还以更短的烷基键合相产品丰富了Accucore HPLC色谱柱家族。新反相柱提升了色谱表现,并可避免产生过多操作压力,提升了实验室的生产量及产品质量。 Acclaim™ Surfactant Plus色谱柱:该产品专为使各种表面活化剂进行高分辨,高效能,高通量的单程分离而设计,上述非离子、活性阴离子、阳离子和两性氧化物等表面活化剂在杀虫剂、洗涤剂、石油产品、化妆品和医药品中得到了广泛应用。依靠新颖的混合型色谱技术,Acclaim™ Surfactant Plus光谱柱实现了更多选择性。其先进的表面改性工艺使其在Corona电雾式检测器(Corona CAD)、质谱仪(MS)或蒸发光散射检测器(ELSD)协同工作时表现出优异的兼容性。 Thermo Scientific MAbPac™ SCX-10小径粒度色谱柱:该产品粒径大小为3µm和5µm,可用于分离极相近单克隆抗体的变种,甚至能够分辨单个带电残基的微小不同。新色谱柱不但具有可比拟10µm粒度色谱柱和Thermo Scientific ProPacWCX-10 4 x 250mm色谱柱的分离高效性,还实现了更快速的分析和更短的分离时间,以及柱与柱之间和批次之间出色的重现性。 Thermo Scientific SOLA固相萃取(SPE)小柱和提取板:SOLA™小柱和提取板实现了更高重复性、更低洗脱体积,提高了灵敏度,并且减少了污染物和洗出液样本萃取物中的杂质。SOLA™小柱和提取板的设计是针对传统SPE样式的一次重大革新,它消除了排空、通道和填压不一致的问题,使得实验结果具有高度的可重复性。这还意味着更少的故障,避免昂贵的重新分析,满足了的高产量的实验室环境,解决了关键性的需求。 Thermo Scientific Titan3和Target2针头过滤器:Titan3 和Target2系列的针头过滤器采用一种新型稳固设计,提供更强大的爆破压力和优异的流动特性,这极大地提升了样品制备的工作流程。此外,新设计中恰当定位的薄膜和优化后的表面积实现了更高效的过滤能力。Titan3系列的新增设计,提供了更好的爆破压力,使30mm模式下可承受120psi的压力。 Thermo Scientific TRACE 1300系列气相色谱产品:该系统拥有独特的插拔式进样口及检测器,方便用户快速更换,直观的界面,可生成可靠的结果和最高灵敏度。TRACE 1300系列气相色谱有两种型号,分别为TRACE 1300气相色谱和 TRACE 1310气相色谱。TRACE 1300 气相色谱是预算受限实验室进行常规分析时的最佳选择;系统简化的界面无需过多用户参与,可在极少工作人员照看的情况下全天候连续运行。TRACE 1310 气相色谱专为常规 QA/ QC或侧重方法开发的实验室设计,特别配有带图标的触摸屏,可实现更精确的控制。
氦质谱检漏方法比较多,根据被检件的测量目的可以分为两种类型,一种是漏点型,另一种是漏率型 在实际检验过程中要根据检验的目的选用最合理的方法,要以被检器件的具体情况而定,灵活运用各种检漏方法。1、测定漏点型氦质谱检漏方法确定漏点型既是确定要检部件的具体漏点或漏孔的位置,在大部件或大型部件中较为常见,如卫星、导弹弹体、弹头、输气管道、气罐、油罐、锅炉等。1.1、喷氦法氦质谱检漏方法这是最常用的一种方法,一般用于检测体积相对较小的部件,将被检器件和仪器连通,在抽好真空后,在被检器件可能存在漏孔的地方(如密封接头,焊缝等) 用喷枪喷氦,如图4 所示,如果被检器件某处有漏孔,当氦喷到漏孔上时,氦气立即会被吸入到真空系统,从而扩散到质谱室中,氦质谱检漏仪的输出就会立即有响应,使用这种方法应注意:氦气是较轻的惰性气体,在喷出后会自动上升,为了准确的在漏孔位置喷氦,喷氦时应自上而下,由近至远(相对检漏仪位置) ,这是因为在喷下方时氦气有可能被上方漏孔吸入,就很难确定漏孔的位置 再者漏孔离质谱室的距离检漏仪反应时间也不同,所以喷氦应先从靠近检漏仪的一侧开始由近至远来进行。常用的几种氦质谱检漏方法-无眼界科技喷氦法检漏示意图在检测较大部件时要借助机械泵进行真空预抽,就可以提高检漏效率和时间,如图所示,喷氦法在检查那些结构比较复杂的,密封口和焊缝又比较多而且挤在一起的小容器时,由于氦喷出后会很快扩散开来,往往不容易准确地确定漏隙所在的部位,要采取从不同角度喷氦,仔细观察反应时间上的差别和将已发现的漏孔用真空封泥暂时封起来等办法,就可以把漏孔逐个检出。常用的几种氦质谱检漏方法-无眼界科技辅助机械泵检漏示意图1.2、吸氦法氦质谱检漏方法吸氦法主要用于检查某些大型密封容器。如导弹弹体、弹头、气罐、油罐等,先将容器抽真空,再给容器充入氦气(为了节省用氦量,可以用低浓度氦气) ,在氦质谱检漏仪的进气法兰处接上橡皮管,橡皮管的前端有直径很小的毛细管,使毛细管在充了氦的被检容器外壁的焊缝和密封接头等处移动,如果该容器有漏隙,经漏隙渗出的氦会被毛细管吸入,检漏仪就会响应。2、测定漏率型氦质谱检漏方法吸氦法检漏示意图图片测定漏率型主要是针对密封性要求严格的部件进行检测,如宇宙飞船、火箭液体燃料储料箱、卫星、电子元器件等。这种方法只能测试试件的漏率,无法确定漏孔的位置和漏孔的个数。
不是吹扫捕集合,专门的顶空质谱的epa,或者水利部,或者iso的方法
同种物质,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]质谱EI模式下的质谱图可以参考液相质谱的电喷雾模式的二级质谱图吗
如题 同种物质,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]质谱EI模式下的质谱图可以参考液相质谱的电喷雾模式的二级质谱图吗
请各位高人指点一下基本的质谱制样方法,或者给个资料链接也好啊,多谢了!
编辑完方法后等待所有条件已Ready,开始进样后,液相各个模块正常运行,但质谱变成预运行PreRun状态,请问这是怎么回事?我的仪器是安捷伦1260-6460液质系统
请问您合并过质谱谱库吗?或者转移过质谱谱库吗?用什么方法?
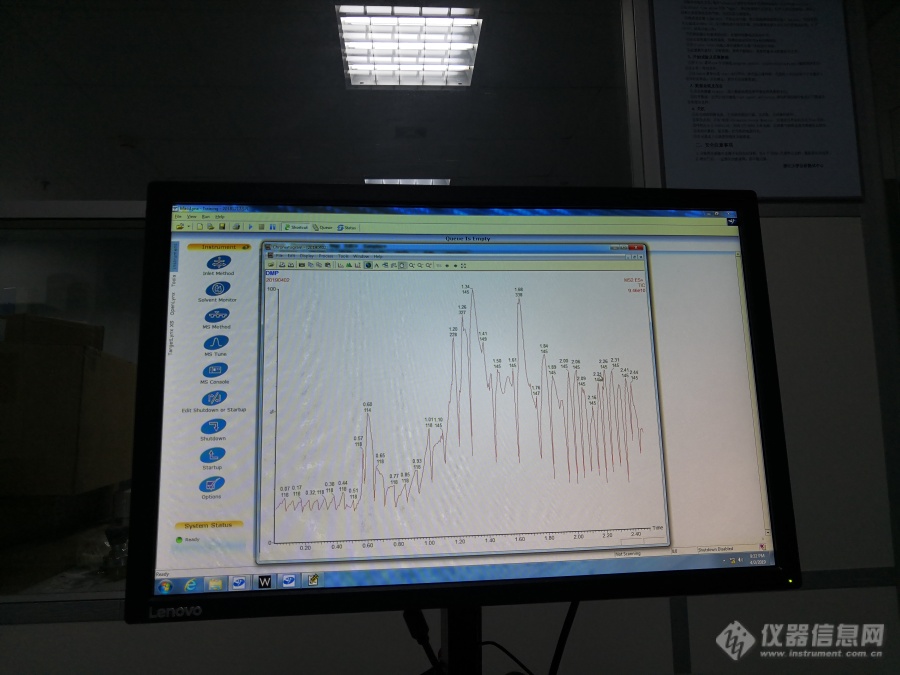
在读研究生一枚刚刚开始接触[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url],做方法开发。老板让我先把混标全扫摸液相条件,可是我全扫后如下图,为何出来的图都是几种一样质和比的响应呀?有点看不懂我自己的理解是先用单标去摸质谱参数cone和CE之类了,再从液相走,用MRM模式下去摸液相条件。请老师们替我解答一下疑惑。[img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/04/201904030930433873_794_3613642_3.jpg!w690x517.jpg[/img]
实验室有哪些清洗质谱配件的方法?
提高质谱灵敏度的方法有哪些?
原标题:英开发出质谱成像技术运用新方法 推动癌组织分析进入数字时代 在癌症研究领域,质谱成像(MSI)是一种非常有前途的技术,但目前该技术的运用还受原始数据预处理、图像精确度及图像识别能力等问题限制。英国帝国理工学院近日发布新闻公报称,该校研究人员开发出一种新方法,可有效解决上述问题。新方法将改变病体组织的检测方式,从而推动癌症组织分析进入数字时代。相关研究成果刊发在最新一期《美国国家科学院院刊》上。 质谱成像技术主要是利用质谱直接扫描生物样品,分析化学成分在细胞或组织中的结构、空间与时间分布信息。这种成像方法不局限于特异的一种或几种蛋白质分子,可在生物组织样本中找到每一种蛋白质分子,并提供它们在组织中空间分布的精确信息。早在几年前,就有科学家提出利用该技术来确定生物组织类型的构想,但却一直没有设计出实用有效的方法。 新方法利用解吸电喷雾电离技术来优化数据预处理,提高图像精确度,并通过提取生物组织特定的分子印记来强化不同生物组织类型的生化特性,以增强图像识别能力。研究人员称,利用新开发的集成生物学信息平台,可将质谱成像技术获得的大量人体组织的具体信息数据,用于构建各种类型的组织数据库。通过多样本分析,并与传统的组织学分析结果进行比较,计算机就可以学习识别不同类型的组织,从而使癌变组织的解析变得相对简单高效。他们将自己设计的工作流程用于直肠结肠癌组织的检测,效果良好。 与标准组织学动辄几周才会得出完整结果的检测手段相比,利用质谱成像技术进行单一检测,仅需几小时即可获得更详尽的信息,不仅会显示组织是否发生癌变,还会显示癌症是哪一种类型和亚型。这些信息对于医生选择最有效的治疗方法十分重要。 研究人员指出,自19世纪后期染色技术用于显示组织结构以来,对组织病理学样本的分析方法鲜有变化。直到今天,染色法依然是医院组织学分析的主流手段,并且变得越来越复杂,耗费也越来越高。而质谱成像技术可能改变组织学的基本范式,科学家将不再根据组织的结构,而是根据它们的化学成分来定义组织类型。将来的检测不再依靠专家的眼睛,而是以海量数据为基础,仅一个检测所得到的信息就远比多个传统组织学检测所得到的更多。他们表示,新研究克服了一些质谱成像技术实际应用所遇到的障碍,将成为创建下一代完全自动化的组织学分析手段的第一步。 总编辑圈点 这是用互联网思维改造传统检测方法的一种尝试,它首先选取了质谱成像方法中最容易快速成像的解吸电喷雾电离技术,实现了数据快速采集;其次,通过将质谱成像得到的结果数字化,建立样本库,提高了数据规模,保证了分析精度;最后,与大数据、云计算等结合,可不断提高检测的准确性,为可靠应用提供保证。新思维已经提高了单个样本的检测精度,我们对它在群体和地区性疾病的检测预防方面也应有所期待。
提高质谱灵敏度的方法有哪些?
各位亲,在临床质谱方法开发中都有哪些经验,有时间可否互相交流学习学习呢?
如何选择质谱分析方法?——是用于研究蛋白,核苷酸还是小分子,这里也许有理想的答案 正如其它先进的技术一样,质谱技术冲击带来了市场的膨胀,造成了多选择性的产品,专业性的术语,这也就无形中增加了研究人员选择合适于他们的系统的困难性。正如西雅图Fred Hutchinson癌症研究中心蛋白组主任Philip Gafken所说的那样,“无论大家相信与否,这种技术并没有如它们所被应用的那样被逐渐的了解,研究人员没有认识到利用这种技术的真正目的。”比如说三级四极质谱仪(Triple Quadrupole Mass Spectrom)是一种相对便宜一点,但扫描速率(scan rate)也相对比较慢的质谱仪,而目前精良的傅立叶变换离子回旋共振质谱仪(Fourier transform ion cyclotron resonance,FTICR)则在精确性和分辨率都是首屈一指的,当然价钱也会比较贵。Gafken说道,“人们总是倾向于购买一些顶级的产品,但是事实上,这些应用中很大一部分都能由一些相对便宜一点的仪器来完成”,所以我们需要购买适用于各自需要的正确仪器。1.Protein Chemist级分析对于protein chemist而言,需要得到的仅仅就是知道他在研究的是什么。通过分析一种蛋白的免疫共沉淀的成份,或者利用二维电泳识别特殊的蛋白斑点,protein chemist就可以了解这种蛋白质的生物学特性了。对于这种应用,快速而并不需要太精确的方法就可以满足需要了。推荐系统:MALDI+TOF理由:肽指纹图谱(PePtide Mass Fingerprinting,PMF)和基质辅助激光解析电离飞行时间(matrix-assisted laser desorption ionization-time of flight,MALDI-TOF)质谱是可以考虑的首选方法。TOF是一种简单的质谱分析系统,灵敏度高,能进行从10原子质量单位到上百上千单位的片段分析。另一个TOF的优点就是分析的速度,伊利诺斯大学的化学副教授Neil Kelleher就表示“这就是它为什么能与MALDI配合工作的原因,你可以以一种高重复率在激光上操作,每秒获得许多光谱。” 而MALDI则是一种首先就可以考虑的方法,但是并不适合如何人,来自华盛顿大学的化学教授,Journal of the American Society for Mass Spectrometry杂志的编辑Michael Gross就说,“如果你的免疫共沉淀中有20或30个蛋白,每一个有50条特殊带,那么你就有1000条带,利用MALDI并不能在[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]中打到全部的”,为了得到更多的信息,必需要考虑一个可以提供序列详细信息的任意构造,比如MALDI-TOF-TOF,或者一个更加灵敏的仪器——离子捕获。