推荐厂家
暂无
暂无
各位前辈,小妹在提取的丹参的之后对照品和供试品不能在同一位置上,对照品总是比供试品高一个点的位置。但颜色、形状都基本相同,想求助各位帮忙解答。[em0905]
药典中丹参的含量测定是用的一测多评法,要求如下,我测得丹参酮IIA在14.027,隐丹参酮在10.573,溶剂峰时间在2.123(我是看的第一个出峰的时间,不知道对不对),请问1.相对保留时间应该是10.573/14.027=0.7537606045,还是(14.027-2.123)/(10.573-2.123)或者有其他算法。2.如果是算法二,相对保留时间就不符合药典规定,我进了一针对照品,隐丹参酮对照品出峰时间在10.363,对照品也不在规定的相对保留时间内,我想问相对保留时间不符合药典,但是我通过对照品能确定是该物质,能用药典规定的校正因子计算含量吗?3.丹参酮IIA理论踏板数不低于60000,是指在供试品中的丹参酮IIA,还是指对照品,我的理论踏板数只有49000,这样计算出的含量能算正确吗?4.药典规定的测定温度为20度,流速为1.2,我能改动的范围怎么计算?恳请各位不吝赐教!
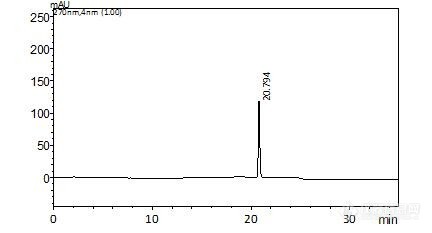
[align=center][b][font=宋体][color=#333333]近期测外样发现丹参对色谱柱的柱效及柱温要求很高,现对实验中注意的问题做一下讨论:[/color][/font][/b][/align][font='Times New Roman', serif]1[/font][font=宋体]材料[/font][font=宋体]丹参药材(送检样);乙腈(色谱级),甲醇、磷酸(分析纯);丹参酮Ⅱ[/font][font='Times New Roman', serif]A[/font][font=宋体]对照品(购自中检院)。[/font][font='Times New Roman', serif]2 [/font][font=宋体]仪器与设备[/font][font=宋体]岛津[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url][/font][font='Times New Roman', serif]LC-20AT[/font][font=宋体]配制[/font][font='Times New Roman', serif]UV/DAD[/font][font=宋体]检测器,安家[/font][font='Times New Roman', serif]Eclipse XDB C18[/font][font=宋体]色谱柱[/font][font='Times New Roman', serif](250mm*4.6μm*5μm)[/font][font=宋体],超声波清洗器。[/font][font='Times New Roman', serif]3 [/font][font=宋体]实验方法[/font][font='Times New Roman', serif]3.1 [/font][font=宋体]色谱条件[/font][font=宋体]流动相(参照中国药典[/font][font='Times New Roman', serif]2020[/font][font=宋体]年第一部):乙腈[/font][font='Times New Roman', serif]-0.02%[/font][font=宋体]磷酸水[/font][font=宋体][color=#333333]为流动相,进行梯度洗脱;检测波长[/color][/font][font='Times New Roman', serif][color=#333333]270nm[/color][/font][font=宋体][color=#333333];柱温:[/color][/font][font='Times New Roman', serif][color=#333333]20 [/color][/font][font=宋体][color=#333333]℃[/color][/font][font=宋体][color=#333333];流速:[/color][/font][font='Times New Roman', serif][color=#333333]1.0mL/min[/color][/font][font=宋体][color=#333333],进样量:[/color][/font][font='Times New Roman', serif][color=#333333]10μL[/color][/font][font=宋体][color=#333333]。[/color][/font][font='Times New Roman', serif][color=#333333]3.2[/color][/font][font=宋体][color=#333333]对照品溶液制备[/color][/font][font=宋体][color=#333333]取丹参酮[/color][/font][font=宋体][color=#333333]Ⅱ[/color][/font][font='Times New Roman', serif][color=#333333]A[/color][/font][font=宋体][color=#333333]对照品适量,精密称定,加甲醇制成每[/color][/font][font='Times New Roman', serif][color=#333333]1mL[/color][/font][font=宋体][color=#333333]含[/color][/font][font='Times New Roman', serif][color=#333333]20 μg[/color][/font][font=宋体][color=#333333]的溶液,即得。色谱图如下:[/color][/font][align=center][img=,432,233]https://ng1.17img.cn/bbsfiles/images/2022/09/202209010920076504_5804_1858223_3.jpg!w432x233.jpg[/img][/align][align=center][/align][font=宋体][/font][align=center][font=宋体][color=#333333]图[/color][/font][font='Times New Roman', serif][color=#333333]1[/color][/font][font=宋体]丹参酮Ⅱ[/font][font='Times New Roman', serif]A[/font][font=宋体][color=#333333]标准品([/color][/font][font='Times New Roman', serif][color=#333333]Eclipse XDB C18 [/color][/font][font=宋体][color=#333333])[/color][/font][/align][font='Times New Roman', serif][color=#333333]3.3 [/color][/font][font=宋体][color=#333333]供试品溶液的制备[/color][/font][font='Times New Roman', serif][color=#333333] [/color][/font][font=宋体][color=#333333](参照中国药典[/color][/font][font='Times New Roman', serif][color=#333333]2020[/color][/font][font=宋体][color=#333333]年版第一部)[/color][/font][font=宋体][color=#333333]供试品溶液的制备[/color][/font][font=宋体][color=#333333]取本品粉末(过三号筛)约[/color][/font][font='Times New Roman', serif][color=#333333]0.3 g[/color][/font][font=宋体][color=#333333],精密称定,置具塞锥形瓶中,精密加入甲醇[/color][/font][font='Times New Roman', serif][color=#333333]50 mL[/color][/font][font=宋体][color=#333333],密塞,称定重量,超声处理[/color][/font][font='Times New Roman', serif][color=#333333]30[/color][/font][font=宋体][color=#333333]分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。测定法[/color][/font][font=宋体][color=#333333]分别精密吸取对照品溶液与供试品溶液各[/color][/font][font='Times New Roman', serif][color=#333333]10[/color][/font][font=宋体][color=#333333]μ[/color][/font][font='Times New Roman', serif][color=#333333]L[/color][/font][font=宋体][color=#333333],注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定。以丹参酮Ⅱ[/color][/font][font='Times New Roman', serif][color=#333333]A[/color][/font][font=宋体][color=#333333]对照品为参照,以其相应的峰为[/color][/font][font='Times New Roman', serif][color=#333333]S[/color][/font][font=宋体][color=#333333]峰,计算隐丹参酮、丹参酮Ⅰ的相对保留时间[/color][/font][font=宋体][color=#333333]。色谱图如下:[/color][/font][align=center][img=,533,590]https://ng1.17img.cn/bbsfiles/images/2022/09/202209010921297596_689_1858223_3.jpg!w533x590.jpg[/img][/align][align=left][font='Times New Roman', serif]4 [/font][font=宋体]结果与讨论[/font][color=#333333][url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]使用中关键因素是流动相和色谱柱,根据待测物质的化学性质,选择合适的色谱柱,但是测定丹参的过程中发现柱温对其影响也比较大,使得待测物质不能能够有效分离,从而不能准确定性定量。丹参药材注意的就是柱温一定要在20[font=宋体]±2[/font][font=宋体][color=#333333]℃左右,进样才能达到有效分离。[/color][/font][/color][font=宋体][color=#333333] [/color][/font][/align]







 400-629-8889
400-629-8889
 留言咨询
留言咨询

 留言咨询
留言咨询

 400-860-5168转4907
400-860-5168转4907
 留言咨询
留言咨询


