便携式药品假药鉴别仪(手持式拉曼光谱仪),这个如何鉴别药品,有谱图库吗
不容易啊,土豆赋闲2年多,对足了电脑屏幕,今天终于有机会对一台仪器了http://simg.instrument.com.cn/bbs/images/brow/em09507.gif,那就是手持式拉曼光谱仪,上头打算用来搞药品快检。不知道各位对这个方法,这个仪器用在这个地方,有何指教啊,欢迎提出。 也顺便纪念本豆今天第一次摸到,用到这台仪器!http://simg.instrument.com.cn/bbs/images/brow/em09510.gif
药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。药品还可被来自包装、运输、仓储中的有机溶剂污染。药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。在可能的情况下,应避免使用这类溶剂。如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。第二类溶剂是指无基因毒性但有动物致癌性的溶剂。按每日用药10克计算的每日允许接触量如下,乙腈(410ppm)、氯苯(360ppm)、氯仿(60ppm)、环己烷(3880ppm)、二氯甲烷(600ppm)、二氧杂环己烷(380ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、2-乙氧基乙醇(160ppm)、2-甲氧基乙醇(50ppm)、环丁砜(160ppm)、1,2,3,4-四氢化萘(100ppm)、嘧啶(200ppm)、甲苯(890ppm)、甲酰胺(220ppm)、1,2-二氯乙烯(1870ppm)、N,N-二甲基乙酰胺(1090ppm)、N,N-二甲基甲酰胺(880ppm)、乙烯基乙二醇(620ppm)、正己烷(290ppm)、甲醇(3000ppm)、甲基环己烷(1180ppm)、N-甲基吡咯烷酮(4840ppm)、二甲苯(2170ppm)。第三类溶剂是指对人体低毒的溶剂。急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。在无需论证的情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证明其合理性。这类溶剂包括戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。
编者按:药品的残留溶剂无治疗作用并可能对人体的健康和环境造成危害,本文对国际协调大会(ICH)制订的指导原则及各国执行情况作了较为详尽的介绍。药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。药品还可被来自包装、运输、仓储中的有机溶剂污染。药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。在可能的情况下,应避免使用这类溶剂。如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。第二类溶剂是指无基因毒性但有动物致癌性的溶剂。按每日用药10克计算的每日允许接触量如下,乙腈(410ppm)、氯苯(360ppm)、氯仿(60ppm)、环己烷(3880ppm)、二氯甲烷(600ppm)、二氧杂环己烷(380ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、2-乙氧基乙醇(160ppm)、2-甲氧基乙醇(50ppm)、环丁砜(160ppm)、1,2,3,4-四氢化萘(100ppm)、嘧啶(200ppm)、甲苯(890ppm)、甲酰胺(220ppm)、1,2-二氯乙烯(1870ppm)、N,N-二甲基乙酰胺(1090ppm)、N,N-二甲基甲酰胺(880ppm)、乙烯基乙二醇(620ppm)、正己烷(290ppm)、甲醇(3000ppm)、甲基环己烷(1180ppm)、N-甲基吡咯烷酮(4840ppm)、二甲苯(2170ppm)。第三类溶剂是指对人体低毒的溶剂。急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。在无需论证的情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证明其合理性。这类溶剂包括戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。除上述这三类溶剂外,在药物、辅料和药品生产过程中还常用其他溶剂,如1,1-二乙氧基丙烷、1,1-二甲氧基甲烷、2,2-二甲氧基丙烷、异辛烷、异丙醚、甲基异丙酮、甲基四氢呋喃、石油醚、三氯乙酸、三氟乙酸。这些溶剂尚无基于每日允许剂量的毒理学资料,如需在生产中使用这些溶剂,必须证明其合理性。美、日、欧洲的药典对这一问题的处理不一样,被列入清单的毒性有机溶剂的种类和相应的可接受限度也不相同。虽然国际协调大会(ICH)关于药品中残留溶剂的指导原则在1997年就已生效,但《美国药典》至今尚未完全采纳该指导原则。《美国药典》的残留溶剂检测归在附录中的“有机挥发性杂质”篇,规定只有在生产商指出产品中可能有残留溶剂存在时才进行此检测,而当生产商根据其产品的生产、运输和储藏的相关知识可以保证产品中无某一种溶剂存在,并且保证如果进行此检测的话,产品能符合残留限度要求的时候,就可不进行此检测。同时还认为,装在气密性容器中的物品在运输过程中不受任何溶剂的污染。《美国药典》推荐进行苯、氯仿、二氧杂环己烷、亚甲基氯、三氯乙烯残留量检测。此外,还在一些药品的各论中指定进行环氧乙烷的残留量检测,除非另有规定,环氧乙烷残留量的可接受限度为10ppm。除此以外,《美国药典》不考虑国际协调大会(ICH)指导原则中的其他溶剂。第14版《日本药典》已采用国际协调大会(ICH)的指导原则,将残留溶剂定义为存在于药品中,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,限度符合国际协调大会(ICH)指导原则规定的有机溶剂。《欧洲药典》完全采纳国际协调大会(ICH)关于残留溶剂的指导原则。第4版《欧洲药典》叙述了如何对第一类和第二类溶剂进行鉴别和定量分析的方法,试验方法还适用于第三类溶剂和限度大于1000ppm(0.1%)的第二类溶剂的定量分析。
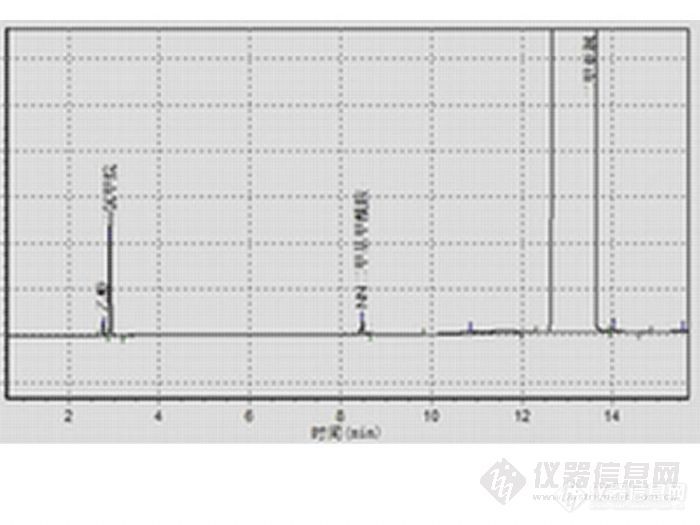
顶空毛细管柱气相色谱法分析测定药品中残留溶剂http://ng1.17img.cn/bbsfiles/images/2011/05/201105211013_295254_2242538_3.jpg 摘要 目前国家对药品中残留溶剂的检测还没有一个统一的国家标准,在关于有机溶剂残留量的指导原则中将二氯甲烷、DMF列为第二类必须控制的毒性试剂,将乙醇、丙酮列为第三类低毒性的溶剂。建立一种快速测定药品中残留溶剂的分析方法很有必要。为此南京科捷采用DK-300A顶空进样器取样,气相色谱毛细管柱分离,分析测定药品中常见的残留溶剂(乙醇、二氯甲烷、NN二甲基甲酰胺、二甲亚枫)。结合相关指标,本实验将二氯甲烷的限量规定为 600ppm,DMF的限量规定为 880ppm,乙醇及丙酮的限量规定为 5000ppm。实验结果表明:顶空毛细管柱气相色谱法快速、简便、准确是测定药品中残留溶剂较为理想的方法。关键词 乙醇 二氯甲烷 NN二甲基甲酰胺 顶空进样 毛细管气相色谱 药品 有机溶剂残留1.药品中乙醇、二氯甲烷、NN二甲基甲酰胺色谱图峰序1. 乙醇2.二氯甲烷3.NN二甲基甲酰胺4.二甲亚枫(溶剂)2.本方法应用范围在合成原料药,辅料或制剂生产的过程中使用或产生的挥发性有机化学物质,它们在实际的生产中未能被完全地清除。本方法可应用在药品中残留溶剂的检测中。近年来,药品中残留有机溶剂的毒性和致癌作用日益引起各方面的重视。药品中残留有机溶剂于1997年被美国FDA列为药品监控项目。我国药品中残留有机溶剂检测也越来越受到有关方面的重视。本文初步研究探索采用顶空毛细管柱气相色谱法分析药品中残留挥发性有机溶剂。顶空气相色谱法只将挥发和半挥发的组份引入柱子,可避免非挥发性的物质对系统的污染,样品前处理简便,分析效率高。结果表明,本方法快速、准确、重现性好。3.仪器及试剂配置色谱仪器配置色谱柱及试剂GC5890(FID检测器)毛细管专用柱30*0.32.*0.5乙醇、二氯甲烷各一瓶顶空进样器:DK-300ANN二甲基甲酰胺1瓶N2000色谱工作站(电脑自备1台)二甲亚枫1瓶氢氮氧一体发生器或钢瓶气各一瓶顶空压盖机1台顶空瓶20ml (带塞) 50只
大家好,请求大家帮助.我打算检药品中的乙醇残留量,我设置的参数是:进样150度,柱温60度,FID250度,分流比为1:10。我用的是毛细管柱,岛津2014。我是直接进样0.5ul,水为溶剂,以乙醇作为对照。外标计算。样品(0.4g药加水5.0ml),对照(8mg乙醇,加水定容到100ml)样品乙醇残留量在300-800PPM 我出现的问题是托尾,重现型差,还有就是出报告时格式。 谁知道我的方法可行不。或者有更好方法的请留言,好吗? 或者加我QQ 94714965
药品溶剂残留
最近在申请实验室认可,对于药品包装溶剂残留标准中没有明确规定,请问做药品包装的大神,药品包装溶剂残留物质种类,大家都有哪些?
为防止中药材粗加工过程中滥用或者过度使用硫黄熏蒸的问题,保证中药质量和安全有效,国家食品药品监督管理局组织制订了中药材及其饮片二氧化硫残留限量标准,并由国家药典委员会自6月10日起面向社会公开征求意见。规定山药、牛膝、粉葛等11种传统习用硫黄熏蒸的中药材及其饮片,二氧化硫残留量不得超过400 mg/kg;其他中药材及其饮片的二氧化硫残留量不得超过150mg/kg。上述限量标准均在世界卫生组织(WHO)认可的安全标准范围内。 国家药典委员会在2003年就已立项对中药材及饮片中的二氧化硫残留量测定方法和限量进行研究,其测定方法在2005年版《中国药典》增补本中开始收载,近年来一直在积累限量标准的研究数据。近来,为保证二氧化硫残留限量标准制定的科学性,在国家食品药品监督管理局组织下,由国家药典委员会多次召集来自药品监管、药品检验、行业协会、科研院校、饮片生产企业的药典委员、专家及饮片生产、质量检验的工作人员对中药材硫黄熏蒸、中药材及饮片二氧化硫残留量检测进行专题研究和论证。参照世界卫生组织(WHO)、国际法典委员会(CAC)、联合国粮食及农业组织(FAO)等国际组织的相关规定,并根据中国食品药品检定研究院等单位的长期研究及监测数据,制订了中药材及饮片中二氧化硫残留限量标准。 使用硫黄熏蒸是一些中药材产地粗加工过程中的一种习用方法,目的在于防霉、防腐和干燥等。目前尚无简便易行且有效的替代方法,因此,现阶段对中药材及其饮片中二氧化硫残留量控制宜分级限定。 征求意见截止时间为2011年9月9日,根据意见确定后正式发布执行。
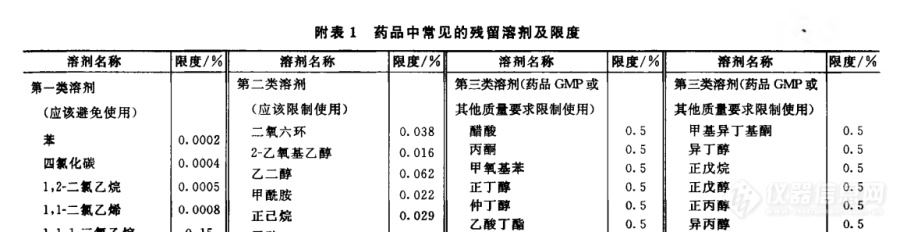
[img=,690,177]https://ng1.17img.cn/bbsfiles/images/2019/02/201902181740213114_5586_3373632_3.png!w690x177.jpg[/img]药典上说的溶剂残留的标准,指的是药品主成分的么,还是整个药品的,举例,比如说醋酸限度0.5%,那么这个0.5%是指谁的0.5%,现有1g某原料药,纯度是0.99g,那么这个醋酸的残留指的1g原料药中的0.5%,还是指有机溶剂残留量比上0.99小于0.5%呢,为什么这么问呢,因为原料药在中间产品阶段是液体,该液体里面有许多其他的杂质,这个环节有机溶剂残留也是0.5%的话,指的整个中间产品药液液体中么,还是药液中中间产品的(中间产品中可不纯,里面有很多杂质的),如果中间产品的话,通过方法我只能知道药液中主成分的量,无法知道整个药液中含有的不纯的中间产品质量
分析原料药中溶剂残留,药品30度左右就分解了,是不是只能用顶空分析了?但是原料药分解产生的小分子和分析的残留物是同一种物质,该如何操作???
现在的化验室有一间单独的药品室,里面就放了一个药品柜,没有留样室。我准备把药品柜挪到理化室的墙角,把药品室做留样室。还是直接在理化室放个柜子做留样柜?药品为常规菌落,大肠,二氧化硫,总糖检验使用药品。
请问测量药品的溶剂残留能用内标法吗?
大家好!正在找一本葛志荣主编的《食品中农业化学品残留量 药品卷》找了好多地方也没能借到,请问这里的大侠们有没有?我只是想找其中的几页内容。在此谢过了![em09509]
现在的化验室有一间单独的药品室,里面就放了一个药品柜,没有留样室。我准备把药品柜挪到理化室的墙角,把药品室做留样室。还是直接在理化室放个柜子做留样柜?药品为常规菌落,大肠,二氧化硫,总糖检验使用药品。
坛子里有专家提到Ahura公司的手持式激光拉曼光谱仪能用在安防领域,我下面要说的是这款产品在药厂车间的应用大有所为。该款产品具有快速(1 min出“通过”或“失败”结果)、准确、上手快(中文界面2分钟学会操作)、轻便(1.7 Kg),透过检测,内置软件不用外联电脑,可以在药厂车间任何一个环节使用,这款仪器已经在国际制药公司得到广泛使用,全球排名前十名药厂基本都配备了该款产品。这款产品最大的特点是软件,可以在1分钟内将待测物质图谱与之前建立标准物质图谱全部匹配一遍,如果图谱匹配上,结果显示“Pass”,同时显示被测物质的名称,如果匹配不上结果显示“Fail”,中文界面结果简单明了,准确率达99.99%。使用范围:药厂和原料药厂进料和出料及中间产品及环节随时检测,可以在原料药下车后、仓库上架前进行原料药快速全检;另外也可用于药品销售流程打假。使用仪器不用取样,可以透过薄膜包装袋和玻璃瓶检测,1min报出“通过”或“失败”结果。实际应用1:原料药进料上架前的快速全检鉴别,同时配合之后的QC抽检,为药厂严把质量关,其实目前大多数药厂质量问题是原料问题,包括2006年的齐二药事件,如果QC部门人员抽检前,再进行一次快速全检,原料质量就等于加上了一道有力保险。同时为企业省去停放进料需要的空间,无需任何耗材。实际应用2:另外生产过程中,制剂工艺质量;也是影响药品的一个重要环节,该款产品也能用于制剂过程中任意一个环节鉴别检测,如果检测不通过,可以交由QC部门进行更为严格的检测。实际应用3:本厂药品的打假,药监部门有的时候并不是很到位,该产品由于体积非常小(一块砖头大),一次充电可以联系使用5个小时,可以在任何药店等地,配合药监部门进行打假,及时发现证据线索,马上向药监部门举报。手持式产品介绍:[img]http://bbs.instrument.com.cn/images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=199140]Ahura手持拉曼中文样本.pdf[/url][img]http://bbs.instrument.com.cn/images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=199141]手持式激光拉曼光谱仪PPT.pdf[/url][img]http://bbs.instrument.com.cn/images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=199142]便携式拉曼光谱仪用于磺胺类药物成分识别的研究.pdf[/url]部分全球知名药企用户名单:[img]http://bbs.instrument.com.cn/images/affix.gif[/img][url=http://bbs.instrument.com.cn/download.asp?ID=199145]手持式激光拉曼光谱全球制药用户名单.pdf[/url][color=#DC143C]广告内容删除.[/color]
食品药品胶体金分析仪是一种先进的科学仪器,主要用于检测食品和药品中的胶体金含量。胶体金是一种微小颗粒的金纳米材料,具有广泛的应用价值。该分析仪通过采用高精度的技术和方法,能够准确测量食品和药品中的胶体金含量,为生产厂商和消费者提供关键的信息和保障。食品药品胶体金分析仪在功能构成上非常全面,主要包括分光光度模块、新型农残检测模块、胶体金检测模块、荧光检测模块、数字化管理模块等,可以快速检测200多种食品安全项目,如兽药残留、农药残留、非法添加剂、细菌数值等指标。 在使用上,该分析仪操作简便。操作人员只需将待测样品放入仪器中,按照指示进行相应操作即可。在仪器运行一段时间后,可以观察屏幕上显示的结果,根据仪器提供的标准曲线,确定目标物质的浓度。同时,该分析仪通常具有连接电脑的功能,可以方便地导出数据进行进一步的分析和处理。 食品药品胶体金分析仪是一款功能强大、操作简便的仪器,为食品和药品行业的质量控制和安全监测提供了强有力的支持。如需了解更多有关食品药品胶体金分析仪的信息,建议查阅相关文献或咨询专业机构。
我想问一下,药品中大孔树脂有机残留溶剂的测定(用[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]de)都要做哪些有机溶剂残留啊?这个规定在哪儿有。(主要是报新药过程中都要测哪些)还有他的加样回收率有什么规定吗?如果有又是在哪儿规定的呢?谢谢各位大侠
顶空毛细管柱[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法分析测定药品中残留溶媒 (摘要) 药品中残留溶媒是指在合成原料药,辅料或制剂生产的过程中使用或产生的挥发性有机化学物质。它们在实际的生产中未能被完全地清除。近年来,药品中残留有机溶剂的毒性和致癌作用日益引起各方面的重视。药品中残留有机溶剂于1997年被美国FDA列为药品监控项目。我国药品中残留有机溶剂检测也越来越受到有关方面的重视。为适应我国医药工业随着WTO进入国际市场的需要,提高药品的使用安全性,开展和完善药品中残留有机溶剂检测工作势在必行。 本文初步研究探索采用顶空毛细管柱[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法分析药品中残留挥发性有机溶剂。顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只将挥发和半挥发的组份引入柱子,可避免非挥发性的物质对系统的污染,样品前处理简便,分析效率高。结果表明,本方法快速、准确、重现性好。

2016年8月,国务院发布《“十三五”国家科技创新规划》(以下简称《规划》),明确了“十三五”时期科技创新的总体思路、发展目标、主要任务和重大举措。其中,食品药品安全内容纳入“十三五”规划,聚焦食品源头污染严重、过程安全控制能力薄弱、监管科技支撑能力不足等突出问题,重点开展监测检测、风险评估、溯源预警、过程控制、监管应急等食品安全防护关键技术研究。在食品药品安全监管方面,全产业链追溯与控制、真伪识别等技术将成为重要技术突破方向,《规定》强调加强食品安全防护关键技术研究,强化食品安全基础标准研究,加强基于互联网新兴业态的监管技术研究,构建食品药品的全产业链质量安全技术体系。http://ng1.17img.cn/bbsfiles/images/2017/04/201704071700_01_2536979_3.jpg食品药品监管离不开追溯体系,手持终端作为追溯体系中数据采集的基础工具,将在食品药品监管中起到重要作用。如果配备手持终端,监管人员可以清楚得看到食品药品的原料来源、制作环节、入库出库及最终售卖,这样将会建立一个整条产业链的追溯体系数据库,让每个环节清晰可见,一旦出现问题,将可随时溯源,查找问题出现的源头,这将是多方共同努力的方向。创新驱动发展是保障食品药品安全的重要基础,食品药品监管系统要深入贯彻落实《规划》提出的要求,大力推进食品药品安全科技创新体系建设,着力提高食品药品安全科技创新能力,积极创造良好的创新生态环境,在这个过程中,手持终端将作为基础工具,助力食品药品监管。
谢谢。还是检测三氟乙酸的问题,我是要检测药品中三氟乙酸的残留量。如果柱子会吸附的话,是否意味检测出药品中的微量三氟乙酸?
我们是用草酸酸化提取出土霉素。怎样测定药品中草酸残余量呢?我用的是高效液相色谱。用的是反向离子柱。
[center]FDA关于美国本土已上市药品残留溶剂的指导原则-20080806[/center]Residual Solvents in Drug Products Marketed in the United States [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=118069]FDA关于美国本土已上市药品残留溶剂的指导原则-20080806[/url]
[size=4][/size]安捷伦6920-GC用来做药品的有机溶剂残留,现在想安装顶空进样, 不知道是否可以?/?? 应该安装进口的还是国产的呢? 各位大侠,有没有知道的 ,帮帮小弟 谢谢了
各位大侠好,最近做药品中磷酸三丁酯残余量时,标准品按药典上的稀释倍数不出峰,但减小稀释倍数又出峰,仪器做其他的含量检测时都正常,所以初步判断是柱子不适合,但又不知道测磷酸三丁酯用什么涂层的柱子合适,还请大侠们告知。谢谢了!
打算建立10个左右的药物+主要代谢物联合检测方法,但是我不太清楚是不是这样:1. 先用单个药品标准谱进质谱摸离子对、DP、CE2. 摸[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件的时候再把药物混合起来进样?直接换各种梯度条件?我担心的是,一下子10个药物去摸条件的话很难一下子摸到合适的[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件,有点浪费? 还是说摸条件也是先单个药品进样,看一下在什么条件下出峰,并且调整峰形、出峰时间?但是这样的话会不会到时候梯度又不好设置?谢谢大家!!
关于举办“有害残留物检测技术学习班”的通知各省、市食品药品检验所,及相关企业质检部门: 中药、保健食品及农产品中有害残留物问题为全社会所高度关注。在国内,《中国药典》及相关食品国家标准规定了一系列有害残留物检测方法与严格的限量标准;在国外,日本、欧盟、美国等均采取了严格的市场准入制度。为进一步配合各药检所、质量监督检验机构相关残留检测实验室建设,为《中国药典》2010版相关检测内容做技术准备,由中国药品生物制品检定所主办、青岛食品药品检验所承办的“有害残留物检测技术”第三期学习班将于2008年9月于山东省青岛市举行,现通知如下:一、培训内容:1、中药中外源性有害残留物的监控及相关国际法律环境介绍。2、日本《肯定列表制》实施情况及检测技术介绍。3、[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]、原子荧光法检测技术及在中药铅、镉、砷、汞、铜残留检测中应用。4、中药注射液中重金属及有害元素测定法。5、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法、[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]法检测技术及在农药多残留检测中的应用。6、有机氯、有机磷、拟除虫菊酯类农药残留量测定法。7、氨基甲酸酯类农药残留量的HPLC柱后衍生测定法及HPLC/MS农药多残留测定法。8、黄曲霉毒素残留量的HPLC测定法。9、二氧化硫残留量测定法。10、参观青岛市食品药品检验所,观摩重点试验步骤(重金属及农残测定的样品前处理、GC/MS及HPLC/MS分析)演示,并进行研讨。二、参加人员:主要面向食品药品检验所的检验人员、药品生产企业的骨干质检人员,以及商检、农业等行业相关质检人员。三、时间:2008年9月16~18日,15日报到。四、地点:山东省青岛市五、费用:每人1200元,含培训、讲义和相关试验观摩费用。食宿及交通费自理。六、报名方式:填写报名表后电子邮件或传真报名,培训的具体时间、地点采用电子邮件另行通知。报名联系人:杜庆鹏、孙磊 地址:北京市崇文区天坛西里二号,中国药品生物制品检定所中药室,邮编100050 电话:(010)67095424传真:(010)67023650电子邮件:dasunlei@sina.com青岛食品药品检验所联系人:吴爱英 地址:山东省青岛市隆德路7号 邮编:266071 传真: (0532)85734979 电话:(0532)85735184 附:报名表姓名单位性别职称/职务固定电话移动电话电子邮件 二○○八年七月十五日
食品药品胶体金分析仪是一种先进的科学仪器,专门用于检测食品和药品中的胶体金含量。该分析仪通过高精度的技术和方法,能够准确测量食品和药品中的胶体金含量,为生产厂商和消费者提供关键的信息和保障。 胶体金分析仪的工作原理基于胶体溶液中纳米颗粒的光学性质,通过测量光的散射强度来得到颗粒的浓度信息。当光与金纳米颗粒相互作用时,根据散射光的洛仑兹-米耳斯理论,可以得到散射强度与颗粒的浓度之间的关系。仪器中的光源会照射到样品中的金纳米颗粒上,部分光会被颗粒散射并检测到。然后,光学传感器,如光电二极管或光散射仪,会测量散射光的强度,并将其转化为电信号。最后,分析仪会处理这些电信号,进而计算出颗粒的浓度。 这种分析仪具有多种功能模块,如分光光度模块、新型农残检测模块、胶体金检测模块、荧光检测模块以及数字化管理模块等,可以快速检测200多种食品安全项目,包括兽药残留、农药残留、非法添加剂、细菌数值等指标。此外,它还具有15.6英寸液晶触摸屏显,搭配运行安卓智能操作系统,使得操作更为方便且性能更强。 食品药品胶体金分析仪在多个领域都有广泛的应用,如食药监局、卫生部门、高教院校、科研院所、农业农村局、食品深加工企业及检验检疫部门等。其高灵敏度、高准确度和高效率的特点,使得它成为食品安全和质量检测的重要工具。 总的来说,食品药品胶体金分析仪是一款集多功能于一体的先进检测设备,为食品和药品行业的质量控制和安全监测提供了强有力的支持。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2024/04/202404231526532789_7703_4214615_3.jpg!w690x690.jpg[/img]
药匙 是用于取用粉末状或小颗粒状的固体试剂的工具。大多数药匙只有一个勺,通常由金属、牛角或者塑料制成。有些药匙两头各有一个勺,一大一小,实验者可以根据用药量大小选择。注意事项:1.根据试剂用量不同,药匙应选用大小合适的。2.不能用药匙取用热药品,也不要接触酸、碱溶液。3.取用药品后,应及时用纸把药匙擦干净。4.药匙最好专匙专用,用玻璃棒制作的小玻璃勺子可长期存放于盛有固体试剂的小广口瓶中,无需每次洗涤。粉末状药品的取用,取用时可以用药匙(或者纸槽).操作要领是:“一斜、二送、三直立”.具体的操作是:先将试管倾斜,把盛药品的药匙(或者纸槽)小心地送入试管底部,再使试管直立起来。固体药品的取用原则: 1.“三不”原则,即“不闻、不摸、不尝”;具体说就是:不要去闻药品的气味,不能用手触摸药品,不能尝试药品的味道. 2.节约原则,即严格按照实验规定的用量取用药品;没有说明用量时,一般按最少量取用,固体只需盖满试管底部即可. 3.“三不一要”原则,即剩余药品的处理方法.具体是就是:既不能放回原瓶,也不能随意丢弃,更不能拿出实验室,要放入指定的容器内。液体药品的取用原则⒈识记化学实验室药品的一些图标。⒉药品取用的基本原则。⑴实验室取用药品要做到“三不”:不能用手接触药品;不要鼻孔凑到容器口去闻药品的气味;不能尝任何药品的味道。⑵取用药品注意节约:取用药品应严格按规定用量。若无说明,应取最少量,即:液体取1~2mL;固体只需盖满试管底部。⑶用剩的药品要做到“三不”:既不能放回原瓶,也不要随意丢弃,更不能拿出实验室,要放在指定的容器里。⒊固体药品的取用⑴取用固体药品的仪器:医学|教育网搜集整理一般用药匙;块状固体可用镊子夹取。⒋液体药品的取用⑴取用少量液体,可用胶头滴管。滴加到另一容器中的方法是将滴管悬空放在容器口正上方,滴管不要接触烧杯等容器壁,取液后的滴管不能倒放、乱放或平放。⑵从细口瓶倒出液体药品时,先把瓶塞倒放在桌面上,以免沾污瓶塞,污染药液;倾倒液体时,应使标签向着手心,以防瓶口残留的药液流下腐蚀标签;瓶口紧靠试管口或仪器口,以免药液流出。倒完药液后立即盖紧瓶塞,以免药液挥发或吸收杂质。⑶取用一定量的液体药品,常用量筒量取。量液时,量筒必须放平,倒入液体到接近要求的刻度,再用滴管逐滴滴入量筒至刻度线。读数时,视线与量筒内液体的凹液面最低处保持水平。液体药品的取用注意事项 :1、取用不定量(较多)液体——直接倾倒a. 瓶塞必须倒放在桌面上【防止药品腐蚀实验台或污染药品】;b. 直接倾倒时瓶口必须紧挨试管口,试管45度,并且缓缓地倒【防止药液损失】;c. 贴标签的一面必须朝向手心处【防止药液洒出腐蚀标签】;d. 倒完液体后,要立即盖紧瓶塞,并把瓶子放回原处,标签朝向外面【防止药品潮解、变质】。2、 取用少量的液体—使用胶头滴管a. 应在容器的正上方垂直滴入;胶头滴管不要接触容器壁【防止沾污试管或污染试剂】;b. 取液后的滴管,应保持橡胶胶帽在上,不要平放或倒置【防止液体倒流,沾污试剂或腐蚀橡胶胶帽】;c. 用过的试管要立即用清水冲洗干净;但滴瓶上的滴管不能用水冲洗,也不能交叉使用。3、取用一定量的液体—使用量筒a. 当向量筒中倾倒液体接近所需刻度时,停止倾倒,余下部分用胶头滴管滴加药液至所需刻度线;b. 读数时量筒必须放平稳,视线与量筒内液体的凹液面的最低处保持水平 .(注意:俯视则读数偏大,仰视则读数遍小。)
为严厉打击制售假劣药品的违法行为,保证公众用药安全,沈阳市食品药品监督管理局开展了非药品冒充药品或药品冒充非药品专项治理。根据《药品管理法》和《沈阳市药品医疗器械监督管理办法》的规定,在我市发现涉嫌违法产品337种,违法产品的名单附后。现将有关事项公告如下: 一、名单所列违法产品以及具有同类违法情形产品的经营企业立即停止销售名单所列涉嫌违法产品,以及具有相同违法情形的产品。二、各经营企业从即日起不得再购进名单所列涉嫌违法产品及具有相同违法情形的产品。三、公告发布后仍销售上述名单所公布产品及具有相同违法情形产品的,食品药品监管部门将依据《药品管理法》和《沈阳市药品医疗器械监督管理办法》的相关规定,按假药进行处罚。四、在专项治理中发现的其他违法产品,我局将陆续予以公布。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=185304]沈阳市关于非药品冒充药品名单公告.doc[/url]