之前听说过土壤场地调查检测GB36600里面的45项基本因子检测必须资质齐全,缺一项也不能开展业务,45项因子不能把其中的几项进行分包检测,但是一直没找到相关文件,有这个说法吗?相关的规定文件在哪里?
一、适用范围适用于食物中毒样品中致病菌的快速筛查,常规样品中卫生指标菌与致病菌的日常监测以及检测样品的采集。 二、工作意义食品在生产、加工、储存、运输和销售等各个环节都有可能受到有害微生物的污染,从而引起食品腐败变质和食源性食物中毒的发生,而且一些危险的致病菌不断涌现出来。据世界卫生组织估计,在全世界每年数以亿计的食源性疾病患者中,70%是由于食用了各种致病性微生物污染的食品和饮水造成的。中国社科院发布的首部食品安全绿皮书《中国食品安全报告(2007)》指出,当前我国食品安全的形式依然严峻,其中微生物污染和化学性食物中毒是影响我国食品安全的最主要因素。微生物污染包括细菌性污染、病毒和真菌及其毒素的污染。2000年至2002年,中国疾病预防控制中心营养与食品安全所对全国部分省市的生肉、熟肉、乳和乳制品、水产品、蔬菜中的致病菌污染状况的监测结果表明,微生物性食物中毒仍居首位,占39.62%;化学性食物中毒占38.56%;动植物性和原因不明的食物中毒均占10%左右。为了减少和防止由微生物污染事件的发生,对食品采用有效的检验方法进行检测和监督是非常必要的。利用传统的检测方法,主要包括形态检查和生化方法,其准确性和灵敏性均较高,但涉及的实验较多、操作繁琐、需要时间较长、准备和收尾工作繁重。有条件的实验室采用了PCR仪、全自动细菌鉴定仪、全自动荧光酶标免疫测试系统等先进设备进行检验,具有快速、灵敏、准确的优点,但这些先进设备价值昂贵,基层检测监管单位和食品生产企业一般难以配备。1955年德国学者F.J.Forg 发明了一种简单快速的大肠菌群快速检测法—纸片法,使原来的检测周期由72小时缩短到15小时,材料成本降低了四分之三,同时大大简化了操作程序。从此,这种集化学、高分子学和微生物学于一体的检测方法开始发展起来,近十几年来发展更为快速。纸片法或测试片法是基于微生物具有复杂多样的酶系统,通过加入特异性酶的底物,在酶的作用下游离出发色基团,直接观察菌落颜色即可对菌类做出鉴定。从而使传统方法需要几步不同反应、几天甚至更长时间才能完成的检测过程简化为一步完成,检测时间缩短到24小时以内,不但能够大大提高检测工作的效率,还可减少大量人工成本。目前国外已有一些知名品牌,国内一些企业出品的此类产品其质量也是越来越好,为此项工作的开展与普及奠定了基础。另外,在国标检测方法基础上研发出的大肠菌检测试剂盒以及致病菌增菌检测试剂盒,采用包被技术将干燥培养基包被在试剂盒中,随时取用,也大大简化了实验前的准备工作。而且,大肠菌检测试剂盒秉承了国标方法中大肠菌阳性结果时的产酸产气的观察理念,保证了检测结果的准确性。至于致病菌增菌检测试剂盒,除日常卫生指标的控制外,更加有利于食物中毒因子的筛选和卫生保障应急处理时使用。
2014 Milliplex多因子检测全国巡回讲座——默克密理博与您携手转化医学研究更少的样本,更短的时间,更低的成本,获得更多的精确数据 基于三十五年深厚的研发经验,默克密理博秉持着严谨、专业的态度在液相悬浮芯片平台上创建了生物标志物快速检测的金标准——Milliplex多因子检测平台。Milliplex应用平台为肿瘤、心血管疾病、糖尿病、神经退行性疾病等重要疾病提供早期发现、病程检测、预后判断以及疾病机制的研究提供检测指标,是涵盖了从基础研究到新药发现和临床研究的转化医学全进程研究的系统化平台。http://blog.merckmilliporechina.com/editor/upload/image/48FCD414_DA900E44.jpg如何将Milliplex多因子检测平台与您的实验相结合,开启科学研究新思路?敬请关注默克密理博2013年Milliplex多因子检测巡回讲座,欢迎您的参加!我们会陆续在北京、上海、广州等城市开展。已经确定的讲座时间及地点,请参考列表。如果您所在的单位希望我们提供该讲座,请将您的具体信息和要求发送到我们技术支持邮箱:asiatechserv@merckgroup.com,我们会尽快和您联系讲座的时间。本次更新为2014年9月28日9月 上海 金山公共卫生中心 上海 东方肝胆外科医院 杭州 浙江大学医学院 广州 中山大学孙逸仙纪念医院 西安 西安交通大学 西安 第四军医大学10月 温州 温州医科大学附属第一医院 广州 中山眼科中心 广州 中山大学医学院 广州 南方医科大学 广州 广东省口腔医院 广州 广东省中医院 北京 医科院药物所 北京 CDC11月 上海 交大免疫所 北京 北京工业大学 北京 北大医学部持续更新中,需要最新讲座信息,请在博客下留言,注明您所在单位。默克密理博Milliplex多因子检测中文网站全新上线!http://blog.merckmilliporechina.com/editor/upload/image/490F3C4D_73F0C019.JPG请登录:http://www.merckmilliporechina.com/milliplex/该网站不但网罗了Biomarker在各种疾病中的应用,还以转化医学应用、仪器、软件、BMS服务为主题展开了多重检测与转化医学研究的平台介绍,同时为资深用户准备了实验攻略饕餮大餐。Milliplex多因子检测平台简介试剂盒 超过1000种蛋白可供选择。检测多达6个物种,包含了人、小鼠、大鼠、非人灵长类、狗和猪。试剂盒中提供了实验所需要的所有试剂,方便操作。严格的质量控制和批次一致性。仪器MAGPIX液相悬浮芯片系统:灵活高效的生物标记验证方案,点亮后ELISA时代的研究智慧!Luminex 200经典液相芯片系统:多重检测领域内评价最高的高通量平台。FLEXMAP3D 超高通量检测系统,提供多达500重检测的高性能平台。软件最优的软件组合:最强的MULTIPLEX 数据分析软件- MILLIPLEX® Analyst 5.1搭配Luminex® xPONENT®数据采集软件。MILLIPLEX® Analyst 5.1软件能够更快速高效地管理、追踪和分析多重检测的海量数据,使您的研究工作事半功倍。服务优选相同批次试剂进行专业化实验,以确保实验结果的最佳准确性和重复性。实验服务采用标准化可控的SOP流程,每个环节均有完善的质量把控和追溯标准。[/fon
土壤45项监测因子是哪些?
水污染生物监测和检测方法及其研究进展摘 要: 扼要介绍了生物监测的理论、方法和特点。综述了近年来水污染生物监测的发展趋势及其研究动态与方向。阐述了水污染生物监测近期研究方向。关键词:水污染 生物监测 研究进展1 引言生物监测是系统地利用生物反应来评价环境的变化,并将其信息应用于环境质量控制程序中的一门科学。生物监测的目的是希望在有害物质还未达到受纳系统之前,在工厂或现场就以最快的速度把它检测出来,以免破坏受纳系统的生态平衡;或是能侦察出潜在的毒性,以免酿成更大的公害[1]。生物监测是理化监测的重要补充,对于评价环境质量状况有着十分重要的作用。理化监测一般只考虑瞬时污染状况,要做到长期连续监测,在经济上往往是不合适的。要了解污染的累积效应,采用生物监测更合适。同时,仅利用污染物质的浓度值来反映污染程度及危害也是不全面的,因为某些污染物质在环境中的含量极微不等于毒性极微,反之亦然。用生物监测进行配合,充分利用指示生物对污染物毒性反应的敏感性,便能较准确地反映真实的污染状况。2 水污染的生物监测2.1 水污染生物监测的理论依据在一定条件下,水生生物群落和水环境之间互相联系、互相制约,保持着自然的、暂时的相对平衡关系。水环境中进入的污染物质,必然作用于生物个体、种群和群落,影响生态系统中固有生物种群的数量、物种组成及其多样性、稳定性、生产力以及生理状况,使得一些水生生物逐渐消亡,而另一些水生生物则能继续生存下去,个体和种群的数量逐渐增加。水污染生物监测就是利用这些变化来表征水环境质量的变化[2]。2.2 水污染生物监测的特点同理化监测相比,生物监测有自己的特点:生物监测能反映各种污染物的综合影响;理化监测是定期采样,结果不能反映采样前、后的情况,而水中生物,汇集了整个生长期环境因素改变的情况;有些水生生物对污染物很敏感,有些连精密仪器都测不出的微量元素的浓度,却能通过“生物放大”作用在生物体内积累而被测出[2]。生物监测也有自己的不足之处:生物监测不能定性和定量地测定水质污染;检测的灵敏性和专一性方面不如理化检测;某些生物检测需时较长。2.3 水污染生物监测的方法2.3.1利用指示生物在水体中的出现或消失、数量的多少来监测水质许木启 [3]利用白洋淀水体中浮游动物群落优势种的变化来判断水体的污染程度和自净程度。结果表明,府河—白洋淀水体从上游至下游,浮游动物耐污种类逐渐减少,广布型种类逐渐出现较多,在下游许多正常水体出现的种类均有分布;同时,原生动物由上游的鞭毛虫至中游出现纤毛虫,在下游则发现很多一般分布在清洁型水体的种类,表明府河—白洋淀水体从上游到下游水体的污染程度不断减轻,水体具有明显而稳定的自净功能。2.3.2利用水生生物群落结构的变化来监测水质蒋昭凤等 [4]用底栖动物的变化趋势评价湘江水质污染,结果发现湘江干流底栖大型无脊椎动物种类数和物种的多样性指数从上游到下游呈减少趋势,表明毒杀生物的有毒物质对湘江的污染较为明显,并且可根据湘江干流各断面种类数的减少程度判断出各断面的污染程度;同时也观察到,随着时间的推移,底栖大型无脊椎动物种类数和多样性指数也呈减少趋势,说明这种有毒污染仍在发展之中。2.3.3水污染的生物测试水污染的生物测试是利用水生生物受到污染物质的毒害所产生的生理机能的变化,测试水质污染状况。Belding [5]根据鱼的呼吸变化指示有毒环境,在有污染物存在的情况下,鱼腮呼吸加快且无规律。德国[6]从1977年开始研究利用鱼的正趋流性开展生物监测,在下游设强光区或适度电击,控制健康鱼向下游的活动;或间歇性提高水流速度,迫使鱼反应。如果鱼不能维持在上游的位置,则表明污染产生了危害。3 国内外水污染生物监测的研究进展近几年来,应用生物监测环境技术的研究广泛开展,出现了一些新方法、新材料和新的监测物,提高了生物检测的灵敏性。3.1 水污染生物监测及其检测的新方法3.1.1 利用遗传毒理学监测水体污染环境污染物质对人类及其它生物危害最为严重的问题是对细胞遗传物质造成的损害。因此,近20年来环境生物检测技术的研究和应用,尤其是细胞微核技术和四分体微核技术在动植物以及人类染色体受外界理化因子的损伤等方面的分析、诱变剂的测试筛选,以及应用于环境监测的研究得到了广泛的发展[7]。微核在生物细胞内的形成途径以及与染色体畸变的相关性早已被人们所认识,用微核测定法替代染色体畸变方法来监测环境污染物对生物遗传物质的损伤具有简便、快速、灵敏度高等优点。最常用的蚕豆根尖细胞微核试验技术是一种以染色体损伤及纺锤丝毒性等为测试终点的植物微核监测方法,该技术自1982年由Degrassi等建立以来,在环境诱变和致癌因子的检测研究中,特别是在水质污染和致突变剂检测研究中得到了广泛应用[8]。吴甘霖 [9]在利用水花生根尖微核技术(MCN)对马鞍山市废水的监测研究中,发现利用水花生根尖微核可作为监测水体污染的新材料。其根尖细胞微核率 MCN(‰),不仅可用于监测不同废水的污染程度,而且由于该植物长期生活在污染水体中,还能反映不同废水的污染物富集程度及现状。当外界环境中存在一定浓度的致突变物时,可使细胞发生损伤,从而使微核细胞率上升。另外微核细胞率的上升,提示环境中存在有致突变物,即受试水样中含有能打断DNA分子的诱变剂或能打断纺锤丝的纺锤丝毒剂,从而表现出遗传毒性。单细胞凝胶电泳(SCGE),即彗星试验也是一种通过检测DNA链损伤来判别遗传毒性的技术。它比微核试验更有益,因为环境中的遗传毒物浓度一般很低,而彗星试验检测低浓度遗传毒物具有高度灵敏性,所研究的细胞不需要处于有丝分裂期。同时,这种技术只需要少量细胞。目前它已经被用于检测哺乳动物、蚯蚓、一些高等植物、鱼类、两栖动物以及海洋无脊椎动物的细胞[11]。Mirjana Pavlica等 [10]用暴露在五氯苯酚(PCP)中的淡水蚌类(Dreissena polymorpha Pallas)血细胞进行彗星试验,观察血细胞中DNA损伤程度。在进行实验室实验和原位实验后,发现高浓度的PCP(80g/L)会引起血细胞中DNA断裂,表明用彗星试验检测DNA损伤能够监测水体中PCP污染。SOS显色法[12]是国内在20世纪80年代发展起来的一种遗传毒性检测新方法,具有快速、准确、灵敏及假阳性率低的特点,被广泛用于遗传毒性的测定中。其原理是:在DNA分子受到外因引起的大范围损伤、其复制又受到抑制的情况下,会导致一种容易发生错误的修复。所有这些在遗传毒物处理后大肠杆菌中出现的一系列反应统称为SOS应答。SOS显色法有许多优于Ames的特点:(1)快速、简便,测定过程只需7h;(2)灵敏,被处理的细胞全产生或不产生SOS反应,用分光光度法测定β-ONPG(邻硝基苯β-D-半乳糖苷)分解产物非常灵敏;(3)准确,SOS显色法测定的是遗传毒物对细胞原发的直接反应,其阳性结果十分可信,而Ames试验的假阳性率较高。因此,SOS显色法已引起人们的密切关注,成为一种值得推广的水质监测评价方法。
我现在检测一种生物碱的盐的含量,但是每一次都算出来的含量超过100%,后来我觉得应该是生物碱和相应的盐分不开!后来我试过用中检所的标准品来做含量。生物碱和相应的盐都是同一个吸收。根本就不能分开!而且生物碱的相应因子比相应的盐好高!我正在郁闷当中!不知道那位大师可以指点迷津!在这里谢过了![em61]
我做蜂王浆的癸烯酸检测 用的是岛津的液相是用对羟基苯甲酸甲酯做内标然后用标准品求校正因子F应该怎么求啊,谢谢大家给点指教啊
我做蜂王浆的癸烯酸检测 用的是岛津的液相是用对羟基苯甲酸甲酯做内标然后用标准品求校正因子F应该怎么求啊,谢谢大家给点指教啊
方案也好,最后的竣工验收报告都好,都有提到/监测因子/这个次,但找了水气声土的标准,都没找到监测因子的具体出处。想了解下HJ行业一些特定名词的解释,各位老师有谁知道的
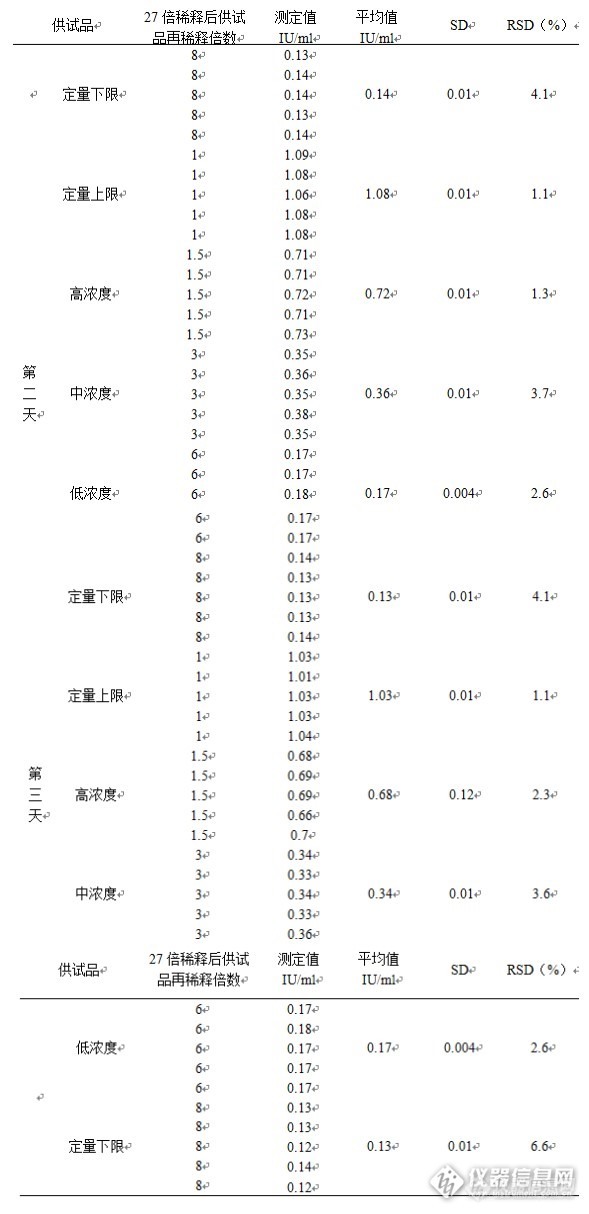
[align=center][b]因子类血液制品效价的检测方法验证[/b][/align][align=left][b]中文摘要[/b]:[b]目的 [/b]验证全自动凝血仪应用于因子类血液制品效价测定时方法的准确性 [b]方法[/b]根据生物制品质量控制分析方法验证技术审评一般原则及《中国药典》2015年版通则9012生物样品定量分析方法验证指导原则,通过线性关系,准确度,精密度(重复性、日间精密度),专属性对本方法进行方法学验证。[b]结果[/b]两种稀释方法的因子效价检测所进行的线性关系,准确度,精密度、日间精密度、专属性验证均符合方法学验证的标准。[b]结论[/b]两种稀释方法适用于因子效价的检测。效从价检测方法的建立可应用于因子类血液制品生产的中间过程控制,通过准确的效价检测可以对中间各个生产环节的中间产品进行指导,可以精确分析各生产环节的效价损耗量,而制定解决方案,提高整个生产过程的产品收率,在半成品的配制环节,可对产品的总效价进行精确控制,从而提高产品质量的均一性,整体提高产品的质量水平。[/align][b]关键词: 因子类血液制品;效价检测; 方法学验证[/b]通过蛋白质含量对凝血因子效价检测影响的研究,发现在供试品稀释中使用含不同蛋白质浓度的稀释液导致因子效价测定的差异。而在制药企业和检测机构中,为追求检测方法的简单化、仪器化和数据可追溯性,大部分采用了全自动血凝仪,并按照血凝仪的使用说明书进行了因子类血液制品的效价检测。选用蛋白浓度为1%的药典稀释液和用人凝血因子缺乏血浆进行预稀释两种方法对人凝血因子进行效价检测全自动血凝仪法通过线性关系,准确度,精密度(重复性、日间精密度),专属性对本方法进行方法学验证。效价检测方法的建立可应用于因子类血液制品生产的中间过程控制,通过准确的效价检测可以对中间各个生产环节的中间产品进行指导,可以精确分析各生产环节的效价损耗量,从而制定解决方案,提高整个生产过程的产品收率,在半成品的配制环节,可对产品的总效价进行精确控制,从而提高产品质量的均一性,整体提高产品的质量水平。[b] 1 实验仪器与试剂1.1 仪器[/b]Stago-compact全自动血凝仪(法国DiagnosticaStago公司),漩涡振荡器(美国ThermoScientific公司)。[b]1.2 试剂人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%),Owren-Koller(稀释液)。2 方法2.1 蛋白含量1%的药典稀释液稀释人凝血因子Ⅷ效价检测方法验证2.1.1线性关系[/b]取复溶后的人凝血因子Ⅷ国家标准品,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅷ效价测定定标程序操作,仪器自动将装入的人凝血因子标准品溶液稀释至1.00 IU/ml、0.50IU/ml、0.25IU/ml、0.13IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅷ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.1.2 准确度[/b]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅷ溶液放入STAGO全自动血凝仪中定标,另取用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.1.3 精密度[/b]取2015ZK0801批人凝血因子Ⅷ质控品,用灭菌注射用水复溶后,用生理氯化钠溶液将其进行27倍稀释,再用药典稀释液稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。[b]2.1.4 日间精密度[/b]在不同的三天分别按照2.1.3进行精密度的测定。[b]2.1.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血因子Ⅷ生产过程中的配制平衡液(含与人凝血因子Ⅷ中相同含量的氯化钠、枸橼酸钠、甘氨酸、甘露醇等),以此作为不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内。[b]2.2 人凝血因子缺乏血浆进行预稀释人凝血因子Ⅷ效价检测方法验证2.2.1 线性关系[/b]取复溶后的人凝血因子Ⅷ国家标准品,用人凝血因子Ⅷ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅷ效价测定定标程序操作,仪器自动将装入的人凝血因子标准品溶液稀释至1.00 IU/ml、0.50IU/ml、0.25IU/ml、0.13IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅷ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.2.2 准确度[/b]将人凝血因子Ⅷ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅷ溶液放入STAGO全自动血凝仪中定标,另取用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.2.3 精密度[/b]取2015ZK0801批人凝血因子Ⅷ质控品,用灭菌注射用水复溶后,用人凝血因子Ⅷ缺乏血浆将其进行27倍稀释,再用Owren-Koller(稀释液)稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。[b]2.2.4 日间精密度[/b]在不同的三天分别按照2.2.3进行精密度的测定。[b]2.2.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血因子Ⅷ生产过程中的配制平衡液(含与人凝血因子Ⅷ中相同含量的氯化钠、枸橼酸钠、甘氨酸、甘露醇等),以此作为不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内[b]2.3 蛋白含量1%的药典稀释液稀释人凝血酶原复合物效价检测方法验证2.3.1 线性关系[/b]取复溶后的人凝血酶原复合物国家标准品,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅸ效价测定定标程序操作,仪器自动将装入的人凝血因子Ⅸ标准品溶液稀释至1.00 IU/ml、0.50IU/ml、0.25IU/ml、0.13IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅸ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.3.2 准确度[/b]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅸ溶液放入STAGO全自动血凝仪中定标,另取用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.3.3 精密度[/b]取2015ZK0901批人凝血酶原复合物质控品,用灭菌注射用水复溶后,用生理氯化钠溶液将其进行15倍稀释,再用药典稀释液稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。[b]2.3.4 日间精密度[/b]在不同的三天分别按照2.3.3进行精密度的测定。[b]2.3.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血酶原复合物生产过程中的配制平衡液(含与人凝血酶原复合物中相同含量的氯化钠、枸橼酸钠、甘氨酸等),以此作为不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内。[b]2.4 人凝血因子缺乏血浆进行预稀释人凝血酶原复合物效价检测方法验证2.4.1 线性关系[/b]取复溶后的人凝血酶原复合物国家标准品,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,按照Stago全自动血凝仪操作规程选择人凝血因子Ⅸ效价测定定标程序操作,仪器自动将装入的人凝血因子Ⅸ标准品溶液稀释至1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml,连续定标3次。定标完成后,仪器建立人凝血因子Ⅸ标准品溶液效价(IU/ml)的对数对其相应的凝固时间(秒)对数的直线回归方程,记录相关系数R值,应不低于0.99。[b]2.4.2 准确度[/b]将人凝血因子Ⅸ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅸ溶液放入STAGO全自动血凝仪中定标,另取用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液(标准曲线范围内高、中、低三个稀释度和定量下限)作为待测样品,按照操作规程进行测定,测定3次,并计算回收率,高、中、低浓度标准品回收率应在85%~115%范围内,定量下限标准品回收率应在80%~120%范围内。[b]2.4.3 精密度[/b]取2015ZK0901批人凝血酶原复合物质控品,用灭菌注射用水复溶后,用人凝血因子Ⅸ缺乏血浆将其进行15倍稀释,再用Owren-Koller(稀释液)稀释1倍,1.5倍,3倍,6倍,8倍,分别作为标准曲线范围内定量上限,高、中、低三个稀释度和定量下限。每一个稀释度重复测定5次。计算每一浓度测定结果的均值、SD和RSD值,高、中、低浓度标准品回收率应在85%~115%范围内,定量上、下限标准品回收率应在80%~120%范围内。2.4.4 日间精密度在不同的三天分别按照2.4.3进行精密度的测定。[b]2.4.5 专属性[/b]为确保当制品中含有其它组分,如杂质、降解物、添加物(如缓冲液、赋形剂、稳定剂)等存在时,能够准确可靠测定供试品的能力而进行分析方法的专属性验证。取人凝血酶原复合物生产过程中的配制平衡液(含与人凝血酶原复合物中相同含量的氯化钠、枸橼酸钠、甘氨酸等),以此作为不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,其检测结果应低于方法定量下限,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,要求至少80%以上的标准品的准确度在±20%范围内。[b]3 结果3.1 蛋白含量1%的药典稀释液稀释人凝血因子Ⅷ效价检测方法验证3.1.1 线性关系结果[/b]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅷ标准品进行Ⅷ效价测定定标,三次直线回归方程相关系数R值结果见表1。[align=center]表1 生理氯化钠稀释FⅧ定标R值检测结果[/align][align=center][img=,573,138]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141653_01_1626619_3.png[/img][/align][align=left][b]3.1.2 准确度结果[/b][/align][align=left]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅷ后再用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表2。[/align][align=center]表2 准确度检测结果[/align][align=center][img=,570,335]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141654_01_1626619_3.png[/img][/align][b]3.1.3 精密度结果[/b]2015ZK0801批人凝血因子Ⅷ质控品用生理氯化钠溶液稀释27倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表3。[align=center]表3 精密度检测结果[/align][align=center][img=,571,422]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141656_01_1626619_3.png[/img][/align][align=center][img=,566,290]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141657_01_1626619_3.png[/img][/align][b]3.1.4 日间精密度结果[/b]在不同的三天2015ZK0801批人凝血因子Ⅷ质控品用生理氯化钠溶液稀释27倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表4。[align=center]表4 日间精密度检测结果[/align][align=center][img=,571,470]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141703_01_1626619_3.png[/img][/align][align=center][img=,589,1214]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141713_01_1626619_3.jpg[/img][/align][b]3.1.5 专属性结果[/b]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅷ溶液定标后,取不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表5。[align=center]表5 专属性检测结果[/align][align=center][img=,565,239]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141714_01_1626619_3.png[/img][/align][b]3.2 人凝血因子缺乏血浆进行预稀释人凝血因子Ⅷ效价检测方法验证3.2.1 线性关系结果[/b]用人凝血因子Ⅷ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅷ标准品进行Ⅷ效价测定定标,三次直线回归方程相关系数R值结果见表6。[align=center]表6 人凝血因子缺乏血浆稀释FⅧ定标R值检测结果[/align][align=center][img=,567,135]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141716_01_1626619_3.png[/img][/align][b]3.2.2 准确度结果[/b]用人凝血因子Ⅷ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅷ后用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表7。[align=center]表7 准确度检测结果[/align][align=center][img=,569,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141717_01_1626619_3.png[/img][/align][b]3.2.3 精密度结果[/b]2015ZK0801批人凝血因子Ⅷ质控品用人凝血因子Ⅷ缺乏血浆稀释27倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表4-8。[align=center]表8 精密度检测结果[/align][align=center][img=,566,570]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141720_01_1626619_3.png[/img][/align][b]3.2.4 日间精密度结果[/b]在不同的三天2015ZK0801批人凝血因子Ⅷ质控品用人凝血因子Ⅷ缺乏血浆稀释27倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表9。[align=center]表9 日间精密度检测结果[/align][align=center][img=,588,1701]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141726_02_1626619_3.jpg[/img][/align][b]3.2.5 专属性结果[/b]将人凝血因子Ⅷ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅷ溶液定标后,取不含人凝血因子Ⅷ的基质溶液,进行人凝血因子Ⅷ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表10。[align=center]表10 专属性检测结果[/align][align=center][img=,569,238]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141728_01_1626619_3.png[/img][/align][b]3.3 蛋白含量1%的药典稀释液稀释人凝血酶原复合物效价检测方法验证3.3.1 线性关系结果[/b]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅸ标准品进行Ⅸ效价测定定标,三次直线回归方程相关系数R值结果见表11。[align=center]表11 生理氯化钠稀释FⅨ定标R值检测结果[/align][align=center][img=,571,139]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141729_01_1626619_3.png[/img][/align][b]3.3.2 准确度结果[/b]用生理氯化钠溶液稀释的每1 ml含1.00 IU人凝血因子Ⅸ后再用药典稀释液再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表12。[align=center]表12 准确度检测结果[/align][align=center][img=,571,274]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141730_01_1626619_3.png[/img][/align][b]3.3.3 精密度结果[/b]2015ZK0901批人凝血酶原复合物用生理氯化钠溶液稀释15倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表13。[align=center]表13 精密度检测结果[/align][align=center][img=,572,506]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141731_01_1626619_3.png[/img][/align][b]3.3.4 日间精密度结果[/b]在不同的三天2015ZK0901批人凝血酶原复合物质控品用生理氯化钠溶液稀释15倍后再用药典稀释液再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表14。[align=center]表14 日间精密度检测结果[/align][align=center][img=,590,1702]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141737_01_1626619_3.jpg[/img][/align][align=left][b]3.3.5 专属性结果[/b][/align]将生理氯化钠溶液稀释至1 IU/ml的人凝血因子Ⅸ溶液定标后,取不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表15。[align=center]表15 专属性检测结果[/align][align=center][img=,566,236]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141739_01_1626619_3.png[/img][/align][b]3.4 人凝血因子缺乏血浆进行预稀释人凝血酶原复合物效价检测方法验证3.4.1 线性关系结果[/b]用人凝血因子Ⅸ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅸ标准品进行Ⅸ效价测定定标,三次直线回归方程相关系数R值结果见表16。[align=center]表16 人凝血因子缺乏血浆稀释FⅨ定标R值检测结果[/align][align=center][img=,567,133]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141740_01_1626619_3.png[/img][/align][b]3.4.2 准确度结果[/b]用人凝血因子Ⅸ缺乏血浆稀释的每1 ml含1.00 IU人凝血因子Ⅸ后用Owren-Koller(稀释液)再稀释1.5倍,3倍,6倍,8倍的标准品溶液的检测结果见表17。[align=center]表17 准确度检测结果[/align][align=center][img=,568,274]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141741_01_1626619_3.png[/img][/align][b]3.4.3 精密度结果[/b]2015ZK0901批人凝血酶原复合物质控品用人凝血因子Ⅸ缺乏血浆稀释15倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表18。[align=center]表18 精密度检测结果[/align][align=center][img=,571,576]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141742_01_1626619_3.png[/img][/align][b]3.4.4 日间精密度结果[/b]在不同的三天2015ZK0901批人凝血酶原复合物质控品用人凝血因子Ⅸ缺乏血浆稀释15倍后再用Owren-Koller(稀释液)再稀释1倍,1.5倍,3倍,6倍,8倍的检测结果见表19。[align=center]表19 日间精密度检测结果[/align][align=center][img=,588,1756]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141747_01_1626619_3.jpg[/img][/align][b]3.4.5 专属性结果[/b]将人凝血因子Ⅸ缺乏血浆稀释至1 IU/ml的人凝血因子Ⅸ溶液定标后,取不含人凝血酶原复合物的基质溶液,进行人凝血因子Ⅸ效价的检测,并对用基质溶液稀释的高浓度和低浓度的标准品进行检测,检测结果见表20。[align=center]表20 专属性检测结果[/align][align=center][img=,568,240]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141748_01_1626619_3.png[/img][/align][b]4讨论[/b]本章对人凝血因子Ⅷ、人凝血酶原复合物中的FⅨ效价测定方法进行了方法学验证,供试品因子效价的测定可采用两种不同的稀释方法进行,先用生理氯化钠溶液稀释至(约)1 IU/ml再用药典稀释液进行稀释或者先用凝血因子缺乏血浆稀释至(约)1 IU/ml再用Owren-Koller(稀释液)稀释。两种稀释方法的因子效价检测所进行的线性关系,准确度,精密度、日间精密度、专属性验证均符合方法学验证的标准,适用于因子效价的检测。其中先用生理氯化钠溶液稀释至(约)1 IU/ml再用药典稀释液进行稀释检测方法适用于开放型(可使用不同厂家试剂)的血凝仪,且所用稀释剂价格低廉,降低了检测成本;而先用凝血因子缺乏血浆稀释至(约)1 IU/ml再用Owren-Koller(稀释液)稀释适用于Stago全自动血凝仪这种封闭式(只能使用本厂配套试剂)的血凝仪,且由于使用凝血因子缺乏血浆这种价格昂贵的试剂提高了检测成本。[b]参考文献[/b] 王卓, 赵雄, 吕茂民, 等. 血液制品的现状与展望 . 生物工程学报, 2011, 27(5):730-746. Newman J, et al. Methods for the productionof clinically effective intermediate and high-factor-Ⅷconcentrates . Brit J Haemat, 1971, 21:1. 王箐舟, 赵卉, 王威, 等. 第四批人凝血因子Ⅷ国家标准品制备和标定 .中国药品标准, 2013,14(3):188-190. 刘大英, 沈琦, 云志宏. 血浆和中纯FⅧ国家标准品FⅧ: C检测结果及分析. 中国输血杂志, 1995,8(2):87-88.
方案也好,最后的竣工验收报告都好,都有提到/监测因子/这个次,但找了水气声土的标准,都没找到监测因子的具体出处。想了解下HJ行业一些特定名词的解释,各位老师有谁知道的
用液相色谱检测生物柴油,检测器只能用蒸发光散射检测器吗?
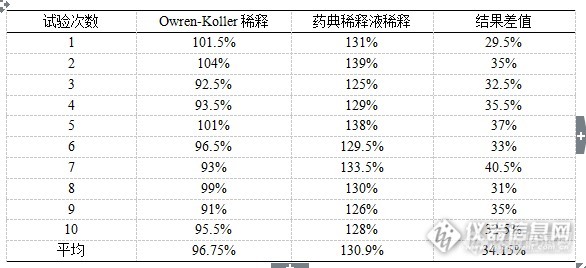
[align=center][/align][align=left][b] 摘要:目的 [/b]确立不同稀释液对凝血因子效价检测的影响,研究因子效价检测的稀释方法,从而完善因子类血液制品效价检测的方法。 [b]方法 [/b]对同一批和连续生产的10批人凝血因子Ⅷ、人凝血酶原复合物样品进行全自动血凝仪法的效价检测,分别选用全自动血凝仪稀释液和含1%人血白蛋白稀释液进行检测,统计10次以上的检测结果以确定不同稀释液之间的差别。 [b]结果 [/b]本实验确定了在人凝血因子Ⅷ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅷ的样品进行稀释,无论是对同一批质控品的测定还是对连续批次样品的测定,检测结果之间存在较大的差别。而在人凝血酶原复合物人凝血因子Ⅸ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅸ的样品进行稀释,同一批质控品和连续批次样品检测结果之间差别较小。[b]结论 [/b]因子类血液制品效价检测时,同一样品采用不同的稀释液进行稀释检测结果可能存在较大差别,应对血凝仪是否可用于因子类血液制品进行评估,并应建立起正确的检测操作规程。[/align][b] 关键词: [/b]凝血因子; 稀释液; 效价测定 目前国内血液制品的生产是以健康人血浆为原料,经过分离纯化和病毒灭活制成,主要分为三大类,人血白蛋白、人免疫球蛋白类产品、人凝血因子类产品。国内已上市或在研的人凝血因子类产品主要有人凝血因子Ⅷ、人凝血酶原复合物、人纤维蛋白原、人纤维蛋白粘合剂、人凝血因子Ⅸ、人抗凝血酶Ⅲ等。人凝血因子Ⅷ主要用于防治甲型血友病和获得性凝血因子Ⅷ缺乏而致的出血症状病人的手术治疗。人凝血酶原复合物主要有效成分为人凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ,主要用于治疗主要用于乙型血友病、 维生素K依赖的凝血因子缺乏症等病症的治疗。 人凝血因子Ⅸ主要用于防治乙型血友病和获得性凝血因子Ⅸ缺乏而致的出血症状病人的手术治疗。因子类血液制品是血液中凝血因子的高纯度浓缩物,在进行效价测定时需要对样品进行稀释,而稀释液中蛋白含量的不同对其检测结果有着影响。因子效价测定方法有一期法、二期法和发色底物法。一期法是目前应用最广泛的检测方法,系用人凝血因子缺乏血浆为基质,在APTT试剂和氯化钙的参与下,根据凝血因子国家标准品和供试品的凝集时间来计算供试品中的人凝血因子效价,实际检测过程中将基于一期法原理的人凝血因子效价测定法分为三种方法,即手工法、半自动血凝仪法、全自动血凝仪法。全自动血凝仪只是对一期法中各反应试剂的加入顺序进行了修订以便实现仪器的自动操作。相对于手工法检测,消除了很多主观因素。在日常工作中,当使用不同种类的稀释剂而采用相同的检测原理和方法进行效价测定应不会对测定结果产生影响,但实际工作中发现使用不同种类的稀释剂对效价测定结果有一定的影响。在人凝血因子Ⅷ效价检测过程中,采用手工法、半自动血凝仪法、全自动血凝仪法进行人凝血因子Ⅷ效价的比对试验,发现手工法、半自动血凝仪法检测结果一致,这两种方法比全自动血凝仪法的检测结果高20%以上。血液制品的原料来源于人血浆,受原料限制,一直较为稀缺,尤其是当前人凝血因子Ⅷ的生产量远远无法满足血友病患者的需求[sup][[/sup][sup]1-5[/sup][sup]][/sup],不同检测方法间20%以上的检测差别可能影响20%的产品收率,所以建立起因子类产品效价准确的检测至关重要。[b][b]1 实验仪器与试剂1.1 仪器[/b][/b]Stago-compact全自动血凝仪(法国Diagnostica Stago公司),漩涡振荡器(美国Thermo Scientific公司)。[b][b]1.2 试剂[/b][/b]人凝血因子Ⅷ缺乏血浆(法国Diagnostica Stago公司),人凝血因子Ⅸ缺乏血浆(法国Diagnostica Stago公司),APTT试剂(法国Diagnostica Stago公司),Owren-Koller(稀释液)(法国Diagnostica Stago公司),0.025 mol/L氯化钙溶液(法国Diagnostica Stago公司),Desorb U(清洗液)(法国Diagnostica Stago公司),人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),生理氯化钠溶液(石家庄四药有限公司),咪唑(天津市巴斯夫化工有限公司),氯化钠(天津市巴斯夫化工有限公司),枸橼酸钠(台山新宁制药有限公司),人血白蛋白(公司自产)。[b][b]2 方法2.1 人凝血因子Ⅷ不同稀释液稀释效价测定2.1.1 人凝血因子Ⅷ供试品Owren-Koller(稀释液)稀释效价测定方法[/b][/b] 人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.1.2 人凝血因子Ⅷ供试品药典稀释液稀释效价测定方法[/b][/b] 人凝血因子Ⅷ国家标准品的定标同2.1.1人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.2 人凝血酶原复合物人凝血因子Ⅸ不同稀释液稀释效价测定2.2.1 人凝血酶原复合物供试品Owren-Koller(稀释液)稀释效价测定方法[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《STAGO Compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]2.2.2 人凝血酶原复合物供试品药典稀释液稀释效价测定方法[/b][/b] 人凝血因子Ⅸ国家标准品的定标同2.1.1。人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]3 结果3.1 人凝血因子Ⅷ不同稀释液稀释效价测定结果[/b][/b] 2015ZK0801批人凝血因子Ⅷ为泰邦公司人凝血因子Ⅷ产品的质控品,取自正常生产的产品,用国家标准品标定后用作工作质控品。在进行人凝血因子Ⅷ效价测定时,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅷ进行再稀释。检验结果见表1,效价检测结果为效价标示量的百分比。[align=center]表1 FⅧ质控品两种稀释液检测结果对比[/align][align=center][img=,586,268]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141920_02_1626619_3.png[/img][/align]用柱形图表示,如图1:[align=center][img=,488,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141921_02_1626619_3.png[/img][/align][align=center]图1 FⅧ质控品两种稀释液检测结果对比[/align] 选取泰邦公司生产的连续10个批次的人凝血因子Ⅷ产品,进行人凝血因子Ⅷ效价测定,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅷ进行再稀释。检验结果见表2,效价检测结果为效价标示量的百分比。[align=center]表2 连续10批FⅧ两种稀释液检测结果对比[/align][align=center][img=,580,273]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141921_03_1626619_3.png[/img][/align]用柱形图表示,如图2:[align=center][img=,499,310]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141922_01_1626619_3.png[/img][/align][align=center]图 2 连续10批FⅧ两种稀释液检测结果对比[/align][b][b]3.2 人凝血酶原复合物不同稀释液稀释效价测定结果[/b][/b] 2015ZK0901批人凝血酶原复合物为泰邦公司人凝血酶原复合物产品的质控品,取自正常生产的产品,用国家标准品标定后用作工作质控品。在进行人凝血酶原复合物人凝血因子Ⅸ效价测定时,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅸ进行再稀释。检验结果见表3,效价检测结果为效价标示量的百分比。[align=center]表3 PCC质控品两种稀释液检测结果对比[/align][align=center][img=,580,269]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141923_01_1626619_3.png[/img][/align]用柱形图表示,如图3:[align=center][img=,548,288]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141923_02_1626619_3.png[/img][/align][align=center]图3 PCC质控品两种稀释液检测结果对比[/align] 选取泰邦公司生产的连续10个批次的人凝血酶原复合物产品,进行人凝血酶原复合物人凝血因子Ⅸ效价测定,分别用Owren-Koller(稀释液)和药典稀释液(取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合,加适量20%人血白蛋白至终浓度为1%配制而成)对每1 ml约含1.00 IU人凝血因子Ⅸ进行再稀释。检验结果见表4,效价检测结果为效价标示量的百分比。[align=center]表4 连续10批PCC两种稀释液检测结果对比[/align][align=center][img=,573,259]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141947_01_1626619_3.png[/img][/align]用柱形图表示,如图4:[align=center][img=,548,327]http://ng1.17img.cn/bbsfiles/images/2017/09/201709141947_03_1626619_3.png[/img][/align][align=center]图4 连续10批PCC两种稀释液检测结果对比[/align][b][b]4 讨论[/b][/b] 本实验确定了在人凝血因子Ⅷ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅷ的样品进行稀释,无论是对同一批质控品的测定还是对连续批次样品的测定,检测结果之间存在较大的差别,另外对FⅧ质控品两种稀释液检测结果运用软件SPSS17.0进行均值单因素ANOVA比较,计算P值,P<0.05表明两种方法的结果有显著性差异,含有蛋白的稀释液的检测结果明显高于不含蛋白的稀释液。而在人凝血酶原复合物人凝血因子Ⅸ的效价检测中,采用不同的稀释液对每1 ml约含1.00 IU人凝血因子Ⅸ的样品进行稀释,同一批质控品和连续批次样品检测结果之间差别较小,另外对PCC质控品两种稀释液检测结果运用软件SPSS17.0进行均值单因素ANOVA比较,计算P值,P>0.05表明两种方法的结果无显著性差异。在使用全自动血凝仪进行人凝血因子Ⅷ和人凝血酶原复合物等因子类血液制品效价检测时,一般按照仪器的使用说明书和配套试剂进行稀释检测,但是忽视了血凝仪的开发目的是用于临床血浆样品的检测,而血浆与高纯度的血液制品浓缩物是不同的,用检测血浆样品的方法进行因子类血液制品的效价检测可能影响检测结果。因子类血液制品效价检测时,同一样品采用不同的稀释液进行稀释检测结果可能存在较大差别,应对血凝仪是否可用于因子类血液制品进行评估,并应建立起正确的检测操作规程。因子类血液制品采用不同的稀释液进行稀释检测结果可能存在较大差别可能跟产品本身的性质有关,因子类血液制品经过分离、纯化,去除了众多的杂质蛋白,为高纯度的浓缩物,活性较高,但蛋白质含量较低,人凝血因子Ⅷ的蛋白质含量约为0.1%,人凝血酶原复合物的蛋白质含量约为2.3%,而临床血浆样本的蛋白质含量约为5%,, 人凝血因子Ⅷ加入含1%人血白蛋白的稀释液后对FⅧ效价测定影响较大,PCC中加入含1%人血白蛋白的稀释液后对FⅨ效价测定影响较小,可能是人凝血因子Ⅷ的蛋白质含量远小于血凝仪设计用于检测的血浆样本的蛋白含量,故建立不同蛋白质浓度梯度的稀释液对因子效价进行测定,从而确认蛋白质浓度对因效价测定的影响。[b]参考文献:[/b]Cheng E, Jinzenji D, Lorthiois AP, et al. Purification of coagulation factorⅧ using chromatographic methods. Direct chromatography of plasma in anion exchange resins . Biotechnol Lett, 2010, 32(9):1207-1214.李策生, 周志军, 胡勇, 等. 人凝血因子Ⅷ中试纯化工艺的质量控制 .中国生物制品学杂志, 2013, 26(10):1508-1512.冉曙光, 刘文芳, 赵辉. 凝血因子Ⅷ浓缩物的制备及安全性和有效性 .中国输血杂志, 2008, 21(2):156-159.倪道明, 朱威. 血液制品 . 北京: 人民卫生出版社, 2013:21.王卓, 赵雄, 吕茂民, 等. 血液制品的现状与展望 . 生物工程学报, 2011, 27(5):730-746.[b] [/b]
请问水质检测中哪些因子不用采集平行样品?
我现在要做微生物的检测,有些问题想请教一下,你们微生物的方法是按照国标检测的吗?国标上写的不是很详细?微生物的检测阳性和阴性对照需要两个房间是吗?是需要用显微镜看,还是肉眼看呢?谢谢了重复发贴, 请看[url]http://bbs.instrument.com.cn/shtml/20100426/2521429/[/url]
检测器对不同物质的响应值不同,测定物质绝对/相对校正因子,是准确定量的基础。采用TCD作为检测器时,如何确定物质相对校正因子?
高效液相色谱带示差折光检测器,检测有关物质,需要考虑每个已知杂质的响应因子吗?药典方法是采用不加校正因子的主成分自身稀释法,但是我们用杂质外标法做出来每个杂质的响应跟主成分差别很大(超出0.9~1.1范围)
蜂蜜中葵烯酸检测校正因子如何计算
我想问一下各位:同一种物质,在同一个检测器(我用的FID)和同一根色谱柱上做内标法检测,它是相对校正因子是不是一样的呢?相对校正因子与载气的流速,柱温,检测器温度,进样温度有关吗?????另外我还想问一下,我发现我所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],不知怎么回事,保留时间总是有点不重复,仪器工作的时间越长,保留时间越提前,我也进行了分析,如果是载气漏气的话,应该会靠后,当然我也检测了载气并不漏气,这样我想只有一个问题那就是载气是不是在仪器工作的时间越长,载气越来越大????????????还请各位能多多帮我分析一下原因,谢谢了!!!
[size=4]葡萄酒中甲醇的检测方法内标法校正因子有哪位高手解答一下?非常感谢!1.用外标法不可以么?什么叫校正因子f,引入校正因子有什么作用,看了一下内标法资料一头雾水,没怎么明白。2.校正因子f计算公式中f=A1/A2*d2/d1中d1、d2相对密度什么意思?和密度有区别么?3.计算公式中I内标物含量mg/L怎么知道的?是添加在酒样中mg/L么?用到内标物密度?4.4-甲基-2-戊醇溶液时内标物?这个怎么配置啊,用乙醇溶液配制,怎么知道含量mg/L[/size]
[font=宋体]来信:[/font][font=Arial][/font][font=宋体] 土壤污染重点监管单位土壤和地下水监测污染因子的选择依据。如果通过自行监测发现土壤或地下水中存在企业特征污染物之外污染物超标情况如何处理。[/font][font=Arial][/font][font=宋体]回复:[/font][font=Arial][/font][font=Arial][/font][font=宋体] 根据《工业企业土壤和地下水自行监测技术指南(试行)》,土壤和地下水自行监测的监测指标分为初次监测和后续监测两种情形。初次监测,原则上所有土壤监测点的监测指标至少应包括[/font][font=Arial]GB 36600[/font][font=宋体]表[/font][font=Arial]1[/font][font=宋体]基本项目,地下水监测井的监测指标至少应包括[/font][font=Arial]GB/T 14848[/font][font=宋体]表[/font][font=Arial]1[/font][font=宋体]常规指标(微生物、放射性除外)。企业内任何重点单元涉及上述范围外的关注污染物,应根据其土壤或地下水的污染特性,将其纳入企业内所有土壤或地下水监测点的初次监测指标。后续监测,按照重点单元确定监测指标,每个重点单元对应的监测指标至少应包括该重点单元对应的任一监测点[/font][font=Arial]/[/font][font=宋体]监测井在前期监测中曾超标的污染物,及该重点单元涉及的所有关注污染物。这是因为考虑到初次监测时,企业对其用地土壤和地下水环境现状并不清楚,监测土壤与地下水标准基本项目中与企业工艺无关的污染物因子,可以有助于企业掌握其用地土壤和地下水环境现状,防控土壤污染风险。[/font][font=Arial][/font][font=宋体] 如通过自行监测发现土壤或地下水中存在企业特征污染物之外的污染物超标的,可以按照《建设用地土壤污染责任人认定暂行办法》有关规定开展土壤污染责任人认定。[/font][font=Arial][/font]
[b]中文摘要:目的[/b] 确立因子类血液制品中蛋白质含量对效价检测结果的影响,从而完善因子类血液制品效价检测的方法。[b]方法 [/b]选取不同蛋白质浓度梯度的稀释液对同一供试品进行稀释来确定蛋白质影响的规律。 [b]结果 [/b]建立起人凝血因子Ⅷ、人凝血酶原复合物的全自动血凝仪因子效价检测方法,根据效价检测反应体系中蛋白浓度对检测结果的影响,建立因子类血液制品效价全自动血凝仪检测的方法。[b]结论 [/b]建立的两种稀释方法均消除了样品中蛋白质含量的不同对检测结果的影响,提高了检测的准确性,不但可以适用于现在产品的效价检测,而且适用于随着生产工艺的提升生产的更高纯度、低蛋白含量的FⅧ和PCC,同时也是对中国药典标准的补充。[b]关键词[/b]:人凝血因子Ⅷ;人凝血酶原复合物;效价;蛋白含量 人凝血因子Ⅷ、人凝血酶原复合物、人凝血因子Ⅸ等因子类血液制品,是以健康人血浆为原料,经分离纯化和病毒灭活制成,在临床上主要用于各种凝血因子缺乏的治疗,这些因子类血液制品的凝血因子效价是药品有效性的指标,凝血因子效价的测定也是药品质量检测中的关键检测项目。血液制品生产企业及各级检测机构一般采用全自动血凝仪并按照仪器使用说明来进行因子效价的检测,然而在不同检测方法结果比对中,发现全自动血凝仪检测结果与中国药典中一期法的检测结果在部分因子效价检测中存在检测差异,差异可能是样品稀释中使用的稀释液的蛋白含量不同引起的,故本课题主要研究因子类血液制品中蛋白质含量对效价检测结果影响。通过蛋白含量对因子效价检测影响的研究建立起的全自动血凝仪因子效价检测方法,消除了产品本身性质的影响,可以准确进行因子效价的测定,方法的建立不但可以准确控制因子类血液制品的质量,保证生产企业持续稳定生产出质量均一的药品,而且可以减少因子类产品在临床使用中的风险。[b]1 实验仪器与试剂[b]1.1 仪器[/b][/b]Stago-compact全自动血凝仪(法国Diagnostica Stago公司),漩涡振荡器(美国Thermo Scientific公司)。[b][b]1.2 试剂[/b][/b]人凝血因子Ⅷ缺乏血浆(法国Diagnostica Stago公司),人凝血因子Ⅸ缺乏血浆(法国Diagnostica Stago公司),APTT试剂(法国Diagnostica Stago公司),Owren-Koller(稀释液)(法国Diagnostica Stago公司),0.025 mol/L氯化钙溶液(法国Diagnostica Stago公司),Desorb U(清洗液)(法国Diagnostica Stago公司),人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),生理氯化钠溶液(石家庄四药有限公司),咪唑(天津市巴斯夫化工有限公司),氯化钠(天津市巴斯夫化工有限公司),枸橼酸钠(台山新宁制药有限公司),人血白蛋白(公司自产)。[b][b]2 方法 2.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备:选取全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液分别定义为稀释液1、稀释液2、稀释液3。向3种稀释液中分别加入人血白蛋白,使其中人血白蛋白的浓度分别为0、0.5%、1%、3%、5%。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.2 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定[/b] [/b]人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.3 人凝血酶原复合物人凝血因子Ⅸ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备同2.1。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]2.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]3 结果3.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0801批人凝血因子Ⅷ进行了不同蛋白质浓度梯度稀释效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表1、2、3,效价检测结果为效价标示量的百分比。[align=center]表1 FⅧ质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][/align][align=center][img=,590,266]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142017_01_1626619_3.png[/img][/align][align=center]表2 FⅧ质控品不同蛋白浓度梯度稀释液2检测结果 [/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_01_1626619_3.png[/img][/align][align=center]表3 FⅧ质控品不同蛋白浓度梯度稀释液3检测结果 [/align][align=center][img=,585,261]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_02_1626619_3.png[/img][/align]人凝血因子Ⅷ质控品2015ZK0801批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释效价检测结果平均值用折线图表示,如图1:[align=center]图1 FⅧ质控品不同蛋白质浓度检测结果对比[/align][align=center][img=,548,295]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_03_1626619_3.png[/img][/align] 选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了不同蛋白质浓度梯度稀释效价测定,人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果见表4、5,效价检测结果为效价标示量的百分比。[align=center]表4 658668A批制剂FⅧ检测结果[/align][align=center][img=,585,99]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142020_01_1626619_3.png[/img][/align][align=center]表5 A3B1814批制剂FⅧ检测结果[/align][align=center][img=,577,97]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142021_01_1626619_3.png[/img][/align]FⅧ效价检测结果用折线图表示,如图2、3:[align=center][img=,563,299]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142029_01_1626619_3.png[/img][/align][align=center]图2 658668A批不同蛋白质浓度检测结果对比[/align][align=center][img=,567,287]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142030_01_1626619_3.png[/img][/align][align=center][/align][align=center]图3 A3B1814批不同蛋白质浓度检测结果对比[/align][b][b]3.2 人凝血酶原复合物不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0901批人凝血酶原复合物进行了不同蛋白质浓度梯度稀释人凝血因子Ⅸ效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、2%、3%、4%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表6、7、8,效价检测结果为效价标示量的百分比。[align=center]表6 PCC质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][img=,583,269]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_01_1626619_3.png[/img][/align][align=center]表7 PCC质控品不同蛋白浓度梯度稀释液2检测结果[/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_02_1626619_3.png[/img][/align][align=center]表8 PCC质控品不同蛋白浓度梯度稀释液3检测结果[/align][align=center][img=,593,263]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142043_01_1626619_3.png[/img][/align]人凝血酶原复合物质控品2015ZK0901批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释FⅨ效价检测结果平均值用折线图表示,如图4:[align=center][img=,556,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_01_1626619_3.png[/img][/align][align=center]图4 PCC质控品不同蛋白质浓度FⅨ检测结果对比[/align][b][b]3.3 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0801批人凝血因子Ⅷ进行了人凝血因子缺乏血浆稀释效价测定,共测定10次。效价检测结果见表9,效价检测结果为效价标示量的百分比。[align=center]表9 FⅧ质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,579,74]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_02_1626619_3.png[/img][/align]选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了人凝血因子缺乏血浆稀释效价测定。效价检测结果见表10,效价检测结果为效价标示量的百分比。[align=center]表10 国外产品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,578,77]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142036_01_1626619_3.png[/img][/align][b][b]3.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0901批人凝血酶原复合物进行了人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价测定,共测定10次。效价检测结果见表11,效价检测结果为效价标示量的百分比。[align=center]表11 PCC质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,582,89]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142047_01_1626619_3.png[/img][/align][b][b]4 讨论[/b][/b] 本实验中对人凝血因子Ⅷ和人凝血酶原复合物分别用不同蛋白浓度梯度的稀释液进行了效价测定,另外用人凝血因子缺乏血浆稀释后进行了效价测定。因子效价测定中,稀释液1、稀释液2、稀释液3中加入相同浓度的人血白蛋白后,得到的因子效价检测结果没有差异,说明全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液作为稀释液时没有区别。 人凝血因子Ⅷ、人凝血酶原复合物不同蛋白浓度梯度效价测定时,随着稀释液中蛋白质含量的增高,效价检测结果也不断升高,但在人凝血因子Ⅷ效价测定中,采用蛋白质含量为1%、3%的稀释液时,效价检测结果间均无显著差别,在人凝血酶原复合物人凝血因子Ⅸ效价测定中,采用蛋白质含量为0、0.5%、1%的稀释液时,效价检测结果间均无显著差别。另外,人凝血因子Ⅷ进行人凝血因子缺乏血浆稀释效价测定效价检测结果与采用蛋白质含量为1%、3%的稀释液得到的检测结果也无显著差异,人凝血酶原复合物人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价检测结果与采用蛋白质含量为0、0.5%、1%的稀释液得到的检测结果也无显著差异。另外,国外生产的人凝血因子Ⅷ和VWF的混合制剂FⅧ效价的检测结果及血浆、稀释液的影响同泰邦公司产品一致。[b]参考文献[/b][align=left] 邬杨斌, 余蓉. 凝血因子Ⅸ复合物的研制 . 华西药学杂志, 2000, 15(3):177-179. Pabinger I, Brenner B, Kalina U, et al. Prothrombin complex concentrate(Beriplexw P/N)for emergency anticoagulation reversal: A prospective multinational clinical trial . J Thromb Haemost, 2008, 6(4):622-631. Kiman E, Elela AA, Ramsis N, et al. Evaluation of the coagulation factors activity of Cryosupernatant . Suez Canal Univ Med J, 2003, 6(2):247-258.Tullis JL, Melin M, Jurigian P. Clinical use of human Prothrombin complexes . N Engl J Med, 1965, 73(13):667-674.马莉, 孙盼, 李长清, 等. 去冷沉淀血浆的质量分析 . 中国生物制品学杂志, 2013, 26(1):81-83.魏舒, 时凯, 刘国荣, 等. 冻干人凝血酶原复合物的生产工艺研究 . 中国输血杂志, 2008, 21(10):282-284.Samama CM. Prothrombin complex concentrates: a brief review . Eur J Anaesthesiol, 2008, 25(10):784-789.焦丽华, 代旭兰, 刘文芳. 凝血酶原复合物的制备及其临床应用进展 .中国输血杂志, 2008, 21(9):737-741.[/align][b] [/b]
请教在食品农药残留检测中稀释因子是怎么计算的,是(30+40)/35吗?
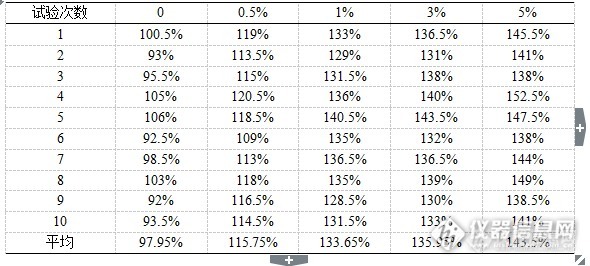
[b]中文摘要:目的[/b] 确立因子类血液制品中蛋白质含量对效价检测结果的影响,从而完善因子类血液制品效价检测的方法。[b]方法 [/b]选取不同蛋白质浓度梯度的稀释液对同一供试品进行稀释来确定蛋白质影响的规律。 [b]结果 [/b]建立起人凝血因子Ⅷ、人凝血酶原复合物的全自动血凝仪因子效价检测方法,根据效价检测反应体系中蛋白浓度对检测结果的影响,建立因子类血液制品效价全自动血凝仪检测的方法。[b]结论 [/b]建立的两种稀释方法均消除了样品中蛋白质含量的不同对检测结果的影响,提高了检测的准确性,不但可以适用于现在产品的效价检测,而且适用于随着生产工艺的提升生产的更高纯度、低蛋白含量的FⅧ和PCC,同时也是对中国药典标准的补充。[b]关键词[/b]:人凝血因子Ⅷ;人凝血酶原复合物;效价;蛋白含量 人凝血因子Ⅷ、人凝血酶原复合物、人凝血因子Ⅸ等因子类血液制品,是以健康人血浆为原料,经分离纯化和病毒灭活制成,在临床上主要用于各种凝血因子缺乏的治疗,这些因子类血液制品的凝血因子效价是药品有效性的指标,凝血因子效价的测定也是药品质量检测中的关键检测项目。血液制品生产企业及各级检测机构一般采用全自动血凝仪并按照仪器使用说明来进行因子效价的检测,然而在不同检测方法结果比对中,发现全自动血凝仪检测结果与中国药典中一期法的检测结果在部分因子效价检测中存在检测差异,差异可能是样品稀释中使用的稀释液的蛋白含量不同引起的,故本课题主要研究因子类血液制品中蛋白质含量对效价检测结果影响。通过蛋白含量对因子效价检测影响的研究建立起的全自动血凝仪因子效价检测方法,消除了产品本身性质的影响,可以准确进行因子效价的测定,方法的建立不但可以准确控制因子类血液制品的质量,保证生产企业持续稳定生产出质量均一的药品,而且可以减少因子类产品在临床使用中的风险。[b]1 实验仪器与试剂[b]1.1 仪器[/b][/b]Stago-compact全自动血凝仪(法国Diagnostica Stago公司),漩涡振荡器(美国Thermo Scientific公司)。[b][b]1.2 试剂[/b][/b]人凝血因子Ⅷ缺乏血浆(法国Diagnostica Stago公司),人凝血因子Ⅸ缺乏血浆(法国Diagnostica Stago公司),APTT试剂(法国Diagnostica Stago公司),Owren-Koller(稀释液)(法国Diagnostica Stago公司),0.025 mol/L氯化钙溶液(法国Diagnostica Stago公司),Desorb U(清洗液)(法国Diagnostica Stago公司),人凝血因子Ⅷ国家标准品(批号20100101),人凝血酶原复合物国家标准品(批号20130306),生理氯化钠溶液(石家庄四药有限公司),咪唑(天津市巴斯夫化工有限公司),氯化钠(天津市巴斯夫化工有限公司),枸橼酸钠(台山新宁制药有限公司),人血白蛋白(公司自产)。[b][b]2 方法2.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备:选取全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液分别定义为稀释液1、稀释液2、稀释液3。向3种稀释液中分别加入人血白蛋白,使其中人血白蛋白的浓度分别为0、0.5%、1%、3%、5%。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.2 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定[/b] [/b]人凝血因子Ⅷ国家标准品的定标:取1支人凝血因子Ⅷ国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1ml含1.00 IU人凝血因子Ⅷ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅷ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅷ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅷ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅷ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅷ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血因子Ⅷ供试品效价测定:取人凝血因子Ⅷ供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅷ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅷ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅷ效价测定选项进行测定。[b][b]2.3 人凝血酶原复合物人凝血因子Ⅸ不同蛋白质浓度梯度稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 不同蛋白质浓度梯度稀释液制备同2.1。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用生理氯化钠溶液将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用含不同蛋白浓度的稀释液做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]2.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定[/b][/b] 人凝血因子Ⅸ国家标准品的定标:取1支人凝血酶原复合物国家标准品,加入1.0 ml纯化水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml含1.00 IU人凝血因子Ⅸ,将Desorb U(清洗液)、复溶后的人凝血因子Ⅸ缺乏血浆、0.025 mol/L氯化钙溶液、APTT以及每1 ml含1.00 IU的人凝血因子Ⅸ标准品溶液分别装入全自动血凝仪的试剂抽屉,将Owren-Koller(稀释液)装入全自动血凝仪的样本抽屉,按照《Stago-compact全自动血凝仪标准操作规程》选择人凝血因子Ⅸ效价测定定标程序进行定标,仪器自动将装入的人凝血因子Ⅸ标准品溶液再进行2倍、4倍、8倍稀释,建立人凝血因子Ⅸ标准品溶液效价(分别为1.00 IU/ml、0.50 IU/ml、0.25 IU/ml、0.13 IU/ml)的对数对其相应凝固时间对数的直线回归方程。 人凝血酶原复合物供试品效价测定:取人凝血酶原复合物供试品,按其标示装量加入灭菌注射用水复溶,轻轻混匀,用人凝血因子Ⅸ缺乏血浆将其稀释成每1 ml约含1.00 IU人凝血因子Ⅸ,再用Owren-Koller(稀释液)做2倍、4倍稀释,将稀释后的供试品溶液装入全自动血凝仪的样本抽屉,选择人凝血因子Ⅸ效价测定选项进行测定。[b][b]3 结果3.1 人凝血因子Ⅷ不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0801批人凝血因子Ⅷ进行了不同蛋白质浓度梯度稀释效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表1、2、3,效价检测结果为效价标示量的百分比。[align=center]表1 FⅧ质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][img=,590,266]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142017_01_1626619_3.png[/img][/align][align=center]表2 FⅧ质控品不同蛋白浓度梯度稀释液2检测结果 [/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_01_1626619_3.png[/img][/align][align=center]表3 FⅧ质控品不同蛋白浓度梯度稀释液3检测结果 [/align][align=center][img=,585,261]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_02_1626619_3.png[/img][/align]人凝血因子Ⅷ质控品2015ZK0801批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释效价检测结果平均值用折线图表示,如图1:[align=center]图1 FⅧ质控品不同蛋白质浓度检测结果对比[/align][align=center][img=,548,295]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142019_03_1626619_3.png[/img][/align] 选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了不同蛋白质浓度梯度稀释效价测定,人血白蛋白的浓度分别为0、0.5%、1%、3%、5%的稀释液1、稀释液2、稀释液3的效价检测结果见表4、5,效价检测结果为效价标示量的百分比。[align=center]表4 658668A批制剂FⅧ检测结果[/align][align=center][img=,585,99]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142020_01_1626619_3.png[/img][/align][align=center]表5 A3B1814批制剂FⅧ检测结果[/align][align=center][img=,577,97]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142021_01_1626619_3.png[/img][/align]FⅧ效价检测结果用折线图表示,如图2、3:[align=center][img=,563,299]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142029_01_1626619_3.png[/img][/align][align=center]图2 658668A批不同蛋白质浓度检测结果对比[/align][align=center][img=,567,287]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142030_01_1626619_3.png[/img][/align][align=center]图3 A3B1814批不同蛋白质浓度检测结果对比[/align][b][b]3.2 人凝血酶原复合物不同蛋白质浓度梯度稀释效价测定结果[/b][/b] 选取2015ZK0901批人凝血酶原复合物进行了不同蛋白质浓度梯度稀释人凝血因子Ⅸ效价测定,不同浓度稀释液分别测定10次。人血白蛋白的浓度分别为0、0.5%、1%、2%、3%、4%、5%的稀释液1、稀释液2、稀释液3的效价检测结果分别见表6、7、8,效价检测结果为效价标示量的百分比。[align=center]表6 PCC质控品不同蛋白浓度梯度稀释液1检测结果[/align][align=center][img=,583,269]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_01_1626619_3.png[/img][/align][align=center]表7 PCC质控品不同蛋白浓度梯度稀释液2检测结果[/align][align=center][img=,586,260]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142031_02_1626619_3.png[/img][/align][align=center]表8 PCC质控品不同蛋白浓度梯度稀释液3检测结果[/align][align=center][img=,593,263]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142043_01_1626619_3.png[/img][/align]人凝血酶原复合物质控品2015ZK0901批用不同蛋白质浓度梯度的稀释液1、稀释液2、稀释液3稀释FⅨ效价检测结果平均值用折线图表示,如图4:[align=center][img=,556,300]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_01_1626619_3.png[/img][/align][align=center]图4 PCC质控品不同蛋白质浓度FⅨ检测结果对比[/align][b][b]3.3 人凝血因子Ⅷ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0801批人凝血因子Ⅷ进行了人凝血因子缺乏血浆稀释效价测定,共测定10次。效价检测结果见表9,效价检测结果为效价标示量的百分比。[align=center]表9 FⅧ质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,579,74]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142032_02_1626619_3.png[/img][/align]选取2批国外产人凝血因子Ⅷ和VWF混合制剂进行了人凝血因子缺乏血浆稀释效价测定。效价检测结果见表10,效价检测结果为效价标示量的百分比。[align=center]表10 国外产品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,578,77]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142036_01_1626619_3.png[/img][/align][b][b]3.4 人凝血酶原复合物人凝血因子Ⅸ人凝血因子缺乏血浆稀释效价测定结果[/b][/b]选取2015ZK0901批人凝血酶原复合物进行了人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价测定,共测定10次。效价检测结果见表11,效价检测结果为效价标示量的百分比。[align=center]表11 PCC质控品人凝血因子缺乏血浆稀释检测结果[/align][align=center][img=,582,89]http://ng1.17img.cn/bbsfiles/images/2017/09/201709142047_01_1626619_3.png[/img][/align][b][b]4 讨论[/b][/b] 本实验中对人凝血因子Ⅷ和人凝血酶原复合物分别用不同蛋白浓度梯度的稀释液进行了效价测定,另外用人凝血因子缺乏血浆稀释后进行了效价测定。因子效价测定中,稀释液1、稀释液2、稀释液3中加入相同浓度的人血白蛋白后,得到的因子效价检测结果没有差异,说明全自动血凝仪的稀释液Owren-Koller、生理氯化钠溶液、取1体积的3.8%枸橼酸钠加入5体积咪唑缓冲液混合液作为稀释液时没有区别。 人凝血因子Ⅷ、人凝血酶原复合物不同蛋白浓度梯度效价测定时,随着稀释液中蛋白质含量的增高,效价检测结果也不断升高,但在人凝血因子Ⅷ效价测定中,采用蛋白质含量为1%、3%的稀释液时,效价检测结果间均无显著差别,在人凝血酶原复合物人凝血因子Ⅸ效价测定中,采用蛋白质含量为0、0.5%、1%的稀释液时,效价检测结果间均无显著差别。另外,人凝血因子Ⅷ进行人凝血因子缺乏血浆稀释效价测定效价检测结果与采用蛋白质含量为1%、3%的稀释液得到的检测结果也无显著差异,人凝血酶原复合物人凝血因子缺乏血浆稀释人凝血因子Ⅸ效价检测结果与采用蛋白质含量为0、0.5%、1%的稀释液得到的检测结果也无显著差异。另外,国外生产的人凝血因子Ⅷ和VWF的混合制剂FⅧ效价的检测结果及血浆、稀释液的影响同泰邦公司产品一致。[b]参考文献[/b][align=left] 邬杨斌, 余蓉. 凝血因子Ⅸ复合物的研制 . 华西药学杂志, 2000, 15(3):177-179. Pabinger I, Brenner B, Kalina U, et al. Prothrombin complex concentrate(Beriplexw P/N)for emergency anticoagulation reversal: A prospective multinational clinical trial . J Thromb Haemost, 2008, 6(4):622-631. Kiman E, Elela AA, Ramsis N, et al. Evaluation of the coagulation factors activity of Cryosupernatant . Suez Canal Univ Med J, 2003, 6(2):247-258.Tullis JL, Melin M, Jurigian P. Clinical use of human Prothrombin complexes . N Engl J Med, 1965, 73(13):667-674.马莉, 孙盼, 李长清, 等. 去冷沉淀血浆的质量分析 . 中国生物制品学杂志, 2013, 26(1):81-83.魏舒, 时凯, 刘国荣, 等. 冻干人凝血酶原复合物的生产工艺研究 . 中国输血杂志, 2008, 21(10):282-284.Samama CM. Prothrombin complex concentrates: a brief review . Eur J Anaesthesiol, 2008, 25(10):784-789.焦丽华, 代旭兰, 刘文芳. 凝血酶原复合物的制备及其临床应用进展 .中国输血杂志, 2008, 21(9):737-741.[/align][b] [/b]
求助:做环评,固废中浇注废铁、感应炉中炉渣、脱模废芯砂和生活垃圾的一般固废,一般需要检测哪些因子?
先谢谢大家:原来的检测方法是用TCD对含水量在20%至5%左右的丙酮检测,一张图谱上能明确的读出水的含量和丙酮的含量,现在采用FID检测,水峰是肯定没有啦,请教一天大概测定10批次左右的丙酮溶液,为了节省检验时间,我打算采用以下方法,请问对吗,是最节省时间的做法吗先进一针标准丙酮(色谱级),计算出当天的校正因子,同时测定含水丙酮的密度,再依照其与标准丙酮的密度比值,校正因子和峰面积折算被测丙酮的含量。含水量不同的丙酮,密度应该不一样,就不能按照TCD采用固定的校正因子面积归一化那样计算了,必须每天按照外标法,测定被测物质的密度折算质量来计算了对吗?
想购买微生物检测相关的设备,包括冰箱、灭菌箱、培养箱、超净工作台等,谁有相关的资料提供,包括型号、要求等,有奖励。
计量所中哪些检测仪器需要做修正因子更新呢?
我是微生物检测的新手,我想请问一下,我们的分析室刚建好,马上就要进行产品的检测,我想请问一下,在做产品的检测之前是不是要先用培养皿做工作台的洁净度检测。其他的还要做什么检测吗?
《地表水环境质量标准(GB3838-2008)中80项特定因子监测方法,主要是有机物。