哪位大侠知道黄酮类标准品的有效时间是多少????????????、、、[em04]
新手求助: 芦丁标准品,用来做类黄酮的标准曲线用的?有知道的请告诉一声。或者发个短信,不胜感激。13969884347 中国海洋大学食品工程学院
总黄酮的标准曲线吸光度范围为0.20-1.2,总多酚则是在0.1-0.4,测定样品时,总黄酮在0.1898,总多酚第一次没稀释是1.14,后来第二次稀释为0.47。请问0.1898和0.47能否代入标准曲线计算?1.14肯定是不能代入标准曲线的,相差太多了。感谢各位老师指导。
请问怎样可以买到像槲皮素等类黄酮物质的标准品?最好有电话,谢谢!
如题请问用芦丁对照品绘制标准曲线是否能用槲皮素或其他的黄酮对照品替代?由于实验室的芦丁标准品不见了,老师建议先用槲皮素替代,请问是否可行?
寻找黄铜的测定方法和标准
求助黄铜板GB2041-89、碳素结构钢GB700-88标准
实验原理黄酮类化合物是植物的重要次生代谢产物,也是一些保健品和中药材的有效成分之一。黄酮类化合物的定量方法常用的有HPLC法和分光光度法,在实际生产和科研过程中,对于黄酮单体的定量常采用HPLC法,而对总黄酮的测定,考虑到方法的简便、快捷以及可行性,多采用在碱性介质中加铝盐显色的分光光度法。在碱性条件下黄酮类化合物与铝盐形成络合物、在500nm波长处有最大吸收峰。标准品选用芦丁。试剂和器材一、试剂芦丁标准品。5%NaNO2;10%A1(NO3)3;5%NaOH;70%乙醇。二、材料新鲜银杏叶。三、器材容量瓶10ml(×7),25ml(×1),100ml(×2);吸管 0.5ml(×2),1ml(×2),2ml(×1),5ml(×1);分光光度计。操作方法一、制作标准曲线精密称取芦丁标准品5mg,用70%乙醇溶解,定容于25mL容量瓶中,摇匀,得0.2mg/mL的标准溶液。精确吸取标准溶液0.0、0.2、0.4、0.6、0.8、1.0、1.2mL,分别置于10mL容量瓶中,加入 5%NaNO20.4mL,摇匀,放置6min;加入10%A1(NO3)3 0.4mL,摇匀,放置6min;加入5%NaOH4.0mL,再加水至刻度,摇匀,放置15min。以试剂空白作为参比溶液。用1cm比色皿,在500nm波长处测定吸光度,绘制标准曲线。二、总黄酮的提取把新鲜的银杏叶低温烘干,使水分小于8%,制成干粉。精确称取干粉1.0g,置于 100mL容量瓶中,加入70%乙醇30mL,浸泡24h。超声波提取30min,过滤,滤液用70%乙醇定容于100mL容量瓶中,得到黄酮提取液,待用。三、测定吸取黄酮提取液1.00mL, 置于10mL容量瓶中,加入5%NaNO30.4mL,摇匀,放置6min;加入10%A1(NO3)3 0.4mL,摇匀,放置6min;加入5%NaOH4.0mL,再加水至刻度,摇匀,放置15min。以试剂空白作为参比溶液。用1cm比色皿,在500nm波长处测定吸光度,由标准曲线法计算总黄酮含量。注意事项对于某些热敏成分的提取,采用超声波破碎法效果较为理想。由于此过程是一个物理过程,浸提过程中无化学反应,被浸提的生物活性物质在一定时间内保持不变。
请问黄酮的标准溶液放置时间长了,里面的物质会发生变化吗?
蜂胶标准存"漏洞" 一些行业虽然已有质量标准,但由于造假技术的不断更新,原来的标准已经不能作为判定产品合不合格的依据。曾遭曝光的"蜂胶造假"事件就是典型的例子。 在被曝光企业提供的原料蜂胶的检测报告上显示:提纯蜂胶的总黄酮含量完全符合国家标准。而事实上,造假者是在树胶里添加了芦丁、槲皮素等黄酮类物质,人为提高了总黄酮含量。前有三聚氰胺,现有蜂胶黄酮,不知道以后还有什么其他产品会曝光出来。产品标准究竟该如何订制?类似造假事件该如何处理?这些不但需要执法部门思考,也希望大家给相关部门支支招!!
总黄酮测试和芦丁测试,总黄酮测试波长建议420nm(需要络和在碱性溶液中显色),而芦丁标准品也在如此处理后的最大吸收波长在507nm。如此二者测试对总黄酮含量的影响?!
化妆品中补骨脂特征成分补骨脂素、异补骨脂素、新补骨脂异黄酮和补骨脂二氢黄酮的检测方法1 适用范围 本方法规定了用高效液相色谱法定性检测化妆品中补骨脂特征成分补骨脂素、异补骨脂素、新补骨脂异黄酮和补骨脂二氢黄酮的方法。 本方法适用于化妆品中补骨脂特征成分补骨脂素、异补骨脂素、新补骨脂异黄酮和补骨脂二氢黄酮的定性测定。2 方法提要 样品在经过提取后,经高效液相色谱仪分离,二极管阵列检测器检测,经与平行操作的补骨脂素、异补骨脂素、新补骨脂异黄酮和补骨脂二氢黄酮对照品及补骨脂对照药材比较,以保留时间和紫外光谱图定性,鉴别补骨脂特征成分补骨脂素、异补骨脂素、新补骨脂异黄酮和补骨脂二氢黄酮的存在。本方法对补骨脂素、异补骨脂素、新补骨脂异黄酮和补骨脂二氢黄酮的检出限和取样品0.5 g时的检出浓度见表1。 表1 4种补骨脂特征成分的检出限和检出浓度化合物检出限(ng)检出浓度(μg/g)补骨脂素0.30.6异补骨脂素0.30.6新补骨脂异黄酮0.30.6补骨脂二氢黄酮0.30.63 试剂和材料 除另有规定外,所用试剂均为分析纯,水为实验室用一级水。3.1 乙腈,色谱纯。3.2 补骨脂素,纯度≥99%。3.3 异补骨脂素,纯度≥99%。3.4 新补骨脂异黄酮,纯度≥98%。3.5 补骨脂二氢黄酮,纯度≥99%。3.6 补骨脂,中国食品药品检定研究院,供鉴别用。3.7 补骨脂特征性成分混合标准溶液(=0.1 μg/mL):分别称取补骨脂素(3.2)、异补骨脂素(3.3)、新补骨脂异黄酮(3.4)、补骨脂二氢黄酮(3.5)对照品各5 mg(精确到0.1 mg),置500 mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,配制成质量浓度各为10 μg/mL的标准溶液。精密量取各标准溶液0.1 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得0.1 μg/mL的混合标准溶液。3.8 补骨脂标准储备溶液:取补骨脂对照药材0.2 g,置50 mL三角瓶中,加30 mL 70%乙醇回流提取1h,滤过,滤液置100 mL量瓶中,加70%乙醇稀释至刻度,摇匀,即得。4 仪器4.1 高效液相色谱仪:具二极管阵列检测器。4.2 分析天平:感量为0.1 mg。4.3 移液器。4.4 涡旋振荡器。4.5 超声波清洗仪(功率不低于200W)。4.6 高速离心机:转速不小于10000 r/min。
目前,[b]我国是植物提取物的第一原料供应大国,也是植物提取物应用大国[/b],据中国海关数据显示,2019年,我国植物提取物行业出口额达23.72亿美元(美国是最大的进口市场),进口额达8.49亿美元(美国、印尼和印度是前三进口市场)。在全球“禁抗、限抗”大背景下,国内外对可饲用植物提取物的需求日益增长,对于其产品和相应检测标准的需求也日益强烈。因为[b]没有统一的相关标准[/b],这就严重影响了其生产效率以及资源浪费,对从事可饲用植物提取物的生产、加工以及进出口贸易的相关企业造成了极大的困扰。因此必须尽快制定颁布并实施可饲用植物提取物的相关标准并实现标准的国际化,确保在国际贸易中有据可依,提高我国可饲用天然植物提取物在国际上的竞争力。[b]2024年3月15日,国家标准《饲料添加剂淫羊藿提取物中黄酮醇苷的测定 高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法》 正式发布[/b]。该标准由TC76(全国饲料工业标准化技术委员会)归口 ,主管部门为国家标准化管理委员会。主要起草单位为中国农业科学院北京畜牧兽医研究所 、中国医学科学院药用植物研究所 、天津博菲德科技有限公司 、湖南农业大学 、北京爱绿生物科技有限公司 、中国农业科学院饲料研究所。[来源:仪器信息网] 未经授权不得转载[align=right][/align]
不加显色剂都是360最大峰,加过显色剂后芦丁标品在510出最大峰,自己提取的黄酮却是在410出峰,请问这是怎么回事?
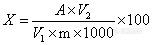
[align=center]胶囊中总黄酮的测定方法验证[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:肖颖[/align]一、目的:对《保健食品检验与评价技术规范》(2003版)中总黄酮测定方法进行方法适用性验证。二、验证内容:方法适用性验证包括检出限、线性范围、重复性、回收率、耐用性。三、验证方法:1 范围 本标准适用于胶囊中总黄酮的含量测定。2 原理 试样中黄酮经乙醇提取,聚酰胺粉吸附,以苯除去杂质,用甲醇洗脱黄酮后,在360nm有最大吸收,其吸收值与黄酮量在一定范围内成正比,与标准系列比较定量。3 试剂和材料3.1 试剂实验室用水为双蒸馏水,所用试剂为分析纯级。3.1.1 无水乙醇:分析纯。(来源:天津奥普升化工有限公司 批号:20161019)3.1.2 芦丁标准溶液:(来源:上海金穗生物科技有限公司 批号:20161027)称取5.0芦丁,加甲醇溶解并定容至100mL。3.1.3 甲醇(来源:天津市天力化学试剂有限公司 批号:20150408 )3.1.4 聚酰胺粉(来源:浙江省台州市路桥四甲生化塑料厂 批号:201600409 )3.1.5 苯(来源:天津市科密欧化学试剂有限公司 批号:20140510 )以上试剂符合检测要求4 仪器和设备4.1超声波清洗器:昆山市超声仪器有限公司 型号:KQ5200B4.2电子天平:沈阳龙腾电子有限公司 型号:JM-B10002 精度:0.0001g4.3分光光度计:北京普析通用仪器有限责任公司 型号:TU-1901或同等程度仪器 以上仪器符合检测要求5 波长选择专属性实验取芦丁标准溶液(3.1.2)1.0mL加乙醇(3.1.1)定容至25mL,摇匀后,超声20min,吸取上清液1.0mL于蒸发皿中,加1g聚酰胺粉(3.1.4)吸附,于水浴上挥去乙醇,然后转入层析柱。先用20mL苯(3.1.5)洗,苯液弃去,然后用甲醇(3.1.3)洗脱,定容至25mL,以甲醇(3.1.3)为参比,进行紫外可见光谱扫描,同时对样品空白进行扫描。6 试样处理样品提取:称取1.0g左右试样,加乙醇(3.1.1)溶解并定容至25mL,摇匀后,超声提取20min,吸取上清液1.0mL于蒸发皿中,加1g聚酰胺粉(3.1.4)吸附,于水浴上挥去乙醇,然后转入层析柱。先用20mL苯(3.1.5)洗,苯液弃去,然后用甲醇(3.1.3)洗脱黄酮,定容至25mL,为待测液。7 测定:标准曲线绘制:分别移取0、1.0、2.0、3.0、4.0、5.0mL芦丁标准溶液于10mL比色管中,加甲醇(3.1.3)至刻度,摇匀。用1cm石英比色皿在360nm处比色,测其吸光度。以吸光度为横坐标,总黄酮含量为纵坐标绘制校正曲线。同时取待测液在360nm测定吸光度,计算试样中总黄酮含量。8 公式试样总黄酮含量按下式进行计算。[img=,153,45]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091803387785_8072_2904018_3.png!w153x45.jpg[/img]式中:X—样品中总黄酮的含量,mg/100g; A—样品测定液中黄酮的含量,μg;m—样品质量,g;V[sub]1[/sub]-测定用样品液体积,mL;V[sub]2[/sub]-试样定容体积,mL。计算结果保留二位有效数字。四、验证数据1.波长选择经过全波长扫描,芦丁标准溶液在360nm处有最大吸收峰,且试剂空白和样品空白在此波长处无干扰,故选择360nm为最佳测定波长。[img=,690,546]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091803507036_5107_2904018_3.png!w690x546.jpg[/img]2.线性范围以总黄酮含量(C)为横坐标,吸光度值(A)为纵坐标,绘制标准曲线,进行线性回归,得回归方程:A=0.0029C-0.0069 R[sup]2[/sup]为0.999。[table][tr][td][align=center]总黄酮含量(μg)[/align][/td][td]0[/td][td]52[/td][td]104[/td][td]156[/td][td]208[/td][td]260[/td][/tr][tr][td][align=center]A[/align][/td][td]0[/td][td]0.133[/td][td]0.284[/td][td]0.445[/td][td]0.598[/td][td]0.730[/td][/tr][/table][align=center][img=,482,290]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091803598216_9725_2904018_3.png!w482x290.jpg[/img] [/align]以上结果表明总黄酮在0-260μg范围内,吸光值与总黄酮含量线性良好,符合要求。3. 检出限以甲醇(3.1.3)为参比,同时在360nm处对标准曲线0管进行20次测定,计算标准偏差,以3倍标准偏差值与斜率的比值为最低检出含量,利用公式计算出检出限。经测定,标准偏差为0.000366,最低检出含量为0.379μg,检出限为1.0mg/100g,满足胶囊中对检出浓度的要求。4.重复性称取6份试样按照上述处理方法进行试样处理,分别吸取适量样液进行比色,求得样液中总黄酮含量。[table][tr][td][align=center]测定编号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][td][align=center]6[/align][/td][/tr][tr][td][align=center]样品含量mg/100g[/align][/td][td]323.1[/td][td]318.9[/td][td]320.2[/td][td]326.1[/td][td]324.6[/td][td]322.7[/td][/tr][tr][td][align=center]平均值mg/100g[/align][/td][td=6,1][align=center]322.6[/align][/td][/tr][tr][td][align=center]相对标准偏差%[/align][/td][td=6,1][align=center]0.831[/align][/td][/tr][/table]由上表可知,试样中总黄酮测定的重复性均值为322.6,RSD值为0.831%,符合规定。5.回收率在进行重复性试验基础上,同时进行加标试验,加标量分别为1.2倍,1.0倍,0.8倍,结果见下表:[table][tr][td][align=center]测定编号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][td][align=center]6[/align][/td][/tr][tr][td][align=center]样品含量mg/100g[/align][/td][td]323.1[/td][td]318.9[/td][td]320.2[/td][td]326.1[/td][td]324.6[/td][td]322.7[/td][/tr][tr][td][align=center]加标量mg/100g[/align][/td][td][align=center]347.30[/align][/td][td][align=center]354.98[/align][/td][td][align=center]304.81[/align][/td][td][align=center]309.28[/align][/td][td][align=center]251.82[/align][/td][td][align=center]258.99[/align][/td][/tr][tr][td][align=center]加标样品含量mg/100g[/align][/td][td]651.22[/td][td]659.02[/td][td]630.58[/td][td]649.8[/td][td]549.98[/td][td]567.79[/td][/tr][tr][td][align=center]加标回收率%[/align][/td][td]94.48 [/td][td]95.81 [/td][td]101.83 [/td][td]104.66 [/td][td]89.50 [/td][td]94.63 [/td][/tr][/table]由上表可以看出胶囊中总黄酮测定的加标回收范围在80%-120%,符合规定。6.耐用性同时进行人员比对和仪器比对检测胶囊中总黄酮,结果见下表。[table][tr][td]编号[/td][td]人员1[/td][td]人员2[/td][td]仪器1[/td][td]仪器2[/td][/tr][tr][td]样品含量mg/100g[/td][td]322.8[/td][td]325.7[/td][td]322.1[/td][td]323.7[/td][/tr][tr][td]相对误差%[/td][td=2,1][align=center]0.89[/align][/td][td=2,1][align=center]0.50[/align][/td][/tr][/table]由上表可知,胶囊中总黄酮测定耐用性符合要求综上所述:从波长选择、检出限、线性范围、重复性、回收率、耐用性测试结果可知,均符合方法要求,本实验方法符合胶囊中总黄酮测定。
硝酸铝显色法测定总黄酮的原理为:在中性或弱碱性及亚硝酸钠存在条件下,黄酮类化合物与铝盐生成螯和物,加入氢氧化钠溶液后显红橙色,在510nm波长处有吸收峰且符合定量分析的比尔定律,一般以芦丁标准品定量。 先用亚硝酸钠还原黄酮, 然后加入硝酸铝络合,最后加氢氧化钠溶液使黄酮类化合物开环,生成 2''''羟基查耳酮而显色。显色原理发生在黄酮醇类成分邻位无取代的邻二酚羟基部位,不具有邻位无取代邻二酚羟基的黄酮醇类成分加入上述试剂时不显色。用亚硝酸钠还原黄酮,还原那个基团?硝酸铝络合,与那个基团?
[color=#444444]高效液相测六种黄酮类物质,六个标准品都出峰了,但是跑样品时一个峰都没有,请问大家,这是什么原因呢?[/color]
我在用液相色谱测蜂胶黄酮时,标准物质的色谱图曲线与蜂胶样品的色谱图曲线在出峰时间上用很大的差距,这样在分析数据时所定义的峰对应不起来。哪位仁兄做过这个试验,告诉小弟如何处理这样的情况。

保健食品中总黄酮的测定Determination of total flavonoid in health food1试剂1.1 聚酰胺粉1.2 芦丁标准溶液:称取5.0mg芦丁,加甲醇溶解并定容至100mL,即得50mg/mL。1.3 乙醇:分析纯。1.4 甲醇:分析纯。2 分析步骤2.1 试样处理:称取一定量的试样,加乙醇定容至25mL,摇匀后,超声提取20min,放置,吸取上清液1.0mL,于蒸发皿中,加1g聚酰胺粉吸附,于水浴上挥去乙醇,然后转入层析柱。先用20mL苯洗,苯液弃去,然后用甲醇洗脱黄酮,定容至25mL。此液于波长360nm测定吸收值。同时以芦丁为标准品,测定标准曲线,求回归方程,计算试样中总黄酮含量。2.2 芦丁标准曲线:吸取芦丁标准溶液:0、1.0、2.0、3.0、4.0、5.0mL于10mL比色管中,加甲醇至刻度,摇匀,于波长360nm比色。求回归方程,计算试样中总黄酮含量。3 计算和结果表示: A ×V2X = _____________________________*100 V1× M× 1000式中:X ___ 试样中总黄酮的含量, mg/100g ;A ___ 由标准曲线算得被测液中黄酮量,ug ;M ___ 试样质量 , g;V1____ 测定用试样体积, mL;V2 ___ 试样定容总体积, mL 。计算结果保留二位有效数字。 新手求帮助,根据上面的公式计算做出来的结果,数据看图片,因为是新手希望大师们给出详细的过程!!!谢谢了!!算得不对啊!!http://ng1.17img.cn/bbsfiles/images/2016/02/201602251646_585141_2724902_3.jpg
有一天然产物样品(黄酮类),怎么用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]定性?(没有标准品)谢谢!
[size=5][font=宋体]准确称取于120℃干燥至恒重的无水芦丁(作黄酮标准对照)9.5 mg,用60%的乙醇定容于50mL容量瓶中,摇匀,得到浓度为[color=#fe2419]0.19 mg/mL[/color]的标准品溶液,作为贮备液备用。准确量取此液0.0、1.0、2.0、3.0、4.0、5.0、6.0、7.0 mL于25 mL容量瓶中,分别加5%亚硝酸钠和10%硝酸铝溶液各[color=#fe2419]0.3mL[/color],放置6 min。[color=#fe2419]加1 mol/mL氢氧化钠溶液4.0mL,分别用30%的乙醇稀释至刻度,混匀,放置16min。[/color]用紫外分光光度计在510 nm处测定吸光度。如上述显色实验,为什么要配置浓度为[color=#fe2419]0.19 mg/mL[/color]的标准品溶液,而不是其他浓度(多少浓度范围内遵循朗伯比尔定律?)。别加5%亚硝酸钠和10%硝酸铝溶液各[color=#fe2419]0.3mL[/color],放置6 min。[color=#fe2419]加1 mol/mL氢氧化钠溶液4.0mL, [/color][color=#000000]显色原理是什么,各溶液用量有什么要求? 各溶液用量之间是否有内在关系? 显色时间有什么要求? 还有就是[/color][color=#fe2419]混匀,放置16min [/color][color=#000000]为什么要放置16min?如何放置?在容量瓶中放置?容量瓶塞需打开还是塞上?还有就是在做实验中 植物黄酮提取,显色后,进紫外分光光度计测量时,分光度总是跳动不稳定。老师说需离心,究竟离心的目的是什么?难道是沉淀Al(no3)3? 不过离心后 含试样的溶液 会有好多沉淀,而参比液几乎没有沉淀,沉淀是什么物质,是否含有大量黄酮类物质,从而影响实验准确度? 究竟 如何解决A值跳动的症状(紫外分光光度计没问题)?还有就是显色溶液是否要现用现配,是否用量,及其浓度都要精密控制? 还有就是吸光度测量的重复试验,每份重复三次,指的是需重新取样提取黄酮物质,再显色测吸光度,还是显色过后,取试液与三比色皿中,测量三次吸光度? 还有就是稳定性实验,为什么要做?[/color][color=#fe2419]我是一名学生,刚刚入手实验,有很多不明白的地方,请各位前辈不吝赐教,还有就是想各位前辈能给些此类光谱测定的参考资料及经验,十分感谢![/color][/font][/size]
【作者中文名】谭承佳; 张艺; 马家骅; 王毓杰;【作者单位】绵阳师范学院; 成都中医药大学药学院;【论文摘要】目的从醋柳黄酮中提取分离熊果酸并建立其含量测定方法。方法采用硅胶柱层析从醋柳黄酮氯仿浸提物中分离得到化合物,经1H-NMR、~(13)C-NMR鉴定为熊果酸;采用Diamonsil~(TM)(钻石)C~(18)(250×4.6mm,5μm),甲醇-8mmol·L~(-1)四丁基溴化铵溶液-三乙胺(90:10:0.2)为流动相,流速1mL·min~(-1),紫外检测波长210nm,柱温40℃。结果熊果酸的标准曲线线性范围为0.59~8.85μg(r=0.9996,n=5);平均加样回收率为97.11%,RSD=1.20%(n=6)。结论该法简便、准确,重复性好,适用于醋柳黄酮中熊果酸的定量分析。
三氯化铝法测定总黄酮的含量,基本上还是可靠的,但对有些样品本身颜色就比较黄比较 深的,我就先用活性碳脱色了,然后再稀释再去与三氯化铝显色,可是却出现了如下 情况 :加入三氯化铝的样品颜色反而浅,样品本身做对照的倒是颜色深,这样一来就没法 代入标准曲线去计算了,因为减去空白后就是负值,请问这是为什么?如何解决?
如题目:新标准参数方法指向其他标准,其他标准已有资质,这种情况做扩项还是变更?例如:蜂胶及其制品的新标准中,新方法中的总黄酮测定指向GB/T20574,我们单位已经有了[color=#000000]GB/T20574的资质,这种情况,需要做[font='Microsoft YaHei',Arial,Helvetica][back=#ffffff]蜂胶及其制品的总黄酮参数的扩项还是变更?[/back][/font][/color]
准确称取干燥后至恒重的异黄酮标准品0.0096g溶于95%的乙醇溶液中,定容100 mL,摇匀。再分别取0、2、4、6、8、10、12 mL用95%乙醇定容于100 mL容量瓶中,然后于260nm处分别测定其吸光度值,并绘制标准曲线。1.3提取后样品含量的测定准确量取一定量样品于容量瓶中,加入95%乙醇定容,摇匀。用紫外可见分光光度计测其吸光度。根据标准曲线和稀释倍数计算出样品中总异黄酮的质量我想请问一下!测吸光度的是用光度测定还是定量测定?校零用的是95%的乙醇么?如果我借用别人测的标准曲线,又该如何测,可以直接跳过标准品的测定直接测待测样品的么?

中药复方口服溶液中总黄酮含量的测定 将传统中药复方加工制成口服溶液,不但可以保留传统中药的临床药效,还极大的方便了患者的携带及服用,并且可以通过改善口感提高患者的顺应性。口服液始于上世纪60年代,当时有人将竹沥灌装于安瓶中制成口服安瓶剂,这是口服液的初步尝试,中国药典77年版首次收载了口服液安瓶剂(即口服液),到了八九十年代,随着中药制药工业的发展,口服液已被广为推崇。 本研究将传统中药汤剂经工艺设计制成口服液作为保健食品,现进行质量研究中,经文献调研该方中其主要功效作用的成分为总黄酮,现将制得的成品进行总黄酮含量测定。 黄酮类化合物广泛存在于药用植物、水果和蔬菜等中,是植物在长期自然选择过程中产生的一些次级代谢产物,它们是一类以2-苯基色原酮为母核的多酚化合物,现代医学研究表明,黄酮类化合物具有降低心肌耗氧量,使冠脉、脑血管流量增加,抗心律,软化血管,降血糖、血脂等作用,同时它还是一种天然的抗氧化剂,具有清除人体中超氧离子自由基,抗衰老,增加机体免疫力的生理活性作用,对总黄酮测定方法的研究报道较多,但基本都是对单一植物中总黄酮的测定,而我国大多中药制剂均为复方制剂,基于中草药复方制剂中总黄酮含量测定的研究还较少,本实验以复方中药为研究对象,来测定总黄酮的含量。试验仪器及试剂:电子天平紫外可见分光光度计100conc(瓦里安)数控超声波清洗器KQ-500DE(昆山市超声仪器有限公司)SHH.W21.420型三用电热恒温水箱芦丁对照品内径1.5cm试管试剂均为分析纯试验样品的制备:首先将口服液取出与小烧杯中,移取3ml于25ml容量瓶中,乙醇定容,摇匀后,超声提取20Min,放置,移取1ml于蒸发皿中,加入1g的聚酰胺(80-100目),搅拌使均匀吸附,(如图):http://ng1.17img.cn/bbsfiles/images/2013/12/201312221536_483960_2217446_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/12/201312221536_483959_2217446_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/12/201312221536_483961_2217446_3.jpg置于水浴上(50℃)挥去乙醇(如图):http://ng1.17img.cn/bbsfiles/images/2013/12/201312221536_483963_2217446_3.jpg将挥好的聚酰胺转移入层析柱中,先用20ml苯液洗脱,弃去苯液,(如图:)然后用甲醇进行洗脱,并将洗脱液接入25ml的容量瓶中,甲醇定容。摇匀后,以0.45微米滤膜过滤与刻度管中。(如图:)http://ng1.17img.cn/bbsfiles/images/2013/12/201312221536_483964_2217446_3.jpg标准曲线的制作:称取5mg芦丁,加甲醇溶解并定容至100mL容量瓶中,即得50微克每毫升的标准溶液。http://ng1.17img.cn/bbsfiles/images/2013/12/201312221536_483958_2217446_3.jpg吸取芦丁标准溶液0、1.0、2.0、3.0、4.0[size=12
小弟今天做了一对H62的黄铜基准物质,分别是0.4342g与0.3806g于150ml的锥形瓶中,前处理是加入10ml的硝酸于电磁炉平板微沸加热。冷却(中途有用自来水人工冷却锥形瓶表面),冷却之后定溶于25ml的容量瓶里,结束样品的前处理。结束样品前处理之后,利用PE的DV-7000的ICP-OES进行仪器分析,选择元素为Pb与Sb,波长分别是Pb:220.353 Sb:206.837 Pb的第二波长为217.000。QC为2PPM的溶液,用标准曲线进行QC,QC过关。但是结果却是0.4342g的样品中Pb220这个波长的结果为232.07mg/kg,217为次波长的Pb结果为108.78mg/kg,Sb206.837为波长的结果为3.7966mg/kg。0.3806g的Pb220这个波长的结果为237.03mg/kg,217为次波长的Pb结果为103.63mg/kg,Sb206.837为波长的结果为5.4531mg/kg。而H62的黄铜Pb结果为280mg/kg,Sb的结果为12mg/kg。其220.353的Pb波长的回收率不足90%,Sb更不用说了。得到结果之后我稀释样品100倍,但结果还是不理想。所以请问各位我是哪一步分做的有疏忽,还是说样品本身就有基体干扰需要利用内标法去做呢?能否有大侠能够告知小弟呢?
【作者】 于敏; 弥宏; 焦连庆;【机构】 吉林省中医中药研究院; 吉林省中医中药研究院 长春130021; 长春130021;【摘要】 目的:建立蜂胶总黄酮中阿魏酸与总酚酸的含量测定方法。方法:阿魏酸采用高效液相色谱法测定,色谱柱:DiamonsilC18(250mm×4·6mm,5μm),流动相:甲醇-1%乙酸(35∶65),检测波长:313nm。总酚酸采用分光光度法测定,以原儿茶酸为对照品。结果:阿魏酸线性范围:0·054~0·420μg,相关系数0·9995。平均回收率为97·90%,RSD=0·80%(n=5)。原儿茶酸线性范围:5·75~28·75μg,相关系数0·9976。平均回收率为97·08%,RSD=0·78%(n=5)。结论:本文建立的方法简便、可靠,可作为蜂胶总黄酮的质量控制标准。 更多还原【关键词】 蜂胶总黄酮; 阿魏酸; 总酚酸;
谁有GB/T 20574-2006蜂胶中总黄酮含量的测定方法 分光光度比色法这个标准,求求大哥,给发一个吧!!!!!!!!!!!!!!
大家好,我现在从树莓叶中提取出了黄酮,需要用FRAP法测黄酮的总抗氧化能力,资料上的方法都是说取适量样品上清(必要时稀释),加入1.8 mlTPTZ(Fe3+一三吡啶三砑嗪)工作液, 混匀后37℃反应10 min,593 nm测定吸光度,以1.0 mmol/LFeSO4为标准,样品抗氧化活性以达到同样吸光度所需的FeSO4的毫摩尔数表示。但我不知道在具体操作时以1.0 mmol/LFeSO4为标准是什么意思,怎么算的,还有593 nm测定吸光度的时候调零的空白加什么试剂,大家有做这方面的热心朋友忘告知一下。[em0818]