电泳原理。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=27904]电泳原理[/url]

毛细管电泳原理及分析策略一、毛细管电泳的基本原理电泳是指电解质中带电粒子在电场力作用下,以不同的速度向电荷相反方向迁移的现象。高效毛细管电泳(HPCE),是指离子或带电粒子以毛细管为分离室,以高压直流电场为驱动力,依据样品中各组分之间迁移速度和分配行为上的差异而实现分离的液相分离分析技术。由于毛细管内径小,表面积和体积的比值大,易于散热,因此毛细管电泳可以减少焦耳热的产生,这是与传统电泳技术的根本区别。http://ng1.17img.cn/bbsfiles/images/2012/05/201205142034_366964_2019107_3.jpgHPCE实际上包含电泳、色谱及其相互交叉的内容,是分析科学中继高效液相色谱之后的又一重大进展,它使得分离分析科学从微升级水平进入到纳升级水平,并使得细胞的分析,乃至单分子的分析成为可能。尤其是对样品珍贵,取样极少的生物大分子,毛细管电泳具有绝对的优势。其突出特点是:(1)所需样品量少;(2)分析速度快,分离效率高,分辨率高,灵敏度高;(3)分离模式多,开发分析方法容易;(4)溶剂用量少,经济、环保;(5)应用范围极广。毛细管电泳技术可用于分离分析多种组分,如核酸/核苷酸、蛋白质/多肽/氨基酸、糖类/糖蛋白、酶、碱氨基酸、微量元素、小的生物活性分子等的快速分析,以及DNA序列分析和DNA合成中产物纯度测定等,还可用于碱性药物分子及其代谢产物、无机及有机离子/有机酸、手性化合物、单细胞分析、药物与细胞的相互作用和病毒的分析。毛细管电泳依分离模式不同,可分为:毛细管区带电泳(CZE)、毛细管胶束电动色谱(MECC/MCKC)、毛细管凝胶电泳(CGE)、毛细管等电聚焦(cIEF)、亲和毛细管电泳(ACE)、毛细管电色谱(CEC)。下面以最常用的毛细管区带电泳(CZE)为例,探讨毛细管电泳原理及分析策略。
无论是DNA电泳图片还是RNA电泳图片,或者是蛋白的凝胶电泳图片包括Western blot膜、或者是化学发光膜图片,在图像分析的角度来看,都是同样的一种条带光密度分析的问题。分析电泳条带有专门的一类图像分析软件。常见的是Bandscan, Quantity One, 由各个凝胶电泳成像系统厂商自己编制的软件就更多了。我喜欢用的是Labworks, 是UVP公司生产的凝胶电泳成像系统上配用的拍摄与分析软件,实际上就是传说中大名鼎鼎的gel-pro。这个软件可以看作是Image-pro plus应用在电泳条带分析上的专业版。所以用惯了IPP后对gel-pro就会感觉很熟悉。很快就能学会使用。现在UVP已经不使用labworks了,另弄了一个visionworks软件,用起来就是没gel-pro舒服。实际上所有的电泳条带分析软件在分析原理与功能上都没什么差别。只是软件界面与操作程序上各有不同。所以,了解了条带的分析原理后也就能自己学会各种软件的使用了。分析电泳条带也是从拍摄电泳照片开始的。用平时玩的数码相机拍摄的电泳条带一般不能用来进行定量的分析。而必须使用专门的拍摄设备。大家一般称它为“凝胶成像系统”。它集中了观察,拍摄与分析凝胶的所有功能。一个凝胶成像系统包括了三个部分,暗箱,相机与电脑上的控制分析程序。让我们从使用成像系统的操作方法中来了解如何正确地拍摄与分析凝胶吧。 0 http://img.dxycdn.com/upload/2009/05/02/72294527.jpg
高效毛细管电泳的基本原理 高效毛细管电泳(high performance capillary electrophoresis,HPCE)是近年来发展起来的分离、分析技术,它是凝胶电泳技术的发展,是高效液相色谱分析的补充。该技术可分析的成分小至有机离子、大至生物大分子如蛋白质、核酸等。可用于分析多种体液样本如血清或血浆、尿、脑脊液及唾液等,HPLC分析高效、快速、微量。 电泳迁移不同分子所带电荷性质、多少不同,形状、大小各异。一定电解质及PH的缓冲液或其它溶液内,受电场作用,样本中各组分按一定速度迁移,从而形成电泳。电泳迁移速度(v)可用下式表示: 其中E为电场强度(E=V/L,V为电压,L为毛细管总长度)。u为电泳淌度。 电渗迁移电渗迁移指在电场作用下溶液相对于带电管壁移动的现象。特殊结构的熔合硅毛细管管壁通常在水溶液中带负电荷,在电压作用下溶液整体向负极移动,形成电渗流。带电微粒在毛细管内实际移动的速度为电泳流和电渗流的矢量和。分析化学博客-jl2~d d&6}8eE4B3q5T I5U0 分离分析类型B[D hv,m cF2Z0 根据其分离样本的原理设计不同主要分为以下几种类型:b[ _0]&uL+\$C0①毛细管区带电泳(capillaryzoneelectrophoresis,CZE);②毛细管等速电泳(capillary chromatography,CITP);③毛细管胶速电动色谱(miceller electrokinetic capillary chromatography,MECC);④毛细管凝胶电泳(capillary gelelectrophoresis,CGE);⑤毛细管等电聚焦(capillary isoelectric focusing ,CIEF)。毛细管区带电泳(CZE)为HPCE的基本操作模式,一般采用磷酸盐或硼酸盐缓冲液,实验条件包括缓冲液浓度、pH值、电压、温度、改性剂(乙腈、甲醇等),用于对带电物质(药物、蛋白质、肽类等)分离分析,对于中性物质无法实现分离。毛细管胶束电动色谱(MECC)为一种基于胶束增溶和电动迁移的新型液体色谱,在缓冲液中加入离子型表面活性剂作为胶束剂,利用溶质分子在水相和胶束相分配的差异进行分离,拓宽了CZE的应用范围,适合于中性物质的分离,亦可区别手性化合物,可用于氨基酸、肽类、小分子物质、手性物质、药物样品及体液样品的分析。毛细管等速电泳(CITP)采用先导电解质和后继电解质,构成不连续缓冲体系,基于溶质的电泳淌度差异进行分离,常用于离子型物质(如有机酸),并因适用较大内径的毛细管而可用于微制备,但本法空间分辨率较差。毛细管等电聚焦电泳(CIEF)用于具兼性离子的样品(蛋白质、肽类),等电点仅差0.001可分离的物质。毛细管凝胶电泳(CGE)依据大分子物质的分子量大小进行分离,主要用于蛋白质、核苷酸片段的分离。此外,还有毛细管电色谱(CEC)及非水毛细管电泳(CNACE),用于水溶性差的物质和水中难进行反应的分析研究。CZE和MECC用得较多,本文以两种方法为例来说明HPLC的原理。
该活动将分为5个系列,系列之间的关系或为递进关系或为并列关系,每周一个系列,形式不定。如为竞猜形式则以多对多得不对不得为原则,竞猜期一个星期,一星期后将公布答案竞猜结束。CE基础知识系列(2):各种电泳模式的分离原理以下给出不同电泳模式的分离原理,请大家回答对应的分离模式及其英文缩写(1)按电质比不同进行分离,在电渗流的作用下,所有组分均向负极移动,正离子移动速度最快,中性粒子次之,负离子最慢。(2)往缓冲溶液中添加一定浓度的表面活性剂以形成胶束,溶质基于在水相和胶束相之间的分配系数不同而得到分离,可以使离子型化合物和中性物质同时得到分离。该方法1984年由Jerabe首先提出。(3)利用某些两性电介质的支持物质在电场中形成pH梯度,使具有两性电介质的蛋白质顺着这一梯度迁移到相当于它们等电点的那个位置,并在该点停下,由此产生一种非常宽的聚焦区带,并使不同等电点的蛋白质聚集在不同的位置上。(4)凝胶电泳是用凝胶物质作为支撑物进行分离的区带电泳。凝胶是一种固态分散体系,它具有多孔性,具有类似于分子筛的作用。被分离物在通过装入毛细管的凝胶时,按照各自分子的体积大小逐一分离,分子体积大的首先被分离出来,其后是较小的分子。根据介质的物理形态,分为毛细管凝胶电泳和毛细管午觉筛分电泳两类。两者均以样品分子大小为分离基础。(5)在毛细管内壁涂布或在凝胶中加入亲和配基,在电泳过程中具有生物专一性亲和力的两种分子受体(receptor)和其配体(ligand)间发生了特异性相互作用,形成了受体-配体复合物,由此达到分离。(6)以电渗流为驱动力,根据样品中各组分在固定相和流动相间分配系数的差异和电场中迁移速率的不同而实现分离。是micro-HPLC和CE的结合。(7)采用先导电解质和后继电解质,使溶质按其电泳淌度不同得以分离,可以对溶剂中带电的物质进行定性定量分析和纯物质的微制备。上期主题:CE基础知识系列(1):CE电泳模式http://bbs.instrument.com.cn/shtml/20120316/3926304/下期预告:CE基础知识系列(3):各种电泳模式的应用本期答案:1.区带电泳CZE, 2. 胶束电动色谱 MEKC, 3. 等电聚焦电泳CIEF, 4. 凝胶电泳CGE, 5. 亲和毛细管电泳ACE, 6. 毛细管电色谱CEC, 7. 等速电泳CITP
阴极电泳,如题.
电泳槽是凝胶电泳系统的核心部分,其系统的迅猛发展主要也是体现在电泳槽上。根据电泳的原理,凝胶都是放在两个缓冲腔之间,电场通过凝胶连接两个缓冲腔。缓冲液和凝胶之问的接触可以是直接的液体接触,也可以间接通过凝胶条或滤纸条。管状凝胶电泳和垂直板状电泳大多采取直接液体接触方式。这种方式可以有效地使用电场,但在装置设计上有一些困难,如液体泄漏,电安全和操作麻烦等问题。水平板状电泳槽大多通过间接方式,用滤纸桥搭接以及最近使用缓冲液制作的凝胶条和滤纸条搭接,即半干技术,后种方式使装置简化,操作也大大方便。
各位大神: 最近有个朋友跟我提到了一个测序电泳槽,想问问各位大神什么事测序电泳槽啊?它的工作原理是怎么样的,电泳基本知识我知道,但测序电泳它是如何实现测序和微卫星分析等等功能的?
分离的原因:电泳迁移,电渗迁移电泳迁移:在高压电场下,带电离子向相反的方向移动。电渗迁移:当毛细管内充满缓冲溶液时,毛细管壁上的硅羟基发生解离,生成氢离子溶解在溶液中,这样就使毛细管壁带上负电荷与溶液形成双电层,在毛细管的两端加上直流电场后,带正电的溶液就会整体的向负极端移动,这就形成了电渗流。在操作缓冲溶液中,带电粒子的运动速度等于电泳速度和电渗速度的矢量和,电渗速度一般大于电泳速度,因此即使是阴离子也会从阳极端流向阴极端。加大缓冲溶液的酸度、在缓冲溶液中加入有机试剂都会减少硅羟基的解离,减小电渗流。分离模式 毛细管电泳的分离模式有以下几种。 (1)毛细管区带电泳(CZE) 将待分析溶液引入毛细管进样一端,施加直流电压后,各组分按各自的电泳流和电渗流的矢量和流向毛细管出口端,按阳离子、中性粒子和阴离子及其电荷大小的顺 序通过检测器。中性组分彼此不能分离。出峰时间称为迁移时间(tm),相当于高效液相色谱和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中的保留时间。 (2)毛细管凝胶电泳(CGE) 在毛细管中装入单体和引发剂引发聚合反应生成凝胶,这种方法主要用于分析蛋白质、DNA等生物大分子。另外还可以利用聚合物溶液,如葡聚糖等的筛分作用进 行分析,称为毛细管无胶筛分。有时将它们统称为毛细管筛分电泳,下分为凝胶电泳和无胶筛分两类。 (3)毛细管等速电泳(CITP) 采用前导电解质和尾随电解质,在毛细管中充入前导电解质后,进样,电极槽中换用尾随电解质进行电泳分析,带不同电荷的组分迁移至各个狭窄的区带,然后依次通过检测器。 (4)毛细管等电聚焦电泳(CIEF) 将毛细管内壁涂覆聚合物减小电渗流,再将样品和两性电解质混合进样,两个电极槽中分别加入酸液和碱液,施加电压后毛细管中的操作电解质溶液逐渐形成pH梯 度,各溶质在毛细管中迁移至各自等电点(pI)时变为中性形成聚焦的区带,而后用压力或改变检测器末端电极槽储液的pH值的办法使溶质通过检测器。 (5)胶束电动毛细管色谱(MEKC或MECC) 当操作缓冲液中加入大于其临界胶束浓度的离子型表面活性剂时表面活性剂就聚集形成胶束,其亲水端朝外憎水非极性核朝内,溶质则在水和胶束两相间分配,各溶 质因分配系数存在差别而被分离。对于常用的阴离子表面活性剂十二烷基硫酸钠,进样后极强亲水性组分不能进入胶束,随操作缓冲液流过检测器(容量因子k′= 0);极强憎水性组分则进入胶束的核中不再回到水相,最后到达检测器(k′=∞)。其他常用的胶束试剂还有阳离子表面活性剂十六烷基三甲基溴化铵,胆酸 等。 (6)毛细管电色谱(CEC) 将细粒径固定相填充到毛细管中或在毛细管内壁涂覆固定相以电渗流驱动操作缓冲液(有时再加辅助压力)进行分离。
气相色谱和液相色谱、离子色谱、毛细管电泳在分离原理和分离效果上有什么区别与联系?
我想知道脉冲场电泳仪国内和国外的牌子哪个比较好,并想了解一下脉冲场电泳的原理,哪位高人指点一下?不胜感激![em61]
根据电泳仪原理、电泳仪功能、电泳仪的使用方法、电泳仪的用途不同可以为:琼脂糖凝胶电泳、毛细管电泳、凝胶电泳、聚丙烯酰胺凝胶电泳、醋酸纤维薄膜电泳、高效毛细管电泳、琼脂糖电泳、SDS-PAGE凝胶电泳、蛋白质电泳、血清蛋白电泳、dna电泳、血红蛋白电泳、蛋白质双向电泳、免疫电泳、等电聚焦电泳、单细胞凝胶电泳、蛋白质凝胶电泳、质粒电泳、对流免疫电泳、变性电泳等。电泳仪分类:1、毛细管电泳仪:其主要部件有0~30kV可调稳压稳流电源,内径小于100μm(常用50~75μm)、长度一般为30~100cm的弹性石英毛细管、电极槽、检测器和进样装置。检测器有紫外/可见分光检测器、激光诱导荧光检测器和电化学检测器,前者最为常用。进样方法有电动法(电迁移)、压力法(正压力、负压力)和虹吸法。成套仪器还配有自动冲洗、自动进样、温度控制、数据采集和处理等部件。 2、常规电泳仪:其组成部件为可调稳压稳流电源,垂直电泳槽,水平电泳槽,电极连接线,支持体【非凝胶性支持体区带电泳(支持体有:①淀粉②纤维素粉③玻璃粉,硅胶等) ;凝胶支持体区带电泳支持体有:①淀粉液②聚丙烯酰胺凝胶③琼脂(糖)凝胶】;陶瓷板,抽水泵,输水管,冰水曹等部件组成。3、其他电泳仪:Tiselius或微量电泳、显微电泳、等电点聚焦电泳技术、等速电泳技术、密度梯度电泳等。是一种非支持体的电泳仪也称为自由电泳法的发展并不迅速,因为其电泳仪构造复杂、体积庞大,操作要求严格,价格昂贵等很少使用。毛细管电泳仪、凝胶电泳仪、垂直电泳仪、微电泳仪、高压电泳仪、水平电泳仪、高效毛细管电泳仪、双向电泳仪、bio rad 电泳仪、脉冲场电泳仪、伯乐电泳仪、北京六一电泳仪上海巴玖均可提供!
我正在做 DNA损伤要用彗星实验进行验证 但是我不知道用哪种电泳好些 ??有哪位高人愿意帮帮忙 ??? 顺便能不能附上一份关于那种电泳的相关原理和使用手册??
电泳是指带电颗粒在电场的作用下发生迁移的过程。许多重要的生物分子,如氨基酸、多肽、蛋白质、核苷酸、核酸等都具有可电离基团,它们在某个特定的pH值下可以带正电或负电,在电场的作用下,这些带电分子会向着与其所带电荷极性相反的电极方向移动。电泳技术就是利用在电场的作用下,由于待分离样品中各种分子带电性质以及分子本身大小、形状等性质的差异,使带电分子产生不同的迁移速度,从而对样品进行分离、鉴定或提纯的技术。
ν电泳时,阴离子在负极最后流出,在这种情况下,不但可以按类分离,除中性粒子外,同种类离子由于受到的电场力大小不一样也同时被相互分离。
使用方法:电泳技术是分子生物学研究不可缺少的重要分析手段。电泳一般分为自由界面电泳和区带电泳两大类,自由界面电泳不需支持物,如等电聚焦电泳、等速电泳、密度梯度电泳及显微电泳等,这类电泳目前已很少使用。而区带电泳则需用各种类型的物质作为支持物,常用的支持物有滤纸、醋酸纤维薄膜、非凝胶性支持物、凝胶性支持物及硅胶-G薄层等,分子生物学领域中最常用的是琼脂糖凝胶电泳。所谓电泳,是指带电粒子在电场中的运动,不同物质由于所带电荷及分子量的不同,因此在电场中运动速度不同,根据这一特征,应用电泳法便可以对不同物质进行定性或定量分析,或将一定混合物进行组份分析或单个组份提取制备,这在临床检验或实验研究中具有极其重要的意义。电泳仪正是基于上述原理设计制造的。使用方法1. 首先用导线将电泳槽的两个电极与电泳仪的直流输出端联接,注意极性不要接反。2. 电泳仪电源开关调至关的位置,电压旋钮转到最小,根据工作需要选择稳压稳流方式及电压电流范围。3. 接通电源,缓缓旋转电压调节钮直到达到的所需电压为止,设定电泳终止时间,此时电泳即开始进行。4. 工作完毕后,应将各旋钮、开关旋至零位或关闭状态,并拨出电泳插头。
我的资料中心可免积分下载 电泳涂装技术研究起于一百多年前,基于人们对金属表面防腐防锈要求的不断提高而相关表面处理工艺技术又不能较好地解决这种需求的压力下,而被逐渐研制开发。直到60年代才由George Brewer博士及福特汽车公司研制开发成功阳极电泳漆。其最早应用于福特汽车公司的涂装线,随着阳极电泳漆生产使用,日渐暴露其漆膜中包含有金属离子造成抗蚀性差的缺陷,因而,高抗蚀性的阴极电泳漆于七十年代被开发成功,并被人们等认可并大力推广应用。之后,电泳技术发展日新月异,产品品种由环氧型树脂型发展到丙烯酸型及聚氨脂型。产品的保护品种也由汽车行业引申到自行车、摩托车及家电、轻工饰品行业,如:空调、彩电、洗衣机、摩托车、眼镜、锁具、灯具及饰品、发夹、领带夹及各个金属行业以及铝材表面防锈行业。二、电泳涂漆之优势三、电泳漆之工作原理 四、不同类型之电泳漆之工艺路线及原因上挂→预清洗→脱脂→热水洗→冷水洗→酸洗→水洗→表调→磷化→水洗→水洗→纯水洗→纯水洗→电泳→回收→回收→纯水洗→纯水洗→进烘箱→下挂 五、电泳漆设备要求及性能指标六、电泳漆之维护及故障处理
早期的电泳技术是由瑞典Uppsala大学物理化学系Svedberg教授提出了荷电的胶体颗粒在电场中移动的现象称其为电泳。于1937年,收ArneTiselius教授——诺贝尔奖金获得者,利用些电泳现象,发明了最早期的界面电泳,用于蛋白质分离的研究,开创了电沪泳技术的新纪元。此后,各种电泳技术及仪器相继问世,先进的电泳仪和电泳技术的不断发展,使它在生物化学实验技术中占重要地位,按电泳的原理有三种形式的电泳分离系统:原则上按电泳的原理来分,即移动界面电泳、区带电泳和稳态电泳或称置换(排代)电泳。在自由移动界面电泳,是带电分子的移动速率通过观察界面的移动来测定,该方法已成为历史。代之以采用支持介质的区带电泳。 区带电泳因所用支持体的种类、粒度大小和电泳方式等不同,其临床应用的价值也各有差异。固体支持介质可分为两类:一类是滤纸、醋酸纤维素薄膜、硅胶、矾土、纤维素等;另一类是淀粉、琼脂糖和聚丙烯酰胺凝胶。由于它们具微细的多孔网状结构,故除能产生电泳作用外,还有分子筛效应,小分子会比大分子跑得快而使分辨率提高。它的最大优点是几乎不吸附蛋白质,因此电泳无拖尾的现象。低浓度的琼脂糖电泳相当于自由界面电泳,蛋白质在电场中可自由穿透,阴力小,分离清晰,透明度高,能透过200~7000nm波长的着色区带的检测敏感性,为此第一类支持介质现已被第二类支持介质所替代。 稳太电泳或称置换电泳的特点是分子颗粒的电泳迁移在一定时间后达到稳态,如等电聚焦和等速电泳。 区带电泳是临床检验领域中应用最广泛的技术,有重要临床意义,尤其是其他新技术,更扩大了其应用范围,提高了检测技术,现对该技术的现状与发展作一评述。
如题?有参加的必要吗?内容包括:毛细管电泳技术原理及应用进展,毛细管电泳质谱联用技术原理及应用进展,如何增加毛细管电泳方法的重现性,如何开发毛细管电泳新方法,两天费用很贵要6000元,不是广告,误删帖子啊!只是想问问各位老师有参加过的吗?给点建议啊http://simg.instrument.com.cn/bbs/images/default/em09501.gif
本人是新生,特来请教。我们在使用毛细管电泳的时候,通常会提供正电源和负电源,我们应该怎么选啊? 还有我看书知道 毛细管电泳分离的原理是 在柱子两端,一段是正电压,一段是负电压,这样才能工作。那提供正负电源又和这个是什么关系?还望各位 大虾 指教指教。
SuperBuffer(100X)简介主要用途DNA的快速电泳,取代传统的TAE和TBE。产品介绍SuperBuffer是一种革命性的超快高分辨核酸电泳液,由于其产热低,故可以以高达20-25V/cm的电压电泳,并且分辨率比传统电泳液更高。该产品能彻底替代TAE、TBE等传统DNA电泳液。主要特点1:快速工作电压可高达20-25v/cm,比TAE和TBE的5-8V/cm(见分子克隆手册)高2-4倍,电泳时间只有使用TAE或TBE时的1/4。分辨率要求不高的定性检测(如PCR检测和酶切检测)可以在十分钟内完成。2:高分辨快速电泳防止了DNA的扩散,用0.5%的胶得到的电泳分辨率与用2-3%的胶(TAE或TBE电泳)得到的相当(效果图见www.tiandz.com网站相关内容)。3.不影响后续的杂交,回收和连接等反应。4.节约成本,0.5-1%的胶适合于分离大小在100bp-50kb之间的DNA,不需要高浓度胶。本产品能反复使用数次。5.销售价格与市售国产TBE更便宜,产品有粉剂、预配液两种规格供客户选择。物理特性无色液体,4度或常温保存二:SuperBuffer(100X)的使用SuperBuffer(100X)必须在使用前用水稀释100倍,其后的使用方法跟TAE或TBE的使用完全一样。如果使用高电压则有以下建议。1.琼脂糖胶浓度分离从100bp到50kb的DNA片段均可使用0.5-1%的胶并能得到较高的分辩率。使用SuperBuffer电泳时由于可以高压电泳,胶浓度似乎越低电泳效果越好,也许是因为电泳速度越快,小片段DNA的弥散现象越轻,速度对小片段DNA弥散的影响超过了胶浓度对它的影响,故不必靠高浓度的胶来提高分辨率。使用高浓度的胶反而会使电泳时间加长,得不偿失。2.EB染色如果使用20-25V/cm电压,最好不要把EB加入上样液中,否则EB很容易在高压下与DNA分离。建议在倒胶前将EB直接加入琼脂糖中, EB的最佳终浓度为0.4 -0.5μg /ml。原理上SuperBuffer与EB以外的其它核酸染料(如SYBR Green)兼容,但天泽基因暂时没有进行相关实验,有待用户自己实验验证。3.样品的离子强度SuperBuffer比TAE和TBE对样品离子强度更敏感。如果待测样品(如酶切产物,PCR产物)的离子强度与DNA分子量对照(如DNA ladder)的离子强度不同,则离子强度低的泳动稍快,估算得到的DNA分子大小可能稍有误差。如果需要准确估计,建议电泳使分子量标准和待测样品的盐浓度一样(在分子量标准中加酶切或PCR缓冲液)。4:电泳液用量与电压的关系 如果电泳槽的容量在100-200ml左右的(迷你型电泳,电极距离10cm左右),可以使用200-250V电压进行电泳。电压如果超过20V/cm,则电泳时间不宜超过三十分钟 (在此电泳条件下,电泳三十分钟足够将0.1-5kb的DNA分开)。如果电泳槽的容量为600ml或更大,22.5V/cm(按正负两极距离)电泳一小时以上一般没有任何问题。5:SuperBuffer的重复使用SuperBuffer缓冲液最多可重复使用4-5次左右(如果电泳槽的容量为600ml的话);重复使用前最好将其搅拌混匀并放置片刻,以恢复其缓冲能力。随着重复使用次数增加,相同电压下DNA电泳速度会稍微加快,但分辨率变化不大。6:电流电压降低现象若在电泳时发生电流或电压逐渐下降的现象,请检查电泳仪是否设置了电流上限或功率上限,如果有上限设置,需将其调高使之与电泳电压匹配。如果原因不明,请与仪器生产厂家联系。部分电泳仪器做最高使用电压为200V。7:与RNA变性胶, 碱变性胶,脉冲电泳和PAGE的兼容性天泽基因没有进行相关兼容性实验。
电泳技术发展简史 1809年俄国物理学家Рейсе首次发现电泳现象。他在湿粘土中插上带玻璃管的正负两个电极,加电压后发现正极玻璃管中原有的水层变混浊,即带负电荷的粘土颗粒向正极移动,这就是电泳现象。 1909年Michaelis首次将胶体离子在电场中的移动称为电泳。他用不同pH的溶液在U形管中测定了转化酶和过氧化氢酶的电泳移动和等电点。 1937年瑞典Uppsala大学的Tiselius对电泳仪器作了改进,创造了Tiselius电泳仪,建立了研究蛋白质的移动界面电泳方法,并首次证明了血清是由白蛋白及α、β、γ球蛋白组成的,由于Tiselius在电泳技术方面作出的开拓性贡献而获得了1948年的诺贝尔化学奖。 1948年Wieland和Fischer重新发展了以滤纸作为支持介质的电泳方法,对氨基酸的分离进行过研究。 从本世纪50年代起,特别是1950年Durrum用纸电泳进行了各种蛋白质的分离以后,开创了利用各种固体物质(如各种滤纸、醋酸纤维素薄膜、琼脂凝胶、淀粉凝胶等)作为支持介质的区带电泳方法。 1959年Raymond和Weintraub利用人工合成的凝胶作为支持介质,创建了聚丙烯酰胺凝胶电泳,极大地提高了电泳技术的分辨率,开创了近代电泳的新时代。30多年来,聚丙烯酰胺凝胶电泳仍是生物化学和分子生物学中对蛋白质、多肽、核酸等生物大分子使用最普遍,分辨率最高的分析鉴定技术,是检验生化物质的最高纯度:即“电泳纯”(一维电泳一条带或二维电泳一个点)的标准分析鉴定方法,至今仍被人们称为是对生物大分子进行分析鉴定的最后、最准确的手段,即“Last Check”。 由80年代发展起来的新的毛细管电泳技术,是化学和生化分析鉴定技术的重要新发展,己受到人们的充分重视。4.2 电泳的基本原理 电泳是指带电颗粒在电场的作用下发生迁移的过程。许多重要的生物分子,如氨基酸、多肽、蛋白质、核苷酸、核酸等都具有可电离基团,它们在某个特定的pH值下可以带正电或负电,在电场的作用下,这些带电分子会向着与其所带电荷极性相反的电极方向移动。电泳技术就是利用在电场的作用下,由于待分离样品中各种分子带电性质以及分子本身大小、形状等性质的差异,使带电分子产生不同的迁移速度,从而对样品进行分离、鉴定或提纯的技术。 电泳过程必须在一种支持介质中进行。Tiselius等在1937年进行的自由界面电泳没有固定支持介质,所以扩散和对流都比较强,影响分离效果。于是出现了固定支持介质的电泳,样品在固定的介质中进行电泳过程,减少了扩散和对流等干扰作用。最初的支持介质是滤纸和醋酸纤维素膜,目前这些介质在实验室已经应用得较少。在很长一段时间里,小分子物质如氨基酸、多肽、糖等通常用滤纸或纤维素、硅胶薄层平板为介质的电泳进行分离、分析,但目前则一般使用更灵敏的技术如HPLC等来进行分析。这些介质适合于分离小分子物质,操作简单、方便。但对于复杂的生物大分子则分离效果较差。凝胶作为支持介质的引入大大促进了电泳技术的发展,使电泳技术成为分析蛋白质、核酸等生物大分子的重要手段之一。最初使用的凝胶是淀粉凝胶,但目前使用得最多的是琼脂糖凝胶和聚丙烯酰胺凝胶。蛋白质电泳主要使用聚丙烯酰胺凝胶。 电泳装置主要包括两个部分:电源和电泳槽。电源提供直流电,在电泳槽中产生电场,驱动带电分子的迁移。电泳槽可以分为水平式和垂直式两类。垂直板式电泳是较为常见的一种,常用于聚丙烯酰胺凝胶电泳中蛋白质的分离。电泳槽中间是夹在一起的两块玻璃板,玻璃板两边由塑料条隔开,在玻璃平板中间制备电泳凝胶,凝胶的大小通常是12cm ? 14 cm,厚度为1mm~2 mm,近年来新研制的电泳槽,胶面更小、更薄,以节省试剂和缩短电泳时间。制胶时在凝胶溶液中放一个塑料梳子,在胶聚合后移去,形成上样品的凹槽。水平式电泳,凝胶铺在水平的玻璃或塑料板上,用一薄层湿滤纸连接凝胶和电泳缓冲液,或将凝胶直接浸入缓冲液中。由于pH值的改变会引起带电分子电荷的改变,进而影响其电泳迁移的速度,所以电泳过程应在适当的缓冲液中进行的,缓冲液可以保持待分离物的带电性质的稳定。
SuperBuffer(100X)简介主要用途DNA的快速电泳,取代传统的TAE和TBE。产品介绍SuperBuffer是一种革命性的超快高分辨核酸电泳液,由于其产热低,故可以以高达20-25V/cm的电压电泳,并且分辨率比传统电泳液更高。该产品能彻底替代TAE、TBE等传统DNA电泳液。主要特点1:快速工作电压可高达20-25v/cm,比TAE和TBE的5-8V/cm(见分子克隆手册)高2-4倍,电泳时间只有使用TAE或TBE时的1/4。分辨率要求不高的定性检测(如PCR检测和酶切检测)可以在十分钟内完成。2:高分辨快速电泳防止了DNA的扩散,用0.5%的胶得到的电泳分辨率与用2-3%的胶(TAE或TBE电泳)得到的相当(效果图见www.tiandz.com网站相关内容)。3.不影响后续的杂交,回收和连接等反应。4.节约成本,0.5-1%的胶适合于分离大小在100bp-50kb之间的DNA,不需要高浓度胶。本产品能反复使用数次。5.销售价格与市售国产TBE更便宜,产品有粉剂、预配液两种规格供客户选择。物理特性无色液体,4度或常温保存二:SuperBuffer(100X)的使用SuperBuffer(100X)必须在使用前用水稀释100倍,其后的使用方法跟TAE或TBE的使用完全一样。如果使用高电压则有以下建议。1.琼脂糖胶浓度分离从100bp到50kb的DNA片段均可使用0.5-1%的胶并能得到较高的分辩率。使用SuperBuffer电泳时由于可以高压电泳,胶浓度似乎越低电泳效果越好,也许是因为电泳速度越快,小片段DNA的弥散现象越轻,速度对小片段DNA弥散的影响超过了胶浓度对它的影响,故不必靠高浓度的胶来提高分辨率。使用高浓度的胶反而会使电泳时间加长,得不偿失。2.EB染色如果使用20-25V/cm电压,最好不要把EB加入上样液中,否则EB很容易在高压下与DNA分离。建议在倒胶前将EB直接加入琼脂糖中, EB的最佳终浓度为0.4 -0.5μg /ml。原理上SuperBuffer与EB以外的其它核酸染料(如SYBR Green)兼容,但天泽基因暂时没有进行相关实验,有待用户自己实验验证。3.样品的离子强度SuperBuffer比TAE和TBE对样品离子强度更敏感。如果待测样品(如酶切产物,PCR产物)的离子强度与DNA分子量对照(如DNA ladder)的离子强度不同,则离子强度低的泳动稍快,估算得到的DNA分子大小可能稍有误差。如果需要准确估计,建议电泳使分子量标准和待测样品的盐浓度一样(在分子量标准中加酶切或PCR缓冲液)。4:电泳液用量与电压的关系 如果电泳槽的容量在100-200ml左右的(迷你型电泳,电极距离10cm左右),可以使用200-250V电压进行电泳。电压如果超过20V/cm,则电泳时间不宜超过三十分钟 (在此电泳条件下,电泳三十分钟足够将0.1-5kb的DNA分开)。如果电泳槽的容量为600ml或更大,22.5V/cm(按正负两极距离)电泳一小时以上一般没有任何问题。5:SuperBuffer的重复使用SuperBuffer缓冲液最多可重复使用4-5次左右(如果电泳槽的容量为600ml的话);重复使用前最好将其搅拌混匀并放置片刻,以恢复其缓冲能力。随着重复使用次数增加,相同电压下DNA电泳速度会稍微加快,但分辨率变化不大。6:电流电压降低现象若在电泳时发生电流或电压逐渐下降的现象,请检查电泳仪是否设置了电流上限或功率上限,如果有上限设置,需将其调高使之与电泳电压匹配。如果原因不明,请与仪器生产厂家联系。部分电泳仪器做最高使用电压为200V。7:与RNA变性胶, 碱变性胶,脉冲电泳和PAGE的兼容性天泽基因没有进行相关兼容性实验。
SuperBuffer(100X)简介主要用途DNA的快速电泳,取代传统的TAE和TBE。产品介绍SuperBuffer是一种革命性的超快高分辨核酸电泳液,由于其产热低,故可以以高达20-25V/cm的电压电泳,并且分辨率比传统电泳液更高。该产品能彻底替代TAE、TBE等传统DNA电泳液。主要特点1:快速工作电压可高达20-25v/cm,比TAE和TBE的5-8V/cm(见分子克隆手册)高2-4倍,电泳时间只有使用TAE或TBE时的1/4。分辨率要求不高的定性检测(如PCR检测和酶切检测)可以在十分钟内完成。2:高分辨快速电泳防止了DNA的扩散,用0.5%的胶得到的电泳分辨率与用2-3%的胶(TAE或TBE电泳)得到的相当(效果图见www.tiandz.com网站相关内容)。3.不影响后续的杂交,回收和连接等反应。4.节约成本,0.5-1%的胶适合于分离大小在100bp-50kb之间的DNA,不需要高浓度胶。本产品能反复使用数次。5.销售价格与市售国产TBE更便宜,产品有粉剂、预配液两种规格供客户选择。物理特性无色液体,4度或常温保存二:SuperBuffer(100X)的使用SuperBuffer(100X)必须在使用前用水稀释100倍,其后的使用方法跟TAE或TBE的使用完全一样。如果使用高电压则有以下建议。1.琼脂糖胶浓度分离从100bp到50kb的DNA片段均可使用0.5-1%的胶并能得到较高的分辩率。使用SuperBuffer电泳时由于可以高压电泳,胶浓度似乎越低电泳效果越好,也许是因为电泳速度越快,小片段DNA的弥散现象越轻,速度对小片段DNA弥散的影响超过了胶浓度对它的影响,故不必靠高浓度的胶来提高分辨率。使用高浓度的胶反而会使电泳时间加长,得不偿失。2.EB染色如果使用20-25V/cm电压,最好不要把EB加入上样液中,否则EB很容易在高压下与DNA分离。建议在倒胶前将EB直接加入琼脂糖中, EB的最佳终浓度为0.4 -0.5μg /ml。原理上SuperBuffer与EB以外的其它核酸染料(如SYBR Green)兼容,但天泽基因暂时没有进行相关实验,有待用户自己实验验证。3.样品的离子强度SuperBuffer比TAE和TBE对样品离子强度更敏感。如果待测样品(如酶切产物,PCR产物)的离子强度与DNA分子量对照(如DNA ladder)的离子强度不同,则离子强度低的泳动稍快,估算得到的DNA分子大小可能稍有误差。如果需要准确估计,建议电泳使分子量标准和待测样品的盐浓度一样(在分子量标准中加酶切或PCR缓冲液)。4:电泳液用量与电压的关系 如果电泳槽的容量在100-200ml左右的(迷你型电泳,电极距离10cm左右),可以使用200-250V电压进行电泳。电压如果超过20V/cm,则电泳时间不宜超过三十分钟 (在此电泳条件下,电泳三十分钟足够将0.1-5kb的DNA分开)。如果电泳槽的容量为600ml或更大,22.5V/cm(按正负两极距离)电泳一小时以上一般没有任何问题。5:SuperBuffer的重复使用SuperBuffer缓冲液最多可重复使用4-5次左右(如果电泳槽的容量为600ml的话);重复使用前最好将其搅拌混匀并放置片刻,以恢复其缓冲能力。随着重复使用次数增加,相同电压下DNA电泳速度会稍微加快,但分辨率变化不大。6:电流电压降低现象若在电泳时发生电流或电压逐渐下降的现象,请检查电泳仪是否设置了电流上限或功率上限,如果有上限设置,需将其调高使之与电泳电压匹配。如果原因不明,请与仪器生产厂家联系。部分电泳仪器做最高使用电压为200V。7:与RNA变性胶, 碱变性胶,脉冲电泳和PAGE的兼容性天泽基因没有进行相关兼容性实验。
[B]电泳法作为色谱法中一类不常用的方法,不怎么被大家关注。今天做一个专题,大家来一起讨论一下:[/B][color=#DC143C]1.电泳法的原理是是什么?2.电泳法应用在那些方面呢?3.有关电泳法用到的仪器有哪些?品牌、价位如何呢?[/color]欢迎您的回帖,符合题意者加分鼓励![em09505]
按照电泳的原理,不同荷质比的金属离子按道理也能分开的。比如说, Ag+和Hg2+能电泳分开吗?各位给点看法吧。谢谢了。
请教毛细管电泳间接紫外法原理,例如测K离子
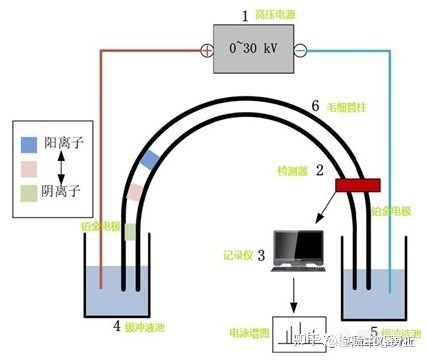
[b]一、毛细管电泳的原理简介:毛细管电泳[/b]又称“高效毛细管电泳 ”,指以高压电场为驱动力,以[b]毛细管[/b]为分离通道,依据试样中各组分[b]间淌度和分配行为[/b]上的差异而实现分离的一种分离技术。[align=center][img=,427,360]https://ng1.17img.cn/bbsfiles/images/2022/12/202212291436449476_2284_3237657_3.jpg!w427x360.jpg[/img][b]图1 毛细管电泳简易装置[/b][/align][align=left][b]二、毛细管电泳的专业术语:[/b][/align][b][/b][align=left][b]1)电泳:[/b]在电解质溶液中,[b]带电粒子[/b]在[b]电场[/b]作用下,以[b]不同的速度[/b]向其所带电荷[b]相反方向迁移[/b]的现象叫[b]电泳[/b]。[/align][align=left][b]2)电渗:[/b]在充满电解质溶液的毛细管柱中,柱内层氧化硅与溶质的界面上形成[b]双电层[/b]。当[b]高电压[/b]通过此含有缓冲溶液的[b]毛细管柱[/b]时,而此时双电层中的水合阳离子引起[b]流体整体[/b]朝负极方向[b]移动的现象叫电渗[/b]。[/align][align=left][b]3)电渗流(EOF):[/b]当高电压通过含有缓冲溶液的毛细管柱时,管内的[b]溶质[/b]向阴极或阳极[b]移动[/b],产生[b]电渗流[/b]。在柱内层氧化硅与溶质的界面上形成[b]双电层[/b]是[b]电渗流[/b]产生的原因。[/align][align=center][img=,526,231]https://ng1.17img.cn/bbsfiles/images/2022/12/202212291441064961_4781_3237657_3.jpg!w526x231.jpg[/img][b]图2 毛细管双电层与电渗流示意[/b][/align][align=left]粒子在电解质中的[b]迁移速度[/b]等于[b]电泳和电渗流(EOF)[/b]两种速度的[b]矢量和[/b]。[/align][align=left]阳离子的移动方向和电渗流一致,最先流出;中性粒子的电泳流速度为“0”,其迁移速度等于电渗流速度;阴离子的移动方向和电渗流相反,但因电渗流速度一般都大于电泳速度,它将在中性粒子之后流出,从而实现分离。[/align]
SuperBuffer(100X)简介主要用途DNA的快速电泳,取代传统的TAE和TBE。产品介绍SuperBuffer是一种革命性的超快高分辨核酸电泳液,由于其产热低,故可以以高达20-25V/cm的电压电泳,并且分辨率比传统电泳液更高。该产品能彻底替代TAE、TBE等传统DNA电泳液。主要特点1:快速工作电压可高达20-25v/cm,比TAE和TBE的5-8V/cm(见分子克隆手册)高2-4倍,电泳时间只有使用TAE或TBE时的1/4。分辨率要求不高的定性检测(如PCR检测和酶切检测)可以在十分钟内完成。2:高分辨快速电泳防止了DNA的扩散,用0.5%的胶得到的电泳分辨率与用2-3%的胶(TAE或TBE电泳)得到的相当(效果图见www.tiandz.com网站相关内容)。3.不影响后续的杂交,回收和连接等反应。4.节约成本,0.5-1%的胶适合于分离大小在100bp-50kb之间的DNA,不需要高浓度胶。本产品能反复使用数次。5.销售价格与市售国产TBE更便宜,产品有粉剂、预配液两种规格供客户选择。物理特性无色液体,4度或常温保存二:SuperBuffer(100X)的使用SuperBuffer(100X)必须在使用前用水稀释100倍,其后的使用方法跟TAE或TBE的使用完全一样。如果使用高电压则有以下建议。1.琼脂糖胶浓度分离从100bp到50kb的DNA片段均可使用0.5-1%的胶并能得到较高的分辩率。使用SuperBuffer电泳时由于可以高压电泳,胶浓度似乎越低电泳效果越好,也许是因为电泳速度越快,小片段DNA的弥散现象越轻,速度对小片段DNA弥散的影响超过了胶浓度对它的影响,故不必靠高浓度的胶来提高分辨率。使用高浓度的胶反而会使电泳时间加长,得不偿失。2.EB染色如果使用20-25V/cm电压,最好不要把EB加入上样液中,否则EB很容易在高压下与DNA分离。建议在倒胶前将EB直接加入琼脂糖中, EB的最佳终浓度为0.4 -0.5μg /ml。原理上SuperBuffer与EB以外的其它核酸染料(如SYBR Green)兼容,但天泽基因暂时没有进行相关实验,有待用户自己实验验证。3.样品的离子强度SuperBuffer比TAE和TBE对样品离子强度更敏感。如果待测样品(如酶切产物,PCR产物)的离子强度与DNA分子量对照(如DNA ladder)的离子强度不同,则离子强度低的泳动稍快,估算得到的DNA分子大小可能稍有误差。如果需要准确估计,建议电泳使分子量标准和待测样品的盐浓度一样(在分子量标准中加酶切或PCR缓冲液)。4:电泳液用量与电压的关系 如果电泳槽的容量在100-200ml左右的(迷你型电泳,电极距离10cm左右),可以使用200-250V电压进行电泳。电压如果超过20V/cm,则电泳时间不宜超过三十分钟 (在此电泳条件下,电泳三十分钟足够将0.1-5kb的DNA分开)。如果电泳槽的容量为600ml或更大,22.5V/cm(按正负两极距离)电泳一小时以上一般没有任何问题。5:SuperBuffer的重复使用SuperBuffer缓冲液最多可重复使用4-5次左右(如果电泳槽的容量为600ml的话);重复使用前最好将其搅拌混匀并放置片刻,以恢复其缓冲能力。随着重复使用次数增加,相同电压下DNA电泳速度会稍微加快,但分辨率变化不大。6:电流电压降低现象若在电泳时发生电流或电压逐渐下降的现象,请检查电泳仪是否设置了电流上限或功率上限,如果有上限设置,需将其调高使之与电泳电压匹配。如果原因不明,请与仪器生产厂家联系。部分电泳仪器做最高使用电压为200V。7:与RNA变性胶, 碱变性胶,脉冲电泳和PAGE的兼容性天泽基因没有进行相关兼容性实验。
电泳技术是分子生物学研究不可缺少的重要分析手段。电泳一般分为自由界面电泳和区带电泳两大类,自由界面电泳不需支持物,如等电聚焦电泳、等速电泳、密度梯度电泳及显微电泳等,这类电泳目前已很少使用。而区带电泳则需用各种类型的物质作为支持物,常用的支持物有滤纸、醋酸纤维薄膜、非凝胶性支持物、凝胶性支持物及硅胶-G薄层等,分子生物学领域中最常用的是琼脂糖凝胶电泳。所谓电泳,是指带电粒子在电场中的运动,不同物质由于所带电荷及分子量的不同,因此在电场中运动速度不同,根据这一特征,应用电泳法便可以对不同物质进行定性或定量分析,或将一定混合物进行组份分析或单个组份提取制备,这在临床检验或实验研究中具有极其重要的意义。电泳仪正是基于上述原理设计制造的。下面简单介绍其使用方法及注意事项。使用方法1.首先用导线将电泳槽的两个电极与电泳仪的直流输出端联接,注意极性不要接反。2.电泳仪电源开关调至关的位置,电压旋钮转到最小,根据工作需要选择稳压稳流方式及电压电流范围。3.接通电源,缓缓旋转电压调节钮直到达到的所需电压为止,设定电泳终止时间,此时电泳即开始进行。4.工作完毕后,应将各旋钮、开关旋至零位或关闭状态,并拨出电泳插头。