[font=inherit]一、项目基本情况[/font]项目编号:SXTHTC-2024-0302项目名称:多病原检测试剂采购项目采购方式:竞争性谈判预算金额:28.800000 万元(人民币)最高限价(如有):28.800000 万元(人民币)采购需求:多病原检测试剂合同履行期限:按双方签订合同办理本项目( 不接受 )联合体投标。[font=inherit]二、申请人的资格要求:[/font]1.满足《中华人民共和国政府采购法》第二十二条规定;2.落实政府采购政策需满足的资格要求:无3.本项目的特定资格要求:本次采购产品为医疗器械,申请人须具备医疗器械经营许可证/第二类医疗器械经营备案凭证,报价产品须具备医疗器械注册证,生产厂家须具备医疗器械生产许可证。[font=inherit]三、获取采购文件[/font]时间:2024年04月01日 至 2024年04月03日,每天上午9:00至12:00,下午14:30至17:30。(北京时间,法定节假日除外)地点:山西省长治市潞州区盛德世家B座715方式:现场报名售价:¥500.0 元(人民币)[font=inherit]四、响应文件提交[/font]截止时间:2024年04月08日 09点30分(北京时间)地点:山西省长治市潞州区捉马西大街10号和颐至尚酒店2层会议室[font=inherit]五、开启[/font]时间:2024年04月08日 09点30分(北京时间)地点:山西省长治市潞州区捉马西大街10号和颐至尚酒店2层会议室[font=inherit]六、公告期限[/font]自本公告发布之日起3个工作日。[font=inherit]七、其他补充事宜[/font]凡有意参加谈判的供应商,请携带加盖公章的以下资料报名:获取采购文件登记表 (格式见附件)、营业执照(三证合一)复印件、法人身份证复印件、经办人身份证复印件、授权书。[font=inherit]八、凡对本次采购提出询问,请按以下方式联系。[/font]1.采购人信息名 称:长治市疾病预防控制中心地址:山西省长治市潞州区漳泽东街79号联系方式:姜先生0355-35598512.采购代理机构信息名 称:山西同和天成项目管理有限公司地 址:山西省长治市潞州区盛德世家B座715联系方式:李女士185387066683.项目联系方式项目联系人:李女士电 话: 18538706668
[b][font=inherit]一、项目基本情况[/font][/b] 项目编号:[350401]YDCG[TP]2024001 项目名称:多病原检测、数字[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测、细菌鉴定血清等试剂 采购方式:竞争性谈判 预算金额:723,760.00元 采购包1(多病原检测、数字[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]检测、细菌鉴定血清等试剂): 采购包预算金额:723,760.00元 采购包最高限价: 723,760.00元 谈判保证金: 14,475.20元 采购需求:(包括但不限于标的的名称、数量、简要技术需求或服务要求等) [table=100%][tr][td]品目号[/td][td]品目编码及品目名称[/td][td]采购标的[/td][td]数量(单位)[/td][td]允许进口[/td][td]简要需求或要求[/td][td]品目预算(元)[/td][td]中小企业划分标准所属行业[/td][/tr][tr][td]1-1[/td][td]A07026899-其他非病人用诊断检验、实验用试剂[/td][td]实验用试剂[/td][td]1(批)[/td][td]否[/td][td]详见采购要求[/td][td]723,760.00[/td][td]工业[/td][/tr][/table] 本采购包不接受联合体投标 合同履行期限:自合同签订之日起10日内 [b][font=inherit]二、申请人的资格要求:[/font][/b] 1.满足《中华人民共和国政府采购法》第二十二条规定 2.落实政府采购政策需满足的资格要求: 采购包1:无 3.本项目的特定资格要求: 采购包1: (1)所投货物若属于医疗器械管理范畴,按照国家《医疗器械监督管理条例》,应符合以下标准 ①投标人为生产企业的,投标货物若属于第一类医疗器械产品,须提供《第一类医疗器械生产备案凭证》复印件(进口产品除外),投标货物若属于第二类、三类医疗器械产品,须提供《医疗器械生产许可证》复印件(进口产品除外);投标人为经营企业的,投标货物若属于第三类医疗器械产品,须提供《医疗器械经营许可证》复印件,投标货物若属于第二类医疗器械产品,须提供《第二类医疗器械经营备案凭证》复印件,投标货物若属于第一类医疗器械产品,则无须提供此项;②投标货物属于《医疗器械监督管理条例》规定的第一类医疗器械产品,须提供《第一类医疗器械产品备案凭证》复印件,属于第二类、第三类医疗器械产品,须提供《医疗器械注册证》复印件。所有证件必须真实有效。;(2)本项目不支持远程谈判。单位负责人参加投标时需随身携带(手持)本人身份证原件及营业执照复印件,授权代表参加投标时需随身携带(手持)本人身份证原件及单位负责人授权书(附单位负责人身份证复印件及被授权人身份证复印件)以便现场核查。开标时投标代表应随身携带CA认证卡用于现场电子签到及解密电子版投标文件。。 [b][font=inherit]三、采购项目需要落实的政府采购政策[/font][/b] 进口产品:不适用于本项目 节能产品:不适用于本项目 环境标志产品:不适用于本项目 [b][font=inherit]四、获取采购文件[/font][/b] 时间: 2024-09-03 至 2024-09-06 ,(提供期限自本公告发布之日起不得少于3个工作日),每天上午00:00:00至12:00:00,下午12:00:00至23:59:59(北京时间,法定节假日除外) 地点:采购文件随同本项目招标公告一并发布,供应商应通过福建省政府采购网上公开信息系统的注册账号(免费注册)并获取竞争性谈判文件(登陆福建省政府采购网上公开信息系统进行文件获取),否则报价响应将被拒绝。 方式:在线获取 售价:免费 [b][font=inherit]五、提交投标文件截止时间、开标时间和地点[/font][/b] 截止时间:2024-09-09 09:00:00(北京时间)(从谈判文件开始发出之日起至供应商提交首次响应文件截止之日止不得少于3个工作日) 地点:福建省三明市三元区东安路锦绣家园1号楼205室三明亿达(锦绣) [b][font=inherit]六、开启[/font][/b] 时间:2024-09-09 09:00:00(北京时间) 地点:福建省三明市三元区东安路锦绣家园1号楼205室三明亿达(锦绣) [b][font=inherit]七、公告期限[/font][/b] 自本公告发布之日起3个工作日。 [b][font=inherit]八、其他补充事宜[/font][/b] 无 [b][font=inherit]九、对本次招标提出询问,请按以下方式联系。[/font] 1.采购人信息[/b] 名称:三明市疾病预防控制中心 地址:福建省三明市沙县区生态新城金泉路26号 联系方式:0598-8241150 [b]2.采购代理机构信息(如有)[/b] 名称:福建省亿达工程咨询有限公司 地址:三明市三元区东安路锦绣家园1号楼205室 联系方式:0598-8221299 [b]3.项目联系方式[/b] 项目联系人:小刘 电话:0598-8221299 网址: zfcg.czt.fujian.gov.cn 开户名:福建省亿达工程咨询有限公司
[font=inherit]一、项目基本情况[/font]项目编号:Z1303002406682001项目名称:呼吸道多病原核酸检测试剂耗材采购项目预算金额:875500最高限价(如有):875500采购需求:采购呼吸道多病原核酸检测试剂耗材一批合同履行期限:按照甲方需要分批供货。合同签订后,甲方提出供货要求后7个工作日内完成供货本项目不接受联合体投标。[font=inherit]二、申请人的资格要求:[/font]1.满足《中华人民共和国政府采购法》第二十二条规定;2.落实政府采购政策需满足的资格要求:专门面向中小企业采购3.本项目的特定资格要求:无[font=inherit]三、获取招标文件[/font]时间:2024年08月05日至2024年08月09日,每天上午0:00至12:00,下午12:00至24:00(北京时间,法定节假日除外)地点:登录《秦皇岛市公共资源交易网》进行网上报名,并下载招标文件。方式:其它售价:0[font=inherit]四、提交投标文件截止时间、开标时间和地点[/font]2024年08月27日09点30分(北京时间)地点:秦皇岛市公共资源交易网不见面开标大厅(本项目采用不见面开标形式,供应商无需到现场)[font=inherit]五、公告期限[/font]自本公告发布之日起5个工作日。[font=inherit]六、其他补充事宜[/font]1、已在河北省公共资源交易平台注册登记的供应商可直接通过秦皇岛市公共资源交易平台报名获取文件,各市场主体登录系统后,可通过地图选择“秦皇岛市公共资源交易平台”,打开到【文件下载】菜单中下载招标文件,可参考“秦皇岛市公共资源交易网”首页办事指南交易响应方操作手册栏目中的《秦皇岛市公共资源交易平台投标人操作手册》。未经主体注册登记的供应商,请按照《关于在秦皇岛市公共资源交易平台市场主体信息登记注册认证的通知》的要求携带相关材料到秦皇岛市公共资源交易中心受理大厅完成注册,具体事宜可联系0335-3602218。技术服务电话:4009980000。2、本项目实行盲评,即投标(响应)文件的商务标、技术标分开制作,评审委员会按要求对商务标采取明标评审、对技术标采取暗标评审。3、特别提醒:本项目施行“双盲”评审、“分散”评标。4、本公告发布媒体:中国河北政府采购网、中国政府采购网、秦皇岛市公共资源交易网。[font=inherit]七、对本次招标提出询问,请按以下方式联系。[/font]1.采购人信息名 称:秦皇岛市疾病预防控制中心地 址:秦皇岛市海港区燕山大街90号联系方式:0335-36526232.采购代理机构信息(如有)名 称:秦皇岛鸿业工程管理咨询有限公司地 址:秦皇岛市海港区嵩山路7号工业大厦南附属楼3楼联系方式:0335-53096963.项目联系方式项目联系人:赵玲电 话:0335-5309696
由于传播途径多样、影响范围广泛,症状发展迅速,传染病仍然是世界范围内引起人类大量死亡的重要原因。21世纪以来多次严重疫情给我们留下深刻印象:一是2003年的“非典”(SARS),二是2009年的甲型H1N1流感(人感染猪流感),再有就是现在席卷全球的新型冠状病毒肺炎疫情。因此,传染病的防控一直是医学科学工作者面临的巨大挑战。其中,对病原体进行快速准确的鉴定是传染病精准防控的基础。中国医学科学院病原生物学研究所彭俊平研员自2000年起即深耕于病原体检测技术方法及基因组学、耐药机制相关的研究工作。近日,仪器信息网特别采访了彭俊平研究员,与他就核酸质谱技术在病原体检测领域的应用现状及前景进行了深入交谈。[align=center][img=彭俊平个人.JPG,600,337]https://img1.17img.cn/17img/images/202204/uepic/3407a132-360a-4424-b8f8-73b9d8028642.jpg[/img][/align][align=center]中国医学科学院病原生物学研究所 彭俊平研究员[/align][color=#ff0000]“国内最早开展核酸质谱病原体检测研究的团队之一”[/color]随着各项科学技术的进步,病原体检测技术也在不断发展,由病原分离、电镜观察、免疫学检测等传统生物学方法发展到[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]技术、芯片技术、测序技术、质谱技术等分子生物学方法。“因为引起疾病的病原体种类繁多,单一的平台技术不能解决所有问题,所以,我们的主要工作是利用各种平台技术对病原体进行筛查。”彭俊平介绍到,“多年来我们课题组一直致力于搭建一个病原体组合筛查技术体系,这也是我国在传染病防控领域的一个重要工作。另外,我们利用多重[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]反应结合飞行时间质谱技术(以下简称:核酸质谱)在病原体检测领域开展了10多年的工作,这也是我们多年来的一个重点发展方向。”核酸质谱是什么?彭俊平为笔者解答到,核酸质谱其实是基质辅助激光解吸电离飞行时间质谱(MALDI-TOF)在核酸水平的应用,是一种将多重[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]反应与质谱结合的复合技术。此前,MALDI-TOF主要应用于蛋白质水平的微生物鉴定研究,应用发展不过30多年,而MALDI-TOF在核酸水平的相关应用则是近些年提出的概念,应用发展时间就更短。最初,MALDI-TOF在核酸研究领域开展的应用是SNP基因分型,其首先通过[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]扩增含有SNP的基因组片段,再通过检测核酸分子在真空管中的飞行时间而获得样品分析物的精确分子量,从而检测出SNP位点信息。因为MALDI-TOF本身的高灵敏度和高通量等特点,使其非常适合应用于SNP多位点的筛查。而MALDI-TOF在病原体检测领域的研究则鲜少有报道。彭俊平课题组是国内最早开展核酸质谱病原体检测研究的团队之一。“我们是在2009年引进的这个技术平台,正好是H1N1全球大流行的时候,当时核酸质谱的技术水平还不足以帮助我们开展相关工作,因此我们就开始自己开发方法。”核酸质谱病原体检测的原理是利用MALDI-TOF检测多重[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]反应的产物,即单碱基延伸的产物质量大小,来判定检测靶基因的有无,从而进一步判定样本中目标病原体的有无。与传统的病原体检测技术相比,核酸质谱在灵敏度、检测通量以及操作简便性等方面均有一定优势。此外,核酸质谱检测的核酸序列均来源于公共数据库,不需要依赖其他的数据库。[color=#ff0000] “开发了7种人冠状病毒的检测方法,成功申请专利”[/color]经过多年的技术摸索,彭俊平团队利用核酸质谱在病原体检测领域做出了很多成果。最近其团队开发了7种人冠状病毒的检测方法,并申请了发明专利。目前,已知可以感染人的冠状病毒共有7种,其中包括2003年的“非典”SARS冠状病毒、2012年在中东地区出现的MERS冠状病毒以及2019年12月爆发的严重性呼吸系统综合征冠状病毒SARS-Cov-2。彭俊平介绍到,课题组是从2012年开始开展人冠状病毒的检测技术研究,其中一部分工作内容就是利用核酸质谱进行检测应用。该部分成果是与岛津公司合作开发的,利用一步法多重反应[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]与MALDI-TOF质谱联用鉴定7种人冠状病毒与新型冠状病毒的重要突变位点。“本次合作中我们将多重[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]反应从两步法改进为一步法,既缩短了实验时间,又减少了人为操作的工作。而且我们改进的方法适用于所有的RNA病毒,可以说是摸索出了一种通用的解决方案。”彭俊平介绍到,“和岛津合作成果的应用价值很明确,我非常期待未来该方法的推广。接下来我们也将继续和岛津合作在MALDI-TOF平台上开发出更多病原体检测解决方案,并合力推动核酸质谱在临床领域的应用。”笔者追问到目前国际上核酸质谱在病原体检测领域的应用现状如何?彭俊平坦言道,国际上相关的成果并不多,而团队于2009年就开展了相关研究,可以说是走在了国际前列。不过,目前核酸质谱病原体检测的应用还以科研阶段为主,临床应用正处于拓展阶段。此外,彭俊平也谈到他认为核酸质谱走向临床所面临的瓶颈,一是MALDI-TOF本身的硬件设备比较贵;其次,基于MALDI-TOF平台提供给临床应用的成熟方法不多。因此,核酸质谱这样的技术平台想要真正推广到临床,首先需要提供“一揽子”的解决方案,这样应用场景就会被打开。不过,彭俊平也观察到,无论国内还是国外,越来越多的团队和厂商开始关注这一领域,相信核酸质谱的临床应用情况将在短短几年之内得到很大的改变。最后彭俊平表示,未来核酸质谱病原体检测值得重点关注的方向有呼吸道感染疾病、腹泻性疾病和性传播疾病等,其涉及的病原体种类繁多,是核酸质谱可以“大展身手”的方向。后记:采访中彭俊平反复提到“病原体的组合筛查技术体系”,他也为笔者解释到,为了获取更全面的生物信息,往往需要多种技术平台共同解决问题,而不是希望用一个技术平台去解决所有的问题。回到MALDI-TOF这一技术来说,总有人拿质谱与NGS测序相比较,其实它们的应用场景和目标都不一样,发展核酸质谱也并不是为了替代测序技术。事实上,核酸质谱只需要在中高通量的检测中建立并巩固其“王者地位”,在此基础上能够再提升灵敏度和分辨率等性能,就为自身的发展开辟了新天地。
水产养殖病原微生物的分子检测注:全文见附件。有用到的鼓掌不要都做伸手党
【金秋计划】+如果病原微生物泼溅在检测人员身上应该如何处置 https://ng1.17img.cn/bbsfiles/images/2024/09/202409181047227788_3745_1502196_3.jpg!w690x457.jpg 在实验室工作,难免会出现操作不当导致液体溅入或洒落吸入,为保障检测工作人员的健康生命安全和国家财产安全,防止和杜绝食盐污染对周围环境造成严重污染,确保一旦发生食盐污染事件及安全事故时,能及时规范,科学,迅速,有效的控制,应做好以下处理: https://ng1.17img.cn/bbsfiles/images/2024/09/202409181048538740_7234_1502196_3.jpg!w412x320.jpg 1.如果病原微生物泼溅在检测人员皮肤上,立即用75%的酒精或碘伏进行消毒,然后用清水冲洗。 2.如果病原微生物泼溅在检测人员眼内,立即用生理盐水或洗眼液冲洗,然后用清水冲洗。 3.如果病原微生物泼溅在检测人员的衣服、鞋帽上或桌面、地面,立即选用75%的酒精、碘伏,0.2-0.5%的过氧乙酸、500-10000mg/L有效氯消毒液等进行消毒。 4.如果工作人员通过意外吸入、意外损伤或接触暴露,应立即紧急处理,并及时报告实验室污染预防应急处置专业小组。如工作人员操作过程中被污染的注射器针刺伤、金属锐器操作应立即实施急救。首先用肥皂和清水冲洗伤口,然后挤伤口的血液,再用消毒液(如75%的酒精、2000mg/L次氯酸钠、0.2%-0.5%过氧乙酸、0.5%的碘伏)浸泡或涂抹消毒,并包扎伤口(厌氧微生物感染不包扎伤口)。 https://ng1.17img.cn/bbsfiles/images/2024/09/202409181046574296_653_1502196_3.jpg!w328x212.jpg 总之,实验室安全不可忽视,在做试验前一定要戴好手套、口罩、帽子、防护鞋、防护衣等,一但不小心弄到身上要第一时间采取有效的处理方法,做好应急处置。
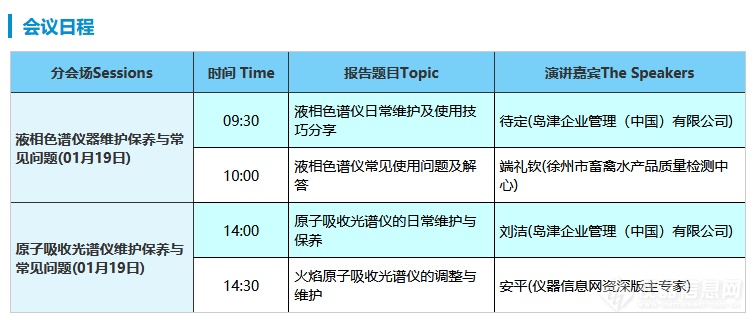
[size=16px][b]仪器信息网[/b]网络讲堂将于[/size][size=18px][color=#6666CC][b]2021年3月9日[/b][/color][/size][size=16px]召开[/size][b][size=18px][color=#FF0000]病原微生物检测技术与进展[/color][/size][/b][size=12px]主题网络研讨会,携手该领域的专家和一线工作者带来精彩的分享。[/size][url=https://www.instrument.com.cn/webinar/meetings/pathogen2021/][color=#000099][size=18px][b]点击报名[/b][/size][/color][/url][size=12px](本次会议旨在为同行提供在线学习机会,实现教育资源共享,并搭建互动平台,增进学术交流,促成项目合作。)[/size][align=center]=======================================================================[/align][url=https://www.instrument.com.cn/webinar/meetings/pathogen2021/][img=,1026,224]https://img1.17img.cn/17img/images/202102/webinar/4bfddb13-0561-4847-ae34-694715375680.jpg[/img][/url] COVID-19新冠病毒的出现让人们再次认识到了冠状病毒的威力。同时,疫情也让我们重新认识了种类繁多且极具威胁的病原微生物。病毒具有复制侵袭能力强、传播力强且体积小的特点;而自然界中的其他病原微生物,如细菌、真菌以及寄生虫等也会对人类健康具有很大的危害,引起多种疾病。 为了控制各类病原微生物,必须建立快速有效的分析检测技术进行鉴别,进而开发临床检测和治疗方案。用于分析检测的相关的技术有基因测序、RT-PCR、代谢组学、免疫学、毒理学研究等。 基于此,[b]仪器信息网[/b]与[b]天津市分析测试协会[/b]拟于2021年3月9日联合举办“病原微生物检测技术与进展”主题网络研讨会,旨在关注[size=18px][color=#FF0000][b]病原微生物与病毒检测[/b][/color][/size],为广大医学工作者和检测人员提供一个交流的空间。[size=12px][size=16px]【报名链接】[/size][/size]:[url=https://www.instrument.com.cn/webinar/meetings/pathogen2021/]点击链接[/url][align=center]=======================================================================[/align][url=https://www.instrument.com.cn/webinar/meetings/pathogen2021/][img=,690,387]https://ng1.17img.cn/bbsfiles/images/2021/03/202103091016056551_1344_2507958_3.png!w690x387.jpg[/img][/url]
求助:血清免疫学做病原菌检测会用到哪些仪器设备?有清单最好。跪求各位大神仗义出手相助。
求助:血清免疫学做病原菌检测会用到哪些仪器设备?有清单最好。跪求各位大神仗义出手相助。
哪位有食品中重要人兽共患疾病病原体检测技术方面的资料,麻烦帮传一下,谢谢!haijun.yunfeng@yahoo.com.cn
奶粉中病源微生物的分子生物学检测
目的:建立抗菌中药对临床常见病原性细菌抑菌作用的检测方法。方法:选择6种常用抗菌中药(黄连、苦参、连翘、大黄、生地、知母),分别采用水提法制备至质量浓度1mg/L。应用液体稀释法测定上述中药对金黄色葡萄球菌、大肠埃希菌和铜绿假单胞菌的最低抑菌浓度(MIC)。结果:建立了中药抑菌作用的检测方法。黄连、大黄与连翘抑制细菌的作用较强,MIC值均≤0.05mg/L,其中黄连对金黄色葡萄球菌的抑菌作用最强(MIC值为0.00625mg/L)。结论:应用本方法可以进行中药抑菌作用的检测。抗菌中药对所试验菌种表现不同的抑菌作用。【关键词】中草药;微生物敏感性试验;抗菌药;细菌 Study on Antibacteral Effects of Six Chinese Herbs Against Pathogenic Bacteria XUE Jianjiang1,QIAO Haixia2,LIU Jinjun2,et al 1.Clinicial Lab,The First Affilited Hospitial,Hebei North University,Zhangjiakou,075000,Hebei,China 2.Department of Microbiology,Hebei North University,Zhangjiakou,075000,Hebei,China 【ABSTRACT】Objective:To establish a method to detect the antibacterialactivity of traditional chinese medicine against pathegenicbacteria.Methods:Six varieties of traditional chinese medicine(Coptisetc)were selected and extracted with pure water to make concentratedwith 1mg/L.Three different common pathogenic bacteria were used todetermine the minimal inhibitory concentration(MIC)in vitro with liquiddilution method to the selected medicine.Results:The methods wereestablished to detect the antibacterial activity of traditional chinesemedicine.Three herbs had inhibition effects on the strains oftest,among which Coptis Chinesis had the strongest effect and MIC was0.00625g/mL to Staphylococcus aureus.Conclusion:The methods can serveas a reference for the antibacterial activity of traditional chinesemedicine.The degree of inhibition effect for different traditionalchinese medicine on different bacteria were different. 【KEY WORDS】Chinese Herb,Microbial Sensitivity Tests,AntiBacterial Agents,Bacteria 中药几千年来为中国人民的健康做出了重大贡献,在现代预防和控制细菌性感染疾病中也发挥了积极作用。应用中药进行抗感染治疗具有副作用小,药物来源广泛,价格低廉等优势。在清热解毒抗菌类中药中开发抗菌药物具有良好的应用前景。长期以来,对于抗菌中药作用机理的较少认识限制了其在临床中的应用。目前,尚无统一规范的中药抗菌作用评价方法。为此,本研究拟应用抗生素最小抑菌浓度检测方法,检测6种常用抗菌中药(大黄、苦参、连翘、黄连、生地、知母)对三种常见病原性细菌(金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌)的抑菌作用,建立一种可以规范的中药抗菌作用检测方法。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=54998]食物和动物饲料的微生物学.食物病原体检测用聚合酶链式反应[/url]
218.75.91.248是这里的IP吗?今天好多病毒啊!江民提示:打开http://218.75.91.248 window.cab-〉Testsign.exe 发现病毒Trojan/Agent.kxp !!!!!!请大家小心了!!![em0705] [em0705] [em0705] [em0705] [em0705]
病原微生物实验室生物安全管理条例中华人民共和国国务院令第424号 《病原微生物实验室生物安全管理条例》已经2004年11月5日国务院第69次常务会议通过,现予公布,自公布之日起施行。 第一章 总则 第一条 为了加强病原微生物实验室(以下称实验室)生物安全管理,保护实验室工作人员和公众的健康,制定本条例。 第二条 对中华人民共和国境内的实验室及其从事实验活动的生物安全管理,适用本条例。 本条例所称病原微生物,是指能够使人或者动物致病的微生物。本条例所称实验活动,是指实验室从事与病原微生物菌(毒)种、样本有关的研究、教学、检测、诊断等活动。 第三条 国务院卫生主管部门主管与人体健康有关的实验室及其实验活动的生物安全监督工作。 [B]文章太长,可下载附件[/B]!
[quote][b]项目概况[/b]呼吸道病原监测试剂和新型冠状病毒基因测序试剂采购 招标项目的潜在投标人应在北京市西城区南滨河路27号贵都国际中心A座1604室获取招标文件,并于2023年02月21日 09点30分(北京时间)前递交投标文件。[/quote][font=inherit]一、项目基本情况[/font]项目编号:HCJS-BJ-2023-001项目名称:呼吸道病原监测试剂和新型冠状病毒基因测序试剂采购预算金额:43.6948000 万元(人民币)最高限价(如有):43.6948000 万元(人民币)采购需求:[font=inherit]1、项目概况:[/font][table][tr][td][align=center]包号[/align][/td][td][align=center]货物名称[/align][/td][td][align=center]规格型号[/align][/td][td][align=center]技术参数[/align][/td][td][align=center]计量[/align][align=center]单位[/align][/td][td][align=center]数量[/align][/td][td][align=center]交货[/align][align=center]时间[/align][/td][td][align=center]交货地点[/align][/td][td][align=center]备注[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]呼吸道病原监测试剂和新型冠状病毒基因测序试剂[/align][/td][td][align=center]详见招标文件[/align][/td][td][align=center]详见招标文件[/align][/td][td][align=center]包[/align][/td][td][align=center]1[/align][/td][td][align=center]以甲方要求为准[/align][/td][td][align=center]甲方指定[/align][/td][td][align=center]/[/align][/td][/tr][/table][font=inherit]2、技术规格[/font]2.1 技术指标参数详见招标文件。2.2 供货周期:以招标人要求为准,一切物流配送、搬运、安装、培训等费用及破损、意外损坏、灭失等风险均由成交供应商承担。2.3资金来源:财政拨款。2.4货物须执行的标准:符合国家标准。2.5售后服务要求:按照客户要求进行改进,符合军队使用需求。2.6 交付(验收)标准及要求:能够满足甲方使用需求。合同履行期限:以甲方要求为准本项目( 不接受 )联合体投标。
长期以来,人们对于病原菌耐药的认识基本上停留在特定病原菌对特定抗生素的耐药机制,以及特定抗生素对病原菌的抑菌机理上。然而相关研究表明,在抗生素使用与病原菌耐药水平之间存在着一种宏观的量化关系,即一定范围内的抗生素使用可以导致病原菌整体耐药水平以及耐药菌感染率的变化,这种关系就是抗生素与病原菌之间的量化关系。 有关抗生素与病原菌之间量化关系研究的历史不长,而对其集中、深入的研究也只是近几年才展开的。在发达国家,特别是对抗生素使用严格控制的北欧国家此类研究开展较多,而在发展中国家则基本为空白。造成这一领域研究起步晚,发展不均衡主要有两方面因素。 首先,相关研究需要通过一定范围内大样本的调查,收集、处理各种病原菌和抗生素使用的相关数据。在发达国家,有关病原菌耐药和抗生素使用的监测机构健全,可以方便地获取和处理大量的相关数据,加之有流行病学、统计学、药理学、微生物学以及临床医学等多学科的协作,可以深入、细致、及时地研究抗生素使用与病原菌耐药之间的量化关系。 而在发展中国家,相关的监测机构不健全。以国内为例,目前各级医疗机构有关病原菌耐药的数据和抗生素使用的数据,由不同的职能科室、部门管理,信息交流困难,导致了我们在这一领域中的研究远远落后于发达国家。 第二,不同抗生素剂量单位以及常用剂量差别很大,在大范围研究中无法比较和叠加。早期相关研究只能以抗生素的使用率和抗生素的费用消耗为指标,不能准确反映抗生素的实际使用情况。为解决这一难题,人们用成人每日常用剂量作为标准剂量,将不同抗生素的消耗量换算为统一标准单位,并命名为每日约定剂量(defined daily doses,DDD),以使用的DDD数表示抗生素的消耗量。每一种抗生素消耗量换算成DDD后可以比较和叠加。WHO于1996年推荐采用此方法来研究、监测抗生素的使用情况。正是在这一标准建立后,相关研究在短时间内取得了很大进展。这一领域的研究大致分为以下二类: 1、针对社区居民的大范围研究 此类研究的对象多为一个地区、一个国家,甚至可以是对多个国家的超大规模研究。研究结果对于指导相关国家和地区制定、修改控制抗生素使用的法规,检验相关控制措施的有效性具有重要指导意义。通过不同国家的对比研究还可以探讨自然条件、环境因素、社会因素、经济发展水平对抗生素使用与病原菌耐药水平之间量化关系的影响。 瑞典在1994年设立专门机构,率先启动了一项针对抗生素使用与病原菌耐药的全国性系统工程STRAMA,采取有针对性的措施消除抗生素不合理的使用,若干年后,瑞典抗生素的消耗量减少了22%,病原菌耐药水平也明显降低。 2、针对医疗机构的小范围研究 此类研究主要关注不同医院、不同病区、不同基础疾病条件下抗生素使用与病原菌耐药之间的量化关系,发现并证实了多种抗生素的消耗量与常见病原菌的感染率和耐药率之间存在密切的关系。 此类研究的重点通常是临床常见、对患者威胁最大的病原菌,如金黄色葡萄球菌、铜绿假单胞菌、肺炎球菌和肠球菌,以及临床重点关注的抗生素,如万古霉素、大环内酯类抗生素和第三代头孢菌素等。其研究结果对于指导临床抗感染治疗即控制病原菌耐药水平的上升具有重要实用价值。 一项研究采用多元回归的方法,分析了以色列一家医院6个内科病区抗生素使用与病原菌耐药的数据,结果表明,这些病区阿米卡星和第3代头孢菌素的消耗量与临床耐药菌感染率密切相关。 目前只有为数不多的研究通过改变临床抗生素的使用,降低病原菌的耐药水平和耐药菌的感染率,可以说是这一领域研究的前沿,也是这一领域探索者的希望所在和最终目的。 Landman等通过减少医院中头孢菌素、亚胺培南、克林霉素和万古霉素的使用,增加含β-内酰胺酶抑制剂抗生素的使用,成功地降低了耐甲氧西林金黄色葡萄球菌(MRSA)和耐头孢他啶肺炎克雷伯菌的感染率。 近期研究还发现,临床增加氨苄西林/舒巴坦的使用量可以明显降低奇异变形杆菌和阴沟肠杆菌的耐药水平;而增加头孢吡肟的使用量可以降低MRSA的感染率。 有研究者曾对其所在医院烧伤病区抗生素使用和病原菌耐药的相关数据进行了统计分析,发现含β内酰胺酶抑制剂类抗生素的使用量与金黄色葡萄球菌耐药水平呈负相关。此外,他们目前已累积了该院烧伤病区8年来临床抗生素使用和病原菌耐药的全部数据,并建成了查询方便的数据库,为进一步进深入研究奠定了基础。 总之,抗生素使用与病原菌结构和耐药水平之间量化关系的研究对于指导临床抗感染治疗、合理使用抗生素,以及制定控制抗生素使用的相关法规具有重要意义,但目前在这一领域有许多方面有待进一步探索。目前国内有关抗生素和病原菌的相关信息的交流存在诸多障碍,这需要包括医疗机构管理者、相关专家以及临床医师共同努力,加强信息交流,通过深入研究抗生素使用与病原菌耐药之间的量化关系,为指导临床抗感染治疗,降低病原菌的耐药水平提供具有实际应用价值的信息。
新华社新加坡4月13日电(记者陈济朋)据新加坡媒体日前报道,新加坡研究人员研发出一种病毒检测芯片,可一次性快速检验上万种病原体。 据介绍,这种病毒检测芯片由新加坡基因组研究所的研究团队研制,通过快速分析病患DNA样本,可在24小时内详细检测出患者感染何种病毒或细菌。 研究人员表示,这种检测芯片可以一次性检测高达7万种病毒和细菌等病原体,其中包括最新出现的H7N9禽流感病毒。 相比之下,传统的病毒或细菌测试方法,一般针对某一种特定的病原体进行测试,难以同时检测多种病原体。 研究人员说,这种新的检测手段可以尽快明确病因,减少确诊时间,并且成本也不高。目前这种病毒检测芯片还只用于实验用途,研究人员希望该芯片通过相关部门批准后尽快投入市场。

[size=16px] 动物疫病诊断仪通常用于检测动物样品,以确定是否存在某种疫病或病原体感染。这些诊断仪器可以用于多种不同类型的样品,包括但不限于以下几种: 血液样品:血液样品是常用的动物疫病检测样品之一,可用于检测各种血液传播的病原体,如病毒、细菌或寄生虫。 血清样品:血清是血液中的液体部分,通常用于检测抗体或抗原,以确定动物是否曾经接触过某种病原体或已经产生了免疫反应。 组织样品:组织样品包括从动物身体各个器官中获取的组织,通常用于检测病变、细胞变化或病原体的存在。 粪便样品:粪便样品通常用于检测肠道疾病或寄生虫感染,因为许多肠道病原体可以在粪便中找到。 尿液样品:尿液样品可以用于检测一些泌尿系统感染或代谢性疾病。 分泌物样品:分泌物样品如唾液、泪液或鼻液也可以用于检测某些感染性疾病。 病死动物的组织样品:如果动物死亡,可以采集组织样品来确定死因或检测可能的疫病。 云唐动物疫病诊断仪通常可以针对不同类型的样品进行检测,并使用不同的分析技术,如[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url](聚合酶链反应)、ELISA(酶联免疫吸附法)等来检测病原体的DNA、RNA、蛋白质或抗体等。具体的样品类型和检测方法会根据需要和研究目的而有所不同。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/09/202309051044532904_8492_6098850_3.png!w690x690.jpg[/img][/size]
[font=inherit]一、项目基本情况[/font]项目编号:BY-HWZB-20240205项目名称:吉林省疾病预防控制中心(吉林省公共卫生研究院)病毒所传染病实验室检测质量提升相关质控品及检测试剂采购项目预算金额:75.592000 万元(人民币)最高限价(如有):75.592000 万元(人民币)采购需求:病毒所传染病实验室检测质量提升相关质控品及检测试剂采购。具体内容详见《招标文件(技术要求)》合同履行期限:签订合同后14天内供货完毕本项目( 不接受 )联合体投标。[font=inherit]二、申请人的资格要求:[/font]1.满足《中华人民共和国政府采购法》第二十二条规定;2.落实政府采购政策需满足的资格要求:本项目专门面向中小企业采购3.本项目的特定资格要求:3.1本次招标要求供应商须具有独立承担民事责任的能力,具有有效的营业执照,供应商应具有履行合同所必需的设备和专业能力;3.2近三年度(2020年、2021年、2022年)财务审计报告,(新成立不足三年的企业需提供自成立之日起至2022年12月31日的财务审计报告,如公司为2022年12月31日以后成立的公司需提供成立之日起至今公司财务状况良好的承诺书);3.3近半年任意一个月的依法缴纳税收和社会保障资金的证明材料;3.4拒绝列入政府取消投标资格记录期间的企业或个人投标,对在“信用中国”网站(www.creditchina.gov.cn)、中国政府采购网(www.ccgp.gov.cn)等渠道列入失信被执行人、重大税收违法失信主体、政府采购严重违法失信行为记录名单及其他不符合《中华人民共和国政府采购法》第二十二条规定条件的供应商,不得参与政府采购活动;3.5本项目对投标申请人的资格审查方式采用资格后审方式,主要资格审查标准和内容详见招标文件中的资格审查文件,只有资格审查合格的投标申请人才能进入后续评审;3.6本项目核心产品为:22重呼吸道病原核酸检测试剂盒、多病原核酸质控品(本项目为非单一产品采购,根据采购文件中载明的核心产品,对多家投标申请人提供的核心产品品牌相同的参加同一合同项下投标的,且通过资格审查、符合性审查的不同投标人,按一家投标人计算,评审后得分最高的同品牌投标人获得中标人推荐资格;评审得分相同的采取随机抽取方式确定,其他同品牌投标人不作为中标候选人)。[font=inherit]三、获取招标文件[/font]时间:2024年02月29日 至 2024年03月06日,每天上午8:30至12:00,下午12:00至16:00。(北京时间,法定节假日除外)地点:吉林省公共资源交易中心网(www.ggzyzx.jl.gov.cn)方式:网上下载售价:¥0.0 元,本公告包含的招标文件售价总和[font=inherit]四、提交投标文件截止时间、开标时间和地点[/font]提交投标文件截止时间:2024年03月21日 09点00分(北京时间)开标时间:2024年03月21日 09点00分(北京时间)地点:吉林省公共资源交易中心开标三室[font=inherit]五、公告期限[/font]自本公告发布之日起5个工作日。[font=inherit]六、其他补充事宜[/font]本次采购公告同时在中国政府采购网、吉林省公共资源交易中心网、中国采购与招标网、中国招标投标公共服务平台上发布。监督部门信息:吉林省财政厅政府采购管理处[font=inherit]七、对本次招标提出询问,请按以下方式联系。[/font]1.采购人信息名 称:吉林省疾病预防控制中心(吉林省公共卫生研究院)地址:长春市景阳大路3145号联系方式:张添一0431-979773032.采购代理机构信息名 称:吉林省博扬招标项目管理有限公司地 址:长春市二道区洋浦大街凯利中心十三楼1308室联系方式:刘美男15004319373(办公电话)3.项目联系方式项目联系人:刘美男电 话: 15004319373(办公电话)
[font='calibri'][size=13px]免疫学检测形成的原因有哪些?免疫学[/size][/font][font='calibri'][size=13px]检测包括哪些?[/size][/font]免疫学检测形成的原因:免疫学检测是基于免疫系统对外来物质或抗原的反应而产生的,可分为体液免疫学检测和细胞免疫学检测两大类。体液免疫学检测是通过血液、唾液、乳汁等体液样本中的免疫球蛋白、补体、免疫复合物等成分的含量及其分布来反映机体的免疫状态。当机体受到病原体或某些生物物质的刺激时,免疫系统会产生相应的抗体和细胞因子等免疫反应,这些免疫反应产物可通过体液免疫学检测方法进行检测。细胞免疫学检测是通过检测机体内的免疫细胞和免疫分子的含量及其分布来反映机体的免疫状态。当机体受到病原体或某些生物物质的刺激时,免疫系统会产生相应的抗原提呈细胞,并引导记忆细胞和效应细胞的产生,这些记忆细胞和效应细胞可以在特定情况下识别和消灭病原体或肿瘤细胞,这些细胞和效应细胞本身也可以被检测出来。总之,免疫学检测的目的是通过检测机体的免疫反应,了解机体的免疫状态,为疾病的诊断、治疗和预防提供重要的依据。免疫学检测包括哪些?免疫学检测是指通过各种方法检测机体对病原体或某些生物物质的免疫反应程度,以及机体内的免疫细胞、免疫分子和免疫活性物质的含量及其分布等情况的一种医学技术。免疫学检测广泛应用于各种疾病的诊断、治疗和预防,包括感染性疾病、自身免疫性疾病、肿瘤免疫学诊断等。以下是一些常见的免疫学检测项目:体液免疫学检测:主要包括免疫球蛋白的测定,如IgA、IgM、IgE等;补体检测,如总补体溶血活性、补体C1、C2等;免疫复合物检测,如抗体-抗原复合物、补体-抗体复合物等;细胞免疫学检测:主要包括T细胞亚群分析、B淋巴细胞分化抗原检测、自然杀伤细胞抗体检测、T细胞活化抗体检测等;抗体检测:如抗药抗体、中和抗体等;细胞因子检测:如白细胞介素-2、-4、-6等;自身抗体检测:如抗核抗体、抗胰岛素抗体等;感染免疫检测:如病毒特异性抗体、细菌特异性抗体等。总之,免疫学检测是一种非常重要的医学技术,可以帮助医生判断机体的免疫状态,为疾病的诊断和治疗提供重要的依据。免疫学检测是根据抗原、抗体反应的原理,利用已知的抗原检测未知的抗体或利用已知的抗体检测未知的抗原,可定性、定位和定量的检测。依托自主研发生产的优质抗体、蛋白试剂、先进的实验仪器以及经验丰富的技术人员,义翘神州建立了全面的免疫学检测平台,包括ELISA、Western Blot、IHC、IF、Flow Cytometry、IP/Co-IP、Biacore、Octet等检测技术。义翘神州免疫学检测服务包含:①WB/Sally Sue高通量检测服务②[url=https://cn.sinobiological.com/services/flow-cytometry-service]流式细胞检测服务[/url]③免疫组化检测服务④多重免疫荧光和免疫组化服务⑤免疫荧光检测服务⑥HE染色及特殊染色服务⑦ELISA/ELISpot检测服务⑧IP/Co-IP检测服务⑨TMA芯片定制服务更多详情可以查看:https://cn.sinobiological.com/services/immunoassay-service
病害肉检测仪主要应用于食品行业,特别是肉类食品生产和加工领域。它的主要功能是检测肉类食品中是否存在病原微生物、污染物和其他不良因素,以确保食品安全和质量。 以下是一些病害肉检测仪在哪些行业中应用的例子: 肉类加工业: 病害肉检测仪在肉类加工业中被广泛应用,用于检测肉类产品中是否含有细菌、寄生虫、病毒等病原微生物,以及其他可能引起食品变质或污染的因素。 食品安全监管机构: 政府食品监管机构可以使用病害肉检测仪来监督和检查市场上的肉类产品,确保它们符合卫生标准和法规要求。 疫病防控机构: 病害肉检测仪也在动物疫病防控机构中得到应用,用于早期发现和诊断动物身上携带的病原微生物,以防止疫病传播。 餐饮业和零售业: 餐厅、超市和食品零售商也可能使用病害肉检测仪来检测他们销售的肉类产品,以确保所售肉类的质量和安全。 肉类生产企业: 肉类生产企业可以在生产线上使用病害肉检测仪,进行原料和成品的检测,从而保障生产过程的质量控制。 科研机构: 在食品科研领域,病害肉检测仪也可用于研究肉类产品的微生物污染、食品变质等问题,以推动食品安全领域的科学研究。 总之,病害肉检测仪在食品安全保障、质量控制和疫病防控等领域发挥着重要作用,有助于确保人们消费的肉类食品安全可靠。
[font=宋体]随着生物技术的飞速发展,生物安全问题日益凸显。为了确保人类健康与环境安全,生物安全检测服务应运而生,成为一道重要的防线。本文将介绍生物安全检测服务的背景、意义、技术方法和应用领域,并探讨其发展趋势和前景。[/font][font=宋体] [/font][font=宋体][b]一、背景与意义[/b][/font][font=宋体] [/font][font=宋体]生物安全检测服务旨在预防、检测和监控生物危害,保护人类健康和环境安全。随着生物技术的广泛应用,新型病原菌、转基因生物等不断涌现,给人类带来潜在风险。因此,生物安全检测服务对于防范和控制生物风险具有重要意义。[/font][font=宋体] [/font][b][font=宋体]二、技术方法[/font][/b][font=宋体] [/font][font=宋体][font=宋体]分子生物学技术:利用分子生物学技术对病原菌进行基因水平检测,包括基因芯片、[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]等。这些技术可快速、准确地检测出病原菌,为防控措施提供科学依据。[/font][/font][font=宋体]免疫学技术:通过抗体检测和抗原检测,对病原菌进行特异性识别,具有灵敏度高、操作简便等优点。[/font][font=宋体]生物传感器技术:利用生物传感器对生物危害进行实时监测,具有快速、便捷的优点,可实现连续监测和自动化分析。[/font][font=宋体]数据分析技术:通过对大量数据的收集和分析,发现病原菌的传播规律和预测未来趋势,为防控决策提供数据支持。[/font][font=宋体] [/font][font=宋体][b]三、应用领域[/b][/font][font=宋体] [/font][font=宋体]食品工业:在食品生产过程中,对病原菌进行严格检测,确保食品安全。[/font][font=宋体]医学领域:在医疗过程中,对病原菌进行监测和防控,保障医护人员和患者的健康。[/font][font=宋体]环境监测:对自然环境和养殖场等重点区域进行病原菌监测,防止病原菌扩散。[/font][font=宋体]进出口检验检疫:对进出口货物进行病原菌检测,防止外来病原菌入侵。[/font][font=宋体] [/font][font=宋体][b]四、发展趋势和前景[/b][/font][font=宋体] [/font][font=宋体]随着科技的不断进步,生物安全检测服务将朝着更加快速、准确、自动化的方向发展。未来,人工智能和大数据技术的应用将进一步优化生物安全检测服务体系,提高监测预警能力。同时,随着全球气候变化和生态系统的改变,新型病原菌的出现和传播将更加频繁,因此生物安全检测服务还需不断加强和完善,以应对未来挑战。[/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州建立了经[/font][font=Calibri]CNAS[/font][font=宋体]认证的实验室,并且拥有生物安全二级实验室,已在北京市备案,该实验室严格按照[/font][font=Calibri]CNAS[/font][font=宋体]和[/font][font=Calibri]GLP[/font][font=宋体]规范进行设计及管理。团队成员具备扎实的生物医学、药学等相关专业背景,对中国[/font][font=Calibri]NMPA[/font][font=宋体]、美国[/font][font=Calibri]FDA[/font][font=宋体]和[/font][font=Calibri]ICH[/font][font=宋体]等的当今要求和未来趋势具有深刻的理解,可根据客户产品提供最佳的病毒清除验证和细胞库检测的方案。详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/services/biosafety-testing-services[/font][/font][font=宋体] [/font][font=宋体]总之,[url=https://cn.sinobiological.com/services/biosafety-testing-services][b]生物安全检测服务[/b][/url]是保障人类健康与环境安全的重要防线。通过采用先进的科学技术和方法,我们能够更加有效地预防、检测和监控生物危害。随着科技的进步和社会的发展,我们相信生物安全检测服务将会在保障人类健康和环境安全方面发挥更加重要的作用。[/font]

[size=16px] 动物疫病快速检测仪有哪些用途 动物疫病快速检测仪是用于检测动物中潜在疫病病原体的仪器,通常被广泛应用于养殖业、畜牧业和野生动物保护等领域。这些检测仪器具有多种用途,包括但不限于以下几个方面: 早期疫情监测:动物疫病快速检测仪可用于早期监测动物种群中的潜在疫病,有助于快速发现疫情爆发并采取相应的控制措施,从而减少疫情的蔓延。 动物健康管理:这些仪器可用于定期监测养殖动物或野生动物的健康状况。通过检测疫病病原体,可以及早发现动物中的潜在疫情,有助于采取预防措施,减少生产损失。 检疫和出口:在国际动物贸易中,一些国家或地区可能要求进行疫病检测以确保进出口的动物和动物产品是安全的。动物疫病快速检测仪可用于符合检疫和质量标准。 疫苗研发和效力评估:这些仪器还可以用于疫苗研发和效力评估。通过检测疫病病原体,可以评估疫苗的效果以及其在控制疫病方面的潜在用途。 野生动物保护:在野生动物保护领域,这些仪器用于监测野生动物中的传染病,帮助保护生态系统的健康,减少野生动物种群的疫病传播。 紧急反应:在疫情爆发或疫情威胁时,这些仪器可用于紧急反应,帮助快速诊断和控制疫情的扩散。 动物疫病快速检测仪通常使用分子生物学技术、免疫学方法和生化分析等技术,能够检测多种疫病病原体,如病毒、细菌、寄生虫等。这些仪器的使用有助于维护动物健康、确保食品安全、保护野生动植物,同时减少农业和养殖业的经济损失。[/size]
国家根据病原微生物的传染性、感染后对个体或者群体的危害程度,将病原微生物分为四类:•第一类病原微生物,是指能够引起人类或者动物非常严重疾病的微生物,以及我国尚未发现或者已经宣布消灭的微生物。•第二类病原微生物,是指能够引起人类或者动物严重疾病,比较容易直接或者间接在人与人、动物与人、动物与动物间传播的微生物。•第三类病原微生物,是指能够引起人类或者动物疾病,但一般情况下对人、动物或者环境不构成严重危害,传播风险有限,实验室感染后很少引起严重疾病,并且具备有效治疗和预防措施的微生物。•第四类病原微生物,是指在通常情况下不会引起人类或者动物疾病的微生物。•第一类、第二类病原微生物统称为高致病性病原微生物。

[size=16px] 病菌检测仪有哪些用途 病菌检测仪具有多种用途,主要包括: 在食品生产、加工和配送过程中,快速检测食品样品中的病原菌、致病菌和其他细菌污染,通过对食品中的细菌进行及时、准确的检测,可以预防食品中毒事件的发生,保障消费者的健康和食品安全。 在医疗机构和临床实验室中,病菌检测仪被广泛应用于医疗器械的清洁和消毒监测,手术室和病房的卫生管理,以及病原菌感染的诊断和监测。通过快速检测细菌的存在和数量,医疗工作者可以采取相应的防控措施,减少交叉感染的风险,提高医疗质量和安全性。 检测物体表面的洁净程度,判断物体表面是否有细菌污染。在食品加工与制造、食品器具卫生、操作人员卫生等方面都有所应用。对于完善食品生产卫生安全体系,帮助生产与监督人员快速确定食品加工仪器设备的洁净度等方面有着积极的推动作用。 总的来说,病菌检测仪在食品安全、医疗卫生等领域发挥着重要作用,有效降低食品安全事故的发生,提高医疗质量和安全性。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/12/202312120930494418_8012_6098850_3.jpg!w690x690.jpg[/img][/size]
德国下萨克森州农业部长林德曼5日晚召开新闻发布会宣布,产自该州的豆芽被初步认定为近来德国大面积传染的肠出血性大肠杆菌EHEC病源。生产这些带菌豆芽的工厂目前已被关闭,待次日实验室检验结果揭晓后再行处理。林德曼称,位于下萨克森俞尔岑(Uelzen)地区的一家企业生产18种芽类蔬菜,生产过程中种子被放在一个滚筒中,经喷洒38度的热水后种子发芽,这个温度同样适合其它菌类的生长。林德曼说,这些芽类在生长过程中没有使用肥料,很可能是发芽用的水产生了污染,或者是种子事先沾染细菌,在发芽的环境中迅速繁殖。该企业的产品被许多餐厅用作沙拉原料。调查结果表明,许多病人在不同餐厅食用了含有该企业生产的豆芽沙拉之后患病。并且该企业亦有两名工作人员感染腹泻,其中一名被证实感染肠出血性大肠杆菌。由于目前还没有得到实验室的准确数据,联邦健康部没有证实这一结果。负责流行病预防及监督的罗伯特-考赫学院认为,在病源没有十分确定的情况下,建议民众继续放弃生吃蔬菜。自五月初德国出现大面积EHEC病菌传染之后,该病菌首先在西班牙进口黄瓜上被发现,后被实验室证实黄瓜上病菌和致病病菌并非同一支。目前德国已知肠出血性大肠杆菌患者近2千人,20死亡,627人感染上并发症血溶性尿毒症。芽类蔬菜曾经有多次致病先例。1996年,小红萝卜芽曾经在日本引起一场严重的肠道传染病。当时感染大肠杆菌的患者有12600余人,但只对少数人造成血溶性尿毒症这样的致命并发。
[font=&][size=16px][color=#333333]点击链接查看更多:[url]https://www.woyaoce.cn/service/info-37732.html[/url]服务背景[/color][/size][/font][font=&][color=#333333][/color][/font]中药是我国传统药物的总称。中药学在我国有着两千多年的历史文化,是中化民族优秀文化的瑰宝,是我国医学的科学的重要组成部分。中医药以其独有的特色和优势与现代医药相互补充,形成了具有中国特色的社会主文医药卫生事业共同承护的增进人民身体健康的任务,对促进经济和社会可持续发展发挥着积极的作用并生有产业发展的优势。的真假、质最的好坏,会真接影响临床应用的效果和患者的生命安全。所以对干的鉴别有着十分重要的意义。中科检测是国科控股旗下独立第三方检测机构,已通过《中国药典》关于中药的CMA检测资质认定,可开展中药材农药残留检测,重金属检测、真菌毒素检测、微生物限度检查等。中药普遍存在的剧毒农药残留相比,中药原有的“三分毒”已变得似乎可以忽略不计,因为前这属于防不胜防的化工污染,对人体健康的危害更为巨大。对人体健康的危害更为巨大,而按照检测结果显示,目前市面上含有农药残留的中药已达到七成以上,这对于常服重要的慢性病人或者体弱多病着们来说无疑是一记迎头闷棒。因此,对于市面上的中药制品生产企业,则需要第三方检测机构来把关,中科检测具有多台进口设备,能够有效的出中药的农残,还包括重金属检测、真菌毒素检测、微生物限度检查等。[font=&][size=16px][color=#333333]检测内容[/color][/size][/font][font=&][color=#333333][/color][/font]中药普遍存在的剧毒农药残留相比,中药原有的“三分毒”已变得似乎可以忽略不计,因为前这属于防不胜防的化工污染,对人体健康的危害更为巨大。对人体健康的危害更为巨大,而按照检测结果显示,目前市面上含有农药残留的中药已达到七成以上,这对于常服重要的慢性病人或者体弱多病着们来说无疑是一记迎头闷棒。因此,对于市面上的中药制品生产企业,则需要第三方检测机构来把关,中科检测具有多台进口设备,能够有效的出中药的农残,还包括重金属检测、真菌毒素检测、微生物限度检查等。[size=18px]中药材农药残留检测项目及标准[/size][table=750][tr][td=1,17,75]农药残留检测[/td][td=1,1,152]甲胺磷[/td][td=1,1,152]氯磺隆[/td][td=1,17,75]中国药典第四部 2341 农药残留量测定法[/td][/tr][tr][td=1,1,75]甲基对硫磷[/td][td=1,1,152]胺苯磺隆[/td][/tr][tr][td=1,1,75]对硫磷[/td][td=1,1,152]甲磺隆[/td][/tr][tr][td=1,1,75]久效磷[/td][td=1,1,152]甲拌磷[/td][/tr][tr][td=1,1,75]磷胺[/td][td=1,1,152]甲基异柳磷[/td][/tr][tr][td=1,1,75]六六六[/td][td=1,1,152]内吸磷[/td][/tr][tr][td=1,1,75]滴滴涕[/td][td=1,1,152]克百威[/td][/tr][tr][td=1,1,75]杀虫脒[/td][td=1,1,152]涕灭威[/td][/tr][tr][td=1,1,75]除草醚[/td][td=1,1,152]灭线磷[/td][/tr][tr][td=1,1,75]艾氏剂[/td][td=1,1,152]氯唑磷[/td][/tr][tr][td=1,1,75]狄氏剂[/td][td=1,1,152]水胺硫磷[/td][/tr][tr][td=1,1,75]苯线磷[/td][td=1,1,152]硫丹[/td][/tr][tr][td=1,1,75]地虫硫磷[/td][td=1,1,152]氟虫腈[/td][/tr][tr][td=1,1,75]硫线磷[/td][td=1,1,152]三氯杀螨醇[/td][/tr][tr][td=1,1,75]蝇毒磷[/td][td=1,1,152]硫环磷[/td][/tr][tr][td=1,1,75]治螟磷[/td][td=1,1,152]甲基硫环磷[/td][/tr][tr][td=1,1,75]特丁硫磷[/td][td=1,1,152]——[/td][/tr][/table][font=&][size=16px][color=#333333]检测标准[/color][/size][/font][font=&][color=#333333][/color][/font][table][tr][td]产品名称[/td][td]检测项目[/td][td]检测标准[/td][/tr][tr][td]中药制品农药残留检测[/td][td]中药材农药残留检测标准[/td][td]中国药典第四部 2341 农药残留量测定法[/td][/tr][/table]
[u]甘肃省疾病预防控制中心[/u]招标项目的潜在投标人应在[u]甘肃海联公共资源交易网(www.gsebidding.com)在线免费获得[/u]获取招标文件,并于[u]2023-05-24 09:30:00[/u](北京时间)前递交投标文件。一、项目基本情况项目编号:2023zfcg00515项目名称:甘肃省疾病预防控制中心病原检测试剂政府采购项目预算金额:230.6679(万元)最高限价:(万元)采购需求:病原检测试剂一批,详见招标文件第四部分。合同履行期限:按合同约定执行本项目(是/否)接受联合体投标:否二、申请人的资格要求1.供应商须符合《中华人民共和国政府采购法》第二十二条之规定,并提供《中华人民共和国政府采购法实施条例》第十七条中要求的材料;供应商未被列入“信用中国”网站(www.creditchina.gov.cn)记录失信被执行人或重大税收违法案件当事人名单或政府采购严重违法失信行为记录名单;不处于中国政府采购网(www.ccgp.gov.cn)政府采购严重违法失信行为信息记录中的禁止参加政府采购活动期间的方可参加本项目的投标;2.落实政府采购政策需满足的资格要求:根据财库[2022]19号《关于进一步加大政府采购支持中小企业力度的通知》规定;根据财库[2014]68号财政部发布的《关于政府采购支持监狱企业发展有关问题的通知》规定;根据财库[2017]141号财政部、民政部、中国残疾人联合会发布的《关于促进残疾人就业政府采购政策的通知》规定;根据财库[2004]185号《节能产品政府采购实施意见》的规定;3.本项目的特定资格要求:供应商须具有医疗器械生产许可证(备案证)或医疗器械经营许可证(备案证)。三、获取招标文件时间:[u]2023-05-04[/u]至[u]2023-05-09[/u],每天上午[u]00:00[/u]至[u]12:00[/u],下午[u]12:00[/u]至[u]23:59[/u]地点:甘肃海联公共资源交易网(www.gsebidding.com)在线免费获得方式:为了规范交易平台的业务流程以及给用户提供方便快捷的服务,凡是拟参与甘肃省公共资源交易活动的供应商需依照甘肃海联公共资源交易平台首页窗口“CA锁办理指南”的相关程序先在甘肃海联公共资源交易平台网上注册,并办理获取CA数字证书。用已办理获取的CA数字证书登录,登记拟参与项目进行投标,免费下载招标文件。甘肃海联公共资源交易平台联系电话:0931-8230753 0931-8230762 0931-8511237联系人:田耀华、王艺颖联系地址:甘肃省兰州市城关区雁滩高新开发区雁南路西脉大厦四层 请供应商随时关注“甘肃政府采购网”及“甘肃海联公共资源交易网”关于本项目相关书面变更及通知,如因未主动登录网站而未获取相关信息,对其产生不利因素由供应商自行承担。售价:0(元)四、提交投标文件截止时间、开标时间和地点时间:2023-05-24 09:30:00地点:甘肃海联公共资源交易平台开标系统(http://www.gsebidding.com:9309/)不见面钉钉在线开标。五、公告期限自本公告发布之日起5个工作日。六、其他补充事宜①甘肃海联公共资源交易网:http://www.gsebidding.com②信用中国”网站:https://www.creditchina.gov.cn③中国政府采购网网址:http://www.ccgp.gov.cn/七、对本次招标提出询问,请按以下方式联系1.采购人信息名 称:[u]甘肃省疾病预防控制中心[/u]地 址:[u]兰州市东岗西路310号[/u]联系方式:[u]0931-8267481[/u]2.采购代理机构信息名 称:[u]中海建国际建设咨询集团有限责任公司[/u]地 址:[u]甘肃省兰州市城关区民主西路97号[/u]联系方式:[u]0931-7842893[/u]3.项目联系方式项目联系人:[u]董全宇、左华娟[/u]电 话:[u]0931-7842893[/u]
[color=#888888][url=http://blog.sina.com.cn/s/blog_17a5fba0f0102xvau.html]《病原微生物实验室生物安全管理条例》[/url][/color][color=#888888]2004年11月12日中华人民共和国国务院令第424号公布 [/color][color=#888888]2016年2月6日《国务院关于修改部分行政法规的决定》修订[/color][color=#888888]2018年04月04日《国务院关于修改和废止部分行政法规的决定》修订[/color] 《国务院关于修改和废止部分行政法规的决定》中华人民共和国国务院令第698号十一、删去《病原微生物实验室生物安全管理条例》第二十一条第二款。第二十二条第一款中的“取得从事高致病性病原微生物实验活动资格证书的实验室,”修改为“三级、四级实验室”。第二十三条第一款中的“取得相应资格证书的实验室”修改为“具备相应条件的实验室”。第二十六条修改为:“国务院卫生主管部门和兽医主管部门应当定期汇总并互相通报实验室数量和实验室设立、分布情况,以及三级、四级实验室从事高致病性病原微生物实验活动的情况。”第五十六条修改为:“三级、四级实验室未经批准从事某种高致病性病原微生物或者疑似高致病性病原微生物实验活动的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令停止有关活动,监督其将用于实验活动的病原微生物销毁或者送交保藏机构,并给予警告;造成传染病传播、流行或者其他严重后果的,由实验室的设立单位对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。”第五十八条中的“卫生主管部门或者兽医主管部门对符合法定条件的实验室不颁发从事高致病性病原微生物实验活动的资格证书,或者对出入境检验检疫机构为了检验检疫工作的紧急需要”修改为“卫生主管部门或者兽医主管部门对出入境检验检疫机构为了检验检疫工作的紧急需要”。第六十一条中的“由原发证部门吊销该实验室从事高致病性病原微生物相关实验活动的资格证书”修改为“责令停止该项实验活动,该实验室2年内不得申请从事高致病性病原微生物实验活动”。 [b]【2018修订版】《病原微生物实验室生物安全管理条例》第一章 总 则[url=http://blog.sina.com.cn/s/blog_17a5fba0f0102xvau.html]点击打开链接[/url][/b]第一条 为了加强病原微生物实验室(以下称实验室)生物安全管理,保护实验室工作人员和公众的健康,制定本条例第二条 对中华人民共和国境内的实验室及其从事实验活动的生物安全管理,适用本条例。 本条例所称病原微生物,是指能够使人或者动物致病的微生物。 本条例所称实验活动,是指实验室从事与病原微生物菌(毒)种、样本有关的研究、教学、检测、诊断等活动第三条 国务院卫生主管部门主管与人体健康有关的实验室及其实验活动的生物安全监督工作。 国务院兽医主管部门主管与动物有关的实验室及其实验活动的生物安全监督工作。 国务院其他有关部门在各自职责范围内负责实验室及其实验活动的生物安全管理工作。 县级以上地方人民政府及其有关部门在各自职责范围内负责实验室及其实验活动的生物安全管理工作。第四条 国家对病原微生物实行分类管理,对实验室实行分级管理。第五条 国家实行统一的实验室生物安全标准。实验室应当符合国家标准和要求。第六条 实验室的设立单位及其主管部门负责实验室日常活动的管理,承担建立健全安全管理制度,检查、维护实验设施、设备,控制实验室感染的职责。 [b]第二章 病原微生物的分类和管理[/b] 第七条 国家根据病原微生物的传染性、感染后对个体或者群体的危害程度,将病原微生物分为四类: 第一类病原微生物,是指能够引起人类或者动物非常严重疾病的微生物,以及我国尚未发现或者已经宣布消灭的微生物。 第二类病原微生物,是指能够引起人类或者动物严重疾病,比较容易直接或者间接在人与人、动物与人、动物与动物间传播的微生物。 第三类病原微生物,是指能够引起人类或者动物疾病,但一般情况下对人、动物或者环境不构成严重危害,传播风险有限,实验室感染后很少引起严重疾病,并且具备有效治疗和预防措施的微生物。 第四类病原微生物,是指在通常情况下不会引起人类或者动物疾病的微生物。 第一类、第二类病原微生物统称为高致病性病原微生物。 第八条 人间传染的病原微生物名录由国务院卫生主管部门商国务院有关部门后制定、调整并予以公布;动物间传染的病原微生物名录由国务院兽医主管部门商国务院有关部门后制定、调整并予以公布。 第九条 采集病原微生物样本应当具备下列条件: (一)具有与采集病原微生物样本所需要的生物安全防护水平相适应的设备; (二)具有掌握相关专业知识和操作技能的工作人员; (三)具有有效的防止病原微生物扩散和感染的措施; (四)具有保证病原微生物样本质量的技术方法和手段。 采集高致病性病原微生物样本的工作人员在采集过程中应当防止病原微生物扩散和感染,并对样本的来源、采集过程和方法等作详细记录。 第十条 运输高致病性病原微生物菌(毒)种或者样本,应当通过陆路运输;没有陆路通道,必须经水路运输的,可以通过水路运输;紧急情况下或者需要将高致病性病原微生物菌(毒)种或者样本运往国外的,可以通过民用航空运输。 第十一条 运输高致病性病原微生物菌(毒)种或者样本,应当具备下列条件: (一)运输目的、高致病性病原微生物的用途和接收单位符合国务院卫生主管部门或者兽医主管部门的规定; (二)高致病性病原微生物菌(毒)种或者样本的容器应当密封,容器或者包装材料还应当符合防水、防破损、防外泄、耐高(低)温、耐高压的要求; (三)容器或者包装材料上应当印有国务院卫生主管部门或者兽医主管部门规定的生物危险标识、警告用语和提示用语。 运输高致病性病原微生物菌(毒)种或者样本,应当经省级以上人民政府卫生主管部门或者兽医主管部门批准。在省、自治区、直辖市行政区域内运输的,由省、自治区、直辖市人民政府卫生主管部门或者兽医主管部门批准;需要跨省、自治区、直辖市运输或者运往国外的,由出发地的省、自治区、直辖市人民政府卫生主管部门或者兽医主管部门进行初审后,分别报国务院卫生主管部门或者兽医主管部门批准。 出入境检验检疫机构在检验检疫过程中需要运输病原微生物样本的,由国务院出入境检验检疫部门批准,并同时向国务院卫生主管部门或者兽医主管部门通报。 通过民用航空运输高致病性病原微生物菌(毒)种或者样本的,除依照本条第二款、第三款规定取得批准外,还应当经国务院民用航空主管部门批准。 有关主管部门应当对申请人提交的关于运输高致病性病原微生物菌(毒)种或者样本的申请材料进行审查,对符合本条第一款规定条件的,应当即时批准。 第十二条 运输高致病性病原微生物菌(毒)种或者样本,应当由不少于2人的专人护送,并采取相应的防护措施。 有关单位或者个人不得通过公共电(汽)车和城市铁路运输病原微生物菌(毒)种或者样本。 第十三条 需要通过铁路、公路、民用航空等公共交通工具运输高致病性病原微生物菌(毒)种或者样本的,承运单位应当凭本条例第十一条规定的批准文件予以运输。 承运单位应当与护送人共同采取措施,确保所运输的高致病性病原微生物菌(毒)种或者样本的安全,严防发生被盗、被抢、丢失、泄漏事件。第十四条 国务院卫生主管部门或者兽医主管部门指定的菌(毒)种保藏中心或者专业实验室(以下称保藏机构),承担集中储存病原微生物菌(毒)种和样本的任务。 保藏机构应当依照国务院卫生主管部门或者兽医主管部门的规定,储存实验室送交的病原微生物菌(毒)种和样本,并向实验室提供病原微生物菌(毒)种和样本。 保藏机构应当制定严格的安全保管制度,作好病原微生物菌(毒)种和样本进出和储存的记录,建立档案制度,并指定专人负责。对高致病性病原微生物菌(毒)种和样本应当设专库或者专柜单独储存。 保藏机构储存、提供病原微生物菌(毒)种和样本,不得收取任何费用,其经费由同级财政在单位预算中予以保障。 保藏机构的管理办法由国务院卫生主管部门会同国务院兽医主管部门制定。 第十五条 保藏机构应当凭实验室依照本条例的规定取得的从事高致病性病原微生物相关实验活动的批准文件,向实验室提供高致病性病原微生物菌(毒)种和样本,并予以登记。 第十六条 实验室在相关实验活动结束后,应当依照国务院卫生主管部门或者兽医主管部门的规定,及时将病原微生物菌(毒)种和样本就地销毁或者送交保藏机构保管。 保藏机构接受实验室送交的病原微生物菌(毒)种和样本,应当予以登记,并开具接收证明。 第十七条 高致病性病原微生物菌(毒)种或者样本在运输、储存中被盗、被抢、丢失、泄漏的,承运单位、护送人、保藏机构应当采取必要的控制措施,并在2小时内分别向承运单位的主管部门、护送人所在单位和保藏机构的主管部门报告,同时向所在地的县级人民政府卫生主管部门或者兽医主管部门报告,发生被盗、被抢、丢失的,还应当向公安机关报告;接到报告的卫生主管部门或者兽医主管部门应当在2小时内向本级人民政府报告,并同时向上级人民政府卫生主管部门或者兽医主管部门和国务院卫生主管部门或者兽医主管部门报告。 县级人民政府应当在接到报告后2小时内向设区的市级人民政府或者上一级人民政府报告;设区的市级人民政府应当在接到报告后2小时内向省、自治区、直辖市人民政府报告。省、自治区、直辖市人民政府应当在接到报告后1小时内,向国务院卫生主管部门或者兽医主管部门报告。 任何单位和个人发现高致病性病原微生物菌(毒)种或者样本的容器或者包装材料,应当及时向附近的卫生主管部门或者兽医主管部门报告;接到报告的卫生主管部门或者兽医主管部门应当及时组织调查核实,并依法采取必要的控制措施。 [b]第三章 实验室的设立与管理[/b] 第十八条 国家根据实验室对病原微生物的生物安全防护水平,并依照实验室生物安全国家标准的规定,将实验室分为一级、二级、三级、四级。 第十九条 新建、改建、扩建三级、四级实验室或者生产、进口移动式三级、四级实验室应当遵守下列规定: (一)符合国家生物安全实验室体系规划并依法履行有关审批手续; (二)经国务院科技主管部门审查同意; (三)符合国家生物安全实验室建筑技术规范; (四)依照《中华人民共和国环境影响评价法》的规定进行环境影响评价并经环境保护主管部门审查批准; (五)生物安全防护级别与其拟从事的实验活动相适应。 前款规定所称国家生物安全实验室体系规划,由国务院投资主管部门会同国务院有关部门制定。制定国家生物安全实验室体系规划应当遵循总量控制、合理布局、资源共享的原则,并应当召开听证会或者论证会,听取公共卫生、环境保护、投资管理和实验室管理等方面专家的意见。 第二十条 三级、四级实验室应当通过实验室国家认可。 国务院认证认可监督管理部门确定的认可机构应当依照实验室生物安全国家标准以及本条例的有关规定,对三级、四级实验室进行认可;实验室通过认可的,颁发相应级别的生物安全实验室证书。证书有效期为5年。 第二十一条 一级、二级实验室不得从事高致病性病原微生物实验活动。三级、四级实验室从事高致病性病原微生物实验活动,应当具备下列条件:(一)实验目的和拟从事的实验活动符合国务院卫生主管部门或者兽医主管部门的规定;(二)具有与拟从事的实验活动相适应的工作人员;(三)工程质量经建筑主管部门依法检测验收合格。国务院卫生主管部门或者兽医主管部门依照各自职责对三级、四级实验室是否符合上述条件进行审查;对符合条件的,发给从事高致病性病原微生物实验活动的资格证书。 第二十二条 三级、四级实验室,需要从事某种高致病性病原微生物或者疑似高致病性病原微生物实验活动的,应当依照国务院卫生主管部门或者兽医主管部门的规定报省级以上人民政府卫生主管部门或者兽医主管部门批准。实验活动结果以及工作情况应当向原批准部门报告。 实验室申报或者接受与高致病性病原微生物有关的科研项目,应当符合科研需要和生物安全要求,具有相应的生物安全防护水平。与动物间传染的高致病性病原微生物有关的科研项目,应当经国务院兽医主管部门同意;与人体健康有关的高致病性病原微生物科研项目,实验室应当将立项结果告知省级以上人民政府卫生主管部门。 第二十三条 出入境检验检疫机构、医疗卫生机构、动物防疫机构在实验室开展检测、诊断工作时,发现高致病性病原微生物或者疑似高致病性病原微生物,需要进一步从事这类高致病性病原微生物相关实验活动的,应当依照本条例的规定经批准同意,并在具备相应条件的实验室中进行。 专门从事检测、诊断的实验室应当严格依照国务院卫生主管部门或者兽医主管部门的规定,建立健全规章制度,保证实验室生物安全。 第二十四条 省级以上人民政府卫生主管部门或者兽医主管部门应当自收到需要从事高致病性病原微生物相关实验活动的申请之日起15日内作出是否批准的决定。 对出入境检验检疫机构为了检验检疫工作的紧急需要,申请在实验室对高致病性病原微生物或者疑似高致病性病原微生物开展进一步实验活动的,省级以上人民政府卫生主管部门或者兽医主管部门应当自收到申请之时起2小时内作出是否批准的决定;2小时内未作出决定的,实验室可以从事相应的实验活动。 省级以上人民政府卫生主管部门或者兽医主管部门应当为申请人通过电报、电传、传真、电子数据交换和电子邮件等方式提出申请提供方便。 第二十五条 新建、改建或者扩建一级、二级实验室,应当向设区的市级人民政府卫生主管部门或者兽医主管部门备案。设区的市级人民政府卫生主管部门或者兽医主管部门应当每年将备案情况汇总后报省、自治区、直辖市人民政府卫生主管部门或者兽医主管部门。 第二十六条 国务院卫生主管部门和兽医主管部门应当定期汇总并互相通报实验室数量和实验室设立、分布情况,以及三级、四级实验室从事高致病性病原微生物实验活动的情况。。 第二十七条 已经建成并通过实验室国家认可的三级、四级实验室应当向所在地的县级人民政府环境保护主管部门备案。环境保护主管部门依照法律、行政法规的规定对实验室排放的废水、废气和其他废物处置情况进行监督检查。 第二十八条 对我国尚未发现或者已经宣布消灭的病原微生物,任何单位和个人未经批准不得从事相关实验活动。 为了预防、控制传染病,需要从事前款所指病原微生物相关实验活动的,应当经国务院卫生主管部门或者兽医主管部门批准,并在批准部门指定的专业实验室中进行。 第二十九条 实验室使用新技术、新方法从事高致病性病原微生物相关实验活动的,应当符合防止高致病性病原微生物扩散、保证生物安全和操作者人身安全的要求,并经国家病原微生物实验室生物安全专家委员会论证;经论证可行的,方可使用。 第三十条 需要在动物体上从事高致病性病原微生物相关实验活动的,应当在符合动物实验室生物安全国家标准的三级以上实验室进行。 第三十一条 实验室的设立单位负责实验室的生物安全管理。 实验室的设立单位应当依照本条例的规定制定科学、严格的管理制度,并定期对有关生物安全规定的落实情况进行检查,定期对实验室设施、设备、材料等进行检查、维护和更新,以确保其符合国家标准。 实验室的设立单位及其主管部门应当加强对实验室日常活动的管理。 第三十二条 实验室负责人为实验室生物安全的第一责任人。 实验室从事实验活动应当严格遵守有关国家标准和实验室技术规范、操作规程。实验室负责人应当指定专人监督检查实验室技术规范和操作规程的落实情况。 第三十三条 从事高致病性病原微生物相关实验活动的实验室的设立单位,应当建立健全安全保卫制度,采取安全保卫措施,严防高致病性病原微生物被盗、被抢、丢失、泄漏,保障实验室及其病原微生物的安全。实验室发生高致病性病原微生物被盗、被抢、丢失、泄漏的,实验室的设立单位应当依照本条例第十七条的规定进行报告。 从事高致病性病原微生物相关实验活动的实验室应当向当地公安机关备案,并接受公安机关有关实验室安全保卫工作的监督指导。 第三十四条 实验室或者实验室的设立单位应当每年定期对工作人员进行培训,保证其掌握实验室技术规范、操作规程、生物安全防护知识和实际操作技能,并进行考核。工作人员经考核合格的,方可上岗。 从事高致病性病原微生物相关实验活动的实验室,应当每半年将培训、考核其工作人员的情况和实验室运行情况向省、自治区、直辖市人民政府卫生主管部门或者兽医主管部门报告。 第三十五条 从事高致病性病原微生物相关实验活动应当有2名以上的工作人员共同进行。 进入从事高致病性病原微生物相关实验活动的实验室的工作人员或者其他有关人员,应当经实验室负责人批准。实验室应当为其提供符合防护要求的防护用品并采取其他职业防护措施。从事高致病性病原微生物相关实验活动的实验室,还应当对实验室工作人员进行健康监测,每年组织对其进行体检,并建立健康档案;必要时,应当对实验室工作人员进行预防接种。 第三十六条 在同一个实验室的同一个独立安全区域内,只能同时从事一种高致病性病原微生物的相关实验活动。 第三十七条 实验室应当建立实验档案,记录实验室使用情况和安全监督情况。实验室从事高致病性病原微生物相关实验活动的实验档案保存期,不得少于20年。 第三十八条 实验室应当依照环境保护的有关法律、行政法规和国务院有关部门的规定,对废水、废气以及其他废物进行处置,并制定相应的环境保护措施,防止环境污染。 第三十九条 三级、四级实验室应当在明显位置标示国务院卫生主管部门和兽医主管部门规定的生物危险标识和生物安全实验室级别标志。 第四十条 从事高致病性病原微生物相关实验活动的实验室应当制定实验室感染应急处置预案,并向该实验室所在地的省、自治区、直辖市人民政府卫生主管部门或者兽医主管部门备案。 第四十一条 国务院卫生主管部门和兽医主管部门会同国务院有关部门组织病原学、免疫学、检验医学、流行病学、预防兽医学、环境保护和实验室管理等方面的专家,组成国家病原微生物实验室生物安全专家委员会。该委员会承担从事高致病性病原微生物相关实验活动的实验室的设立与运行的生物安全评估和技术咨询、论证工作。 省、自治区、直辖市人民政府卫生主管部门和兽医主管部门会同同级人民政府有关部门组织病原学、免疫学、检验医学、流行病学、预防兽医学、环境保护和实验室管理等方面的专家,组成本地区病原微生物实验室生物安全专家委员会。该委员会承担本地区实验室设立和运行的技术咨询工作。 [b]第四章 实验室感染控制[/b] 第四十二条 实验室的设立单位应当指定专门的机构或者人员承担实验室感染控制工作,定期检查实验室的生物安全防护、病原微生物菌(毒)种和样本保存与使用、安全操作、实验室排放的废水和废气以及其他废物处置等规章制度的实施情况。 负责实验室感染控制工作的机构或者人员应当具有与该实验室中的病原微生物有关的传染病防治知识,并定期调查、了解实验室工作人员的健康状况。 第四十三条 实验室工作人员出现与本实验室从事的高致病性病原微生物相关实验活动有关的感染临床症状或者体征时,实验室负责人应当向负责实验室感染控制工作的机构或者人员报告,同时派专人陪同及时就诊;实验室工作人员应当将近期所接触的病原微生物的种类和危险程度如实告知诊治医疗机构。接诊的医疗机构应当及时救治;不具备相应救治条件的,应当依照规定将感染的实验室工作人员转诊至具备相应传染病救治条件的医疗机构;具备相应传染病救治条件的医疗机构应当接诊治疗,不得拒绝救治。 第四十四条 实验室发生高致病性病原微生物泄漏时,实验室工作人员应当立即采取控制措施,防止高致病性病原微生物扩散,并同时向负责实验室感染控制工作的机构或者人员报告。 第四十五条 负责实验室感染控制工作的机构或者人员接到本条例第四十三条、第四十四条规定的报告后,应当立即启动实验室感染应急处置预案,并组织人员对该实验室生物安全状况等情况进行调查;确认发生实验室感染或者高致病性病原微生物泄漏的,应当依照本条例第十七条的规定进行报告,并同时采取控制措施,对有关人员进行医学观察或者隔离治疗,封闭实验室,防止扩散。 第四十六条 卫生主管部门或者兽医主管部门接到关于实验室发生工作人员感染事故或者病原微生物泄漏事件的报告,或者发现实验室从事病原微生物相关实验活动造成实验室感染事故的,应当立即组织疾病预防控制机构、动物防疫监督机构和医疗机构以及其他有关机构依法采取下列预防、控制措施: (一)封闭被病原微生物污染的实验室或者可能造成病原微生物扩散的场所; (二)开展流行病学调查; (三)对病人进行隔离治疗,对相关人员进行医学检查; (四)对密切接触者进行医学观察; (五)进行现场消毒; (六)对染疫或者疑似染疫的动物采取隔离、扑杀等措施; (七)其他需要采取的预防、控制措施。 第四十七条 医疗机构或者兽医医疗机构及其执行职务的医务人员发现由于实验室感染而引起的与高致病性病原微生物相关的传染病病人、疑似传染病病人或者患有疫病、疑似患有疫病的动物,诊治的医疗机构或者兽医医疗机构应当在2小时内报告所在地的县级人民政府卫生主管部门或者兽医主管部门;接到报告的卫生主管部门或者兽医主管部门应当在2小时内通报实验室所在地的县级人民政府卫生主管部门或者兽医主管部门。接到通报的卫生主管部门或者兽医主管部门应当依照本条例第四十六条的规定采取预防、控制措施。 第四十八条 发生病原微生物扩散,有可能造成传染病暴发、流行时,县级以上人民政府卫生主管部门或者兽医主管部门应当依照有关法律、行政法规的规定以及实验室感染应急处置预案进行处理。 [b]第五章 监督管理[/b] 第四十九条 县级以上地方人民政府卫生主管部门、兽医主管部门依照各自分工,履行下列职责: (一)对病原微生物菌(毒)种、样本的采集、运输、储存进行监督检查; (二)对从事高致病性病原微生物相关实验活动的实验室是否符合本条例规定的条件进行监督检查; (三)对实验室或者实验室的设立单位培训、考核其工作人员以及上岗人员的情况进行监督检查; (四)对实验室是否按照有关国家标准、技术规范和操作规程从事病原微生物相关实验活动进行监督检查。 县级以上地方人民政府卫生主管部门、兽医主管部门,应当主要通过检查反映实验室执行国家有关法律、行政法规以及国家标准和要求的记录、档案、报告,切实履行监督管理职责。 第五十条 县级以上人民政府卫生主管部门、兽医主管部门、环境保护主管部门在履行监督检查职责时,有权进入被检查单位和病原微生物泄漏或者扩散现场调查取证、采集样品,查阅复制有关资料。需要进入从事高致病性病原微生物相关实验活动的实验室调查取证、采集样品的,应当指定或者委托专业机构实施。被检查单位应当予以配合,不得拒绝、阻挠。 第五十一条 国务院认证认可监督管理部门依照《中华人民共和国认证认可条例》的规定对实验室认可活动进行监督检查。 第五十二条 卫生主管部门、兽医主管部门、环境保护主管部门应当依据法定的职权和程序履行职责,做到公正、公平、公开、文明、高效。 第五十三条 卫生主管部门、兽医主管部门、环境保护主管部门的执法人员执行职务时,应当有2名以上执法人员参加,出示执法证件,并依照规定填写执法文书。 现场检查笔录、采样记录等文书经核对无误后,应当由执法人员和被检查人、被采样人签名。被检查人、被采样人拒绝签名的,执法人员应当在自己签名后注明情况。 第五十四条 卫生主管部门、兽医主管部门、环境保护主管部门及其执法人员执行职务,应当自觉接受社会和公民的监督。公民、法人和其他组织有权向上级人民政府及其卫生主管部门、兽医主管部门、环境保护主管部门举报地方人民政府及其有关主管部门不依照规定履行职责的情况。接到举报的有关人民政府或者其卫生主管部门、兽医主管部门、环境保护主管部门,应当及时调查处理。 第五十五条 上级人民政府卫生主管部门、兽医主管部门、环境保护主管部门发现属于下级人民政府卫生主管部门、兽医主管部门、环境保护主管部门职责范围内需要处理的事项的,应当及时告知该部门处理;下级人民政府卫生主管部门、兽医主管部门、环境保护主管部门不及时处理或者不积极履行本部门职责的,上级人民政府卫生主管部门、兽医主管部门、环境保护主管部门应当责令其限期改正;逾期不改正的,上级人民政府卫生主管部门、兽医主管部门、环境保护主管部门有权直接予以处理。 [b]第六章 法律责任[/b] 第五十六条 三级、四级实验室未经批准从事某种高致病性病原微生物或者疑似高致病性病原微生物实验活动的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令停止有关活动,监督其将用于实验活动的病原微生物销毁或者送交保藏机构,并给予警告;造成传染病传播、流行或者其他严重后果的,由实验室的设立单位对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第五十七条 卫生主管部门或者兽医主管部门违反本条例的规定,准予不符合本条例规定条件的实验室从事高致病性病原微生物相关实验活动的,由作出批准决定的卫生主管部门或者兽医主管部门撤销原批准决定,责令有关实验室立即停止有关活动,并监督其将用于实验活动的病原微生物销毁或者送交保藏机构,对直接负责的主管人员和其他直接责任人员依法给予行政处分;构成犯罪的,依法追究刑事责任。 因违法作出批准决定给当事人的合法权益造成损害的,作出批准决定的卫生主管部门或者兽医主管部门应当依法承担赔偿责任。 第五十八条 卫生主管部门或者兽医主管部门对出入境检验检疫机构为了检验检疫工作的紧急需要,申请在实验室对高致病性病原微生物或者疑似高致病性病原微生物开展进一步检测活动,不在法定期限内作出是否批准决定的,由其上级行政机关或者监察机关责令改正,给予警告;造成传染病传播、流行或者其他严重后果的,对直接负责的主管人员和其他直接责任人员依法给予撤职、开除的行政处分;构成犯罪的,依法追究刑事责任。 第五十九条 违反本条例规定,在不符合相应生物安全要求的实验室从事病原微生物相关实验活动的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令停止有关活动,监督其将用于实验活动的病原微生物销毁或者送交保藏机构,并给予警告;造成传染病传播、流行或者其他严重后果的,由实验室的设立单位对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第六十条 实验室有下列行为之一的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令限期改正,给予警告;逾期不改正的,由实验室的设立单位对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;有许可证件的,并由原发证部门吊销有关许可证件: (一)未依照规定在明显位置标示国务院卫生主管部门和兽医主管部门规定的生物危险标识和生物安全实验室级别标志的; (二)未向原批准部门报告实验活动结果以及工作情况的; (三)未依照规定采集病原微生物样本,或者对所采集样本的来源、采集过程和方法等未作详细记录的; (四)新建、改建或者扩建一级、二级实验室未向设区的市级人民政府卫生主管部门或者兽医主管部门备案的; (五)未依照规定定期对工作人员进行培训,或者工作人员考核不合格允许其上岗,或者批准未采取防护措施的人员进入实验室的; (六)实验室工作人员未遵守实验室生物安全技术规范和操作规程的; (七)未依照规定建立或者保存实验档案的; (八)未依照规定制定实验室感染应急处置预案并备案的。 第六十一条 经依法批准从事高致病性病原微生物相关实验活动的实验室的设立单位未建立健全安全保卫制度,或者未采取安全保卫措施的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令限期改正;逾期不改正,导致高致病性病原微生物菌(毒)种、样本被盗、被抢或者造成其他严重后果的,责令停止该项实验活动,该实验室2年内不得申请从事高致病性病原微生物实验活动;造成传染病传播、流行的,该实验室设立单位的主管部门还应当对该实验室的设立单位的直接负责的主管人员和其他直接责任人员,依法给予降级、撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第六十二条 未经批准运输高致病性病原微生物菌(毒)种或者样本,或者承运单位经批准运输高致病性病原微生物菌(毒)种或者样本未履行保护义务,导致高致病性病原微生物菌(毒)种或者样本被盗、被抢、丢失、泄漏的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令采取措施,消除隐患,给予警告;造成传染病传播、流行或者其他严重后果的,由托运单位和承运单位的主管部门对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第六十三条 有下列行为之一的,由实验室所在地的设区的市级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令有关单位立即停止违法活动,监督其将病原微生物销毁或者送交保藏机构;造成传染病传播、流行或者其他严重后果的,由其所在单位或者其上级主管部门对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;有许可证件的,并由原发证部门吊销有关许可证件;构成犯罪的,依法追究刑事责任: (一)实验室在相关实验活动结束后,未依照规定及时将病原微生物菌(毒)种和样本就地销毁或者送交保藏机构保管的; (二)实验室使用新技术、新方法从事高致病性病原微生物相关实验活动未经国家病原微生物实验室生物安全专家委员会论证的; (三)未经批准擅自从事在我国尚未发现或者已经宣布消灭的病原微生物相关实验活动的; (四)在未经指定的专业实验室从事在我国尚未发现或者已经宣布消灭的病原微生物相关实验活动的; (五)在同一个实验室的同一个独立安全区域内同时从事两种或者两种以上高致病性病原微生物的相关实验活动的。 第六十四条 认可机构对不符合实验室生物安全国家标准以及本条例规定条件的实验室予以认可,或者对符合实验室生物安全国家标准以及本条例规定条件的实验室不予认可的,由国务院认证认可监督管理部门责令限期改正,给予警告;造成传染病传播、流行或者其他严重后果的,由国务院认证认可监督管理部门撤销其认可资格,有上级主管部门的,由其上级主管部门对主要负责人、直接负责的主管人员和其他直接责任人员依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第六十五条 实验室工作人员出现该实验室从事的病原微生物相关实验活动有关的感染临床症状或者体征,以及实验室发生高致病性病原微生物泄漏时,实验室负责人、实验室工作人员、负责实验室感染控制的专门机构或者人员未依照规定报告,或者未依照规定采取控制措施的,由县级以上地方人民政府卫生主管部门、兽医主管部门依照各自职责,责令限期改正,给予警告;造成传染病传播、流行或者其他严重后果的,由其设立单位对实验室主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;有许可证件的,并由原发证部门吊销有关许可证件;构成犯罪的,依法追究刑事责任。 第六十六条 拒绝接受卫生主管部门、兽医主管部门依法开展有关高致病性病原微生物扩散的调查取证、采集样品等活动或者依照本条例规定采取有关预防、控制措施的,由县级以上人民政府卫生主管部门、兽医主管部门依照各自职责,责令改正,给予警告;造成传染病传播、流行以及其他严重后果的,由实验室的设立单位对实验室主要负责人、直接负责的主管人员和其他直接责任人员,依法给予降级、撤职、开除的处分;有许可证件的,并由原发证部门吊销有关许可证件;构成犯罪的,依法追究刑事责任。 第六十七条 发生病原微生物被盗、被抢、丢失、泄漏,承运单位、护送人、保藏机构和实验室的设立单位未依照本条例的规定报告的,由所在地的县级人民政府卫生主管部门或者兽医主管部门给予警告;造成传染病传播、流行或者其他严重后果的,由实验室的设立单位或者承运单位、保藏机构的上级主管部门对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第六十八条 保藏机构未依照规定储存实验室送交的菌(毒)种和样本,或者未依照规定提供菌(毒)种和样本的,由其指定部门责令限期改正,收回违法提供的菌(毒)种和样本,并给予警告;造成传染病传播、流行或者其他严重后果的,由其所在单位或者其上级主管部门对主要负责人、直接负责的主管人员和其他直接责任人员,依法给予撤职、开除的处分;构成犯罪的,依法追究刑事责任。 第六十九条 县级以上人民政府有关主管部门,未依照本条例的规定履行实验室及其实验活动监督检查职责的,由有关人民政府在各自职责范围内责令改正,通报批评;造成传染病传播、流行或者其他严重后果的,对直接负责的主管人员,依法给予行政处分;构成犯罪的,依法追究刑事责任。 [b]第七章 附 则[/b] 第七十条 军队实验室由中国人民解放军卫生主管部门参照本条例负责监督管理。 第七十一条 本条例施行前设立的实验室,应当自本条例施行之日起6个月内,依照本条例的规定,办理有关手续。 第七十二条 本条例自公布之日起施行。