各位老师,IC2500脉冲安培检测器基线不稳定是什么原因
各位老师,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]脉冲安培检测器基线不稳定是什么原因?
请问各位大侠,有没有哪个厂家的液相色谱带有脉冲安培检测器,除了戴安之外,戴安的有点贵。请提示,谢谢谢谢啦
想了解下配脉冲安培检测器的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]多吗?北京地区有哪家不错的可对外使用?因为在糖测定上有优势,一直在关注中.
脉冲安培检测器一般被用来检测糖和氨基酸,那么它对一般的阳离子和阴离子,如Na离子Cl离子这些有没有响应?高手请指教。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=103301]高效[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-脉冲安培检测法测定食品中多聚葡萄糖[/url]
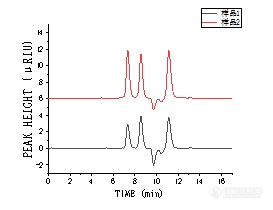
国产离子色谱-脉冲安培检测器测定饮料中常见的糖类化合物郎 蕾1,刘格林1,2,施超欧3*(华东理工大学化学与分子工程学院 分析测试中心,上海 200237)摘要:使用国产离子色谱系统检测饮料中常见的葡萄糖、果糖、乳糖、蔗糖和麦芽糖,并进行方法学验证。结果表明,5种糖类化合物在各自线性范围内R2不小于0.9990,对葡萄糖、果糖、乳糖、蔗糖和麦芽糖的检出限(RSN=3)分别为3.42 μgL-1、11.4 μgL-1;6.76 μgL-1、22.5 μgL-1;10.1 μgL-1。5种糖类化合物的相对标准偏差均小于2.47%,样品的加标回收率范围在94.13% ~ 114.2%之间,均符合相关检测标准要求,能应用于日常实验室的常规糖分析。为考察国产仪器分析的准确性和评价主要模块的性能,与Thermo ICS-5000+离子色谱安培检测系统和Dionex Ultimate 3000-液相色谱示差检测器系统进行比较,对比结果表明,三者的分析结果一致性良好,其中国产脉冲安培离子色谱系统的检出限和定量限比Thermo仪器高3~4倍,除此之外,国产离子色谱仪器各个模块性能稳定,可满足常规糖类化合物含量的测定,填补国产离子色谱在糖类化合物检测领域的空白。关键词:国产离子色谱仪;国产脉冲安培检测器;饮料;糖类化合物中文分类号:O657.7+5 文献标志码:A Determination of Common Carbohydrate Compounds in Beverages by Ion Chromatography with Pulsed Amperometric Detector Made by MyselfLANG Lei1,LIU Gelin1,2,SHI Chaoou3*(Analysis and Research Center,East China University of Science and Technology,Shanghai 200237)Abstract: Using the self-developed pulse amperometric detector, it is assembled with other domestic instrument components to form a complete set of domestic ion chromatography instruments, and applied to the analysis of glucose, fructose, lactose, sucrose and maltose commonly found in beverages, and methodological verification. The results showed that the R2 of the five carbohydrate compounds was not less than 0.9990 in their respective linear ranges, and the detection limits (RSN=3) for glucose, fructose, lactose, sucrose and maltose were 3.42 μgL-1 and 11.4 μgL-1, respectively. 6.76 μgL-1、22.5 μgL-1;10.1 μgL-1。 The relative standard deviation of the five carbohydrates was less than 2.47%, and the spiked recovery of the samples ranged from 94.13% to 114.2%. All meet the requirements of relevant testing standards and can be applied to daily laboratory testing. And in the full import Thermo ICS-5000+ ion chromatography system and Dionex Ultimate 3000 liquid chromatography difference detector repeated the same experimental process, the comparison results show that the analysis results are consistent, but the domestic amperometer detection limit and quantitative limit is 3 to 4 times higher than the imported instrument, the reason for the exploration is that there is a certain gap between the domestic pump and the inlet pump in the stable output mobile phase. The performance of each module and machine of domestic ion chromatography instrument is stable.Keywords:Domestic ion chromatography Domestic pulse amperometric detector Soft drinks Carbohydrate compounds 糖类是植物和动物的主要能量来源,对生理活动等有着极大影响。食品中常见中的糖主要包括葡萄糖、果糖、乳糖、蔗糖和麦芽糖。目前检测食品中糖的测定方法主要有化学法、酶比色法、酶电极法、高效液相色谱法、气相色谱法,毛细管电泳法和高效阴离子交换色谱法等。其中高效液相色谱法测糖主要包括高效液相色谱-示差折光法、高效液相-蒸发光散射法和高效液相质谱法等。高效液相色谱-示差折光检测法只适用于等度洗脱的测试,且只适用于高浓度含量糖样品的分析,在进行多组分分析时效果不好。高效液相色谱-蒸发光散射法对不挥发的溶质具有较高的检测灵敏度,蒸发发光法不受溶剂成分及温度的影响,能够进行梯度洗脱的测试,适于低聚糖的分析。近年来,该方法主要应用于中药材、烟草、食品中糖含量的测定。高效阴离子交换色谱-脉冲安培(high performance anion exchange chromatography with pulsed amperometric detection,HPAEC-PAD)法采用NaOH为流动相,并添加NaAc。能实现糖醇、单糖、双糖、寡糖、低聚糖、多糖以及糖衍生物的分析。其在检测糖时主要使用金电极的脉冲安培检测器,可检测ugL-1级的糖,不需要进行衍生反应和复杂的样品纯化处理,基体干扰少,有着较好的方法重复性和稳定性。但是,目前国内所有文献安培法测糖的报道都使用进口检测器,未见国产安培检测器的应用报道。目前带脉冲安培检测器的进口离子色谱仪器价格昂贵,维护费用高。因此,开发国产带脉冲安培检测器的离子色谱仪十分必要。本实验使用GI5000离子色谱系统包含脉冲安培检测器,对饮料中常见的葡萄糖、果糖、乳糖、蔗糖和麦芽糖的分析,进行了相关的方法学实验,并选取了三种市面上常见的含糖饮料进行了检测。与Thermo ICS-5000+离子色谱安培检测系统和Dionex Ultimate 3000液相色谱示差检测器系统进行比较,以此来验证GI5000离子色谱系统在检测糖类化合物方面的性能,从而填补了国产离子色谱仪器对糖类化合物检测的空白,同时考察了国产自研安培检测器和国产泵与进口仪器的性能差距。 1 试验部分 1.1 仪器与试剂GI5000离子色谱系统:包括GI3000软件、四元梯度泵、自动进样器和GI5250安培检测器(包括自研安培检测池、自研参比电极和自研Au工作电极); Thermo ICS 5000+离子色谱系统,包括变色龙7.2软件、SP-DP单元四元梯度泵、AS-AP自动进样器、DC模块(带安培检测器)。Dionex Ultimate 3000液相色谱系统,包括变色龙6.8软件、四元梯度泵、自动进样器、柱温箱和RI-101型示差折光检测器Millipore-Q A10超纯水系统,AL204电子分析天平。5种糖混合标准储备溶液:1.000 gL-1,称取葡萄糖51.0 mg、果糖50.5 mg、乳糖50.5 mg、蔗糖51.0 mg、麦芽糖51.0 mg于50 mL容量瓶中,加入超纯水充分溶解后定容至刻度,储存于于4 ℃冰箱中冷藏保存,可放置半个月。使用时用超纯水稀释到所需质量浓度。可口可乐溶液:先将可口可乐溶液进行超声处理,用0.22 μm的滤膜进行过滤,称取可乐样品126 mg,加入超纯水稀释50倍。样品溶液:将样品1(脉动饮料)和2(茶π饮料)用0.22μm的滤膜进行过滤,再分别称取496 mg和507 mg于50 ml容量瓶中,加入超纯水定容至刻度,得到浓度为9920 mgL-1和10140mgL-1的两份实际样品溶液。使用时用超纯水稀释到所需质量浓度。50% NaOH(W/W)(电子级) 德国Merck公司;D-无水葡萄糖( D-Glucose anhydrous,≥98%) 上海笛柏化学品有限公司;D-果糖(D-Fructose,≥99%)、蔗糖(sucrose,≥99.5%)、麦芽糖(maltose,≥98%) 上海阿拉丁生化科技股份有限公司;无水乳糖(lactose,≥98%) 上海麦克林生化科技有限公司;可口可乐、实际样品1(脉动)和实际样品2(茶π),均为超市购买;实验用水均采用电阻率不低于18.2 MΩcm的超纯水。所有试剂使用前均使用0.22 μm的滤膜过滤。1.2 色谱条件GI5000离子色谱系统和Thermo ICS-5000+离子色谱系统:Dionex CarboPac PA1色谱柱(250 mm×4 mm),Dionex CarboPac PA1保护柱(50 mm×4 mm);柱温为30℃;流量为1 mlmin-1;进样量为25 μL;流动相为200 mmolNaOH溶液;安培检测器电位波形为糖标准四电位。图1为5 mgL-1 5种糖类化合物混合标准溶液在GI5000离子色谱系统中的色谱图。Dionex Ultimate 3000液相色谱系统:Shodex-SP0810色谱柱(8.0 mm×300 mm);柱温70 ℃;流量为1mlmin-1;进样量为25μL;流动相为超纯水。 https://ng1.17img.cn/bbsfiles/images/2022/12/202212151708218665_5415_3389662_3.jpg!w310x240.jpg 图1 5种糖类混合标准溶液色谱图Fig.1 Chromatogram of mixed solution of 5 sugar standards 2 结果与讨论2.1 GI5000离子色谱系统与Thermo ICS-5000+离子色谱系统灵敏度对比实验显示GI5000离子色谱仪器的噪音稳定在0.12 nC,而Thermo ICS-5000+离子色谱仪器的噪音稳定在0.02 nC,探索了造成这种现象的原因,首先将与检测器相连接的安培池体部件进行了拆卸,对自研Au工作电极进行打磨维护,冲洗了自研参比电极,重新组装后安装在Thermo安培检测器上,用Thermo DP泵进行测试,观察Au工作电极噪音的变化,结果发现噪音值稳定在0.02 nC,与进口安培池体噪音一致,排除了自研安培池体部件对噪音的影响。又将自研安培池体转移至GI5250安培检测器上并与Thermo DP泵串联起来进行测试,噪音值稳定在0.06 nC,说明GI5250安培检测器自身和国产泵较进口仪器存在一定差距,但已符合日常的检测灵敏度的要求。2.2 方法学验证1)标准曲线分别配置质量浓度为0.2、0.5、1.0、2.0、5.0 mgL-1的5种糖类化合物混合标准溶液,以质量浓度(x,mgL-1)为横坐标,以峰面积(y)为纵坐标,绘制标准曲线。各组分的线性范围、线性方程、相关系数、检出限(RSN=3)和定量限(RSN=10)见表1,5种糖类化合物在各自线性范围内线性关系R2不小于0.9990,满足分析方法的要求。Thermo ICS-5000+离子色谱系统对葡萄糖、果糖、乳糖蔗糖和麦芽糖的检出限和定量限分别为1.200 μgL-1、4.010 μgL-1;1.830 μgL-1、6.100 μgL-1;2.960 μgL-1、9.860 μgL-1;6.230 μgL-1、20.78 μgL-1;10.15 μgL-1、33.82 μgL-1。 表1 GI5000离子色谱仪测定5种糖类化合物的线性数据和检出限Table 1 The GI5000 ion chromatograph determines linear data and detection limits for five carbohydrate compounds糖类化合物线性范围/(mgL-1)线性方程相关系数检出限/(μgL-1)定量限/(μgL-1)葡萄糖0.2~5y = 621.5x + 24.910.99983.42011.40果糖0.2~5y = 366.7x + 23.920.99966.75922.53乳糖0.2~5y = 328.0x + 39.460.999010.1233.72蔗糖0.2~5y = 218.1x + 21.340.999320.4368.09麦芽糖0.2~5y = 272.5x + 14.950.999031.37104.6 2)进样重复性取适量的浓度为5 mgL-1的5种糖类化合物混合标准溶液于进样瓶中,分两批分别在GI5000离子色谱系统和Thermo ICS-5000+离子色谱系统上重复进样8次,记录所测得的峰高和峰面积,计算RSD实验结果如表2所示,表明葡萄糖、果糖、乳糖、蔗糖和麦芽糖的峰高和峰面积RSD≤2.47%,结果稳定,与Thermo ICS-5000+离子色谱系统检测结果的RSD几乎一致,说明了GI5000离子色谱系统在重复性方面与进口仪器保持一致,性能良好,实验结果稳定可靠。 表2 5种糖类化合物进样重复性考察结果Table 2 Results of repeated sampling of five sugars糖类化合物GI5000Thermo ICS-5000+峰高RSD/(%)峰面积RSD/(%)峰高RSD/(%)峰面积RSD/(%)葡萄糖0.570.481.411.56果糖0.560.481.982.19果糖0.720.912.172.54蔗糖0.932.471.251.40麦芽糖0.841.780.460.51 3)5种糖类化合物加标回收率测定对可口可乐样品进行加标回收率实验,对于样品中含有的糖类化合物,以其质量分数的80%、100%和120%进行加标,重复进样5次,计算峰面积的RSD,检测结果如表3所示,样品的加标回收率范围在94.13%~114.2%之间,相对标准偏差在0.22%~4.14%。经计算得,可口可乐中葡萄糖质量浓度为41.6 gL-1,果糖质量浓度为54.4 gL-1、乳糖质量浓度为1.5 gL-1、蔗糖质量浓度为4.1 gL-1、麦芽糖质量浓度为1.8 gL-1,总含糖量为103.4 gL-1,可口可乐厂家标注碳水化合物总量为104.6 gL-1,误差1.14%,说明检测结果可靠。图2为可口可乐样品色谱图。 表3 5种糖类化合物加标回收率测定结果Table 3 Determination of the recovery rate of five sugars糖类化合物本底/(mgL-1)加标量/(mgL-1)测得量/(mgL-1)回收率/%相对标准偏差/%葡萄糖1.9551.6003.55399.881.802.0003.89997.200.382.4004.21494.130.22果糖2.1401.6003.69397.803.832.0004.07396.650.252.4004.629103.74.14乳糖1.010.8001.885109.40.191.0002.151114.20.231.2002.353111.90.8蔗糖0.7740.8001.54496.250.971.0001.847107.40.171.2002.043105.80.15麦芽糖0.8920.8001.755107.92.721.0001.915102.30.451.2002.128103.00.75https://ng1.17img.cn/bbsfiles/images/2022/12/202212151708335940_9325_3389662_3.png!w424x327.jpg 图2 可口可乐样品色谱图Fig.2 Coca-Cola sample chromatography 2.3 三种仪器检测结果对比离子色谱法中两种实际样品稀释100倍,液相色谱法中两种实际样品稀释10倍。分别在全进口仪器Thermo ICS 5000+离子色谱系统、GI5000离子色谱系统以及Dionex Ultimate 3000液相色谱仪器上重复进样5针,测试结果如表4所示。 表4 实际样品1和样品2中含糖量测定结果Table 4 Measurement results of sugar content in actual sample 1 and sample 2糖类化合物离子色谱法-Thermo安培离子色谱法-GI5000安培液相色谱法-Dionex示差样品1样品2样品1样品2样品1样品2含糖量/(gL-1)含糖量/(gL-1)含糖量/(gL-1)含糖量/(gL-1)含糖量/(gL-1)含糖量/(gL-1)葡萄糖15.8723.1016.6222.1816.3322.08果糖19.7131.1919.9029.5021.5730.86乳糖------------蔗糖12.8523.5512.2823.0911.7223.72麦芽糖------------总含糖量/g/L48.4377.8448.8074.7749.6276.66样品1和样品2厂家标注的总含糖量分别为49 gL-1和75 gL-1。如表4所示,全进口仪器Thermo ICS 5000+测得两种样品的总含糖量分别为48.43 gL-1和77.84 gL-1,GI5000离子色谱系统测得两种样品的总含糖量分别为48.80 gL-1和74.77 gL-1。Dionex Ultimate-3000液相色谱示差法测得两种样品的总含糖量分别为49.62 gL-1和76.66 gL-1。三种仪器的所测得的两种实际样品中糖类化合物总量相差5%以内,结果均较为准确,同时也证明了国产离子色谱仪器性能稳定可靠。三台仪器对两种实际样品的分离色谱图如图3和4所示。https://ng1.17img.cn/bbsfiles/images/2022/12/202212151708443314_437_3389662_3.png!w273x210.jpghttps://ng1.17img.cn/bbsfiles/images/2022/12/202212151708496041_6974_3389662_3.png!w273x210.jpg 图3 样品1和样品2中糖分离色谱图Thermo离子色谱仪(左)、国产离子色谱仪(右)Fig.3 Separation chromatograms of sugars in samples 1 and 2 Thermo ion chromatograph (left), domestic ion chromatograph (right)https://ng1.17img.cn/bbsfiles/images/2022/12/202212151708552407_2039_3389662_3.png!w273x210.jpg 图4 液相-示差法测得样品1和样品2中糖分离色谱图Fig.4 Separation chromatogram of sugar in sample 1 and sample 2 by liquid-differential method 3 讨论与结论 通过将GI5250安培检测器和进口仪器相互串联等实验得到GI5000离子色谱系统的检出限和定量限约为全进口仪器的3~4倍,其原因是GI5250安培检测器自身性能与进口检测器存在差距,并且进口泵在稳定输出流动相上优于国产泵。后续需要针对国产安培检测器和泵性能进一步优化。使用GI5000离子色谱系统检测饮料中糖类化合物,进行了方法学测试,对比了全进口Thermo ICS 5000+仪器的检测结果,验证了GI5000离子色谱系统在检测糖类化合物方面的性能。结果显示,5种糖类化合物在0.2~5 mgL-1范围内线性关系良好,检测的线性相关系数均在0.9990以上,重复性RSD≤2.47%,除麦芽糖外,其余四种糖检出限均在0.1 mg L-1以内,麦芽糖检出限为0.105 mgL-1。NY/T 3902-2021标准中葡萄糖的检出限为0.4 mg L-1、果糖和麦芽糖的检出限为1.2 mgL-1、蔗糖的检出限为0.6 mgL-1,表明GI5000离子色谱系统所测得的结果,均能够满足上述相关标准的要求,可满足日常实验室检测需求。以市面上售卖的可口可乐为样品,对5种糖类化合物进行加标回收实验,5种糖类化合物的加标回收率范围为94.13%~114.2%。相对标准偏差在0.22%~4.14%。测得可口可乐中的5种糖类化合物总量为10.34 g/100 g。分别使用全进口仪器Thermo ICS-5000+、GI5000离子色谱系统以及Dionex Ultimate 3000液相色谱仪检测了脉动和茶π饮料中糖类化合物的含量,三种方法检测的结果几乎一致,证明了GI5000离子色谱系统性能的可靠。 参考文献 佚名. 碳水化合物—化学结构. 淀粉与淀粉糖, 2010(2): 36-44. ZHANG Z, KHAN N M, NUNEZ K M, et al. Complete monosaccharide analysis by high-performance anion-exchange chromatography with pulsed amperometric detection. Analytical Chemistry, 2012, 84(9): 4104-4110.DOI:10.1021/ac300176z. 岳虹, 赵贞, 刘丽君, 李翠枝, 邵建波.高效液相色谱法测定发酵乳饮料中果糖、葡萄糖、蔗糖、麦芽糖及乳糖含量.乳业科学与技术, 2017, 040(002): 23-26. 樊宏, 陈强. 乳制品中乳糖直接比色测定方法探讨. 中国卫生检验杂志, 2006, 16(3): 296-297. 钟宁, 侯彩云. 三种乳糖检测方法的比较. 食品科技, 2011, 36(7): 263-265. 中华人民共和国卫生部. GB/T 5009.7—2003 食品中还原糖的测定. 北京: 中国标准出版社, 2003. Zhang J L, Dai X, Song Z L, Han R, Ma L Z, Fan G C, Luo X L,One-pot enzyme- and indicator-free colorimetric sensing of glucose based on MnO2 nano-oxidizer, Sensors and Actuators B: Chemical, 2020, 304. ZIELINSKI A A F, BRAGA C M, DEMIATE M I, et al. Development and optimization of a HPLC-RI method for the determination of major sugars in apple juice and evaluation of the effect of the ripening stag. Food Science and Technology, 2013, 34(1): 38-43. DOI:10.1590/S0101-20612014005000003. SHANMUGAVELAN P, KIM S Y, KIM J B, et al. Evaluation of sugar content and composition in commonly consumed Korean vegetables, fruits, cereals, seed plants, and leaves by HPLC-ELSD. Carbohydrate Research, 2013, 380(20): 112-117. DOI:10.1016/j.carres.2013.06.024. MA C M, SUN Z, CHEN C B, et al. Simultaneous separation and determination of fructose, sorbitol, glucose and sucrose in fruits by HPLC-ELSD. Food Chemistry, 2014, 145: 784-788. DOI:10.1016/j.foodchem.2013.08.135. WU X D, JIANG W, LU J J, et al. Analysis of the monosaccharide composition of water-soluble polysaccharides from Sargassum fusiforme by high performance liquid chromatography/electrospray ionisation mass spectrometry. Food Chemistry, 2014, 145: 976-983. DOI:10.1016/j.foodchem.2013.09.019. BAI W D, FANG X D, ZHAO W H, et al. Determination of oligosaccharides and monosaccharides in Hakka rice wine by precolumn derivation high-performance liquid chromatography.Journal of Food Drug Analysis, 2015, 23: 645-651. DOI:10.1016/j.jfda.2015.04.011. HE J Z, XU Y Y, CHEN H B, et al. Extraction, structural characterization, and potential antioxidant activity of the polysaccharides from four seaweeds. International Journal of Molecular Medicine, 2016, 17(12): 1-17. DOI:10.3390/ijms17121988. DANIEL D, LOPES F S, SANTOS V B D, et al. Detection of coffee adulteration with soybean and corn by capillary electrophoresistandem mass spectrometry. Food Chemistry, 2018, 243: 305-310. DOI:10.1016/j.foodchem.2017.09.140. 张欢欢, 李疆, 赵珊, 等. 毛细管区带电泳-间接紫外检测法快速测定食品中乳糖、蔗糖、葡萄糖和果糖. 色谱, 2015, 33(8): 816-821. 马海宁, 华玉娟, 屠春燕, 等. 毛细管电泳法分析藏红花植物细胞多糖中单糖组成. 色谱, 2012, 30(3): 304-308. DOI:10.3724/SP.J.1123.2011.11015. LV X Y, GUO Y X, ZHUANG Y P, et al. Optimization and validation of an extraction method and HPAEC-PAD for determination of residual sugar composition in L-lactic acid industrial fermentation broth with a high salt content. Analytical Methods, 2015, 7: 9076-9083. DOI:10.1039/c5ay01703c. WANG X, XU Y, LIAN Z N, et al. A one-step method for the simultaneous determination of five wood monosaccharides and the corresponding aldonic acids in fermentation broth using highperformance anion-exchange chromatography coupled with a pulsed amperometric detector. Journal of Wood Chemistry and Technology, 2013, 34(1): 67-76. DOI:10.1080/02773813.2013.838268. ZHANG Y, WU J R, NI Q H, et al. Multicomponent quantification of astragalus residue fermentation liquor using ion chromatographyintegrated pulsed amperometric detection. Experimental and Therapeutic Medicine, 2017, 14: 1526-1530. DOI:10.3892/.2017.4673. Young C S . Evaporative light scattering detection methodology for carbohydrate analysis by HPLC.. Cereal Foods World, 2002, 47(1):14-16. 梁亚丽, 张彦玲, 何颖娜. 糖类化合物分离分析方法进展. 河北化工, 2006, (06): 42-44. 梁智安, 王成龙, 龙飞. 液相色谱示差折光法测定酒中的总糖和还原糖.食品安全质量检测学报, 2018, 9(09): 2188-2194. 陈琴呜, 刘文英. HPLC—ELSD在中药糖类分析中的应用. 中草药, 2008, 39(6): 955-957. BAI W D, FANG X D, ZHAO W H, et al. Determination of oligosaccharides and monosaccharides in Hakka rice wine by precolumn derivation high-performance liquid chromatography.Journal of Food Drug Analysis, 2015, 23: 645-651. DOI:10.1016/j.jfda.2015.04.011. HE J Z, XU Y Y, CHEN H B, et al. Extraction, structural characterization, and potential antioxidant activity of the polysaccharides from four seaweeds. International Journal of Molecular Medicine, 2016, 17(12): 1-17. DOI:10.3390/ijms17121988. INDORF C, BODé S, BOECKX P, et al. Comparison of HPLC methods for the determination of amino sugars in soil hydrolysates. Analytical Letters, 2013, 46: 2145-2164. DOI:10.1080/00032719.2013.796558. 水果、蔬菜及其制品中阿拉伯糖、半乳糖、葡萄糖、果糖、麦芽糖和蔗糖的测定 离子色谱法:NY/T 3902-2021. 2021.
[b][/b][align=center][b]脉冲安培检测器之自主研制的金电极性能测试[/b][/align][b]前言[/b][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-脉冲安培法是近年发展起来的一种糖类物质分析方法,糖类经高效阴离子交换色谱柱分离后在脉冲安培检测器的金电极表面发生氧化反应,引起电流变化而被检测,避免了衍生过程。该方法具有选择性好、灵敏度和准确度高的优势。影响安培检测器分析准确性的因素很多,金电极、参比电极、检测池体和垫片等。根据经验得知其中影响最大的还要数金电极。本文对自主研制的金电极进行性能测试,并将其与Thermo进口金电极进行比对。[b]1 实验部分1.1 仪器与试剂[/b]Thermo ICS5000+ 型[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],包括单元四元梯度泵,AS-AP自动进样器,DC模块含安培检测器,Chromeleon 6.80色谱工作站;色谱柱为Dionex CarboPac PA10(4×250 mm);Thermo金电极,自主研制的第四批金电极(4-1,4-3,4-4)。乳糖,阿拉丁试剂有限公司;50% NaOH(w/w),分析纯,德国Merck公司。[b]1.2 溶液的配制[/b]1.2.1 乳糖标准溶液的配制精确称取10.0 mg乳糖标准品于50 mL容量瓶中,用超纯水溶解定容,配制得到200 mg/L标准储备液,稀释得到10 mg/L的乳糖标准溶液。1.2.2 NaOH溶液的配制称取81.09 g 50%NaOH(w/w)于2.0 L PP淋洗液瓶中,加超纯水到2000 mL,摇匀,所得溶液的浓度约为500 mmol/L。[b]1.3 色谱条件[/b]淋洗液:A 超纯水(50%),B 500 mmol/LNaOH溶液(50%),流速为1.0 mL/min等度淋洗;波形:糖四电位电位;进样量:25 μL。[b]2 结果与讨论[/b]金电极专用于[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]测定糖,从2018年5月开始,请国内主要专业电极生产厂家定制,但都无法满足实验需求,自己生产了三批只有一批可用,但寿命不长,稳定性差,还是不能满足实际检测需要。国内几乎都是制作圆盘电极,方形电极无人会制作,在无数次的失败后,对电极的结构和性能进行系统分析,设计了全新的制作方式,经过一年半的实验,终于制作出与进口电极性能相当的金电极。实验分别采用Thermo进口金电极、4-1、4-3和4-4金电极作为安培检测器的工作电极参与氧化还原反应,测定10 mg/L的乳糖标准溶液。每个电极每次测定8次,根据峰面积的大小和重复性及噪音的大小来评估不同电极的性能。并且每隔2-4天对金电极进行检测,根据日间的峰面积偏差对其稳定性及耐用性进行评测。每次单个电极测试完后,采用施氏安培使用宝典的方法进行保存和维护。检测结果如表1所示。[align=left] [/align][align=center]表1 不同金电极测定10 ppm乳糖的检测结果[/align][align=center] [/align] [table=0][tr][td] [align=center]金电极[/align] [/td][td=4,1] [align=center]Thermo[/align] [/td][td=4,1] [align=center]4-1[/align] [/td][/tr][tr][td] [align=center]时间[/align] [/td][td] [align=center]峰面积/nC*min[/align] [/td][td] [align=center]RSD(n=8)[/align] [/td][td] [align=center]噪音/nC[/align] [/td][td] [align=center]背景/nC[/align] [/td][td] [align=center]峰面积/nC*min[/align] [/td][td] [align=center]RSD(n=8)[/align] [/td][td] [align=center]噪音/nC[/align] [/td][td] [align=center]背景/nC[/align] [/td][/tr][tr][td] [align=center]9月26日[/align] [/td][td] [align=center]39.8943[/align] [/td][td] [align=center]0.70%[/align] [/td][td] [align=center][color=red]0.2700[/color][/align] [/td][td] [align=center][color=black]16[/color][/align] [/td][td] [align=center]47.6906[/align] [/td][td] [align=center]0.14%[/align] [/td][td] [align=center]0.0278[/align] [/td][td] [align=center][color=black]22.4[/color][/align] [/td][/tr][tr][td] [align=center]9月28日[/align] [/td][td] [align=center]43.8591[/align] [/td][td] [align=center]1.08%[/align] [/td][td] [align=center]0.0338[/align] [/td][td] [align=center][color=black]16.8[/color][/align] [/td][td] [align=center]49.2144[/align] [/td][td] [align=center]0.04%[/align] [/td][td] [align=center]0.0256[/align] [/td][td] [align=center][color=black]22.2[/color][/align] [/td][/tr][tr][td] [align=center]9月30日[/align] [/td][td] [align=center]42.2816[/align] [/td][td] [align=center]0.62%[/align] [/td][td] [align=center]0.0299[/align] [/td][td] [align=center][color=black]17.3[/color][/align] [/td][td] [align=center]47.2476[/align] [/td][td] [align=center]0.08%[/align] [/td][td] [align=center]0.0203[/align] [/td][td] [align=center][color=black]22[/color][/align] [/td][/tr][tr][td] [align=center]10月3日[/align] [/td][td] [align=center]39.3699[/align] [/td][td] [align=center]0.73%[/align] [/td][td] [align=center]0.0996[/align] [/td][td] [align=center][color=black]19.4[/color][/align] [/td][td] [align=center]46.2975[/align] [/td][td] [align=center]0.10%[/align] [/td][td] [align=center]0.0296[/align] [/td][td] [align=center][color=black]22[/color][/align] [/td][/tr][tr][td] [align=center]10月6日[/align] [/td][td] [align=center]38.7942[/align] [/td][td] [align=center]0.79%[/align] [/td][td] [align=center][color=red]0.2366[/color][/align] [/td][td] [align=center][color=black]15.6[/color][/align] [/td][td] [align=center]46.3227[/align] [/td][td] [align=center]0.05%[/align] [/td][td] [align=center]0.0200[/align] [/td][td] [align=center][color=black]19.2[/color][/align] [/td][/tr][tr][td] [align=center]10月10日[/align] [/td][td] [align=center]38.0609[/align] [/td][td] [align=center]0.57%[/align] [/td][td] [align=center]0.1683[/align] [/td][td] [align=center][color=black]16.4[/color][/align] [/td][td] [align=center]45.1849[/align] [/td][td] [align=center]0.28%[/align] [/td][td] [align=center]0.0194[/align] [/td][td] [align=center][color=black]17.8[/color][/align] [/td][/tr][tr][td] [align=center]10月15日[/align] [/td][td] [align=center]36.4223[/align] [/td][td] [align=center]0.30%[/align] [/td][td] [align=center]0.1390[/align] [/td][td] [align=center][color=black]14.2[/color][/align] [/td][td] [align=center]44.9905[/align] [/td][td] [align=center]0.57%[/align] [/td][td] [align=center]0.0295[/align] [/td][td] [align=center][color=black]16.6[/color][/align] [/td][/tr][tr][td] [align=center]平均值[/align] [/td][td] [align=center]39.8118[/align] [/td][td] [align=center]0.69%[/align] [/td][td] [align=center]0.1396[/align] [/td][td] [align=center][color=black]16.5286[/color][/align] [/td][td] [align=center]46.7069[/align] [/td][td] [align=center]0.18%[/align] [/td][td] [align=center]0.0246[/align] [/td][td] [align=center][color=black]20.3143[/color][/align] [/td][/tr][tr][td] [align=center]日间RSD[/align] [/td][td] [align=center][b]6.34%[/b][/align] [/td][td] [align=center][b] [/b][/align] [/td][td] [align=center] [/align] [/td][td] [align=center][b] [/b][/align] [/td][td] [align=center][b]3.17%[/b][/align] [/td][td] [align=center] [/align] [/td][td] [align=center] [/align] [/td][td] [align=center] [/align] [/td][/tr][/table] [table=0][tr][td] [align=center]金电极[/align] [/td][td=4,1] [align=center]4-3[/align] [/td][td=4,1] [align=center]4-4[/align] [/td][/tr][tr][td] [align=center]时间[/align] [/td][td] [align=center]峰面积/nC*min[/align] [/td][td] [align=center]RSD(n=8)[/align] [/td][td] [align=center]噪音/nC[/align] [/td][td] [align=center]背景/nC[/align] [/td][td] [align=center]峰面积/nC*min[/align] [/td][td] [align=center]RSD(n=8)[/align] [/td][td] [align=center]噪音/nC[/align] [/td][td] [align=center]背景/nC[/align] [/td][/tr][tr][td] [align=center]9月26日[/align] [/td][td] [align=center]44.5527[/align] [/td][td] [align=center]0.19%[/align] [/td][td] [align=center]0.0353[/align] [/td][td] [align=center][color=black]37.2[/color][/align] [/td][td] [align=center]45.0656[/align] [/td][td] [align=center]0.30%[/align] [/td][td] [align=center]0.0524[/align] [/td][td] [align=center][color=black]38.2[/color][/align] [/td][/tr][tr][td] [align=center]9月28日[/align] [/td][td] [align=center]44.6819[/align] [/td][td] [align=center]0.17%[/align] [/td][td] [align=center]0.0251[/align] [/td][td] [align=center][color=black]36.4[/color][/align] [/td][td] [align=center]43.8768[/align] [/td][td] [align=center]0.43%[/align] [/td][td] [align=center]0.0353[/align] [/td][td] [align=center][color=black]35.4[/color][/align] [/td][/tr][tr][td] [align=center]9月30日[/align] [/td][td] [align=center]44.1855[/align] [/td][td] [align=center]0.21%[/align] [/td][td] [align=center]0.0301[/align] [/td][td] [align=center][color=black]37.4[/color][/align] [/td][td] [align=center]45.8564[/align] [/td][td] [align=center]0.17%[/align] [/td][td] [align=center]0.0349[/align] [/td][td] [align=center][color=black]33.8[/color][/align] [/td][/tr][tr][td] [align=center]10月3日[/align] [/td][td] [align=center]44.3116[/align] [/td][td] [align=center]0.13%[/align] [/td][td] [align=center]0.0261[/align] [/td][td] [align=center][color=black]33.6[/color][/align] [/td][td] [align=center]45.6930[/align] [/td][td] [align=center]0.12%[/align] [/td][td] [align=center]0.0460[/align] [/td][td] [align=center][color=black]33.8[/color][/align] [/td][/tr][tr][td] [align=center]10月6日[/align] [/td][td] [align=center]44.1716[/align] [/td][td] [align=center]0.12%[/align] [/td][td] [align=center]0.0135[/align] [/td][td] [align=center][color=black]34.6[/color][/align] [/td][td] [align=center]44.4248[/align] [/td][td] [align=center]1.18%[/align] [/td][td] [align=center]0.0254[/align] [/td][td] [align=center][color=black]30.5[/color][/align] [/td][/tr][tr][td] [align=center]10月10日[/align] [/td][td] [align=center]44.6800[/align] [/td][td] [align=center]0.20%[/align] [/td][td] [align=center]0.0194[/align] [/td][td] [align=center][color=black]33.4[/color][/align] [/td][td] [align=center]44.2642[/align] [/td][td] [align=center]0.13%[/align] [/td][td] [align=center]0.0211[/align] [/td][td] [align=center][color=black]26.8[/color][/align] [/td][/tr][tr][td] [align=center]10月15日[/align] [/td][td] [align=center]44.0805[/align] [/td][td] [align=center]0.18%[/align] [/td][td] [align=center]0.0360[/align] [/td][td] [align=center][color=black]33.8[/color][/align] [/td][td] [align=center]43.6248[/align] [/td][td] [align=center]0.62%[/align] [/td][td] [align=center]0.0454[/align] [/td][td] [align=center][color=black]28.6[/color][/align] [/td][/tr][tr][td] [align=center]平均值[/align] [/td][td] [align=center]44.3805[/align] [/td][td] [align=center]0.17%[/align] [/td][td] [align=center]0.0249[/align] [/td][td] [align=center][color=black]35.2000[/color][/align] [/td][td] [align=center]44.6865[/align] [/td][td] [align=center]0.42%[/align] [/td][td] [align=center]0.0372[/align] [/td][td] [align=center][color=black]32.4429[/color][/align] [/td][/tr][tr][td] [align=center]日间RSD[/align] [/td][td] [align=center][b]0.57%[/b][/align] [/td][td] [align=center] [/align] [/td][td] [align=center] [/align] [/td][td] [align=center][b] [/b][/align] [/td][td] [align=center][b]1.95%[/b][/align] [/td][td] [align=center] [/align] [/td][td] [align=center] [/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center] [/align][align=left] [/align][align=left]由检测结果可得,四个金电极单日内的进样重复性良好,RSD均小于等于1.18%,且峰面积差距不大,在40-50 nC*min范围内,说明这批金电极的检测灵敏度良好。[/align][align=left]经过共七次不同天的测试,20天中,四个金电极的峰面积日间偏差分别为6.34%,3.17%,0.57%,1.95%,其中Thermo金电极的偏差最大为6.34%,自主研制的三个金电极的日间偏差均小于3.17%,说明这批金电极的性能优异接下去对其进行更持久的测试,确保该批电极能长时间使用。[/align][align=left]从噪音来看,其中Thermo金电极的噪音较大,且最大达到0.27nC,而自主研制的三个金电极的噪音大致范围在0.01-0.06nC,并且从背景来看,这四个金电极的背景都在合理范围内波动,说明自主研制的金电极性能优异。[/align][align=left]进口Thermo金电极的日间偏差和噪音都较大,推测因为该金电极之前使用过很长一段时间,不是新电极,表面已被污染,故而导致其检测重复性不够,且不够稳定。[/align][align=left] [/align][b]3 结论[/b][align=left]经过多次失败,一年半的不断地改良,这次这批金电极的性能优异,不论是日内偏差还是日间偏差都很小,并且噪音也很小,灵敏度高,各方面性能都可以与进口的金电极匹敌,自主研制出替代进口金电极的国产金电极接近成功。[/align]
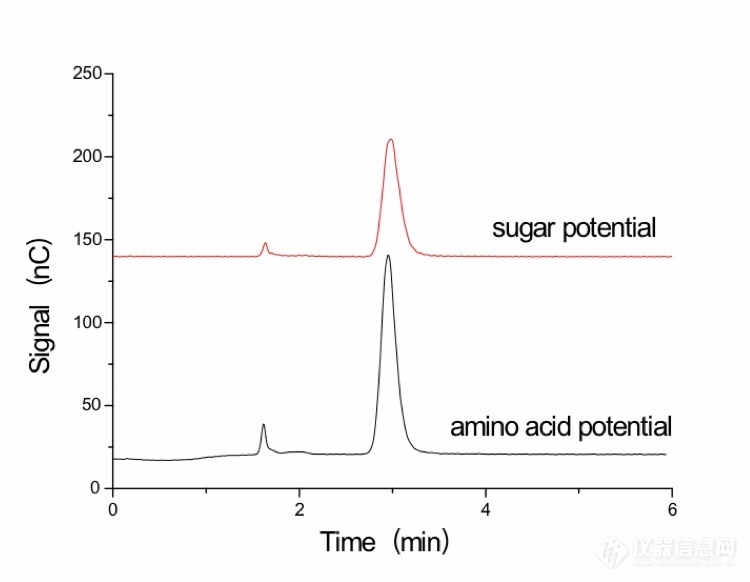
[align=center][b][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-积分脉冲安培法检测阿立哌唑中残留三乙胺[/b][/align][b]摘要[/b]目的:建立测定阿立哌唑原料药中三乙胺残留量的新方法。方法:采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-积分脉冲安培法。采用阳离子交换柱,以30 mmol/L甲烷磺酸为淋洗液,流速1.0 mL/min;柱后补液为500 mmol/L NaOH溶液,流速0.2 mL/min;波形为氨基酸电位。结果:三乙胺在0.1322-1.322 mg/L范围内线性关系良好(R[sup]2[/sup]=0.9994),加标回收率在101.7%~105.9%之间,RSD为1.85%(n=6)。结论:建立的方法准确、可靠、灵敏度高,适用于测定阿立哌唑原料药中三乙胺的残留量分析。[b]关键词[/b][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url];积分脉冲安培;阿立哌唑;三乙胺阿立哌唑(aripiprazole),化学名为7-{4--丁氧基}-3,4-二氢-2(1H)喹啉酮,是日本Otsuka公司开发的新型非典型抗精神病药,临床主治各种急、慢性精神分裂症和情感障碍[sup][/sup]。阿立哌唑的合成路线较多[sup][/sup],在合成过程中曾用到三乙胺,因此产品中有可能会残留微量的基因毒性杂质三乙胺,由于三乙胺具有助溶和轻度的防腐作用,因此对三乙胺残留量的监测是阿立哌唑药物质量控制过程中必不可少的一部分。目前三乙胺已收载于人用药品注册技术要求国际协调会(ICH),Q3C(R6)中[sup][/sup],规定其限度为500mg/Kg,欧洲药品质量管理局(EDQM)也规定其残留限度为320mg/Kg。通常,三乙胺采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[sup][/sup]和溴酚蓝分光光度法[sup][/sup]进行测定。有不少人采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]检测乙醇胺、二甲胺等胺类[sup][/sup],但用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]测定三乙胺很少见。李向春[sup][/sup]等采用Dionex IonPac CS17色谱柱,MSA 6mM等度淋洗,采用CSR循环再生电抑制模式测定了草甘膦合成工艺中的三乙胺。上述方法中检出限最低的为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,可达约48 mg/kg。但阿立哌唑中残留的三乙胺含量很低,采用上述方法灵敏度不够,且阿立哌唑中主体干扰较大,无法满足要求。潘思[sup][/sup]等采用柱后衍生[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-脉冲安培法来测定盐酸羟胺,采用Dionex IonPac CS16 (4×250 mm)色谱柱,流动相是30 mmol/L甲磺酸溶液,流速为1.0 ml/min;衍生剂为500 mmol/L氢氧化钠,流速为0.3 ml/min,该方法检测限为0.012 mgL[sup]-1[/sup],定量限为0.037 mgL[sup]-1[/sup]。因此本文借鉴该方法来测定三乙胺的含量,并对淋洗液浓度及流速、柱后补液的浓度及流速、电位波形进行优化,通过考察其线性关系、精密度、稳定性来验证方法的可行性。[b]1实验部分1.1 仪器与试剂[/b]Thermo ICS5000+ 型[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],包括单元四元梯度泵,AS-AP自动进样器,DC模块含安培检测器,Chromeleon 6.80色谱工作站;色谱柱为Dionex IonPac CS17 (4×250 mm),保护柱为Dionex IonPac CG17(4×50 mm); Mettler Toledo AL204型电子分析天平;Millipore-Q Advantage A10型超纯水机。三乙胺(99.5%),盘锦研峰科技有限公司;甲烷磺酸(99.5%),阿拉丁试剂有限公司;50% NaOH(w/w),分析纯,德国Merck公司; OnGuard[sup]TM [/sup]RP柱(1 cc),美国Thermo公司;阿立哌唑供试品(1[sup]#[/sup],2[sup]#[/sup],3[sup]#[/sup]),某药厂提供。[b]1.2 溶液的配制[/b]1.2.1 三乙胺标准溶液的配制精确称取66.1 mg三乙胺标准品于50 mL容量瓶中,用30 mmol/L MSA淋洗液溶解定容,配制得到132 2 mg/L标准储备液,稀释得到26.44 mg/L的标准溶液。再逐级用淋洗液稀释得到浓度分别为1.322 mg/L、0.661 0 mg/L、0.440 7 mg/L、0.264 4 mg/L、0.132 2 mg/L的三乙胺系列储备液。1.2.2 甲烷磺酸淋洗液溶液的配制称取19.28 g 甲烷磺酸于2.0 L PP淋洗液瓶中,加超纯水到2000 mL,摇匀,所得溶液的浓度约为100 mmol/L。1.2.3 NaOH溶液的配制称取81.09 g 50%NaOH(w/w)于2.0 L PP淋洗液瓶中,加超纯水到2000 mL,摇匀,所得溶液的浓度约为500 mmol/L。1.2.4 实际样品溶液的配制称取50.1 mg 阿立哌唑供试品于25 mL容量瓶中,准确加入10 mL乙腈,置于50℃水浴中溶解,摇匀,随后准确加入10 mL超纯水,置于冰箱中冷藏60分钟后取出,阿立哌唑会以沉淀形式析出。静置后离心,取上清液用经活化的RP柱(活化方式:先用5 mL甲醇对RP柱进行冲洗,放置30 min后,用10 mL超纯水进行冲洗,备用)进行过滤,先丢弃最初的3 mL,取滤液即得浓度约为2500 mg/L的供试品溶液。[b]1.3 色谱条件[/b]淋洗液:A 超纯水(70%),B 100 mmol/L甲烷磺酸(30%),流速为1.0 mL/min,等度淋洗;柱后补液:500 mmol/L NaOH溶液,流速为0.2 mL/min;波形:氨基酸电位;进样量:25 μL;柱后衍生管:375μL。[b]2 结果与讨论2.1 色谱条件的确定[/b]2.1.1 淋洗液浓度的选择实验选取20 mmol/L、25 mmol/L、30 mmol/L的甲烷磺酸溶液作为淋洗液分别测定1.322 mg/L的三乙胺标样,检测结果显示其保留时间分别为3.567min、3.189min、2.953min,峰高分别为47.31 nC、103.7 nC、119.8 nC。表明30 mmol/L的淋洗液灵敏度最高,且保留时间适宜。若使用更高浓度的甲烷磺酸溶液作为淋洗液,则三乙胺的保留时间会更短,但可能存在与其他快出峰杂质分离度变差,影响定量。因此选取30 mmol/L的甲烷磺酸溶液作为实验的淋洗液。2.1.2 检测电位的选择伯胺的有机化合物,在碱性条件下,用金电极采用糖电位和氨基酸电位都有较高的响应。糖电位为脉冲安培检测,氨基酸电位为积分安培检测,脉冲安培检测在一个脉冲周期中对电流积分所施加的电位是单一的,它存在一个短暂的间歇以使充电电流衰减,而积分安培对工作电极施加的是一种对应时间波形的循环电位,即电极先被氧化然后再被还原为其原始状态。因此,在CS17柱分离后,用NaOH补液调节pH到碱性。选取糖电位和氨基酸电位这两种波形分别测定1.322 mg/L的三乙胺标样,结果如图1。从图1可以看出,二者的噪音差别不大,且氨基酸电位波形的响应值高,因此选取氨基酸电位波形作为实验的波形。[align=center][img=,690,535]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312150078580_1354_3426139_3.jpg!w690x535.jpg[/img][/align][align=center][b]图1 电位波形的影响[/b][/align][align=center]Fig.1 Effect of potential waveform[/align]2.1.3 柱后补液流速的选择实验选取氨基酸电位波形的柱后补碱NaOH溶液的0.2 mL/min、0.3 mL/min流速分别测定1.322 mg/L的三乙胺标样,结果如图2。从图2可以看出,氨基酸电位波形时,0.2 mL/min柱后补碱NaOH溶液的响应值高于0.3 mL/min柱后补碱NaOH溶液。若柱后补液流速到0.1ml/min,由于淋洗液为酸,补液为强碱,过低的补液流速和淋洗液的混合效果不好,且流量精度会降低,导致噪音变大。因此实验选择柱后补碱NaOH溶液流速为0.2 mL/min。[align=center][img=,690,531]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312150354680_6766_3426139_3.jpg!w690x531.jpg[/img][/align][align=center][b]图2 柱后补液流速的影响[/b][/align][align=center]Fig.2 Effect of post-column rehydration flow rate[/align][b]2.2 方法学验证[/b]2.2.1 线性关系、检出限和定量限本实验考察0.132 2-1.322 mg/L 范围内三乙胺的线性关系。待仪器稳定后,将配制的标准系列溶液由低浓度到高浓度顺序依次进样,平行测定三次,计算峰面积并取平均值。结果表明,三乙胺的线性关系良好,回归方程为y=1.076x+0.344 5,R2为0.999 4。三乙胺检测方法的检出限浓度为0.045 mg/L,相当于样品检出限含量为18.2 mg/kg,定量限浓度为0.15 mg/L,相当于样品的定量限含量为60.7 mg/kg。2.2.2 标准溶液进样重复性取三乙胺测定线性关系中浓度为0.661 0 mg/L的标准溶液作为进样重复性溶液,连续测定6次,记录峰面积。结果显示测得三乙胺峰面积的RSD为1.9 %(n=6),说明该分析方法较稳定,具有较好的进样重复性。2.2.3 实际样品分析取三批供试品,配制好实际样品溶液(约2500 mg/L),按上述色谱条件,对实际阿立哌唑样品进行检测,色谱图见图3。从图3中可以看出,阿立哌唑供试品中未检测到三乙胺毒性杂质,小于18.2 mg/kg。[align=center][img=,690,478]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312150529972_3514_3426139_3.jpg!w690x478.jpg[/img][/align][align=center][b]图3 实际样品色谱图[/b][/align][align=center]Fig.3 Chromatogram of the actual sample[/align]2.2.4 加标回收实验对供试品1[sup]#[/sup]中成分三乙胺进行回收率实验。精密量取2.5 mL浓度为2500 mg/L的实际样品溶液分别置于5 mL容量瓶中,分别精密加入2.5 mL浓度为1.322 mg/L、0.661 0 mg/L、0.440 7 mg/L的对照品储备液,混合均匀。在上述色谱条件下进样测定,每个浓度平行测定三次,回收率结果见表1。从表1中可以看出,样品不同水平加标回收率在101.7%~105.9%之间,说明该检测方法可信度较高。[align=center][b]表1 样品加标回收率[/b][/align][align=center]Table 1 Results ofrecovery tests for sample[/align] [table=657][tr][td] [align=center]化合物[/align] [align=center](compound)[/align] [/td][td] [align=center]样品含量[/align] [align=center](sample amount)/( mg/L)[/align] [/td][td] [align=center]加标量[/align] [align=center](addition)/( mg/L)[/align] [/td][td] [align=center]检测量[/align] [align=center](measured amount)/( mg/L)[/align] [/td][td] [align=center]回收率[/align] [align=center](recovery)/%[/align] [/td][/tr][tr][td=1,3] [align=center]三乙胺(Triethylamine)[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]0.066 1[/align] [/td][td] [align=center]0.070 0[/align] [/td][td] [align=center]105.9[/align] [/td][/tr][tr][td] [align=center]-[/align] [/td][td] [align=center]0.132 2[/align] [/td][td] [align=center]0.134 4[/align] [/td][td] [align=center]101.7[/align] [/td][/tr][tr][td] [align=center]-[/align] [/td][td] [align=center]0.220 4[/align] [/td][td] [align=center]0.232 4[/align] [/td][td] [align=center]105.4[/align] [/td][/tr][/table][align=center][/align][b]3 结论[/b]上述实验结果表明,采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-安培法,在30 mmol/L的甲烷磺酸溶液淋洗液,流速为1 mL/min,柱后补碱为500 mmol/L的NaOH溶液,流速为0.2 mL/min,氨基酸电位波形的色谱条件下,能准确地分析阿立哌唑中基因毒性杂质三乙胺的残留量,最低检出限为18.2 mg/kg,灵敏度高,满足药典的要求,该方法准确度、精密度和稳定性较好。在阿立哌唑的质量控制中,该方法对三乙胺残留量的控制有重大意义。[b]参考文献:[/b] Zhang P, Li Z D, Jiao Z. Second generation atypical antipsychoticdrug aripiprazole. Chin Pharm J, 2005, 40(3): 238-240.张璞,李中东,焦正.第二代非典型抗精神病药一阿立哌唑. 中国新药杂志,2005,40(3):238-240. Wu C Y, Zhu Y C. Synthesis ofaripiprazole. Chin J Mod Drug Appl, 2010, 4(1): 11-12.吴春艳,朱永超. 阿立哌唑的合成 . 中国现代药物应用,2010,4(1):11-12. Li M D, Cai J, JiM. Synthesis of atypical antipsychotic new drug aripiprazole. Prog PharmSci, 2004, 28(6): 274-276.李铭东,蔡进,吉明. 非典型抗精神病新药阿立哌唑的合成.药学进展,2004,28(6):274-276. Liu X J, Wang T T,Zhong Y L, et al. Synthesis of antipsychotic aripiprazole. JShengyang Pharm Univ, 2013, 30(4): 253-255.刘秀杰,王媞媞,钟永亮,等. 抗精神病新药阿立哌唑的合成. 沈阳药科大学学报,2013,30(4):253-255. Xu J M, Wu Q Y,Zhang J, et al. Research on preparation of aripiprazole. J PharmPractice徐建明,吴秋业,张俊,等. 阿立哌唑的制备工艺研究. 药物实践杂志,2005,23(5):269-270. Ge H X, Wang L C,Ni S L. Improved Synthesis of Antipsychotic DrugAripiprazole. Chin JMAP, 2007, 24(4): 294-295.葛海霞,王礼琛,倪生良. 抗精神病药阿立哌唑的合成工艺改进. 中国现代应用药学,2007,24(4):294-295. Chen G Y, Chen X B,Liu G M, et al. Improved Synthesis of Aripiprazole. Shandong Chem Ind,2009, 38(9): 3-5.陈光勇,陈旭冰,刘光明,等. 阿立哌唑的合成工艺改进. 山东化工,2009,38(9):3-5. ICH guideline Q3C (R6 on impurities: guideline for residual solvents. (2016-12). Ma Z Q, Lu G H, YinJ J, et al. Determination of Residual Triethylamine in Rupatadine Fumarate byGas Chromatography. Guangdong Chem, 2018, 45(14): 213-214.马振千,鹿贵花,印嘉佳,等. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定富马酸卢帕他定中三乙胺的含量. 广东化工,2018,45(14):213-214. Guo J T, Yu F.Determination of Triethylamine Residue in Tetraethyl Ammonium Bromide AqueousSolution by Capillary Gas Chromatography. Guangdong Chem, 2018, 45(14):213-214.郭建亭,于飞. 毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定四乙基溴化铵水溶液中三乙胺的残留. 化学世界,2017,12:727-729. Wu W P, Ming D.Determination of Triethylamine Residues in Raw Material of Mirtazapine by GasChromatography. Yunnan Chem Tech, 2018, 45(8): 130-131.伍蔚萍,明丹. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定米氮平原料药中三乙胺残留量. 云南化工,2018,45(8):130-131. Jin Z Q.Discussion on problems of water Triethylamine determination. Tech Wind,2014, 23: 108.金梓谦. 分光光度法测定水中三乙胺有关问题探讨. 科技风,2014,23:108. Chen Z, Wang D,Zhang J N, et al. Optimization of Detection Technology for TriethylamineHydrochloride in Industrial Effluent. Salt Sci and Chem Ind J, 2019, 48(3):29-32.陈峥,王丹,张金娜,等. 工业废水中三乙胺盐酸盐检测技术的优化. 盐科学与化工,2019,48(3):29-32. Chen M S, Liang Z,Tang H Y, et al. Simultaneous determination of the migration of five alcoholamines in plastics food contact materials and articles by non-suppressed ion chromatography.AL, 2018, 37(10): 1183-1188.陈旻实,梁震,唐寰宇,等. 非抑制[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定塑料食品接触材料中五种醇胺迁移量. 分析试验室,2018,37(10):1183-1188. Fang L M, Hu M,Chen A L, et al. Determination of the residual dimethylamine in arbidolhydrochloride by ion chromatography. Chin J Pharm Anal, 2016,36(10):1852-1856.方琳美,胡咪,陈爱连,等. [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定盐酸阿比朵尔中残留的二甲胺含量. 药物分析杂志,2016,36(10):1852-1856. Li X C, Ding M M,Cai Q, et al. Determination of Triethylamine in Glyphosate Synthesis by IonChromatography. Qingdao: Proceedings of the 13th Ion Chromatography AcademicConference. 2010.李向春,丁敏敏,蔡琪,等. [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定草甘膦合成工艺中的三乙胺. 青岛:第13届[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]学术报告会论文集. 2010. Pan S, Shi C O,Liu Y M, et al. Determination of hydroxylamine hydrochloride in micafunginsodium by ion chromatography with pules amperometric detection. Anal Instru,2018(2): 58-61.潘思,施超欧,刘玉梅,等. [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-积分脉冲安培法检测米卡芬净钠中残留盐酸羟胺. 分析仪器,2018(2):58-61.
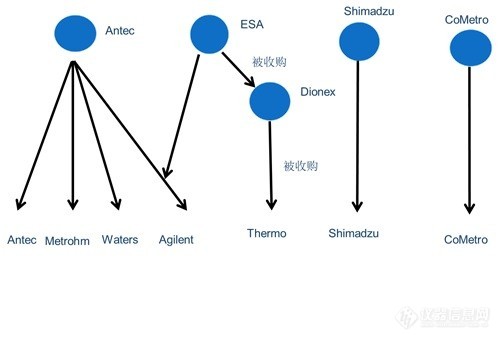
[align=left][font='Times New Roman','serif']5.3 [/font][font=宋体]安培检测器[/font][/align][align=left][font='Times New Roman','serif']5.3.1 [/font][font=宋体]安培检测器的发展历史[/font][/align][font='Times New Roman','serif']5.3.2 [/font][font=宋体]国内外主要安培检测器厂家[/font][align=left][font='Times New Roman','serif']5.3.3 [/font][font=宋体]安培检测器的原理[/font][/align][font='Times New Roman','serif']5.3.3.1 [/font][font=宋体]伏安法[/font][font='Times New Roman','serif']5.3.3.2 [/font][font=宋体]直流安培法([/font][font='Times New Roman','serif']Direct amperometric detection[/font][font=宋体],[/font][font='Times New Roman','serif']DC[/font][font=宋体])[/font][b]5.3.3.3 [font=宋体]脉冲安培法([/font]Pulsedamperometric detection, PAD[font=宋体])[/font]5.3.3.4 [font=宋体]积分安培法([/font]Integratedpulsed amperometric detection, IPAD[font=宋体])[/font]5.3.3.5 [font=宋体]迟滞时间[/font]5.3.3.6 [font=宋体]电位极限[/font][/b][font='Times New Roman','serif']5.3.4 [/font][font=宋体]安培检测器各组成的结构[/font][b]5.3.4.1 [font=宋体]安培池的结构[/font]5.3.4.2 [font=宋体]热电(戴安)安培检测器(池)的结构[/font][/b][font='Times New Roman','serif']5.3.4.3 [/font][font=宋体]万通安培检测器(池)的结构[/font][font='Times New Roman','serif']5.3.4.4 Antec [/font][font=宋体]安培检测器(池)的结构[/font][font='Times New Roman','serif']5.3.4.5 [/font][font=宋体]工作电极[/font][font='Times New Roman','serif']5.3.4.6 [/font][font=宋体]参比电极[/font][font='Times New Roman','serif']5.3.4.7 [/font][font=宋体]膜片[/font][font='Times New Roman','serif']5.3.5 [/font][font=宋体]薄层式安培池检测响应的关系[/font][font='Times New Roman','serif']5.3.6[/font][font=宋体]安培检测器的应用[/font][b]5.3.6.1 [font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]直流安培检测技术([/font]IC-CP[font=宋体])[/font]5.3.6.2 [font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]脉冲安培检测技术([/font]IC-PAD[font=宋体])[/font]5.3.6.3[font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]积分脉冲安培检测技术([/font]IC-IPAD[font=宋体])[/font]5.3.7 [font=宋体]安培检测器各部件的使用和维护[/font]5.3.7.1 [font=宋体]热电安培检测器的使用和维护[/font]5.3.7.2 [font=宋体]万通安培检测器的使用和维护[/font]5.3.8 [font=宋体]安培检测器的故障判断和注意事项[/font][font=宋体][/font][font=宋体][/font][/b][align=left][font='Times New Roman','serif']5.3.1 [/font][font=宋体]安培检测器的发展历史[/font][/align][font=宋体]电化学检测的起源可追溯到[/font][font='Times New Roman','serif']20[/font][font=宋体]世纪初,当时为了发展碳氢燃料,研究了对污染的贵金属电极的再活化。[/font][font='Times New Roman','serif']1924[/font][font=宋体]年,[/font][font='Times New Roman','serif']Hammett[/font][font=宋体]等[/font][sup][font='Times New Roman','serif'][15][/font][/sup][font=宋体]首先对[/font][font='Times New Roman','serif']Pt[/font][font=宋体]电极施加脉冲电势对其进行清洗。[/font][font='Times New Roman','serif']Armstrong[sup][16][/sup][/font][font=宋体]在[/font][font='Times New Roman','serif']1934[/font][font=宋体]年分别将脉冲电位用于[/font][font='Times New Roman','serif']H[sub]2[/sub][/font][font=宋体]的阳极氧化和[/font][font='Times New Roman','serif']O[sub]2[/sub][/font][font=宋体]的阴极还原。[/font][font='Times New Roman','serif']Kolthoff[/font][font=宋体]和[/font][font='Times New Roman','serif']Tanaka[sup][17][/sup][/font][font=宋体]研究了在多种支持电解质作用下的[/font][font='Times New Roman','serif']Pt[/font][font=宋体]电极的极化曲线,为以后通过电位氧化和还原脉冲对电极进行再活化的研究工作奠定了基础。随着[/font][font='Times New Roman','serif']IC[/font][font=宋体]在上世纪七十年代的发展,刺激了贵金属电极表面脉冲电位再活化的发展。[/font][font='Times New Roman','serif']1981[/font][font=宋体]年,爱荷华州立大学的[/font][font='Times New Roman','serif']Johnson[/font][font=宋体]和他的同事以及学生们引入了脉冲安培检测([/font][font='Times New Roman','serif']PAD[/font][font=宋体]),用于测定流动注射系统中[/font][font='Times New Roman','serif']Pt[/font][font=宋体]电极上的简单醇和糖类[/font][sup][font='Times New Roman','serif'][18][/font][/sup][font=宋体]。在[/font][font='Times New Roman','serif']Johnson[/font][font=宋体]和[/font][font='Times New Roman','serif'] Dionex[/font][font=宋体]公司(现为[/font][font='Times New Roman','serif']Thermo Scientific[/font][font=宋体])的共同努力下,研制出了第一台能够进行脉冲电化学检测([/font][font='Times New Roman','serif']pulsed electrochemicaldetection, PED[/font][font=宋体])的电化学检测器[/font][sup][font='Times New Roman','serif'][19][/font][/sup][font=宋体]。[/font][font='Times New Roman','serif']1983[/font][font=宋体]年,[/font][font='Times New Roman','serif']Polta[/font][font=宋体]等[/font][sup][font='Times New Roman','serif'][21][/font][/sup][font=宋体]采用脉冲安培检测器,[/font][font='Times New Roman','serif']Pt[/font][font=宋体]电极作为工作电极,[/font][font='Times New Roman','serif']NaOH[/font][font=宋体]为淋洗液,成功检测了三种氨基酸,并且灵敏度良好,甘氨酸、苯胺和羟基脯氨酸的检测限分别为[/font][font='Times New Roman','serif']13ng[/font][font=宋体]、[/font][font='Times New Roman','serif']7ng[/font][font=宋体]和[/font][font='Times New Roman','serif']23ng[/font][font=宋体]。[/font][font='Times New Roman','serif']1998[/font][font=宋体]年,[/font][font='Times New Roman','serif']Rocklin[/font][font=宋体]等[/font][sup][font='Times New Roman','serif'][22][/font][/sup][font=宋体]开发了一种采用四电位波形的脉冲安培法检测糖类,与常用的三电位波形相比,四电位波形能使工作电极即金电极由于金氧化物形成和溶解而导致的表面损耗最小化,从而提高了检测的信噪比,并且大大提高了测样的长期重现性。[/font][font='Times New Roman','serif']1989[/font][font=宋体]年,[/font][font='Times New Roman','serif']Welch[/font][font=宋体]等[/font][sup][font='Times New Roman','serif'][23][/font][/sup][font=宋体]提出了积分脉冲安培检测法([/font][font='Times New Roman','serif']IPAD[/font][font=宋体]),并将其成功应用于氨基酸的检测,[/font][font=宋体]积分安培检测可解决含[/font]N[font=宋体]、[/font]S[font=宋体]等化合物在检测过程中致使电极钝化的问题[/font][font=宋体]。[/font][font='Times New Roman','serif']Clarke[/font][font=宋体]等[/font][sup][font='Times New Roman','serif'][24][/font][/sup][font=宋体]在[/font][font='Times New Roman','serif']1999[/font][font=宋体]年通过对施加电位波形的优化,开发了一种新的不用衍生化的六电位波形检测方法检测氨基酸和氨基糖,基线非常稳定,信噪比和测样重现性都有了很大提高,并且降低了工作电极的损耗,该方法对于大多数分析物的检出限小于[/font][font='Times New Roman','serif']1 pmol[/font][font=宋体]。[/font][font=宋体]就国内而言,最早是在[/font][font='Times New Roman','serif']1985[/font][font=宋体]年南京分析仪器研究所的蒋孝忠等[/font][sup][font='Times New Roman','serif'][25][/font][/sup][font=宋体]制作了薄层流动式安培检测器,其性能良好,并且灵敏度高,成功应用于大白鼠脑组织中的儿茶酚胺类及其代谢物,检测限为[/font][font='Times New Roman','serif']10[sup]-12[/sup] g[/font][font=宋体]。[/font][font='Times New Roman','serif']1987[/font][font=宋体]年,纪华民等[/font][sup][font='Times New Roman','serif'][26][/font][/sup][font=宋体]制造了多工作电极的薄层流通式安培检测器,并且将其与液相色谱结合成功检测了五种儿茶酚胺化合物,检出限达到[/font][font='Times New Roman','serif']10 pg[/font][font=宋体]。[/font][font='Times New Roman','serif']1993[/font][font=宋体]年,吴守国等[/font][sup][font='Times New Roman','serif'][27][/font][/sup][font=宋体]研制了一种多功能安培检测器,具有壁面射流型、薄层型和工作电极串行或并行四种模式。[/font][font='Times New Roman','serif']1996[/font][font=宋体]年,上海分析仪器厂项目组金成等[/font][sup][font='Times New Roman','serif'][28][/font][/sup][font=宋体]成功研制了商品化的脉冲安培检测器[/font][font='Times New Roman','serif']XP-206PAD[/font][font=宋体],并且经过了严格的测试与试用,其性能优异,推动了我国[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]领域的发展。随后国内的科研工作者继续研制了一些新型安培检测器,如毛细管电泳柱端[/font][font='Times New Roman','serif']/[/font][font=宋体]柱上安培检测器、微安培检测器等[/font][sup][font='Times New Roman','serif'][29-32][/font][/sup][font=宋体]。[/font][font=宋体]在2010年前其中上海天美与华东师范大学合作曾成功研制一款脉冲和直流集一体的安培检测器,但后期这款安培检测器并未商品化。[/font][font=宋体]但是这些研制的安培检测器并没有得到良好的实际应用。国内商品化的安培检测器基本仍处于空白。国内[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]厂家目前能见到的是青岛普仁的伏安检测器,盛瀚的直流安培检测器,但并没有相应的使用论文发表。华东理工大学的施超欧,成功研发了脉冲安培检测器,,发表了国内第一篇全国产的脉冲安培检测器的论文[/font][font='Times New Roman','serif'][][/font][font=宋体],安徽皖仪,近日也推出了带脉冲安培检测器的高端[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url],目前还有更多的厂家在研发脉冲安培检测器。[/font][b][font=宋体][font=宋体][font='Times New Roman','serif']5.3.2 [/font][font=宋体]国内外主要安培检测器厂家[/font][font=宋体]目前商品化的安培检测器厂家不多,国外主要有荷兰的[/font][font='Times New Roman','serif']Antec[/font][font=宋体]、美国的[/font][font='Times New Roman','serif']Thermo[/font][font=宋体],瑞士[/font][font='Times New Roman','serif']Metrohm[/font][font=宋体]、美国[/font][font='Times New Roman','serif']Agilent[/font][font=宋体]、美国[/font][font='Times New Roman','serif']Waters[/font][font=宋体](其中[/font][font='Times New Roman','serif']Metrohm[/font][font=宋体]、[/font][font='Times New Roman','serif']Agilent[/font][font=宋体]、[/font][font='Times New Roman','serif']Waters OEM Antec[/font][font=宋体]的电化学检测器)、[/font][font=宋体]以及日本的[/font][font='Times New Roman','serif']Shimadzu[/font][font=宋体]等。其中荷兰的[/font][font='Times New Roman','serif']Antec[/font][font=宋体]在电化学检测器上整体实力最强,是国际著名的专业电化学检测器厂家。[/font][/font][/font][font=宋体][font=宋体][font=宋体][img=,502,341]https://ng1.17img.cn/bbsfiles/images/2021/11/202111231033388876_7732_1617661_3.jpg!w502x341.jpg[/img][/font][/font][/font][font=宋体][font=宋体][font=宋体]国外主要安培检测器厂家之间的关系[/font][font='Times New Roman','serif'] [/font][font=宋体]国内[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]厂家还是以电导检测器为主,青岛盛瀚有直流安培检测器,普仁有伏安检测器,可运行脉冲电位,但不能用于糖的分析,安徽皖仪和深圳通用成功开发了脉冲安培检测器,可用于糖的检测,除此外历元等也在研究安培检测器。[/font][/font][/font][font=宋体][font=宋体][/font][/font][/b]
各位大神,最近在做糖的测定,看到赛默飞的安培检测器上有个工作模式是3D扫描模式,一直没搞明白是怎么回事。哪位大神指导一下。
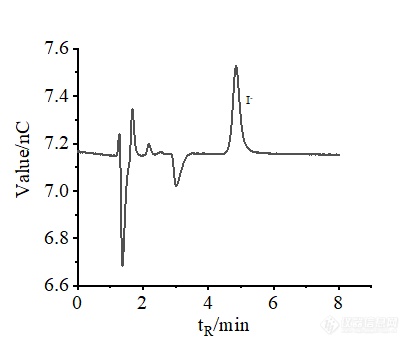
[align=center][font='cambria'][size=21px][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/size][/font][font='cambria'][size=21px]紫外及[/size][/font][font='cambria'][size=21px]脉冲安培[/size][/font][font='cambria'][size=21px]法[/size][/font][font='cambria'][size=21px]快速[/size][/font][font='cambria'][size=21px]检测[/size][/font][font='cambria'][size=21px]废水中碘离子[/size][/font][/align][align=center][font='cambria'][size=13px]ION CHROMATOGRAPHY ULTRAVIOLET AND PULSE AMPEROMETRIC METHODFOR RAPID DETECTION OF IODINE ION CONTENT IN WASTEWATER[/size][/font][/align][align=center][size=18px]李泳谊[/size][size=18px] [/size][size=18px]赵晓含[/size][size=18px] [/size][size=18px]李晓[/size][size=18px] [/size][size=18px]刘格林[/size][size=18px] [/size][size=18px] [/size][size=18px]施超欧[/size][size=18px]*[/size][/align][align=center][size=13px]华东理工大学[/size][size=13px] [/size][size=13px]化学与分子工程学院[/size][size=13px] [/size][size=13px]分析测试中心[/size][size=13px] 200237[/size][/align][align=left][size=12px]摘要:[/size][size=12px]针对[/size][size=12px]碘离子[/size][size=12px]快速[/size][size=12px]柱[/size][size=12px]([/size][size=12px]3*150mm[/size][size=12px])[/size][size=12px]建立[/size][size=12px]了快速测定碘离子的[/size][size=12px]分析[/size][size=12px]方法,[/size][size=12px]采用[/size][size=12px]8mmol/L[/size][size=12px]碳酸钠[/size][size=12px]为淋洗液,流速[/size][size=12px]0.4mL/min[/size][size=12px],结果表明:[/size][size=12px]常见的在[/size][size=12px]安培或[/size][size=12px]紫外检测器下有响应的阴离子对其无干扰[/size][size=12px]。[/size][size=12px]安培[/size][size=12px]模式[/size][size=12px]下[/size][size=12px]1[/size][size=12px].0μg/L [/size][size=12px]~100μg/L[/size][size=12px]的碘离子[/size][size=12px]线性关系良好,[/size][size=12px]R[/size][font='times new roman'][size=12px]2[/size][/font][size=12px]在[/size][size=12px]0.999[/size][size=12px]9[/size][size=12px]以上,加标回收率在[/size][size=12px]86.[/size][size=12px]97[/size][size=12px]%~1[/size][size=12px]07[/size][size=12px].[/size][size=12px]9[/size][size=12px]%[/size][size=12px]之间[/size][size=12px],[/size][size=12px]检出限为[/size][size=12px]0.35[/size][size=12px]μg[/size][size=12px]/L[/size][size=12px]。紫外模式下[/size][size=12px]10μg/L~1000μg/L[/size][size=12px]的浓度范围内线性关系良好,[/size][size=12px]R[/size][font='times new roman'][size=12px]2[/size][/font][size=12px]达到[/size][size=12px]0.9998[/size][size=12px]以上,[/size][size=12px]检出限为[/size][size=12px]2.6μg/L[/size][size=12px],加标回收率在[/size][size=12px]93.4[/size][size=12px]%~[/size][size=12px]99.[/size][size=12px]0[/size][size=12px]%[/size][size=12px]。[/size][size=12px]可用于碘[/size][size=12px]离子[/size][size=12px]的快速高灵敏度分析[/size][size=12px]。[/size][/align][align=left][size=12px]关键词:碘离子[/size][size=12px] [/size][size=12px]快速柱[/size][size=12px] [/size][size=12px][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/size][size=12px] [/size][size=12px]安培检测器[/size][size=12px] [/size][size=12px]紫外检测器[/size][/align][align=left][size=13px]碘,控制着人体内甲状腺素的合成,在维持人正常发育方面具有重要意义。碘的摄入量与甲状腺疾病密切相关,缺乏或者过量摄入都会引起一系列的疾病[/size][font='times new roman'][size=13px][color=#080000][1[/color][/size][/font][font='times new roman'][size=13px][color=#080000]][/color][/size][/font][size=13px]。[/size][/align][align=left][size=13px]碘[/size][size=13px]相关[/size][size=13px]的分析方法很多,例如[/size][size=13px]碘化物国家检测标准[/size][size=13px]的方法有砷[/size][size=13px]铈[/size][size=13px]催化分光光度法[/size][font='times new roman'][size=13px][2[/size][/font][font='times new roman'][size=13px]、[/size][/font][font='times new roman'][size=13px]4[/size][/font][font='times new roman'][size=13px]、[/size][/font][font='times new roman'][size=13px]6[/size][/font][font='times new roman'][size=13px]][/size][/font][size=13px]、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[/size][font='times new roman'][size=13px][2][/size][/font][size=13px]、比色法[/size][font='times new roman'][size=13px][2][/size][/font][size=13px]、容量法[/size][font='times new roman'][size=13px][2][/size][/font][size=13px]、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/size][font='times new roman'][size=13px][3[/size][/font][font='times new roman'][size=13px]、[/size][/font][font='times new roman'][size=13px]8-9[/size][/font][font='times new roman'][size=13px]][/size][/font][size=13px]、氧化还原滴定法[/size][font='times new roman'][size=13px][3[/size][/font][font='times new roman'][size=13px]、[/size][/font][font='times new roman'][size=13px]4-5[/size][/font][font='times new roman'][size=13px]][/size][/font][size=13px]、[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱[/color][/url]法[/size][font='times new roman'][size=13px][4[/size][/font][font='times new roman'][size=13px]、[/size][/font][font='times new roman'][size=13px]7[/size][/font][font='times new roman'][size=13px]、[/size][/font][font='times new roman'][size=13px]10][/size][/font][size=13px]、直接滴定法[/size][font='times new roman'][size=13px][4][/size][/font][size=13px]。[/size][size=13px]除上述[/size][size=13px]方法外[/size][size=13px],应用较多的还有中子活化法[/size][font='times new roman'][size=13px][11][/size][/font][size=13px]、[/size][size=13px]HPLC-[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url][/size][font='times new roman'][size=13px][12][/size][/font][size=13px]、毛细管电泳法[/size][font='times new roman'][size=13px][13][/size][/font][size=13px]等。[/size][/align][align=left][size=13px]而[/size][size=13px]碘[/size][size=13px]在天然水体中含量极微[/size][size=13px],[/size][size=13px][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法作为分析水溶液中[/size][size=13px]无机[/size][size=13px]阴离子的[/size][size=13px]首选[/size][size=13px]方法,[/size][size=13px]国家环境保护标准[/size][font='times new roman'][size=13px][[/size][/font][font='times new roman'][size=13px]3[/size][/font][font='times new roman'][size=13px]][/size][/font][size=13px]中[/size][size=13px]使用抑制[/size][size=13px]-[/size][size=13px]电导[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法的检出限[/size][size=13px]为[/size][size=13px]2.0 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]([/size][size=13px]进样量[/size][size=13px]250[/size][size=13px] [/size][size=13px]μ[/size][size=13px]L[/size][size=13px])[/size][size=13px],[/size][size=13px]但在实际检测中往往检出限满足不了要求[/size][size=13px];相对而言,使用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/size][size=13px]-[/size][size=13px]安培测定水系沉积物和土壤中碘的检出限略高[/size][font='times new roman'][size=13px][9][/size][/font][size=13px],为[/size][size=13px]0.2 [/size][size=13px]μg[/size][size=13px]/g[/size][size=13px]。饮用天然矿泉水[/size][font='times new roman'][size=13px][1[/size][/font][font='times new roman'][size=13px]4[/size][/font][font='times new roman'][size=13px]][/size][/font][size=13px]的检验方法中对碘化物的测定也使用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法,在[/size][size=13px]进样量[/size][size=13px]100μL[/size][size=13px],采用银工作电极[/size][size=13px]-[/size][size=13px]安培检测器,施加电压[/size][size=13px]+0.26 V[/size][size=13px]的条件下,定量限为[/size][size=13px]10.25 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]。[/size][/align][align=left][size=13px]为开发快速检测水中碘离子含量的方法,[/size][size=13px]定制了[/size][size=13px]3*150 mm[/size][size=13px]的碘离子快速分析柱[/size][size=13px],[/size][size=13px]可以[/size][size=13px]兼容[/size][size=13px]国标中的电导检测[/size][size=13px]法[/size][size=13px],即兼容紫外[/size][size=13px]-[/size][size=13px]安培[/size][size=13px]-[/size][size=13px]电导[/size][size=13px]三[/size][size=13px]种[/size][size=13px]检测体系,[/size][size=13px]定制快速[/size][size=13px]柱[/size][size=13px]的[/size][size=13px]尺寸[/size][size=13px]提高了分析速度、[/size][size=13px]降低了[/size][size=13px]淋洗液[/size][size=13px]的浓度从而降低[/size][size=13px]了[/size][size=13px]检测背景,提高检测灵敏度。[/size][size=13px]另外,碳酸盐体系的[/size][size=13px]pH[/size][size=13px]值比[/size][size=13px]氢氧根[/size][size=13px]体系低,对于[/size][size=13px]安培检测的[/size][size=13px]银[/size][size=13px]工作[/size][size=13px]电极,[/size][size=13px]稳定性更高[/size][size=13px]、[/size][size=13px]重复性更好[/size][size=13px]、[/size][size=13px]噪音更低[/size][size=13px]。[/size][size=13px]本[/size][size=13px]方法简单可靠,操作难度低,[/size][size=13px]具有较高的实用价值。[/size][/align][align=left][size=13px][color=#000000]1[/color][/size][size=13px][color=#000000] [/color][/size][size=13px][color=#000000]仪器和材料[/color][/size][/align][align=left][size=13px]ICS 5000+[/size][size=13px]多功能[/size][size=13px][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],[/size][size=13px]AS-AP[/size][size=13px]自动进样器、[/size][size=13px]DP[/size][size=13px]双泵、[/size][size=13px]DC[/size][size=13px]模块[/size][size=13px]配有[/size][size=13px]安培检测器[/size][size=13px]、[/size][size=13px]VWD[/size][size=13px]紫外检测器[/size][size=13px],[/size][size=13px]Ag[/size][size=13px]工作电极[/size][size=13px],[/size][size=13px]Chromeleon[/size][size=13px] [/size][size=13px]7[/size][size=13px].[/size][size=13px]2[/size][size=13px]0[/size][size=13px]色谱工作站,美国[/size][size=13px]Thermo[/size][size=13px]公司;色谱柱:[/size][size=13px]碘离子快速分析柱[/size][size=13px]([/size][size=13px]3*150 mm[/size][size=13px])[/size][size=13px];[/size][size=13px]Millipore-Q A10[/size][size=13px]超纯水机。[/size][/align][align=left][size=13px][color=#000000]无水[/color][/size][size=13px][color=#000000]Na[/color][/size][font='times new roman'][size=13px][color=#000000]2[/color][/size][/font][size=13px][color=#000000]CO[/color][/size][font='times new roman'][size=13px][color=#000000]3[/color][/size][/font][size=13px][color=#000000],优级纯,纯度≥[/color][/size][size=13px][color=#000000]99.8%[/color][/size][size=13px][color=#000000],上海阿拉丁生化科技公司;[/color][/size][size=13px]水中碘[/size][size=13px]离子[/size][size=13px],[/size][size=13px]100 [/size][size=13px]μg[/size][size=13px]/mL[/size][size=13px],国家有色金属及电子材料分析测试中心;[/size][size=13px] [/size][/align][align=left][size=13px][color=#000000]2[/color][/size][size=13px][color=#000000] [/color][/size][size=13px][color=#000000] [/color][/size][size=13px][color=#000000]溶液的配制[/color][/size][/align][align=left][size=13px]2.1 [/size][size=13px] [/size][size=13px]淋洗液的配制[/size][/align][align=left][size=13px]精确称取[/size][size=13px]4.2[/size][size=13px]4[/size][size=13px] g[/size][size=13px]无水[/size][size=13px]碳酸钠[/size][size=13px]于淋洗液瓶中,使用超纯水溶解并超声,[/size][size=13px]定容至[/size][size=13px]2 L[/size][size=13px],得到[/size][size=13px]20 mmol/L[/size][size=13px]的[/size][size=13px]碳酸钠[/size][size=13px]溶液作为淋洗液[/size][size=13px]B[/size][size=13px]流[/size][size=13px]路。[/size][/align][align=left][size=13px]2.2[/size][size=13px] [/size][size=13px]标准溶液的配制[/size][/align][align=left][size=13px]移取上述碘标准溶液[/size][size=13px]1 mL[/size][size=13px],使用超纯水逐级稀释得到[/size][size=13px]1 mg/L[/size][size=13px]的[/size][size=13px]碘离子[/size][size=13px]标准溶液,现配现用。[/size][/align][align=left][size=13px]2.3 [/size][size=13px] [/size][size=13px]样品溶液的配制[/size][/align][align=left][size=13px]采集[/size][size=13px]华东理工大学河道[/size][size=13px]排污[/size][size=13px]废水样,使用[/size][size=13px]0.45 [/size][size=13px]μm[/size][size=13px]水系微孔滤膜进行过滤,弃去初滤液[/size][size=13px]3[/size][size=13px] mL[/size][size=13px]后,将后续废水滤液收集至离心管中。检测中发现该废水[/size][size=13px]样[/size][size=13px]未能[/size][size=13px]检出[/size][size=13px]碘离子[/size][size=13px]。因此在废水样中,加入一定浓度的[/size][size=13px]碘离子[/size][size=13px],作为[/size][size=13px]待测[/size][size=13px]废水样[/size][size=13px]1[/size][size=13px]和[/size][size=13px]2[/size][size=13px](浓度分别为[/size][size=13px]10[/size][size=13px]和[/size][size=13px]30[/size][size=13px]μ[/size][size=13px]g/L[/size][size=13px])[/size][size=13px],冷藏待用。[/size][/align][align=left][size=13px][color=#000000]3 [/color][/size][size=13px][color=#000000] [/color][/size][size=13px][color=#000000]色谱条件[/color][/size][/align][align=left][size=13px]色谱柱:[/size][size=13px]定制[/size][size=13px]碘离子[/size][size=13px]快速分析柱[/size][size=13px]3*150 mm[/size][size=13px];[/size][size=13px]流速:[/size][size=13px]0.4 mL/min[/size][size=13px]。[/size][/align][align=left][size=13px]淋洗液:超纯水[/size][size=13px]:[/size][size=13px]20 mmol/L Na[/size][font='times new roman'][size=13px]2[/size][/font][size=13px]CO[/size][font='times new roman'][size=13px]3[/size][/font][size=13px]=[/size][size=13px] [/size][size=13px]60[/size][size=13px]:[/size][size=13px]40[/size][size=13px];[/size][/align][align=left][size=13px]柱温:[/size][size=13px]30℃[/size][size=13px];进样量:[/size][size=13px]25 [/size][size=13px]μL[/size][size=13px];[/size][size=13px]Ag[/size][size=13px]工作电极[/size][size=13px]([/size][size=13px]1mm[/size][size=13px])[/size][size=13px],厚度[/size][size=13px]1mil[/size][size=13px];[/size][/align][align=left][size=13px]检测器:紫外检测器[/size][size=13px]([/size][size=13px]226[/size][size=13px]nm[/size][size=13px])[/size][size=13px]与安培检测器[/size][size=13px](脉冲电位)[/size][size=13px]串联[/size][size=13px]。[/size][/align][align=left][font='宋体'][size=13px]4 结果与讨论[/size][/font][/align][align=left][size=13px]4.1 [/size][size=13px]色谱条件的确定[/size][/align][align=left][size=13px]4.1.1[/size][size=13px]柱温对[/size][size=13px]分离的影响[/size][/align][align=left][size=13px]依据[/size][size=13px]Van't[/size][size=13px] Hoff[/size][size=13px]方程进行热力学探究,[/size][size=13px]考察[/size][size=13px]不同温度[/size][size=13px]下[/size][size=13px]1mg/L[/size][size=13px]的[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]在定制柱上的洗脱情况[/size][size=13px]。[/size][size=13px]保持相同的保留时间,[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]在[/size][size=13px]303.15 K[/size][size=13px]下的灵敏度最高,因此选取[/size][size=13px]303.13 K[/size][size=13px]([/size][size=13px]30 ℃[/size][size=13px])作为[/size][size=13px]柱温[/size][size=13px],[/size][size=13px]同时[/size][size=13px]正常情况下,实验室测试温度[/size][size=13px]一般[/size][size=13px]不低于[/size][size=13px]30[/size][size=13px] [/size][size=13px]℃[/size][size=13px]。[/size][/align][align=center][size=12px]Table[/size][size=12px] [/size][size=12px]1[/size][size=12px] [/size][size=12px]不同条件下安培检测的结果[/size][/align][table][tr][td][align=center][size=12px][color=#000000]T[/color][/size][/align][align=center][size=12px][color=#000000]/K[/color][/size][/align][/td][td][align=center][size=12px]Na[/size][font='times new roman'][size=12px]2[/size][/font][size=12px]CO[/size][font='times new roman'][size=12px]3[/size][/font][size=12px][color=#000000]浓度[/color][/size][/align][align=center][size=12px][color=#000000]/(mmol/L)[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]t[/color][/size][font='times new roman'][size=12px][color=#000000]R[/color][/size][/font][/align][align=center][size=12px][color=#000000]/min[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]峰面积[/color][/size][size=12px][color=#000000]/([/color][/size][size=12px][color=#000000]nC[/color][/size][size=12px][color=#000000]*min)[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]峰高[/color][/size][/align][align=center][size=12px][color=#000000]/[/color][/size][size=12px][color=#000000]nC[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]噪音[/color][/size][/align][align=center][size=12px][color=#000000]/[/color][/size][size=12px][color=#000000]nC[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]背景[/color][/size][/align][align=center][size=12px][color=#000000]/[/color][/size][size=12px][color=#000000]nC[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]检出限[/color][/size][size=12px][color=#000000]/([/color][/size][size=12px]μg[/size][size=12px]/L[/size][size=12px][color=#000000])[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]303.15[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]7.1[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.940[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]5.660[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]18.56[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.002[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]6.990[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.3[/color][/size][size=12px][color=#000000]2[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]308.15[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]5.5[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.930[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]5.150[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]17.13[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.002[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]6.670[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.35[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]313.15[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.5[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.950[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.570[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]15.67[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.002[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]6.370[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.38[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]318.15[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.0[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.920[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.400[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]15.08[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.002[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]6.340[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.40[/color][/size][/align][/td][/tr][/table][align=left][size=13px]4.1[/size][size=13px].2[/size][size=13px] [/size][size=13px]流[/size][size=13px]速[/size][size=13px]和淋洗液浓度[/size][size=13px]的[/size][size=13px]选取与优化[/size][/align][align=left][size=13px]基于定制柱的尺寸(直径[/size][size=13px]3[/size][size=13px] [/size][size=13px]mm[/size][size=13px])[/size][size=13px],优化后[/size][size=13px]选定流速为[/size][size=13px]0[/size][size=13px].4 [/size][size=13px]mL/min[/size][size=13px],[/size][size=13px]选择[/size][size=13px]8.0 [/size][size=13px]mmol[/size][size=13px]/[/size][size=13px]L[/size][size=13px]的[/size][size=13px]Na[/size][font='times new roman'][size=13px]2[/size][/font][size=13px]CO[/size][font='times new roman'][size=13px]3[/size][/font][size=13px]为淋洗液。[/size][/align][align=left][size=13px]4.1.[/size][size=13px]3 [/size][size=13px] [/size][size=13px]干扰离子实验[/size][/align][align=left][size=13px]为验证该体系下其他阴离子对于[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]的测定无影响,以在安培和紫外检测器上有响应的[/size][size=13px]NO[/size][font='times new roman'][size=13px]3[/size][/font][font='times new roman'][size=13px]-[/size][/font][size=13px]、[/size][size=13px]NO[/size][font='times new roman'][size=13px]2[/size][/font][font='times new roman'][size=13px]-[/size][/font][size=13px]、[/size][size=13px]Br[/size][size=13px] [/size][font='times new roman'][size=13px]-[/size][/font][size=13px]、[/size][size=13px]C[/size][size=13px]N[/size][font='times new roman'][size=13px]-[/size][/font][size=13px]、[/size][size=13px]S[/size][font='times new roman'][size=13px]2-[/size][/font][size=13px]、[/size][size=13px]SCN[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]共[/size][size=13px]6[/size][size=13px]种常见阴离子进行干扰实验。[/size][size=13px]结果[/size][size=13px]表明[/size][size=13px]在安培检测器[/size][size=13px]和[/size][size=13px]紫外检测器上[/size][size=13px]相应的离子[/size][size=13px]均对[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]无干扰。[/size][/align][align=left][size=13px][color=#000000]4[/color][/size][size=13px][color=#000000].[/color][/size][size=13px][color=#000000]2[/color][/size][size=13px][color=#000000] [/color][/size][size=13px][color=#000000] [/color][/size][size=13px][color=#000000]方法学验证[/color][/size][/align][align=left][size=13px]4[/size][size=13px].[/size][size=13px]2[/size][size=13px].1 [/size][size=13px] [/size][size=13px]线性关系与检出限[/size][/align][align=left][size=13px]在[/size][size=13px]最佳色谱条件[/size][size=13px]下,[/size][size=13px]串联紫外[/size][size=13px]-[/size][size=13px]安培检测器[/size][size=13px](脉冲安培电位)[/size][size=13px]。[/size][size=13px]对配制好的一系列的线性标准溶液进行测定,每个浓度标准溶液平行测定[/size][size=13px]3[/size][size=13px]次。[/size][/align][align=center][size=12px]Table[/size][size=12px] [/size][size=12px]2[/size][size=12px] [/size][size=12px]不同标准碘离子浓度[/size][size=12px]安培与[/size][size=12px]紫外的测试结果[/size][/align][table][tr][td=2,1][align=center][size=12px]安培检测器[/size][/align][/td][td=3,1][align=center][size=12px]紫外检测器[/size][/align][/td][/tr][tr][td][align=center][size=12px]浓度[/size][/align][align=center][size=12px]/([/size][size=12px]μg[/size][size=12px]/L)[/size][/align][/td][td][align=center][size=12px]峰面积[/size][/align][align=center][size=12px]/([/size][size=12px]nC[/size][size=12px]*min)[/size][/align][/td][td][align=center][size=12px]浓度[/size][/align][align=center][size=12px]/([/size][size=12px]μg[/size][size=12px]/L)[/size][/align][/td][td=2,1][align=center][size=12px]峰面积[/size][/align][align=center][size=12px]/([/size][size=12px]mAU[/size][size=12px]*min)[/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]1[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.0078[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]10[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.0548[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]2[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.0164[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]25[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.1584[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]5[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.0413[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]50[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.3563[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]10[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.0719[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]100[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.874[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]25[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.1858[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]250[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]2.087[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]50[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.3642[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]500[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]4.098[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]100[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]0.7181[/color][/size][/align][/td][td=2,1][align=center][size=12px][color=#000000]1000[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]8.245[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]线性关系[/color][/size][/align][/td][td][align=center][size=12px][color=#000000]y = 0.0072x + 0.0031[/color][/size][/align][/td][td=3,1][align=center][size=12px][color=#000000]y = 0.0083x - 0.0174[/color][/size][/align][/td][/tr][tr][td][align=center][size=12px][color=#000000]R[/color][/size][font='times new roman'][size=12px][color=#000000]2[/color][/size][/font][/align][/td][td][align=center][size=12px][color=#000000]0.9999[/color][/size][/align][/td][td=3,1][align=center][size=12px]0.9998[/size][/align][/td][/tr][/table][align=left][size=13px]由表[/size][size=13px]2[/size][size=13px]可得,[/size][size=13px]安培检测器[/size][size=13px]在[/size][size=13px]1.0 [/size][size=13px]μg[/size][size=13px]/L~100 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]的浓度范围内线性关系良好,[/size][size=13px]检出限为[/size][size=13px]0.35 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px],定量限为[/size][size=13px]1.1 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px] [/size][size=13px]。该体系联用紫外检测器测定[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]时,检测的灵敏度[/size][size=13px]低于[/size][size=13px]安培检测器[/size][size=13px],[/size][size=13px]得出[/size][size=13px]I[/size][font='times new roman'][size=13px]- [/size][/font][size=13px]在该体系[/size][size=13px]-[/size][size=13px]紫外检测模式下的检出限为[/size][size=13px]2.6 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px],定量限为[/size][size=13px]8.8 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px] [/size][size=13px],[/size][size=13px]在[/size][size=13px]10 [/size][size=13px]μg[/size][size=13px]/L~1000 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]的浓度范围内线性关系良好[/size][size=13px] [/size][size=13px]。[/size][/align][align=left][size=13px]4[/size][size=13px].[/size][size=13px]2[/size][size=13px].2 [/size][size=13px] [/size][size=13px]进样重复性[/size][/align][align=left][size=13px]在[/size][size=13px]上述最佳色谱条件,[/size][size=13px]安培检测模式下[/size][size=13px]分别取高中低浓度的标准样品溶液:[/size][size=13px]5 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]、[/size][size=13px]10 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]、[/size][size=13px]50 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px] [/size][size=13px]的[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]标准溶液连续进样,每个标准浓度重复测定[/size][size=13px]8[/size][size=13px]次[/size][size=13px]。[/size][size=13px]保留时间的重复性最佳,[/size][size=13px]RSD[/size][size=13px]值[/size][size=13px]均≤[/size][size=13px]0.22[/size][size=13px]%[/size][size=13px],峰面积的[/size][size=13px]RSD[/size][size=13px]值[/size][size=13px]≤[/size][size=13px]2.[/size][size=13px]2[/size][size=13px]%[/size][size=13px]。[/size][size=13px]而在紫外检测中,分别取高中低浓度的标准样品溶液:[/size][size=13px]10 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]、[/size][size=13px]50 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px]、[/size][size=13px]500 [/size][size=13px]μg[/size][size=13px]/L[/size][size=13px] [/size][size=13px]的[/size][size=13px]I[/size][font='times new roman'][size=13px]-[/size][/font][size=13px] [/size][size=13px]标准溶液连续进样,每个标准浓度重复测定[/size][size=13px]8[/size][size=13px]次。[/size][size=13px]保留时间的[/size][size=13px]RSD[/size][size=13px]值[/size][size=13px]均≤[/size][size=13px]0.19[/size][size=13px]%[/size][size=13px],相对[/size][size=13px]安培检测器[/size][size=13px]而言峰面积的精密度较低,[/size][size=13px]R[/size][size=13px]SD[/size][size=13px]值[/size][size=13px]≤[/size][size=13px]3.2%[/size][size=13px]。[/size][/align][align=left][size=13px]4.[/size][size=13px]2.3 [/size][size=13px] [/size][size=13px]实际样品和方法加标回收率测定[/size][/align][align=left][size=13px]取已处理好的[/size][size=13px]待测[/size][size=13px]废水样,使用[/size][size=13px]上述色[/size][size=13px]谱条件,直接进样进行分析。[/size][size=13px]待测废水样[/size][size=13px]1[/size][size=13px]的安培检测结果如[/size][size=13px]图[/size][size=13px]1[/size][size=13px]所示。[/size][size=13px]进行[/size][size=13px]二个浓度[/size][size=13px]([/size][size=13px]1[/size][size=13px]0[/size][size=13px]和[/size][size=13px]3[/size][size=13px]0[/size][size=13px]mg/L[/size][size=13px])[/size][size=13px]两个水平的加标回收测定,每个加标样品平行测定[/size][size=13px]6[/size][size=13px]次。[/size][size=13px]安培检测[/size][size=13px]体系测定废水样品[/size][size=13px]1[/size][size=13px]的加标回收率[/size][size=13px]在[/size][size=13px]86[/size][size=13px].97[/size][size=13px]%~1[/size][size=13px]07.[/size][size=13px]9[/size][size=13px]%[/size][size=13px]之间。[/size][/align][align=left] [img=,410,346]https://ng1.17img.cn/bbsfiles/images/2021/09/202109211835112538_6416_3458762_3.png!w410x346.jpg[/img] [img=,420,327]https://ng1.17img.cn/bbsfiles/images/2021/09/202109211835597575_979_3458762_3.png!w420x327.jpg[/img][/align][align=left][size=12px] F[/size][size=12px]ig. [/size][size=12px]1[/size][size=12px] [/size][size=12px]样品[/size][size=12px]1[/size][size=12px] [/size][size=12px]的安培检测结果[/size][size=12px] [/size][size=12px]F[/size][size=12px]ig. [/size][size=12px]2[/size][size=12px] [/size][size=12px]样品[/size][size=12px]2[/size][size=12px]的紫外[/size][size=12px]测试[/size][size=12px]结果[/size][/align][align=left][size=13px]废水样[/size][size=13px]2[/size][size=13px]的[/size][size=13px]紫外检测[/size][size=13px]图谱[/size][size=13px]如[/size][size=13px]图[/size][size=13px]2[/size][size=13px]所示[/size][size=13px]。[/size][size=13px]进行[/size][size=13px]二个浓度([/size][size=13px]30[/size][size=13px]和[/size][size=13px]60mg/L[/size][size=13px])[/size][size=13px]两个水平的加标回收测定,每个加标样品平行测定[/size][size=13px]6[/size][size=13px]次。[/size][size=13px]紫外[/size][size=13px]检测[/size][size=13px]体系测定废水样品[/size][size=13px]2[/size][size=13px]的加标回收率在[/size][size=13px]在[/size][size=13px]93.4[/size][size=13px]%~[/size][size=13px]99.[/size][size=13px]0[/size][size=13px]%[/size][size=13px]之间。[/size][size=13px]符合国家标准[/size][size=13px]要求,优于电导法[/size][size=13px]。[/size][/align][align=left][/align][align=left][size=13px]5[/size][size=13px]结论[/size][/align][align=left][size=13px]针[/size][size=13px]对定制[/size][size=13px]的[/size][size=13px]碘[/size][size=13px]离子[/size][size=13px]快速分析柱,优化了色谱条件,并[/size][size=13px]进行[/size][size=13px]方法学验证[/size][size=13px]实验[/size][size=13px],结果表明,[/size][size=13px]使用脉冲安培法[/size][size=13px]灵敏度高,远胜于国标的[/size][size=13px]抑制[/size][size=13px]-[/size][size=13px]电导法[/size][size=13px],[/size][size=13px]如果按照相同的进样量,检测限仅为国标[/size][font='times new roman'][size=13px][[/size][/font][font='times new roman'][size=13px]3[/size][/font][font='times new roman'][size=13px]][/size][/font][size=13px]的六十分之一,而且[/size][size=13px]抗干扰能力强[/size][size=13px];连接[/size][size=13px]紫外[/size][size=13px]检测器[/size][size=13px],检测限是[/size][size=13px]国标[/size][size=13px]的八分之一[/size][size=13px]。[/size][size=13px]在碳酸盐体系中,[/size][size=13px]Ag[/size][size=13px]工作[/size][size=13px]电极较为稳定,[/size][size=13px]方法操作简单,同时可兼容电导和紫外[/size][size=13px]检测器[/size][size=13px],可取代国标的[/size][size=13px]抑制[/size][size=13px]-[/size][size=13px]电导法[/size][size=13px],使得实验者操作更简单,[/size][size=13px]准确性更高[/size][size=13px]。[/size][/align][align=left][size=13px][/size][/align][align=left][font='黑体']参考文献[/font][/align][align=center][/align][font='times new roman'][size=16px][1] [/size][/font][font='times new roman'][size=16px]姜海霞[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]碘对甲状腺疾病影响及机制的研究进展[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px][J]. [/size][/font][font='times new roman'][size=16px]中华实用诊断与治疗杂志[/size][/font][font='times new roman'][size=16px],[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]2016,[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]30(7):[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]639-641[/size][/font][font='times new roman'][size=16px].[/size][/font][font='times new roman'][size=16px][2] [/size][/font][font='times new roman'][size=16px]中华人民共和国卫生部、中国国家标准化管理委员会[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]生活饮用水标准检验方法[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]无机非金属指标[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]GB/T 5750.5-2006[s].[/s][/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]2006.[/size][/font][font='times new roman'][size=16px][3] [/size][/font][font='times new roman'][size=16px]水质[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]碘化物的测定[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]HJ 778-2015[s]. 2015.[/s][/size][/font][font='times new roman'][size=16px][4] [/size][/font][font='times new roman'][size=16px]中华人民共和国国家卫生健康委员会、国家市场监督管理总局[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]食品安全国家标准[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]食品中碘的测定[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]GB 5009.267-2020[s]. 2020.[/s][/size][/font][font='times new roman'][size=16px][5] [/size][/font][font='times new roman'][size=16px]中华人民共和国国家质量监督检验检疫总局、中国国家标准化管理委员会[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]制盐工业通用试验方法[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]碘的测定[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]GB/T 13025.7-2012[s]. 2012.[/s][/size][/font][font='times new roman'][size=16px][6] [/size][/font][font='times new roman'][size=16px]中华人民共和国国家卫生和计划生育委员会[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]尿中碘的测定[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]第[/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px]部分[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]砷[/size][/font][font='times new roman'][size=16px]铈[/size][/font][font='times new roman'][size=16px]催化分光光度法[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]WS/T 107.1-2016[s]. 2016.[/s][/size][/font][font='times new roman'][size=16px][7] [/size][/font][font='times new roman'][size=16px]中华人民共和国国家卫生和计划生育委员会[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]尿中碘的测定[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]第[/size][/font][font='times new roman'][size=16px]2[/size][/font][font='times new roman'][size=16px]部分[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]电感耦[/size][/font][font='times new roman'][size=16px]合等离子体制谱法[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]WS/T 107.2-2016[s]. 2016.[/s][/size][/font][font='times new roman'][size=16px][8] [/size][/font][font='times new roman'][size=16px]工作场所空气有毒物质测定[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]第[/size][/font][font='times new roman'][size=16px]58[/size][/font][font='times new roman'][size=16px]部分[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]碘及其[/size][/font][font='times new roman'][size=16px]化合物(发布稿)[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]GBZ/T 300.58-2017[s]. 2017.[/s][/size][/font][font='times new roman'][size=16px][9] [/size][/font][font='times new roman'][size=16px]区域地球化学样品分析方法[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]第[/size][/font][font='times new roman'][size=16px]23[/size][/font][font='times new roman'][size=16px]部分[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]碘量测定[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/size][/font][font='times new roman'][size=16px]:DZ/T 0279.23-2016[s]. 2016.[/s][/size][/font][font='times new roman'][size=16px][10] [/size][/font][font='times new roman'][size=16px]区域地球化学样品分析方法[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]第[/size][/font][font='times new roman'][size=16px]24[/size][/font][font='times new roman'][size=16px]部分[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]碘量测定[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱[/color][/url]法[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]DZ/T 0279.24-2016[s]. 2016.[/s][/size][/font][font='times new roman'][size=16px][11] [/size][/font][font='times new roman'][size=16px]Johansen O, [/size][/font][font='times new roman'][size=16px]Steinnes[/size][/font][font='times new roman'][size=16px] E. Determination of iodine in plant material by a neutron-activation method[J]. Analyst, 1976, 101: 455-457.[/size][/font][font='times new roman'][size=16px][12] [/size][/font][font='times new roman'][size=16px]孙凯峰[/size][/font][font='times new roman'][size=16px], [/size][/font][font='times new roman'][size=16px]徐红斌[/size][/font][font='times new roman'][size=16px], [/size][/font][font='times new roman'][size=16px]周陶忆[/size][/font][font='times new roman'][size=16px], [/size][/font][font='times new roman'][size=16px]等[/size][/font][font='times new roman'][size=16px]. HPLC-[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url][/size][/font][font='times new roman'][size=16px]联用技术测定奶粉中不同形态的碘[/size][/font][font='times new roman'][size=16px][J]. [/size][/font][font='times new roman'][size=16px]食品工业[/size][/font][font='times new roman'][size=16px], 2015, 036(002): 287-289.[/size][/font][font='times new roman'][size=16px][13] [/size][/font][font='times new roman'][size=16px]Huang Z, Ito K, Morita I, et al. Sensitive monitoring of iodine species in sea water using capillary electrophoresis: vertical profiles of dissolved iodine in the Pacific Ocean[J]. Journal of Environmental Monitoring, 2005, 7(008): 804-808.[/size][/font][font='times new roman'][size=16px][14] [/size][/font][font='times new roman'][size=16px]中华人民共和国国家卫生和计划生育委员会、国家食品药品监督管理总局[/size][/font][font='times new roman'][size=16px]. [/size][/font][font='times new roman'][size=16px]食品安全国家标准[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]饮用天然矿泉水检验方法[/size][/font][font='times new roman'][size=16px]:[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]GB 8538-2016[s]. 2016.[/s][/size][/font]
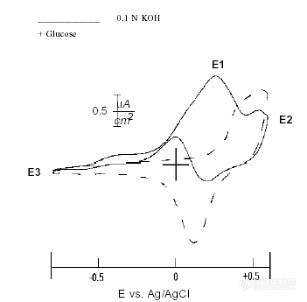
[align=left][font=宋体][font=Times New Roman]5.3.3 [/font][font=宋体]安培检测器的原理[/font][/font][font='Times New Roman'][font=宋体]安培检测器属于电化学检测器中的一种[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]是在外加电压的作用下[/font][/font][font=宋体],[/font][font='Times New Roman'][font=宋体]待测物质[/font][/font][font=宋体](具有电活性)[/font][font='Times New Roman'][font=宋体]会在[/font][/font][font=宋体]工作[/font][font='Times New Roman'][font=宋体]电极表面上发生氧化还原反应[/font][/font][font=宋体]。在氧化反应过程中,电活性被测化合物的电子从工作电极转移到安培池;反之,在还原过程中,电子从被测化合物转移到工作电极。这些[/font][font='Times New Roman'][font=宋体]电流的变化[/font][/font][font=宋体],该电流[/font][font='Times New Roman'][font=宋体]符合法拉第定律[/font][/font][font=宋体][font=宋体],通过对电流的检测可以推算出待测物质的浓度。其主要用于易于发生氧化还原反应的物质分析,[/font] 如果有些干扰物无法发生氧化还原反应,就没有检测信号,不被检测到。[/font][font=宋体]在[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]应用中安培检测主要包括恒电位(直流安培)、脉冲安培以及积分脉冲安培三种方式。[/font][font=宋体][font=Times New Roman]5.3.3.1 [/font][font=宋体]伏安法[/font][/font][font=宋体] [font=宋体]在现成的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]中,基本所有的被测化合物的分析方法已经固定,但作为未知化合物的分析,需要采用伏安法,其是确定安培检测器最佳工作电位的一种电化学技术。[/font][/font][font=宋体]其方法是工作电极表面不断通过含有被测化合物组分的溶液和支持流动相介质,测量其氧化和还原反应过程中产生的电流。并以此电流对指定范围内扫描的工作电极作图,得到伏安波形图。[/font][font=宋体][font=宋体]扫描时,先以正向对电流进行扫描,然后反向进行扫描,从起始点开始,到起始点结束,起点电位等于终点电位,此法称为[/font]“循环伏安法”。[/font][font=宋体][font=宋体]下图是葡萄糖在[/font][font=Times New Roman]0.1mol/L KOH[/font][font=宋体]条件下,在金电极和[/font][font=Times New Roman]Ag/AgCl[/font][font=宋体]参比电极上的循环伏安图[/font][/font][img=,307,302]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241058091910_5585_3237657_3.jpg!w307x302.jpg[/img][font=宋体] [/font][font=宋体][font=宋体]图中虚线是[/font][font=Times New Roman]0.1mol/L KOH[/font][font=宋体]溶液在没有葡萄糖时所引起的电流,即为背景电流。从[/font][font=Times New Roman]-0.8V[/font][font=宋体]开始正向扫描到[/font][font=Times New Roman]0.25V[/font][font=宋体]还是平坦的,再升高电压后,金电极开始表面氧化。接着从[/font][font=Times New Roman]0.6V[/font][font=宋体]开始反向扫描,金氧化物还原成金,负峰电流在[/font][font=Times New Roman]0.1V[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]在溶液中加入葡萄糖,从[/font][font=Times New Roman]-0.8V[/font][font=宋体]开始正向扫描,电流略有变化,但不太明显,从[/font][font=Times New Roman]-0.15V[/font][font=宋体]开始变化明显,电流升高,到[/font][font=Times New Roman]0.25V[/font][font=宋体]为峰值,然后电流减少,其原因是表面的大部分葡萄糖已经被氧化,另一个因素是金氧化物的生成阻止了葡萄糖的进一步氧化。当反向扫描时,金氧化物开始被还原成金,葡萄糖也一样,负峰电流在[/font][font=Times New Roman]0.15V[/font][font=宋体]左右。[/font][/font][font=宋体]在下述电化学反应中:[/font][img=,76,26]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241058264178_4191_3237657_3.jpg!w76x26.jpg[/img][font=宋体][font=宋体]当反应正向进行时,[/font][font=Times New Roman]A[/font][font=宋体]将[/font][font=Times New Roman]n[/font][font=宋体]个电子转移至工作电极,并被氧化成[/font][font=Times New Roman]B[/font][font=宋体],反向进行时,[/font][font=Times New Roman]B[/font][font=宋体]被还原成[/font][font=Times New Roman]A[/font][font=宋体],用[/font][font=Times New Roman]Nerst[/font][font=宋体]方程表示为:[/font][/font][font=宋体] [/font][font='Cambria Math'][/font][img=,143,41]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241058385867_7954_3237657_3.jpg!w143x41.jpg[/img][font=宋体][font=宋体]公式:均有特定的[/font][font=Times New Roman]E[/font][/font][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体],[/font][font=宋体][font=宋体]式中,[/font][font=Times New Roman]Eapp[/font][font=宋体]为工作电极,[/font][font=Times New Roman]E[/font][/font][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体][font=宋体]为[/font][font=Times New Roman][A]=[b][/b][/font][b][font=宋体]时的电位,[/font][font=Times New Roman][A][/font][font=宋体]、[/font][font=Times New Roman][b][/b][/font][b][font=宋体]分别为电极表面[/font][font=Times New Roman]A[/font][font=宋体]与[/font][font=Times New Roman]B[/font][font=宋体]浓度,[/font][font=Times New Roman]mmol/L[/font][font=宋体]。[/font][/b][/b][/font][b][b][font=宋体][font=宋体]在实际的每个氧化还原反应中,都有一特征[/font][font=Times New Roman]E[/font][/font][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体]值[/font][font='Times New Roman'][font=宋体],[/font][/font][font=宋体][font=宋体]在[/font][font=Times New Roman]Eapp=E[/font][/font][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体][font=Times New Roman],[/font][/font][font='Times New Roman'] lg [b]/[A][/b][/font][b][font=宋体][font=宋体]为零;因此[/font][font=Times New Roman][b]=[A][/b][/font][b][font=宋体]。如果[/font][font=Times New Roman]Eapp[/font][font=宋体]设定为大于[/font][font=Times New Roman]E[/font][/b][/font][b][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体][font=宋体],[/font] 因此,[font=Times New Roman][b][A][/b][/font][b][font=宋体]。反应向右进行,这一反应过程代表[/font][font=Times New Roman]A[/font][font=宋体]物质氧化成为[/font][font=Times New Roman]B[/font][font=宋体]物质,产生阳极电流,相反,设定[/font][font=Times New Roman]Eapp[/font][font=宋体]小于[/font][font=Times New Roman]E[/font][/b][/font][b][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体][font=宋体],导致[/font][font=Times New Roman]B[/font][font=宋体]还原成[/font][font=Times New Roman]A[/font][font=宋体],产生阴极电流。[/font][/font][font=宋体][font=宋体]考虑仅有[/font][font=Times New Roman]A[/font][font=宋体]物质存在于溶液中,而[/font][font=Times New Roman]E[/font][/font][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体][font=宋体]为+[/font][font=Times New Roman]0.4V[/font][font=宋体],对[/font][font=Times New Roman]Ag/AgCl[/font][font=宋体]参比电极,图[/font][font=Times New Roman]3-7[/font][font=宋体]所示为电流与施加电位函数的伏安图。[/font][/font][font=宋体][font=宋体]从伏安图可见,当外加电压为[/font][font=Times New Roman]0.2V[/font][font=宋体]时,[/font][font=Times New Roman]Eapp[/font][font=宋体]小于[/font][font=Times New Roman]E[/font][/font][sup][font=宋体][font=Times New Roman]0[/font][/font][/sup][font=宋体][font=宋体],[/font][font=Times New Roman]B[/font][font=宋体]更易还原成[/font][font=Times New Roman]A[/font][font=宋体],因此溶液仅含有物质[/font][font=Times New Roman]A[/font][font=宋体],没有反应发生。随着电位的增加,[/font][font=Times New Roman]A[/font][font=宋体]被氧化[/font][font=Times New Roman]B[/font][font=宋体],并且[/font][font=Times New Roman][b][/b][/font][b][font=宋体]与[/font][font=Times New Roman][A][/font][font=宋体]的比值随之增加。在更高的电位下([/font][font=Times New Roman]0.6V[/font][font=宋体]),到达工作电极表面的[/font][font=Times New Roman]A[/font][font=宋体]被[/font][font=Times New Roman]100%[/font][font=宋体]氧化成[/font][font=Times New Roman]B[/font][font=宋体],而电流不再随着电位的增加而增大。[/font][/b][/font][b][img=,390,203]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241058533092_653_3237657_3.jpg!w390x203.jpg[/img][font=宋体]施加电位与电流的关系曲线[/font][b][font=宋体] [font=宋体]安培检测器根据所施加的电位的方式不同,可分为直流安培法,施加固定的单电位;以及脉冲安培法和积分安培法,施加多重顺序的电位。[/font][/font][/b][font=Calibri] [/font][font=Calibri]5.3.3.2 [/font][font=宋体]直流安培法([/font][font='Times New Roman']Direct[/font][font=宋体] [/font][font='Times New Roman']amperometric detection[/font][font=宋体],[/font][font='Times New Roman']DC[/font][font=宋体])[/font][font=宋体][font=宋体]直流安培法又称恒电位安培法,在液相色谱中直流安培检测器是使用最广泛的电化学检测器,直流安培中施加到工作电极上的是一个恒定的直流电位,当待测物发生氧化还原反应时会产生电流信号,但电极本身为惰性,不参与氧化反应,或者电极可以与待测物形成沉淀[/font][font=Times New Roman]/[/font][font=宋体]络合物参与氧化反应。[/font][/font][font=宋体]选择最佳的工作电位对于直流安培的检测非常关键,选择合适的工作电位是为了使电化学活性分子处于扩散的控制平台区,取得最佳的信噪比。最佳的工作电位是极限扩散电流最小时的电位。[/font][font=宋体]若选择的电位高于最佳电位(待测物可以产生极限扩散电流的最小电位)时,会使其他不需要检测的物质响应从而降低了选择性,并且噪声增加[/font][sup][font=宋体][font=Times New Roman][33][/font][/font][/sup][font=宋体][font=宋体]。低于最佳电位,虽然噪声下降,但检测灵敏度也下降,从图上可以看到,对于[/font][font=Times New Roman]5-[/font][font=宋体]羟色胺最佳的施加电位约在[/font][font=Times New Roman]0.7V[/font][font=宋体]左右。[/font][/font][/b][/b][/b][/b][/b][/b][/align][align=center][img=,355,206]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241059093350_8509_3237657_3.jpg!w355x206.jpg[/img][font='Times New Roman'] [/font][/align][font=宋体][font=宋体]图[/font][font=Calibri]3-10[/font][font=宋体]为施加电位与色谱峰信号的关系图([/font][font=Calibri]5-[/font][font=宋体]羟色胺)[/font][/font][font=宋体][font=宋体]直流安培具有很高的灵敏度,可以测定[/font][font=Times New Roman]ug/L[/font][font=宋体]的无机物和有机物,主要用于测定那些被氧化还原反应对工作电极不易产生污染的化合物。例如含有酚或儿茶酚功能基的化合物,许多药物或生物分子带有这类功能基,其中最重要的是儿茶酚胺类中的多巴胺、多巴及其它生物神经传递物质;止痛药醋氨酚也含有酚功能基并易于检测;氨基酸中的酪氨酸也含有酚功能基,不仅这个氨基酸可以被检测,而且任何含有酪氨酸多肽也可以用安培检测。[/font][/font][font=宋体]此外还有一些含芳香胺、硫醇和含硫的有机化合物也可以采用直流安培检测。除了这些有机分子,一些易于与银形成络合物的无机阴离子如氰、硫化物和碘可以用银电极以直流安培方式检测。[/font][font='Times New Roman'] [/font][b][font='Times New Roman']5.3.3.3 [/font][font=宋体][font=宋体]脉冲安培法([/font][font=Times New Roman]Pulsed amperometric detection, PAD[/font][font=宋体])[/font][/font][/b][font=宋体][font=宋体]脉冲安培检测器是起源于对糖检测的需要,绝大多数糖在低紫外区的灵敏度和选择性较差,示差检测器的灵敏度不够无法满足糖的检测需求,当时并没有[/font][font=Times New Roman]ELSD[/font][font=宋体]、[/font][font=Times New Roman]NQAD[/font][font=宋体]以及[/font][font=Times New Roman]CAD[/font][font=宋体]、[/font][font=Times New Roman]MS[/font][font=宋体]检测器,脉冲安培成为糖检测优先考虑的方法。[/font][/font][font=宋体][font=Times New Roman]20[/font][font=宋体]世纪[/font][font=Times New Roman]80[/font][font=宋体]年代中期,之前作为测糖的主要方法的光度法逐渐被[/font][font=Times New Roman]PAD[/font][font=宋体]取代。由于使用恒定电位进行检测时,在工作电极表面会富集氧化反应的产物,从而抑制了进一步的检测。为了解决工作电极表面被钝化的问题,[/font][font=Times New Roman]PAD[/font][font=宋体]中使用了[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体][font=宋体]、[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]oxd[/font][/font][/sub][font=宋体][font=宋体]、[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]red[/font][/font][/sub][font=宋体][font=宋体]三阶电位,每个电位的持续时间分别为[/font][font=Times New Roman]t[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体][font=宋体]、[/font][font=Times New Roman]t[/font][/font][sub][font=宋体][font=Times New Roman]oxd[/font][/font][/sub][font=宋体][font=宋体]、[/font][font=Times New Roman]t[/font][/font][sub][font=宋体][font=Times New Roman]red[/font][/font][/sub][font=宋体],如图[/font][font='Times New Roman']1.2[/font][font=宋体][font=宋体](左)所示。[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体][font=宋体]用于检测时间段[/font][font=Times New Roman](t[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体][font=Times New Roman])[/font][font=宋体],是工作电位,在该电位下测待测物的氧化电流,为了扣除电极表面的充电电流,其中包括一个延迟时间周期[/font][font=Times New Roman](t[/font][/font][sub][font=宋体][font=Times New Roman]del[/font][/font][/sub][font=宋体][font=Times New Roman])[/font][font=宋体];然后[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]oxd[/font][/font][/sub][font=宋体] [font=宋体]是比[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体][font=宋体]高的氧化清洗电位,使得吸附在电极表面的反应产物能够脱离电极从而继续进行检测;[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]red[/font][/font][/sub][font=宋体][font=宋体]为比[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体][font=宋体]负得多的还原清洗电位,使工作电极表面还原为金属本身,再回到电位[/font][font=Times New Roman]E[/font][/font][sub][font=宋体][font=Times New Roman]det[/font][/font][/sub][font=宋体],如此循环,这样保证了检测的重复性和灵敏度。[/font][font=宋体]脉冲安培检测的电位和时间参数的设置非常关键,在将脉冲安培法应用于糖类化合物检测时,要求糖类在检测电位处被氧化,工作电极的响应在清洗和调整脉冲期间恢复。检测、清洗和调节电位的选择应基于金工作电极的伏安特性和用于分离的移动相中要检测的糖类[/font][sup][font=宋体][font=Times New Roman][[/font][/font][/sup][sup][font='Times New Roman']34][/font][/sup][font=宋体]。[/font][font='Times New Roman']Rocklin[/font][font=宋体]等[/font][sup][font=宋体][font=Times New Roman][22][/font][/font][/sup][font=宋体][font=宋体]在[/font][font=Times New Roman]1998[/font][font=宋体]年提出了新的四电位波形,如图[/font][/font][font='Times New Roman']1.2[/font][font=宋体](右)所示。该波形能够降低工作电极的损耗,提高了测样的重复性,延长了工作电极的使用寿命。[/font][img=,566,273]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241059243635_7421_3237657_3.png!w566x273.jpg[/img][align=center][b][font=宋体]图[/font][font='Times New Roman']1[/font][font=宋体][font=Times New Roman].[/font][/font][font='Times New Roman']2 [/font][font=宋体]脉冲安培检测的三电位(左)和四电位图(右)[/font][/b][/align][font=宋体]除了糖以外,脉冲安培可以用于检测含有醇、乙醛、胺以及含硫基团的化合物的检测。[/font][b][font='Times New Roman']5.3.3.4 [/font][font=宋体][font=宋体]积分安培法([/font][font=Times New Roman]Integrated [/font][/font][font='Times New Roman']pulsed amperometric detection, IPAD[/font][font=宋体])[/font][/b][font=宋体] [font=宋体]积分脉冲安培是另一种新形式的脉冲安培技术,[/font][font=Times New Roman]1989[/font][font=宋体]年由[/font][font=Times New Roman]D.Johnson[/font][font=宋体]等提出,并将其用于氨基酸的分析,早期积分脉冲安培被称为电位扫描脉冲库伦检测。[/font][/font][font=宋体]积分安培的电位也可以通过循环伏安法进行,下图是亮氨酸的脉冲和积分的伏安图。[/font][img=,299,275]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241059464894_4756_3237657_3.jpg!w299x275.jpg[/img][font=宋体][font=宋体]图所示在[/font][font=Times New Roman]0.1mol/L NaOH[/font][font=宋体]溶液中,金电极分析亮氨酸时,脉冲和积分安培检测器的循环伏安图的比较。对于脉冲安培,在一个脉冲周期中,在单一电位下对电流积分。当用积分安培时,在一个循环电位下的正反向扫描得到的电流积分。[/font][/font][font=宋体][font=宋体]也就是说,脉冲安培([/font][font=Times New Roman]PAD[/font][font=宋体])对电流的测量是基于单次脉冲,所以需要一个短暂的间隙过程以便使充电电流衰减。而积分安培的检测由于其电流的检测是在一个循环过程中,正反向连续积分的,没有待测物存在时,净电荷为零,因此大大降低了氧化还原产物对电极的影响。其优点在于能消除由于在色谱中使用梯度而引起的[/font][font=Times New Roman]pH[/font][font=宋体]值和流动相组成的微小变化所带来的漂移和变化,使得检测基线稳定并且检测信号变强[/font][font=Times New Roman][[/font][/font][font='Times New Roman']35][/font][font=宋体]。[/font][font=宋体][font=宋体]积分安培检测,需要反应基团的原子至少有一对孤对电子的存在,使其在未氧化的电极表面吸附,鉴于其特点,非常适合那些具有未成键电子基团[/font][font=Times New Roman]N[/font][font=宋体],[/font][font=Times New Roman]S[/font][font=宋体]的胺和硫化合的检测。例如糖、氨基酸、蛋白质、抗生素等。[/font][/font][img=,320,199]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241100164090_4457_3237657_3.jpg!w320x199.jpg[/img][align=center][img=,225,217]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241100310782_2628_3237657_3.png!w225x217.jpg[/img][/align][align=center][b][font=宋体]图[/font][font='Times New Roman']1[/font][font=宋体][font=Times New Roman].[/font][/font][font='Times New Roman']3 [/font][font=宋体]积分安培检测的四电位图[/font][/b][/align][align=center][b][font='Times New Roman'] [/font][/b][/align][font=宋体][font=宋体]为了减少工作电极的溶解,[/font] 也就是解决金电极表面生成的金氧化物对电极重现性的负面影响,[font=Times New Roman]Clark[/font][font=宋体]等[/font][/font][sup][font=宋体][font=Times New Roman][[/font][/font][/sup][sup][font='Times New Roman']36][/font][/sup][font=宋体][font=宋体]对[/font][font=Times New Roman]IPAD[/font][font=宋体]的波形也做了改进,在无需衍生化的情况下使用了六电位波形来分析氨基酸和氨基糖。通过在波形积分之前加入更多的负电位,可以最大限度地减少由于过多的氧化物形成而导致的电极表面贵金属的损耗。此外,与传统的[/font][font=Times New Roman]IPAD[/font][font=宋体]波形相比,包含了更短的吸附步长,从而实现了更有效的循环,而不会限制氨基酸的线性范围。利用六电位波形进行检测结果显示,该工作电极干净且无明显的电极衰退和信号丢失,在连续一周的检测下,检测所有氨基酸的峰面积的[/font][font=Times New Roman]RSD[/font][font=宋体]小于[/font][font=Times New Roman]2%[/font][font=宋体]。[/font][/font][font=宋体]蔡亚琪等比较了三电位、四电位和六电位对氨基糖苷类抗生素测定的信号响应、信噪比、检测灵敏度和线性等参数的影响,六电位可以获得最好的结果,并用于氨基糖苷类抗生素的检测,见下图。[/font][img=,408,254]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241100450571_310_3237657_3.jpg!w408x254.jpg[/img][table][tr][td][font=等线][font=等线]时间[/font]/s[/font][/td][td][font=等线][font=等线]电位[/font]/V [/font][/td][td][font=等线]积分[/font][/td][/tr][tr][td][align=right][font=等线]0[/font][/align][/td][td][align=right][font=等线]-0.25[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.04[/font][/align][/td][td][align=right][font=等线]-0.25[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.05[/font][/align][/td][td][align=right][font=等线]-0.05[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.21[/font][/align][/td][td][align=right][font=等线]-0.05[/font][/align][/td][td][font=等线]开始[/font][/td][/tr][tr][td][align=right][font=等线]0.22[/font][/align][/td][td][align=right][font=等线]0.22[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.46[/font][/align][/td][td][align=right][font=等线]0.22[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.47[/font][/align][/td][td][align=right][font=等线]-0.05[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.56[/font][/align][/td][td][align=right][font=等线]-0.05[/font][/align][/td][td][font=等线]终止[/font][/td][/tr][tr][td][align=right][font=等线]0.57[/font][/align][/td][td][align=right][font=等线]-2[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.58[/font][/align][/td][td][align=right][font=等线]-2[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.59[/font][/align][/td][td][align=right][font=等线]0.55[/font][/align][/td][/tr][tr][td][align=right][font=等线]0.6[/font][/align][/td][td][align=right][font=等线]-0.25[/font][/align][/td][/tr][/table][font=黑体]5.3.3.5迟滞时间[/font][font=宋体][font=宋体]采用脉冲安培和积分安培检测器,氧化电流积分迟滞允许电荷电流衰退。类似的三电位波形用于检测其它物质,特别是糖和醛。图[/font]3-15为金工作电极糖类测定时[/font][font=宋体],[/font][font=宋体]背景电流与迟滞时间的相关性。[/font][align=center][img=,284,271]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241101010290_2295_3237657_3.jpg!w284x271.jpg[/img][/align][align=center][font=宋体][font=宋体]图[/font]3-15 金工作电极的迟滞时间与背景电流的关系图[/font][/align][font=宋体][font=宋体]图[/font][font=Calibri]3-16[/font][font=宋体]是通过改变积分时间后得到的结果。[/font][font=Calibri]0.2[/font][font=宋体]秒的迟滞时间是足够允许电荷电流迟滞并接近于零。[/font][/font][align=center][img=,318,231]https://ng1.17img.cn/bbsfiles/images/2021/11/202111241101154504_7297_3237657_3.jpg!w318x231.jpg[/img][/align][align=center][font=宋体][font=宋体]图[/font][font=Calibri]3-16 [/font][font=宋体]色谱峰面积与迟滞时间的相关性[/font][/font][/align][font=宋体][font=宋体]从[/font][font=Calibri]0[/font][font=宋体]到[/font][font=Calibri]0.2[/font][font=宋体]秒之间的响应值减少不多,但迟滞时间至少[/font][font=Calibri]0.2[/font][font=宋体]秒可提供最佳信号[/font][font=Calibri]-[/font][font=宋体]噪声比。[/font][/font][font=黑体] [/font][font=黑体]5.3.3.6电位极限[/font][font=宋体][font=宋体]负电位极限是流动相或支持电解质被还原的电位。正电位极限是流动相,支持电解质或电极本身能够被氧化的电位。因为这些反应产生的电流远远超过溶质氧化还原反应所产生的电流,因此用于检测被测物的电位必须限定在此范围内。在表[/font]3-2列出的4种电极材料在酸性或碱性条件下的电位极限[/font][font=宋体],[/font][font=宋体][font=宋体]这些电位极限受流动相的[/font]pH影响很大。在碱性条件下,负电位极限更负,而在酸性条件下,正电位极限更正。[/font][font=宋体]当施加电位接近于电位极限,噪声将随着背景电流的增加而增加。对于金属电极上,背景电流的快速增加就是电位极限的接近。而玻碳电极中,背景电流的增加更为平稳。电位极限值是根据所要求的信噪比测定得到的。[/font][font=宋体] [/font][align=center][font=宋体][font=宋体]表[/font][font=Calibri]3-4[/font][font=Calibri]Ag/AgCl[/font][font=宋体]参比电极下的电极电位[/font][/font][/align][table][tr][td][align=center][font=宋体]工作电极[/font][/align][/td][td][align=center][font=宋体][font=宋体]溶液([/font][font=Calibri]0.1mol/L[/font][font=宋体])[/font][/font][/align][/td][td][align=center][font=宋体][font=宋体]负电位极限([/font][font=Calibri]V[/font][font=宋体])[/font][/font][/align][/td][td][align=center][font=宋体][font=宋体]正电位极限([/font][font=Calibri]V[/font][font=宋体])[/font][/font][/align][/td][/tr][tr][td][align=center][font=宋体][font=宋体]玻碳([/font][font=Calibri]G.C.[/font][font=宋体])[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]KOH[/font][/font][/align][align=center][font=宋体][font=Calibri]HClO[/font][/font][sub][font=宋体][font=Calibri]4[/font][/font][/sub][/align][/td][td][align=center][font=宋体][font=Calibri](-1.5)[/font][/font][/align][align=center][font=宋体][font=Calibri](-0.8)[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri](+0.6)[/font][/font][/align][align=center][font=宋体][font=Calibri](+1.3)[/font][/font][/align][/td][/tr][tr][td][align=center][font=宋体][font=宋体]金([/font][font=Calibri]Au[/font][font=宋体])[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]KOH[/font][/font][/align][align=center][font=宋体][font=Calibri]HClO[/font][/font][sub][font=宋体][font=Calibri]4[/font][/font][/sub][/align][/td][td][align=center][font=宋体][font=Calibri]-1.25[/font][/font][/align][align=center][font=宋体][font=Calibri]-0.8[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]+0.75[/font][/font][/align][align=center][font=宋体][font=Calibri]+1.50[/font][/font][/align][/td][/tr][tr][td][align=center][font=宋体][font=宋体]银([/font][font=Calibri]Ag[/font][font=宋体])[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]KOH[/font][/font][/align][align=center][font=宋体][font=Calibri]HClO[/font][/font][sub][font=宋体][font=Calibri]4[/font][/font][/sub][/align][/td][td][align=center][font=宋体][font=Calibri]-1.20[/font][/font][/align][align=center][font=宋体][font=Calibri]-0.55[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]+0.10[/font][/font][/align][align=center][font=宋体][font=Calibri]+0.40[/font][/font][/align][/td][/tr][tr][td][align=center][font=宋体][font=宋体]铂([/font][font=Calibri]Pt[/font][font=宋体])[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]KOH[/font][/font][/align][align=center][font=宋体][font=Calibri]HClO[/font][/font][sub][font=宋体][font=Calibri]4[/font][/font][/sub][/align][/td][td][align=center][font=宋体][font=Calibri]-0.90[/font][/font][/align][align=center][font=宋体][font=Calibri]-0.20[/font][/font][/align][/td][td][align=center][font=宋体][font=Calibri]+0.65[/font][/font][/align][align=center][font=宋体][font=Calibri]+1.30[/font][/font][/align][/td][/tr][/table][font=宋体][font=Calibri]*[/font][font=宋体]不像金属电极,玻碳电极的电位极限不会明显出现。不同的应用其噪声和背景水平必须通过实验决定。[/font][/font]
有哪位大虾用过美国热电带脉冲放电检测器(PDD)的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],它的性能如何?能检测那些组分,灵敏度怎样? ------------------------------------------------------------------------------------------- [em06]
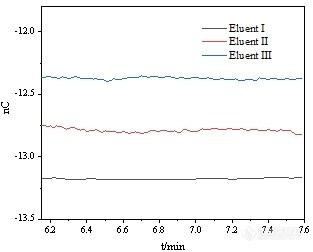
[b][font=宋体]摘要:[/font][/b][font=宋体]硫化氢([/font]H[sub]2[/sub]S[font=宋体])是生活中常见气体污染物,人体短时内吸入少量高浓度硫化氢便可导致死亡,也可对动植物、建筑设施等造成危害。针对离子色现有谱检测方法存在的问题,建立了一种准确、高效地测定微量硫化氢气体的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]脉冲安培定量分析新方法。该法使用传统[/font]IonPac AS7 (250mm×4mm)[font=宋体]阴离子交换色谱柱,采用新型氢氧化钠[/font]-[font=宋体]草酸钠淋洗液组合,替代原有方法中氢氧化钠[/font]-[font=宋体]乙酸钠淋洗液组合,优化脉冲安培检测电位参数和积分时长。比较添加剂的种类和含量对硫化物稳定性的影响,探索了硫化物的最佳保存条件。实验结果表明,硫化物在[/font]0.01~0.20 mg/L[font=宋体]的范围内线性关系良好[/font]([font=宋体]相关系数[/font][i]r[sup]2[/sup][/i][font=宋体]可达到[/font]0.999)[font=宋体],检出限[/font]([i]S/N[/i]=3)[font=宋体]和定量限[/font]([i]S/N[/i]=10)[font=宋体]分别为[/font]1.03μg/L[font=宋体]和[/font]3.45 μg/L[font=宋体],硫化物的相对保留时间和相对峰面积的相对标准偏差[/font](RSD)[font=宋体]均小于[/font]0.2% ([i]n=6[/i])[font=宋体]。改进后方法稳定性好,基线噪音显著降低,淋洗液试剂成本只有原来的[/font]10%[font=宋体],[/font]100 μg/L[font=宋体]以下的硫化物也可检出,且峰型更为对称,更适用于实际样品中低浓度硫化物的检测。采用[/font]250 mmol/L[font=宋体]氢氧化钠[/font]-0.8%[font=宋体]乙二胺四乙酸二钠稳定液可使硫化物稳定保存[/font]10[font=宋体]小时以上,回收率和大批量、长时检测的可靠性大幅提高。将新建立的检测方法应用于学校垃圾处理站,结合被动采样法富集测定空气中硫化氢含量,检测结果均未超过国家规定限值,此法可满足硫化氢气体相关鉴定检测工作的要求。[/font][font=宋体]关键词:[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url];安培检测;硫化物;电位;草酸钠[/font][b][font=宋体]前言[/font][/b][font=宋体]硫化氢[/font](H[sub]2[/sub]S) [font=宋体]是人类生产生活中常见的气态污染物,低浓度即具有臭鸡蛋气味,且浓度足够高时能麻痹嗅觉反而不易被察觉。石油和天然气加工、采矿、造纸、废水处理、垃圾处理等均会产生硫化氢气体,来源广泛,控制困难。[/font]H[sub]2[/sub]S[font=宋体]对所有器官均有毒性,尤其是中枢神经和肺部系统,长期暴露于硫化氢环境中会出现头晕恶心,大量吸入还会造成呼吸衰竭而迅速死亡[/font][sup][1,2][/sup][font=宋体];[/font]H[sub]2[/sub]S[font=宋体]也是形成酸雨的原因之一,被氧化后形成硫酸腐蚀管道和植物根茎;对人类生产生活、自然环境产生严重影响[/font][sup][3,4][/sup][font=宋体]。[/font][font=宋体]近年来常用检测方法有分光光度法[/font][sup][5][/sup][font=宋体]、化学分析法[/font][sup][6][/sup][font=宋体]、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法[/font][sup][7][/sup][font=宋体]、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/font][sup][8][/sup][font=宋体]、现场快速检测法,如醋酸铅试纸、硫化氢报警法[/font][sup][9][/sup][font=宋体]等,以及使用气体检测器进行检测,如利用电化学、比色和光学方法进行定性定量,应用在工业环境中可对高浓度硫化氢起到警示作用[/font][sup][10,11][/sup][font=宋体]。上述方法虽能提供较可靠的检测结果,但存在灵敏度低、样品预处理较复杂、检测成本高,无法准确高效地定量低浓度的硫化氢气体等问题,即使是高浓度下,有些方法也只能半定量[/font][sup][12,13][/sup][font=宋体]。[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]高效、简便、灵敏度高等优点使其逐渐应用到测定硫化氢的工作中。已有研究是将采样的硫化氢氧化,电导检测器检测,此过程干扰众多,灵敏度较差[/font][sup][14][/sup][font=宋体];或利用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font]-[font=宋体]安培检测法,将富集的硫化氢以离子形式分离,直流或脉冲安培法检测电流变化,反映出硫化氢的浓度[/font][sup][15,16][/sup][font=宋体]。但在日常检测中发现,硫化物在常规氢氧化钠碱性溶液中[/font]2h[font=宋体]就会有[/font]20%[font=宋体]左右的损失,保存困难,易被金属离子络合;且现有方法检出限高、灵敏度低,导致低浓度硫化物峰严重拖尾或不能检出,回收率仅有[/font]60%[font=宋体]左右,给实际应用带来重重困难。[/font][font=宋体]本文在原有[/font]Ag[font=宋体]电极测硫的基础上优化淋洗液条件,利用草酸钠金属络合剂的特性避免分析物损失,降低了基线噪音,分离效果更好,且成本大大降低;优化脉冲安培检测电位,在默认的硫化物电位基础上,针对低浓度硫化物优化电位参数,清洗电位中施加正向电压,探索积分时长的影响。最终线性范围拓宽,检出限、定量限更低,延长了[/font]Ag[font=宋体]电极使用寿命,建立了一套准确、可靠地测定低浓度硫化物的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]方法;对比加入几种添加剂后硫化物稳定存在时间,得到硫化物的最佳保存条件,提高了硫化物的回收率。随后结合被动采样法将其应用于学校垃圾处理站进行实际样品检测。[/font][b]1 [font=宋体]实验部分[/font]1.1 [font=宋体]仪器[/font][font=宋体]、试剂及材料[/font][/b][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url](美国[/font]Thermo Fisher [font=宋体]公司,[/font]ICS5000+[font=宋体])配备安培检测器和自动进样器([/font]AS-AP[font=宋体]);[/font]KQ5200DA[font=宋体]型数控超声波清洗器[/font][font=宋体](昆山市超声仪器有限公司);[/font]Milli-QA10[font=宋体]超纯水仪(美国[/font] Millipore [font=宋体]公司);[/font]50%[font=宋体]氢氧化钠溶液([/font]NaOH[font=宋体],分析纯)、乙二胺([/font]EDA [font=宋体]纯度[/font]99%[font=宋体])均购自赛默飞世尔科技中国有限公司;草酸钠([/font]Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体],纯度[/font]99.5%[font=宋体])、乙酸钠([/font]NaAc[font=宋体],纯度[/font]99%[font=宋体])均购自德国[/font]Sigma-Aldrich[font=宋体]公司;乙二胺四乙酸二钠([/font]EDTA[font=宋体],纯度[/font]99.99%[font=宋体])、硫化物标准溶液([/font]100 mg/L[font=宋体])购自上海麦克林生化科技公司[/font][b]1.2 [font=宋体]溶液的配制[/font]1.2.1 [font=宋体]稳定液的配置[/font] [/b][align=left]250mmol/L NaOH-0.8% EDTA[font=宋体]溶液:称取[/font]2.0 g 50%[font=宋体]氢氧化钠溶液、[/font]0.8 g [font=宋体]乙二胺四乙酸二钠于[/font]100 mL [font=宋体]容量瓶中,加入煮沸后冷却的超纯水,定容摇匀。[/font][/align][b]1.2.2 [font=宋体]标准溶液的配置[/font][/b][font=宋体]准确移取[/font]100 mg/L[font=宋体]的硫化物标准溶液,使用[/font]250 mmol/L NaOH-0.8% EDTA[font=宋体]溶液逐级稀释至[/font]1000[font=宋体]、[/font]500[font=宋体]、[/font]200[font=宋体]、[/font]100[font=宋体]、[/font]50[font=宋体]、[/font]20[font=宋体]、[/font]10 μg/L[font=宋体]。硫化物极易被氧化,应现配现用,避光、冷藏保存。(负二价态的硫在[/font]pH[font=宋体]>[/font]8[font=宋体]的碱性溶液中以[/font]HS[sup]-[/sup][font=宋体]状态存在,此后均用硫化物代称)[/font][b]1.2.3[font=宋体]淋洗液的配制[/font][/b][align=left][font=宋体]淋洗液(一)[/font]200 mmol/L NaOH-7.5 mmol/L Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体]溶液:称取[/font]2.0 g[font=宋体]草酸钠、[/font]32.0 g 50% [font=宋体]氢氧化钠溶液于流动相瓶中,加入超纯水至[/font]2 L[font=宋体],超声[/font]30 min[font=宋体]均匀溶液并除去气泡。淋洗液(二)[/font]100 mmol/L NaOH-500 mmol/LNaAc[font=宋体]溶液:称取[/font]41.0 g[font=宋体]乙酸钠、[/font]8.0 g 50% [font=宋体]氢氧化钠溶液于流动相瓶中,加入超纯水至[/font]1 L[font=宋体],超声[/font]30 min[font=宋体]均匀溶液并除去气泡。淋洗液(三)[/font]100 mmol/L NaOH-500 mmol/LNaAc-0.5% EDA[font=宋体]溶液:在淋洗液(二)的基础上添加[/font]5 mL[font=宋体]乙二胺溶液,加入超纯水至[/font]1 L[font=宋体]。[/font][/align][b]1.3 [font=宋体]色谱条件[/font][/b][font=宋体]色谱柱:[/font]IonPacAS7 (250mm×4mm)[font=宋体];保护柱:[/font]IonPacAG7 (50mm×4mm)[font=宋体];检测模式:安培检测;工作电极:[/font]Ag[font=宋体]电极;参比电极:[/font]Ag-AgCl[font=宋体]复合参比电极;电位波形见表[/font]5[font=宋体];淋洗液:[/font]200 mmol/L NaOH-7.5 mmol/L Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体],流速:[/font]1mL/min[font=宋体];柱温:[/font]30℃[font=宋体];进样量:[/font]25μL[font=宋体];[/font][font='Times New Roman',serif]2[/font]结果与讨论[b]2.1[font=宋体]色谱条件的优化[/font]2.1.1[font=宋体]色谱柱的选择[/font][/b] [font=宋体]硫化物分析常用[/font] IonPac AS7[font=宋体]色谱柱,该柱填料微粒较大,柱容量高,适合用于安培检测器测定高离子强度基质中的硫化物、氰化物。选取[/font]IonPac AS7[font=宋体]色谱柱使用[/font]Thermo[font=宋体]默认方法对硫化物进行分析。[/font]AS7[font=宋体]色谱柱说明书中色谱条件:色谱柱:[/font]IonPac AS7 (250mm[font=宋体]×[/font]4mm)[font=宋体];保护柱:[/font]IonPac AG7 (50mm[font=宋体]×[/font]4mm)[font=宋体];检测模式:脉冲安培检测;工作电极:[/font]Ag[font=宋体]电极;参比电极:[/font]Ag-AgCl[font=宋体]复合参比电极;电位波形见表[/font]1[font=宋体];淋洗液:[/font]100 mmol/L NaOH-500 mmol/LNaAc[font=宋体],流速:[/font]1mL/min[font=宋体];柱温:[/font]30 [font=宋体]℃;进样量:[/font]25 μL[font=宋体]。[/font][align=center][b][font=宋体]表[/font] 1 [font=宋体]默认电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]-1.0[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.93[/align] [/td][td] [align=center]-0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]-0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][font=宋体]实验结果显示,硫化物峰存在拖尾现象,低于[/font]100 μg/L[font=宋体]硫化物不能检出,且信号基线较高、噪音较大,掩盖部分低浓度硫化物色谱峰[/font][sup][17][/sup][font=宋体]。[/font][b]2.1.2 [font=宋体]流动相类型的选择[/font][/b][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]使用的专用乙酸钠等级较高,目前国内无法生产,全部依赖进口;此外,淋洗液中高浓度乙酸钠使基线高、噪音大且成本较高,不利于日常分析检测。尝试使用草酸钠替代乙酸钠降低基线噪音,且草酸能与硫化物样品中可能存在的金属离子形成络合物,以避免分析物的损失;乙二胺可作为掩蔽剂减小对硫化物测定的影响。使用淋洗液(一)、(二)(三)测定相同浓度硫化物,考察替换乙酸钠和加入乙二胺的影响。[/font][align=center][font=宋体][img=,313,252]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311053440504_285_1617661_3.jpg!w313x252.jpg[/img][/font][/align][font=宋体][/font][align=center][b][font=宋体]图[/font]1 [font=宋体]不同种淋洗液对基线噪音的影响[/font][/b][/align][font=宋体]实验发现乙二胺加入后硫化物峰形没有改善。低浓度草酸钠代替高浓度的乙酸钠,降低了约五倍噪音(见图[/font]1[font=宋体]),且有非常好的柱效和选择性,草酸钠成本仅是乙酸钠的[/font]0.2%[font=宋体],淋洗液总成本降低近九成,故选用[/font]200 mmol/L NaOH-7.5 mmol/L Na[sub]2[/sub]C[sub]2[/sub]O[sub]4[/sub][font=宋体]进行后续实验。[/font][b]2.1.3 [font=宋体]电位参数的选择[/font][/b][font=宋体]除在流动相中适当添加络合剂外,电位参数的改变可更好改善硫化物峰的突然消失和严重拖尾现象。常规方法分析时[/font]100 μg/L[font=宋体]以下硫化物的色谱峰消失,猜测原因一是部分硫化物被系统中残留的金属离子络合;二是安培检测电位参数不合理,导致部分硫化物未完全参与氧化还原反应;三是电位参数中清洗电位不合理,导致色谱峰拖尾且降低电极一次打磨后的使用寿命[/font][sup][18,19][/sup][font=宋体]。在默认电位波形(表[/font]1[font=宋体])的基础上,尝试改变清洗电位参数,对于低浓度硫化物,施加正向电位[/font]0.1 mV[font=宋体],积分电位[/font]-0.1 mV[font=宋体],仅积分[/font] 0.1 s[font=宋体]。改进电位波形如表[/font]2[font=宋体]所示[/font][sup][20][/sup][font=宋体]。[/font][align=center][b][font=宋体]表[/font]2 [font=宋体]硫化物改进电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.30[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.31[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.40[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center][img=,231,189]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311055220716_7826_1617661_3.jpg!w289x237.jpg[/img][/align][align=center][b][font=宋体]图[/font]2 [font=宋体]改进电位波形下[/font]10 μg/L[font=宋体]硫化物色谱图[/font][/b][/align][font=宋体]由图[/font]2[font=宋体]所示,低浓度[/font]10 μg/L[font=宋体]的硫化物也可检出,且拖尾问题得到明显改善。其中峰尾基线的减少是由于[/font]Ag[sub]2[/sub]S[font=宋体]沉淀后电极表面的电化学恢复,硫化银沉淀被还原,换言之,[/font]Ag[sub]2[/sub]S[font=宋体]沉淀通过产生总体负电流的电势循环而被消除[/font][sup][20][/sup][font=宋体]。[/font][b]2.1.4 [font=宋体]安培积分时长的选择[/font][/b][font=宋体]新改进电位峰面积较小,不利于降低检出限和应用于实际采样检测,尝试增加积分时长以增加积分定量的准确性,提高灵敏度。设置积分时间[/font]0.2[font=宋体]、[/font]0.3[font=宋体]、[/font]0.4[font=宋体]、[/font]0.5[font=宋体]、[/font]0.6[font=宋体]、[/font]0.7s[font=宋体],进样相同浓度的硫化物标准溶液。[/font][align=center][b][font=宋体]表[/font]3 [font=宋体]积分时长对峰面积的影响[/font][/b][/align] [table][tr][td] [align=center][color=black]Integration time[i]/[/i]s[/color][/align] [/td][td] [align=center][color=black]Peak area/(nCmin)[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.2[/color][/align] [/td][td] [align=center][color=black]9.4919[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.3[/color][/align] [/td][td] [align=center][color=black]18.8029[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.4[/color][/align] [/td][td] [align=center][color=black]28.3009[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.5[/color][/align] [/td][td] [align=center][color=black]37.4532[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.6[/color][/align] [/td][td] [align=center][color=black]47.9043[/color][/align] [/td][/tr][tr][td] [align=center][color=black]0.7[/color][/align] [/td][td] [align=center][color=black]57.3832[/color][/align] [/td][/tr][tr][td] [align=center][color=black]Linare equation[/color][/align] [align=center][i][color=black]r2[/color][/i][/align] [/td][td] [align=center][i][color=black]y = 8.307x[sup]2[/sup] + 88.50x - 8.526[/color][/i][color=black] 0.9998[/color][/align] [/td][/tr][/table][align=left][font=宋体]以积分时间([/font]x, s[font=宋体])为横坐标,色谱峰面积([/font]Y[font=宋体])为纵坐标进行线性拟合,表[/font]4[font=宋体]可以看出,满足二次线性方程[/font][i]y = 8.307x[sup]2[/sup] +88.50x - 8.526[/i][font=宋体],线性关系良好,[/font][i]r2[/i] = 0.9998[font=宋体]。但积分时间增加,清洗电位没有改变,硫化物在[/font] Ag [font=宋体]电极上与[/font] AgO [font=宋体]等银氧化物的反应时间延长,加剧银电极消耗,对后续硫化物在电极上响应有影响[/font][sup][21, 22][/sup][font=宋体]。尝试设置积分时长和清洗时长[/font]1[font=宋体]:[/font]1[font=宋体],[/font]3[font=宋体]:[/font]1[font=宋体]等电位波形,观察硫化物色谱峰均不理想,继续改进后选定四电位波形即加入默认电位中的反向清洗电位以期望得到最佳峰形和使用寿命。使用表[/font]4[font=宋体]所示电位检测[/font]100[font=宋体]、[/font]20[font=宋体]、[/font]10 μg/L[font=宋体]硫化物标准溶液,结果见图[/font]3[font=宋体]。[/font][/align][align=center][b][font=宋体]表[/font]4 [font=宋体]硫化物高浓度新电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.80[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.81[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]0.3[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center][img=,690,193]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311056125232_554_1617661_3.png!w690x193.jpg[/img][/align][align=center][b][font=宋体]图[/font] 3 [font=宋体]高浓度电位波形下[/font]100, 20, 10 μg/L[font=宋体]硫化物色谱图[/font][/b][/align][align=left][font=宋体]结果可见中等浓度的色谱峰峰形对称,[/font]100 μg/L[font=宋体]浓度的样品有较好峰形,而低浓度色谱峰出现拖尾现象,故认为表4中四电位波形应用到大于[/font]100 μg/L[font=宋体]较高浓度[/font][font=宋体]硫化物的检测中,能得到令人满意的峰形、灵敏度以及最佳电极使用寿命。 [/font][/align][align=left][font=宋体]而实际环境中能采集到的硫化氢较少,故以低浓度硫化物得到最佳色谱峰形为准,认为正向清洗电位下的色谱峰形最能接受。[/font][font=宋体]最后基于色谱峰形、整个安培电位循环时长、实际采集样品浓度以及[/font] Ag [font=宋体]电极一个打磨周期使用寿命的考虑,在表[/font]4[font=宋体]电位基础上延长积分时间为[/font] 0.7 s[font=宋体]。低浓度样品脉冲安培电位波形如表[/font]5[font=宋体]所示。[/font][/align][align=center][b][font=宋体]表[/font]5 [font=宋体]硫化物低浓度新电位波形[/font][/b][/align] [table][tr][td] [align=center]Time/s[/align] [/td][td] [align=center]Waveform/mV[/align] [/td][td] [align=center]Integration/s[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]Begin[/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]-0.1[/align] [/td][td] [align=center]End[/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]0.1[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center][img=,251,202]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311056231564_7993_1617661_3.jpg!w315x253.jpg[/img][/align][align=center][b][font=宋体]图[/font]4 [font=宋体]低浓度新电位波形下[/font]10 μg/L[font=宋体]硫化物色谱图[/font][/b][/align][font=宋体]图[/font]4[font=宋体]结果表明,此电位下低浓度峰型良好,可应用于实际样品中低浓度硫化物检测。[/font][b]2.2 [font=宋体]硫化物稳定性研究[/font][/b][font=宋体]为延长硫化物稳定存在的时间,尝试在溶剂中添加一定量[/font]EDTA[font=宋体]、[/font]EDA[font=宋体]和抗氧化剂(抗坏血酸([/font]AsA[font=宋体])、次亚磷酸钠([/font]SHP[font=宋体]))减少硫化物的损失[/font][sup][23,24][/sup][font=宋体]。[/font]5[font=宋体]种稳定液作为稀释溶剂,将[/font]100 mg/L[font=宋体]的硫化物标准溶液稀释后避光冷藏储存,于[/font] 0[font=宋体]、[/font]1[font=宋体]、[/font]2[font=宋体]、[/font]3[font=宋体]、[/font]4[font=宋体]、[/font]5[font=宋体]、[/font]8[font=宋体]、[/font]12[font=宋体]、[/font]16 h[font=宋体]后进样,根据色谱峰面积计算剩余浓度,得到不同保存时长下的硫化物含量。结果表明,抗坏血酸的加入,出现杂峰,其他溶液并未出现杂峰;除[/font]EDTA[font=宋体]外几种稳定液中硫化物含量[/font]8 h[font=宋体]即降到[/font]60%[font=宋体]以下,[/font]EDTA[font=宋体]稳定液[/font]3 h[font=宋体]内无明显变化,[/font]16 h[font=宋体]可保持在[/font]90%[font=宋体]以上。[/font][font=宋体]随后讨论加入[/font]EDTA[font=宋体]的最佳含量,选取种质量分数的[/font]250 mmol/L NaOH - EDTA[font=宋体]溶液作将硫化物稀释至[/font]1 mg/L[font=宋体],间隔[/font]0[font=宋体]、[/font]2[font=宋体]、[/font]4[font=宋体]、[/font]6[font=宋体]、[/font]8[font=宋体]、[/font]10 h[font=宋体]进样,各保存时间下硫化物的含量如图[/font]5[font=宋体]所示。[/font][align=center][img=,237,195]https://ng1.17img.cn/bbsfiles/images/2023/10/202310311056308605_1960_1617661_3.jpg!w297x243.jpg[/img][/align][align=center][b][font=宋体]图[/font]5 [font=宋体]不同质量分数的[/font]EDTA [font=宋体]对硫化物稳定性的影响[/font][/b][/align][font=宋体]图[/font]5[font=宋体]结果表明,质量分数为[/font]0.8%[font=宋体]和[/font]1.0%[font=宋体]的[/font]EDTA[font=宋体]均能保证[/font]10 h[font=宋体]内损失[/font]2%[font=宋体]左右,从效果和使用量考虑,使用[/font]250 mmol/L NaOH-0.8% EDTA[font=宋体]作为稳定溶液。[/font][b]2.3 [font=宋体]方法学验证[/font]2.3.1 [font=宋体]线性范围、检出限和定量限[/font][/b][font=宋体]将[/font]100 mg/L[font=宋体]硫化物标准溶液逐级稀释为[/font]0.20[font=宋体]、[/font]0.10[font=宋体]、[/font]0.05 [font=宋体]、[/font]0.02[font=宋体]、[/font]0.01 mg/L [font=宋体]。选择新色谱条件,低浓度电位波形下对系列标准样品依次进样,平行测定[/font]3[font=宋体]次。[/font][align=center][b][font=宋体]表[/font]6 [font=宋体]硫化物的素的线性范围、线性方程、相关系数、检出限和定量限[/font][/b][/align] [table=554][tr][td] [align=center]Compond ([i]n[/i]=3[font=宋体])[/font][/align] [/td][td] [align=center]Linear range /(mg/L )[/align] [/td][td] [align=center]Linear equation[/align] [/td][td] [align=center][i]r2[/i][/align] [/td][td] [align=center]LOD/(μg/L)[/align] [/td][td] [align=center]LOQ/(μg/L)[/align] [/td][/tr][tr][td] [align=center]Sulfide[/align] [/td][td] [align=center]0.01~0.20[/align] [/td][td] [align=center][i]y = 28.99x - 0.467[/i][/align] [/td][td] [align=center]0.9997[/align] [/td][td] [align=center]1.03[/align] [/td][td] [align=center]3.45[/align] [/td][/tr][/table][align=left][font=宋体]以标准样品浓度([/font]x, mg/L[font=宋体])为横坐标,色谱峰面积([/font]Y[font=宋体])为纵坐标进行线性拟合。结果如表[/font]7[font=宋体]所示,在[/font]0.01~0.20 mg/L[font=宋体]范围内线性关系良好[/font][i]r[sup]2[/sup][/i][font=宋体]>[/font]0.999[font=宋体],以信噪比[/font][i]S/N[/i]≥[font=宋体]3确定检出限为[/font] 1.03 μg/L[font=宋体],以[/font][i]S/N[/i] ≥ 10[font=宋体]确定定量限为[/font]3.45 μg/L[font=宋体]。与原方法相比,新色谱条件可用于[/font]100 μg/L[font=宋体]以下硫化物的分析,检出限和定量限更低,对空气中微量硫化氢气体检测有重要意义。[/font][/align][b]2.3.2 [font=宋体]重复性[/font][/b][font=宋体]对配制好的[/font]0.1 mg/L[font=宋体]硫化物标准样品平行进样[/font]6[font=宋体]次。结果表明,硫化物的峰面积和保留时间均[/font]RSD%≤0.20%[font=宋体],说明该方法精密度高,重复性好且适用于实际样品检测。[/font][b]2.3.3 [font=宋体]回收率[/font][/b][font=宋体]使用徽章式被动采样器[/font][sup][25][/sup][font=宋体]采集硫化物,对回收率进行验证。向[/font]100 μL[font=宋体]硫化氢被动采样吸收液中加入[/font]0.2[font=宋体]、[/font]0.1 mg/L[font=宋体]硫化物标准溶液[/font]0.05 mL[font=宋体],[/font]30 min[font=宋体]后,加入[/font]250 mmol/L NaOH-0.8% EDTA [font=宋体]溶液[/font]5 ml[font=宋体]超声提取[/font]15 min[font=宋体]检测,获得被动采样方法回收率。向准备好的被动采样器中分别加入[/font]50 mg/L[font=宋体]硫化物标准溶液[/font]0.025[font=宋体]、[/font]0.05[font=宋体]、[/font]0.1 mL[font=宋体],得低、中、高三组加标采样器,与另一组不加标采样器相同条件下采样三天,加入[/font]250 mmol/L NaOH-0.8% EDTA [font=宋体]溶液[/font]5 ml[font=宋体]超声提取[/font]15 min[font=宋体]后检测,获得实际采样回收率。[/font][align=center][b][font=宋体]表[/font]7 [font=宋体]硫化物两个浓度下被动采样方法回收率和实际采样回收率[/font][/b][/align] [table=99%][tr][td] [color=black] [/color] [/td][td=3,1] [align=center][color=black]Method recovery[/color][sup][color=black]*[/color][/sup][/align] [/td][td=4,1] [align=center][color=black]Sampling recovery[/color][sup][color=black]*[/color][/sup][/align] [/td][/tr][tr][td] [align=center][color=black] [/color][/align] [/td][td] [align=center][color=black]Found[/color][/align] [align=center][color=black]mg/L[/color][/align] [/td][td] [align=center][color=black]Added[/color][/align] [align=center][color=black]mg/L[/color][/align] [/td][td] [align=center][color=black]Recovery[/color][/align] [align=center][color=black]%[/color][/align] [/td][td] [align=center][color=black]Background[/color][/align] [align=center][color=black] mg/L[/color][/align] [/td][td] [align=center][color=black]Added mg/L[/color][/align] [/td][td] [align=center][color=black]Found[/color][/align] [align=center][color=black]mg/L[/color][/align] [/td][td] [align=center][color=black]Recovery[/color][/align] [align=center][color=black]%[/color][/align] [/td][/tr][tr][td] [align=center][color=black]High concentration[/color][/align] [/td][td] [align=center][color=black]0.1910[/color][/align] [/td][td] [align=center][color=black]0.2000[/color][/align] [/td][td] [align=center][color=black]95.5[/color][/align] [/td][td] [align=center][color=black]0.9557[/color][/align] [/td][td] [align=center][color=black]0.2500[/color][/align] [/td][td] [align=center][color=black]1.1344[/color][/align] [/td][td] [align=center][color=black]80.7[/color][/align] [/td][/tr][tr][td] [align=center][color=black]Low concentration[/color][/align] [/td][td] [align=center][color=black]0.0988[/color][/align] [/td][td] [align=center][color=black]0.1000[/color][/align] [/td][td] [align=center][color=black]98.9[/color][/align] [/td][td] [align=center][color=black]0.5019[/color][/align] [/td][td] [align=center][color=black]0.5000[/color][/align] [/td][td] [align=center][color=black]0.9456[/color][/align] [/td][td] [align=center][color=black]91.2[/color][/align] [/td][/tr][/table] [font=宋体]*[/font] Method Recovery=Found/Added [font=Symbol]′[/font] 100%.[font=宋体]*[/font]SamplingRecovery=(Found[font=宋体]-[/font]Background)/Added[font=Symbol]′[/font] 100%.[align=left][font=宋体]结果表明(见表[/font]7[font=宋体]),两种浓度下方法回收率均大于[/font]95%[font=宋体],采样回收率均大于[/font]80%[font=宋体]。[/font][/align][b]2.4 [font=宋体]实际样品检测[/font][/b]垃圾站是日常生活场所中硫化氢含量较高的区域,由微生物在厌氧条件下分解有机物产生[sup][font='Times New Roman',serif][26][/font][/sup]。将组装好的被动采样器置于学校两处垃圾处理站,隔[font='Times New Roman',serif]12 h[/font]取出一批,加入[font='Times New Roman',serif]250 mmol/L NaOH-0.8% EDTA [/font]溶液[font='Times New Roman',serif]5 ml[/font]超声提取[font='Times New Roman',serif]15min[/font]后检测。根据如下公式[sup][font='Times New Roman',serif][25][/font][/sup]计算得到环境中的硫化氢气体含量,结果如表[font='Times New Roman',serif]9[/font]所示。[align=center]C=m[sub]s[/sub]/at[/align]式中[font='Times New Roman',serif]t[/font]为被动采样的时间[font='Times New Roman',serif]h[/font],[font='Times New Roman',serif]C[/font]为硫化氢气体在时间[font='Times New Roman',serif]t[/font]内空气中硫化氢的平均浓度[font='Times New Roman',serif]μg/m[sup]3[/sup][/font],[font='Times New Roman',serif]m[sub]s[/sub][/font]为采样器在时间[font='Times New Roman',serif]t[/font]小时内采集到硫化氢气体的总质量[font='Times New Roman',serif]μg[/font]。[font='Times New Roman',serif]a=1.1836×10[sup]-4[/sup][/font]为被动采样的吸收系数[font='Times New Roman',serif]m[sup]3[/sup]/h[/font]。[align=center][b][font=宋体]表[/font]8 [font=宋体]学校垃圾站点硫化氢浓度检测结果[/font][/b][/align] [table=631][tr][td=4,1] [align=center]Position[font=宋体]Ⅰ[/font][/align] [/td][td=4,1] [align=center]Position[font=宋体]Ⅱ[/font][/align] [/td][/tr][tr][td] [align=center]Time (h)[/align] [/td][td] [align=center]Concentration in the extract/(mg/L)[/align] [/td][td] [align=center]Adsorbed H[sub]2[/sub]S mass/(μg)[/align] [/td][td] [align=center]Concentration in the air (μg/m[sup]3[/sup])[/align] [/td][td] [align=center]Time (h)[/align] [/td][td] [align=center]Concentration in the extract/(mg/L)[/align] [/td][td] [align=center]Adsorbed H[sub]2[/sub]S mass/(μg)[/align] [/td][td] [align=center]Concentration in the air /(μg/m[sup]3[/sup])[/align] [/td][/tr][tr][td] [align=center]12[/align] [/td][td] [align=center]0.028[/align] [/td][td] [align=center]0.140[/align] [/td][td] [align=center]9.856[/align] [/td][td] [align=center]12[/align] [/td][td] [align=center]0.017[/align] [/td][td] [align=center]0.085[/align] [/td][td] [align=center]5.985[/align] [/td][/tr][tr][td] [align=center]24[/align] [/td][td] [align=center]0.036[/align] [/td][td] [align=center]0.180[/align] [/td][td] [align=center]6.337[/align] [/td][td] [align=center]24[/align] [/td][td] [align=center]0.026[/align] [/td][td] [align=center]0.130[/align] [/td][td] [align=center]4.576[/align] [/td][/tr][tr][td] [align=center]36[/align] [/td][td] [align=center]0.073[/align] [/td][td] [align=center]0.365[/align] [/td][td] [align=center]8.550[/align] [/td][td] [align=center]36[/align] [/td][td] [align=center]0.0563[/align] [/td][td] [align=center]0.280[/align] [/td][td] [align=center]6.571[/align] [/td][/tr][tr][td] [align=center]48[/align] [/td][td] [align=center]0.089[/align] [/td][td] [align=center]0.445[/align] [/td][td] [align=center]7.833[/align] [/td][td] [align=center]48[/align] [/td][td] [align=center]0.085[/align] [/td][td] [align=center]0.425[/align] [/td][td] [align=center]7.481[/align] [/td][/tr][tr][td] [align=center]72[/align] [/td][td] [align=center]0.126[/align] [/td][td] [align=center]0.630[/align] [/td][td] [align=center]7.393[/align] [/td][td] [align=center]72[/align] [/td][td] [align=center]0.097[/align] [/td][td] [align=center]0.485[/align] [/td][td] [align=center]5.691[/align] [/td][/tr][/table][font=宋体]表[/font]9[font=宋体]可以看出学校内两个垃圾站点中硫化氢含量均未超过国家规定居民区硫化氢的限值[/font]0.01 mg/m[sup]3[/sup] [sup][27][/sup][font=宋体]。[/font][font='Times New Roman',serif]3 [/font]结论[font=宋体]本文针对硫化物常规安培检测中灵敏度不高以及保存稳定性差的问题,对比不同环境下硫化物的保存效果,最终选定质量分数[/font]250 mmol/L NaOH-0.8% EDTA[font=宋体]作为稳定剂,可保证[/font]10 h[font=宋体]内测定结果稳定;在淋洗液中加入草酸钠替代醋酸钠,同时对安培积分电位、积分时长等条件进行优化。结果表明该分析方法试剂成本只有原来的[/font]10%[font=宋体],线性范围拓宽,拟合效果更好,检出限、定量限更低,采样回收率提高到[/font]80%[font=宋体]以上,[/font][font=宋体]更适用于日常微量硫化氢的实际检测。[/font][font=宋体] [/font][font=宋体] [/font][b][font=宋体]参考文献:[/font][/b][font='Times New Roman',serif][1] [/font][font='Times New Roman',serif]Czarnota J,Mas?oń A, Pajura R. Int. J. Environ. Res. Public Health, 2023, 20 (7): 5379[/font][font='Times New Roman',serif][2] [/font][font='Times New Roman',serif]Godoi A F L,Grasel A M, Polezer G, et al. Total Environ, 2018, 610-611: 583-590[/font][font='Times New Roman',serif][3] [/font][font='Times New Roman',serif] Zeng Z G, Lin T, Kang T. Guang Xi Journal ofLight Industry, 2008, (03): 89-90 [/font][font=宋体]曾志果,林铁,康媞[/font][font='Times New Roman',serif]. [/font][font=宋体]广西轻工业[/font][font='Times New Roman',serif], 2008, (3): 89-90[/font][font='Times New Roman',serif][4] [/font][font='Times New Roman',serif]Zhou W, PengM, Liang Q X, et al. Chin. J. Org. Chem, 2023, 43, 1-9[/font][font='Times New Roman',serif][5] [/font][font='Times New Roman',serif]He C T,Morden Chemical Research, 2022, (19):72-74[/font][font=宋体]何楚婷[/font][font='Times New Roman',serif]. [/font][font=宋体]当代化工研究[/font][font='Times New Roman',serif], 2022, (19): 72-74[/font][font='Times New Roman',serif][6] [/font][font='Times New Roman',serif]GB/T7714-2017, Soil and sediment - Determination of sulfide -Methylene bluespectrophotometric method:[s][/s][/font][s][font='Times New Roman',serif]GB/T 7714-2017, [/font][font=宋体]土壤和沉积物[/font][font=宋体]硫化物的测定[/font][font=宋体]亚甲基蓝分光光度法[/font][font='Times New Roman',serif]: [s][/s][/font][s][font='Times New Roman',serif][7] [/font][font='Times New Roman',serif]GB/T14678-1993, Air quality-Determination of sulfuretted hydrogen, methylsulfhydryl, dimethyl sulfide and dimethyl disulfide - Gas chromatography[s][/s][/font][s][font='Times New Roman',serif]GB/T 14678-1993, [/font][font=宋体]空气质量[/font][font=宋体]硫化氢、甲硫醇、甲硫醚和二甲二硫的测定[/font][font=宋体]气相色谱法[/font][font='Times New Roman',serif][s][/s][/font][s][font='Times New Roman',serif][8] [/font][font='Times New Roman',serif]Liu B, Liu JL, Wang R, et al. Chinese Journal of Inorganic Analytical Chemistry, 2023, 13(04):349-355[/font][font=宋体][color=#333333][back=white]刘[/back][/color][/font][font=宋体]冰,刘金蓉,王莹,等[/font][font='Times New Roman',serif]. [/font][font=宋体]中国无机分析化学[/font][font='Times New Roman',serif], 2023, 13(04): 349-355[/font][font='Times New Roman',serif][9] [/font][font='Times New Roman',serif]Liu H Y,Metrology & Measurement Technique, 2021, 48(11): 79-81[/font][font=宋体]刘红英[/font][font='Times New Roman',serif]. [/font][font=宋体]计量与测试技术[/font][font='Times New Roman',serif], 2021, 48 (11)[/font][font=宋体]:[/font][font='Times New Roman',serif]79-81[/font][font='Times New Roman',serif][10] [/font][font='Times New Roman',serif] Ba H S, Khir M H, Al-douri Y, et al. J PhysConf Ser, 2021, 1962(1): 012003[/font][font='Times New Roman',serif][11] [/font][font='Times New Roman',serif] Chen S W, Song T T, Yin X W, Electron Devices,2020, 43(4): 736-40[/font][font=宋体]陈书旺,宋彤彤,尹晓伟[/font][font='Times New Roman',serif]. [/font][font=宋体]电子器件[/font][font='Times New Roman',serif], 2020, 43(4): 736-40[/font][font='Times New Roman',serif][12] [/font][font='Times New Roman',serif]Jiang H,Morden Chemical Research, 2020, (20): 119-120[/font][font=宋体]蒋辉[/font][font='Times New Roman',serif]. [/font][font=宋体]当代化工研究[/font][font='Times New Roman',serif], 2020, (20): 119-120[/font][font='Times New Roman',serif][13] [/font][font='Times New Roman',serif] Zhou L L, Zhou C, Sun H X, Hunan NonferrousMetals, 2022, 38(4): 74-77[/font][font=宋体]周璐璐,周超,孙海侠[/font][font='Times New Roman',serif]. [/font][font=宋体]湖南有色金属[/font][font='Times New Roman',serif], 2022, 38(4): 74-77[/font][font='Times New Roman',serif][14] [/font][font='Times New Roman',serif]Jiao Y J, LiY J, Ningxia Journal of Agriculture and Forestry Science and technology, 2013, 54(03):100-102[/font][font=宋体]焦玉娟,李玉洁[/font][font='Times New Roman',serif]. [/font][font=宋体]宁夏农林科技[/font][font='Times New Roman',serif], 2013, 54(03): 100-102[/font][font='Times New Roman',serif][15] [/font][font='Times New Roman',serif]Zhang Y, FuJ, Cao J B, et al, Occupation and Health, 2017, 33(15): 2068-2070[/font][font=宋体]张妍,傅佳,曹建彪[/font][font='Times New Roman',serif]. [/font][font=宋体]职业与健康[/font][font='Times New Roman',serif], 2017, 33(15): 2068-2070[/font][font='Times New Roman',serif][16] [/font][font='Times New Roman',serif] Li R Y, Liang L N, Li J, Chinese Journal ofChromatography, 28(12): 1158-1161[/font][font=宋体]李仁勇,梁立娜,李静[/font][font='Times New Roman',serif]. [/font][font=宋体]色谱[/font][font='Times New Roman',serif], 2010, 28 (12): 1158-1161[/font][font='Times New Roman',serif][17] [/font][font='Times New Roman',serif]Jaszczak E,Koziol K, Kielbratowska B, et al. J Chromatogr B, 2019, 1110-1111: 36-42[/font][font='Times New Roman',serif][18] [/font][font='Times New Roman',serif] Liu X L, Wang J, Materials Protection, 2001,34(3): 1-3[/font][font=宋体]刘秀玲,王佳[/font][font='Times New Roman',serif]. [/font][font=宋体]材料保护[/font][font='Times New Roman',serif], 2001, 34(3): 1-3[/font][font='Times New Roman',serif][19] [/font][font='Times New Roman',serif]Jaszczak E,Narkowicz S, Namiesik J, et al. Monatsh Chem, 2017, 148(9): 1645-1649[/font][font='Times New Roman',serif][20] [/font][font='Times New Roman',serif] Caterina G, Silvano C, Alfredo G, et al. JChromatogr A, 2004, 1023(1): 105-112[/font][font='Times New Roman',serif][21] [/font][font='Times New Roman',serif] Inoue A, Earley R L, Lehmann M W, et al.Talanta, 1998, 46(6): 1507-1540[/font][font='Times New Roman',serif][22] [/font][font='Times New Roman',serif] Liang L, Cai Y, Mou S, et al. J Chromatogr A,2005, 1085(1): 37-41[/font][font='Times New Roman',serif][23] [/font][font='Times New Roman',serif]Hafer E,Holzgrabe U, Kraus K, et al. Magn Reson Chem, 2020, 58(7): 653-655[/font][font='Times New Roman',serif][24] [/font][font='Times New Roman',serif] Wang Y Z, Yu T X, Xing Y, Chemistry andAdhesion, 2011, 33(3): 77-79[/font][font=宋体]王玉芝,于天霞,邢宇[/font][font='Times New Roman',serif]. [/font][font=宋体]化学与黏合[/font][font='Times New Roman',serif], 2011, 33(3): 77-79[/font][font='Times New Roman',serif][25] [/font][font='Times New Roman',serif]Ni T,[/font][font=宋体][[/font][font='Times New Roman',serif]MSDissertation[/font][font=宋体]][/font][font='Times New Roman',serif]East China University of Science and Technology, 2023[/font][font=宋体]倪彤[/font][font='Times New Roman',serif].[/font][font=宋体][硕士学位论文][/font][font='Times New Roman',serif]. [/font][font=宋体]上海[/font][font='Times New Roman',serif]: [/font][font=宋体]华东理工大学[/font][font='Times New Roman',serif], 2023[/font][font='Times New Roman',serif][26] [/font][font='Times New Roman',serif]Murei A,Kamika I, Samie A, et al. Sci Rep, 2023, 13(1): 6250[/font][font='Times New Roman',serif][27] GBZ2.1-2019 Occupational exposure limits for hazardous agents in the workplace[/font][font=宋体]—[/font][font='Times New Roman',serif]Part 1: Chemical hazardous agents[/font][font='Times New Roman',serif]GBZ 2.1-2019 [/font][font=宋体]工作场所有害因素职业接触限值[/font][font=宋体]第[/font][font='Times New Roman',serif]1[/font][font=宋体]部分:化学有害因素[/font][font='Times New Roman',serif] [/font][font='Times New Roman',serif] [/font][/s][/s][/s][/s]
因化学原料药出口,需要依照国外药典检测组分和杂质,相关仪器要求如下,希望有能力的检测单位留下联系方式,或者和我联系0755-26514276,QQ34498139,谢谢大家!Column:— size: l =0.25m, Ф=4.6mm,— stationary phase: styrene-divinylbenzene copolymer R (8 μm) with a pore size of 100 nm,— temperature: 55°CPost-column solution: a carbonate-free sodium hydroxide solution diluted 1 to 25, previously degassed, which is added pulse-less to the column effluent using a 375 μl polymeric mixing coil.Detection: pulsed amperometric detector or equivalent with a gold indicator electrode, a silver-silver chloride reference electrode, and a stainless steel auxiliary electrode which is the cell body, held at respectively + 0.05 V detection, + 0.75 V oxidation and 0.15 V reduction potentials, with pulse durations according to the instrument used.
脉冲测试仪是检测什么用的?
脉冲式均质器在食品微生物快速检测中应用研究 随着经济的发展,人民对食品安全性的要求也日益提高,如何更快更好的检测出食品能否放心食用就显得尤为重要。微生物指标是食品检测中一个重要的指标,而传统的检测方法操作准备繁琐且样品前处理带有一定的缺陷和局限性。为了提高检测效率,微生物检测可使用快速检测方法。现行国际上常用的快速检测方法为使用快速测试片。由于测试片上含有冷水可溶性凝胶,因此无需传统方法中倾倒琼脂的步骤,从而避免了对细菌可能造成的热损伤。相对于传统平板检测方法操作简便、结果稳定,具有良好的实用性能,可大大简化操作程序,提高检测速度。为了快速检测方法能更好的开展,选择适宜的样品前处理的均质方式可使检测数据更真实可靠。本文通过研究新式的脉冲式均质器与传统的拍打式、旋转搅拌式在使用效果上的差异,以得出使用脉冲式均质器在食品微生物快速检测中更优的结论。 一.材料(1) 试验材料 美国3M公司细菌总数测试片,美国3M公司酵母菌/霉菌测试片,检测样品来源于市场随机购买。(2) 主要培养基平板计数琼脂培养基、孟加拉红培养基、伊红美蓝琼脂、Baird-Parker 琼脂基础、亚硫酸铋(BS)琼脂。以上培养基均由广东环凯微生物科技有限公司提供。(3) 主要仪器设备ShockMixer-1 脉冲式样品前处理器(环凯制造)、拍打式均质器、搅拌式均质器、振荡器、高压蒸气灭菌锅、超净工作台、电子天平、移液枪、生化培养箱。(4) 菌株大 肠 埃 希 菌 、金黄色葡萄球菌、福氏志贺氏菌、乙型副伤寒沙门氏菌。以上菌种均由广东环凯微生物科技有限公司提供。(5) 脉冲式均质器的工作原理通过高频率震动内装食品样品的专用胶袋,产生强烈冲击波与高速搅动联合作用,将食品中的微生物驱赶到样品悬液中,形成菌浓度均匀的样品稀释液。减轻了对样品的破坏,从而极大地减少了样品碎片的产生。食品样液澄清度高,能与快速检测方法更配套。 二.试验方法1.平板法
[b]脉冲放电检测器[/b] 脉冲放电检测器(pulsed discharge detector)是一种氦光离子化检侧器,当用纯氮作载气和放电气体时,它具通用型检测器功能,像氦离子化检测器(HID)一样,既能灵敏检测无机气体。如H2、O2、CO、CO2、H2O等。又能灵敏检测有机化合物.如烃、含杂原子(氧、硫、卤素)化合物、农药、金属配合物等,称PDHID,最小可检度低至皮克级,线性范围是105。若放电气中有微量氩、氪或氙作掺杂气时,则会改变光子能里,使检测器具有相当于11.7eV, 10.2eV和9.5eV三种PID的功能,它们分别称为Ar-PDPID,Kr-PDPID和Xe-PDPID。如果氦中有CH4掺杂气,就可以改变为非放射源的电子俘获检测器(PDECD)。此外还可以在PDHID)上收集光谱信号以取得分析物的定性和定量信息,称脉冲放电发射检测器(PDED)。1.检测器结构 PDHID、PDECD是l992年Wentworth等在HID的基础上提出引入的,以后又逐步作了改进,近两年已正式成为商品仪器, PDHID和PDECD的结构基本一样,图2.90是PDECD池的横截面图。检侧池主体是一个长95mm内径14mm的中空不锈钢圆筒。分隔成放电区和反应区,放电区(1)是在一块20mm长3mm内径的石英圆筒块〔7)上装有两个放电电极〔3),放电电极的末端是ф0.25-0.5mm的铂金尖端,两个电极间距约1.6mm ,脉冲放电周期是300μs,脉冲宽度是20-40μs,放电电压20V,产生20mA放电电流,放电互径是0.1-0.15mm.在反应区(2)有两个偏压电极(4.5;150V,2V)和一个收集电极(6),它们之间用四块长8mm,内径3mm的蓝宝石绝缘(8),用黄金O型圈压紧密封,He(30mL/min)从检测池顶部(9)引进放电区,色谱柱(11)从检测池底部插人,柱出口在收集电极(6)和偏压电极(5)之间,PDECD的掺杂气亦是从检测池底部的管(12)引入,管直伸至两个偏压电极(4)和(5)之间,亦即掺杂气是在毛细管桂出口上方加人,也有从偏压电极(4)处加人掺杂气。色谱柱流出物、掺杂气流与He放电气逆流。在反应区发生离子化。PDECD很长容易就可以改成PDEID,PDHID不需加入掺杂气,收集电极(6)和偏压电极(5)的位置互换,收集极位于两个偏压电极之间.因为采用石英和蓝宝石作绝缘材料,检测器使用温度提高了,最高操作温度可达400℃。
各位有无求有关脉冲放电离子化检测器的资料?原理,使用注意事项等?[em33]
火焰光度检测器( FPD)和脉冲火焰光度检测器( PFPD)的区别测有机磷可以使用 : 火焰光度检测器( FPD)或脉冲火焰光度检测器( PFPD),我们单位只有使用过火焰光度检测器( FPD)检测有机磷,请问大家其与脉冲火焰光度检测器( PFPD)检测有机磷有什么区别?
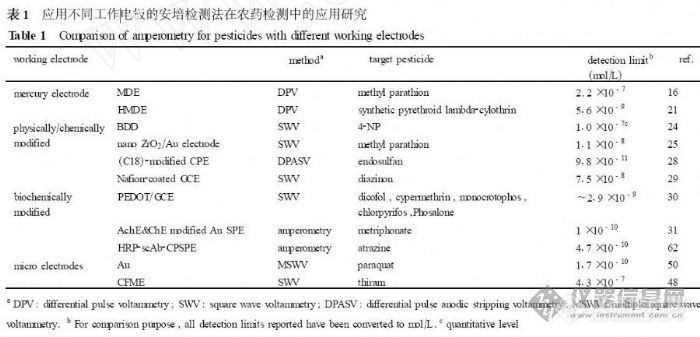
[B]农药残留的安培检测法[/B][I]李竹赟 王敏[/I]摘 要:建立灵敏高效的农药分析方法对于有效解决由农残超标引起的食品卫生安全和环境污染等问题具有重要意义。安培检测法作为一种简便、快速、灵敏、准确的电化学方法,最近几年来被越来越多地应用于农药分析研究,其研究热点主要集中于通过对电化学体系中工作电极的选择和优化来改善检测的性能,提高灵敏度,降低检测限。本文根据检测体系中工作电极的分类从常规电极、修饰电极以及微电极等3方面对农药残留安培检测体系的研究进展作了综述,认为集成便携化是农残电化学检测方法的研究发展趋势。关键词 农药残留 安培检测法 修饰电极 微电极 农药的广泛应用有效解决了农作物的病虫害问题,但由于许多农药及其降解产物会使农作物、畜禽和水产等动植物体受到不同程度的污染,通过食物链的富集作用,危害人体的健康与食品安全, 因而长期大量使用农药又引发了相应的食品安全问题和环境污染问题。建立灵敏和高效的农药残留分析方法对于有效解决由农残超标引起的卫生安全和环境污染甚至由此涉及的经济贸易等问题具有重要意义。[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]、高效液相色谱以及色谱-质谱联用技术等仪器分析方法具有准确、高效、灵敏和高通量等特点, 已被广泛应用于农药残留分析的实际工作。与此同时,灵敏的农残光谱检测法也得到了发展。但上述方法分析周期长、设备昂贵且需要特殊的测试环境,因而不易推广。为满足环境中大量样品的现场快速检测要求,基于农药生化特性制得的各种酶试剂盒和速测卡不断推出。但据调查研究,许多速测卡的灵敏度、重现性不高而成本较高,因此多数仅用于农药残留的初步定性筛选。事实上,许多农药或其衍生物含有硝基、苯环以及卤素等具有电化学活性的基团,它们在电极表面具有很好的氧化还原性,非常适合于电化学检测。与上述方法相比,电化学检测方法可直接得到电信号,易传递,具有设计简单、成本低、易于微型化和多元化、并有多种电化学研究方法可供选择等优点,适合于自动控制和在线灵敏、快速分析。其中,对可控电压下样品在电极表面发生氧化或还原反应产生的电解电流进行检测的方法,即安培检测法,具有极高的灵敏度,并可能一次性测出多种成分。因此,安培检测法多年来已被广泛应用于生物医学、环境科学、药物学以及食品科学等领域,成为分析科学中最具活力、最有发展前景的研究领域之一。 但是,农药分子的直接电化学检测并没有得到足够的重视,在这方面报道很少。直到最近几年,电化学检测尤其是安培检测法才逐渐成为农药残留检测方法研究的热点。为提高检测灵敏度,很多研究工作都集中在对安培检测体系的工作电极进行选择和修饰加工方面。本文根据安培检测法工作电极的不同,按照常规电极、修饰电极和微电极进行分类对农残安培检测法的研究作了综述,并简要讨论了检测体系的集成化研究情况。文中将以最佳检测结果为依据,列举典型的工作电极组成的农药安培检测方法于表1 ,以便于读者对不同方法进行比较。[img]http://ng1.17img.cn/bbsfiles/images/2008/03/200803011152_80213_1613333_3.jpg[/img][color=#DC143C][B]全文附件在7楼,有需要的可以下载。[/B][/color]
代人问个问题,安培检测器和电导检测器不同吧?有没有版友的离子色谱配的是安培检测器?离子色谱的检测器有几种类型啊?
脉冲检测器突然没有信号显示是什么原因啊
使用的ICS6000+安培检测器的搭配,淋洗液是醋酸盐缓冲液加甲醇,在进样过程中出峰的响应不稳定,一直增加!(同一个溶液一个小时内的峰面积增加3%),想知道有可能是什么原因导致的响应一直增加
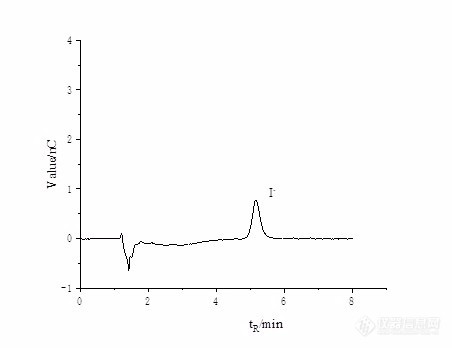
[align=left][font=times new roman][size=24px][color=#ff0000]本论文是国内第一篇采用全国产设备和色谱柱的,使用脉冲安培器的研究论文。[/color][/size][/font][/align][align=left][font='times new roman'][size=16px][/size][/font][/align][align=left][font='times new roman'][size=16px]国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]安培检测器快速测定废水中碘离子含量[/size][/font][/align][align=left][font='times new roman'][size=16px]施超欧[/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px]*[/size][/font][font='times new roman'][size=16px] 赵晓含[/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px] 李泳谊[/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px] 李晓[/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]张业平[/size][/font][font='times new roman'][size=16px]2[/size][/font][font='times new roman'][size=16px] [/size][/font][/align][align=left][font='times new roman'][size=16px]([/size][/font][font='times new roman'][size=16px]1[/size][/font][font='times new roman'][size=16px].[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]华东理工大学 化学与分子工程学院[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]分析测试中心[/size][/font][font='times new roman'][size=16px] 上海 200237[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]2[/size][/font][font='times new roman'][size=16px].[/size][/font][font='times new roman'][size=16px] [/size][/font][font='times new roman'][size=16px]通用(深圳)仪器有限公司 深圳 [/size][/font][font='times new roman'][size=16px][color=#333333]518038[/color][/size][/font][font='times new roman'][size=16px][color=#333333])[/color][/size][/font][/align][align=left][b][font=宋体]摘[/font][font=宋体]要:[/font][/b][font=宋体]目前国内利用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定水中碘离子含量的多数报道是利用进口仪器如[/font]Thermo[font=宋体]和[/font]Metrohm[font=宋体],鲜有利用全套国产仪器进行水中碘离子含量的测定,特别是国产脉冲安培检测器并没有相关报道。将在[/font]Thermo ICS5000+ [font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]上开发的快速测定水中碘[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]条件应用到全套国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font]-[font=宋体]安培检测器上进行方法学验证实验。结果表明:[/font]I[sup]-[/sup] [font=宋体]在[/font]5 μg/L~100 μg/L[font=宋体]的浓度范围内线性关系良好,相关系数达到[/font]0.9998[font=宋体]以上,进样量[/font]100 μl[font=宋体]时检出限为[/font]1.03 μg/L[font=宋体],定量限为[/font]3.42 μg/L[font=宋体]([/font]3S/N[font=宋体]),进样重复性良好,加标回收率在[/font]93 %~99.4 %[font=宋体]之间。检出限和测定下限仅为国标抑制[/font]-[font=宋体]电导法的[/font]1/5[font=宋体]左右,符合国家标准,能够满足[/font]I[sup]-[/sup] [font=宋体]的低浓度检测,为国产仪器的推广应用提供一个可行的方案。[/font][b][font=宋体]关键词:[/font][/b][font=宋体]国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url] 脉冲安培检测碘离子 快速柱[/font][/align][align=left][font=宋体][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]是液相色谱的一个分支,因其前处理简单,检测灵敏度高,已成为分析无机阴离子的首选方法[/font][sup][1][/sup][font=宋体]。碘离子在天然水体中含量很低,而[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法对低含量的无机阴离子检测灵敏度极高,常见阴离子在电导检测器中检出限[/font]≤10 μg/L[font=宋体],安培检测器基于电活性物质在给定电位下发生氧化或还原反应产生的相应电流为响应,检出限相比电导检测器更低。因此近年来应用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法安培法测定水中碘离子含量愈加广泛。[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定水中碘离子的检测方法主要有抑制[/font]-[font=宋体]电导法、紫外和安培法,淋洗液通常选用碳酸盐体系或氢氧根体系,碳酸盐体系洗脱能力强且[/font]pH[font=宋体]较低,氢氧根体系洗脱能力弱于碳酸盐体系,但在抑制[/font]-[font=宋体]电导法中检测背景较碳酸盐体系小。张俊华[/font][sup][2][/sup][font=宋体]和李叙柏[/font][sup][3][/sup][font=宋体]利用抑制[/font]-[font=宋体]电导法在氢氧根体系检测水中碘化物,两篇报道的方法检出限小于[/font]0.35 μg/L[font=宋体](进样量[/font]500 μL[font=宋体]),碘离子保留时间为[/font]10 min[font=宋体]左右;宋冰冰等人[/font][sup][4][/sup][font=宋体]利用抑制[/font]-[font=宋体]电导法在碳酸盐体系快速检测水中碘离子,方法检出限为[/font]2 μg/L[font=宋体](进样量[/font]250 μL[font=宋体]),碘离子在[/font]12 min[font=宋体]内出峰;刘克纳等人[/font][sup][5][/sup][font=宋体]在氢氧根体系分别使用电导、直流安培和紫外检测器建立痕量碘离子的快速检测方法,碘离子保留时间分别为[/font]5.97[font=宋体]、[/font]4.43[font=宋体]和[/font]4.46 min[font=宋体],[/font]50 μL[font=宋体]进样量检出限分别为[/font]30[font=宋体]、[/font]1[font=宋体]和[/font]25 μg/L[font=宋体]。蒋园园等人[/font][sup][6][/sup][font=宋体]在碳酸盐体系分别用电导和直流安培检测器测定清洁水样中碘离子含量,进样量[/font]250 μL[font=宋体]时电导检测器检出限为[/font]2 μg/L[font=宋体],直流安培检测器检出限为[/font]0.03 μg/L[font=宋体],碘离子在[/font]22.5 min[font=宋体]出峰。在氢氧根体系使用脉冲安培检测器测定高浓度氯离子存在下的痕量碘离子,佘小林等人[/font][sup][7][/sup][font=宋体]建立的方法检出限为[/font]0.2 μg/L[font=宋体],碘离子在[/font]7 min[font=宋体]内出峰;而韩静等人[/font][sup][8][/sup][font=宋体]使用浓缩柱对饱和卤水中的痕量碘离子进行富集,进样量[/font]50 μL[font=宋体]时检出限低至[/font]0.07 μg/L[font=宋体]。[/font][font=宋体]可以看出,抑制[/font]-[font=宋体]电导法灵敏度较安培法低,因此需要大体积进样才能获得较低的检出限,直流安培法是在固定电位下检测,银工作电极表面容易中毒导致检测重复性和灵敏度稍差,而脉冲安培法具备清洗电位,检测灵敏度和稳定性较直流安培法更优,另外在实际操作中发现,高[/font]pH[font=宋体]条件下[/font]Ag[font=宋体]电极稳定性较差,不超过[/font]2[font=宋体]天就要抛光打磨,而碳酸盐体系下[/font]Ag[font=宋体]电极稳定性较好,可以连续使用一个星期以上。[/font][font=宋体]目前国内利用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定水中碘离子含量的多数报道是利用进口仪器如[/font]Thermo[font=宋体]和[/font]Metrohm[font=宋体],少有利用全套国产仪器进行水中碘离子含量的测定,郭芳芳等人[/font][sup][9][/sup][font=宋体]用青岛盛瀚的[/font]CIC300[font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],抑制[/font]-[font=宋体]电导法检测水中碘离子含量,方法检出限为[/font]2 μg/L[font=宋体],但利用国产安培检测器测定碘离子并没有报道。本文基于针对定制尺寸的碘离子快速分析柱在[/font]Thermo ICS5000+[font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]上开发的快速测定水中碘离子方法,基于碳酸盐体系下,安培检测器的稳定性和重复性优于氢氧根体系,选定了碳酸钠作为淋洗液,脉冲安培法具备更优的检测灵敏度和稳定性。将最佳色谱条件应用到自行研制的全套国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]上,包括自动进样器、四元梯度泵、安培检测器(脉冲电位)、安培检测池、参比电极、[/font]Ag[font=宋体]工作电极([/font]1 mm[font=宋体])和膜片,进行方法学验证实验,由此评价国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器整机的性能。[/font][b]1 [font=宋体]仪器和材料[/font][/b][font=宋体]国产[/font]GI 5000 [font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],包括自动进样器,四元梯度泵,[/font]Eclipse[font=宋体]色谱工作站,国产安培检测器[/font]GI-5250[font=宋体],含国产安培检测池、国产参比电极、国产自制银电极([/font]1 mm[font=宋体])、自制膜片([/font]25 μm[font=宋体]),通用(深圳)仪器有限公司;色谱柱为[/font]I[sup]- [/sup][font=宋体]快速分析柱([/font]3*150 mm[font=宋体]),自主定制;[/font]Millipore-QA10[font=宋体]超纯水机,美国[/font]Millipore[font=宋体]公司。[/font][font=宋体]无水[/font]Na[sub]2[/sub]CO[sub]3[/sub][font=宋体],优级纯,纯度[/font]≥99.8%[font=宋体],上海阿拉丁生化科技公司;水中碘,[/font]100 μg/mL[font=宋体],国家有色金属及电子材料分析测试中心。[/font][b]2 [font=宋体]溶液的配制[/font][/b]2.1 [font=宋体]淋洗液的配制[/font][font=宋体]精确称取[/font]4.24 g[font=宋体]无水[/font]Na[sub]2[/sub]CO[sub]3[/sub][font=宋体]于淋洗液瓶中,使用超纯水溶解并超声,定容至[/font]2 L[font=宋体],得到[/font]20 mmol/L[font=宋体]的[/font]Na[sub]2[/sub]CO[sub]3[/sub][font=宋体]溶液作为淋洗液[/font]B[font=宋体]路。[/font]2.2 [font=宋体]标准溶液的配制[/font][font=宋体]移取上述碘标准溶液[/font]1 mL[font=宋体],使用超纯水逐级稀释得到[/font]1 mg/L[font=宋体]的[/font]I[sup]- [/sup][font=宋体]标准溶液,现配现用。[/font]2.3 [font=宋体]样品溶液的配制[/font][font=宋体]采集华东理工大学不同河道排污废水样,使用[/font]0.45 μm[font=宋体]水系微孔滤膜进行过滤,弃去初滤液[/font]3mL[font=宋体]后,将后续废水滤液收集至离心管中,作为待测废水样,冷藏待用。[/font]2.4 [font=宋体]色谱条件[/font][font=宋体]色谱柱:定制尺寸的碘离子快速分析柱[/font]3*150 mm[font=宋体];流速:[/font]0.4 mL/min[font=宋体]。[/font][font=宋体]淋洗液:[/font]A[font=宋体]路[/font][font=宋体]超纯水:[/font]B[font=宋体]路[/font] 20 mmol/L Na[sub]2[/sub]CO[sub]3[/sub]=60:40[font=宋体];[/font][font=宋体]柱温:[/font]30 ℃[font=宋体];进样量:[/font]100 μL[font=宋体];检测器:安培检测器(脉冲电位)。[/font][font=宋体]脉冲电位如表[/font]1[font=宋体]。[/font][/font][/align][align=left][font=宋体][font=宋体][/font][/font][/align][align=center][font=宋体]表[/font]1 [font=宋体]脉冲安培检测电位[/font][/align][align=center]Table 1 Pulse ampere detection potential[/align] [table=304][tr][td] [align=center][font=宋体]时间[/font]/s[/align] [align=center]Time/s[/align] [/td][td] [align=center][font=宋体]电位[/font]/V[/align] [align=center]Potential/V[/align] [/td][/tr][tr][td] [align=center]0.00[/align] [/td][td] [align=center]-0.10[/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]-0.10[/align] [/td][/tr][tr][td] [align=center]0.90[/align] [/td][td] [align=center]-0.10[/align] [/td][/tr][tr][td] [align=center]0.91[/align] [/td][td] [align=center]-1.00[/align] [/td][/tr][tr][td] [align=center]0.93[/align] [/td][td] [align=center]-0.30[/align] [/td][/tr][tr][td] [align=center]1.00[/align] [/td][td] [align=center]-0.30[/align] [/td][/tr][/table][align=left][font=宋体][b]3 [font=宋体]实验结果与讨论[/font][/b]3.1[font=宋体]色谱条件的选择[/font][font=宋体]基于定制柱的尺寸(直径[/font]3 mm[font=宋体])选定流速为[/font]0.4 mL/min[font=宋体];选取[/font]303.13 K[font=宋体]([/font]30 [font=宋体]℃)保证方法普适性与检测灵敏度;[/font]Ag[font=宋体]工作电极在高[/font]pH[font=宋体]环境下稳定性较差,使检测背景逐渐升高,而碳酸钠体系,[/font]pH[font=宋体]较低,[/font]Ag[font=宋体]电极稳定性较好,同时考虑可兼容电导,因此最终选择[/font]8.0 mmol/L[font=宋体]的[/font]Na[sub]2[/sub]CO[sub]3[/sub][font=宋体]。[/font]3.2 [font=宋体]干扰实验[/font][font=宋体]为验证该体系下其他阴离子对于[/font]I[sup]-[/sup] [font=宋体]的测定无影响,以在安培检测器上有响应的[/font]Br[sup] -[/sup][font=宋体]、[/font]CN[sup]-[/sup][font=宋体]、[/font]S[sup]2-[/sup][font=宋体]、[/font]SCN[sup]- [/sup][font=宋体]共[/font]4[font=宋体]种常见阴离子进行干扰实验,在安培检测器上[/font]Br[sup] -[/sup][font=宋体]、[/font]CN[sup]-[/sup][font=宋体]、[/font]S[sup]2-[/sup][font=宋体]、[/font]SCN[sup]-[/sup] [font=宋体]均不会对[/font]I[sup]-[/sup] [font=宋体]在该定制柱上的保留时间和相应峰高、峰面积产生影响,该体系适用于实际样品中[/font]I[sup]-[/sup] [font=宋体]的测定。[/font]3.3 [font=宋体]线性关系和检出限[/font][font=宋体]在最佳色谱条件下,对配制好的一系列的线性标准溶液在国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器上进行测定,采用[/font]100 μL[font=宋体]定量环。每个浓度的[/font]I[sup]-[/sup] [font=宋体]标准溶液平行测定[/font]3[font=宋体]次,检测结果如下表。[/font][/font][/align][align=left][font=宋体][font=宋体][/font][/font][/align][align=center][font=宋体]表[/font]2 [font=宋体]不同浓度的[/font]I- [font=宋体]标准样品的安培检测结果[/font][/align][align=center]Table 2 Amperometric detection results of I- standard samples with different concentrations [/align] [table=479][tr][td] [align=center][font=宋体]浓度[/font][/align] [/td][td] [align=center][font=宋体]峰面积[/font][/align] [/td][td] [align=center]RSD%[/align] [/td][td] [align=center][font=宋体]峰高[/font][/align] [/td][td] [align=center]RSD%[/align] [/td][td] [align=center][font=宋体]噪音[/font][/align] [/td][td] [align=center][font=宋体]背景[/font][/align] [/td][/tr][tr][td] [align=center]/(μg/L[font=宋体])[/font][/align] [/td][td] [align=center]/(nC*s)[/align] [/td][td] [align=center][font=宋体]([/font]n=3[font=宋体])[/font][/align] [/td][td] [align=center]/nC[/align] [/td][td] [align=center][font=宋体]([/font]n=3[font=宋体])[/font][/align] [/td][td] [align=center]/nC[/align] [/td][td] [align=center]/nC[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]3.970[/align] [/td][td] [align=center]2.4[/align] [/td][td] [align=center]0.2267[/align] [/td][td] [align=center]2.5[/align] [/td][td] [align=center]0.014[/align] [/td][td] [align=center]2.850[/align] [/td][/tr][tr][td] [align=center]10[/align] [/td][td] [align=center]8.640[/align] [/td][td] [align=center]1.9[/align] [/td][td] [align=center]0.4533[/align] [/td][td] [align=center]1.3[/align] [/td][td] [align=center]0.016[/align] [/td][td] [align=center]2.860[/align] [/td][/tr][tr][td] [align=center]25[/align] [/td][td] [align=center]20.04[/align] [/td][td] [align=center]0.32[/align] [/td][td] [align=center]1.083[/align] [/td][td] [align=center]0.53[/align] [/td][td] [align=center]0.013[/align] [/td][td] [align=center]2.860[/align] [/td][/tr][tr][td] [align=center]50[/align] [/td][td] [align=center]40.44[/align] [/td][td] [align=center]0.38[/align] [/td][td] [align=center]2.117[/align] [/td][td] [align=center]0.98[/align] [/td][td] [align=center]0.016[/align] [/td][td] [align=center]2.870[/align] [/td][/tr][tr][td] [align=center]100[/align] [/td][td] [align=center]81.22[/align] [/td][td] [align=center]1.4[/align] [/td][td] [align=center]4.100[/align] [/td][td] [align=center]0.98[/align] [/td][td] [align=center]0.012[/align] [/td][td] [align=center]2.860[/align] [/td][/tr][tr][td] [align=center][font=宋体]线性关系[/font][/align] [/td][td=2,1] [align=center]y = 0.8105x + 0.062[/align] [/td][td=2,1] [align=center]y = 0.0407x + 0.0498[/align] [/td][/tr][tr][td] [align=center]R2[/align] [/td][td=2,1] [align=center]0.9999[/align] [/td][td=2,1] [align=center]0.9998[/align] [/td][/tr][/table][align=left][font=宋体][font=宋体]如表[/font]2[font=宋体]所示,在国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器上进行[/font]I[sup]- [/sup][font=宋体]测定时,每个浓度的[/font]I[sup]- [/sup][font=宋体]标准溶液平行测定的[/font]RSD[font=宋体]值≤[/font]2.5 %[font=宋体],说明国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器状态较为稳定。工作电极打磨后,背景值较低,稳定在[/font]2.860 nC[font=宋体]附近,噪音则≤[/font]0.016 nC[font=宋体]。[/font][font=宋体]使用国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]测定[/font]I[sup]- [/sup][font=宋体]时,在[/font]5 μg/L~100 μg/L[font=宋体]的浓度范围内线性关系良好,峰面积相关系数达到[/font]0.9999[font=宋体]以上。经计算可得,检出限为[/font]1.03 μg/L[font=宋体],定量限为[/font]3.42 μg/L[font=宋体]([/font]3[font=宋体]倍信噪比)。[/font]3.4 [font=宋体]重复性[/font][font=宋体]为考察该国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font]-[font=宋体]安培检测器是否符合实际检测应用需求,需进一步考察其稳定性。分别取高中低浓度的标准样品溶液:[/font]10 μg/L[font=宋体]、[/font]50 μg/L[font=宋体]、[/font]250 μg/L[font=宋体]的[/font] I[sup]- [/sup][font=宋体]标准溶液连续进样,每个标准浓度重复测定[/font]8[font=宋体]次,结果如下表[/font]3[font=宋体]。[/font][/font][/align][align=center][font=宋体]表[/font]3 [font=宋体]国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]上不同浓度的[/font]I[sup]-[/sup] [font=宋体]标准样品的重复性考察结果([/font]n=8[font=宋体])[/font][/align][align=left][font=宋体][font=宋体] [/font][/font][table=628][tr][td=1,2] [align=center][font=宋体]序号[/font][/align] [/td][td=4,1] [align=center]10 μg/L[/align] [/td][td=3,1] [align=center]50 μg/L[/align] [/td][td=4,1] [align=center]250 μg/L[/align] [/td][/tr][tr][td] [align=center]t[sub]R[/sub][/align] [align=center]/min[/align] [/td][td] [align=center][font=宋体]峰面积[/font][/align] [align=center]/(nC*s)[/align] [/td][td] [align=center][font=宋体]峰高[/font][/align] [align=center]/nC[/align] [/td][td=2,1] [align=center]t[sub]R[/sub][/align] [align=center]/min[/align] [/td][td] [align=center][font=宋体]峰面积[/font][/align] [align=center]/(nC*s)[/align] [/td][td=2,1] [align=center][font=宋体]峰高[/font][/align] [align=center]/nC[/align] [/td][td] [align=center]t[sub]R[/sub][/align] [align=center]/min[/align] [/td][td] [align=center][font=宋体]峰面积[/font][/align] [align=center]/(nC*s)[/align] [/td][td] [align=center][font=宋体]峰高[/font][/align] [align=center]/nC[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]5.36[/align] [/td][td] [align=center]8.340[/align] [/td][td] [align=center]0.46[/align] [/td][td=2,1] [align=center]5.34[/align] [/td][td] [align=center]41.02[/align] [/td][td=2,1] [align=center]2.16[/align] [/td][td] [align=center]5.29[/align] [/td][td] [align=center]190.9[/align] [/td][td] [align=center]9.38[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]5.36[/align] [/td][td] [align=center]8.240[/align] [/td][td] [align=center]0.48[/align] [/td][td=2,1] [align=center]5.33[/align] [/td][td] [align=center]41.06[/align] [/td][td=2,1] [align=center]2.18[/align] [/td][td] [align=center]5.29[/align] [/td][td] [align=center]188.4[/align] [/td][td] [align=center]9.31[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]5.36[/align] [/td][td] [align=center]8.680[/align] [/td][td] [align=center]0.46[/align] [/td][td=2,1] [align=center]5.33[/align] [/td][td] [align=center]42.25[/align] [/td][td=2,1] [align=center]2.20[/align] [/td][td] [align=center]5.30[/align] [/td][td] [align=center]187.0[/align] [/td][td] [align=center]9.23[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]5.36[/align] [/td][td] [align=center]8.530[/align] [/td][td] [align=center]0.46[/align] [/td][td=2,1] [align=center]5.33[/align] [/td][td] [align=center]41.11[/align] [/td][td=2,1] [align=center]2.16[/align] [/td][td] [align=center]5.30[/align] [/td][td] [align=center]187.0[/align] [/td][td] [align=center]9.33[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]5.36[/align] [/td][td] [align=center]8.260[/align] [/td][td] [align=center]0.45[/align] [/td][td=2,1] [align=center]5.33[/align] [/td][td] [align=center]40.58[/align] [/td][td=2,1] [align=center]2.16[/align] [/td][td] [align=center]5.29[/align] [/td][td] [align=center]190.3[/align] [/td][td] [align=center]9.34[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]5.35[/align] [/td][td] [align=center]8.370[/align] [/td][td] [align=center]0.46[/align] [/td][td=2,1] [align=center]5.32[/align] [/td][td] [align=center]40.55[/align] [/td][td=2,1] [align=center]2.16[/align] [/td][td] [align=center]5.30[/align] [/td][td] [align=center]186.2[/align] [/td][td] [align=center]9.27[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]5.35[/align] [/td][td] [align=center]8.480[/align] [/td][td] [align=center]0.46[/align] [/td][td=2,1] [align=center]5.33[/align] [/td][td] [align=center]42.52[/align] [/td][td=2,1] [align=center]2.20[/align] [/td][td] [align=center]5.29[/align] [/td][td] [align=center]188.2[/align] [/td][td] [align=center]9.44[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]5.36[/align] [/td][td] [align=center]8.040[/align] [/td][td] [align=center]0.45[/align] [/td][td=2,1] [align=center]5.33[/align] [/td][td] [align=center]41.43[/align] [/td][td=2,1] [align=center]2.20[/align] [/td][td] [align=center]5.29[/align] [/td][td] [align=center]192.0[/align] [/td][td] [align=center]9.34[/align] [/td][/tr][tr][td] [align=center]RSD%[/align] [/td][td] [align=center]0.086[/align] [/td][td] [align=center]2.4[/align] [/td][td] [align=center]2.0[/align] [/td][td=2,1] [align=center]0.10[/align] [/td][td] [align=center]1.7[/align] [/td][td=2,1] [align=center]0.91[/align] [/td][td] [align=center]0.10[/align] [/td][td] [align=center]1.1[/align] [/td][td] [align=center]0.69[/align] [/td][/tr][/table][/align][align=left][font=宋体]从表中可得,保留时间的重复性最佳,[/font]RSD[font=宋体]值均≤[/font]0.10%[font=宋体],峰高的[/font]RSD[font=宋体]值≤[/font]2.0%[font=宋体],峰面积的[/font]RSD[font=宋体]值在[/font]2.4%[font=宋体]以下,以上结果表明该国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font]-[font=宋体]安培检测器的检测重复性良好,可满足检测需求。[/font]3.5 [font=宋体]实际样品的测定和加标回收率[/font]I[sup]-[/sup] [font=宋体]标样色谱图如图[/font]1[font=宋体],使用相同的色谱条件,将待测废水样品在国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器上直接进样进行分析,未检测出碘离子。加标废水样品色谱图如图[/font]2[font=宋体]。[/font][img=,452,348]https://ng1.17img.cn/bbsfiles/images/2021/09/202109211739586401_7706_1617661_3.jpg!w452x348.jpg[/img][img=,452,348]https://ng1.17img.cn/bbsfiles/images/2021/09/202109211740039838_3464_1617661_3.jpg!w452x348.jpg[/img][/align][align=center][font=宋体]图[/font]1 I[sup]- [/sup][font=宋体]标样色谱图 [/font][font=宋体]图[/font][font=宋体]2 [/font][font=宋体]加标废水样品的检测图谱[/font][/align][align=center][font=宋体][font=宋体]进行高低两个水平的加标回收测定,平行测定[/font]6[font=宋体]次。检测结果如表[/font]4[font=宋体]所示。[/font][/font][/align][align=center][font=宋体]表[/font]4 [font=宋体]废水样品检测结果、加标量以及回收率测定[/font][/align][align=center]Table 4 The detection results, standard addition and recovery rate determinationof wastewater samples [/align] [table=505][tr][td] [align=center][font=宋体]测定次数[/font][/align] [/td][td] [align=center][font=宋体]加标量[/font]1[font=宋体]([/font]15μg/L[font=宋体])[/font][/align] [align=center][font=宋体]测定值[/font]μg/L[/align] [/td][td] [align=center][font=宋体]加标量[/font]2[font=宋体]([/font]25μg/L[font=宋体])[/font][/align] [align=center][font=宋体]测定值[/font]μg/L[/align] [/td][td] [align=center][font=宋体]加标回收率[/font]1[/align] [align=center]%[/align] [/td][td] [align=center][font=宋体]加标回收率[/font]2[/align] [align=center]%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]14.34[/align] [/td][td] [align=center]23.25[/align] [/td][td] [align=center]95.6[/align] [/td][td] [align=center]93.0[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]14.62[/align] [/td][td] [align=center]23.40[/align] [/td][td] [align=center]97.5[/align] [/td][td] [align=center]93.6[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]14.62[/align] [/td][td] [align=center]24.21[/align] [/td][td] [align=center]97.5[/align] [/td][td] [align=center]96.8[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]14.65[/align] [/td][td] [align=center]24.24[/align] [/td][td] [align=center]97.7[/align] [/td][td] [align=center]97.0[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]14.73[/align] [/td][td] [align=center]24.60[/align] [/td][td] [align=center]98.2[/align] [/td][td] [align=center]98.4[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]14.77[/align] [/td][td] [align=center]24.85[/align] [/td][td] [align=center]98.5[/align] [/td][td] [align=center]99.4[/align] [/td][/tr][/table][font=宋体]总的来看,加标回收率集中在[/font]93.0%~99.4%[font=宋体]之间,符合国家标准。以上数据表明,国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font]-[font=宋体]安培检测器的开发已经较为成熟,可满足实际样品的分析测定。[/font]3.6 [font=宋体]与国标方法对比[/font][font=宋体]将采用全套国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器([/font]GI-5000[font=宋体])测定结果的检出限和定量限,与进口仪器测定结果和国标方法规定值进行对比。[/font][align=center][font=宋体]表[/font]5 [font=宋体]国产仪器检测灵敏度与国标方法对比[/font][/align][align=center]Table 5 Comparison of detection sensitivity of domestic instruments withnational standard methods[font=宋体]([/font]3S/N[font=宋体])[/font][/align] [table=693][tr][td] [align=center][font=宋体]仪器设备[/font][/align] [/td][td] [align=center][font=宋体]方法[/font][/align] [/td][td] [align=center][font=宋体]进样量[/font]/μL[/align] [/td][td] [align=center][font=宋体]检出限[/font]/(μg/L)[/align] [/td][td] [align=center][font=宋体]定量限[/font]/(μg/L)[/align] [/td][/tr][tr][td] [align=center][font=宋体]进口仪器[/font][/align] [/td][td] [align=center][font=宋体]常规阴离子交换柱[/font]-[font=宋体]抑制电导法[/font][sup][10][/sup][/align] [/td][td] [align=center]250[/align] [/td][td] [align=center]2.00[/align] [/td][td] [align=center]8.00[/align] [/td][/tr][tr][td] [align=center]GI 5000[/align] [/td][td] [align=center][font=宋体]定制[/font]I[sup]- [/sup][font=宋体]快速分析柱[/font]-[font=宋体]安培检测器[/font][/align] [/td][td] [align=center]100[/align] [/td][td] [align=center]1.03[/align] [/td][td] [align=center]3.42[/align] [/td][/tr][/table][font=宋体]如表[/font]5[font=宋体]所示,采用全套国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]器设备,并采用定制柱开发的方法测定[/font]I[sup]- [/sup][font=宋体],灵敏度高,检出限低,仅为国标方法检出限和测定下限的[/font]1/5[font=宋体]左右(按照相同的进样量换算),符合国家标准,能够满足[/font]I[sup]- [/sup][font=宋体]的低浓度快速检测。根据众多用户的反馈,在很多情况下即使根据国标法采用进口设备进行检测,很多情况下也难以达到[/font]2 μg/L[font=宋体]的检出限,而采用本文的全套国产安培系统,在常规的条件下,检出限优于国标中的抑制[/font]-[font=宋体]电导法,实际操作难度更低,可为实验提供更为可靠简单的方案。[/font][b]4 [font=宋体]结论[/font][/b][font=宋体]利用全套国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font]-[font=宋体]安培检测器对已开发方法进行方法学验证实验,结果表明:国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font]-[font=宋体]安培检测器测定[/font]I[sup]- [/sup][font=宋体]时,在[/font]5 μg/L~100 μg/L[font=宋体]的浓度范围内线性关系及进样重复性良好,加标回收率在[/font]93%~99.4%[font=宋体]之间,在[/font]250 μL[font=宋体](换算后)进样量时检出限和定量限为国标方法的[/font]1/5[font=宋体]左右,能够实现[/font]I[sup]- [/sup][font=宋体]的低浓度快速检测,这填补了国产[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]尤其是安培检测器应用的空白。[/font][align=center][font=宋体][font=宋体][/font][/font][/align][align=center][font=宋体]参考文献[/font][1][font='Times New Roman'] [/font]MouS F, Liu K N, Ding X J. Ion Chromatography Method and Application (2[sup]nd[/sup]Edition) [M].Beijing: Chemical IndustryPress, 2005: 1.[font=宋体]牟世芬[/font],[font=宋体]刘克纳[/font], [font=宋体]丁晓静[/font]. [font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]方法及应用[/font]. [font=宋体]第[/font]2[font=宋体]版[/font][M]. [font=宋体]北京[/font]: [font=宋体]化学工业出版社[/font], 2005: 1.[2][font='Times New Roman'] [/font]ZhangJ H. Shanxi Science and Technology[J], 2020,35(2): 94-96.[font=宋体]张俊华[/font].[font=宋体]山西科技[/font][J], 2020,35(2): 94-96.[3][font='Times New Roman'] [/font]LiX B, Zhang Y, Jiang W W. Water Purification Technology[J], 2017,36(4): 84-86.[font=宋体]李叙柏[/font],[font=宋体]张琰[/font],[font=宋体]姜巍巍[/font]. [font=宋体]净水技术[/font][J], 2017,36(4): 84-86.[4][font='Times New Roman'] [/font]SongB B, Tian Y, Li R Y, Qin D L, Lin H L, Guo Q, Zhu Y, Luo Y P. TheAdministration and Technique of Environmental Monitoring[J], 2017,29(4): 50-52,56.[font=宋体]宋冰冰[/font],[font=宋体]田耘[/font], [font=宋体]李仁勇[/font], [font=宋体]秦迪岚[/font], [font=宋体]林海兰[/font], [font=宋体]郭倩[/font], [font=宋体]朱颖[/font], [font=宋体]罗岳平[/font]. [font=宋体]环境监测管理与技术[/font][J], 2017,29(4):50-52,56.[5][font='Times New Roman'] [/font]LiuK N, Mou S F, Chai C W. PTCA (PART B: CHEMICAL ANALYSIS) [J], 2001,37(8): 337-338,342.[font=宋体]刘克纳[/font],[font=宋体]牟世芬[/font], [font=宋体]柴成文[/font]. [font=宋体]理化检验[/font] ([font=宋体]化学分册[/font]) [J],2001,37(8):337-338,342.[6][font='Times New Roman'] [/font]JinagY Y, Cheng H, Xu L. Environmental Monitoring and Forewarning[J], 2020,12(2): 31-35.[font=宋体]蒋园园[/font],[font=宋体]程海[/font], [font=宋体]徐蕾[/font]. [font=宋体]环境监控与预警[/font][J], 2020,12(2): 31-35.[7][font='Times New Roman'] [/font]SheX L, Li R Y, Chen Y Y, Hu L. Modern Scientific Instruments[J], 2010(6): 139-140.[font=宋体]佘小林[/font],[font=宋体]李仁勇[/font], [font=宋体]陈园园[/font], [font=宋体]胡兰[/font]. [font=宋体]现代科学仪器[/font][J], 2010(6):139-140.[8][font='Times New Roman'] [/font]HanJ, Liang L N, Mou S F, Cai Y Q, Lu Y Q. Chinese Journal of Analytical Chemistry[J],2008,36(2):187-191.[font=宋体]韩静[/font],[font=宋体]梁立娜[/font], [font=宋体]牟世芬[/font], [font=宋体]蔡亚岐[/font], [font=宋体]鲁毅强[/font]. [font=宋体]分析化学[/font][J],2008,36(2): 187-191.[9][font='Times New Roman'] [/font]GuoF F, Dai C, Zhang S Y. Chemical Enterprise Management[J],2017(35): 192.[font=宋体]郭芳芳[/font],[font=宋体]戴超[/font], [font=宋体]张书玉[/font]. [font=宋体]化工管理[/font][J],2017(35): 192.[10][font='Times New Roman'] [/font]HJ 778-2015 Waterquality-Determination of iodide-Ion chromatiography[s].HJ 778-2015 [font=宋体]水质[/font][font=宋体]碘化物的测定[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/font][s]. [/s][/s][/align][align=left][font=宋体][b][font='Times New Roman','serif'][/font][/b][/font][/align]
请问有哪位专家使用过PDD(脉冲放电检测器),它的原理,性能,特点,及能检测的组分,急盼赐教!
离子色谱安培检测器能检测哪些离子?
RT.现在接触到一些便携式、或在线检测的重金属仪器,大都使用阳极溶出伏安法ASV,而没有使用微分脉冲伏安法DPV?请问大侠们,为啥啊?
要用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]检测糖,原来测定其他项目用的电导池,现在要换成安培检测。但工作站的控制面板上检测器那块积分安培栏输不了电压数据,参比电极那块也不能操作,而检测器液晶面板上显示的也是电导池的数据,用LOCAL方式把界面改成积分安培模式了,一接工作站就变回了电导模式,请教各位老师怎么办?我刚接触[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url],好多不懂的,急!