呵呵,各位同仁,想请大家帮个忙:一般药品质量的检测会用到哪些仪器设备?知道的请尽快回个贴,请大家帮帮忙了,很急的![em0804]
有没有哪位大虾知道怎样证明药物检测包括药品质量检测技术这个专业?我也知道我问的问题很搞笑,显而易见药物检测就是包含药品质量检测技术这个专业,但是我所在地的人事局非要让你拿出依据证明药物检测包含药品质量检测技术,要不然就不给报考。很明显就是故意刁难啊!可是我不服,希望哪个大虾能给予指点!!!
药品质量检测是根据药物的剂型来制订. 片剂:有重量差异检查,崩解时限检查,溶出度检查,含量均匀度检查,还有外观检查. 注射剂:澄明度,装量,注射用无菌粉末的装量差异,注射液中不溶性微粒,热原试验,无菌试验,注射剂中油溶剂的检查,含量测定 胶囊剂:胶囊的外观检查,装量差异检查,崩解时限检查,含量测定 软膏剂:外观检查,最低装量检查,粒度检查,微生物限度检查,含量测定 复方制剂比较复杂....考虑剂型的附加剂,赋形剂,所含有效成分之间的互相干扰.
2010年11月8日,中检所支持广州亚运会药品质量快速检测车交接仪式在广州举行。国家食品药品监管局办公室副主任王桂忠、中检所副所长李波、广东省食品药品监管局局长陈元胜及省局领导班子成员、广州市食品药品监管局党委书记房明玉、局长姚建明、广州市药品检验所所长江英桥等领导出席了交接仪式。交接仪式由广东省食品药品监管局党组成员、纪检组长、监察专员陈鲁峰主持。为支援广州亚运会期间的药品质量安全监管保障工作,中检所为广州市药品检验所配备了1台国内最先进的药品质量快速检测车。在国家局的高度重视和大力支持下,中检所于2003年主持研制了具有自主知识产权的药品检测车,把信息技术、化学分析技术和近红外无损伤检测技术融于一体,建立了车载的移动快检实验室,是用于假劣药品快速筛查的一类新技术、新方法。此次为支援广州亚运会赛会药品质量安全监管,在原有检测设备的基础上新配备了车载高效液相色谱仪和拉曼光谱仪以及大量简便易用的小型快检仪器,是目前我国技术最先进、设备最齐全、各种仪器设备配备最新的“旗舰车”。房明玉介绍了涉亚运食品药品保障工作情况,并就对全力以赴做好赛时亚运餐饮服务食品和药品安全保障工作进行了总动员。他表示,一定会举全系统之力,尽心尽力,尽职尽责地做好广州亚运会和残运会药品质量安全保障工作。最后,李波和江英桥共同签署了支持2010年广州亚运会药品质量快速检测保障工作备忘录。
药品质量监督检验检测规章制度与工作标准规范实务全书由于本书容量过大19.5MB,故分成三个压缩分卷[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=45617]药品质量监督检验检测规章制度与工作标准规范实务全书.part1[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=45618]药品质量监督检验检测规章制度与工作标准规范实务全书.part2[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=45619]药品质量监督检验检测规章制度与工作标准规范实务全书.part3[/url]药品监督与检验是控制和保证药品质量的重要手段,药品检验的结果准确与否直接关系到人民群众的用药安全和生命健康,涉及到药品行政监督机关的处罚。药品监督检验部门和药品检验人员在工作中药努力做到药品监督检验标准化、规范化和管理科学化,确保药品检验数据及检验结论的准确公正,避免和杜绝差错事故的发生。推进药品检验检测工作标准化,规范化和管理科学化,健全药品监督检验检测制度,确保药品检验准确公正【目录浏览】:《药品质量监督检验检测规章制度与工作标准规范实务全书》《药品质量监督检验检测规章制度与工作标准规范实务全书》第一篇 总论第一章 概论第二章 药品管理体制机构第三章 药品监督管理组织与管理制度第四章 药品监督管理职能和任务第五章 药品管理行政执法第六章 药品管理法律责任第七章 国家药物管理政策第二篇 药品检验工作规章制度第一章 药品检验人员管理第二章 药检人员工作职责与制度第三章 药检所管理工作程序第四章 药检工作规范第五章 药检业务管理工作制度第六章 科室管理与考核第三篇 药品质量检验、检测综合管理制度第一章 概论第二章 药品标准第三章 药品检验标准物质第四章 药品检验菌种管理第五章 药品检验信息管理第六章 药品检验仪器设备管理第七章 药品不良反应监测制度第八章 药品检验技术管理第九章 药品检验化学试剂第四篇 药品质量检验鉴定技术与操作规范第一章 概论第二章 假劣药的一般鉴别试验第三章 药品的一般鉴别试验第四章 药物物理常数的测定第五章 药物含量的化学测定第六章 药品生物测定第七章 药物杂质检查第八章 药物仪器分析检验方法第九章 制剂质量检查第十章 质量标准分析方法验证和稳定性试验第五篇 药品生产质量检验管理与药品GMP监管制度第一章 药品生产质量管理第二章 药品生产质量管理的基本准则第三章 药品生产厂房与设施规范第四章 药品生产管理操作规范第五章 质量管理第六章 卫生管理第七章 生产自检第八章 药品GMP认证管理制度第六篇 药品经营质量管理制度与行政监督第一章 药品经营质量管理第二章 医药商品经营质量监管第三章 药品经营企业开办审批管理第四章 药品采购管理制度第五章 药品供应管理政策第七篇 医疗机构药品、药剂质量检验监管制度与管理规范第一章 概论第二章 医疗机构药事管理第三章 医药行业标准化制度和管理规范第四章 医疗机构药剂采购保管制度第五章 医疗机构药品质量检验制度第六章 医疗单位处方和调剂管理制度第七章 医疗机构药剂质量标准和质量管理制度第八章 医疗机构药品效期管理制度和方法第九章 合理用药制度第八篇 药品行政管理制度与国家法律监管第一章 概论第二章 药品研制管理制度与法律监管第三章 医疗器械管理制度与法律监管第四章 药品生产管理制度与法律监管第五章 药品价格管理及其违法责任第六章 药品经营管理制度与法律监管第七章 中药管理制度与法律监管第八章 特殊药品管理制度与法律监管第九章 药品使用管理制度与法律监管第九篇 药品、药材检验检测规范与国家标准第十篇 药品监管与药品法规规范读者对象各食品药品监督管理局、医药管理局、卫生局各省市县药检所各制药生产企业各药品经营企业、销售集团公司各全国各大医院、医疗卫生机构各工商局(所)、质监局各大专院校、科研单位、图书馆

2015年04月16-17日第五届中国药品质量安全大会在杭州开元名都大酒店成功举行,此次大会组委会邀请中外著名专家学者、企业家代表出席,对我国药品安全相关法规政策及新的技术标准做解读,并进行新技术应用方案交流。吸引了全国各地方药检机构,制药企业、科研院所等领域专家和学者近600人前来交流学习。http://ng1.17img.cn/bbsfiles/images/2017/10/2015042216524214_01_1987954_3.jpg2015第五届中国药品质量安全大会会议现场迪马科技作为全球领先的色谱消耗品制造商,始终关注药品质量安全,并积极为药品检测机构及企业提供整体解决方案,开发了一系列关于药品含量测定、杂质分析、有关物质鉴定、药物合成等方面的应用。目前在迪马科技官网应用数据库可检索到的药品应用近千篇,《迪马科技产品发表文献集》收录的国内外使用迪马科技产品发表的药品质量安全文献近3500篇,以实际行动为药品质量安全保驾护航。http://ng1.17img.cn/bbsfiles/images/2015/04/201504221658_543079_1987954_3.jpg迪马科技应用数据库及产品发表文献集参与此次药品质量安全大会,迪马科技为与会药品分析工作者带来了多款可用于药品分析检测的气、液相色谱柱,特别带来了Diamonsil(钻石)家族新产品——Diamonsil Plus,该产品具有“超长使用寿命 & 极性改性 & 100%水相~100%有机相 & 快速分析 & 超高柱效”等多重优异性能于一身,极大扩展色谱柱应用范围,减少色谱柱选择和方法开发时间。同时超长的色谱柱使用寿命,极大降低色谱柱使用成本,为药品质量安全控制提供了检测利器。另外,迪马科技也为参会者现场实物展示了ProElut系列固相萃取柱、2 mL样品瓶、针头式过滤器等药品质量分析过程中涉及的色谱消耗品,各参会专家和学者纷纷前来与迪马工作人员进行交流,咨询相关产品及药品检测应用案例。两天的药品质量安全会议已落下帷幕,但迪马科技关注药品质量安全的行动仍将继续。我们将始终践行为药品安全保驾护航的诺言,以更多的应用,更好的产品服务于药品质量控制分析工作者。http://ng1.17img.cn/bbsfiles/images/2015/04/201504221659_543080_1987954_3.jpg迪马科技展位现场
3月26日,中国食品药品检定研究院(以下简称中检院)发布《国家药品抽检年报(2023)》(以下简称《年报》)。《年报》显示,2023年国家药品抽检共完成132个品种18762批次制剂产品与中药饮片的抽检任务,样品来源涉及1114家药品生产、2528家经营企业和511家使用单位,由中检院等47个承检机构负责检验样品,检出136批次不符合规定产品。抽检结果显示,当前我国药品安全形势总体平稳可控,药品质量持续保持在较高水平。 药品抽检作为药品上市后监管的重要手段之一,是实现风险管理、科学管理、监管前置的重要技术支撑。2023年,国家药监局紧紧围绕药品监管实际需求,聚焦重点任务,完善运行机制,创新监管方式,采取“分散抽样、集中检验、探索研究、综合评价”的抽检模式,此外,通过优化抽检模式,进一步提升抽检服务监管的效能。 抽检制剂产品16604批次 2023年国家药品抽检共抽检制剂产品16604批次。经检验,16531批次产品符合规定,73批次产品不符合规定。 在化学药品方面,共抽检74个品种10893批次,经检验不符合规定44批次,不符合规定项目包括检查和含量测定。 在中成药方面,共抽检43个品种5584批次,涉及11个剂型。经检验,不符合规定29批次,不符合规定项目主要涉及鉴别和检查。 在生物制品方面,共抽检6个品种127批次。经检验,所检项目均符合规定,合格率为100%。 根据制剂产品抽检结果,《年报》对生产企业、经营企业加强管理进行了提示,并给予监管部门建议。《年报》建议监管部门严格审查企业批生产记录,核查原辅料投料量,推动质量标准提升 加强对生产企业的监督检查,督促其严格按照处方工艺投料,严格执行GMP规范,从而保证中成药的质量及疗效。 《年报》还显示,2023年国家药品抽检共抽检国家基本药物39个品种6140批次,不符合规定13批次,国家基本药物整体质量状况较好 共抽检国家集中采购中选品种20个品种3435批次,集中采购涉及样品均符合规定,国家药品集中采购中选品种整体质量状况较好 共抽检进口药品309批次,均符合规定。 2023年,国家药监局继续组织开展中药饮片专项抽检,共抽检9个中药饮片品种2158批次,不符合规定63批次 继续组织开展中药材质量监测,共监测9个品种251批次样品。抽检及监测结果显示,我国中药饮片总体质量状况良好,但中药饮片全产业链参与者应进一步增强质量意识和责任意识,中药饮片生产企业应提升全程质量控制意识。 充分利用探索性研究利器 在国家药品抽检过程中,探索性研究可为进一步提升药品质量水平、加强药品监管提供技术支持。在多年技术储备的基础上,2023年各药品检验机构充分利用探索性研究这一监管利器,全面考察药品质量的稳定性、现行标准的完善性,同时探寻可能存在的潜在风险,为提升药品质量标准、提高监督管理水平提供科学可靠的技术支撑。 2023年国家药品抽检探索性研究发现的主要问题有:中药制剂生产中使用伪品、中药材及饮片掺伪问题仍然存在 个别企业违法违规生产问题,如擅自改变生产工艺,低限或使用伪品、替代品投料,擅自改变或添加辅料、防腐剂、抑菌剂等 因原料药质量差异、生产工艺不稳定等原因,导致产品均一性较差 外源性有害物质超限,个别批次产品重金属、农药、真菌毒素残留量超限 包装材料相容性问题影响产品质量稳定性等。 据《年报》,对探索性研究中发现的有关生产工艺、处方、原辅料、包装材料、说明书等方面可能存在的一般性问题,药品监管部门通过“药品质量提示函”等形式反馈相关企业,提升企业的质量意识,加强企业主体责任的落实。相关企业主动采取修订内控标准、完善工艺、加强供应商审计、修订说明书等整改措施,提升产品质量水平 各省级药监局也通过多部门联席会、约谈企业、风险沟通、跟踪检查等方式,利用提示信息强化对企业的监督指导。通过寓服务于监管的风险提示,加深了监管部门、药检机构和企业之间的信任与理解,促进了持有人主体责任的落实,是主动排查、预防为主监管方式的有益探索。 记者获悉,对探索性研究发现的个别企业涉嫌存在的违法违规线索,监管部门在综合分析研判的基础上,及时对涉及企业开展了有针对性的有因检查,并根据检查结果及时采用有效的风险控制等措施。例如,今年1月,湖北省药监局根据2023年国家药品抽检探索性研究结果对武汉贝参药业股份有限公司某厂区进行了有因检查,发现该公司杏苏止咳糖浆生产质量管理存在严重缺陷2项、主要缺项3项、一般缺陷8项,不符合《药品生产质量管理规范》(2010年修订) 2月21日,湖北省药监局发布公告,依据相关法律法规,决定暂停该品种的生产、销售。 应用结果推动产业提质升级 2023年,国家药监局通过政策支持、开展专项风险监测、深入排查风险、公开信息等方式加强抽检工作,并积极运用抽检成果持续提升药品质量,推动产业提质升级,助力产业高质量发展。 为推动抽检工作更加科学,国家药监局持续加强抽检制度建设和顶层设计,于2023年印发《关于进一步做好地方药品抽检有关工作的通知》,对地方抽检工作提出更为明确且具体的要求,加强国家与地方抽检的衔接互补。同时,持续推进药品抽检制度体系优化创新,健全完善抽检工作机制和工作程序,加快推进修订《药品抽检探索性研究原则及程序》,规范指导探索性研究 修订《药品抽样原则及程序》,细化完善中药材和中药饮片取样,探索网抽购样方式方法。据悉,《药品抽检探索性研究原则及程序》即将于近日发布。 近年来,国家药品抽检每年设置不同专项,对重点品种进行专项研究。2023年,针对可能的风险点,国家药品抽检还设置溶剂残留研究、网络抽检等专项,潜在风险得到有效控制,其中溶剂残留研究的相关工作成果已被收入《国际药典》。 2023年,国家药监局依照“风险控制-依法处置-排查原因并整改-信息公开”的监管模式,确保风险关闭、警示用药安全,严厉打击了制售假劣药品的行为,发挥震慑不法企业、净化市场环境的作用。此外,国家药监局在2023年共发布药品补充检验方法4个,为打击隐蔽性极强的掺杂掺假等违法行为提供了监管利器,也为企业提供了保障药品质量安全的科学依据。 2023年,国家药监局共发布药品抽检通告7期,对全部不符合规定药品及涉及企业依法公开,震慑不法企业、警示安全用药。中检院在官方网站持续公开国家药品抽检的探索性研究结果,新发布39个品种的新建检验方法,累计发布新建检验方法601个。通过信息的共享利用,进一步促进药品上市许可持有人及相关生产经营企业的质量安全意识和主体责任自律意识,增强药品质量风险控制能力,促进产品研发创新升级。[size=14px][color=#707d8a][ 来源:中国食品药品网 ][/color][/size][size=14px][color=#707d8a][i]编辑:张圣斌[/i][/color][/size]
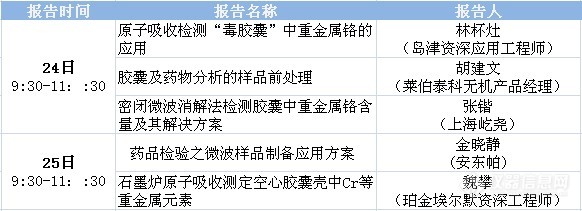
http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646471_1604352_3.gif【免费在线讲座】“毒胶囊中重金属铬的检测及药品质量控制”专题网络研讨会主办:仪器信息网 活动时间:2012年4月24、25日(周二、周三) 上午 9:30—11:30http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646471_1604352_3.gif 近期,央视《每周质量报告》曝光9大药企,13个批次药用胶囊重金属铬超标,部分超过国家标准接近90倍。据悉,这些药用胶囊用皮革废料所生产的明胶做原料。此事件一经曝光立即引起了群众极大的关注。 胶囊类药品作为广泛使用的一类药物,人们大多关注于药品本身的功效及成分,但是作为辅料的胶囊同样也会被人体消化吸收,亦会影响服药者的身体健康。仪器信息网针对本次事件,聚焦“毒胶囊”中重金属铬的检测及药品质量控制等问题,特举办专题研讨会,邀请4-6位资深应用专家进行相关报告,在线介绍“毒胶囊”中重金属铬的检测方法及我国药品检测方面的技术进展、解决方案及质量控制现状等,“面对面”解答用户问题。http://ng1.17img.cn/bbsfiles/images/2012/04/201204191411_362254_2961690_3.gifhttp://ng1.17img.cn/bbsfiles/images/2012/04/201204201002_362408_1632253_3.jpg1、报名条件:只要您是仪器网注册用户均可报名参加。2、参加人数:100-200人。3、参与互动:本次讲座采取网络讲堂直播模式,欢迎大家积极发言提问。 *参会期间您还可以将有疑问的数据通过上传的形式给老师予以展示,并寻求解答*4、报名参会:"毒胶囊中重金属铬的检测及药品质量控制"专题网络研讨会(上)http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg"毒胶囊中重金属铬的检测及药品质量控制"专题网络研讨会(下)http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg5、环境配置:只要您有电脑、外加一个耳麦就能参加。建议使用IE浏览器进入会场。6、提问时间:现在就可以在此帖提问啦,截至2012年4月23日7、会议进入:2012年4月24日9:00点就可以进入会议室8、开课时间:2012年4月24日9:309、http://simg.instrument.com.cn/webinar/20110223/images/zb_11.gif特别说明:报名并通过审核将会收到1 封电子邮件通知函(您已注册培训课程),请注意查收,并按提示进入会议室!为了使您的报名申请顺利通过,请填写完整而正确的信息哦~http://ng1.17img.cn/bbsfiles/images/2012/04/201204191411_362254_2961690_3.gif
FDA药品质量办公室宣告正式成立大家翘首以待的美国FDA药品质量办公室(OPQ)经过2年多的筹备,终于正式成立了。美国政府的办公室(Office)相当于我国的司,通常编制从几十人到几百人,下属若干个处(Division)。但OPQ预计的编制上千人,下属8个司,属于“超级”办公室。OPQ一跃成为FDA药品审评与研究中心(CDER)中最大的办公室,超过了过去的新药、药学及合规等三个超级办公室。实际上,上述三个办公室中的药品质量部分,包括新药超级办公室(OND)下属的新药质量评估办公室(ONDQA),仿制药超级办公室(OGD)中所有化学审评功能(仿制药审评的核心部分),合规超级办公室(OC)中批准前检查及上市后监测部分今后都划归OPQ了。来自我国浙江的余煊强博士(Lawrence Yu),荣任OPQ唯一的副主任。值得注意的是在今天宣布的OPQ主任和副主任,以及8位下属办公室主任的任命中,绝大多数都是暂时(Acting)任命,只有余博士和生物技术产品办公室(OBP)主任两位是长期任命。鉴于代理主任Janet Woodcock博士是整个CDER的主任,OPQ的具体工作预计将会落在余博士的肩上,包括今后FDA对药品质量监管的整体思路、布局和具体实施等。这是全体旅美华人科学家和监管者的自豪。成立OPQ标志着FDA进入了药品质量监管的新时期,其主要变革点,余煊强博士在今年6月底在北京大学国际药物工程管理(IPEM)硕士项目举办的药品质量研讨会上已经明确指出,具体讲就是:(1)方向上改变 - 过去的质量标准是和数据连在一起,而不是和病人连在一起。今后,质量高不高,不是看标准高不高,而是看对病人的效果。(2)机制上改变:通过整合CMC审评、GMP合规审评、及GMP现场检查,实现质量监管统一的声音。药品质量监管历来不易,既要确保百姓用药安全,又不能给药企增加不必要的负担;既要科学合理,又要依附于国家的政法体系,同时还要与时俱进。FDA的药品监管及美国的药品质量,多年来已经走在国际前列,但其不满足于现状,抓住时机(包括近年发生的药品质量安全事故,行之有效并进一步扩大的收费制度)勇于进取的做法,值得借鉴。 药品质量办公室 药品审评与研究中心(CDER)下属药品质量办公室(OPQ)的使命是确保供应给美国公众高品质的药品。OPQ的职责OPQ是CDER创建的一个独立的致力于产品质量的新办公室。新架构将于2015年1月正式运行,预计将为CDER的所有药品质量工作,包括审评、检查和研究提供更好的定位。OPQ将把非强制执法相关的药品质量工作整合到一个超级办公室,发出统一的质量声音,通过药品生命周期改善监管质量。OPQ贯穿所有生产场区—无论国内还是国外,横跨所有药品领域—新药、仿制药和非处方药,建立一致的药品质量计划。OPQ的组织架构以及新的流程和政策,将支持我们的使命,以确保供应给美国公众安全、有效、高品质的药品。改变包括:将制药科学办公室的职能和人员重组到OPQ 将合规办公室(OC)的批准前和监测检查活动重组到OPQ 将合规办公室下科学调查办公室关于生物等效性/生物利用度和非临床研究的相关检查活动重组到转化科学办公室药品质量办公室下设机构及领导以下人员将于2015年1月起任职:代理主任:Janet Woodcock, M.D.副主任:Lawrence Yu, Ph.D.项目和监管运营办公室(OPRO):Giuseppe Randazzo(代理) 药品质量政策办公室(OPPQ):Ashley Boam (代理) 生物技术产品办公室(OBP):Steve Kozlowski 新药产品办公室(ONDP):Sarah Pope Miksinski(代理) 生命周期产品办公室(OLDP):Susan Rosencrance(代理) 检验和研究办公室(OTR):Lucinda (Cindy) Buhse (代理) 工艺和设施办公室(OPF):Christine Moore(代理) 监测办公室(OS):Theresa Mullin(代理)
国家食药监管总局即日起至12月5号就《药品飞行检查办法(征求意见稿)》公开征求意见,药品飞行检查覆盖面大幅拓宽,药品监督管理将进一步规范和加强。此规定,将药品的飞行检查纳入整个药品监管的日常检查中,可以使我国的药品监管能力和水平进一步成熟、提高。 据中国之声《全国新闻联播》消息,国家食药监管总局即日起至12月5号就《药品飞行检查办法(征求意见稿)》公开征求意见, 药品飞行检查覆盖面大幅拓宽,药品监督管理将进一步规范和加强。 药品飞行检查 药品监管 药品质量 所谓“药品飞行检查”,是药品监督管理部门针对药品生产、经营等环节开展的不预先告知的突击检查或者暗访调查。在《药品飞行检查办法(征求意见稿)》之前,原国家食品药品监督管理局2006年《关于印发药品GMP飞行检查暂行规定的通知》是目前药监部门执法检查的主要依据。中国药学会医药政策研究中心执行主任宋瑞霖介绍,两者相比,征求意见稿的覆盖范围大大拓宽。 宋瑞霖:GMP是指导制药企业、保证药品质量的重要规范。我们从原料进料到生产全过程,GMP包括了最核心点,但它不是药品生产的全部。现在我们把GMP检查改成药品飞行检查,把它扩展到整个药品质量的控制体系中来了。 征求意见稿规定,被检查单位及有关人员应当及时按照检查组要求,提供真实、有效的记录、票据、凭证等相关材料,开放相关计算机管理系统,不得拒绝和隐瞒。不配合或者阻挠检查、拒绝提供或者提供虚假材料、故意隐瞒违法违规生产经营行为,其违法违规事实一经查实,按情节严重情形从重处罚。宋瑞霖表示,尽管相比当前的药品飞行检查规定,征求意见稿并没有作出大幅更改,但规范飞行检查、强化药品监管是大势所趋。 宋瑞霖:最大的区别是把药品的飞行检查纳入整个药品监管的日常检查中,我们的药品监管能力和水平进一步成熟、提高。
[font=Calibri][size=10.5pt][font=宋体]仪器信息网于[/font]5[/size][/font][font=Calibri][size=10.5pt][font=宋体]月[/font]18[font=宋体]日组织召开[/font][b] 2020药典——“药品微生物检测技术”主题网络研讨会[/b][/size][/font][font=Calibri][size=10.5pt][font=宋体],特邀嘉宾陈向东(中国药科大学)[/font][font=宋体],带来报告[b]《微生物检测新技术在药品质量控制中的应用》[/b];[/font][/size][/font][font=宋体]欢迎感兴趣的你,报名参会![/font][url=https://www.instrument.com.cn/webinar/meetings/6604/][b][u][font='Times New Roman'][color=#0563c1]https://www.instrument.com.cn/webinar/meetings/Drug2020/[/color][/font][/u][/b][/url]
近年来,随着国民经济的发展,食品、药品、农产品的安全问题受到了空前的重视,食品、药品、农残检测新技术、新设备、新标准不断涌现,频频传出药品质量不合格致病事件,越来越多的食品、农产品中被检测出含有超标有害物质,而欧盟、美国、日韩、加拿大等发达国家和地区,则相继对进口食品、农产品安全指标提出了愈来愈严格的要求。此种情况下,中国仪器仪表学会定于2010年5月在广州召开“2010年“全国食品、药品、农产品安全及品质分析检测技术交流会”,就如何应对挑战,加强食品、药品、安全管理,提高食品、药品、农产品检测技术水平等问题进行深入的交流与探讨。届时,会议特邀食品、药品、农产品质量安全方面的专家作专题报告,报告内容涉及目前食品、药品、农产品质量安全方面的多个热点问题。谨此,我们诚邀各位从事食品、药品、农产品质量安全检测及控制工作的业内人士,以及关心食品、药品、农产品质量安全的专家和学者莅临本届研讨会。同时,欢迎各位专家学者提供与此内容相关的文章,以便我们从中选取有代表性的优秀论文在大会上宣讲。大会还将编印论文集,[b]评选优秀论文,颁发获奖证书,获奖论文将由大会委员会直接推荐给相关中文核心期刊[/b]。我们也欢迎仪器制造商介绍新产品、新技术。现将有关事项通知如下:[b]一、主办单位[/b]中国仪器仪表学会、中国仪器仪表学会科学仪器学术工作专业委员会[b]二、会议时间、地点:[/b]2010年5月24日-5月26日(5月23日报到) [b]广州[/b][b]三、会议日程:[/b] 5月23日(周日) 全天报到 5月24日(周一) 上午:开幕式、嘉宾致词、大会报告 下午:大会报告 晚上:夜游珠江 5月25日(周二) 上午:大会报告 下午:大会交流 5月26日(周三)参观访问相关单位[b]四、会议内容[/b]1、 食品、药品安全的概念及食品、药品、农产品安全管理最新动态 2、 食品、药品、农产品分析技术国内外发展综述 3、 国内外食品、药品、农产品安全法规介绍 新《食品法》、《药典》解析 4、 色谱技术在食品、药品、农产品检测分析中的应用 5、 质谱技术在食品、药品、农产品检测分析中的应用 6、 光谱技术在食品、药品、农产品检测分析中的应用 7、 食品、药品、农产品的热点检测方法介绍 8、 国内外食品、药品分析检测技术与仪器设备的最新进展。9、 药品快速检测技术的研究与应用 10、奶制品、鸡蛋及饲料中三聚氰胺及添加物同时检测技术研究 [b]五、 征稿内容和要求[/b](一)凡在2009下半年至大会投稿截止日之前未在刊物上发表和未在学术会议上宣读过的反映近期食品、药品、农产品安全、管理模式、检测仪器、分析检测技术基础研究,新技术新方法的发展以及在各个领域的分析应用等论文或综述均可投稿。(二)、征文要求:1)论文内容应包括样品预处理,实验条件,数据处理方法、图表,结果和讨论。2)全文不超过6000字,不少于3000字(包括论文题目、主要参考文献,英文题目和简单英文摘要)。3)论文格式:A4版面。页面均应为整页,不留部分空白页面,便于排版。4)因是学术交流会征稿,投稿时请一并寄上参加会议的回执,否则稿件不予受理。5)投稿单位不限,涉及生物制品、食品、药品、农产品、医疗器械等相关企事业单位、仪器厂商、个人均可投稿。(三)会议征文请在2010年4月15日前通过邮局邮寄(同时提供电子版)、电子邮件发送到会议筹备组(三日内收到筹备组的回复邮件方为发送成功),并请注明联系人、详细通信地址、联系电话、传真号码及e-mail地址,并注明“全国食品、药品、农产品分析检测技术交流会”论文字样。 论文邮寄地址:北京市海淀区知春路锦秋国际大厦2304 燕泽程 刘继红收 邮政编码:100088(四)优秀论文评选:由论文评审委员会对论文进行评选,颁发获奖证书 获奖论文由大会委员直接推荐给相关中文核心期刊。论文评选结果出来以后,大会将及时通知论文作者。[b]六、报名、注意事项:[/b](一)欲参加会议的人员,于2010年5月10日前将《报名回执表》填写后,传真、E-mail、电话或邮寄到科学仪器学术工作专业委员会,以便提前安排。专业委员会收到《报名回执表》后,会尽快与您联系。会议通知也可在中国仪器仪表学会网站上查看,网址:[u]http://www.cis.org.cn[/u]。(二)与会者应积极参加大会交流,会议期间,服从学术会安排。(三)会议注册费:每人1500元(学生1200元)。往返旅费自理。[size=5][b]联系方式[/b][/size][color=#0045df]联系人:[/color]刘继红 燕泽程[color=#0045df]电 话:[/color]010-63979302 82800721[color=#0045df]传 真:[/color]010-68343165[color=#0045df]邮 箱:[/color]training@cis.org.cn[url]http://expo.cqvip.com/meet_detail.asp?id=96[/url]
这是一个中国医药教育协会举办的活动,我想请问这类会议对我的工作会有帮助吗?能学到东西吗?请参加过的朋友谈谈看法,谢谢! 附件是我收到的全部文件!一、参会对象各级药品检验所(院)和口岸药品检验所的有关研究人员;各制药企业和新药研究机构的研发人员;各药品生产企业高层技术与质量管理负责人,新药研发CRO实验室人员及高管;各药品安全检测仪器设备研发生产、代理商;各高等院校、科研院所、医疗机构等相关专业人员。二、时间及地点报到日期:2011年4月22日会议时间:2011年4月23日—25日报到地点:北京市新悦宏国际酒店(北京市海淀区复兴路65号乙)报名截止日期:2011年4月15日三、有关费用及证书参加代表须交研讨费1880元(含资料、专家报告、茶歇、场租等)。统一安排食宿,费用自理,报到时统一交纳。请将报名表传回,我们收到报名表后,于举办前七天将正式日程和报到通知传真给参会代表。学习结束经考核合格颁发由中国医药教育协会继续教育培训证书,记入学时学分。四、论文征集1、本次会议将征集与会议主题和研讨内容有关的论文。届时将出论文集。来稿应具有科学性、实用性,且论点鲜明、数据可靠、文字精练通顺,文稿请用word文档(A4纸)电子邮件投递至专用信箱,一般文章以3000~5000字为宜。来稿须列出题目、作者姓名、工作单位(全称)、地名(城市)及邮政编码、论文摘要、关键词、正文、主要参考文献。多位作者的署名之间,应用空格隔开。不同工作单位的作者,应在姓名之后标注作者工作单位,并列出工作单位、地名、邮政编码。无意参会,请不要投递论文。2、截稿日期:2011年4月15日。五、联系方式电 话:010—68631433 15652660105传 真:010—68639711联 系 人:刘 枫邮 箱:fengliu82@163.com附件一:日程安排表附件二:报名表
[size=6][b]“首届全国药品质量分析论坛”顺利开幕[/b][/size]http://www.instrument.com.cn 来源:仪器信息网 2010-3-11 23:13:11 点击427次[align=left] [b]仪器信息网讯[/b] 2010年3月11日,由中国药学会药物分析杂志编辑部主办、国家食品药品监督管理局药品市场监督办公室协办的“首届全国药品质量分析论坛”在河南省郑州市嵩山饭店顺利召开,会期两天;本次会议旨在为了不断提高药品质量,交流药物分析技术及方法,促进药品生产工艺改进,保障公众用药安全有效。从事药品检验、药物分析、药品生产质量控制等相关领域专业人员约500余人参加了此次会议。[/align][align=center][b][font=楷体_GB2312][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010311231459653.jpg[/img][/font][/b][/align][align=center][b][font=楷体_GB2312]会议现场[/font][/b][/align] 论坛开幕式由中国药品生物制品检定所原常务副所长、药物分析杂志主编金少鸿研究员主持,中国药品生物制品检定所丁丽霞副书记和河南省食品药品监督管理局陶勉超副局长分别致辞;当日上午主题报告会由中国药品生物制品检定所党委副书记丁丽霞研究员和药物分析杂志编辑部杨腊虎主任主持。[align=center][b][font=楷体_GB2312][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010311231459490.jpg[/img][/font][/b][/align][align=center][b][font=楷体_GB2312]中国药品生物制品检定所党委副书记丁丽霞研究员致辞[/font][/b][/align][align=center][b][font=楷体_GB2312][/font][/b][/align][align=center][b][font=楷体_GB2312][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/20103120844686.jpg[/img][/font][/b][/align][align=center][b][font=楷体_GB2312]河南省食品药品监督管理局陶勉超副局长致辞[/font][/b][/align][align=center][b][font=楷体_GB2312][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010311231459987.jpg[/img][/font][/b][/align][align=center][b][font=楷体_GB2312]药物分析杂志编辑部杨腊虎主任主持专题报告会[/font][/b][/align] 本次论坛以“药品质量分析研究”为主题,内容涉及“化学药品、药用辅料、药品包装材料质量分析,生化药物、抗生素质量分析,中药质量分析”三大方面。除邀请多位药品质量分析专家做专题报告外,论坛还采用了大会报告、分会交流、壁报展览的表现形式。现对主题报告内容作基本介绍,以飨读者。[align=center][b][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010311231459454.jpg[/img][/b][/align][align=center][b][font=楷体_GB2312]中国药品生物制品检定所原常务副所长、药物分析杂志主编 金少鸿研究员[/font][/b][/align][align=center][b][font=楷体_GB2312]报告题目:我国药品质量分析研究的实践与进展[/font][/b][/align] 金少鸿研究员在报告中首先从当前常用药品的特点、药品质量观点的变迁、药品质量分析的分类与目的等方面系统回顾了我国药品质量分析的历史;同时,对药品质量分析研究的现状也进行了系统阐述,自2008年全国开展药品评价性分析以来,各级药检机构通过对市场流通的不同生产厂家200种药品样品进行全方位检验与深入分析,获得令人瞩目的成果:提出了质量标准必须提高,指出了检测方法必须修订,发现了检测方法必须修订,发现了生产工艺必须改进,提示了包装材料必须重视,揭示了企业诚信必须加强。 最后,指出了药品质量分析研究的几点展望:(1)药品质量分析与质量标准提高相结合;(2)药品质量分析与药品检测技术研究相结合;(3)药品质量分析与药品不良反应监测相结合;(4)药品质量分析与药品市场监督检查相结合;(5)药品质量分析与药品上市后再评价相结合;(6)药品质量分析与药品定价招标采购相结合;(7)药品质量分析与药品检验人员培养相结合。[align=center][font=楷体_GB2312][b][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010311231459406.jpg[/img][/b][/font][/align][align=center][font=楷体_GB2312][b]总后卫生部药品仪器检验所副所长 姜雄平主任药师[/b][/font][/align][align=center][font=楷体_GB2312][b]报告题目:溶出度及其评价[/b][/font][/align] 姜雄平主任药师在报告中从药品制剂质量分析谈起,对影响固体制剂质量的关键因素(安全与稳定、有效)进行了简单解释,通过引用大量数据与实验事例系统分析了溶出度适用范围、方法的建立与验证、溶出曲线的测定、溶出过程评价;最后提出了几个方面的问题与建议:药品标准或处方工艺存在的问题;药品质量问题;药品再评价;溶出度再研究的目的;建立我国的“橙皮书”——确定参比制剂:国家规定有参比制剂的就要选择国家规定的参比制剂,没有规定的按“原创上产品、国内著名品牌产品、国内公认质量好的产品、国内销售量大的品牌产品”顺序选择参比制剂。
求助:药品质量研究规范的标准。谢谢好心人能给我提供一个标准,主要是质量研究的内容太多,而且知道的都是大框架,而不知道细枝末节。谢谢啦
(申明:本文只是参与本科答辩的论文,没有公开发表,只为参加原创,一共四篇,11月份发布了《GSP中药品购进管理的思考》和《对GSP中药品储存管理的认识与思考》;继“购进管理”和“储存管理”后,今天发布“验收管理”和“销售环节管理”两篇,至此,我们小组四人的本科答辩论文也就发布完了,作为2011年最后一个月个人原创大赛参赛的收尾,2012年原创再见)浅谈GSP中药品质量验收管理学生:周小丽 指导老师:罗玉臻 : 目的:认识GSP中药品质量验收管理的必要性以及具体要求,并就有关问题提出对策及建议。方法:通过参与实践,查阅文献并结合省内药品经营单位的相关资料进行汇总、分析。结果:企业管理制度不系统,管理方法落后,质量验收人员培训不严格等问题是当前GSP中药品质量验收存在的主要问题。结论:只有重视GSP中药品质量验收管理,进一步完善管理体系,采取更先进的方法,才能更进一步的把好药品经营单位的质量关。 GSP 药品质量 验收 管理It is shallow to talk the GSP Chinese herbal medicine amount of quality checks before acceptance the managementSpecial subject student: Zhou Xiao-liLead teacher: Luo Yu-zhen Purpose The cognition GSP Chinese herbal medicine amount of quality checks before acceptance necessity and concrete requests of the management, combining to put forward related counterplan and suggestions for the relevant problem. Method Pass to participate the fulfillment, check combinative drugs inside the province that cultural heritage combine related data operate the unit proceeds to gather, analyze. Results Business enterprise management system not system, manage the method fall behind, the quantity checks before acceptance the personnel the training not wait strictly the problem is a key problem that current GSP Chinese herbal medicine amount of quality check before acceptance the inside. Conclusions Only valuing the GSP Chinese herbal medicine amount of quality checks before acceptance the management, further perfect management system, adopt the more advanced method, the talent is further to operate the quantity pass of the unit to good drugs. GSP Drugs quantity Check before acceptance Management 《药品经营质量管理规范》对应的英文是good supply practice, 缩写是GSP,意为良好供应规范。我国现行的GSP是2000年6月原国家药品监督管理局发布的《药品经营质量管理规范》。GSP是药品经营企业管理的基本准则,适用于中国境内经营药品的专营或兼营企业。GSP的基本精神是:药品经营企业应在药品的购进、储运、销售等环节实行质量管理,建立包括组织结构、职责制度、过程管理和设施设备等方面的质量体系,并使之有效运行。药品经营过程的质量管理,是药品生产质量管理的延伸,是控制、保证已形成的药品质量的保持,也是药品使用质量管理的前提和保证。药品经营过程质量管理的目的是,控制和保证药品的安全性、有效性、稳定性不变化、药品不变质;控制和保证假药、劣药及一切不合格、不合法的药品不进入流通领域,不到使用者手中,做到按质、按量、按期、按品种,以合格的价格满足医疗保健的需求。我国GSP的主要内容包括管理职责、人员与培训、设施与设备、进货、验收与检验、储存与养护、出库与运输、销售与售后服务等。其中验收工作是药品经营企业把好药品质量关的关键。1. 药品质量验收管理的必要性药品是一种特殊的商品,它是用于预防、治疗、诊断人的疾病,有目的地调节人的生理功能并规定有适应证或者功能与主治、用法和用量的物质。药品与人体健康紧密相连,且药品具有高质量性的特征,药品的纯度、稳定性、均一性与药品的使用价值有密切关系,杂质、异物混入药品,可出现异常生理现象、毒副作用、药品不良反应,甚至中毒。因此对药品质量的把关显得尤为重要。而验收正是药品经营企业中把握质量的关键程序。因此,验收工作也就显得尤为重要了。2. GSP中对药品质量验收管理的具体要求[font
2月27日下午,国家食品药品监管局副局长吴浈接受中国政府网专访时表示,GMP是一个好制度,要肯定它。他驳斥了社会上有的人认为GMP是形象工程的说法。 据介绍,中国从开始颁布GMP到全面强制实施GMP用了14年的时间,这既符合中国国情,也顺应国际趋势。实施GMP认证以来,提高了制药行业准入标准,整个制药企业的水平上了一个台阶。同时,也规范了药品的生产行为,药品质量可以得到进一步保证。 吴浈说,2006年,一些GMP认证的企业出现了质量问题,出了这些问题,并不能说GMP的制度不好。但药品监管部门将会加强对GMP执行情况的检查力度。去年通过检查,共收回86张GMP认证证书,对不执行GMP规范的进行严厉处理,今年还要加大日常跟踪检查力度。 吴浈强调说,药品质量是生产出来的,不是监督出来的,所有保证药品质量的制度都要靠企业自觉的来执行,需要企业提高自行GMP制度的自觉性。他希望所有的企业都认真执行GMP的规范,把群众的用药安全放在首位,正确处理好商业利益和公众利益的关系。
[em0801][em0802]药品质量管理是一个复杂的体系,是一个大的系统工程。至少包括五个子系统,从药品的研究(GLP/GCP)开始,经过生产(GMP/GAP)、经营(GSP)、使用(GUP)、最后是药品上市后的再评价(ADR)。只有这五个阶段的质量都得到可靠的保证,整个药品的质量才可万无一失。它们构成了药品质量管理的完整链环。本讲义针对这五方面展开![img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=108451]药品质量管理与质量控制[/url]
广西自治区食品药品监督管理局近日发布2011年广西药品质量公告(总第25期)。根据公告,2011年上半年,从全区60个药品生产、经营、使用单位抽取42个品种87批次的国家基本药物进行全项目检验,检验合格87批,合格率为100.0%。2010年度抽验的标示广西药用植物园制药厂生产的复方丹参片(批号:100709)检验、复验均不合格。2011年广西药品质量公告(总第25期)列表 序号标示药品名称标示生产企业标示批号标示规格检品来源检验依据检验单位检验结果不合格项目备注1阿莫西林克拉维酸钾颗粒南京先声东元制药有限公司60-1101030.15625g(C16H19N3O5S 0.125g与C8H9NO5 0.03125g)公馆民兴医院《中国药典》2010年版二部北海食品药品检验所符合规定/ 2阿莫西林克拉维酸钾片珠海联邦制药股份有限公司中山分公司010055010.457g(C16H19N3O5S 0.4g与C8H9NO5 0.057g)广西翰林医药有限公司《中国药典》2005年版二部北海食品药品检验所符合规定/ 3阿莫西林克拉维酸钾片山西仟源制药有限公司1004050.375g(C16H19N3O5 0.25g与C8H9NO5 0.125g)贺州市平桂管理区羊头卫生院《中国药典》2005年版二部北海食品药品检验所符合规定/ 4阿莫西林克拉维酸钾胶囊(4:1)浙江巨泰药业有限公司20100906156.25mg ( C16H19N3O5S 125mg与 C8H9NO5 31.25mg )岑溪市中医医院《国家药品标准》新药转正标准第75册北海食品药品检验所符合规定/ [t
药品生产企业质量检验存在问题及对策(中国医药报,2006.12.7) 药品检验即依据药品质量标准规定的各项指标,运用一定的检验方法和技术,对药品质量进行综合评定,又称药品质量检验。 我国药品管理法律、法规的逐步完善及2005版《中国药典》的施行,对药品生产企业质量检验工作提出了新的更高要求。如何帮助生产企业提高药品质量检验水平, 严格按照2005版《中国药典》对药品(包括原料药和制剂)进行全检,是保证药品质量的重要措施和有效手段,对防止不合格原料或中间体进入下一环节,杜绝不合格成品出厂销售,以及保证药品质量起到重要作用。然而,由于种种原因,一些药品生产企业尚不能做到对产品及原辅料进行全检。 究其原因,有以下几点: 一是认识不到位。一些药品生产企业负责人忽视对法律、法规的学习,对药品质量检验的重要性认识不足,只考虑眼前的经济利益。由于种种原因,未按要求购买必要的仪器、设备;对企业无能力检验的项目又不按规定进行委托检验,致使企业在药品质量管理和检验中存在漏洞。 二是人员素质与检验要求不相适应。2005版《中国药典》的施行以及药品标准的提高,对药品检验人员的素质提出了更高的要求。而目前,一些企业的药品检验人员对质量标准理解不到位,不会操作先进的检验设备,不懂得如何处理检验数据。部分药品生产企业在通过GMP认证后,人员流动频繁,现有检验人员不能较好地掌握需检验药品的标准和方法,药品检验能力和水平较低。 三是检验仪器设备不能满足现实需要。国家食品药品监管局要求对原辅料必须进行全项检验,并修订了部分药品标准,增加了中药材检测项目,对部分检验方法也做出了新的明确规定。要求药品企业生产的药品(包括制剂和原料药)必须按药品标准项下的规定进行全项检测,除动物试验暂可委托检验外,其余均不得委托其他单位进行;无菌、疫苗制品的动物试验不得委托;药品生产企业对进厂的原料、辅料、包装材料的检验,如需使用频次较少的大型检验仪器设备(如核磁、红外等),相应的检验项目可委托具有资质的单位进行检验。上述要求决定了药品生产企业必须配备相关的检验仪器设备。但在实际中,许多药品生产企业由于认识不到位、资金不足等原因,检测仪器设备不全,主要缺少的仪器有:[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度计、红外分光光度计、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]、高效液相色谱仪、薄层扫描仪、集菌仪等。 四是不能按要求对药品进行全检。一种情况是由于无相应的检验仪器而不能进行药品全检。另一种情况是由于无标准品(对照品、对照药材)而不能进行药品全检,主要表现在中药材全检中漏检问题比较严重。许多中药饮片生产企业对购进和销售的药材及饮片不能进行全检,不能检验的项目主要有重金属及有害元素、红外吸收图谱、含量测定、农药残留等。在不具备检验条件的情况下,部分企业采取了委托检验的做法,个别企业则未进行委托检验。 五是管理存在问题。一些药品生产企业的质量管理部门不能较好地履行职责,主要表现在:对部分原辅料和成品未经全检就予放行;未严格按照药品标准规定的检验方法进行检验,部分企业因无相关检验仪器,无法按照药品标准规定的方法进行检验,就用其他方法代替,但未进行方法验证,如纯水的微生物检测等;对标准品(对照品、对照药材)试剂等未按规定管理,如标准品无相关记录,检验用试剂未标明有效期或已过有效期等;对质量检验工作管理不规范,部分企业存在质量检验报告书书写不规范、原始记录填写不实等问题;不按照检验规范操作,无检验仪器使用记录,部分检验用仪器未及时校验等。 ■对策 加强监督管理。各级食品药品监管部门要严格按照《药品管理法》、《药品生产质量管理规范》的规定,认真贯彻落实国务院和国家食品药品监管局关于整顿和规范药品市场秩序专项行动的精神,加大对药品生产企业日常监督检查的力度,督促企业及时购置相关检验仪器设备,配备具有相应检验能力的质量检验人员,严格按照GMP要求加强质量控制,满足药品质量检验工作的需要,把质量监管责任落到实处,确保药品质量。 有序委托检验。按照国家食品药品监管局的有关规定:药品生产企业在对进厂原辅料、包装材料进行检验时,如遇使用频次较少的大型检验仪器设备,相应的检验项目可向具有资质的单位进行委托检验,但有关委托情况须报省级食品药品监管部门备案。笔者认为,上述规定与当前我国药品生产企业的实际状况不相适应。应当根据实际情况,做到有序备案监管,充分利用各级药品检验机构的资源优势。 提高人员素质。一是严格对药品检验人员的专业、学历要求。二是建立定期学习培训机制,由药品检验机构专业技术人员定期对企业药品质量检验人员进行培训和指导,通过公开招聘、派员外出学习、强化质量检验人员操作技能培训等方式,提高药品质量检验人员的素质。三是对生产企业的药品质量检验人员由其所在地药品监管部门实行备案管理,力求稳定药品生产企业质量检验人员队伍,使其严把药品质量检验关,杜绝不合格物料投入生产和不合格中间体流入下道工序,防止不合格成品出厂销售。 增强检验能力。药品生产企业一定要清醒地认识到药品质量检验的重要性,严格按照GMP要求,加强管理,完善制度,把责任落实到相关岗位和人员。根据药品质量标准的要求,配备必要的检验仪器、设备,以满足检验工作的需要,逐步做到企业生产的所有药品,从原料、辅料到中间体、半成品及成品全项目检验。 (罗兰 高宏亮)

药品质量管理是PPT文件,共68页[img]http://ng1.17img.cn/bbsfiles/images/2009/03/200903310733_141385_1626679_3.jpg[/img][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=141386]药品质量管理[/url]
农产品质量安全检测中心等检测单位招人啦,有适合你的吗? 许昌市农产品质量安全检测检验中心公招食品科学与工程、食品质量与安全、农产品质量与安全和化学类的本科、硕士人才了,看有适合自己的吗,赶快报名吧!还有许昌市食品药品检验所、许昌市疾病预防控制中心、河南省畜产品质量监督检验中心许昌分中心等单位也在招考优秀人才。详情请登录许昌毕业生就业信息网(http://www.xcbys.com)、许昌人事人才网(http://www.xcrcsc.gov.cn)和许昌市人事考试中心网(http://www.xcrskszx.com)等网站查看,网上报名时间为2015年6月24日8:00至6月30日18:00,要报名的坛友抓紧吧。
[b][size=4] 3.15又到了,质量问题是老生常谈也要谈啊,化药版块当然是关注药品质量问题了,以下各药品质量各方面,您对哪项最不放心,意见最大?[/size][/b]

[size=16px] 食品药品检测仪器适用于哪些场所 食品药品检测仪器适用于多个场所,包括但不限于: 食品生产环节:在食品生产过程中,食品安全检测仪器可以用于原料、半成品、成品的检测,以确保产品质量。 食品流通环节:在食品流通领域,食品安全检测仪器可用于超市、餐馆、食堂等场所的食品检测,以确保上市食品的安全性。 实验室研究:食品安全检测仪器也是实验室研究的重要工具,可用于研究食品中的各种成分和污染物。 农业部门和养殖场:这些场所可以使用食品药品检测仪器对农产品和动物饲料进行检测,以确保农产品的质量和安全。 屠宰场和肉制品加工企业:这些场所可以使用食品药品检测仪器对肉类和肉制品进行检测,以确保产品的质量和安全。 检验检疫部门:这些部门可以使用食品药品检测仪器对进出口食品进行检测,以确保产品的质量和安全,符合相关法规和标准。 总的来说,食品药品检测仪器适用于需要检测食品药品质量的各个场所,为食品安全和药品安全提供技术支持。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/12/202312200957152570_3592_6098850_3.jpg!w690x690.jpg[/img][/size]
[size=6][b]“首届全国药品质量分析论坛”落下帷幕[/b][/size]http://www.instrument.com.cn 来源:仪器信息网 2010-3-15 15:22:52 点击322次 [b]仪器信息网讯[/b] 为期2天的“首届全国药品质量分析论坛”于2010年3月12日下午在郑州嵩山饭店胜利落下帷幕。[align=center][font=楷体_GB2312][/font][/align][align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010315152410924.jpg[/img][/align][align=center][font=楷体_GB2312][b]中国药学会药物分析专业委员会田颂九研究员主持论坛闭幕式主题报告会[/b][/font][/align] 赛默飞世尔科技SID色谱与质谱应用工程师刘婷女士、国家食品药品监督管理局药品市场监督办公室抽验处姜典才处长、国家药典委员会副秘书长王平研究员在闭幕式上分别做了报告,主题报告会由中国药学会药物分析专业委员会田颂九研究员主持。[align=center][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010315151729682.jpg[/img][/align][align=center][font=楷体_GB2312][b]赛默飞世尔科技SID色谱与质谱应用工程师 刘婷女士[/b][/font][/align][align=center][font=楷体_GB2312][b]报告题目:现代仪器在药品检验中的应用[/b][/font][/align] 刘婷女士介绍,药物从研发到生产,药物分析起着至关重要的作用。目前,药品检验的主要分析技术有分子光谱(傅里叶红外和拉曼光谱)、元素分析([url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url]和[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url])和色谱质谱([url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]联用、GS-MS联用和LC-GC)三大类。其中,分子光谱主要用于中药红外指纹图谱、中药材无损分析、药物降解和杂质分析、生产过程控制、药物含量定量检测等;元素分析用于药物中重金属含量及含金属元素药物的测定;色谱质谱技术则用于中药打假、中药指纹图谱、生物标志物鉴定、药物筛选、代谢组学研究等。这三种技术各有优势,若能综合其优点,将大大提高药物分析检验的能力。例如,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]联用技术广泛应用于生物标志物鉴定、合成产物快速确证、天然产物有效成份筛选、中药分析和质量标准鉴定、药物质量控制等多个领域中;高分辨质谱则可以提高复杂样品的分析能力,主要用于中药、化药的质量分析、生产工艺控制及代谢组学的研究等。[align=center][font=楷体_GB2312][b][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/201031515180777.jpg[/img][/b][/font][/align][align=center][font=楷体_GB2312][b]国家食品药品监督管理局药品市场监督办公室抽验处 姜典才处长[/b][/font][/align][align=center][font=楷体_GB2312][b]报告题目:药品抽验机制探讨[/b][/font][/align] 通过国外药品上市后的监督体制,姜处长表示:“药品抽验机制符合国情,服务于药品监管,正在不断的发展完善,但可借鉴少。”经过多年的摸索探讨,我国的药品抽检模式已趋于科学化规范化。此外,姜处长就我国药品评价抽验模式还作了进一步地探讨: 抽验目的:评价抽验用于了解、掌握辖区内药品质量总体水平;监督抽验则是监督检查中发现的可疑药品进行的针对性抽验; 样品检验:分散检验与集中检验应有机结合,资源充分利用;检验标准应包括法定标准、探索性研究检验等; 结果方式:可以“合格或不合格、质量分析报告、质量风险评估及质量公告”等多种方式呈现; 结果利用:可作为管理部门间、管理部门与生产企业间的信息交流机制;也可用于产品使用的选择标准; 企业作用:树立正确的质量理念与责任感,调动企业积极性,积极参与,积极配合,积极整改。[align=center][font=楷体_GB2312][b][img]http://bimg.instrument.com.cn/lib/editor/UploadFile/20103/2010315151838226.jpg[/img][/b][/font][/align][align=center][font=楷体_GB2312][b]国家药典委员会副秘书长 王平研究员[/b][/font][/align][align=center][font=楷体_GB2312][b]报告题目:中国药典2010年版介绍及国家药品标准要求[/b][/font][/align] 王平副秘书长首先对标准、技术标准、国家药品标准的定义进行了细致入微地介绍。此外,关于《中国药典》2010版,王平副秘书长提到,2010年版《中国药典》药品安全性得到进一步保障、药品有效性与可控性大幅提升、技术现代化与标准国际化明显增加。与2005版药典相比,2010版药典占国标现存总数的比例有所增加,但仍有很大差距。下一阶段的工作重点将集中在以下三方面:国家药品标准提高行动、2010版配套工作(英文版和注释等)、2015版药典编制(编制大纲、组委会筹建等)。 最后,王平副秘书长表示,在全国同仁的共同努力下,2010年版《中国药典》取得了长足的进步和实质性的提升,其颁布实施必将在保证我国药品质量、提高药品质量标准及推进我国药品走向国际三方面起到重要的作用。
中国实施GMP以来,虽然说药品质量取得很大的进步,得到了很大改善,但是为什么中国的药害事故仍然层出不穷呢,从齐二药、上海华联、安徽华源、百易~~~~~~~~到最近的完达山刺五加事件,可以说没有安静过!你认为这正常吗,中国的药品质量能让你信耐吗?请你参与,谢谢!
[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2024/04/202404100935560995_5393_5604214_3.jpg!w690x690.jpg[/img] 随着科技的飞速发展,食品药品检测仪器在保障人们生命健康和提高生活质量方面发挥着越来越重要的作用。这些仪器通过精确、高效地检测食品和药品中的有害物质,确保了人们的饮食用药安全,为社会带来了显著的应用价值。 首先,食品药品检测仪器在保障公众健康方面发挥着重要作用。通过检测食品中的农药残留、重金属等有害物质,以及药品中的非法添加剂、有害成分等,这些仪器有效地减少了有害物质对人体的危害。同时,它们还能及时发现食品药品安全问题,为监管部门提供有力支持,促使企业加强自律,保障公众的健康权益。 其次,食品药品检测仪器在提高食品药品质量方面具有重要意义。随着人们对食品药品安全的要求越来越高,对质量的要求也随之提升。食品药品检测仪器通过精确的检测数据,为生产企业和消费者提供了可靠的质量保障。这不仅有助于提高食品药品的整体质量水平,还促进了行业的健康发展。 此外,食品药品检测仪器还具有推动科技创新和产业发展的价值。随着科技的不断进步,食品药品检测仪器的性能也在不断提升,为科研人员和企业提供了更多创新的空间。这些仪器的研发和应用,不仅推动了相关产业的发展,还为科技创新提供了有力支持,促进了经济社会的可持续发展。 总之,食品药品检测仪器在保障公众健康、提高食品药品质量以及推动科技创新和产业发展等方面具有显著的应用价值。随着科技的进步和社会的发展,这些仪器的应用前景将更加广阔。我们期待更多的科技创新成果在食品药品检测领域涌现,为保障人们生命健康和提高生活质量作出更大贡献。
随着“欣弗”、“齐二药”等药品不良事件的发生,药品质量成为药品研发、生产、评价、监管、使用等各环节最关注的焦点。如何对药品生产全过程进行良好的质量控制,从而获得高质量的药品以满足临床需要,是药品研发者、生产者以及评价者共同关心的问题。本人结合对审评工作中的一些浅显认识,就有效改进质量控制模式,提升质量控制水平提出一点个人不成熟的看法,欢迎大家批评指正。所谓质量控制,其范围包括了为确保药品的质量可控性并进而对安全有效性提供支持的全部药学研究工作,强调了对原料或制剂生产全过程进行控制,是药品研发和生产的关键环节和基础。目前一般认为,质量控制包括过程控制和终点控制两方面,其中过程控制与生产过程同步进行,以经验证的参数为依据,可在全过程中进行多点控制;而终点控制属于滞后行为,于生产结束后进行,并以质量标准为依据进行单点控制。总体上,在实际生产过程中,应以过程控制和终点控制双管齐下的模式进行,以便持续地规模化生产出质量稳定、安全有效性有保障的药品。纵观我国药品生产的历程,不难发现,根据对过程控制和终点控制权重的认识和把握,质量控制方面存在着检验模式??生产模式??设计模式的逐级递进:1、检验模式检验模式主要特征为仅通过终端检验确认药品质量,惯常的做法是以药品质量标准为检验依据,根据质量研究以及稳定性结果判断药品质量是否符合标准的限度要求,并进而判断药品质量是否符合要求。在我国药品研发的早期,此种模式应用普遍,然而已不能满足现阶段对药品质量的要求:1.1 质量标准的局限性导致无法全面体现药品质量。通常,不论自拟标准还是已有国家标准,都无法将检查项目覆盖到药品质量的方方面面,这样就不可避免会出现药品某一方面质量已不符合要求但仍能通过标准检验的情况。例如,多数质量标准都不会将辅料的相关检查项订入标准,而如果辅料种类发生替换,必然影响药品质量,却无法通过标准检验获知这一改变。1.2 质量标准部分项目无法反映药品质量实际情况。即使对于已订入标准的项目,因其自身的局限性也会导致无法反映药品质量。以无菌检查为例,由于微生物在药品中的分布不均匀,且抽检样品数量有限,故所得结果不能真实代表整批药品的无菌状态。1.3 依据标准检验可能会导致一旦产生质量问题难以着手加以解决。依据质量标准只能进行是非判断,无法对异常原因进行溯源。以溶出度为例,如某批片剂药品溶出度检查不合格,而影响溶出度不合格的因素有很多,处方种辅料的来源、性能、制粒过程、中间体粒度、干燥时间、压片压力等等都在其中,此时无法简单判断引起变化的关键点,必须逐项排查,无形中降低了效率,提高了成本。综上,单一的检验模式已不能有效对药品的质量进行控制。2、生产模式鉴于检验模式的局限,业界在上个世纪九十年代参考国外药品生产情况进一步提出了“好的药品是生产出来的,不是检验出来的”这一观点,并正式引入了生产模式概念。生产模式的核心是在检验模式的基础上,将控制重心前移至生产过程中,通过强化过程控制来保证药品质量。与检验模式相比,生产模式在一定程度上解决了一些问题:2.1 全面的过程控制可较好体现药品质量。与质量标准不同,生产过程的全程控制对药品质量有了全方位的覆盖,更能全面反映药品实际质量。只要控制点完善合理,任何未纳入质量标准而可能影响产品质量的因素都会得到有效控制。2.2 与质量标准不同,如果控制得当,质量即可得到保证。仍以无菌检查为例,对于注射液,只要进行了规范的灭菌工艺研究和验证,例如掌握了灭菌前微生物污染水平且灭菌工艺经微生物挑战试验,通过F0的计算,就能保证产品的无菌保证水平(Sterility Assurance Level, SAL)≥6,符合无菌安全性要求。2.3 多数问题得以避免且一旦发生可及早解决。通过过程跟踪,中间体或终产品如出现问题可及时追溯到原因。仍以溶出度为例,如通过过程控制发现某批片剂在制粒干燥过程中设备温度曾发生过变化,其他步骤均无明显变化,最终产品溶出度不合格,则必然是干燥步骤带来的影响,可马上针对此点加以解决。综上,生产模式可较好地保证药品质量。然而,仅仅通过对生产过程的监控来被动“保证”产品质量还不足够,仍需进一步考虑措施主动“决定”药品质量。3、设计模式基于生产模式仍不能完全满足质量控制要求,近两年,国外特别是美国FDA提出了“质量源于设计(Quality by Design, QbD)”的概念,进一步指出如果要确定药品质量,必须有好的设计作为前提,也就是说,好的药品是通过良好设计而生产出来的,如此一来,设计模式的概念应运而生(FDA关于QbD的试点工作将另行撰文介绍)。该模式的核心是在生产模式的基础上,将控制重心进一步前移,在最初确定研发目标时就强化全盘设计的理念,通过系统的设计,预估出拟生产产品的质量,并严格生产过程以达到预期的药品质量。与生产模式相比,设计模式使得提升药品质量成为可能。常规的QbD模式思路是:首先确认目标(该目标不仅仅指一个具体药物或制剂,而是包括了该药物或制剂的相关物理、化学、生物学等具体指标),在设计理念已确认到位的前提下,全方位收集设计目标的相关信息(包括理论、文献以及试验信息),然后全面考虑确定生产方案设计,并通过试验等手段确定关键影响因素(Critical Quality Attributes, CQAs),同时将所有的CQAs与原辅料影响因素和工艺参数关联,根据认知和对工艺的控制程度,逐步建立设计空间(Design Space),最终完成设计并完善整体战略方案,并在药品整个生命周期(Life Cycle)包括后续的质量提升过程中进行有效管理。应该说,药品质量在这样的模式应能得以真正的控制。除了控制产品质量,QbD还很好地在设计中引入风险评估概念,通过对每一设计步骤的评估,可更好地帮助药品研发者判断前进方向(即使是通过评估认为应停止继续研发,及时中止研发也是风险的降低),引导研发。此外,QbD的设计空间对于变更研究还有重要的意义:只要空间设计合理,在所述设计空间内,生产工艺的调整变更风险明显降低,这也有助于药品监管当局拓展出更灵活的变更管理办法。总体来说,设计模式对目前的药品质量控制有很大优势。
如题,小弟就要去了,有没有同行一起交流下啊,有木有游玩计划啊,欢迎大家积极回帖报名,站短联系。 第二届国际药品快速检测技术研讨会暨第三届中美药品分析技术与检测方法研讨会会议名称:第二届国际药品快速检测技术研讨会暨第三届中美药品分析技术与检测方法研讨会会议简介:为加强国内外先进药品分析检测技术和快检技术的交流与合作,以提高检验检测能力和水平,提升快检技术研究和应用,促进药检事业的发展,更好、更全面地发挥技术支撑、技术保障和技术服务作用。本次会议重点就药品检验技术与方法、药品快检技术、药品标准物质、实验室质量管理4个重点领域进行研讨和交流。拟邀请来自WHO、美国FDA、欧洲EDQM等国内外著名专家做专题演讲。会场内同时设置来自国内外的展报展示发表。本届研讨会将邀请国内外多名中美知名药检专家报告,欢迎各有关单位参加交流和投稿。会议时间: 2011年11月15日~16日(星期二至星期三),14日全天报到。会议地点:杭州第一世界大酒店(杭州市萧山区风情大道2555号)会议主题:药品质量与公众健康会议形式:采用大会报告、分会交流、壁报展览的形式,为广大从业人员提供充分、详实的交流、合作平台。征文内容与要求:本次研讨会实行网上投稿。主要包括:1)药品检验技术与方法;2)药品快检技术;3)药品标准物质;4)实验室质量管理。欢迎广大从事药物分析、药品质量控制、药品监督管理及其他相关领域人员积极参会和投稿,所投稿件应为未公开发表的研究论文、专题报告、成果展示、综述及评述等。论文体例、格式请参考《药物分析杂志》。论文采用中英文撰写均可;摘要字数不超过1000字,可适当结合图表;研究论文全文不超过5000字。论文征稿截止日期为2011年10月5日,投稿请务必于2011年10月5日前登录(www.IFRDT.com),有关论文经专家审定后,可优先在《药物分析杂志》上发表。会议注册费:会议代表注册费1200元/人;交通、食宿费自理参会对象与报名方式:各省、市、自治区、直辖市药检所、口岸药检所人员,药品研发机构从事决策、科研、注册部门人员、高等院校,科研院所、药品生产企业及保健食品、食品、化妆品等相关领域的专业人员。国内外机构、企业、学者等。本次研讨会实行网上注册,请各位参会代表务必于2011年11月11日前登录 (www.IFRDT.com),填写相关注册信息。
药品质量标准分析方法验证的目的是证明采用的方法适合于相应检测要求。在建立药品质量标准时,分析方法需经验证;在药品生产工艺变更、制剂的组分变更、原分析方法进行修订时,则质量标准分析方法也需进行验证。方法验证理由、过程和结果均应记载在药品标准起草说明或修订说明中。 需验证的分析项目有:鉴别试验,杂质定量检查或限度检查,原料药或制剂中有效成分含量测定,以及制剂中的其他成分(如防腐剂等)的测定。药品溶出度、释放度等功能检查中,其溶出量等的测试方法也应作必要验证。 验证内容有:准确度、精密度(包括重复性、中间精密度和重现性)、专属性、检测限、定量限、线性、范围和耐用性。视具体方法拟订验证的内容。附表中列出的分析项目和相应的验证内容可供参考。 方法验证内容如下。一、准确度准确度系指用该方法测定的结果与真实值或参考值接近的程度,一般用回收率(%)表示。准确度应在规定的范围内测试。 1.含量测定方法的准确度 原料药可用已知纯度的对照品或样品进行测定,或用本法所得结果与已知准确度的另一个方法测定的结果进行比较。制剂可用含已知量被测物的各组分混合物进行测定。如不能得到制剂的全部组分,可向制剂中加入已知量的被测物进行测定,或用本法所得结果与已知准确度的另一个方法测定结果进行比较。 如该分析方法已经测试并求出了精密度、线性和专属性,在准确度也可推算出来的情况下,这一项可不必再做。 2.杂质定量测定的准确度 可向原料药或制剂中加入已知量杂质进行测定。如不能得到杂质或降解产物,可用本法测定结果与另一成熟的方法进行比较,如药典标准方法或经过验证的方法。在不能测得杂质或降解产物的响应因子或对原料药的相对响应因子情况下,可用原料药的响应因子。应明确表明单个杂质和杂质总量相当于主成分的重量比(%)或面积比(%)。 3.数据要求 在规定范围内,至少用9个测定结果进行评价,例如,设计3个不同浓度,每个浓度各分别制备3份供试品溶液,进行测定。应报告已知加入量的回收率(%),或测定结果平均值与真实值之差及其相对标准偏差或可信限。 (意见3:是否对所设定的浓度范围作出要求,如:该方法用于药品的含量测定,回收率试验的样品浓度应设定于含量100%的±20%之间;用于溶出(释放)曲线考察时,回收率试验的样品浓度应设定于全曲线范围的上、中、下部位。)二、精密度 精密度系指在规定的测试条件下,同一个均匀样品,经多次取样测定所得结果之间的接近程度。精密度一般用偏差、标准偏差或相对标准偏差表示。 在相同条件下,由一个分析人员测定所得结果的精密度称为重复性;在同一个实验室,不同时间由不同分析人员用不同设备测定结果之间的精密度,称为中间精密度;在不同实验室由不同分析人员测定结果之间的精密度,称为重现性。 含量测定和杂质的定量测定应考虑方法的精密度。 1.重复性 在规定范围内,至少用9个测定结果进行评价,例如,设计3个不同浓度,每个浓度各分别制备3份供试溶液,进行测定。或100%的浓度水平,用至少测定6次的结果进行评价。 2.中间精密度 为考察随机变动因素对精密度的影响,应设计方案进行中间精密度试验。变动因素为不同日期、不同分析人员、不同设备。 3.重现性 当分析方法将被法定标准采用,应进行重现性试验,例如,建立药典分析方法时通过协同检验得出重现性结果。协同检验的目的、过程和重现性结果均应记载在起草说明中。应注意重现性试验用的样品本身的质量均匀性和贮存运输中的环境影响因素,以免影响重现性结果。 4.数据要求 均应报告标准偏差、相对标准偏差和可信限。三、专属性 专属性系指在其他成分(如杂质、降解产物、辅料等)可能存在下,采用的方法能正确测定出被测物的特性。鉴别反应、杂质检查、含量测定方法均应考察其专属性。如方法不够专属,应采用多个方法予以补充。 1.鉴别反应 应能与可能共存的物质或结构相似化合物区分。不含被测成分的样品,以及结构相似或组分中的有关化合物,应均呈负反应(不呈正反应?)。2.含量测定和杂质测定 色谱法和其他分离方法,应附代表性图谱,以说明方法的专属性,并应标明诸成分在图中的位置。色谱法中的分离度应符合要求。 在杂质可获得的情况下,对于含量测定,试样中可加入杂质或辅料,考察测定结果是否受干扰,并可与未加杂质或辅料的试样比较测定结果。对于杂质测定也可向试样中加入一定量的杂质,考察杂质能否得到分离。 在杂质或降解产物不能获得的情况下,可将含有杂质或降解产物的试样进行测定,与另一个经验证了的或药典方法比较结果。用强光照射,高温,高湿,酸、碱水解或氧化的方法进行加速破坏,以研究可能的降解产物和降解途径。含量测定方法应比对二法的结果,杂质检查应比对检出的杂质个数,必要时可采用二极管阵列检测和质谱检测,进行峰纯度检查。四、检测限 检测限系指试样中被测物能被检测出的最低量。药品的鉴别试验和杂质检查方法,均应通过测试确定方法的检测限。常用的方法如下。 1.非仪器分析目视法用已知浓度的被测物,试验出能被可靠地检测出的最低浓度或量。 2.信噪比法 用于能显示基线噪声的分析方法,即把已知低浓度试样测出的信号与空白样品测出的信号进行比较,算出能被可靠地检测出的最低浓度或量。一般以信噪比为3∶1或2∶1时相应浓度或注入仪器的量确定检测限。 3.数据要求 应附测试图谱,说明测试过程和检测限结果。五、定量限 定量限系指样品中被测物能被定量测定的最低量,其测定结果应具一定准确度和精密度。杂质和降解产物用定量测定方法研究时,应确定方法的定量限。 常用信噪比法确定定量限。一般以信噪比为10∶1时相应浓度或注入仪器的量确定定量限。六、线性 线性系指在设计的范围内,测试结果与试样中被测物浓度直接呈正比关系的程度。 应在规定的范围内测定线性关系。可用一贮备液经精密稀释,或分别精密称样,制备一系列供试样品的方法进行测定,至少制备5份供试样品。以测得的响应信号作为被测物浓度的函数作图,观察是否呈线性,再用最小二乘法进行线性回归。必要时,响应信号可经数学转换,再进行线性回归计算。 数据要求:应列出回归方程、相关系数和线性图。(意见4:“线性”、“范围”中,如测定方法用于溶出(释放)曲线考察时,是否规定样品浓度的范围应涵盖整条曲线。)七、范围 范围系指能达到一定精密度、准确度和线性,测试方法适用的高低限浓度或量的区间。 范围应根据分析方法的具体应用和线性、准确度、精密度结果和要求确定。原料药和制剂含量测定,范围应为测试浓度的80%~120%;制剂含量均匀度检查,范围应为测试浓度的70%~130%,根据剂型特点,如气雾剂、喷雾剂,范围可适当放宽;溶出度或释放度中的溶出量测定,范围应为限度的±20%,如规定了限度范围,则应为下限的-20%至上限的+20%;杂质测定,研究时,范围应根据初步实测,拟订为规定限度的±20%。如果含量测定与杂质检查同时进行,用百分归一化法,则线性范围应为杂质规定限度的-20%至含量限度(或上限)的+20%。八、耐用性 耐用性系指在测定条件有小的变动时,测定结果不受影响的承受程度,为把方法用于常规检验提供依据。开始研究分析方法时就应考虑其耐用性。如果测试条件要求苛刻,则应在方法中写明。典型的变动因素有:被测溶液的稳定性,样品的提取次数、时间等。液相色谱法中典型的变动因素有:流动相的组成和pH值,不同厂牌或不同批号的同类型色谱柱,柱温,流速等。气相色谱法变动因素有:不同厂牌或批号的色谱柱、固定相,不同类型的担体,柱温,进样口和检测器温度等。 经试验,应说明小的变动能否通过设计的系统适用性试验,以确保方法有效。 附表 检验项目和验证内容 项目 鉴别 杂质测定 含量测定及溶出量测定 内容 定量 限度 准确度 - + - + 精密度 - - - + 重复性 - + - + 中间精密度- +① - +① 专属性② + + + + 检测限 - -③ + - 定量限 - + - - 线性 - + - + 范围 - + - + 耐用性 + + + + ① 已有重现性验证,不需验证中间精密度。 ② 如一种方法不够专属,可用其他分析方法予以补充。 ③ 视具体情况予以验证。