部分血浆样本出现絮状物,请问产生原因是什么?对于[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICPMS[/color][/url]的测定结果是否有影响?谢谢!
翻了一下帖子,发现大家基本上都是用2%-5%的硝酸进行样本间的冲刷,但是我的样本是人血浆,用相对高浓度的硝酸冲刷是否更容易形成絮状沉淀从而堵塞?而Triton X-100(曲拉通)是表面活性剂,用1%硝酸+0.1%Triton X-100冲刷效果会不会更好一些?谢谢大家
部分血浆样本出现絮状物,请问产生原因是什么?对于[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICPMS[/color][/url]的测定结果是否有影响?谢谢解答!
老师,请教一下,标准品纯溶液的保留时间比加入空白血浆后经处理后进样的保留时间提前05分钟,能确定加入空白血浆后的峰是标准品的峰吗?
标准品纯溶液的保留时间比加入空白血浆后经处理后进样的保留时间提前05分钟,能确定加入空白血浆后的峰是标准品的峰吗?
我用沉淀蛋白处理血浆样品,为了使药物更好的从血浆蛋白中释放 需要加入磷酸盐 可以进质谱么?
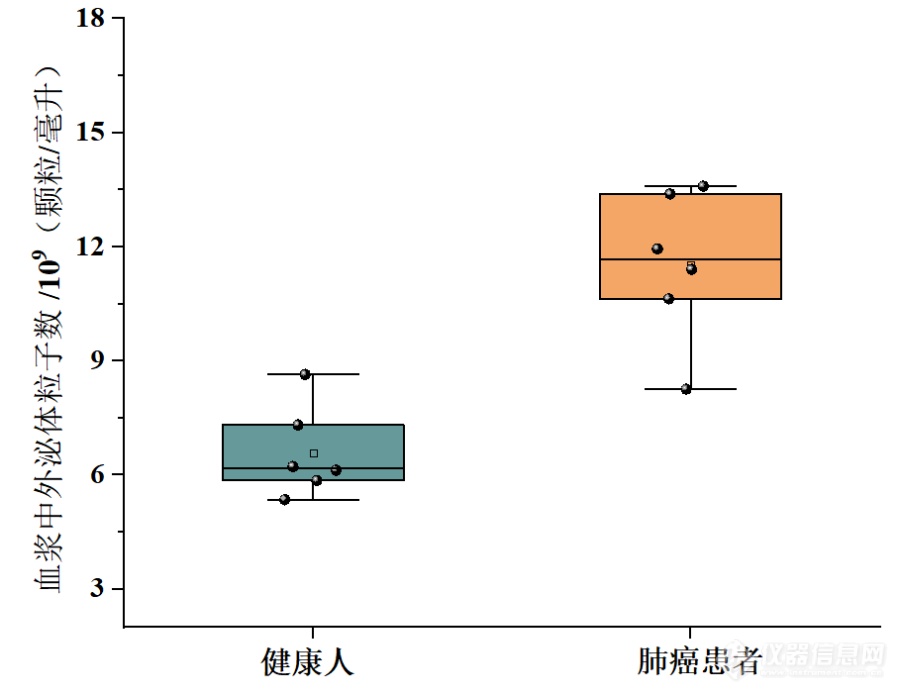
[align=center][font='times new roman'][size=16px]血浆外泌体[/size][/font][font='times new roman'][size=16px]在肺癌诊断中的应用[/size][/font][/align][font='times new roman'][size=16px]引言[/size][/font][font='宋体']外泌体作为重要的信息载体,参与肿瘤的发生、进展、转移和化疗耐药等过程,外泌体携带大量的遗传物质,已成为液体活检最理想的分析目标。外泌体也是目前最有前途的非侵入性诊断和预后的生物标志物之一。目前,超速离心法是外泌体分离的金标准。为了实现外泌体的临床价值,本研究以超速离心法富集了人血浆中的外泌体,并对健康人及肺腺癌患者的血浆样品做了区分,用于下游的肺癌诊断[/font][font='宋体']。[/font][align=left][font='times new roman'][size=16px]血浆外泌体用于肺癌诊断的策略[/size][/font][/align]肺癌仍然是世界范围内癌症相关死亡的主要诱因,因为大多数患者被诊断时均为晚期。因此,我们初步评估了超速离心法富集外泌体用于肺癌诊断的潜在适用性。我们收集了6名健康捐赠者和6名肺癌患者的血浆样本。利用超速离心法富集1 mL血浆样本中的外泌体,对比健康捐赠者和肺癌患者的血浆外泌体,结合数据分析,评估血浆外泌体在监测肺癌诊断方面潜在的适用性。[align=left][font='times new roman'][size=16px][color=#000000] [/color][/size][/font][font='times new roman'][size=16px]血浆中外泌体表征[/size][/font][/align]测试了超速离心法对复杂血浆样品的适用性。首先,利用纳米颗粒示踪分析对超速离心法得到的血浆外泌体进行了表征。如图(a)所示, 纳米颗粒示踪分析显示分离的外泌体粒径分布同样较窄,平均粒径为128.8 nm。与细胞上清样品类似,Western blot方法验证了分离外泌体的有效性。如图(b)所示,经富集后,典型的低丰度外泌体标记物同样得到了有效检测。以上结果证明,超速离心法能[img]" style="max-width: 100% max-height: 100% [/img]够成功的用于血浆中外泌体的富集。[align=center][font='黑体'][size=14px]图[/size][/font][font='黑体'][size=14px] (a)重悬液中血浆外泌体的[/size][/font][font='黑体'][size=14px]纳米颗粒示踪分析技术[/size][/font][font='黑体'][size=14px]表征,(b)[/size][/font][font='黑体'][size=14px]Western blot方法[/size][/font][font='黑体'][size=14px]表征血浆[/size][/font][font='黑体'][size=14px]外泌体标记物HSC70、TSG101、CD63和CD9[/size][/font][font='黑体'][size=14px]蛋白条带[/size][/font][/align][align=left][font='times new roman'][size=16px]血浆外泌体用于肺癌[/size][/font][font='times new roman'][size=16px]的[/size][/font][font='times new roman'][size=16px]诊断[/size][/font][/align][font='宋体']我[/font]们收集了6名健康捐赠者和6名肺癌患者的血浆样本。利用超速离心法富集血浆样本中的外泌体。采用纳米颗粒示踪分析技术对血浆外泌体标进行表征。如图所示,与健康对照组相比,肺癌患者的血浆外泌体显著上调。对比健康捐赠者和肺癌患者的血浆外泌体,结合数据分析,证明血浆外泌体在监测肺癌诊断方面具有潜在的适用性。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310171534194891_9083_6197575_3.png[/img][font='黑体'][size=14px]图[/size][/font][font='黑体'][size=14px] [/size][/font][font='黑体'][size=14px]健康人与肺癌患者血浆中外泌体的[/size][/font][font='黑体'][size=14px]纳米颗粒示踪分析[/size][/font][font='黑体'][size=14px]技术[/size][/font][font='黑体'][size=14px]表征[/size][/font][/align][align=left][font='黑体'][size=18px]小结[/size][/font][/align]超速离心法可以高效、特异性地从人血浆中富集、纯化外泌体,在此我们评估了超速离心法在复杂血浆样品中的适用性。肺癌是全球癌症相关死亡的主要原因,因为在原发癌症扩散之前进行早期诊断具有挑战性。以6例肺癌患者(6例健康供者为对照)的人血浆为样本,进一步研究超速离心法富集外泌体在肺癌筛查和诊断中的应用。这些结果证实了血浆外泌体在肺癌筛查和监测中的应用潜力。
各类仪器平稳使用的条件下,稳定可靠的样品前处理也是关键步骤,为大家分享血浆样品的获取途径和方法。
本人主要做生物样本的检测,现在有一个项目要测定人血浆中的Bi元素,从样本前处理过程和稳定性和分析时间方面考虑,用AFS好还是用ICP-MS好?纯外行,没有测过金属元素,希望各位提供宝贵的意见
血浆速冻技术的新进展血浆是抗凝全血经物理方法分离制备的一种血液成分,其临床应用是现代成分输血的重要组成部分,尤其是新鲜冰冻血浆(PPT),在临床治疗中更有其重要的作用。血浆是多种血浆蛋白质的混合物,其中包含白蛋白、免疫球蛋白和凝血因子类蛋白。为了有效的保护血浆内的有效成分,特别是凝血因子,并随着我国成分输血技术的发展,新鲜冰冻血浆及冷沉淀的制备技术及应用随之也越来越广泛。目前我国《血站基本标准》实施细则中第92条规定:制备新鲜冰冻血浆时,抗凝剂为CPD、CP2D、CPDA-1的血液应在8小时内分离并速冻;抗凝剂为ACD的血液应在6小时内分离并速冻。其质量要求: 含有全部凝血因子。血浆蛋白为6~8g/%;纤维蛋白原0.2~0.4g%;Ⅷ因子含量:≥0.7 IU/ml 规格。可以看出,时间和温度是制备出质量合格的新鲜冰冻血浆两个关键点,尤其是对于活性很高的凝血因子VIII和V,时间和温度是影响其活性的重要因素。中国医学检验杂志1995年3月第18卷第2期《血浆凝血因子测定的影响因素探讨》,作者通过对比经过不同温度和时间后FVIII含量发现:32℃条件下6小时活性只有48%,24小时5%4℃条件下6小时活性有95%,24小时剩29%。由于在血浆结冰过程中,凝血因子VIII含量与时间呈指数下降关系,所以速冻时间越短,凝血因子VIII和V的损失也就越小。国际上通用的标准是1个小时内速冻完成,如果能在30分钟内完成速冻,那么效果将会更好。因此要保证新鲜冰冻血浆及冷沉淀等成分的疗效,必需在采供血过程中控制好冷链和时间链,其中血浆速冻技术是其中一个重要环节,速冻的时间和效果将直接关系到血浆及冷沉淀产品的质量和疗效。 随着《中华人民共和国献血法》的实施和无偿献血的深入开展,血站的采血方式已由有偿献血时代的站内采血为主转向站外无偿流动采血。要达到采血后6h(或8 h)内分离血浆并冻结有时存在一定的困难。因此为保证临床使用新鲜冰冻血浆、血浆冷沉淀的质量尽可能的缩短血浆速冻的时间就显的尤为重要了。我国血站采用的血浆速冻技术主要经过了以下几个发展阶段:1、用超低温冰箱来进行血浆速冻。此种方法的主要不足在于:冰箱内空间有限,将血浆叠加在一起,上下接触不均匀。冰箱制冷效率有限,速冻时间较长(通常需要6-8h)。显然是达不到要求的。2、强制对流型速冻机。最初的血浆速冻设备我们称为强制对流型速冻机(blast freezer)。该类设备的设计思路来源于普通冰箱,也是使用空气作为冷媒。通过更强的制冷功率来得到低温空气,并且使冷空气快速的流动,加快冷空气与溶液的热交换来实现快速冻结的目的,因此,也称之为“冷风制冷”。由于这类设备内冷空气流动速度比冰箱内空气流动速度有了很大提高,使得制冷效果得到提高,缩短了血浆冻结的时间。对于超低温冰箱来说,这种方式使得速冻的时间已经得到了大大的缩短,但由于关键技术的不足,其速冻时间通常都需要2h。3、平板接触式速冻机。这类设备是根据最新的平板接触制冷技术制造而成。它通过改变传统的“空气”冷媒,用特制不锈钢作为冷媒,加快血浆热交换实现速冻,从而达到缩短速冻时间的目的。今天,我们来讲讲血浆速冻技术的新进展:平板接触式血浆速冻技术。平板接触式速冻(contact plate freezing)。该技术通过高效压缩机使金属板稳定在-50℃的温度,血浆袋通过与-50℃的低温金属板直接接触进行热传递,由于空气的热传导率仅为0.28 w/m•k,而金属的热传导率为58.02w/m•k是空气的上百倍。因此使得降温效率得到极大的提高,降温过程所需时间更少,因此可以得到更多的凝血因子,得到更好质量的新鲜冰冻血浆。平板接触式速冻技术,虽然出现的时间不长,但是它已经以其强大的技术优势已经在国际上占据了血浆速冻市场40%的份额。
我现在正在做生物样本的浓度检测,所用仪器是菲尼根的半定量质谱检测仪器,血浆处理方法是甲醇沉淀蛋白后进样。进了两套标准曲线,一套是在空白血浆中的标准曲线,一套是刚配制好的标准溶液,但是每一套标准曲线都不好,曲线一共设置8个点,前5个点的线性非常好,但是低浓度的三个点已经重复了好几遍了,其响应与浓度没有任何关系,比例关系也比较乱,检测过程中是加了内标的,而且内标的响应也一致,没有较大变化。还有,最低血浆浓度设在800ng/ml,实际进样浓度稀释5倍。请各位同仁指点下我怎么来分析原因,及可能采取的措施呢。
报道了一种新颖的织物相吸附萃取-高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-光电二极管阵列检测(FPSE-HPLC-PDA)方法,用于同时萃取和分析包括二苯甲酮(BZ)在内的六种二苯甲酮衍生物紫外滤光剂;5-苯甲酰基-4-羟基-甲氧基苯磺酸(BP-4);双(4-羟基苯基)甲酮(4-DHB);双(2,4-二羟基苯基)甲酮(BP-2);(2,4-二羟基二苯甲酮) (BP-1) 和 2,2'-二羟基-4-甲氧基二苯甲酮 (DHMB) 在人类全血、血浆和尿液样本中。色谱分离方法使用 Spherisorb ODS 1 (C 18 ) 色谱柱以等度洗脱模式进行,运行时间 25 分钟。FPSE-HPLC-PDA 方法在 0.1 至 10 μg/mL 范围内对所有 UV 过滤化合物进行了验证。4-羟基苯甲酸丙酯(也称为对羟基苯甲酸丙酯)用作内标(IS)。定量限为 0.1 μg/mL,六种 UV 滤光片的加权矩阵匹配标准校准曲线在高达 10 μg/mL 的浓度下表现出良好的线性。详见[url]https://doi.org/10.1016/j.jchromb.2019.04.028[/url]
大家好,讨论下血浆中药物萃取回收率的计算问题,分析方法是用液相做的,加了内标溶液,我要计算药物的萃取回收率怎么算?从体内药物分析书上看,如果加入了内标的话,应该是用血浆处理样品中药物和内标峰面积比值除以未经萃取处理的标准品中药物和内标峰面积的比值但是从文献上看,并没有用比值做,而是直接用血浆中药物峰面积除以标准品中药物峰面积这两种方法用哪种,为什么文献上没有用药物和内标的比值,原因何在????急!!急!!
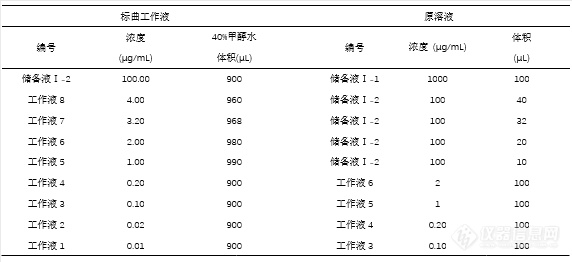
[align=center][font=宋体][size=14px]生物样本处理日志的书写格式[/size][/font][/align][font=宋体][size=14px]每次在整理文章或专利时,我们都需要理清整个实验的流程和步骤,针对每一个实验过程中出现的问题,开展讨论及研究。生物样本的操作日志尤其重要,因为生物样本的方法学与溶液不同,相对溶液要复杂很多,例如生物样本的方法学需要考察基质效应和溶液稳定性、血浆样本的稳定性等,在这些实验的进行中,我们需要将实验开始的时间、中间操作的流程及出现的问题和如何解决的方案一一列出,这样在多久后我们翻出处理日志都可以回忆起当时的操作。[/size][/font][font=宋体][size=14px]下面为大家展示一个我们平常实验过程需要总结的日志和记录。[/size][/font][b][font=宋体][size=14px]血浆标准曲线配制:[/size][/font][/b][font=宋体][size=14px]用[/size][/font][b][u][font='Times New Roman',serif][size=14px]2017-12-17[/size][/font][/u][/b][font=宋体][size=14px]配制的[/size][/font][b][u][font='Times New Roman',serif][size=14px]FDST[/size][/font][/u][/b][font=宋体][size=14px]标准溶液,按照血浆标准品处理方法,配制标血浆准曲线,包括溶剂,空白血浆和[/size][/font][font='Times New Roman',serif][size=14px]0[/size][/font][font=宋体][size=14px]点。[/size][/font][b][font=宋体][size=14px]血浆质控样本配制:[/size][/font][/b][font=宋体][size=14px]用[/size][/font][b][u][font='Times New Roman',serif][size=14px]2017-12-17[/size][/font][/u][/b][font=宋体][size=14px]配制的[/size][/font][b][u][font='Times New Roman',serif][size=14px]FDST[/size][/font][/u][/b][font=宋体][size=14px]标准质控溶液,按照血浆标准品处理方法,配制质控样本,[/size][/font][b][u][font='Times New Roman',serif][size=14px]L1~2[/size][/font][/u][/b][font=宋体][size=14px],[/size][/font][b][u][font='Times New Roman',serif][size=14px]M1~2[/size][/font][/u][/b][font=宋体][size=14px]和[/size][/font][b][u][font='Times New Roman',serif][size=14px]H1~2[/size][/font][/u][/b][font=宋体][size=14px],作为质控样本。[/size][/font][b][font=宋体][size=14px]生物样本处理[/size][/font][font='Times New Roman',serif][size=14px]:[/size][/font][/b][font=宋体][size=14px]按照血浆样本处理方法,处理餐后[/size][/font][b][u][font='Times New Roman',serif][size=14px]1~12[/size][/font][/u][/b][font=宋体][size=14px]号健康志愿者样本共计[/size][/font][font='Times New Roman',serif][size=14px]109[/size][/font][font=宋体][size=14px](包括空白样本)。选择复测样本的大约是:[/size][/font][font='Times New Roman',serif][size=14px]Cmax[/size][/font][font=宋体][size=14px]和消除相附近的样本,按总样本量的约[/size][/font][font='Times New Roman',serif][size=14px]10%[/size][/font][font=宋体][size=14px]选取。[/size][/font][b][font=宋体][size=14px]样本检测[/size][/font][font='Times New Roman',serif][size=14px]:[/size][/font][/b][font=宋体][size=14px]样本进样顺序为:[/size][/font][font=宋体][size=14px]溶剂([/size][/font][font='Times New Roman',serif][size=14px]sol[/size][/font][font=宋体][size=14px]),空白样本([/size][/font][font='Times New Roman',serif][size=14px]Blank[/size][/font][font=宋体][size=14px]),血浆标准曲线,空白样本消除可能的高浓度残留,然后是生物样本,在此过程中每[/size][/font][font='Times New Roman',serif][size=14px]17[/size][/font][font=宋体][size=14px]个样本的前、后各插入两个质控样本,最后再将血浆标准曲线重新进样一次。数据和结果均存放于文件夹[/size][/font][b][u][font='Times New Roman',serif][size=14px]SAM-I[/size][/font][/u][/b][font=宋体][size=14px]中。[/size][/font][font=宋体][size=14px]按[/size][/font][font='Times New Roman',serif][size=14px]6-1[/size][/font][font=宋体][size=14px]表精密量取坎地沙坦储备液[/size][/font][font='Times New Roman',serif][size=14px]I-2[/size][/font][font=宋体][size=14px],用[/size][/font][font='Times New Roman',serif][size=14px]50%[/size][/font][font=宋体][size=14px]的甲醇[/size][/font][font='Times New Roman',serif][size=14px]-[/size][/font][font=宋体][size=14px]水配置成系列坎地沙坦标准工作溶液,浓度分别为:[/size][/font][font='Times New Roman',serif][size=14px]0.01[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]0.02[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]0.1[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]0.2[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]1[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]2[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]3.2[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]4 μg /mL[/size][/font][font=宋体][size=14px],保存于[/size][/font][font='Times New Roman',serif][size=14px]4[/size][/font][font=宋体][size=14px]℃[/size][/font][font=宋体][size=14px]备用。[/size][/font][align=center][font=宋体][size=14px]表[/size][/font][font='Times New Roman',serif][size=14px]6-1[/size][/font][font=宋体][size=14px]坎地沙坦标曲工作液配制方法[/size][/font][/align][align=center][font='Times New Roman',serif][size=14px] [img=,572,262]https://ng1.17img.cn/bbsfiles/images/2020/07/202007262111252711_212_3255306_3.png!w572x262.jpg[/img][/size][/font][/align][font='Times New Roman',serif][size=14px]6[/size][/font][font='Times New Roman',serif][size=14px].8[/size][/font][font='Times New Roman',serif][size=14px].3 [/size][/font][font='Times New Roman',serif][size=14px]KDST[/size][/font][font=宋体][size=14px]质控工作液配制[/size][/font][font=宋体][size=14px]按表[/size][/font][font='Times New Roman',serif][size=14px]6-2[/size][/font][font=宋体][size=14px]所示,精密量取坎地沙坦浓溶液,用[/size][/font][font='Times New Roman',serif][size=14px]40%[/size][/font][font=宋体][size=14px]的甲醇[/size][/font][font='Times New Roman',serif][size=14px]-[/size][/font][font=宋体][size=14px]水配置成系列坎地沙坦质控工作液,浓度分别为:[/size][/font][font='Times New Roman',serif][size=14px]0.03[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]0.6[/size][/font][font=宋体][size=14px],[/size][/font][font='Times New Roman',serif][size=14px]3 μg/mL[/size][/font][font=宋体][size=14px]。保存于[/size][/font][font='Times New Roman',serif][size=14px]4 [/size][/font][font=宋体][size=14px]℃[/size][/font][font=宋体][size=14px]冰箱备用。[/size][/font][align=center][font=宋体][size=14px]表[/size][/font][font='Times New Roman',serif][size=14px]6-2[/size][/font][font=宋体][size=14px]坎地沙坦质控工作液配制方法[/size][/font][/align][align=center][img=,563,154]https://ng1.17img.cn/bbsfiles/images/2020/07/202007262111442856_7728_3255306_3.png!w563x154.jpg[/img][/align][b][font='Times New Roman',serif][size=14px]6.8.4 KDST-d4[/size][/font][font=宋体][size=14px]储备溶液[/size][/font][/b][font='Times New Roman',serif][size=14px](2018-11-19[/size][/font][font=宋体][size=14px]配制的浓溶液[/size][/font][font='Times New Roman',serif][size=14px])[/size][/font][font=宋体][size=14px]将[/size][/font][font='Times New Roman',serif][size=14px]1.0mg[/size][/font][font=宋体][size=14px]坎地沙坦[/size][/font][font='Times New Roman',serif][size=14px]-d4[/size][/font][font=宋体][size=14px]用[/size][/font][font='Times New Roman',serif][size=14px]1 mL[/size][/font][font=宋体][size=14px]甲醇溶解,配制成[/size][/font][font='Times New Roman',serif][size=14px]1 mg/mL[/size][/font][font=宋体][size=14px]储备液[/size][/font][font=宋体][size=14px]Ⅱ[/size][/font][font='Times New Roman',serif][size=14px]-1[/size][/font][font=宋体][size=14px],取储备液[/size][/font][font=宋体][size=14px]Ⅱ[/size][/font][font='Times New Roman',serif][size=14px]-1 40 μL[/size][/font][font=宋体][size=14px],加[/size][/font][font='Times New Roman',serif][size=14px]40%[/size][/font][font=宋体][size=14px]甲醇[/size][/font][font='Times New Roman',serif][size=14px]40mL[/size][/font][font=宋体][size=14px],配制成含[/size][/font][font='Times New Roman',serif][size=14px]KDST-d4 [/size][/font][font=宋体][size=14px]浓度为[/size][/font][font='Times New Roman',serif][size=14px]1000 ng/mL[/size][/font][font=宋体][size=14px]内标工作液,保存于[/size][/font][font='Times New Roman',serif][size=14px]4 [/size][/font][font=宋体][size=14px]℃[/size][/font][font=宋体][size=14px]备用。[/size][/font][font=宋体][size=14px]实验人员签字:[/size][/font][font='Times New Roman',serif][size=14px] [/size][/font][font=宋体][size=14px]实验时间:[/size][/font][font='Times New Roman',serif][size=14px] [/size][/font][font=宋体][size=14px]最后感谢仪器信息网组织原创大赛为我们提供交流平台。[/size][/font][font='Times New Roman',serif][size=14px] [/size][/font][font='Times New Roman',serif][size=14px] [/size][/font]
本人是主要做生物样本检测的,日常主要使用液质联用,现在有一个项目要测定血浆中的Bi元素,请问从样品前处理过程,以及分析时间和稳定性等方面考虑,是用ICP-MS好还是原子荧光好?本人纯外行,希望各位提供宝贵的意见
仪器型号为PE nexlon 2000,采用KED模式,手动进样,雾化气流速为1.02L/min,He气流速为4ml/min,wash设为-42 rpm 25s,用1%HNO3冲洗,sample flush为-35 rpm 25s,read delay设为 -35 rpm 25s。样本为人血浆,样品前处理为1%硝酸+0.1%曲拉通稀释40倍,待测元素为Mg、Ca、V、Cr、Mn、Fe、Co、Ni、Cu、Zn、As、Se、Sr、Mo、Cd、Sb、Pb,内标选用的是Sc、In、Ge、Bi,采用的是在线加内标,内标浓度为500ppb(内标管比样品管细,实际浓度预计为50ppb),目前还在用血浆质控摸方法,还没有做样本。目前出现的问题是,在测低浓度质控时,V、Mn、Ni、Mo、Cd均为负值,已经试过把相应元素积分时间调为1.5s,He气流速调为4ml/min,但是还是不行,请问大家有没有什么解决办法?谢谢大家!
大家好,讨论下血浆中药物萃取回收率的计算问题,分析方法是用液相做的,加了内标溶液,我要计算药物的萃取回收率怎么算?从体内药物分析书上看,如果加入了内标的话,应该是用血浆处理样品中药物和内标峰面积比值除以未经萃取处理的标准品中药物和内标峰面积的比值但是从文献上看,并没有用比值做,而是直接用血浆中药物峰面积除以标准品中药物峰面积这两种方法用哪种,为什么文献上没有用药物和内标的比值,原因何在????急!!急!!
实验过程中用过甲醇,乙腈,丙酮沉淀蛋白,但由于该多酚酸属于小分子的水解鞣质,与蛋白结合紧密,回收率很低,后来又试了C18和waters的HLB固相萃取小柱,结果我要检测的这个东西没有了,不知道跑哪去了,过小柱时,我直接用水稀释标准品上样的,将上样流下来的和接下来洗脱的每一个馏分都进样后,没有发现要检测的这个多酚酸,请教各位还有没更好的血浆处理方法呢,谢谢了。
我在最近的实验中用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS测定一类头孢药物,用的是沉淀蛋白法。发现标准品在现在流动相情况下出峰,但是一但加入到血浆样品中就不出峰,我试过很多沉淀蛋白的方法,把处理样品的沉蛋白剂调节PH值都没有效果,不知道哪位高手曾经做过此类药物,请给提个建议吧![em63]
[color=#444444]请教大神,走头孢喹肟血浆样品紫外高效液相色谱,标准品样能走出来,用血浆经前处理后的样就走不出来了,血浆前处理过程主要是用乙腈重复提两次,取上清液,然后氮吹干,进样,请问走不出峰是什么原因呢?急求,多谢![/color]
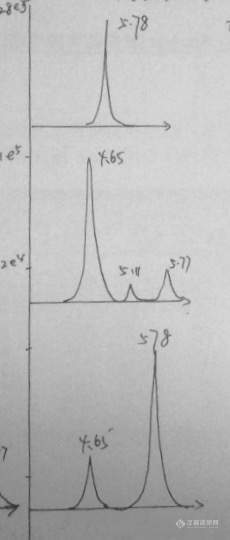
[color=#444444]仪器:[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]AB5500[/color][color=#444444]流动相:乙腈-甲酸水[/color][color=#444444]梯度洗脱,出峰时间在88%等度洗脱中[/color][color=#444444]对于待测成分进行了回收率测试80%, 空白血浆加标准品走标曲r=0.996 ,[/color][color=#444444]其中两个成分出峰时间分别为3.0和5.70,无杂峰[/color][color=#444444]采集的血浆样品进样,一个成分在5.7min不再出峰,但于4.6和5.1min出了两个响应的峰[/color][color=#444444] 另一个成分在2.8min和3.0出峰,两个峰连在一起无法定量[/color][color=#444444] (上传的图自上而下依次是:空白血浆+标准品;采集样品;采集样品+标准品)[/color][color=#444444]现在这两个成分都无法定量,我觉得可能是其他成分代谢产物在同一通道出峰,影响了待测化合物的出峰,但是又分不开[/color][color=#444444]想求助大家,该怎么定量这两个化合物?[/color][color=#444444][img=,230,540]https://ng1.17img.cn/bbsfiles/images/2019/06/201906111123585259_1609_1843534_3.jpg!w230x540.jpg[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/06/201906111123589171_8887_1843534_3.jpg!w690x517.jpg[/img][/color]
做一个药物的药物动力学,样品是血浆基体,药物极性特强,含氮多碱性,在C18上基本不保留,想用离子色谱做试试,但没有查到离子色谱做血浆样品的文献,样品准备用乙腈沉淀蛋白后离心的上清液直接进样,离子色谱柱可以吗?
我们按照一篇文献报道,用液相色谱做血浆中脂肪酸测定,脂肪酸标准品经过衍生化以后进样却未见峰出来,但有一些杂峰。请问在做衍生化时,应注意哪些问题?

作者:http://d.g.wanfangdata.com.cn/Images/head_pic.gif吴秀君 http://d.g.wanfangdata.com.cn/Images/head_pic.gif李国信 http://d.g.wanfangdata.com.cn/Images/head_pic.gif肇丽梅 Author:WU Xiu-jun LI Guo-xin ZHAO Li-mei 作者单位:中国医科大学附属第二医院临床药理研究室,沈阳,110004 辽宁中医药火学附属第二医院,沈阳摘要: 目的 建立测定血浆、尿样本中丹皮酚含量的反相高效液相色谱法.方法 血浆样品经沉淀蛋白,尿样经稀释后,以乙腈-0.1%磷酸pH 3.5(55:45)为流动相,经Diamonsil C18柱分离,进行色谱分析.结果 本方法丹皮酚的血浆浓度在20~1 000μg·L-1,尿中浓度在20~800μg·L-1内线性关系良好,方法回收率在81.0%~85.0%之间,日内、日间RSD均小于11.0%.结论 本方法简便、快速、灵敏度高,可用于丹皮酚的药动学研究.http://ng1.17img.cn/bbsfiles/images/2012/08/201208271811_386615_2379123_3.jpg
实验室是做新药研发的,需要往药监局申报,在药代动力学这块,为了提高效率,我们的生物样本前处理只沉蛋白,取上清,过滤膜,进LC/MS检测。现在不知道在考察基质效应的样品该怎么处理了。请各位前辈指导一下,谢谢!
各位大侠!我是刚毕业的本科生,我做生物等效性的,在处理空白血浆的时候一直有干扰峰,换流动相没法消除,分不开峰,现急求血浆处理方法,我准备用5%高氯酸沉淀蛋白的方法,但是对于高氯酸沉淀后,取上清液直接进样有点担心,PH值合适吗?能直接进样吗?会不会伤柱子啊?请各位大侠帮帮新人!先谢谢啦!我做了好多次了,空白一直有干扰,是新鲜的空白血,应该不会污染到的.
[color=#444444]最近在用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]建方法……标准品溶液用该方法做标准曲线基本做完,但是空白血浆液液萃取,进样,提取二级[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]峰后,总有干扰,而且峰面积还很大……想请教下这个干扰可能与哪些因素有关……我用的溶剂都进过样儿,均没有干扰,感觉不是外部引入的……会不会因为是避孕药,然后体内某些激素的干扰……萃取剂换了几种还是有干扰,求大神帮帮我吧[/color]
标准偏差总体和样本的差别是什么?
想问一下做血浆脂肪酸检测,血浆质控样品要经过怎样的处理才能混匀做成质控呀?先前涡旋三分钟定量分析有些脂肪酸RSD相差比较大?所以想问问大家是怎样做的?
高效液相色谱法测定大鼠血浆和全血中核黄素的含量韦京豫, 郭长江, 杨继军, 蒋与刚, 李云峰, 徐琪寿(军事医学科学院卫生学环境医学研究所,天津)摘要:为了直接反映核黄素营养状况对血中核黄素水平的影响,建立了高效液相色谱测定大鼠血浆及全血中核黄素含量的方法。采用Diamonsil C18色谱柱250mmx4.6mm i.d.5um)分离,以甲醇5mol/l乙酸铵(体积比为1.2ml/min)为流动相,流速1.2ml/min,荧光检测器检测(激发波长450nm,发射波长:520nm)。样品经乙腈、三氯甲烷处理后进样分析。核黄素测定的线性范围5-200nmol/l,最低检测限为2.5nmol/l(s/n=2),日内测定的峰面积的相对标准偏差(RSD)为1.2%,日间测定的RSD=4.3%。核黄素在血浆样品中的加标回收率为97.0%-104%,在全血样品中的加标回收率为97.4%-104.4%.关键词:高效液相色谱法;核黄素;血浆;全血;大鼠http://ng1.17img.cn/bbsfiles/images/2012/07/201207241234_379356_2355529_3.jpg