罗红霉素使用2005年版药典高效液相法检测,拖尾现象很严重?有没有很好的解决方法?
2010版药典中,罗红霉素的含量检测项下的系统适用性下新增加的红霉素峰与罗红霉素峰的分离度不得小于15.0,我们试做了几次都不成功,请教各位前辈,是否可告知具体操作
罗红霉素按《中国药典》2005版分析,峰严重拖尾,拖尾因子在2点几,不知各位有什么经验,交流一下!
用HPLC检测罗红霉素,紫外检测器,检出限能达到多少呢?有没有可能达到100ppb,求教详细方法
[em09509]请大家帮帮忙,看看是出现什么问题了。我用的仪器是agilent 1100周五的时候白天做了一个检验芦荟苷的样品,实验过程中没有出现什么异常。于是,晚上就序列上了罗红霉素的含测。做罗红霉素时要求用流动相做溶剂溶解样品,所以最初配制流动相的时候就配了8000ml,已经用了大概4000ml的流动相做了两批样品,做第三批的时候应该不会出现什么问题了,于是就序列上了。但是第二天看图谱的时候发现出现很大的异常。首先,出峰时候比以前晚很多,以前是大概11分钟出峰,而这些样品的出峰时间都推后到了大概15分钟,峰明显展宽,像是蒙谷包。峰面积也出现了很大差别。其次,当时晚上也序列上了有关物质,对照的出峰时间是大概15分钟,而样品却出现在40分钟,而且峰形很难看。基于上述问题我做了一些工作。首先换了一根色谱柱,用那个流动相和样品,但是未出峰(以前这个柱子能够做出来结果),其次,还是用这个流动相和样品在岛津上做有关物质,能够出峰也比较正常。今天,我重新配了流动相换了多根色谱柱在agilent1100上做,发现要么出峰,峰形展宽,要么就不出峰。请问大家这倒底是什么原因?谢谢。
我做罗红霉素的时候,峰拖尾很严重.大家有什么方法解决啊
新法罗红霉素有谁做过?柱子温度15度,进样器温度8度这个温度是怎么控制的,有人做过吗
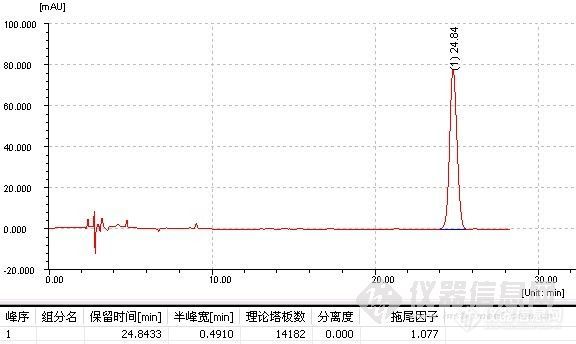
罗红霉素的分析向来让各位做这个品种的色友大伤脑筋,主要是峰形极差,而加三乙胺来改善峰形也是不太好使,因为三乙胺在这个波长有强吸收,加进去后本底上升,峰高很低,甚至看不到峰。经过我们的一番努力,终于让它变老实了,得到了非常漂亮的对称峰形,贴出来跟大家一起分享呵呵。。。罗红霉素药典方法色谱柱:Ultimate XB-C18, 5um, 4.6×250mm 检测波长:210 nm 流动相:67mM磷酸二氢铵(用三乙胺调节pH值至6.5):乙腈=65:35 温度:室温 21度 流速: 1.0 ml/min 进样量:20 ulhttp://ng1.17img.cn/bbsfiles/images/2009/11/200911101512_183486_1896702_3.jpg开发的新方法色谱柱:Ultimate® XB-C18, 5um, 4.6×250mm检测波长:210 nm 流动相:甲醇:乙腈:10mM硫酸四丁氢铵溶液=11:26:63(三者混合好后用NaOH溶液调节pH至4.90)10mM硫酸四丁氢铵溶液的配制:准确称取硫酸四丁氢铵3.395g溶于1000ml水中,搅拌均匀,使之溶解 温 度:室温21℃流 速:1.0ml/min;进样量:20ulhttp://ng1.17img.cn/bbsfiles/images/2009/11/200911101513_183487_1896702_3.jpg
问题: 请问哪位做20762大环内酯类,用内标法,罗红霉素的定量离子对是?
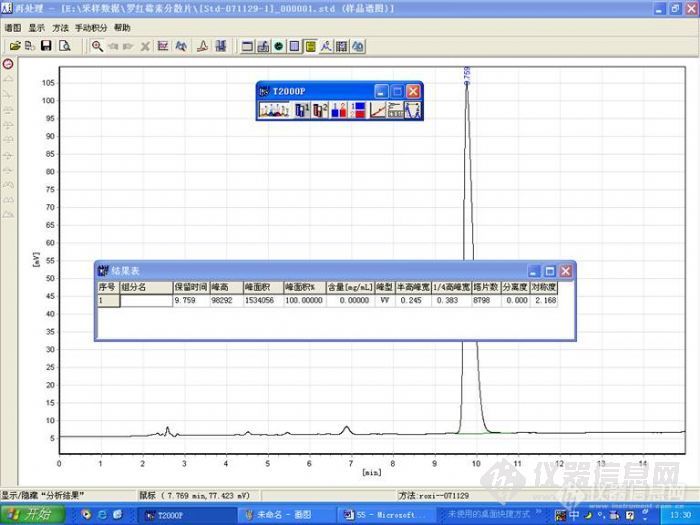
罗红霉素分散片含量的测定一.样品分子结构分子式:C41H76N2O15分子量:837.05CAS号:80214-83-1罗红霉素分散片测定主成分的结构http://ng1.17img.cn/bbsfiles/images/2009/11/200911202247_185655_1621890_3.gif二. 样品来源记录样品商品名 样品测定描述(主成分含量测定):生产厂家:海南xxx医药生物技术有限公司,批号:080502,规格:150mg三. 液相方法条件液相色谱条件:色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;以0.067mol/L磷酸二氢铵溶液(用三乙胺调节pH值至6.5)-乙腈(65﹕35)为流动相;检测波长为210nm;罗红霉素的保留时间不少于9分钟,其与前相邻杂质峰的分离度不得小于1.0,与后相邻杂质峰的分离度不得小于2.0;理论板数按罗红霉素峰计算不低于2500。测定法 取本品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含1mg的溶液,精密量取20µl注入色谱仪,记录色谱图;另取罗红霉素对照品,同法测定。按外标法以峰面积计算供试品中C41H76N2O15的含量。谱图:使用UltimateTM XB-C18, 5um, 4.6×200mm柱子得到的色谱图详见图一http://ng1.17img.cn/bbsfiles/images/2009/11/200911202249_185656_1621890_3.jpg
[color=#444444]最近 我在做猪肉中红霉素、林可霉素、替米考星遇到点问题,想请教同仁一些关键控制点,首先我用的标准是GB 20762 内标用的罗红霉素,发现不过柱内标跑步出来,林可霉素外标法回收率能做到60%多,请教同仁谢谢![/color]
[color=#444444]最近 我在做猪肉中红霉素、林可霉素、替米考星遇到点问题,想请教同仁一些关键控制点,首先我用的标准是GB 20762 内标用的罗红霉素,发现不过柱内标跑步出来,林可霉素外标法回收率能做到60%多,请教同仁谢谢![/color]
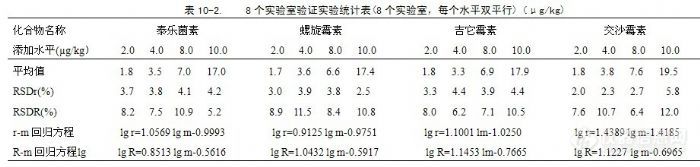
0.9940。河豚鱼中的8种抗生素和鳗鱼中林可霉素、红霉素、泰乐菌素、吉它霉素方法检出限(LOD)为2.0 μg/kg;鳗鱼中螺旋霉素、竹桃霉素、交沙霉素、替米考星方法检出限(LOD)为5.0µg/kg。回收率在75.4%~124.0%之间。八种大环内酯类抗生素重复性相对标准偏差(RSDr)在1.34%~5.79%之间,再现性相对标准偏差(RSDR)在6.20%~15.27%之间。可以用于河豚鱼和鳗鱼中8种大环内酯类抗生素残留检测的高效液相色谱-串联质谱方法的定性和定量。河豚鱼和鳗鱼在中国有着悠久的食用历史,营养丰富。由于目前中国的河豚鱼和鳗鱼主要是养殖的,在养殖过程中不可避免使用抗生素用于保护鱼体正常生长。养殖用药主要是林可霉素、竹桃霉素、红霉素、替米考星和泰乐菌素等,该类抗生素通过羟基以苷键与去氧氨基糖或二甲氨基糖缩合成碱性苷,作用于细胞核糖体50 S亚单位,阻碍细菌蛋白质合成,有较强的抗菌活性。曾广泛应用于食用动物作为预防和治疗用药,而通过食用途径进入人体,导致中毒,甚至死亡。世界各国对抗生素药物残留均有严格的限量要求,欧盟已限制在供食用动物中的饲料中使用,中国也有相应的要求。近年来,日本、韩国针对河豚鱼以药物残留为借口相继对中国河豚鱼实行贸易技术壁垒,限制和排斥中国河豚鱼出口。因此,为破解该类壁垒、促进出口,一种高灵敏度的测定河豚鱼和鳗鱼中大环内酯类抗生素的多残留方法是十分必要的。林可霉素等抗生素的吸收光谱多在紫外末端区,缺乏可用的特征紫外吸收区位。已见报道的文献中,主要分析方法有微生物法、荧光光度法、紫外分光光度法、气相色谱、薄层谱法、高效液相色谱法、毛细管电泳法(CE)和液质联用技术LC-MSn法法。在近期的文献报道中,测定大环内酯类残留,样品前处理大多采用缓冲溶液提取合固相萃取技术分析技术,采用液相色谱-串联质谱方法检测。这种技术灵敏度高、选择性和特异性好,能够对低浓度的样品进行很好的定性确认,已经成为食品和环境中污染物定性、定量分析的重要手段。文献报道的测定大环内酯类分析方法多应用于食品和动物产品,未见到同时适用于河豚鱼、鳗鱼的相关检测研究。在参考以上文献的基础上,建立用Tris缓冲溶液提取河豚鱼和鳗鱼中8种大环内酯类抗生素残留,Oasis HLB固相萃取柱萃取、净化,罗红霉素为内标,LC-MS-MS检测河豚鱼和鳗鱼中8种大环内酯类抗生素的新方法。该方法经过4年的推广使用,提取操作简单、回收率稳定、灵敏度高、选择性好,未发现不良反应,林可霉素、红霉素、泰乐菌素、吉它霉素检出限达到2.0µg/kg,鳗鱼中的螺旋霉素、竹桃霉素、交沙霉素、替米考星检出限达到5.0µg/kg,低于国际上该类药物残留限量的检测要求。1 实验过程1.1 主要试剂水,符合GB/T 6682,一级。甲醇、乙腈,色谱纯。甲醇溶液(2+3)。定容液:0.01 mol/L乙酸铵溶液+乙腈(17+3)。tris溶液:依次溶解12.0 g三羟甲基氨基甲烷(tris)和7.35 g氯化钙(CaCl2·2H2O)于1000 mL水中,用盐酸调节pH值为9。标准物质:林可霉素(CAS 7179-49-9)、竹桃霉素(CAS 7060-74-4)、红霉素(CAS 59319-72-1)、替米考星(CAS 108050-54-0)、泰乐菌素(CAS 74610-55-2)、螺旋霉素(CAS 8025-81-8)、吉它霉素(CAS 1392-21-8)、交沙霉素(CAS 16846-24-5)和内标物质罗红霉素(CAS 80214-83-1),纯度≥95%。2.0 μg/mL标准工作溶液:依次准确称取每种标准物质适量,用甲醇溶解至浓度为1.0 mg/mL的标准储备溶液;将标准储备溶液用甲醇逐步稀释为2.0 μg/mL的标准工作溶液。1.0 μg/mL内标标准溶液:准确称取罗红霉素适量,用甲醇溶解为浓度1.0 mg/mL的内标储备溶液;将内标储备溶液用甲醇逐步稀释为1.0 μg/mL内标标准溶液。测定河豚鱼用基质标准混合工作溶液系列:分别吸取1.0 μL、2.0 μL、5.0 μL、25.0 μL浓度为2.0 μg/mL的标准工作溶液,依次加入到相应的试剂瓶中,再分别加入20.0 μL内标工作溶液,用河豚鱼样品空白提取液定容至1.0 mL。配成内标物浓度均为20 ng/mL,林可霉素、竹桃霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、吉它霉素和交沙霉素分别为2.0 ng/mL、4.0 ng/mL、10.0 ng/mL、50.0 ng/mL的四个浓度水平的测定河豚鱼用基质标准混合工作溶液系列。测定鳗鱼用基质标准混合工作溶液:分别吸取浓度为2.0 μg/mL的林可霉素、红霉素、泰乐菌素、吉它霉素标准工作溶液各1.0 μL、2.0 μL、5.0 μL、25.0 μL和螺旋霉素、竹桃霉素、交沙霉素、替米考星标准工作溶液各2.5 μL、5.0 μL、10.0 μL、25.0 μL,依次加入相应的试剂瓶中,再分别加
[size=4] 请教各位抗生素发酵过程检测的高手,由于我公司现在在转产,即将上马红霉素。但是由于各方面的原因在红霉素发酵与提炼过程中红霉素效价检测的方法过于繁琐,不太适合批量检测。现在的检测方法大致是根据效价的高低,稀释倍数也就不相同,加入碳酸钾的量也不同,但是发酵液与碳酸钾的总量20ml,再加入乙酸丁酯20ml,摇匀,静置,分层后取上层液10ml,再加入HCL溶液10ml,摇匀,静置,分层后取下层溶液5ml,再加入5ml硫酸。摇匀后放入水浴锅中30min。最后,冷却至室温,利用分光光度计检测吸光度。得出的吸光度带入线性公式计算,再乘以稀释倍数就得到效价。我们也尝试了利用高效液相检测红霉素发酵液的效价,但是杂质峰比较难分开,而且理论值与测定的值相差比较大。[/size] 化学方法很是繁琐,不知道各位高手中有没有做过红霉素的,请教一下各位有没有其他快速的检测方法,能够提供高效液相的方法最好。在此本人深表谢意!
[size=4]请教各位抗生素发酵过程检测的高手,由于我公司现在在转产,即将上马红霉素。但是由于各方面的原因在红霉素发酵与提炼过程中红霉素效价检测的方法过于繁琐,不太适合批量检测。现在的检测方法大致是根据效价的高低,稀释倍数也就不相同,加入碳酸钾的量也不同,但是发酵液与碳酸钾的总量20ml,再加入乙酸丁酯20ml,摇匀,静置,分层后取上层液10ml,再加入HCL溶液10ml,摇匀,静置,分层后取下层溶液5ml,再加入5ml硫酸。摇匀后放入水浴锅中30min。最后,冷却至室温,利用分光光度计检测吸光度。得出的吸光度带入线性公式计算,再乘以稀释倍数就得到效价。我们也尝试了利用高效液相检测红霉素发酵液的效价,但是杂质峰比较难分开,而且理论值与测定的值相差比较大。[/size] 化学方法很是繁琐,不知道各位高手中有没有做过红霉素的,请教一下各位有没有其他快速的检测方法,能够提供高效液相的方法最好。在此本人深表谢意!
有没有专门检测红霉素的设备。
大家好,求助红霉素的液相色谱检测方法,急用,谢谢![em61]
求救诸位大神,请问有人用液质做过林可霉素吗?我现在跟GB/T 20762-2006做,用罗红霉素作为内标,但是回收率一直只有40%左右,也不知道是哪里出了问题,请教大家怎样才能把回收率提上去,谢谢~
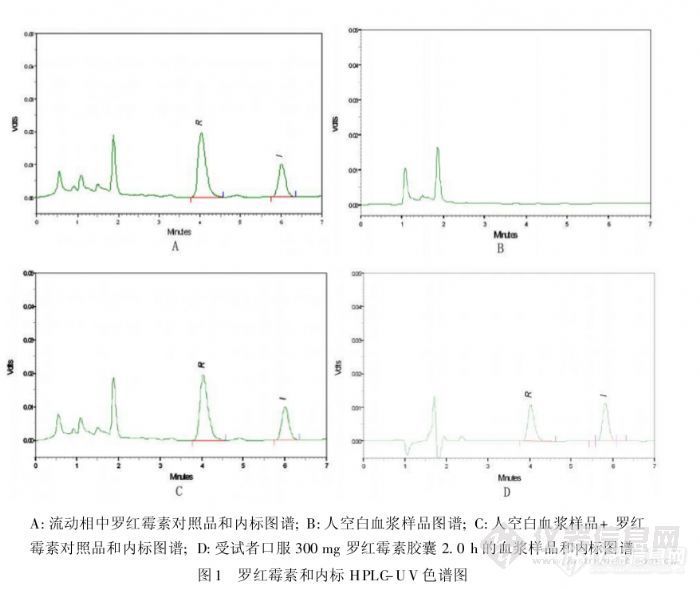
147.1 HPLC-UV法用于人血浆中罗红霉素的浓度测定及药代动力学和生物等效性研究 【作者】 张娟 张红 隋双明 刘建明 王萍 熊玉卿【Author】 ZHANG Juan,ZHANG Hong,SUI Shuang-ming,LIU Jian-ming,WANG Ping,XIONG Yu-qing(Institute of Clinical Pharmacology,Medical College of Nanchang University,Nanchang 330006,China)【机构】 南昌大学医学院临床药理研究所【摘要】 目的建立HPLC-UV法测定人血浆中罗红霉素的方法,并探讨罗红霉素的药代动力学和生物等效性。方法采用Diamonsil C18柱(150 mm×4.6 mm,5μm),流动相为乙腈∶0.01 mol磷酸二氢铵=39∶61(v/v),流速1 mL/min;以卡马西平为内标,检测波长为210 nm。血浆样品用正己烷(含5%的异丙醇)液-液萃取后经C18分离。结果罗红霉素在0.25~16.0 mg/L线性关系良好,r=0.999,最低检测限为0.25 mg/L。萃取回收率70%,方法回收率99.8%~110.5%,批内、批间精密度均15%。结论HPLC-UV方法结果准确、灵敏度高,适用于罗红霉素药代动力学和生物等效性研究。 http://ng1.17img.cn/bbsfiles/images/2012/11/201211042246_401316_2379123_3.jpg
中科院上海有机化学研究所刘文领衔的课题组立足于国内生物产业的现实需求,结合该所在化学合成方面的优势,致力于化学的理念促进现代生物技术的合理运用。他们与华东理工大学教授张嗣良等合作,在国家“863”项目“红霉素发酵工业用菌种改造和过程优化控制技术”中取得了重要突破,获得了一批具有自主知识产权、质量和产量得以明显提升的新型红霉素生产重组菌株。目前该成果已在湖北东阳光生化制药有限公司成功地进行了放大和试生产,其潜在经济、社会效益显著。在人类与致病微生物的斗争历史上,以抗生素为代表的微生物药物起到了至关重要的作用。红霉素是一类广泛使用、用于治疗革兰氏阳性菌感染的广谱大环内酯类抗生素。其临床应用领域的扩大和以阿奇霉素、罗红霉素、克拉霉素等为代表的新型半合成红霉素的出现,快速拉动了红霉素原料药的生产需求。过去几年,国际抗生素的市场规模大约在350亿~380亿美元之间,2012年有望达到450亿美元。据西方经济学家预测,2010年红霉素系列产品的全球市场总规模达70亿美元以上,市场前景乐观。抗生素发酵生产本身是高耗能产业,存在环境污染等问题,发达国家近年来正逐步把抗生素原料药的生产转移到中国等发展中国家。目前,我国是世界上红霉素生产和出口的第一大国,年产量超过7000吨。刘文介绍,由于许多抗生素具有十分复杂的化学结构,采用化学方法大量合成往往需要繁杂的工艺途径和苛刻的反应条件,在制药工业上的实际应用价值相当有限。采用微生物发酵是获取药用抗生素原料的主要途径,而我国作为世界上原料抗生素的主要生产大国,发酵单位偏低、产品质量偏低、缺乏自主知识产权的新型抗生素药物等一系列原因却严重制约了这一产业的发展。自红霉素作为一种广谱抗生素药物进入临床以来,以提高其产生菌种发酵单位为目的的遗传育种工作一直未曾停止。由于对微生物次级代谢产物生物合成的机制了解不多,常规诱变选育的方法存在周期长、效率低和随机性大的缺点,近年来在红霉素高产菌株的筛选方面收效不大。随着分子生物学技术的发展,国际上在红霉素产生菌种的基因工程改造方面进行了诸多尝试;然而,这些研究主要集中在与红霉素产生相关的底物供应或限制因素的改进方面,并未就红霉素生物合成的次生代谢途径做特异性的遗传修饰,因此,在解决红霉素生产中经常面临的有效组分偏低等问题时,缺乏有效的针对性。作为中科院“百人计划”、国家杰出青年基金获得者,自2007年以来,刘文带领课题组以包括红霉素、阿维菌素、林可霉素、泰乐菌素和螺旋霉素等大宗抗生素产品为对象,就我国抗生素原料药产业普遍存在的问题进行了分析,提出了以组分优化为切入点、采用遗传操作来控制体内合成的化学反应,从而改善产品质量和产量的研究思路。基于红霉素各组分结构的差异和相互转化的化学本质,他们运用组合生物合成技术的方法和原理对红霉素工业用高产菌株进行了针对性的遗传改良。通过发酵过程中后修饰酶的表达比例调整,他们将无效副产物组分B和C几乎完全转化为有效组分红霉素A,从而在提高了产品质量(基本消除主要的副产物)的同时,有效地提高了产品的产量达25%左右。部分研究成果发表在国际著名学术刊物《应用和环境微生物》上,引起国内外同行的关注。有关重组菌株在华东理工大学的协助下完成了中试,已在湖北宜都东阳光生化制药有限公司进行了放大和试生产,具备了工业化生产的价值。据厂方估计,相关生产技术若能得以推广使用,每年所产生的经济效益将达10亿元以上。这一重要成果还获得了上海市科技进步奖一等奖,并申请国家专利4项。有关专家认为,其在红霉素发酵工业方面的应用,将明显改善产品质量、简化下游纯化工艺;同时,缓解企业在环境污染方面所面临的压力。“抗生素在微生物体内的合成其本质是化学问题,化学过程和机制的解析可以使生物学技术的运用找到合适的目标并发挥更大作用。”刘文表示,“以上是我们构建的第一代红霉素生产重组菌株,主要侧重于品质(组分优化)的提升。目前我们侧重于产量提高的第二代重组菌株已完成中试,结合前两代优势、综合提高质量和产量的第三代重组菌株完成了小试,初步数据表明效果明显。”作为上海有机所开展红霉素菌种遗传改造工作的最初建议者,中国科学院院士戴立信高度关注面向国家重大需求的科学研究。“以汪猷先生为代表的有机所老一辈科学家早在上世纪50年代就开展了抗生素的研究工作,并在实际生产中得到应用,解决了当时有和无的问题。我国现在已经成为红霉素第一生产大国,对于技术创新的需求尤为迫切。”他思路非常清晰,“我听了刘文教授关于生物合成的学术报告后,又了解了一些红霉素生产企业的现状和需求,感觉在生物技术中融入化学的理念,应该有可能解决一些生产中的瓶颈问题并产生不错的效果。”“这是有机所在知识创新过程中,在面向国家需求、立足原始创新方面所做的一件有重要意义的研究工作,充分体现了学科交叉的优势。”中科院上海有机所所长丁奎岭表示,“我们以化学的思想促进生物技术的应用,以提高大宗医药抗生素产品的产量和质量为研究目标,所要解决的关键问题在抗生素生产中具有普遍意义。红霉素工业用生产菌种的遗传改造取得的系列创新技术在生产中成功实施,预示着这样的理念在其他抗生素发酵生产中将有着普遍的推广意义,有利于促进我国传统抗生素生产行业整体技术水平的提升。”

167.1 HPLC-MS测定人血浆中罗红霉素的浓度姜俊1,ZHEN w2,潘杰3,徐艳1,施爱明3(1苏州留学人员创业园,江苏省苏州新药创制中心,江苏苏州21 5011;2.Nu probeInc,FosterCity,CA,US;3.苏州大学附属第二医院,江苏苏州21 5004)【摘要】目的:建立人血浆中罗红霉素的高压液相城谱(HPLC,MS)5m4定方法。方法:采用Diamonsil—c 18柱(200mmX 4 6mm,5um),流动相为甲醇(10mmol/L)醋酸铵缓冲液(PH=3 5)80:20,流速为1 0 ml/min。用含内标(克拉霉素)的乙腈液沉淀蛋白,离心后取上清液进样,以质谱为检测手段,按内标击定量。结果:本法在0 05~10.0 ug/mL范围内线性关系良好,批内RSD
[color=#ba4b01][size=3]维权声明:本文为[size=2]11093661[/size]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/size][/color]在红霉素发酵过程中,对红霉素发酵液效价的检测,能够起到对红霉素发酵过程起到一定的监督作用,对发酵过程提供参考价值,对生产异常起到眼睛的作用。而传统化学检测法对红霉素的检测不仅程序繁琐,周期长,而且容易受操作者水平,熟练程度等各方面的限制,导致结果误差较大,不利于对生产的监控。红霉素发酵过程中有红霉素A,红霉素B,红霉素C等产生,其中红霉素A成分活性最大,而其它成分活性小,而且有一定副作用,而传统化学吸光度方法的检测并不能准确检测红霉素A的成分,而是有可能是检测出的含有红霉素所有的物质。这样就不能更好的对发酵生产中起到更为准确的数据依据。 红霉素发酵过程中如果应用液相色谱分析,能够准确分离出红霉素A,红霉素B,红霉素C等物质,对红霉素A的效价检测更加准确。但红霉素发酵液中各类物质复杂,如果用蒸馏水定容,再色谱分析,结果发现基线漂移比较厉害,这样就限制了红霉素发酵生产中高效液相色谱仪的应用。本人通过多方查找资料,多次做试验发现,如果在定容过程中能够对发酵液中的各类复杂物质能够分离出来的话,有利于解决色谱分析中基线漂移问题。发酵液中的各类复杂物质容易溶于水,而难溶于有机相中,而红霉素则相反。利于这个原理,在分析定容中如果用有机相定容,各类复杂物质被分离出来,而红霉素溶于有机相中,在将物质摇匀后离心分离,使分离效果更好,基线漂移的问题能够得到相当程度的解决。 这个方法纯属个人自己试验中,查阅资料中摸索得到的,过程中没有依靠任何已有的分析方法,当然传统的吸光度法除外。而本人所在单位因为即将改产才有这个机会做的实验。所以可能有错误之处,或与某些方法雷同。我个人纯属将我自己的经验方法提出与朋友分享,希望广大朋友不吝赐教。 本人所在城市为四川成都。有空多联系。
方法:HPLC基质:药品应用编号:103727化合物:红霉素、依托红霉素固定相:Spursil C18色谱柱/前处理小柱:Spursil C18 5u 250 x 4.6mm样品前处理:供试品:依托红霉素样品,5mg/mL,溶剂为乙腈。对照品:红霉素,0.15mg/mL,溶剂为乙腈。 分离度溶液:样品和红霉素浓度均为0.5mg/mL,溶剂为流动相。色谱条件:2015药典方法: 色谱柱: Spursil C18 250*4.6 mm,5 μm(Cat#:82006) 流动相: 磷酸二氢钾溶液(磷酸二氢钾3.4g+三乙胺2.75mL+水稀释至1000mL):乙腈=65:35,用稀盐酸调节pH=3.0 流速: 1.0 mL/min 柱温: 30℃ 检测器: 195 nm 进样量: 20.0 uL 调整后方法: 色谱柱: Spursil C18 250*4.6 mm,5 μm(Cat#:82006) 流动相: 磷酸二氢钾溶液(磷酸二氢钾3.4g+三乙胺2.75mL+水稀释至1000mL),取650mL用乙腈定容到1000mL ,再用稀盐酸调节pH=3.0 流速: 1.0 mL/min 柱温: 30℃ 检测器: 195 nm 进样量: 20.0 uL文章出处:天津应用实验室关键字:依托红霉素、Spursil C18、2015药典、红霉素、依托红霉素、HPLC摘要:Spursil C18检测依托红霉素。谱图:2015药典结果http://www.dikma.com.cn/u/image/2016/01/13/1452666540639280.pnghttp://www.dikma.com.cn/u/image/2016/01/13/1452666544570343.pnghttp://www.dikma.com.cn/u/image/2016/01/13/1452666612135089.png调整方法后结果http://www.dikma.com.cn/u/image/2016/01/13/1452666663710368.pnghttp://www.dikma.com.cn/u/image/2016/01/13/1452666616666777.pnghttp://www.dikma.com.cn/u/image/2016/01/13/1452666630275876.png
检测有机磷,氨基甲酸酯类、磺胺类、呋喃类,氯霉素类、红霉素、青霉素等,用什么色谱柱?
[b]Q:[b][b][b][/b][/b]依托红霉素的检测,所使用的色谱柱货号是?[/b]A:82020===============================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:mengzhaocheng(注册ID:mengzhaocheng)zengzhengce163(注册ID:zengzhengce163)yy_0324(注册ID:yy_0324)初心(注册ID:m3170710)sdlzkw007(注册ID:sdlzkw007)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/10/201810291508033807_5993_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/10/201810291508056917_3421_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:103728化合物:红霉素、依托红霉素色谱柱:[url=http://www.dikma.com.cn/product/details-978.html]Spursil C18 3μm 250 x 4.6mm[/url]样品前处理:供试品:依托红霉素样品,5mg/mL,溶剂为乙腈。对照品:红霉素,0.15mg/mL,溶剂为乙腈。分离度溶液:样品和红霉素浓度均为0.5mg/mL,溶剂为流动相。色谱条件:色谱柱: Spursil C18 250*4.6 mm,3μm(Cat#:82020)流动相: 磷酸二氢钾溶液(磷酸二氢钾3.4g+三乙胺2.75mL+水稀释至1000mL),取650mL用乙腈定容到1000mL ,再用稀盐酸调节pH=3.0流速: 1.0 mL/min柱温: 30℃检测器: 195 nm进样量: 20.0 uL文章出处:天津应用实验室关键字:依托红霉素、Spursil C18、2015药典、红霉素、依托红霉素、HPLC摘要:Spursil C18检测依托红霉素。图谱:[img]http://www.dikma.com.cn/u/image/2016/01/13/1452667176367405.png[/img][img]http://www.dikma.com.cn/u/image/2016/01/13/1452667180115015.png[/img][img]http://www.dikma.com.cn/u/image/2016/01/13/1452667183133458.png[/img]

按照10版药典检测依托红霉素原料项下的游离红霉素,有些情况需要请教一下检测过这个品种的专家们供试品和标准品用乙腈溶解系统适应性用流动相溶解系统适应性是不错的,但是主峰就不行了,谱图就没有重现性,完全按照药典来检测的系统适应性http://ng1.17img.cn/bbsfiles/images/2010/11/201011241337_261743_1606820_3.jpg第一针供试品http://ng1.17img.cn/bbsfiles/images/2010/11/201011241337_261744_1606820_3.jpg第二针供试品http://ng1.17img.cn/bbsfiles/images/2010/11/201011241338_261745_1606820_3.jpg有没有谁做过,大家给我指点一下吧

[b][center]【第二届网络原创作品赛】药检之路:分散片检测解析过程[/center][/b][center][img]http://ng1.17img.cn/bbsfiles/images/2017/01/201701191651_625775_1612824_3.gif[/img][/center][center][img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240012_167324_1612824_3.jpg[/img][/center][b][color=#00008b][size=4]药检的同行们,你们平时都做哪些药物的检测?在检测中是否遇到过很棘手的问题呢?解析我们的检验,谈谈我们的看法,你今天的检测还都顺利吗?以下是我在工作中对片剂检测,还请大家多提宝贵意见,其中的错误与不足望老师专家斧正。[/size][/color][/b][color=#00008b][b]==================================================================================================================[/b][/color][color=#dc143c][size=3]罗红霉素分散片的检测[/size][/color][b]什么是分散片[/b]:系指在水中能迅速崩解并均匀分散的片剂。 分散片中的药物应是难溶性的。分散片可加水分散后口服,也可将分散片含于口中吮服或吞服。 分散片 应进行溶出度和分散均匀性检查。产品检测引用标准:《中华人民共和国药典》现行版技术标准:[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240032_167326_1612824_3.jpg[/img]规格:75mg (每片含罗红霉素约75mg)有效期24个月(见包装封口)[b][color=#dc143c]********************************************************************************************************************[/color][/b][size=4][b][color=#dc143c]检验方法[/color][/b][/size][b]1.性状[/b]本品为白色或类白色[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240038_167327_1612824_3.jpg[/img][color=#00008b]一般是目测,如发现变黄或缺损则判为不合格,同时假冒药片光泽性不好,易碎。[/color][b]2.鉴别[/b]在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液的主峰的保留之间一致.[color=#00008b]可参照含量测定时色谱图(略)[/color][b]检查3.溶出度[/b][img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240046_167328_1612824_3.jpg[/img][color=#00008b]调试仪器到达试验要求,包括一些参数设定。[/color]测试前,调整装置,使转篮底部距溶出杯底部25mm±2mm.量取经脱气处理的盐酸溶液(1-1000)900ml为溶出介质,注入6个溶出杯中,加温使盐酸溶液温度保持在37±0.5度,转速为每分钟100转,并使其稳定.取本品6片,分别投入6个干燥的转篮内,将转篮降入容器中,立即开始计时,经30分钟时,取溶液适量,(取样点位置在转篮顶端至液面的中点,距溶出杯10mm处),立即经不大于0.8um的微孔滤膜过滤,自取样至过滤应在30秒完成,取续滤液作为供试溶液.另取本品10片,研细,精密秤取适量(相当于平均片重)加乙醇适量,(每5mg罗红霉素加乙醇1ml)使罗红霉素溶解,用溶出介质稀释100ml 过滤,取续滤液10ml加溶出介质80ml,制成每1ml约含80ug 罗红霉素溶液,作为对照.精密量取上述溶液各5ml,分别精密加入硫酸溶液(75-100)5ml,放置30分钟,冷却至室温,照”紫外分光光度计标准操作规程”在482nm的波长处分别测定吸光度,计算出每片的溶出度.应符合规定[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240048_167329_1612824_3.jpg[/img][color=#00008b]注意取样时,取样的随机性,不能只在一盒药中取。[/color]计算含量A样:样品吸光度 A对:对照吸光度C对:对照溶液的浓度 g/mlW: 秤取的 供试品的量 gWo:为平均片重 g[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240053_167330_1612824_3.jpg[/img][color=#00008b]注意取样时要迅速,并做好过滤处理,最好2人同时进行。在进行样品前处理时应避免样品二次污染。[/color][b]结果判定[/b]符合下列条件之一者,可判为符合规定(1)6片中,每片的溶出量,按标示量计算,均不低于82%,(2)6片中,如有1-2片低于82%,但不低于72%,且平均溶出量不低于82%(3)6片中,有1-2片低于82%,其中尽有一片低于72%,但不低于62%,且平均溶出量不低于82%时,应另取6片复试 初复试的12片中有1-3片低于82%,其中仅有1片低于72%,但不低于62%,且平均不低于82%.[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908240058_167331_1612824_3.jpg[/img][color=#00008b]紫外检测,认真填写检验记录,同时注意仪器使用和维护并做好记录。[/color]
[align=center][size=21px]大环内酯类抗生素[/size][size=21px]检测国内标准比较解读[/size][/align][size=18px]大环内酯类抗生素[/size][size=18px]是一类分子结构中具有碳[/size][size=18px]大[/size][size=18px]环内酯的抗菌药物的总称[/size][size=18px],主要由链霉菌培养液中提取获得[/size][size=18px]。[/size][size=18px]主要包括[/size][size=18px]:红霉素、竹桃霉素、克拉霉素、罗红霉素、地红霉素[/size][size=18px]([/size][size=18px]1[/size][size=18px]4[/size][size=18px]元[/size][size=18px]环[/size][size=18px])[/size][size=18px];阿奇霉素[/size][size=18px](1[/size][size=18px]5[/size][size=18px]元环)[/size][size=18px];[/size][size=18px]麦迪霉素、吉他霉素[/size][size=18px]、交沙霉素、螺旋霉素[/size][size=18px]、[/size][size=18px]罗他霉素[/size][size=18px](1[/size][size=18px]6[/size][size=18px]元环)[/size][size=18px]等。[/size][size=18px]《[/size][size=18px]GB 31650-2019[/size][size=18px] [/size][size=18px]食品中兽药残留最大限量[/size][size=18px]》规定了部分大环内酯类抗生素在动物源食品中残留限量:红霉素(40~200 [/size][size=18px]ug[/size][size=18px]/kg),[/size][size=18px]吉他霉素(200 [/size][size=18px]ug[/size][size=18px]/kg)[/size][size=18px],[/size][size=18px]螺旋霉素([/size][size=18px]20[/size][size=18px]0~[/size][size=18px]8[/size][size=18px]00 [/size][size=18px]ug[/size][size=18px]/kg)[/size][size=18px]等,还有很多该类药物没有规定残留限量,存在一定风险隐患,需要进一步补充完善。[/size][size=18px]目前,国内[/size][size=18px]大环内酯类抗生素[/size][size=18px]相关检测方法标准主要包括[/size][size=18px]:[/size][table][tr][td]序号[/td][td]标准名称[/td][td]检测原理[/td][td]药物数量、种类[/td][/tr][tr][td]1[/td][td]GB/T 20762-2006 畜禽肉中林可霉素、竹桃霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉它霉素、交沙霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用乙腈提取,正己烷除脂浓缩后用磷酸盐溶液溶解,HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]9 种:林可霉素、竹桃霉素、红霉素、替米考星、泰乐菌素、克林霉素、螺旋霉素、吉它霉素、交沙霉素[/td][/tr][tr][td]2[/td][td]SN/T 1777.2-2007 动物源性食品中大环内酯类抗生素残留测定方法 第2部分:高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱法[/td][td]试样用乙腈提取,正己烷脱脂,C18固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]7 种:螺旋霉素、替米考星、竹桃霉素、泰乐菌素、红霉素、罗红霉素、交沙霉素[/td][/tr][tr][td]3[/td][td]SN/T 2062-2008 进出口蜂王浆中大环内酯类抗生素残留量的检测方法 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱法[/td][td]试样用甲醇沉淀蛋白,在磷酸盐缓冲盐溶液介质中,用聚苯乙烯吡咯烷酮填料固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]7 种:螺旋霉素、替米考星、竹桃霉素、泰乐菌素、红霉素、罗红霉素、交沙霉素[/td][/tr][tr][td]4[/td][td]GB/T 22964-2008 河豚鱼、鳗鱼中林可霉素、竹桃霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、吉他霉素、交沙霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用三羟甲基氨基甲烷(Tris)缓冲溶液提取,用HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,内标法定量。[/td][td]8 种:林可霉素、竹桃霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、吉他霉素、交沙霉素[/td][/tr][tr][td]5[/td][td]GB/T 22941-2008 蜂蜜中林可霉素、红霉素、螺旋霉素、替米考星、泰乐霉素、交沙霉素、吉他霉素、竹桃霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用三羟甲基氨基甲烷(Tris)缓冲溶液提取,用HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,内标法定量。[/td][td]8 种:林可霉素、红霉素、螺旋霉素、替米考星、泰乐霉素、交沙霉素、吉他霉素、竹桃霉素[/td][/tr][tr][td]6[/td][td]GB/T 22988-2008 牛奶和奶粉中螺旋霉素、吡利霉素、竹桃霉素、替米卡星、红霉素、泰乐菌素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用乙腈提取, HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]6 种:螺旋霉素、吡利霉素、竹桃霉素、替米卡星、红霉素、泰乐菌素[/td][/tr][tr][td]7[/td][td]GB/T 22946-2008 蜂王浆和蜂王浆冻干粉中林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用三羟甲基氨基甲烷(Tris)缓冲溶液提取,用HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,内标法定量。[/td][td]8 种:林可霉素、红霉素、替米考星、泰乐菌素、螺旋霉素、克林霉素、吉他霉素、交沙霉素[/td][/tr][tr][td]8[/td][td]GB/T 23408-2009 蜂蜜中大环内酯类药物残留量测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]试样用0.1 mol/L碳酸钠-碳酸氢钠缓冲溶液提取,用C18固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]8 种:罗红霉素、替米考星、泰乐菌素、北里霉素、交沙霉素、竹桃霉素、螺旋霉素-I、红霉素[/td][/tr][tr][td]9[/td][td]SN/T 4747.3-2017 进出口食用动物大环内酯类药物残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]试样用叔丁基甲醚提取,氮吹浓缩后,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定,外标法定量。[/td][td]7 种:红霉素、螺旋霉素、替米考星、泰乐菌素、交沙霉素、吉他霉素、竹桃霉素[/td][/tr][tr][td]10[/td][td]GB 31660.1-2019 食品安全国家标准 水产品中大环内酯类药物残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用乙腈提取,正己烷除脂,中性氧化铝固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]9 种:竹桃霉素、红霉素、克拉霉素、阿奇霉素、吉他霉素、交沙霉素、螺旋霉素、替米考星、泰乐菌素[/td][/tr][/table][size=18px]需要[/size][size=18px]注意的是,[/size][size=18px]虽然[/size][size=18px]大环内酯类药物一般呈弱碱性[/size][size=18px]易溶于酸性/极性溶剂,[/size][size=18px]使用乙腈或甲醇[/size][size=18px]从[/size][size=18px]动物组织中提取大环内酯类药物时,如果[/size][size=18px]目标组分中有红霉素,则需要保证提取溶液体系中不能含有甲酸,因为红霉素对酸很[/size][size=18px]敏感会[/size][size=18px]导致回收率偏低;提取溶液过C[/size][font='等线'][sub][size=18px]18[/size][/sub][/font][size=18px] SPE小柱后能显著减小基质效应。[/size]
在抗生素类的标准物质使用时,经常会遇到标准品和对照品的概念。关于这二者的区别,现在比较流行的说法是在做HPLC时使用的标准物质应为对照品。摘录典型观点如下:[B]“标准品都是按效价单位(或μg)计,以国际标准品进行标定。标准品的标示量是按生物活性来计算的,不是按纯度来标示,此种标示法对单组分或多组分物质均适用,尤适用于多组分物质,如乙酰螺旋霉素标准品,是由4种有效成分组成,若欲于一个纯度来标示其含量是不可能的,但用效价(即生物活性)来标示是可行的;对照品的标示量则必定是某单一组分的纯度指标。所以日常工作中,标准品和对照品在定量时是不可相互替代的。以罗红霉素为例,现今是国家标准品与对照品并存,以抗生素微生物检定法测其含量时,必须使用罗红霉素标准品;但以HPLC法测定其含量时,又必须使用罗红霉素对照品,不可混淆。”[/B]但是我见过一些行业标准,比方说HPLC测土霉素残留中,在说到标准液的配制时,写得就是“土霉素标准品”。难道这里面的“标准品”是“对照品”的错误用法?[em0716] 请大家发表一下看法
如何开发高效的前处理的材料和方法,提高样品前处理水平,已经成为目前食品分析化学的研究热点之一,由于分子印迹聚合物具有功能预定性、选择特异性、适用范围广等特点,基于分子印迹聚合物(Molecularly imprinted polymers, MIPs)的分子印迹固相萃取技术(Molecularly imprinted solid phase extraction, MISPE)已经成为食品安全检测技术发展的新趋势。本论文针对肉用家畜和水产品中应用广泛且危害严重的红霉素和氯丙嗪兽药制备了特异的分子印迹聚合物,对制备的聚合物的结合机理和识别特性进行了深入分析,并最终制备了这两类兽药的分子印迹固相萃取小柱,应用于实际样品中红霉素和氯丙嗪的残留分析。研究获得的主要结果如下:本课题采用本体聚合的分子印迹方法从制备的 6 组红霉素分子印迹聚合物中选取一组特异性较强的聚合物用于后续研究。该组合模板红霉素和单体 MAA(methacrylic acid)的比例为(1:2),交联剂为 EGDMA(ethylene glycol dimethacrylate),采用甲醇/乙腈(2:3, v/v)作为致孔剂,热聚合温度为 60℃。利用扫描电镜观察、孔径分析、热重分析、紫外光谱和红外光谱分析等方法对聚合物的物理特征进行了评价。同时通过对聚合物吸附能力的热力学和动力学特性以及高效液相色谱分析,对聚合物与红霉素之间可能的印迹机理和识别能力进行了研究,证明了制备的聚合物对模板的吸附能力主要来自于低亲和力和高亲和力两类结合位点,并计算出两个结合位点的最大结合量分别为 12.30 mg g1-和 72.09 mg g1-。课题以分子印迹聚合物为固相萃取的填料,制备了红霉素分子印迹固相萃取小柱并对小柱的萃取条件进行了优化。当红霉素分子印迹聚合物固相萃取条件采用的上样缓冲液为 40%甲醇,淋洗液为 2.5 mL80%甲醇,洗脱液为 3mL 的甲醇/PBS (0.5 M) (80:20, v/v)时,固相萃取柱对红霉素的回收率超过 80%,非印迹聚合物固相萃取小柱的回收率则小于 30%。采用优化后的固相萃取的方法,研究了聚合物的选择性,结果显示红霉素分子印迹聚合物对大环内酯类药物具有一定的交叉反应性。说明在印迹反应过程中模板的立体构型对特异性识别的建立起主要作用。试验中将制备的红霉素分子印迹固相萃取小柱用于猪肉样品中红霉素残留的前处理,结果显示经过 MIPs 净化的样品,基质对检测的干扰大大降低,同时极大提高了检测器的灵敏度。在选用的三个加标浓度下,红霉素的回收率都大于 79%。采用红霉素分子印迹固相萃取小柱从水中富集红霉素的实验,同时证明制备的聚合物在自来水中可以高效的富集红霉素。另外,我们制备了氯丙嗪的 MIPs,摸索了不同的合成方法和不同组成成分对产物的选择能力的影响。结果证明,通过本体法制备的聚合物,当使用 MAA 做为单体,模板单体的比例为 1:4,选用 TRIM(Trimethylolpropane trimethacrylate)作为交联剂时,得到的聚合物的选择性最高。试验通过色谱分析试验、红外光谱试验等研究了氯丙嗪与功能单体之间的自组装过程。选择性分析和容量分析的结果表明制备的氯丙嗪分子印迹聚合物相对于非印迹聚合物具有明显的选择性和吸附容量。当使用水溶液作为溶剂时,氯丙嗪分子印迹聚合物的最大特异吸附容量为 10mg mL1-。使用氯丙嗪分子印迹聚合物固相萃取柱对猪尿样品中该药残留的富集和净化相对于商业化的 C18 小柱的效果更明显。