推荐厂家
暂无
暂无

 400-860-5168转3974
400-860-5168转3974
 留言咨询
留言咨询

 400-860-5168转6009
400-860-5168转6009
 留言咨询
留言咨询

 400-860-5168转0822
400-860-5168转0822
 留言咨询
留言咨询



我们的下个实验要用到这个仪器,老师说先看下这个仪器的说明书。网上找很多都是产品的短介,都没有要如何操作。还有的是对声级计做一个原理上的介绍,没有针对性。希望有这个仪器的大大来一份说明书。急求,谢谢!
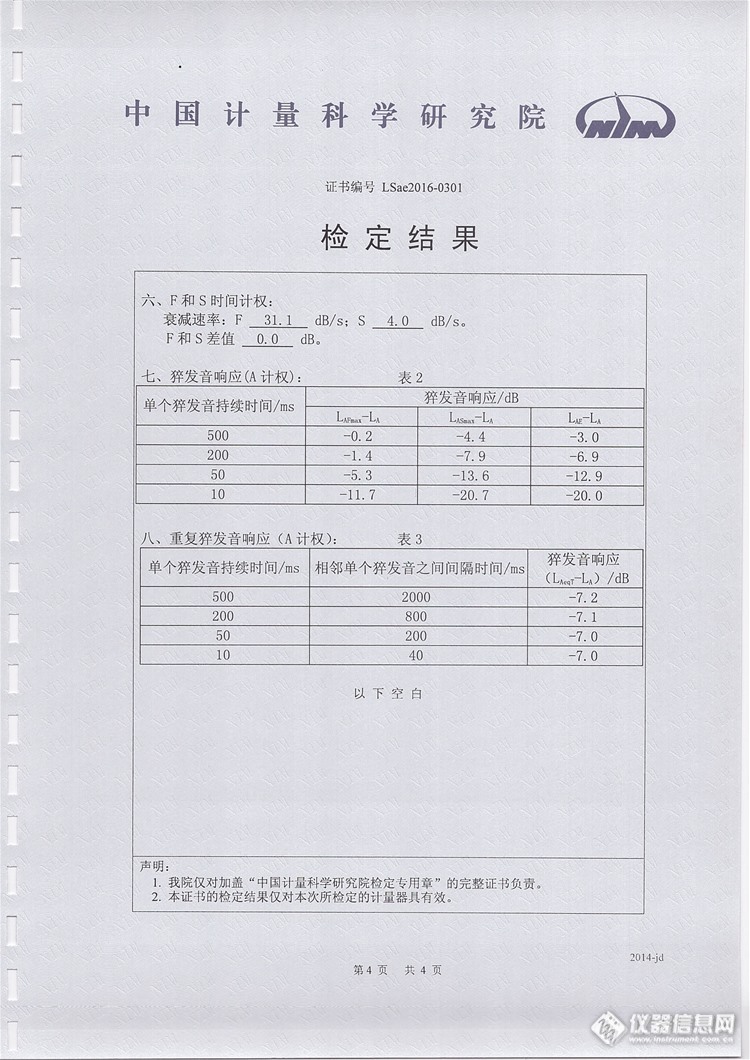
通过AWA5680多功能声级计说明书和检定证书确定其测量范围,请各位版友参与讨论。谢谢!!
声级计校准器的分贝是94.0但是我看说明书说是校准分贝为93.8,现在我想问问大家,声级计校准到底是校准到93.8还是94.0?[em09511]