复方氨基比林注射液说明书(兽用)【兽药名称】通用名:复方氨基比林注射液 英文名:Compound Aminophenzone Injection 汉语拼音:Fufang Anjibilin Zhusheye【主要成分】为氨基比林与巴比妥混合制成的灭菌水溶液。含氨基比林7.15%和巴比妥2.85%。【性 状】本品为无色或淡黄色的澄明液体。【药理作用】本品给药后即时产生镇痛作用,其解热镇痛作用强而持久,氨基比林与巴比妥合用能增强其镇痛作用,有利于缓解疼痛症状。本品还有抗风湿和消炎作用。半衰期为1~4小时。【适 应 症】用于发热性疾患、关节炎、肌肉痛和风湿症等。【用法用量】 肌内、皮下注射:一次量,马、牛20~50mg;羊、猪5~10mg。【注意事项】连续长期应用可引起粒性白细胞减少症,应定期检查血象。【停 药 期】28日,弃奶期7日。【有 效 期】二年【规 格】10ml【包 装】10ml /支×5支/盒【贮 藏】遮光、密闭保存。
喜炎平脉络宁注射液引起严重过敏2012年06月27日08:47新华网国家食品药品监督管理局26日发布通报,提示生产企业和医患人员关注喜炎平注射液和脉络宁注射液引起严重过敏反应的问题。据了解,喜炎平注射液的成分是穿心莲内酯磺化物,主要用于解热消炎。2011年,国家药品不良反应监测中心病例报告数据库有关喜炎平注射液的病例报告数共计1476例,其中涉及14岁以下儿童报告达1048例。主要不良反应表现为过敏样反应、过敏性休克、紫绀、呼吸困难等。脉络宁注射液是2009版国家基本药目录品种,其功能与主治为清热养阴、活血化瘀。用于血栓闭塞性脉管炎、动脉硬化性闭塞症、脑血栓形成及后遗症、静脉血栓形成等。2011年,国家药品不良反应监测中心病例报告数据库共收到有关脉络宁注射液药品不良反应病例报告1500例,其中严重病例报告189例。严重不良反应主要为呼吸系统损害、全身性损害和心血管系统损害等。国家食品药品监管局建议,由于这两种注射液易发生过敏反应,建议医护人员在用药前详细询问患者的过敏史,特殊人群和过敏体质者应慎重使用。使用时应严格按照说明书规定的用法用量给药,不得超剂量使用;谨慎联合用药。如确需联合使用其他药品时,应谨慎考虑与此两种药品的间隔时间以及药物相互作用等问题。对于药品生产企业,国家食品药品监管局建议,加强临床合理用药的宣传,确保产品的安全性信息及时传达给患者和医生;完善生产工艺、提高产品质量标准,开展相应安全性研究。(新华网)
注射液内含毛发异物 山东齐都药业身陷“质量门” 近日,国家食品药品监管总局(以下简称“药监总局”)发布公告指出,吉林省长春市一诊所发现山东齐都药业有限公司(以下简称“齐都药业”)生产的盐酸左氧氟沙星氯化钠注射液有类似毛发状异物。事发后,涉事产品被该公司业务员销毁,该公司生产管理体系存在缺陷。目前,山东省食品药品监督管理局已责令该企业停产整顿,并对涉事批次药品按劣药论处。 记者发现,其实早在2014年7月,该产品的说明书修订问题就曾被人投诉;而在此前的2014年5月,齐都药业生产的替硝唑片也曾被江苏省药监局部署采取查控措施,该公司为何频繁曝出药品质量问题?停产整顿 2月6日,药监总局发布《关于山东齐都药业有限公司产品质量问题的通告》称,该局2015年2月6日因产品质量问题约谈山东齐都药业有限公司,山东省、吉林省食品药品监管局参加了约谈。 经查,长春市一诊所发现山东齐都药业有限公司生产的盐酸左氧氟沙星氯化钠注射液有类似毛发状异物,事发后涉事产品被该公司业务员销毁,但有关证据证明涉事产品确实存在上述问题。2月7日,齐都药业在其官网发布关于产品质量问题的道歉信,承认上述事实,并承担全部责任。 药监总局在约谈中指出,山东齐都药业有限公司生产管理体系存在缺陷,必须立即开展自查,尽快找出药品生产质量管理体系中存在的问题,及时向监管部门提出整改报告。另外,山东齐都药业有限公司业务员销毁证据、掩盖事实的行为,严重违反《药品生产质量管理规范》诚实守信的基本要求,性质极其恶劣,总局已责成山东省食品药品监管局对该企业依法处理。 据记者了解,山东齐都药业有限公司生产的涉事盐酸左氧氟沙星氯化钠注射液批号为C13042201,总计21700瓶,2013年4月22日生产,有效期至2015年3月底。产品销往吉林8000瓶、河北10500瓶、黑龙江2300瓶、辽宁900瓶。药监总局已要求上述省食品药品监管部门关注产品的流通使用情况,采取有力措施监督企业召回产品;同时要求药品不良反应监测机构加强监测,发现不良反应事件及时报告并依法予以处置。 公开资料显示,齐都药业主要生产大容量注射剂、片剂、胶囊剂、冲洗剂、原料药等172个品种规格的产品。企业大输液产销量排名全国第三位,单体工厂全国第一位。 “事件发生后,公司主动采取召回措施,对该批次产品实施召回。组织专业人员对质量管理体系的各个环节进行自查,排查分析问题原因,并及时采取相应整改措施。还派出相关人员,就有关问题积极进行协调处理。”齐都药业在道歉信中表示。 2月16日,山东省药监局公开表示,药监总局通告山东齐都药业有限公司盐酸左氧氟沙星氯化钠注射液事件后,省局立即成立联合调查组对该企业进行了全面监督检查。一是监督企业全力召回所有涉事产品,截至2015年2月12日,该企业已完成召回工作,经终端使用单位确认,涉事批次药品已全部销售使用;二是监督山东齐都药业有限公司停产整顿,深入查找风险隐患和管理上存在的漏洞,确保类似问题不再发生,整改完成后由省局进行全面检查,符合相关要求后方可恢复生产;三是对涉事批次药品按劣药论处,依照有关法律法规严厉处理;四是监督企业质量保证体系运行和整改措施落实,并采取有效措施,确保药品生产质量安全。 3月5日,齐都药业办公室崔主任在电话里向本报记者表示,药监部门正在对“异物门”事件进行调查,还没有最终处理结论,该公司现在对此不便回应。屡现问题 据记者了解,左氧氟沙星是氧氟沙星的左旋体,属第三代喹诺酮类药物。左氧氟沙星注射剂是临床使用广泛的抗感染药,因其抗菌谱广、疗效好、使用方便等原因,在抗菌治疗领域发挥着重要作用。然而,随着药品的大量应用,其不良反应也日益突显。 2009年5月,国家药监总局第22期药品不良反应信息通报指出,左氧氟沙星注射剂严重病例报告突出,建议药品生产等加强临床合理使用抗菌药物的教育与宣传,充分告知医生和患者可能存在的潜在风险。 2012年12月31日,国家药监总局(国食药监注373号)通知:“决定对左氧氟沙星(包括盐酸左氧氟沙星、甲磺酸左氧氟沙星、乳酸左氧氟沙星)口服和注射剂说明书进行修订。药品生产企业要尽快修订说明书及标签的相关内容,按照有关规定进行备案。”新版说明书增加了相关警示语、不良反应警示语、不良反应等相关内容。 2013年8月2日,国家药监总局发布第56期通报指出,2012年,收到左氧氟沙星注射剂严重不良反应/事件病例报告1431例,占总例次的60.24%。要求生产企业修改完善药品说明书相关内容,保障公众用药安全。 2013年11月21日,药监总局第58期通报“及时修订氟喹诺酮类药品的产品说明书,更新相关的用药风险信息如不良反应、注意事项等,以有效的方式将氟喹诺酮类药品的风险告知医务人员和患者”。 据山东省田先生向记者反映,截至2014年7月,齐都药业药品“迪诺新”盐酸左氧氟沙星氯化钠注射液仍在使用2007年5月核准的说明书。 事实上,早在2014年5月,齐都药业生产替硝唑片就因说明书问题被江苏省药监局部署采取查控措施。 据无锡市锡山食品药品监督管理局官网信息显示,按照省局紧急通知要求,该局第一时间部署查控问题药品工作,督促辖区内相关经营企业及医疗机构开展排查,对库存的山东齐都药业有限公司生产的替硝唑片(批号:1312041,规格:0.5克),立即停止经营使用,并采取暂控等措施,同时要求上报库存产品数量以及举一反三检查相近批次的药品说明书情况。 经统计,锡山区涉及问题药品零售及使用单位2家,药品批发企业1家,涉及药品销售数量为300盒。2014年5月9日下午13时,辖区药品批发企业下发药品召回通知,开展涉及药品的召回工作。截至2014年5月12日下午16时,已召回110盒。据业内人士介绍,2013年10月16日,药监总局办公厅发布关于修订替硝唑口服片剂和胶囊剂说明书的通知。为保障公众用药安全,根据国家食品药品监督管理总局监测评价结果,决定对替硝唑口服片剂和胶囊剂说明书进行修订。要求生产企业在2013年12月15日前,依据《药品注册管理办法》等有关规定提出修订说明书的补充申请报备案。说明书的其他内容应当与原批准内容一致。补充申请批准之日起生产的药品,不得继续使用原药品说明书。 上述人士分析认为,无锡药监部门要求举一反三检查相近批次的药品说明书情况,这说明可能是齐都药业修订说明书的补充申请批准后,该批次替硝唑片继续使用了原药品说明书,从而导致被药监部门采取查控措施。 替硝唑片被药监部门采取暂控等措施的最终处理结果如何?(迪诺新)盐酸左氧氟沙星氯化钠注射液是什么时候开始按照药监总局要求修改产品说明书的?患者田先生的反映是否属实? 对此,崔主任仅向记者表示:“这件事情已经过去很久,没有什么新闻价值,你就不要关注了。”
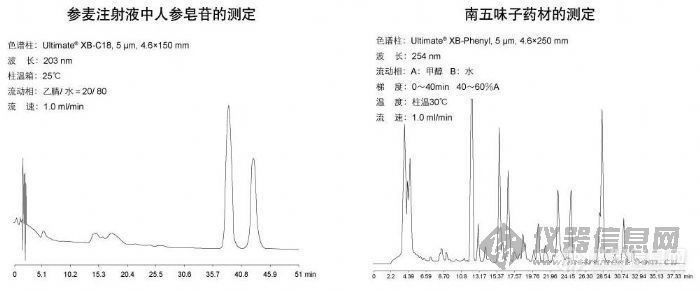
参麦注射液中人参皂苷的测定和南五味子药材的测定http://ng1.17img.cn/bbsfiles/images/2009/10/200910161341_175971_1896702_3.jpg

【作者】 王小平; 刘峰; 杨东华; 屠鹏飞; 马存德;【Author】 WANG Xiao-ping1,2,LIU Feng2,YANG Dong-hua1,TU Peng-fei3,MA Cun-de2(1.Shaanxi University of Traditional Chinese Medicine,Xianyang 712046,China;2.Shaanxi BuchangPharmaceuyical Co.Ltd,Xianyang 712000,China;3.Beijing University,Beijing100191,China)【机构】 陕西中医学院; 陕西步长制药有限公司; 北京大学;【摘要】 目的:建立丹红注射液中迷迭香酸在大鼠血浆中浓度的测定方法。方法:雄性SD大鼠6只,静脉注射丹红注射液(10 mL.kg-1)后,分别于不同时间取血,以肉桂酸为内标,液液萃取处理后,HPLC测定浓度。Diamonsil(钻石)C18色谱柱(4.6 mm×250 mm,5μm),乙腈-0.4%的磷酸水为流动相,梯度洗脱,流速1.0 min.mL-1,检测波长286 nm。结果:迷迭香酸在4.0~100.0 mg.L-1呈良好线性关系(R2=0.996 5);回收率在85.0%~101.4%,方法的日内、日间精密度(RSD)分别为4.00%~6.76%,4.50%~7.81%。不同时间点血浆中迷迭香酸的质量浓度分别为85.44,75.09,61.13,54.73,43.02,20.92,10.12,7.18,4.28 mg.L-1。结论:建立的方法灵敏度好、准确率高,可用于丹红注射液中迷迭香酸的药代动力学研究。 http://ng1.17img.cn/bbsfiles/images/2012/07/201207231612_379232_2379123_3.jpg
求助SAN++流动注射中文说明书,我的邮箱1007256035@qq.com,万分感谢
[center]脑蛋白水解物注射液药品标准不完善[/center] 据国家药监局网站消息,为确保公众用药安全,国家药监局日前通知要求各地进一步加强对脑蛋白水解物注射液的监督检查。 通知称,在全国开展注射剂类药品生产工艺和处方核查工作中,发现脑蛋白水解物注射液品种在药品标准和执行工艺处方等方面存在着较为突出的问题,主要是企业选用猪脑原料的质量标准不完善;企业之间现行生产工艺差别较大;猪脑水解所用的蛋白酶种类、酶量及水解温度、时间等不一致,甚至有补加氨基酸的行为。针对上述突出问题,部分地区已采取了控制措施。 通知指出,一、要充分认识到脑蛋白水解物注射液在产品质量方面存在的安全风险,各地应在注射剂类药品生产工艺和处方核查工作的基础上,积极组织力量认真做好监督检查工作。要建议辖区内脑蛋白水解物注射液生产企业主动停止该品种的生产,并要求脑蛋白水解物注射液生产企业按相关技术要求,组织开展改进工艺和质量控制方法的研究工作,在相关工艺改进和质量标准未经批准前,暂不宜恢复生产。 二、对于生产企业认为其脑蛋白水解物注射液生产工艺合理、质量可控,继续进行生产的,所在地省级食品药品监督管理局应对其生产全过程予以跟踪检查,并对监督生产的产品进行现场抽样,由省级药品检验所检验。 凡生产企业存在未按批准变更生产处方工艺生产,或在制成品中补加氨基酸等违法违规行为,以及现场抽样检验不合格的,应依法予以严厉查处。 三、国家局将组织有关专家开展脑蛋白水解物注射液有效性、安全性评价工作,组织对脑蛋白水解物注射液生产工艺的改进、质量控制标准的提高工作,并在此基础上提出监管措施和改进意见。信息来源:中国新闻网
RT、硫酸鱼精蛋白注射液告急什么原因造成的???有知道的吗?
[font=宋体]丹参是鼠尾草属植物丹参[/font][i]Salvia miltiorrhiza [/i]Bunge[font=宋体]的根以及根茎经过干燥炮制后而成。别名郄蝉草、奔马草等,最早被[color=var(--weui-LINK)]《神农本草经》[i][/i][/color]列为上品[/font][font=宋体],丹参整体作用平和,具有活血祛瘀而不伤正气之效[/font][font=宋体],[/font][font=宋体]常有“一味丹参饮,功同四物汤”之说。中医认为,丹参具有活血祛瘀、通经止痛等功效,适用于血瘀诸证。高血压慢性病程导致的肾损害,病机虚实夹杂,病势缓慢而持久,正如古人云:“久病必瘀”,故高血压肾病以肾络血瘀为基本病机,贯穿疾病始终,临床治疗上多以活血通络为主要治法[/font][font=宋体]。《神农本草经》中认为:“(丹参)破癥除瘕,止顿满,益气”。《日华子本草》记载丹参能“通利关脉”“破宿血,补新生血”。[color=var(--weui-LINK)]《本草正义》[i][/i][/color]中认为:“《本经》所谓益气,《名医别录》所谓养血,皆言其积滞既去,而正气自伸之意,亦以通为补耳。”故丹参古往今来被广泛应用于肾络血瘀为主要病机的各种肾系病证。[/font][font=宋体]现代研究发现,丹参具有抗氧化应激、抗炎、抗肿瘤、抗纤维化、抗动脉粥样硬化、降血压、调节血脂等功效,广泛应用于心脑血管疾病、癌症、肾脏疾病以及肝脏疾病中[/font][font=宋体]。 随着现代药理研究的不断深入,提取出的丹参的主要化学成分为二萜类、三萜类、酚酸类、黄酮类以及含氮类化合物、内酯类化合物、多糖等共百余种物质,其中活性成分主要以二萜类与酚酸类化合物为主。二萜类主要包括丹参酮[/font][color=black]I[/color][font=宋体]、丹参醇[/font]A[font=宋体]、丹参酮[/font]II[sub]A[/sub][font=宋体]、丹参酮[/font]II[sub]B[/sub][font=宋体]等含有醌类结构母核及二萜类结构特征的化合物。三萜类以齐墩果酸和熊果酸的衍生物居多。酚酸类成分有以丹参素([/font]danshensu[font=宋体],[/font]DSS[font=宋体])、丹酚酸[/font]A[font=宋体]([/font]salvianolic acid A[font=宋体],[/font]Sal A[font=宋体])、丹酚酸[/font]B[font=宋体]([/font]salvianolic acid B[font=宋体],[/font]Sal B[font=宋体])、原儿茶醛([/font]protocatechuic aldehyde[font=宋体],[/font]PAL[font=宋体])等为主。其中丹参酮[/font]II[sub]A[/sub][font=宋体]、丹参多酚酸和丹参素是保护肾功能的主要成分。通过以丹参为主要成分的中药组方(如大黄丹参汤)、丹参提取液(如丹参注射液)及生物活性成分的临床和基础实验证实,丹参能够通过抑制氧化应激、抗炎、抗纤维化及对血压调节等作用,广泛应用于抑制肾脏纤维化中,同时对包括高血压肾病和糖尿病肾病在内的慢性肾脏病具有较好的治疗作用。[/font]
5-单硝异山梨醇酯检查时HPLC的问题5-单硝异山梨醇酯注射液检查有关物质时,色谱图在溶剂峰处有时会出现一个很大很尖的峰,有时又没有,有做过的来讨论一下。有时含量测定时也会出现。是5-单硝异山梨醇酯分解产物吗?困惑。
需要日立K-1000流动注射分析的说明书或者若没有这个型号的日立同类产品的也可以。
求一份油墨注射器说明书
我测的是注射液里的钠,钾,铯,可是注射液里有葡萄糖和枸橼酸,是不是必须硝化啊,硝化的方法在那里着找啊,我是新手,忘各位前辈指点指点。我在一些专利网上没有查到。
注射液是常用的药品之一,而且因其药效迅速、作用可靠,正越来越广泛地应用于临床。因注射液直接进入血液,对其无菌性的要求非常高,《中国药典》规定,注射液中不应含有任何活的微生物,这就需要抗氧剂来帮忙。那么在注射液中常用的抗氧剂 有哪些?
中药注射液,确切的说我要做香丹注射液的重金属及有害元素检查,可以制剂取10ml加5ml置赶酸仪中130°,加热至近干,就稀释等上机做可以吗?
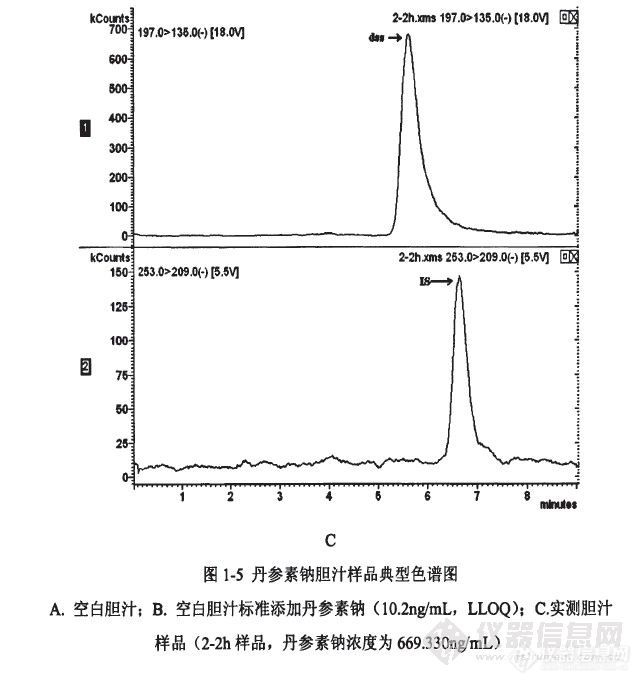
【作者】魏华 【摘要】:药物代谢动力学旨在通过测定生物样本中的药物或者代谢产物的浓度,定量描述药物进入体内以后的吸收、分布、代谢、排泄过程,进而阐明药物的药效或者毒性,为新药研究的代谢筛选和临床用药的疗效评价提供重要依据。丹参素为从唇形科植物丹参Salvia miltiorrhiza Bunge的干燥根中提取出的单体化合物,具有明显的药理活性。作为丹参的主要活性成分之一,有必要对丹参素进行药代动力学研究,探讨其体内过程。本文建立的LC-MS/MS法测定血浆、尿液、胆汁等多种生物样本中的丹参素钠浓度,满足临床前药代动力学研究对高灵敏度、高选择性检测的技术要求。此外,本文还进行了丹参素钠的体内、体外代谢研究,初步建立了体外代谢筛选研究平台,为进一步开展临床用药及剂型开发提供参考依据。 一、生物样品中丹参素钠定量分析方法的建立与确证 在临床前药代动力学研究中,定量分析方法的建立与确证占有举足轻重的地位,只有建立可靠、专一、灵敏、快速的生物样品分析方法,才能保证药代动力学研究的顺利进行。本文采用高灵敏度的LC-MS/MS方法检测生物样品中丹参素钠的浓度,生物样品以盐酸酸化后用乙酸乙酯提取其中的丹参素钠。色谱分析采用迪马Diamonsil C-18,5μm,200×4.6mm,柱温25℃;流动相组成为甲醇:水=80:20(含0.01‰甲酸),采用等梯度洗脱方式,流速0.80mL/min,3:2分流入质谱的流速为0.32mL/min,进样量20μl。质谱检测采用ESI离子源、负离子检测模式,选择MRM工作方式进行质谱分析。经完整的方法学确证,所有测定生物样品的线性、准确度、精密度、回收率、基质效应、稀释效应、稳定性等均满足生物样品的定量分析要求。该方法成功用于SD大鼠的药代动力学研究及尿液和胆汁的排泄研究。 二、丹参素钠在SD大鼠体内的临床前药代动力学研究 本试验设计SD大鼠单剂量尾静脉注射给药丹参素钠15mg/kg、30mg/kg、60mg/kg三个剂量组进行药代动力学研究。采用LC-MS/MS测定方法分别测定了给药后不同时间的体内丹参素钠血药浓度。按血浆样品预处理操作,测得数据代入相应样品随行标准曲线中求得含量。经非房室模型法估算药代动力学参数。结果表明,大鼠单剂量静注给药丹参素钠15mg/kg、30mg/kg、60mg/kg三个剂量组药代动力学药时曲线末端相消除半衰期(t1/2)分别为2.73h、2.37h、1.95h;AUC0~∞分别为15.29μg·h/mL、34.58μg·h/mL和58.49μg·h/mL,AUC与给药剂量基本呈正相关,相关系数r~2为0.9836。 SD大鼠单剂量尾静脉注射给药丹参素钠30mg/kg后,于给药后收集0~96h的尿液,按尿液样品预处理操作,测得数据代入相应样品随行标准曲线中求得含量。结果表明,丹参素钠在SD大鼠体内主要经尿液排泄,96h药物累积排泄量为46.99%。SD大鼠单剂量尾静脉注射给药丹参素钠30mg/kg后,于给药后0~24h取其胆汁,按胆汁样品预处理操作,测得数据代入胆汁样品随行标准曲线中求得含量。结果表明,丹参素钠在SD大鼠体内经胆汁排泄量少,24h内胆汁累积排泄量为给药剂量的0.82%。综上所述,丹参素钠在SD大鼠体内主要以原型药的形式直接由尿排出体外。 三、丹参素钠体内外代谢的初步研究 丹参素钠给药后大鼠胆汁和尿液样品的分析结果显示,其进入体内后,主要发生II相代谢反应,主要代谢物为:甲基化丹参素~-、硫酸酯结合物~-、甲基化硫酸酯结合物-、经尿液排出体外;胆汁中主要存在着甲基化丹参素。丹参素钠经在体肠灌流、原位肝灌流等实验后,主要产生甲基化代谢产物,说明这些器官组织中存在着参与其甲基化反应的酶。经过体外肝匀浆、肝微粒体、肾匀浆、肾微粒体温孵后,主要代谢产物为甲基化丹参素。丹参素钠在大鼠肝微粒体酶中代谢的酶动力学结果显示,它在大鼠肝微粒体酶中代谢的Vmax为185.19ng/(mL·min·mg)蛋白,Km为98940.74ng/mL,即5.0×10~(-4)mol/L,内在代谢清除率Clint为1.87×10~(-3)mL/(min·mg)蛋白。此外,本章还进行了丹参素钠在COMT单一酶中的酶促反应动力学研究。与肝微粒体酶相比,丹参素钠与COMT有较大的亲和力,Vm、Km与Clint均偏大:Vmax为243.90ng/(mL·min·mg)蛋白,Km为102156.1ng/mL,即5.16×10~(-4)mol/L,内在代谢清除率Clint为2.34×10~(-3)mL/(min·mg)蛋白。说明催化丹参素发生甲基化反应的主要酶是COMT。【关键词】:丹参素 LC-MS/MS 药代动力学 排泄 大鼠 代谢产物 肝微粒体 酶促反应动力学 COMT 【学位授予单位】:第二军医大学【学位级别】:硕士【学位授予年份】:2010【分类号】:R96http://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384889_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384890_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384891_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384892_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210834_384893_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384894_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384895_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384896_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384898_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384899_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210835_384900_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208210836_384901_2352694_3.jpg
近日有群友求助,群里尚未有人应答,现在版面上贴出,希望有人予以回应: 依据依######注射液处方,配制#####注射液作为制剂空白。精密量取B、Mg、Al、K、Ca、Cr、Fe、Zn、Ba、As、Cd、Pb、Co、Ti、Mn、Sb标准液适量于10ml量瓶中,用1%硝酸稀释至刻度,得对照储备液精密量取对照储备液适量于50ml量瓶中,加入制剂空白溶液10ml, 1%硝酸稀释至刻度,得系列浓度溶液。以含20%制剂空白的1%硝酸溶液为标准空白溶液。测定标准空白溶液和标准溶液系列,仪器自动绘制标准曲线。然后根据此线性进行样品测定,及方法学考察。不知这样的做法是否有不妥的地方?
多多药业有限公司生产的双黄连注射液被叫停。今天,国家食品药品监督管理局在其网站上发出通知,要求各地暂停销售使用标示为多多药业有限公司生产的双黄连注射液。 16日,国家药品不良反应监测中心报告称,标示为黑龙江多多药业有限公司生产的双黄连注射液在使用中出现严重不良事件。为确保公众用药安全,决定暂停销售和使用标示为多多药业有限公司生产的双黄连注射液。 目前,国家食品药品监督管理局和卫生部正在对该事件发生的原因进行调查。 大家对此事件如何看待的,有什么想法、看法、观点,说说,晒晒![em09502]
在英国药典附录colour of solution中指描述了标准比色液的配制,但如果注射液正文中没有对颜色的描述,是否就表明对该品种的颜色不做要求呢?还是说没有描述就是要求澄清无色?药典的其他地方有没有溶液颜色的规定?请指点,谢谢!
想配制一个不含主药成分的注射液空白,看了下某注射液的辅料,为丙二醇,但没写浓度。有人告诉我大概就按照1%~10%的浓度配制这个辅料溶液就可以了,但我一估算,主药成分是10ml:0.1g,相当于1%的浓度。想不到名为辅料,这个浓度居然跟主药浓度相当甚至还超过啊,所以有点吃不准,特来请教各位老师,还望赐教。
作者:偶志红,徐丹丹,郭薇 来源:中国论文下载中心【摘要】 目的 建立薄层层析-紫外分光光度法测定香丹注射液中原儿茶醛的含量。方法 以原儿茶醛为对照品,展开剂为二氯甲烷-乙酸乙酯-甲酸(8∶5∶0.8)分离得到原儿茶醛,采用紫外分光光度法,检测波长281nm,测定原儿茶醛的含量。结果 原儿茶醛在0.55~4.95μg/ml 范围内线性关系良好,r=0.9998。平均含量为0.174mg/ml,加样回收率为97.3%~102.3%,RSD为1.6%。结论 实验结果表明,薄层层析-紫外分光光度法测定香丹注射液中原儿茶醛的含量,方法操作简便,准确度高,精密度好,可作为样品的检测方法。 【关键词】 香丹注射液;原儿茶醛;薄层层析-紫外分光光度法;含量测定
注射液粘度不算小,稀释了5倍检测其中的铝,含量约为0.009,但加标回收很低。想着应该再加大稀释倍数,但是样品中的铝浓度会更低,担心检测误差会更大。记得对于很微量的检测,可以通过加标来测定,但具体怎么操作,或者测完后怎么计算样品中的铝呢?请知道的老师详细指导一下。
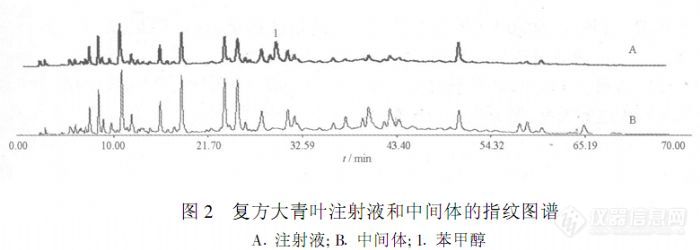
【作者中文名】刘瑞; 刘志刚; 李磊; 任冲; 袁波; 李发美;【作者英文名】LIU Rui; LIU Zhi-gang; LI Lei; REN Chong; YUAN Bo; LI Fa-mei(School of Pharmacy; Shenyang Pharmaceutical University; Shenyang 110016; China);【作者单位】沈阳药科大学药学院; 沈阳药科大学药学院 辽宁沈阳; 辽宁沈阳;【摘要】目的:采用HPLC建立复方大青叶注射液的指纹图谱测定方法。方法:采用Diamonsil C18色谱柱,甲醇-水-磷酸为流动相进行梯度洗脱,流速1.0 mL.min-1,检测波长254 nm。结果:建立了复方大青叶注射液的HPLC对照指纹图谱,标示了注射液中的20个共有峰,并初步确定注射液的相似度阈值为0.85。结论:该方法准确、重复性好,为复方大青叶注射液的质量控制提供了依据。http://ng1.17img.cn/bbsfiles/images/2012/08/201208131758_383604_2379123_3.jpg
土霉素注射液用高效液相怎么检测?谢谢!
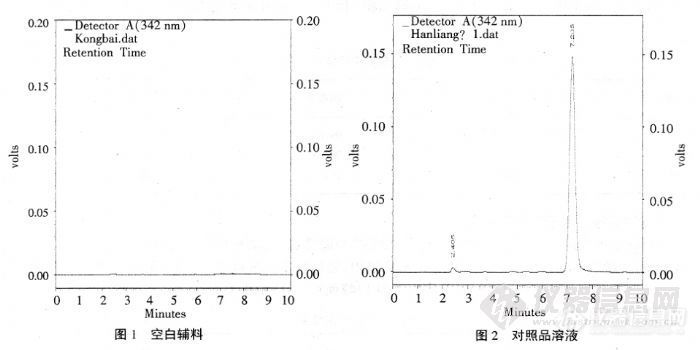
标题:5.1 甲钴胺注射液含量的方法学研究作者:常 明 1, 李 晶 1, 武玉洁 2, 张文双 2( 1.石家庄学院 化工学院, 河北 石家庄 050035; 2.石家庄栢奇制药有限公司, 河北 石家庄 050035)摘要: 摘 要: 以乙腈- 甲醇- 0.05 mol /L磷酸二氢钾溶液( 10∶ 20∶ 70) (用磷酸调节 pH 值为 4.0)为流动相, 采用迪马钻石 C18( 250 mm× 4.6 mm, 5 μ m)色谱柱及紫外检测器, 建立了甲钴胺注射液中甲钴胺含量的反相高效液相色谱检测方法. 柱温: 40℃; 检测波长为 264 nm; 流速: 1.0 mL /min. 本方法测定的日内精密度为 0.59%, 日间精密度为 0.67%, 回收率为 99.7%~ 100.5%, 在 160~ 240 μ g /mL范围内线性关系满足要求( r=0.999 9) ; 结果表明方法准确、 操作简单、 专属性强, 可用于定量测定甲钴胺注射液含量.http://ng1.17img.cn/bbsfiles/images/2012/07/201207161648_377914_2379123_3.jpg
看到氢化可的松注射液的辅料里有乙醇和注射用水,想扣除辅料干扰就得配制相应浓度的辅料,谁能透露下,这处方里头的乙醇大概浓度多少啊? 叩谢各位大大。
为对庆大霉素和林可霉素注射液的安全性进行毒理学评价,采用急性毒性试验、溶血试验、局部血管刺激性试验、肌肉及皮肤刺激试验及豚鼠全身用药的过敏试验,考察庆大霉素和林可霉素注射液制剂的安全性。结果表明,庆大霉素和林可霉素注射液对小鼠肌肉注射的LD 。为4.989 mL/kg,0.1~0.5 mL该注射液在4 h内对兔红细胞不产生溶血和凝聚作用;静脉注射部位血管及周围组织均未见充血、水肿、出血和坏死等病理改变,肌肉注射部位充血范围在0.5 cm×1.0 cm 以下,4块股四头肌反应级的最高与最低之差等于0,家兔四块股四头肌反应级之和小于1O;以相当于临床用量2倍的剂量涂抹皮肤,停药后1、24、48、72 h镜下观察均未见明显异常的病理变化;豚鼠首次致敏后第14天及第21天静脉注射液攻击,在观察期内未见过敏反应。表明庆大霉素和林可霉素注射液在该试验条件下是安全的。过敏试验猪链球菌病是由猪链球菌引起的人畜共患传染病,是规模化养猪场中最常见的细菌病之一(蔡宝祥,2001)。本病一年四季均可发生,但以5一l1月发生较多,大小猪均能感染发病,但多见于断奶仔猪和育肥猪。庆大霉素和林可霉素注射液主要用于治疗断奶仔猪链球菌病,临床多肌肉注射给药。为了考察该给药方法的安全性,根据《新药注册管理办法》及有关法规的要求,作者对庆大霉素和林可霉素注射液进行了急性毒性试验、溶血试验、局部刺激性试验(肌肉、血管、皮肤)及全身过敏试验,供临床参考。
【中国药典】从1985年版至1995年版均采用显微镜法检查注射液中的不溶性微粒。检查≥10μm与≥25μm两档,与美国药典标准基本相同。在2000年版【中国药典】显微镜法检查注射液中不溶性微粒的基础上增加了第二法----光阻法。在2005年版【中国药典】中增加了对小剂量注射液的检测。【中国药典】2005年版初稿对注射液中不溶性微粒污染的监控作了修订,将光阻法修订为第一法,显微镜法为第二法。修订后的结果判定也与美、英、欧共体、日本基本一致。原文来自:http://pssnicomp.cn/zhuanti.html
利用[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法建立复方苦参注射液中7个成分(甲基氧化偶氮甲醇樱草糖苷、苦参碱、槐果碱、槐定碱、氧化槐果碱、氧化苦参碱、番石榴酸)的含量测定方法。采用Waters Xselect CSHTM C18色谱柱(250 mm×4.6 mm, 5μm),以甲醇-0.2%磷酸二氢钾为流动相,梯度洗脱,流速0.6 mLmin-1,柱温30℃,检测波长211 nm。测定的甲基氧化偶氮甲醇樱草糖苷、苦参碱、槐果碱、槐定碱、氧化槐果碱、氧化苦参碱、番石榴酸7个成分的平均加样回收率分别为95.7%、101.3%、100.8%、101.7%、102.6%、102.5%、99.5%,RSD分别为2.0%、0.72%、0.90%、0.74%、1.4%、0.96%、1.8% 10批次样品中7个成分的含量分别为0.53~0.73、2.66~4.22、0.75~1.11、0.70~0.89、2.20~2.84、7.62~9.95、1.63~2.20 mgmL-1。该方法稳定可靠,可为复方苦参注射液的质量控制与评价提供参考。详见王鹏飞等,药物分析杂志. 2022,42(07)
中药注射液的前途渺茫还是?大家说说看[em0801]