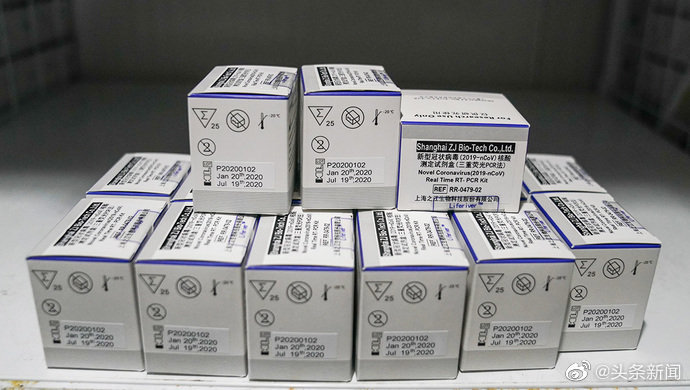
非洲猪瘟病毒提取检测试剂盒(AB盒)即口鼻拭子非洲猪瘟检测试剂盒
非洲猪瘟病毒提取检测试剂盒(AB盒)FT-FWSJ_风途批发_非洲猪瘟病毒提取检测试剂盒(AB盒)_Go tšwa ga poledišano ya sešireletši sa go dira modumo ya sešireletši sa go tswalela ka Afrika (AB Kit)_好试剂选风途错不了 非洲猪瘟的爆发对我国养殖业构成了空前的挑战,将对我国养猪业及相关产业的发展产生深远的影响。近期有报道称,从部分猪血浆蛋白粉中检测出非洲猪瘟病毒核酸,这几乎宣告了猪源性饲料添加剂( 如血浆粉、血球粉、肉骨粉)的死刑。如何解决这些添加剂的出路和替代途径是需要研究的重要课题。目前频繁的生猪调运和简易的运猪车辆,是疫情长距离扩散的主要风险因素,亟待建立可监测、可追溯、符合生物安全的生猪/猪肉调运和监管系统。 【产品名称】 通用名称:病毒DNA提取试剂盒 英文名称:Extraction Kit for Virus DNA 【预期用途】 本试剂盒主要用于疑似病毒等病原感染抗凝血、血淸、拭子、组织、饲料及环境中的病毒DNA的提取,纯化的核酸可适用于各种常规操作及PCR试验。 【试剂盒组分】 I、试剂盒组成及贮藏条件名称20 T50 T1、吸附柱20个50个2、收集管20个50个3、裂解液5 mL11 mL4、洗液I13 mL32 mL5,洗液II13 mL32 mL6.洗脱液1.2 mL3 mL 2、 保存条件及有效期:室温下保存,有效期12个月. 3、 需自备材料:无水乙醇、1.5 mL无菌离心管、1.5 mL无菌离心管(长臂型)、生理盐水、研钵、无菌 1mL, 2OOuL、10uL枪头、记号笔等。 【操作步骤】 一、样品制备 1、 血液样品:抗凝血样品置离心管中,8000转/分钟离心2分钟,取上层血浆 非抗凝血样品置离心 管中,待凝固后,8000转/分钟离心2分钟,取上层血清,置于灭菌离心管中,编号待检。 2、 组织样品:采集脾脏、肝脏、淋巴结、扁桃体等病变组织样品0.1g.组织匀浆器或研钵中充分匀浆或研磨,加入1 mL生理盐水混匀,8000转/分钟离心2分钟,取上清于灭菌离心骨中,编号待检。 3、 口腔液:进食前用拭子/口腔液采集袋或自制棉线绑纱布团吸引动物咀嚼,收集口腔液大于 500uL, 8000转/分钟离心2分钟,取上清于灭菌离心管中,编号待检。 4、 饲料:取适量研磨后的饲料(约0.2g),放入含1 mL生理盐水或PBS(PH为7.4)缓冲液的2 mL EP 管屮,振荡混匀,8000转/分钟离心2分钟,取上清于灭菌离心管中,编号待检. 5、 灰尘:用无菌棉签蘸取适量环境表面上的灰尘,放入含1 mL生理盐水或PBS(PH为7.4)缓冲液的2 mL EP管中,振荡混匀,8000转/分钟离心2分钟,取上清于灭菌离心管中,编号待检。 二、DNA的提取 1、取裂解液200uL加入无核酸酶1.5 mL离心曾屮,分别加入血浆/血清/组织液等样品液200uL. 震荡混匀10秒或颠倒混匀10次,室温放置5分钟(如果室内温度较低时.需放置25C水浴温育),再加入200uL无水乙醇,颠倒混匀10秒 若样品浑浊则先12000转/分钟离心1分钟处理,取上清液,以避免堵塞柱子 2、 将液体转入套有收集管的吸附柱中, 12000rpm离心1分钟: 3、 弃收集管液体,向吸附柱中加600uL洗液I , 12000 rpm离心1分钟 4、 弃收集管液体,向吸附柱中加600uL洗液II, 12000 rpm离心I分钟 5、 弃收集管液体,12000 rpm离心2分钟,以彻底去除残留洗液 6、将吸附柱转入新的无核酸酸1.5mLEP管(长臂型)中,向柱中央滴加50 uL洗脱液,静置1分钟, 12000 rpm离心1分钟,EP管中液体即为病毒DNA。 【注意事项】 1、 实验前诺仔细阅读本试剂盒说明书,严格按照操作步骤执行.在操作过程中对时间、试剂体积等 粘确控制可以获得好的结果。 2, 样本应新鲜采集使用,或低温运输储存 3, 样本具有潜在感染风险,核酸的提取应在核酸提取实验室的生物安全柜中进行。 4、 核酸提取冇关耗材确保高温灭菌,提取后核酸尽快进入下一步试验或冷冻保存待用。 5, 试剂使用前应混合均匀,试剂具有一定腐蚀性,使用时请戴手套、口罩做好防护。 6. 低温下裂解液出现结晶数属正常现象,可在60°C水浴加热助溶后使用。 7、 实验产生的废弃物应及时收集,远离PCR实验室进行无害化处理。 仅供兽医诊断使用 非洲猪瘟病毒荧光PCR核酸检测试剂盒说明书 【兽药名称】 通用名称:非洲猪瘟病毒荧光PCR核酸检测试剂盒 汉语拼音:Feizliouzhuwen Bingdu Yingguang PCR Hesuan Jianceshijihe 英文名称:African swine Fever Virus (ASFV) PCR Nucleic Acid Diagnostic Kit 商品名称:无 【主要成分与含量】试剂盒中含有如下组分:试剂盒组分含量阳性对照250μL/管×1管 阴性对照250μL/管×1管 PCR反应液850μL/管×1管 萌混合液150μL/管×1管 说明书1份/盒【作用与用途】 本试剂盒可用于血液、脾脏、肝脏、淋巴结、 样品中非洲猪瘟病毒核酸的检测。扁桃体、肾脏、肌肉、环境样品等 【用法与判定】 1 用法 1.1待检样品釆集、保存及运输 1.1.1样品釆集 (1) 活猪样品 无菌采集抗凝血或血清5mL (2) 病死猪剖检样品或屠宰场剖检样品 无菌采集死猪的牌、肺、肾、扁桃体、淋巴结、肌肉等组织样品。2〜8°C低温运至实验室用于检测。 (3) 病猪污染的周边环境 采集与病猪相关场所的粪便、饲料、污水样品。2〜8°C低温运至实验室用于检测。 1.1.2样品保存 采集的样品在2〜8°C保存应不超过24小时,-70°C条件下保存,避免反复冻 融。 1.1.3样品运输泡沫箱加冰袋后密封进行运输。包装和运输应符合农业农村部《高致病性动 物病原微生物菌(毒)种或者样品运输包装规范》和交通运输部门关于危险品运输管理的有关规定。 1.2样品处理 1.2.1血液样品处理 抗凝血样品置于离心管中,8000 r/min离心2分钟取上层血浆,编号待 检。非抗凝血样品置于离心管中,待凝固后,8000 r/min离心2分钟取200μL上层血清,编号待检。 1.2.2组织样品处理取适量脾脏、肝脏、淋巴结、扁桃体、肌肉等组织,置于研磨器或研磨管中研磨,再加适量生理盐水混匀,制成约10%的组织匀浆,8000 r/min离心2分钟,取200μL上 清于RNase/DNase-free无菌离心管中,编号备用。 1.2.3环境样品处理 1.2.3.1粪便、饲料样品处理方法取适量的粪便、饲料放入盛有PBS缓冲液的研磨管中研磨混匀,制成约10%的匀浆液.8000 r/min离心2分钟,取200μL上清于RNase/DNase-free无菌离心 管中,编号备用。 1.2.3.2污水样品处理方法 直接取200μL污水进行核酸提取。 1.3病毒核酸的提取用磁珠法或柱式法进行DNA核酸提取。 1.4荧光PCR反应: 1.4.1从试剂盒中取出荧光PCR反应液、酶混合液,室温融化后,2000 r/min离心5秒。设被 检样品、阳性对照和阴性对照总和为n,则反应体系配制如下: 试剂 体系 PCR 反应液 17× (n+1) μL 酶混合液 3× (n+1) μL 1.4.2在新的RNase/DNase-fire 1.5 ml离心管中加入上述试剂,充分混匀后瞬时离心。按照20μL/ 管分装量将试剂分装至荧光PCR反应管。 1.4.3在上述制备好的荧光PCR反应管中分别加入阴性对照、阳性对照各5μL、处理好的待测核酸各5μL,终体积25μL/管,盖好荧光PCR反应管盖,混匀后瞬时离心,转移到荧光PCR仪器 上。 144将PCR反应管放置在荧光PCR仪样品槽中,在荧光PCR仪上运行以下程序:步骤条件循环数UNG处理50 ℃, 2分钟1预变性95 ℃, 3分钟1预扩增95 ℃: 8 秒 55 ℃: 8 秒 5PCR扩増95 ℃: 8 秒 55 ℃: 8 秒 40 荧光通道选择FAM,在PCR扩增阶段每个循环的55℃时采集荧光信号。设置扩增体系为25μL, 同时要选择passive reference和quencher为none的模式。(注:若荧光PCR仪(如AB17500)按说明 书中的反应程序设置后因持温时间短无法运行,可将预扩增和PCR扩增条件变更为95C: 5秒 55°C: 30 秒) 2结果判定 2.1试验有效性判定 阳性对照有典型扩增曲线且Ct值≤30.且阴性对照无Cl值或无扩增曲线,线形为直线或轻微斜线,无指数增长期。则判试验结果有效。否则,此次试验视为无效。 2.2样品判定 2.2.1阳性:样本检测结果Ct值≤35且有明显指数增长期,判定检出非洲猪瘟病毒核酸。 2.2.2可疑:样本检测结果Ct值在35〜38范围内。此时应对样本进行重复检测,如果重复实验 结果Ct值仍在35〜38范围内,有明显指数增长期.则判定为阳性,否则为阴性。 2.2.3阴性:样本检测结果Ct值38或无Ct值,判定未检出非洲猪瘟病毒核酸。 【注意事项】(1)实验前请仔细阅读本试剂盒说明书,严格按照操作步骤执行,在操作过 程中对时间、试剂体积等精确控制可以获得好的结果。 (2) 实验室应严格按照有关规定分区管理,依照配液区-模板提取区-扩增区-分析区顺序 进行基因检测。各区间人员、器材、试剂及空气流向应有严格要求。 (3) 核酸提取有关耗村确保洁净、无DNase/RNase,提取过程尽量低温、快速,完成后进入 下一步实验或冻保。 (4) 对于顶部采光仪器要带新的一次性PE手套对荧光PCR管封盖,对于底部采光仪 器要避免徒手或使用过的手套接触荧光PCR管底,检测过程中使用不带荧光物质一次性乳胶手套。 (5) 冻存试剂使用前应于室温下完全融化,瞬时离心使液体完全沉于管底。避免反复冻融, 以免影响试剂性能。 (6) 样品、阳性对照等在使用后及时封盖,.避免组分间及气溶胶等的污染造成假阳性。 (7) 扩增产物禁止开盖,实验产生的废弃物应及时收集,远离PCR实验室进行无害化处理。 【规格】50头份/盒 【贮藏与有效期】试剂盒置-20°C以下避光保存,有效期12个月。 【批准文号】兽药生字163668871