瑞士万通743氧化稳定性测定仪的外推法是怎么操作的?
求大家推荐测定仪器稳定性的样品。 我们的液相主要是反应中控检测,每天的流动相都不变,就只是边边梯度。最近有人反应,他们最近测的样品和前几周测的一次的保留时间差了0.2。所以我想找几个样品或者试剂,配成溶液,隔一段时间测一次,看看仪器的稳定性怎么样,好做到心里有数。求大家推荐稳定又好得的试剂名称。
胶水贮存稳定性测试中应在什么条件下最易
ISO 20783-1-2003 石油及相关产品.测定抗火液体的乳剂稳定性 .第1部分:HFAE类液体Petroleum and related products - Determination of emulsion stability of fire-resistant fluids - Part 1: Fluids in category HFAE ISO 20783-2-2003石油及相关产品.测定抗火液体的乳剂稳定性.第2部分:HFB类液体Petroleum and related products - Determination of emulsion stability of fire-resistant fluids - Part 2: Fluids in category HFB这种标准可能不好找,不过还是抱着试试看的心态来求助一下,谢谢
乳液是热力学不稳定的体系,其寿命是有限的。预示乳液的稳定性是化妆品配方师重要的问题。市售化妆品必须有2—3年的货架寿命。乳液货架寿命可定义为乳液变坏至消费者不可接受的程度所经历的时间长短。市售化妆品由于分销、储存至消费者全部用完,需经历较长一段时间,一般化妆品货架寿命为2~3年,一些国家要求含防晒剂非处方药(OTC)的乳液,稳定性长于5年。由于实时货架寿命测定费时,一般化妆品公司较少进行实时货架寿命的研究,所以设计准确预示乳液货架寿命的试验是重要的。尽管目前这类方案也不少,但还是与实际有一定距离,预示乳液的稳定性不是一件简单的事情。 (一)乳液不稳定性的机理 当乳液陈化时,经历物理变化使乳液不稳定。其中包括重力作用分层、絮结和歧化作用。 重力作用分离可能的结果是絮凝,絮凝是一种沉降或分层现象,絮凝时仍然是被乳化,但富被分散相层浓集在上层(在O/W乳液中),或在下层(在W/O乳液中)。这两种重力引起变化是可逆的,摇动可使聚集的物料重新分散。这些情况服从Stokes定律,即分离速度与油相和水相之间的密度差,连续相的黏度和被分散相粒子大小成比例。因而,增加连续相的黏度,或使用胶体磨或均质作用降低粒子大小可增加乳液的稳定性。 当被分散相液滴聚到一起,结合形成较大的液滴,发生聚结作用。最终会产生相分离。如果当乳化剂的用量不足以使液滴保持较小的尺小,但足以防止絮凝,或进一步聚结成有较大粒子分布的乳液时,这样情况称为有限聚结作用。 歧化作用是由于液滴内部压力较液滴外部压力大引起的结果。这样推动力将引起化学组分由小液滴扩散至较大的液滴,或可能扩散至连续相。由于表面活性剂体系不同组分可能由以不同的速率由小液滴扩散至大液滴,结果小液滴变小,大液滴变大。
0.01%的硅测定稳定性不好,是样子问题还是仪器问题?
谁对稳定性肥料的测定比较精通啊?可以留下联系方式讨论一下吗?将不胜感激!!!!
要做乳化香(用于饮料中)的稳定性跟踪,需要看看该乳化香精在不同的条件及BRIX中的乳化稳定性,请问怎么选择稳定性跟踪的条件和BRIX?
1、最近在做产品的起泡性检测,做的我手都软了。过程倒是不麻烦,就是将干燥后产品按照比例与水进行复比还原成原来的液体状态后再加糖进行搅拌起泡测定。2、想找一个比较简便的方法,大家给点意见。3、想参考一下啤酒泡沫稳定性的测定方法,谁有该方法给一份呗!谢谢~~~
对饮料、化妆品等乳化液的稳定性及粒径分布进行测量。
测定汞的时候,消解完了后,大家是立即上机测试还是再等一会才测的?我今天在做的时候,在各个不同的时段,出现不同的数值,而且同样配制的平行样,相差也很大,不知道毛病出在哪里了?求指点! 做标准样品的时候稳定性很好,平行测定4次基本没什么偏差!谢谢
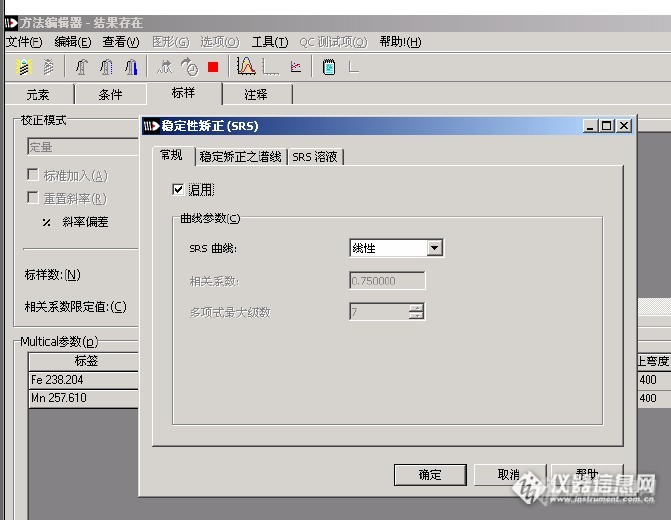
VARIAN中ICP软件操作中的稳定性矫正:(SRS)用来提高长期分析精密度以及在不采用内标的情况下提高稳定性。进入稳定性矫正页面,选择矫正曲线的相关系数(或线性),矫正谱线及标准溶液后按确定。[img=,636,574]http://ng1.17img.cn/bbsfiles/images/2017/05/201705142216_01_2140715_3.png[/img][img=,671,520]http://ng1.17img.cn/bbsfiles/images/2017/05/201705142217_01_2140715_3.png[/img]大家实际操作中是否选择,能否谈谈对VARIAN中的稳定性矫正的理解?
有没有做过乳粉热稳定性试验的? 快来交流一下。
药品的稳定性是指原料药及制剂保持其物理、化学、生物学和微生物学的性质,通过对原料药和制剂在不同条件(如温度、湿度、光线等)下稳定性的研究,掌握药品质量随时间变化的规律,为药品的生产、包装、贮存条件和有效期的确定提供依据,以确保临床用药的安全性和临床疗效。 稳定性研究是药品质量控制研究的主要内容之一,与药品质量研究和质量标准的建立紧密相关。稳定性研究具有阶段性特点,贯穿药品研究与开发全的过程,一般始于药品的临床前研究,在药品临床研究期间和上市后还应继续进行稳定性研究。 本文为一般性原则,具体的试验设计和评价应遵循具体问题具体分析的原则。 二、稳定性研究设计的考虑要素 稳定性研究的设计应根据不同的研究目的,结合原料药的理化性质、剂型的特点和具体的处方及工艺条件进行。 (一)样品的批次和规模 一般地,影响因素试验采用一批样品进行,加速试验和长期试验采用三批样品进行。 稳定性研究应采用一定规模生产的样品,以能够代表规模生产条件下的产品质量。原料药的合成工艺路线、方法、步骤应与生产规模一致;药物制剂的处方、制备工艺也应与生产规模一致。 稳定性研究中,原料药的供试品量应满足其制剂稳定性试验所要求的用量。口服固体制剂如片剂、胶囊应为10000个制剂单位左右。大体积包装的制剂(如静脉输液等)每批中试规模的数量至少应为各项试验所需总量的10倍。特殊品种、特殊剂型所需数量,视具体情况而定。 (二)包装及放置条件 稳定性试验要求在一定的温度、湿度、光照条件下进行,这些放置条件的设置应充分考虑到药品在贮存、运输及使用过程中可能遇到的环境因素。 原料药的加速试验和长期试验所用包装应采用模拟小包装,所用材料和封装条件应与大包装一致。药物制剂应在影响因素试验结果基础上选择合适的包装,在加速试验和长期试验中的包装应与拟上市包装一致。 稳定性研究中所用设备应能较好地对各项试验条件的要求的环境参数进行控制和监测。 (三)考察时间点 由于稳定性研究目的是考察药品质量随时间变化的规律,因此研究中一般需要设置多个时间点考察样品的质量变化。 考察时间点应基于对药品的理化性质的认识、稳定性趋势评价的要求而设置。如长期试验中,总体考察时间应涵盖所预期的有效期,中间取样点的设置要考虑药品的稳定性特点和剂型特点。对某些环境因素敏感的药品,应适当增加考察时间点。 (四)考察项目 稳定性研究的考察项目应选择在药品保存期间易于变化,并可能会影响到药品的质量、安全性和有效性的项目,以便客观、全面地反映药品的稳定性。根据药品特点和质量控制的要求,尽量选取能灵敏反映药品稳定性的指标。 一般地,考察项目可分为物理、化学、生物学和微生物学等几个方面。具体品种的考察项目设置应结合药品的特性进行。 (五)显著变化 稳定性研究中如样品发生了显著变化,则试验应中止。一般来说,原料药的“显著变化”应包括: 1、性状,如颜色、熔点、溶解度、比旋度超出标准规定,及晶型、水分等变化超出标准规定。 2、含量测定超出标准规定。 3、有关物质,如降解产物、异构体的变化等超出标准规定。 4、结晶水发生变化。 一般来说,药物制剂的“显著变化”包括: 1、含量测定中发生5%的变化;或者不能达到生物学或者免疫学检测过程的效价指标。 2、药品的任何一个降解产物超出标准规定。 3、性状、物理性质以及特殊制剂的功能性试验(如颜色、相分离、再混悬能力、结块、硬度、每揿给药剂量等)超出标准规定。 4、pH值超出标准规定; 5、制剂溶出度或释放度超出标准规定。 (六)分析方法 评价指标所采用的分析方法应经过充分的验证,能满足研究的要求,具有一定的专属性、准确性、灵敏度、重现性等。
10版药典拟收载维C银翘片中维生素C的测定方法探讨此维C银翘片新标准方法,我做了一些测定实验,测定的结果就是维生素C的降解很快,方法不稳定。在稳定性的考察中,同一个样品,每隔2小时进样一次,测定结果要降底1%,甚至超过1%,放置过夜后(24小时),降低17--18个百分点。维生素C的易分解,这是大家都知道的,但是这种方法的稳定性实在是太差了,如果同时测定很多检品的话,处理好的样品要及时进样,那后面的样品测定结果肯定是比实际的要低了,这样的结果能有说服力吗?与各位大侠探讨。。
氯胺T的稳定性测定水中的氰化物测定出来的标准溶液吸光度很低查看资料说是 氯胺T的问题氯胺T的稳定性这么差?如何保存呢
稳定性指示性的分析方法(Stability-indicating method)是指一种应用于制药工业中稳定性样品的测试方法,利用这类方法测定样品能够反映出在稳定性试验条件下产品质量的变化。FDA、ICH、EMEA等各类药政部门都对该方法有严格的要求,并且强调稳定性考察的样品必须采用具有稳定指示性的方法,那么到底哪些方法具有稳定指示性呢?请大家谈谈自己的看法哟
大家好,请问含量测定的时候稳定性怎么考察,需要考察哪些方面,谢谢
莽草酸的紫外分析,测定其温度、光照、ph值稳定性研究。遇到如下问题,请高手解决:1、我在网上查的资料,莽草酸最大吸收波长在213-219nm之间,但我测的最大吸收波长在213nm以下,基本上在203nm左右,我是用水做溶剂的,请问这跟仪器有关吗?我用的是日立3010的机子!2、在做ph值的稳定性,请教高手,莽草酸显酸性,ph值约为5,做稳定性要做到几最合适,我设计的时候是从1-14的ph值。请问高手是否合理?3、我做的浓度梯度吸光值随浓度增加而增大,我用500ug/ml的浓度,最大吸光值有3点几,20ug/ml时在1点几到2点几之间,请问吸光值和浓度有关系吗?4、稳定性的研究不一定是吸光值要变小,增大也能反应出稳定性不好吗?我查的资料都是说稳定性不好,那么吸光值就小。以上问题请高手赐教,我是新手。谢谢
稳定性研究的目的是考察药物在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,并确定药品的有效期。药品的稳定性是其质量的重要评价指标之一。中成药稳定性研究的范围一般根据稳定性变化的实质分为化学的、物理的及生物学的三种。中成药在制备和储存过程中,因温度、水分、光线、pH值、微生物等因素的影响,易发生变质,轻则引起制剂外观的变化,重则导致药效降低,甚至毒性增大,影响药品的安全性和有效性。通过研究揭示中药制剂稳定性变化的实质,探讨其影响因素,可采取相应的措施避免或延缓制剂的不稳定性,确定有效期,是中药制剂稳定性研究的基本任务。药品的安全、有效、质量稳定、可控是对药品的基本要求,而稳定性又是保证有效性和安全性的重要因素。因此稳定性研究在中药新药研究中占有重要的地位,是不可缺少的内容。一、中药稳定性研究的现状 1.中药新药稳定性研究技术要求 (1)《中药新药研究指南》中有明确要求。在申报临床时,待测样品于临床试验用包装条件下(在包装材料质地和结构上相当于上市药品的包装)放置,并记录室温和湿度,根据该制剂申报资料临床研究质量标准草案所列性状、鉴别、检查、浸出物、含量测定等项并结合《新药审批办法》“有关中药部分的修订和补充规定“(1992年)以下《补充规定》中附件八之附表中不同剂型的稳定性考察项目要求进行。但需注意检测成分是否能说明该制剂的稳定性。如含大黄的制剂,不能单测总蒽醌,应同时检测游离蒽醌或结合蒽醌才能确定反映其成分的变化。在常温下进行考察,开始考察时间应在样品制备后1个月之内,以开始考察的结果作为0月结果,以后每月考察一次,不得少于3个月。如预测药品远期稳定性,也可在37℃一40℃和相对湿度75%条件下保存,以开始考察的结果作为0月结果,以后每月考察一次,不得少于3个月,如稳定,相当于样品保存2年内质量稳定。但稳定性试验结果,仍以常温下为准。考察样品应在3批以上,各批样品应达中试以上规模,不得将同一批样品分成3份代表3批样品,每批样品均应留有足够在稳定性试验中各次考察所需的数量。在申请生产时,药品在上市包装条件下,根据该制剂生产用质量标准草案所列项目并结合补充规定附件八附表中不同剂型的稳定性考察项目要求进行考察。同时应注意观察直接与药品接触的包装材料对药品稳定性的影响。在常温下进行考察,一般可在初步稳定性考察后继续考察,即在初步稳定性考察3个月后,放置3个月再考察一次,然后每半年一次。药品的稳定性试验在达到规定的考察时间后还可在正常室温下继续考察,每半年一次,不超过5年,为该药品审定使用期限提出依据。(2)1999年底颁布的“中药新药质量稳定性研究技术要求“,其对稳定性的要求与1992年技术要求内容基本相同。稳定性试验结果、有效期的确定,仍以常温下为准。(3)仿制药及增加规格品种,稳定性研究参照新药要求。由于申报时间较短,在提供常温稳定性资料时应同时申报3~6个月加速稳定性试验资料,以暂定有效期。但应继续进行常温试验考察,以常温下为准,最终确定有效期。2.中药稳定性研究状况从上世纪50年代开始,人们对化学药制剂的稳定性进行研究至今已积累了不少丰富的资料和经验,对考察药物制剂的质量、确定有效期、保证临床疗效的发挥起了积极的作用。中成药稳定性研究工作是从液体制剂开始的,且多为单方制剂。最先报道…的是对威灵仙注射液中原白头翁素稳定性的研究。经考察pH值、温度、光线、添加剂等因素对原白头翁素的稳定性均有影响。通过对恒温加速试验数据处理后,认为原白头翁素的化学动力学为伪一级反应,预测有效期t25℃0.9为2.3d。近10余年来,对这方面的研究引起了药学界的普遍重视,有关研究报告逐年增多,研究水平不断提高,尤其在利用稳定性研究来筛选处方、优化工艺、预测有效期等方面取得了可喜的成绩。由于液体制剂溶液的颜色、澄明度等对pH值、温度、光线、添加剂等因素较敏感,经常出现颜色变化、产生沉淀等问题,经研究不仅是物理的变化,还有化学的变化,从而影响到药效的变化,这就促使液体制剂稳定性研究的发展。由于液体制剂的稳定性影响因素较多,不容易控制,所以对液体制剂稳定性的研究报道较多,研究的范围亦较广。固体、半固体制剂一般较液体制剂稳定,但也存在不稳定的问题,且比液体制剂复杂,近几年研究报道亦在逐年增加。由于中药成分的复杂性,1992年《补充规定》要求必须报送稳定性研究资料以来,新药研究中稳定性研究工作向规范、研究内容深度和广度迈进了一大步。1999年又颁布了稳定性技术要求。但中药稳定性研究中仍存在着一些需进一步探讨的问题。如:考察稳定性指标的选择、复方中各成分相互干扰的问题,辅料对稳定性的影响及反应机理等,有些试验方法尚需进一步完善。3.目前存在的主要问题现阶段申报的稳定性资料中仍存在着以下问题:(1)没有说明包装材料的材质及包装情况;(2)没有说明稳定性试验储存条件;(3)0月考察时间表达不准确,开始考察时间应在样品制备后一个月之内,以开始考察的结果作为O月结果;(4)没有按质量标准及制剂要求进行全面检查;(5)对于中药新药注册分类l、5类原料药没有对高温、高湿等与储存条件有关的影响因素进行考察;(6)稳定性考察所用样品不是中试生产样品;(7)没有提供包装材料对药品稳定性影响的研究资料等。
论坛中有需要GB/T 1573-2001《煤的热稳定性测定方法》的,现分享给大家。
[font=微软雅黑, sans-serif]1 [/font][font=微软雅黑, sans-serif]引言[/font][font=微软雅黑, sans-serif]在计量检定规程《JJG 700-2016 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]》中,[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]的计量性能要求主要包括载气流速稳定性、柱箱温度稳定性、程序升温重复性、基线噪声、基线漂移、灵敏度/检测限、定性重复性和定量重复性等。其中,基线噪声、基线漂移、灵敏度/检测限用以表征检测器的性能指标;载气流速稳定性、柱箱温度稳定性、程序升温重复性、定性重复性和定量重复性则用以表征仪器整体性能。[/font][font=微软雅黑, sans-serif]载气流速稳定性一方面影响色谱峰的流出时间,影响定性重复性;另一方面会影响进样时的样品汽化和分流过程,影响定量重复性;再则,对于热导池检测器(TCD)、电子捕获检测器(ECD)等浓度型检测器,载气流速会影响峰面积,也会影响定量重复性,因此尤其需要进行测定。本文介绍依据《JJG 700-2016 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]》测定[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]载气流速稳定性的方法、工具和结果分析。[/font][font=微软雅黑, sans-serif]2 [/font][font=微软雅黑, sans-serif]载气流速稳定性的测定[/font][font=微软雅黑, sans-serif]2.1 [/font][font=微软雅黑, sans-serif]载气流速稳定性的测定要求[/font][font=微软雅黑, sans-serif]依据《JJG 700-2016 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]》的要求,在仪器安装有热导池检测器(TCD)、电子捕获检测器(ECD)时需要测定载气流速稳定性。[/font][align=center][img]https://img.antpedia.com/instrument-library/attachments/wxpic/d6/f5/bd6f5114b371f075b851307475b87bf4.png[/img][/align][font=微软雅黑, sans-serif]测定方法和要求为[/font][font=微软雅黑, sans-serif]:选择适当的载气流速,待稳定后,使用流量计在10min内连续测量7次,以7次测量平均值的相对标准偏差为载气流速稳定性的测定结果;使用热导池检测器(TCD)和电子捕获检测器(ECD)时,测定的载气流速稳定性数值,均要求≤1%。[/font][font=微软雅黑, sans-serif]在仪器检定的不同情况下是否需要进行载气流速稳定的测定,可以参考《JJG 700-2016 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]》5.3项,下图:[/font][align=center][img]https://img.antpedia.com/instrument-library/attachments/wxpic/90/4c/7904cbf5c04a614f8acbafd95a2ca01d.png[/img][/align][font=微软雅黑, sans-serif][/font][font=微软雅黑, sans-serif]2.2 [/font][font=微软雅黑, sans-serif]载气流速稳定性的测定工具[/font][font=微软雅黑, sans-serif]测定时,需要使用经过计量检定过的皂膜流量计(或者其他类型流量计),以及秒表,下图:[/font][align=center][img]https://img.antpedia.com/instrument-library/attachments/wxpic/8c/5c/08c5cf17306605cebb27fe93fc18938c.png[/img][/align][align=center][img]https://img.antpedia.com/instrument-library/attachments/wxpic/b7/31/6b731651e2d07427de82f3319ab7c593.png[/img][/align][font=微软雅黑, sans-serif][/font][font=微软雅黑, sans-serif]2.3 [/font][font=微软雅黑, sans-serif]载气流速稳定性的测定步骤[/font][font=微软雅黑, sans-serif]以测定热导池检测器(TCD)为例,介绍载气流速稳定性的过程:[/font][font=微软雅黑, sans-serif]1[/font][font=微软雅黑, sans-serif]) 准备好[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]和秒表、皂膜流量计和记录本;设定合适的载气流量从TCD检测器中通过(建议20 ml/min -30ml/min);[/font][font=微软雅黑, sans-serif]2[/font][font=微软雅黑, sans-serif]) 将皂膜流量计连接在TCD检测器载气出口处,测量载气流速;点击链接,了解皂膜流量计的使用方法:[url=https://ibook.antpedia.com/x/541772.html][color=#7030a0]如何使用皂膜流量计测量[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]的相关流量[/color][/url]。[/font][align=center][img]https://img.antpedia.com/instrument-library/attachments/wxpic/b7/f3/0b7f3455f7602d622070d94b7b45ed11.png[/img][/align][font=微软雅黑, sans-serif][/font][font=微软雅黑, sans-serif]3[/font][font=微软雅黑, sans-serif])按照步骤2)的操作方法,连续测量七次,记录数据,填入下表;并以7次测量平均值的相对标准偏差为载气流速稳定性的测定结果:[/font][align=center][img]https://img.antpedia.com/instrument-library/attachments/wxpic/26/90/b26908d25524c8a0ea12f50835b81974.png[/img][/align][font=微软雅黑, sans-serif][/font][font=微软雅黑, sans-serif]3 [/font][font=微软雅黑, sans-serif]小结[/font][font=微软雅黑, sans-serif]载气流速稳定性的测定较为简单,其关键是设定合适的载气流速从检测器中流过,并掌握皂膜流量计的正确使用方法[/font]

我是高校制药工程实验室的实验技术人员,从业13年。目前,实验室有各种设备200余台(套),主要涉及的是压片机、制粒机、包衣机、均质机、纳米粒度仪、水分测定仪、崩解仪、溶出仪、透皮测定仪、紫外分光光度计、液相、[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]、[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]、旋蒸、搅拌器、离心机、培养箱、超净台等各种制剂制造、质量检测、合成等方面的仪器设备。制药工程专业人才培养需要的相关设备基本齐备。 (图源于网络) 这些设备是经过数次集中采购陆续进入实验室的。现有设备总价值约六百余万元,其中国产设备占台套数的九成,但是价值只占到六成。国产设备主要是合成设备、制剂设备等,比如搅拌器、压片机等;进口设备主要是分析仪器,比如紫外、液相、[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]、粒度仪等精密高值设备。[align=center][img=,690,460]https://ng1.17img.cn/bbsfiles/images/2021/10/202110281631240292_2744_2977147_3.jpg!w690x460.jpg[/img][/align][b][color=#ff6666] 国产和进口设备的差别 [/color][/b]说到国产和进口设备的差别,印象最深刻的是紫外分光光度计。实验室现有紫外12台,其中5台日本产、1台德国产、4台上海产(来自两个厂家)、2台北京产,单价从1万到8万不等。德国产最贵,资历也最老,2007年开始使用,至今正常。紫外分光光度计是较成熟的设备,国内生产厂家很多。在仪器信息网上搜索紫外分光光度计,厂商有数百个。我们有一个实验“双波长法测定磺胺甲恶唑片含量”,见图。这个实验要求设备稳定,具体对应的仪器参数是重复性和基线稳定性,背景物质在两个波长下的吸光度应相同。国产的6台设备中,两台价值较高的是可以满足实验要求的,但这个稍微好点的设备却没有办法长时间保持基线稳定,比如开机8小时,基线直接飘到3上了,需要重复开关机操作,性能没有办法与进口商品抗衡。[align=center] [img=,690,567]https://ng1.17img.cn/bbsfiles/images/2021/10/202110281630584481_7140_2977147_3.jpg!w690x567.jpg[/img][/align][color=#ff6666][b]国产精密的科学仪器发展,道阻且长[/b][/color] 作为科学仪器的消费主力之一,高校是希望买到好用又便宜的国产设备的。毕竟,相对于进口设备,国产设备采购手续更简单。今年,我们壮着胆子买了几台国产液相,接触了5-6家厂商,比较震惊的一个事情是,国产液相只有紫外检测器,没有二极管阵列检测器,接触的几个厂家中只有一家可以提供一个进口的PDA可选件。在精密的科学仪器领域,我们国家仍处于远古时代,非常的弱,前方道阻且长。 国产设备跟进口设备之间不仅仅是技术的断崖式差距,更是包括销售、售后、技术、品控、生产等一系列的巨大差距,希望从业者们乘着政策的东风,扶摇直上青云,如家电行业一样,做大做强,让我们这些使用者可以发自内心的愿意购买和使用国产科学设备。
做[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]的PQ性能确认 是氢化法做的做元素砷 ,先要做个基线稳定性 要求测定60次 看他的漂移值应不大于2%,那问一下各位老师,做这个基线稳定性之前需要进标样吗,是做出来那个标曲后再做基线稳定性吗
近日测白银中的Si发现稳定性差,连测几次,一次比一次的值低,功率1.2Kw,等离子气流量15L/min辅助气1.5L/min,雾化气流量0.9L/min,请各位指教,那位有测Si 的方法?
紫外中二个参数噪声的定义:无样品时仪器自身的波动。测定方式:在时间扫描方式下,500nm波长连续测量120s,由所记录的吸光度--时间光谱图峰,峰值即为仪器的噪声。稳定性的定义:是指不放样品的情况下,零吸收读数在一定时间内偏离的程度。(1小时内仪器自身的漂移量)。测定方式:在时间扫描方式下,仪器预热啊2小时,于500nm波长处连续测量一小时,由所记录的吸光度--时间光谱图峰,峰值检测仪器的稳定性。感觉噪声就是稳定性,只是测量时间不同而已。不明白二者本质区别在哪里?
看到书上讲到在新的FTIR到货后,其中一项是要检测FTIR的稳定性,方法是仪器稳定后,用4cm-1的分辨率测定100%(透过)线,每隔10分钟测定一次,共测定六次,将6次测定得到的100%线用共同坐标画在一张图上,如果6次测定的基线重复,而且基本很平,说明仪器在此50分钟时间内,重复性和稳定性比较好。问题:这个基线的测定是不是和测定样品的红外光谱方法一样,先测背景,然后测再继续测100%线?另外,是不是每次测100%线时都要先进行一次背景扫描?我们这里的红外一般是半天扫描一次背景,不过FTIR是放在恒温恒湿房间里。
按照光谱检定规则:1.A级 B级仪器短程稳定性RSD/% 2.0 4.0仪器长期稳定性RSD/% 4.0 8.0性能低于B级的,不能用于公证数据测试。2. 一般验收时的两个稳定性要求:短期稳定性:repeat n=10 RSD0.5%长期稳定性:repeat/10min,n=24 RSD2%你的ICP-OES稳定性如何?
[align=center][b]记一次成功的全血稳定性试验[/b][/align]本周已经是第五次做右佐匹克隆全血稳定性试验了,由于此药非常不稳定,因此全血稳定性数据很重要,牵扯着我们在血浆中测定的药物浓度是否为真正的右佐匹克隆在人体全血中的含量。前几次做全血稳定性得出一个结论,这个试验还是很费柱子的,我们有一根资生堂CAPCELL PAC MGIII的色谱柱被堵塞了。由于全血需要在水浴中孵育3个小时,存在红细胞破裂的现象,导致3小时的全血离心后真实存在为暗红色血浆,这样极大的影响了后续的血浆样本处理,进而堵塞色谱柱。关于具体实验步骤可浏览我之前发的分享帖:浅谈[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS药动学方法学考察中的全血稳定性实验[url=https://bbs.instrument.com.cn/topic/7346669_1][color=#0000ff]https://bbs.instrument.com.cn/topic/7346669_1[/color][/url]。而本次分享主要分析结果数据。右佐匹克隆的主要水解产物和代谢产物均为ACP,此物质也是代谢产物的水解产物,而如何保持右佐匹克隆这个药物在样品处理过程中稳定存在,是我们的实验目的和基础,那么同时测定ACP的含量即可验证这一目标。在此次实验中,我们做了两组对照实验,一组是空白全血,加标准溶液后孵育;另一组则是加了“秘方”的全血,加标准溶液孵育。到了特定的时间,我们模拟人体取血的过程,将孵育了一段时间的全血取出,在离心机4000rpm离心取血浆,后样品处理。最终得到的结果如下图所示。我们可以发现ACP的含量在最低定量限以下,且是20%以下。并且空白存在小吸收的干扰,可以证明ACP在30分钟内不会因样品降解和水解而产生。且不会对右佐匹克隆药物含量测定的真实性产生影响。但我们同时发现,右佐匹克隆的含量却随时间的延长而增加,那么原因在哪里呢?是没有充分混匀吗?我们在取血前会在轻微振荡器上震荡。当我们咨询教授后才了解,可能是随着时间的推移,我们的红细胞破裂,从而产生基质影响右佐匹克隆的含量。那么今天的分享到这里就结束了,感谢仪器信息网提供原创大赛平台让我互相学习分享!有老师专家对我的实验产生疑惑,可以在底部留言。[img=,690,378]https://ng1.17img.cn/bbsfiles/images/2019/10/201910241049225558_3661_3255306_3.png!w690x378.jpg[/img]
环境微生物学提到, 细菌在液体培养基中存在稳定性和不稳定性。稳定性的成为S型,为光滑型,周身亲水,在液体培养基成均匀分布。不稳定性的成为R型,成为粗糙型,呈现脱离液体的趋势,多沉淀到底部。那么,居于稳定或不稳定性这一理论,在污水活性污泥法工艺中,曝气池末端的活性污泥应该为不稳定性状态,才便于在沉淀池中易絮凝沉淀。但是,活性污泥的核心是菌胶团,而菌胶团是由能形成荚膜的细菌粘附到一起并形成公共荚膜的形成体。既然是外围是公共荚膜,那么菌胶团就应该是亲水的,怎么才能成为R型呢?有点疑惑,请高人赐教。