QIAcuity数字PCR为您的基因细胞治疗研究保驾护航
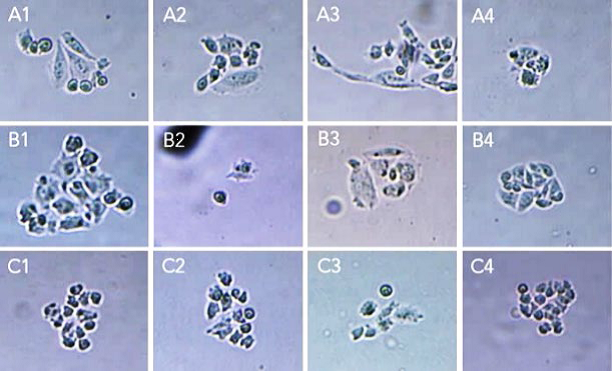
基因治疗是将外源功能基因导入人体靶细胞,以纠正或补偿基因缺陷和异常所导致的疾病,达到治疗目的的新型疗法。根据其治疗途径的不同,基因治疗可分为体内治疗和体外治疗。与基因治疗不同的是,细胞治疗则是利用患者自身或供体的活细胞,经体外改造后回输患者体内,替换受损细胞、病变细胞或刺激人体免疫反应和再生,从而达到治疗疾病的目的[1]。目前,基因细胞治疗有望从根本上治愈肿瘤、遗传病和感染性疾病等常规疗法不能解决的疾病。得益于生物技术的进步和相关政策的利好,基因细胞治疗技术正在迅速发展,同时也面临诸多挑战。我国《细胞治疗产品研究与评价技术指导原则(试行)》指出[2],无菌检测、支原体检测、内毒素检测、细胞存活率、总细胞数量、病毒载体滴度/纯度、效应细胞比率、CAR转导/转染效率、CAR基因拷贝数、复制型病毒残留等质控指标必须通过严格测试,以保证相关产品的安全和有效性。细胞治疗质控流程基因治疗质控流程质量控制贯穿于整个基因细胞治疗的研发和生产过程,如何确保和提高质量控制的精准性是基因细胞治疗的成功研发和顺利生产的关键。与传统荧光定量PCR技术相比,数字PCR作为一种可精准实现核酸分子绝对定量的新技术,已被广泛应用于载体构建、细胞转染/病毒包装、污染监测和生物分布等完整的质控过程,为基因细胞治疗相关产品的成功研发和安全生产保驾护航[3]。自动化的质控检测是提高基因细胞治疗产品安全性和质量可控性的重要途径之一。质控检测的自动化不仅可以减少不同批次产品间的差异变化和交叉污染,还可降低时间成本。QIAcuity集成式纳米微孔板的数字PCR系统,将微反应体系制备、PCR扩增和数据分析集成到全自动仪器中,整个流程只需一步手工操作即可在2小时内快速获得实验结果。在提升检测速度和操作简便性的同时,也最大程度减少由于人工操作不当等外界因素引入而导致的实验误差。如何确保和提高基因细胞治疗的安全性、有效性和一致性是开发基因细胞治疗产品亟待解决的问题。QIAcuity dPCR系统作为一种全自动化的基因细胞治疗产品质控工具,结合经优化设计的高度特异和灵敏dPCR Assays,可精准实现支原体和残留宿主细胞等污染物的单拷贝检出以及重复展现病毒载体的拷贝数(95%的置信区间,CV<10%),更大程度提高基因细胞治疗产品的安全性和有效性[4]。10x梯度稀释的CAR-T细胞线性关系(LOD为0.13copies/ul)dPCR检测载体拷贝数一致性评估(a样本CV值为3%;b样本CV值为4%)在基因细胞治疗的整个质控流程,QIAGEN可实现CD3、CD28和ICOS等外源目的基因、AAV病毒滴度、残留宿主细胞、总细胞量、支原体和大肠杆菌的检测,所有Assays均经过严格的湿实验验证,确保其检测特异性和灵敏度。细胞治疗应用基因治疗应用参考文献1. B Furuta-Hanawa,T Yamaguchi,et al.Two-Dimensional Droplet Digital PCRas a Tool for Titration and Integrity Evaluation of Recombinant Adeno-Associated Viral Vectors[J]. Human gene therapy methods,2019,30(4):2. 食药监总局发布细胞治疗产品研究与评价技术指导原则[J].中国医药生物技术,2018,13(01):47.3. X Dai,Y Mei,et al.Standardizing CAR-T therapy:Getting it scaled up[J]. Biotechnology advances,2019,37(1):4. Lu Alex,Liu Hui,et al. Application of droplet digital PCR for the detection of vector copy number in clinical CAR/TCR T cell products[J]. Journal of translational medicine,2020,18(1):END