推荐厂家
暂无
暂无
 银牌6年
银牌6年
 400-860-5168转4231
400-860-5168转4231
 留言咨询
留言咨询
 银牌4年
银牌4年
 400-860-5168转4836
400-860-5168转4836
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-860-5168转2623
400-860-5168转2623
 留言咨询
留言咨询

 400-860-5168转2623
400-860-5168转2623
 留言咨询
留言咨询

 400-860-5168转2623
400-860-5168转2623
 留言咨询
留言咨询

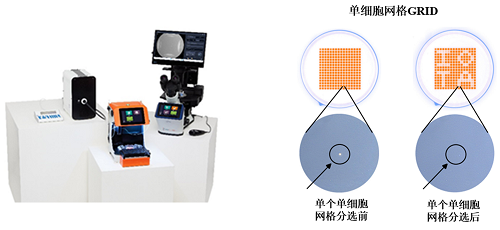
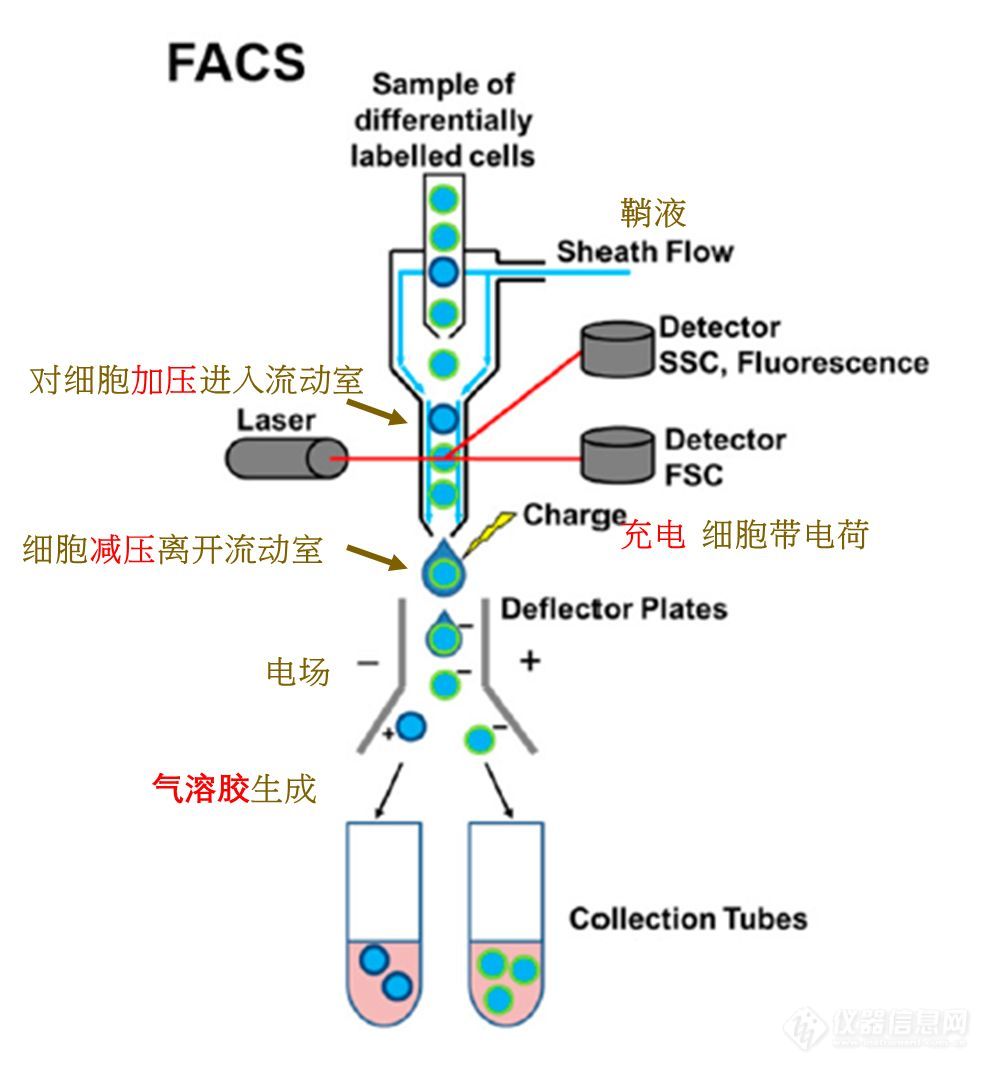



[size=15px][color=#333333]细胞的机械特性对其生物学功能(如增殖、分化和凋亡)和形态状态(如迁移、附着和病理状态)至关重要。目前常用的细胞弹性模量测量技术包括原子力显微镜、微管吮吸、光镊和磁镊等。这些技术可以有效测量单个细胞的机械性质,但是通量低,限制了其实际应用。[/color][/size][size=15px][color=#333333]近年来,微流控芯片因其在小体积液体操控方面的独特优势,也被用于测量细胞弹性模量。现有的微流控芯片主要侧重于平台开发,虽然通量大幅提高,但很少将测量后的细胞进一步收集以实现后续分析。[/color][/size][size=15px][color=#333333]单细胞分析技术的发展要求能够准确地打印单个细胞。传统单细胞打印技术包括荧光激活细胞分选、有限稀释和手动细胞挑选,这些方法打印效率较低且难以实现自动化。[/color][/size][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#333333]近年来,各种微流控技术被开发用于高通量精确打印单个细胞,如喷墨打印、精确分配、双阀门筛选和移液管式单细胞分离等。这些技术可以根据目标细胞的荧光、形态等特征进行识别并打印,但是大多技术难以获得单细胞的机械信息。[/color][/size][/font][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#333333]因此,本研究报道了一款基于 U 型阵列的微流控系统,集成了单细胞连续捕获,弹性测量和可寻址打印。该装置在研究细胞力学与其他生物学特性的关系方面具有强大的应用潜力。[/color][/size][/font][b]研究内容[/b][size=15px]近日,哈尔滨工业大学(深圳)[color=#004976][b]陈华英课题组[/b][/color]在英国皇家化学会(RSC)期刊[color=#004976][b] Lab on a chip[/b][/color] 上发表题为“Continuous trapping, elasticity measuring and deterministic printing of single cells using arrayed microfluidic traps” ([color=#007aaa]《单细胞连续捕获、弹性模量测量和可寻址分选打印》[/color])的研究论文,报道了一款创新的微流控芯片,实现了基于精确调节的压力对微球/细胞进行捕获和逐个打印,并将已知弹性模量的单细胞确定性地打印到孔板中(图 1)。[/size][size=15px]该论文第一作者是哈工大(深圳)在读硕士研究生[color=#004976][b]蔡逸珂[/b][/color]和硕士毕业生[color=#004976][b]余恩[/b][/color]。[color=#004976][b]陈华英副教授[/b][/color]为通讯作者。[/size][img=图片]https://img1.17img.cn/17img/images/202403/uepic/b3ebc9a4-6d42-4ef1-bfd0-c7cf1f5c3a15.jpg[/img]微流控芯片(图 1A)由冲洗入口、样品入口、打印入口、压力维持口和两个平行的主通道组成,下游有打印出口。在所有入口通道中设计了宽度从 200μm 减小到 25μm 的微通道阵列,以过滤介质中较大的颗粒/细胞碎片。如图 1A 和 B 所示,在每个主通道的一侧有 16 个 U 型捕获陷阱,且吮吸通道的高度比分流通道的高度低 15 μm,以保证细胞停留在 U 型陷阱中并诱导其微小变形。[img=图片]https://img1.17img.cn/17img/images/202403/uepic/b3ee5e4c-b99c-4b5e-8904-b5a6d2817633.jpg[/img][table=677][tr][td=1,1,5]▲[/td][td=1,1,549][b]图1[/b] 单细胞连续捕获、弹性测量和可寻址打印系统。(A)微流控芯片连接到压力泵,将单细胞精确分配到孔板中;(B)通过调节打印压力(Po)捕获(Pi-Po0)和释放(Pi-Po0)单个细胞的机制;(C)用于捕获和分离细胞的吮吸通道;(D)用于捕获和分离微球的分流通道。[/td][/tr][/table][来源:陈华英团队 RSC英国皇家化学会][align=right][/align]
[b][url=http://www.f-lab.cn/cell-analyzers/puncher.html][b]单细胞转移分离系统[/b][/url]是可用于单细胞转移,单细胞分离和单细胞隔离,单细胞成像应用的多功能单细胞分离操作仪器,它可以实现从微孔芯片转移单细胞到细胞收集管中。单细胞转移分离系统[/b][color=#666666]集单细胞成像,单细胞隔离,单细胞选择功能于一体,自动聚焦成像。[/color][b]单细胞转移分离系统转移单细胞到Eppendorf微管,PCR微孔板或其它反应微管中,[/b][color=#666666]在隔离单细胞后,它可以对选定收集的细胞进行扫描并成像。[/color][b]单细胞转移分离系统[/b][color=#666666]采用Nikon Ti-2倒置荧光显微镜,配备自动扫描显微镜载物台,自动聚焦器件,高灵敏度荧光CCD相机和LED激发光源组建而成。[/color][img=单细胞转移分离系统]http://www.f-lab.cn/Upload/single-cell-isolation.JPG[/img][b]单细胞转移分离系统[/b]特点完全自动化,步进系统高质量单细胞荧光成像单细胞分离的效率超过90% 超过70%分离的细胞增殖 分离后兼容所有的单细胞的WGA工具包(放大器的‐1,picoplex,复制‐G)实惠微Wells基于硅微孔微腔。由薄膜封闭70µ m,井底直径(1µ m),包含一个单孔。样品流体进入威尔斯并从底部的孔隙中流出。单个细胞被拖着走。一旦单个细胞降落到孔隙上,流动停止,其他细胞就不会进入井内。有用的细胞被识别出来。选定的细胞穿孔从微孔到384孔PCR板或离心管等等。单细胞转移分离系统:[url]http://www.f-lab.cn/cell-analyzers/puncher.html[/url]
[b][i]Deepcell周一表示,已与英伟达合作开发用于单细胞研究应用的生成人工智能技术。[/i][/b][align=center][b][i][img=image.png,113,83]https://img1.17img.cn/17img/images/202401/uepic/174b29e0-2f00-4d45-af22-8d08603d1fda.jpg[/img][/i][/b][/align][align=center][b][i][img=e763286044be6f856573c041d533273b_logo_with_R.jpg]https://img1.17img.cn/17img/images/202401/uepic/ee51f257-73e0-4f4c-beab-da55f87c445f.jpg[/img][/i][/b][/align]通过合作,公司将利用英伟达的计算专业知识和Clara一套专注于医疗保健的计算平台和软件,为基于细胞形态的分析应用程序构建新的算法,这些算法可以与Deepcell最近推出的REM-I高维细胞分析和分选平台等工具结合使用。Deepcell联合创始人、总裁兼首席技术官Mahyar Salek在一份声明中表示:“我们看到了将多模式和生成性人工智能融入我们的平台的多种可能性,并利用我们拥有的数十亿细胞图像的专有数据库来训练更多的人工智能模型。我们与英伟达的关系将帮助我们加快此类增强,并将这些进步带给我们的客户。”总部位于加利福尼亚州门洛帕克的Deepcell成立于2017年,是斯坦福大学的子公司,于2022年初筹集了7300万美元的B轮资金。Deepcell 是人工智能(AI)驱动的单细胞分析领域的先驱,旨在推动深度生物学发现,早在2023年2 月 6 日宣布,它已经发布了三个数据集,使研究人员能够探索新的高维形态数据。这些数据集是在 Deepcell 的高通量平台上生成的,该平台由成像和分选仪器、AI 模型和软件套件组成。Deepcell的首席技术官 Mahyar Salek曾经表示:“Deepcell的数据表明,深度学习可以实现较高的分类准确率,揭示了精确描述细胞特征和表型的新方法,并能够对感兴趣的细胞进行无标记分离,以进行进一步的深度分析。这项技术为生物医学界的科学家、转化研究机构和制药行业提供了一种新的工具,以从细胞形态学数据中获得对细胞的深度认识。”[b]关于 Deepcell[/b]Deepcell 是一家生命科学公司,它将 AI 引入细胞生物学,开启了称为形态组学的高维生物发现新领域。通过 Deepcell 的人工智能成像和微流体解决方案 REM-I 平台,该公司正在利用细胞形态学进行无限发现,从而实现新规模的细胞生物学研究和单细胞分析。Deepcell 的平台利用其 AI 模型,即人类基础模型,根据形态差异来识别和分类细胞,有助于推动基础和转化研究,并提供诊断测试和治疗靶向方面的未来应用。该公司于 2017 年从斯坦福大学分拆出来,已筹集近 1 亿美元的风险投资。[来源:仪器信息网译] 未经授权不得转载[align=right][/align]