能否请教下用液相色谱来检测多糖及多糖的氧化和还原态的方法?另外我对液相色谱仪的使用还不是特别了解,希望能知道更多有关仪器使用的方法和其需要的注意事项。谢谢!
有人做过液相色谱测定糖含量的吗??不管是多糖还是单糖。我目前想测定一个原料原料为酵母细胞壁多糖(主要为葡聚糖和甘露糖)目前现有的试验条件为 氨基柱、示差检测器/C18柱,紫外检测器;望有做过的能提供些方法参考下,谢谢
有谁知道葡萄糖中葡萄糖含量的检测方法。(不包括液相色谱检测法)请知道的帮个忙哈。谢谢!
液相方法开发和色谱柱选择,检测糖的仪器方法和色谱柱选择如你们喜欢,可以加入我们的小团队。 名为:shooter 团队里面有大学的教授(帅气的老外教授(我们的最终决策人)),各个地方的检验人员,和对液相感兴趣的年轻朋友。我们团队现在的进程是讨论液相色谱的条件,通过我们来把一些在液相上分析时间长的旧方法改为快速高效的方法(必须要成为实例)。 希望你们的加入,具体方法在论坛留言给我,我会尽快回复你们。 我们需要的你是能和我们融合为一个Team!

高效液相色谱法测定白酒中糖精钠的方法探讨摘要 本文主要参照GB5009.28-2016标准从三个方面:改变流动相配比、改变色谱柱、改变液相色谱的检测器,运用高效液相色谱法将白酒特别是酱香型白酒中存在的干扰糖精钠检测的物质:糠醇、糠醛得以分离,以达到对白酒中糖精钠准确测定的目的。关键词 白酒;参照GB 5009.28-2016标准;糖精钠;糠醇;糠醛[b]1 前言[/b]白酒是深受人们喜爱的一种饮料,近年来有一些不法商家为了改善白酒的口感,会人为的添加糖精钠等非法甜味剂,糖精钠在GB2760-2014[sup][/sup]中明确规定为不得使用。因此,国抽、省抽等监督指令性任务中有要求检测白酒中是否有违规添加糖精钠的项目。糖精钠的检测依据为GB5009.28-2016[sup][/sup],依此法检测白酒这类样品时,常常会在糖精钠标准溶液的出峰时间附近出现“假的色谱峰”而液相色谱法是根据保留时间进行定性的,由此造成误判。由于白酒为粮食类原料经微生物发酵、酿造而成,成分复杂。有的酒中含有香味物质:糠醛、糠醇,特别是酱香型白酒[sup][/sup]。糠醛、糠醇与糖精钠结构相近,均为带呋喃环类的物质,极有可能产生干扰糖精钠定性的色谱峰。下面通过三个方面:改变流动相配比、改变色谱柱、改变液相色谱的检测器来将糠醛、糠醇与糖精钠得以有效的分离,并通过PDA检测器来验证白酒中确实存在着糠醇、糠醛,从而提高糖精钠检测结果的正确性。[b]2 实验方法与材料2.1 标准物质、样品[/b] 糖精钠标准溶液浓度:1.00mg/mL,(中国计量科学院,证书号: GBW(E)10080);糠醛、糠醇,分析纯,购于安谱公司;色谱纯甲醇、优级纯乙酸铵,购于国药集团;密理博超纯水:自制;酒样品(监督抽样,有清香型,浓香型,酱香型,兼香型白酒)[b]2.2 仪器及设备[/b]电子天平:AL-204; 恒温水浴锅:上海精密科学仪器有限公司; Waters e2695 HPLC(配紫外检测器及PDA检测器);色谱柱A:ZORBAX SB-C18:4.6mm×250mm, 5um;色谱柱B:Sunfire C18:4.6mm×250mm, 5um[b]2.3 实验方法 [/b]酒样经水浴加热去除酒精度后,补足蒸发去除的水份,然后直接进色谱分析。色谱条件A:依GB 5009.28-2016 《食品安全国家标准 食品中苯甲酸、山梨酸和糖精钠的测定》:液相色谱条件:流动相:甲醇:0.02mol/L乙酸铵=5:95; 色谱柱A ;流速:1.0mL/min;进样量:10uL;检测器:紫外检测器,230nm;色谱条件B:将方法A中的流动相:甲醇:0.02mol/L乙酸铵=5:95调整为甲醇:0.02mol/L乙酸铵=3:97;其余条件一样; 色谱条件C:将方法A中的色谱柱A改为色谱柱B,其余条件一样; 色谱条件D:将方法C中的紫外检测器改为PDA检测器,其余条件一样,主是是对糠醛、糠醇、糖精钠进行光谱扫描,看它们的光谱图是否相似,以利于对它们进行准确定性;[img=,690,223]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011345_01_2166779_3.png[/img][img=,690,307]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011345_02_2166779_3.png[/img]图2 糠醇、糠醛、糖精钠混合标准溶液色谱图(色谱条件A)[img=,690,253]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011351_01_2166779_3.png[/img][img=,690,265]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011351_02_2166779_3.png[/img][img=,690,254]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011351_03_2166779_3.png[/img][img=,690,276]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011351_04_2166779_3.png[/img][img=,690,253]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011351_05_2166779_3.png[/img][img=,690,267]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011351_06_2166779_3.png[/img] 图3 酱香型白酒测定色谱图(色谱条件A)[b] 从图2可以看出:糖精钠、糠醛、糠醇在色谱条件A下,它们的保留时间非常接近,前言中也提到白酒为粮食类经微生物发酵酿造、蒸馏而成的,成分复杂,极有可能产生微量的糠醇、糠醛干扰糖精钠的测定,因此本文通过改变色谱条件,尝试着将糠醇、糠醛、糖精钠得以有效分离,以达到对白酒中糖精钠的准确测定。3.2 改变色谱条件 [/b]在现有的实验条件下,采用色谱条件B,通过改变流动相中的甲醇比例,来尝试糠醇、糠醛、糖精钠能否达到基线分离,由于甲醇在流动相中的比例越高的话,糠醇、糠醛、糖精钠在C18柱反相色谱中应该是出峰时间更快的,因此为了尽量使三者分离,应该减少流动相中的甲醇比例,采用色谱柱耐受甲醇的极限比例:甲醇:0.02mol/L乙酸铵=3:97进行实验,结果见图4~5。[img=,690,289]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011354_01_2166779_3.png[/img][img=,690,288]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011354_02_2166779_3.png[/img][img=,690,289]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011354_03_2166779_3.png[/img][img=,690,291]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011354_04_2166779_3.png[/img] 图4 糠醇、糠醛、糖精钠混合标准溶液色谱图(甲醇:0.02mol/L乙酸铵 = 8:92 )[img=,690,253]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011356_01_2166779_3.png[/img][img=,690,227]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011356_02_2166779_3.png[/img] 图5 糠醇、糠醛、糖精钠混合标准溶液色谱图(色谱条件B即甲醇:0.02mol/L乙酸铵 = 3:97 )从图5可以看出:该方法虽然也能将糠醇、糠醛、糖精钠三者实现基线分离,由于流动相中缓冲盐的比例高,运行时间长了,会极大地缩短色谱柱的使用寿命,为此根据实验室的条件, 尝试更换色谱柱及检测器,根据GB 5009.28-2016 及色谱条件C、D进行实验,其结果见图6及图7。[img=,649,416]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011358_01_2166779_3.png[/img][img=,672,538]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011358_02_2166779_3.png[/img][img=,286,129]http://ng1.17img.cn/bbsfiles/images/2017/07/201707011359_03_2166779_3.png[/img] 图7 酱香型白酒样品的测定结果从图6可以看出:在色谱条件C下糠醇的出峰时间为18.15min、 糠醛的出峰时间为19.207min、而糖精钠的出峰时间则为24.875min;因此比较色谱条件A及色谱条件C,色谱柱A与色谱柱B同样为C18柱,但是由于它们之间填料的差异,虽然再同样的流动相下,还是会造成各化合物在色谱柱中有不同行为的。通过PDA检测器对三者进行光谱扫描,它们三者的光谱图也有明显的区别,因此在色谱条件C或D下能对白酒中的糖精钠进行准确定性,从图7可以看出白酒中的确存在着不同量的糠醇、糠醛这两种物质,干扰着白酒的糖精钠的测定。4 结论 本文主要参照GB 5009.28-2016标准从三个方面:改变流动相配比、改变色谱柱、改变液相色谱的检测器,运用高效液相色谱法将白酒特别是酱香型白酒中存在的干扰糖精钠检测的物质:糠醇、糠醛得以分离,以达到对白酒中糖精钠准确测定的目的。参考文献 GB 2760-2014 食品安全国家标准 食品添加剂使用标准[s] . GB 5009.28-2016 食品安全国家标准 食品中苯甲酸、山梨酸和糖精钠的测定[s] . 许汉英. 白酒中糠醛含量与香型之间关系的研究. 酿酒. 2002, 29 (5) : 37—39.[/s][/s]
如题,请问武汉哪里有测糖类的液相色谱呀,
[color=#444444]我想请问一下我用的液相色谱分离糖醇,检测器是ELSD,柱子是碳水化合物柱,流动相乙腈和水,可是我摸了很多条件,阿拉伯糖醇和木糖醇总是分不开,怎么回事啊? [/color]
[color=#444444]近来准备用高效液相色谱测葡萄糖的含量,第一次做这种实验,没有多少经验,忘大神指点啊!!!波长多少?流动相的选择?色谱柱?[/color]
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-2003,糖精钠的检测参照GB/T 5009.28-2003,即可开展实验。 苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。 2 样品前处理的注意事项 GB/T5009.28-2003和GB/T5009.29-2003 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。 食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。 GB/T5009.29-2003使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。 具体操作步骤如下: 取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。 用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。 3 检测仪器的选择 虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下: 3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。 3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。 3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。 4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。 该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。 如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。 在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。 糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。 5 选用液相色谱仪的注意事项 按照GB/T5009.29,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。 5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。 不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。 为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。 醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。
示差折光检测器[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url],用的是sugar-d的色谱柱,测蔗果三糖标准品,标准品是新拆的,用超纯水稀释的,水膜过滤,方法都是按照国标走的,但是跑出的峰只有四分钟左右一个小峰,按照国标蔗果三糖在16分钟出峰,浓度从大到小都试过了,一直不出峰,求大神指教。
示差折光检测器[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url],用的是sugar-d的色谱柱,测蔗果三糖标准品,标准品是新拆的,用超纯水稀释的,水膜过滤,方法都是按照国标走的,但是跑出的峰只有四分钟左右一个小峰,按照国标蔗果三糖在16分钟出峰,浓度从大到小都试过了,一直不出峰,求大神指教。
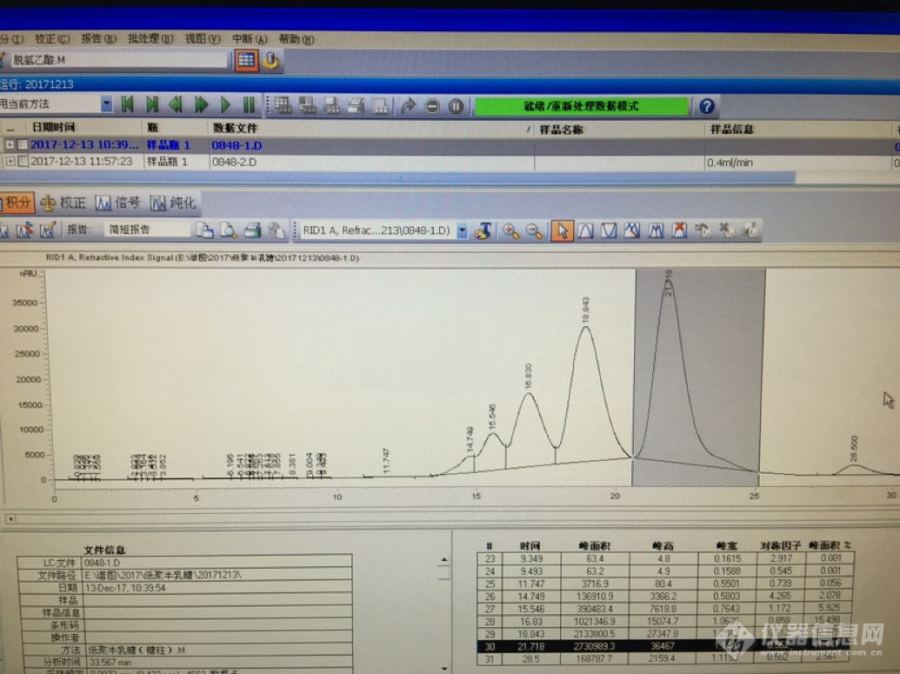
高效液相色谱使用钙型离子交换柱测低聚半乳糖,流动相是超纯水,柱温80℃,流速0.4ml/min。峰分不开怎么办?[img=,690,516]http://ng1.17img.cn/bbsfiles/images/2017/12/201712131552_01_3330811_3.png[/img]
不溶性糖精的高效液相色谱测定方法?请问用高效液相色谱法测定不溶性糖精的具体测量条件,如流动相、流速等,越详细越好,谢谢!!!!
请教用过高效液相色谱测定糖种类和含量,糖提纯都采用什么方法啊??
摘要糖精钠是有机化工合成产品,是食品添加剂。是一种甜味剂。除了在味觉上引起甜的感觉外,对人体无任何营养价值。相反,当食用较多的糖精时,会影响肠胃消化酶的正常分泌,使食欲减退。因此,糖精钠的含量的控制很有必要。为此南京科捷应用LC-600液相色谱仪器对糖精钠的分析方法进行了研究,可同时应用高效液相色谱法对橙汁、碳酸饮料中山梨酸、苯甲酸、糖精钠的含量进行检测,检测快速,结果准确可靠。关键词:食品添加剂 饲料添加剂饮料 糖精钠中山梨酸 苯甲酸 橙汁 甜味剂 液相色谱法1.苯甲酸、山梨酸、糖精钠(0.04mg/mL)高效液相色谱图http://ng1.17img.cn/bbsfiles/images/2011/05/201105311535_297105_2242538_3.jpg2.本方法的应用范围 1) 食品:冷饮、饮料、果冻、凉果、蛋白糖等 2) 饲料添加剂:猪饲料、香甜剂等 3) 日化行业:牙膏、嗖口水、眼药水等 4) 电镀行业:电镀光亮剂3.仪器配置检测项目苯甲酸、山梨酸、糖精钠本项目实验单位南京科捷分析仪器应用研究所实验仪器型号及配置LC-600液相色谱仪P600宝石恒流泵 1台UV600紫外检测器 1台7725i六通进样阀 1只WS600色谱工作站 1套[
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-1996,糖精钠的检测参照GB/T 5009.28-1996,即可开展实验。苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。2 样品前处理的注意事项 GB/T5009.28-1996和GB/T5009.29-1996 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。GB/T5009.29-1996使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。3 检测仪器的选择虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下:3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29-1996所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。5 选用液相色谱仪的注意事项 按照GB/T5009.29-1996,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。苯甲酸、山梨酸、糖精钠在液相上的出峰次序很有特点。在流动相5:95及以下比例时,次序是苯甲酸、山梨酸、糖精钠(注意一下[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的出峰次序),逐步增大甲醇含量,苯甲酸、山梨酸的出峰时间逐步提前,而糖精钠是出峰时间迅速提前,随着甲醇比例的逐步增大(15%-30%),原先在最后出峰的糖精钠集次和前面的山梨酸、山梨酸重叠,并位于最前面,其次序变为糖精钠、苯甲酸、山梨酸。再提高甲醇浓度,次序不变。用高甲醇比例条件(甲醇15%以上)做出的三种标准物质色谱图峰形较好,出峰时间也较快,但做实际样品时干扰较大;因此建议尽量使用低甲醇比例条件(甲醇5%左右)。6 苯甲酸、山梨酸超标时的判断苯甲酸、山梨酸超标的样品较多,由于它们往往牵涉到一批货物是否合格,因此责任重大。由于该方法定量较准确,因此遇到超标样品时应将精力集中于定性方面。如同时有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]和液相色谱仪,建议用这两种性质相差较大的仪器进行对照,如定量结果差不多,即可确认。如只有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],应利用其在填充柱保留时间稳定的特性,同时进五针标准液和五针样品液(注:峰面积应差不多,否则需对一方按比例稀释),如标准和样品液的保留时间相差时间超过1 秒,可认为不是。(如进针的技术不过关,请不要做此实验)如用液相色谱仪,当检测器为二极管阵列检测器时,根据保留时间和紫外吸收图结合定性,当只有紫外检测器时,改检测波长为220nm,230nm,250nm,重复进标准和样品液,由标准和样品在不同波长的峰高比值看是否吻合。如有微生物检测手段,可加样品于有菌培养基中,观察有无抑菌现象,如无抑菌现象则无防腐剂。不是很推荐用双柱法,因为有时柱极性相差不大,反而会影响最终判断。7 糖精钠超标时的判断当检测糖精钠超标时,除了采用二极管阵列检测器或波长验证,还可以利用糖精钠的荧光特性,用荧光检测器进行验证。荧光条件是激发波长为277nm,荧光波长为410nm。只有当用荧光检测器和用紫外检测器做出的定量结果相差不多,才可以判断为是。还有一个简单粗糙、却也行之有效的验证方法,即感官法。糖精钠是一种甜味剂,用舌头可以感觉到它的甜味,如果含量超标,一定能尝出来。8 标准溶液的配制贮存问题苯甲酸、山梨酸、糖精钠的标准溶液如用水、乙醇作基体,一般几个月后会严重降解,。如用甲醇溶解再放于冰箱冷冻层,可保持稳定一两年。因此推荐用甲醇作溶剂。在配制标准溶液时,初学者常犯的错误多为用甲醇溶解苯甲酸钠,用水溶解苯甲酸,晃了半天才发现怎么也不没溶解。应该用弱碱性水溶解苯甲酸钠、山梨酸钾,用甲醇溶解苯甲酸、山梨酸。9 苯甲酸、山梨酸的应用范围首先应注意到,并不是所有食品都需要加入防腐剂,只有那些富含营养物质,且需要长时间暴露于空气的才有这样的需要,否则对厂家来说会增加不必要的成本。酱油、酱料、咸菜、浓缩果汁等由于开封后不可能短期内吃完,月饼等需在货架上摆放,如不加防腐剂很快会发霉变质,有添加防腐剂的必要。而利乐装或易拉罐装的饮料由于很快可以食用完毕,即在细菌大量繁殖前己被消化了,因而没有添加的必要。苯甲酸、山梨酸如果要起到防腐的作用,含量就不能太低。如果我们检测样品时只有几个ppm的浓度,有可能是从原料中带来的或由其它添加剂转化来的,而不是厂家出于防腐目的加入的。苯甲酸、山梨酸也只是防腐剂中的两种。并不是所有需要加入防腐剂的食品都会添加苯甲酸、山梨酸,有可能使用防霉剂或其它种类的防腐剂,或自行规定需冷藏(如某些月饼)。因此有些食品检测不出也属正常。另外,我们应该比较清楚地理解苯甲酸与苯甲酸钠、山梨酸与山梨酸钾之间的关系。在食品中添加防腐剂通常以苯甲酸钠、山梨酸钾形式加入,它们不易汽化,易溶于水,但不溶于甲醇等有机试剂;而苯甲酸、山梨酸易汽化,易溶于有机试剂,但
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-1996,糖精钠的检测参照GB/T 5009.28-1996,即可开展实验。苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。2 样品前处理的注意事项 GB/T5009.28-1996和GB/T5009.29-1996 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。GB/T5009.29-1996使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。3 检测仪器的选择虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下:3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29-1996所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。5 选用液相色谱仪的注意事项 按照GB/T5009.29-1996,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。苯甲酸、山梨酸、糖精钠在液相上的出峰次序很有特点。在流动相5:95及以下比例时,次序是苯甲酸、山梨酸、糖精钠(注意一下[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的出峰次序),逐步增大甲醇含量,苯甲酸、山梨酸的出峰时间逐步提前,而糖精钠是出峰时间迅速提前,随着甲醇比例的逐步增大(15%-30%),原先在最后出峰的糖精钠集次和前面的山梨酸、山梨酸重叠,并位于最前面,其次序变为糖精钠、苯甲酸、山梨酸。再提高甲醇浓度,次序不变。用高甲醇比例条件(甲醇15%以上)做出的三种标准物质色谱图峰形较好,出峰时间也较快,但做实际样品时干扰较大;因此建议尽量使用低甲醇比例条件(甲醇5%左右)。6 苯甲酸、山梨酸超标时的判断苯甲酸、山梨酸超标的样品较多,由于它们往往牵涉到一批货物是否合格,因此责任重大。由于该方法定量较准确,因此遇到超标样品时应将精力集中于定性方面。如同时有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]和液相色谱仪,建议用这两种性质相差较大的仪器进行对照,如定量结果差不多,即可确认。如只有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],应利用其在填充柱保留时间稳定的特性,同时进五针标准液和五针样品液(注:峰面积应差不多,否则需对一方按比例稀释),如标准和样品液的保留时间相差时间超过1 秒,可认为不是。(如进针的技术不过关,请不要做此实验)如用液相色谱仪,当检测器为二极管阵列检测器时,根据保留时间和紫外吸收图结合定性,当只有紫外检测器时,改检测波长为220nm,230nm,250nm,重复进标准和样品液,由标准和样品在不同波长的峰高比值看是否吻合。如有微生物检测手段,可加样品于有菌培养基中,观察有无抑菌现象,如无抑菌现象则无防腐剂。不是很推荐用双柱法,因为有时柱极性相差不大,反而会影响最终判断。7 糖精钠超标时的判断当检测糖精钠超标时,除了采用二极管阵列检测器或波长验证,还可以利用糖精钠的荧光特性,用荧光检测器进行验证。荧光条件是激发波长为277nm,荧光波长为410nm。只有当用荧光检测器和用紫外检测器做出的定量结果相差不多,才可以判断为是。还有一个简单粗糙、却也行之有效的验证方法,即感官法。糖精钠是一种甜味剂,用舌头可以感觉到它的甜味,如果含量超标,一定能尝出来。8 标准溶液的配制贮存问题苯甲酸、山梨酸、糖精钠的标准溶液如用水、乙醇作基体,一般几个月后会严重降解,。如用甲醇溶解再放于冰箱冷冻层,可保持稳定一两年。因此推荐用甲醇作溶剂。在配制标准溶液时,初学者常犯的错误多为用甲醇溶解苯甲酸钠,用水溶解苯甲酸,晃了半天才发现怎么也不没溶解。应该用弱碱性水溶解苯甲酸钠、山梨酸钾,用甲醇溶解苯甲酸、山梨酸。9 苯甲酸、山梨酸的应用范围首先应注意到,并不是所有食品都需要加入防腐剂,只有那些富含营养物质,且需要长时间暴露于空气的才有这样的需要,否则对厂家来说会增加不必要的成本。酱油、酱料、咸菜、浓缩果汁等由于开封后不可能短期内吃完,月饼等需在货架上摆放,如不加防腐剂很快会发霉变质,有添加防腐剂的必要。而利乐装或易拉罐装的饮料由于很快可以食用完毕,即在细菌大量繁殖前己被消化了,因而没有添加的必要。苯甲酸、山梨酸如果要起到防腐的作用,含量就不能太低。如果我们检测样品时只有几个ppm的浓度,有可能是从原料中带来的或由其它添加剂转化来的,而不是厂家出于防腐目的加入的。苯甲酸、山梨酸也只是防腐剂中的两种。并不是所有需要加入防腐剂的食品都会添加苯甲酸、山梨酸,有可能使用防霉剂或其它种类的防腐剂,或自行规定需冷藏(如某些月饼)。因此有些食品检测不出也属正常。另外,我们应
成分:乙腈,水,少量葡萄糖,想检测其中葡萄糖的含量,用高效液相色谱可以吗?谢谢!
资生堂,化妆品生产企业中唯一的液相色谱从业者,液相色谱产品生产企业中唯一的化妆品从业者。这独特的双重身份使得资生堂先端科学事业推进部(Frontier Science)自2010年5月进入中国市场以来,一直热衷于推进中国化妆品检测能力,并进行了一系列的相关工作。2011年,中国食品药品检定研究院与资生堂集团技术交流会召开。2012年,资生堂与岛津合作启动HPLC化妆品分析系统研发工作。2013年,资生堂岛津HPLC化妆品分析系统开发完成,在北京、上海和广州召开新品发布会后,开展了试用和评估工作。2014年,资生堂岛津HPLC化妆品分析系统正式发售。2015年,新版化妆品安全技术规范征求意见稿发布,针对其中有关液相色谱分析的47个项目,资生堂FS技术中心已经完成了其中25项的实验工作,现将检测数据整理成册,希望能给您的工作带来帮助。具体的分析数据请下载附件查阅。
液相色谱检测糖精钠时如何使出峰时间提早?
检测中药中的多糖,皂苷,黄酮,木脂素用什么液相色谱柱?
[color=#444444]最近在做废水中甲醛的检测分析,参考相关文献,用DNHP衍生做的标准曲线效果非常不好。。求助各位虫子,哪里有甲醛液相色谱检测的标准啊,或者相应的方法告知一下,谢谢。。。就是检测未知水样中是否含有甲醛相关方法,谢谢。。。实验室条件有限,只有液相色谱,没有[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]和质谱。。。未知是否含有甲醛用分光光度法检测可以吗??[/color]
大家好,新手提个问题,我现在用安捷伦液相色谱1260测量果实中的糖组分,发现葡萄糖和山梨醇很难分开,我用的柱子是安捷伦的糖柱(ZORBAX CarbohydrateAnalysis Column),有懂得麻烦分享下方法,谢谢大家了
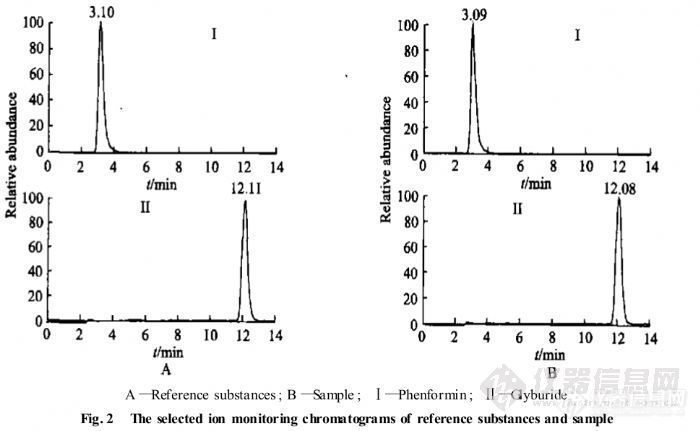
【作者】 董宇; 孔璋; 钟大放;【Author】 DONG Yu, KONG Zhang, ZHONG Da-fang(Laboratory of Drug Metabolism and Phamacokinetics,Shenyang Pharmaceutical University,Shenyang 110016, China)【机构】 沈阳药科大学药物代谢与药物动力学实验室; 沈阳药科大学药物代谢与药物动力学实验室 辽宁沈阳110016; 辽宁沈阳110016; 辽宁沈阳110016;【摘要】 目的建立检测中药降糖制剂中非法掺入的苯乙双胍和格列本脲专属性方法 ,并对若干市售药品进行检测。方法采用液相色谱 离子阱质谱联用法。选用DiamonsilC18柱 ,以乙腈 水 甲酸(V∶V∶V =6 0 0∶4 0 0∶0 1)为流动相 ,对中药降糖制剂的提取液进行液相色谱 离子阱质谱分析。通过与对照品的色谱及质谱行为相比较 ,对中药降糖制剂中非法掺入的合成降糖药进行定性鉴别。结果在 4种受试中药降糖制剂中 ,2种被检测到同时掺有苯乙双胍和格列本脲 ,1种被检测到掺有格列本脲。结论该方法选择性强 ,灵敏度高 ,可作为分析检测非法中药降糖制剂的有效方法 http://ng1.17img.cn/bbsfiles/images/2012/07/201207301530_380586_2379123_3.jpg
建立采用高效液相色谱-蒸发光散射检测(HPLC-ELSD)法同时测定大枣多糖酸性条件下水解产物中阿拉伯糖和D-半乳糖含量的方法。实验结果表明:制备的样品中阿拉伯糖和D-半乳糖分离良好,阿拉伯糖和D-半乳糖分别在2.00~10.00 μg(r2 = 0.9957)和2.08~10.40 μg(r2 = 0.9903)范围内呈良好的线性关系;平均加样回收率分别为103.87%(RSD = 5.42%,n = 9)和93.04%(RSD = 4.90%,n = 9)。该方法稳定性和重复性好,可为大枣质量评价和控制提供参考。
药典方法示例:[b]黄曲霉毒素测定法[/b]混合对照品溶液的制备:精密量取黄曲霉毒素混合标准品(黄曲霉毒素B1、黄曲霉毒素B2、黄曲霉毒素G1、黄曲霉毒素G2标示浓度分别为1.0μg/ml、0.3μg/ml、1.0μg/ml、0.3μg/m1)0.5ml,置10ml量瓶中,用甲醇稀释至刻度,作为储备液。精密量取储备液1ml,置25ml量瓶中,用甲醇稀释至刻度,即得。分别精密吸取上述混合对照品溶液5μl、10μl、15μl、20μl、25μl,注入液相色谱仪,测定峰面积,以峰面积为纵坐标,进样量为横坐标,绘制标准曲线。[b]硫酸依替米星[/b]第二法 照高效液相色谱法(通则 0512)测定测定法:取依替米星对照品适量,精密称定,分别加水溶解并定量稀释制成每1ml中约含依替米星1.0mg、0.5mg和0.25mg的溶液作为对照品溶液(1)、(2)、(3)。精密量取上述三种溶液各20μl,分别注入液相色谱仪,记录色谱图,以对照品溶液浓度的对数值对相应的峰面积的对数值计算线性回归方程,相关系数(r)应不小于0.99;[b]蜂蜜[/b]标准曲线的制备:分别精密称取果糖对照品1.0g,葡萄糖对照品0.8g,置同一具塞锥形瓶中,精密加入40%乙腈20ml,溶解,摇匀,作为果糖、葡萄糖对照品储备液。另精密称取蔗糖对照品0.2g,麦芽糖对照品0.2g,置同一具塞锥形瓶中,精密加入40%乙腈10ml,溶解,摇匀,作为蔗糖、麦芽糖对照品储备液。分别精密量取果糖、葡萄糖对照品储备液和蔗糖、麦芽糖对照品储备液,加40%乙腈配成不同浓度的果糖、葡萄糖、蔗糖、麦芽糖混合对照品溶液。精密吸取混合对照品溶液各15μl,注入液相色谱仪,分别测定。以对照品浓度为横坐标,以峰面积值为纵坐标,绘制标准曲线,计算回归方程。[b]制作方法总结如下:[/b]1.称一份对照品制备作为对照品储备液;2.稀释成系列梯度浓度,取相同的进样量上机检测或配制一份对照品溶液取不同的进样量。 有一个系统风险在里面,就是对照品如果称量不准确,整个标准曲线就不准确。一般外标法都要求配制两份标准溶液,标准曲线法也应该配制两份标准溶液,一份用于制作标准曲线,另一份标准溶液用于标准曲线的校验,以减少系统风险。最准确的方法应该是每一个标准浓度点都应从称量开始,但也是成本最高的方法。
[center]液相色谱测VFA的条件及方法[/center] 本人在做厌氧发酵实验,实验过程中产生的VFA是本实验的重点,因此需测其VFA组分,现在恳请各位高手帮忙教我如何通过液相色谱测其VFA组分,条件及步骤等,十分感谢!
求大神告知液相色谱仪检测吡啶的方法,谢谢!!!
想测混合液中有什么物质用什么方法想知道我染料废水的处理后的出水中的产物是什么。用什么方法测,液相色谱可以吗
请问各位大虾有谁知道苯丁锡的液相色谱监测方法