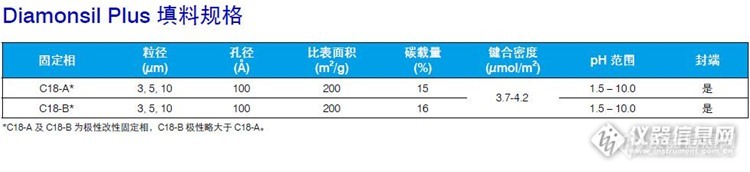
常规C18 色谱柱在高水相条件下长时间操作,经常会出现“柱塌陷” 现象,造成分析物的保留时间和分离度骤降。极性改性反相色谱柱由于采用独特的极性改性技术,通过引入极性基团使其表面更容易被水润湿,从而有效地避免了该现象的发生。此外,极性改性反相液相色谱柱在高有机相下表现同样出色,能在LC-MS 测试中加快去溶剂化的过程,从而有效提高LC-MS 的检测灵敏度。极性改性反相液相色谱柱的流动相适用范围可以从100% 水相到100% 有机相,使方法开发更加简单易行。极性改性反相色谱柱是以高纯硅胶为基质,采用独特的极性改性技术生产的色谱柱。这个系列的色谱柱不但保留了传统硅胶基质反相色谱柱的性能,而且又增加了一些新的特性:• 填料表面具有极性基团,适合于高水相条件下的分离• 增强了对亲水性、极性化合物的保留能力• 独特的选择性和优异的分离度• 降低了碱性化合物与残余硅羟基的相互作用,提高了色谱峰的对称性• pH 范围更宽,适合于分析酸、碱化合物迪马科技极性改性反相液相色谱柱有两个系列:一个是Spursil(思博尔)系列,包括Spursil C18 和Spursil C18-EP,二者的结构差异如下http://ng1.17img.cn/bbsfiles/images/2015/06/201506021619_548446_1610895_3.jpg一个是Diamonsil Plus 系列,包括Diamonsil Plus C18-A 及 Diamonsil Plus C18-B,Diamonsil Plus C18-B的极性略大约Diamonsil Plus C18-Ahttp://ng1.17img.cn/bbsfiles/images/2015/06/201506021624_548450_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/06/201506021624_548451_1610895_3.jpg
怎么判断一个物质的极性,是通过化学结构吗,有没有啥网址能够根据CAS号或结构查询物质的极性大小呀,正向色谱和反向色谱一般用来检测何种极性的物质(非极性,极性大。极性小),反向色谱中使用高清水系的色谱柱,说明物质极性大吗?[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]这块我一直把极性比作“相似相容”原理,物质极性大,那就采用极性大的柱子,然后再使用极性大的流动相洗脱?
如题:迪马科技极性改性的液相色谱柱有哪几款?很遗憾,今天没有人给出正确答案,今天没有人获得奖励了http://simg.instrument.com.cn/bbs/images/default/em09508.gif正确答案是 4 款Spursil C18Spursil C18-EPDiamonsil Plus C18-ADiamonsil Plus C18-B*******************************************************************************************************************************************今天看到了版友的质疑,也询问了出题者的意图,给大家统一回复一下:1. “迪马科技极性改性的液相色谱柱有哪几款?”出题者的意图是问:极性改性的反相色谱柱有哪几款?因为我们对于“极性改性色谱柱”的定义都是反相C18键合相引入极性基团(极性改性后)才称之为极性改性色谱柱;2. 关于HILIC色谱柱:是指固定相是强亲水性的极性吸附剂,如硅胶键合相(Platisil Silica)、氰丙基键合相(Platisil CN)、二醇基键合相(Inspire Diol)、极性改性键合相(Inspire HILIC)等都可以作为HILIC色谱柱使用;3. 我司关于HILIC色谱柱的描述是“Inspire HILIC柱采用了极性改性的固定相,能够在其表面形成一层富水层......”,如产品描述,此款色谱柱固定相也是极性改性的固定相,只不过极性改性是在硅胶上。虽然Inspire HILIC也使用了极性改性的固定相,但是它并不是对于C18色谱柱的极性改性,因此不能称之为极性改性色谱柱,而是HILIC色谱柱。因此,综上所述得出的结论即是:极性改性色谱柱是我司对反相C18固定相引入极性基团的一类色谱柱的称呼,而其他固定相即使也有极性改性,但不能称之为极性改性色谱柱(如Inspire HILIC)
液相色谱柱分为正相和反相,我想问他们除了极性强弱的和固定相的差别还有什么不同?洗脱程序呢?
[color=#444444]液相色谱中的流动相的极性参数P'有关的公式,不知哪位大神指教一下?[/color][color=#444444]例如甲苯的P'=0.29为流动相组分的调整保留时间为30分钟,如果改用乙醚P'=0.38为流动相,组分的调整保留时间是多少?[/color]
高效液相色谱仪的使用过程中,若遇到使用不当的情况,会大大缩短色谱柱的使用寿命。为了延长色谱柱的使用寿命,应对色谱柱进行适当的保护。 反相色谱柱在经过出厂测试后是保存在乙腈-水中的;由于色谱柱在储存或运输过程中固定相可能会干掉,这会引起键合相的空间结构发生变化。因此,新的色谱柱在用来分析样品之前,请一定要充分平衡色谱柱。反相色谱柱的平衡方法是:以纯乙腈或甲醇作流动相,首先用低流速0.2ml/min将色谱柱平衡过夜,然后,将流速增加到0.8mL/min冲洗30min以便将色谱柱的填料充分平衡至最佳状态。平衡过程中,将流速缓慢地提高直到获得稳定的基线,这样可以保证色谱柱的使用寿命,并且保证在以后的使用中,获得分析结果的重现性。请一定确保所使用的流动相和乙腈-水互溶。如果您所使用的流动相中含有缓冲盐,应注意首先用20倍柱体积的5%的乙腈-水流动相“过渡”,然后使用分析样品的流动相直至得到稳定的基线。 对于正相色谱柱来讲,硅胶柱或极性色谱柱需要更长的时间来平衡。这些色谱柱在出厂测试后是保存在正庚烷中的,如果极性色谱柱需要使用含水的流动相,请在使用流动相之前用乙醇或异丙醇平衡。当使用乙醇、异丙醇、乙酸等粘度大的流动相时,色谱柱的平衡时间要延长,甚至要加倍。
液相色谱仪由高压液体泵、检测器及液相色谱柱等三部分组成,其中液相色谱柱的正确安装和使用,是液相色谱工作的关键;也是液相色谱工作者获得正确可靠的实验数据的必经之路。 一、液相色谱柱的安装: 1、液相色谱柱的结构: a、空柱由柱接头、柱管及滤片组装而成。 柱接头采用低死体积结构,柱接头是两端螺纹组件,一端是为7/16英寸外螺纹,另一端是3/16英寸的内螺纹(国内外已规范化)。7/16英寸外螺纹与1/4英寸柱管(Φ6.35mm)连接,中间放置压坏用于密封。3/16英寸的内螺纹与1/16英寸(Φ1.57mm)的连接管连接,中间也放置压环用于柱接头的密封。为了尽量减少柱外死体积,在安装色谱柱时,用Φ1.57mm连接管通过空心螺钉压环后要尽量插到底,然后再拧紧空心螺钉。压环被空心螺钉挤压变形后紧箍在连接管上(连接管通过压环后露出的管长度应严格控制在2.5mm长或其他固定尺寸)。 在两端柱接头内,柱管两端各放置一片不锈钢滤片(或滤网),用于封堵柱填料不被流动相冲出柱外而流失。空柱各组件均为316#不锈钢材质,能耐受一般的溶剂作用。但由于含氯化物的溶剂对其有一定的腐蚀性,故使用时要注意,柱及连接管内不能长时间存留此类溶剂,以避免腐蚀。 b、柱填料: 液相色谱柱的分离作用是在填料与流动相之间进行的,柱子的分类是依据填料类型而定。 正相柱:多以硅胶为柱填料。根据外型可分为无定型和球型两种,其颗粒直径在3—10 µm的范围内。另一类正相填料是硅胶表面键合—CN,-NH2等官能团即所谓的键合相硅胶。 反相柱:主要是以硅胶为基质,在其表面键合十八烷基官能团(ODS)的非极性填料。也有无定型和球型之分。 常用的其他的反相填料还有键合C8、C4、C2、苯基等,其颗粒粒径在3—10 µm之间。 2[/font
液相色谱柱残留大的原因及解决方案
首先,要选择合适的色谱填料,就必须对此有一定的认识和了解,因为色谱填料的选择范围太宽了,分别为聚合物填料、硅胶基质填料和其它无机填料。 一、聚合物填料,聚合物填料多为聚苯乙烯—二乙烯基苯或聚甲基丙烯酸脂等,其优点是在PH值为1—14均可使用。这类填料具有较强的疏水性,而且大孔的聚合物对蛋白质等样品的分离非常有效。其缺点是相对硅胶基质填料,色谱柱柱效较低。 二、硅胶基质填料 1、正相色谱,正相色谱用的固定相通常为硅胶以及其他具有极性官能团胺基团,如(NH2,APS)和氰基团的键合相填料。由于硅胶表面的硅羟基或其他极性基团极性较强,因此,分离的次序是依据样品中各组分的极性大小,即极性较弱的组份最先被冲洗出色谱柱。正相色谱使用的流动相极性相对比固定相低,如正已烷,氯仿,二氯甲烷等。 2、反向色谱,反向色谱用的填料常是以硅胶为基质,表面键合有极性相对较弱官能团的键合相。反向色谱所使用的流动相极性较强,通常为水、缓冲液与甲醇、乙腈等的混合物。样品流出色谱柱的顺序是极性较强的组分最先被冲洗出,而极性弱的组分会在色谱柱上有更强的保留。常用的反向填料有:C18(ODS)、C8(MOS)、C4(Butyl)、C6H5(Phenyl)等。 三、其它无机填料,其它HPLC的无机填料色谱柱也已经商品化由于其特殊的性质,一般仅限于特殊的用途。 上面教了大家如何选择色谱填料,其实光选好色谱填料是不够的,我们还要选择填料粒度,下面就教大家如何选择填料粒度。 如何选择填料粒度?目前,高效液相色谱柱厂家色谱填料粒度从1um到超过30um均有销售,而目前分析分离主要用3和5um填料进行。填料的粒度主要影响填充柱的两个参数,即柱效和背压。粒度越小,柱压越大,柱压的增加限制了粒度小于3um的填料应用。在相同选择性条件下,提高柱效可提高分离度,但不是唯一的因素。如果固定相选择是正确,但是分离度不够,那么选用更小的粒度的填料是很有用的。3um填料填充柱的柱效比相同条件下的5um填料的柱效提高近30% 然而,3um的色谱柱的背压却是5um的2倍。与此同时,柱效提高意味着在相同条件下可以选用更短的色谱柱,即相同的塔板数或分离能力,但是柱长更短,以缩短分析时间。另外,可以采用低粘度的溶剂做流动相或增加色谱柱的使用温度,比如用乙腈代替甲醇,以降低色谱柱的压力。 对于如何选择高效液相色谱柱这个问题,一定要多了解色谱填料,只有了解它了,在高效液相色谱中,我们就能取得好的分离效果。
液相色谱柱碳18柱,国产的和进口的在使用上区别大么?
1对于一根常用的C18柱,拿到一根新柱的时候应该怎样进行活化及维护?为什么要这样做? 答:新柱活化,实际上是一个平衡的过程,除了用流动相平衡外,有时候还必须用所测样品对新柱进行平衡,特别是测定分子量比较高的多肽,尤其重要。因为分子量高的物质分子,扩散速度慢,平衡所需时间也相应较长。具体平衡方式也很简单,多进几次样品,直到峰面积和保留时间稳定,再进行正式进样测定。 如果要加快平衡时间,把前面用来平衡的进样样品浓度加大,或者不等洗脱完成,连续进样多针。用待测物对新柱平衡,目的是将硅胶基质填料表面具有非特异性吸附的位点的吸附能力饱和掉。2测定多肽,一般采用什么柱子?流动相是乙腈和水,还有微量的TFA。特别是像类似三肽的短肽,应该怎么选择柱子? 答:分子量不高的多肽一般选用常规C18柱就能测定,也有用离子交换柱、水性C18柱和Hilic亲水作用柱的。3氨基柱在进酸性样品时,很伤柱子,如使用一段时间后,柱效降低,峰形改变,如何恢复? 答:氨基柱测酸性样品,应该是用氨基柱的HILIC模式。酸的存在可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。4色谱柱的技术都有哪些?比如封尾等,这些技术在应用时都体现在哪里? 答:色谱柱技术包括填料技术和装柱技术,填料技术自不待言,填料的好坏对色谱柱分离性能和选择性有决定性影响。装柱技术也没有想象中的这么简单,不同固定相、不同粒径、不同柱管内径和长度,装柱工艺都有所不同,要装出紧密、稳定、均一的柱床,更多是一门艺术,需要经验积累。 国内和国外想比,我认为色谱柱的差距在于:国内公司以前都不会自己开发填料,一般买国外现成填料装柱,买到的填料质量控制权不在自己手里。另外因为装柱历史短,经验积累少,装柱工艺也没有完全达到国外水平。另外,对色谱柱性能很关键的基础材料-----裸硅胶,国产的还不过关,在纯度、粒径和孔径的均一性方面和国外产品相比,差距很大。5色谱柱技术的差距在哪里? 答:液相色谱柱装填实际上是有一定技巧和程序,可能还有一些运气。一般使用高压匀浆方法装填。也就是能让填料在溶剂内均匀地悬浮。然后用瞬间高压压实,这实际上用到了不同比例的匀浆液体,和合适的压力。压力太大,颗粒破碎,压力太小,塔板数少。同时压力需要稳定,不然分布不均,拖尾严重。同时还有头上平整程度。套上套,就可以用了。6柱子在什么情况下可以清洗一下筛板呢?原来也讨论过这个问题,我也拆下来清洗过,但我看到柱前段的污染更甚,于是就用刀片刮了刮,然后把清洗好的筛板安装上去。问题解决了,但使用寿命会不会减少呢? 答:柱头污染了,就取出污染的,再装一些填料。因为加入你刮了些填料,那么微观的塔板数就少了。假入你刮得不多,仅表面,可能就是一些脏物,所以,问题解决。但是今后还会有同样问题,再挂,那么不小心刮,影响柱效。建议还是装一个预柱。7如果柱子取下来放置一段时间,需要做什么保护吗? 答:对一般的反相柱,也就是洗干净后放到纯甲醇(乙腈)或者是80%左右的甲醇(乙腈)水中,然后用堵头塞紧柱两头,以免保存溶剂挥发,应该不需要做特殊的保护。8流动相中加入适量的四氢呋喃可以改善峰形的机理是什么? 答:《高效液相色谱方法及应用》于世林编著的上面说:甲醇为质子给予体、乙腈为质子接受体、四氢呋喃是偶极溶剂,应该除了极性影响,还有另外的影响因素,至于分离机理,还是比较复杂的,不能看成是个万能方法。9关于色谱柱的填装问题。我个人认为现在色谱柱的填装一般有3种情况: (1)国外生产填料并填装完成成品卖到国内; (2)国外生产填料,国内填装销售; (3)国内生产填料,国内填装销售。 一般情况下,第1种情况卖的最贵,也质量最好!可是如果是填料的生产很复杂的话,那么填装上国内也跟不上去吗?为什么换在国内填装就会出现或多或少的一些小问题呢? 答:国内填装会出现质量小问题,和国内目前普遍做事没有国外严谨有关吧。如果工艺技术上没有问题,又能制订并切实执行一整套严格的生产质量管理措施,国内填装和国外填装并无区别。10国产色谱柱在市场上占有比例如何啊? 国内色谱柱市场还没有人进行过科学统计,连一年色谱柱销售总量也众说纷云,更别说国内生产色谱柱所占份额了。我估计是占30%左右吧。11预柱或保护柱用还是不用的问题!原来分析中药品种时,我一直都是用保护柱。但来到新公司后,发现大家都没有使用,几个实验室连保护柱都没找到一个,也就是说大家从来都没有用过。后来问一个老员工,说是有可能影响药品分析。想问:安装保护柱后会影响样品分析吗?我们做的大多是头孢类的抗生素。 答:应该这样说,加上保护柱,肯定有利于保护色谱柱不受一些颗粒物质的堵塞,肯定有害于分离度和柱效,因为保护柱中间有着死体积的存在。但是如果保护柱接得好,并且尽量控制其匹配性和经常更换,分离度和柱效应该影响并不大。头孢类的抗生素也要看到底是原料药还是制剂喽,有些原料药,可以根据色谱柱的损耗选择添加预柱(中间是个筛板),制剂的话,如果有辅料严重干扰或者流动相盐分比较大,那还是最好配个保护柱。12用的是四元梯度泵A50%甲醇B50%水经常出现停或进气泡这是什么原因? 答:水/甲醇比例在55:45时,黏度和柱压有个极大值。50:50接近了这个极值,柱压是比较高的,但影响柱压最大的还是填料粒径和色谱柱内径,你这个实例中不知用的什么规格的色谱柱?系统压力高,可能会因溶剂泵中的过滤头供液速度跟不上而导致气泡进入系统,停机也应该是因为气泡进入压力下降的原因,可考虑更换液体通量更大的过滤头。13资料显示:在正常条件下,填料粒度>20μm时,干法填充制备柱较为合适;颗粒<20μm时,湿法填充较为理想。各种填充方法有什么区别?答:填充方法一般有4种 ①高压匀浆法,多用于分析柱和小规模制备柱的填充; ②径向加压法,Waters专利; ③轴向加压法,主要用于装填大直径柱; ④干法。柱填充的技术性很强,大多数实验室使用已填充好的商品柱。为什么以20um为分界点?填料方法的前三种都是湿法吗,能不能对四种填充方法做一个简短的说明?14想请您具体说明一下反冲色谱柱的方法,是不连检测器吗? 答:反冲就是将柱子反向连到系统中。因为有污染物反冲出来,当然不连检测器,出液端直接接到废液瓶就可以。15网上对柱子是否可以反冲一直有争论,那什么样的柱子可以反冲,什么不可以。反冲后是正者用,还是反着用。具体到各型号柱子不仅是ODS柱,其他如正向柱、氨基柱、离子交换柱等最好都有解释。 答:一般的正相反相柱应该都能反冲,只有两端筛板孔径不对称的柱子不能反冲,不过目前这样的柱子已经比较少见了。反冲是为了把柱头的污染物冲洗掉,反冲后还是正着用比较好,以免柱子的两头都被污染。我们一直提倡的是:正向使用,反向冲洗。16在做方法开发的时候,用乙腈和水作为流动相,在调整梯度的时候发现,刚开始用60%乙腈,RT为2.5分钟,调到40%乙腈,RT没有变化,30%也没有变化,一直调到20%的时候,RT突然变到了约13分钟,请问这是什么原因?我用的是离子交换柱。 答:离子交换柱的保留时间主要由洗脱液的离子强度和pH决定,你现在讲的比较简单,需要把你的方法说的详细一点才能做具体的分析。譬如分析物是什么情况,其含有极性电离基团和非极性基团是什么性质?离子交换柱是聚合物基质还是硅胶基质?水相是什么缓冲盐?转自公众号《化工信息网》
液相色谱柱年鉴(2013)目录tables of contents第1章 中国品牌液相色谱柱 31.1. Dikma(迪马.中国) 31.1.1. 介绍 31.1.2. 迪马液相色谱柱 31.2. Anpel(安谱.中国) 31.2.1. 介绍 41.2.2. CNW液相色谱柱 41.3. Welch(月旭.中国) 41.3.1. 介绍 41.3.2. 月旭液相色谱柱 41.4. Bonna-Agela(博纳-艾杰尔.中国) 51.4.1. 介绍 51.4.2. 博艾液相色谱柱 5第2章 美国品牌液相色谱柱 72.1. Agilent(安捷伦.美国) 72.1.1. 安捷伦ZORBAX液相色谱柱 7(1). 硅胶类别 72.1.2. 安捷伦Poroshell液相色谱柱 82.2. Waters(沃特世.美国) 82.2.1. 沃特世液相色谱柱 8(1). 颗粒类型 82.2.2. ACQUITY UPLC Columns 92.2.3. HPLC分析和制备柱 9(1). Xbridge 9(2). Xselect 9(3). Atlantis 10(4). Sunfire 102.2.4. SFC(超临界流体色谱)柱 112.3. Phenomenex(菲罗门.美国) 112.3.1. Phenomenex HPLC/UHPLC色谱柱 112.4. Thermo-Fisher(赛默飞.美国) 112.4.1. 主要色谱柱产品 122.4.2. 生物分子色谱柱 122.4.3. 极性和可选择性色谱柱 132.4.4. 扩展pH型色谱柱 132.4.5. 经典型色谱柱 132.4.6. LC/MS色谱柱和工具包 132.4.7. 保护柱 132.4.8. 离子交换型色谱柱 142.4.9. 体积排阻色谱柱 142.5. Dionex(戴安.美国Thermo旗下) 142.5.1. 介绍 142.5.2. 戴安公司液相柱 15(1). DIONEX Acclaim Surfactant色谱柱 15(2). DIONEX Acclaim OA色谱柱 15(3). DIONEX Acclaim PA2色谱柱 15(4). DIONEX Acclaim PA色谱柱 15(5). DIONEX Acclaim 120 C18分析柱 15(6). DIONEX Acclaim 120 C8分析柱 16(7). DIONEX Acclaim 300色谱柱 16(8). DIONEX Acclaim explosives色谱柱 162.6. Sigma-Aldrich(西格玛-奥德里奇.美国) 162.6.1. Supelco(色谱科.美国) 162.6.2. 美国Sigma-Aldrich公司(美国西格玛奥德里奇公司) 172.7. GRACE-Alltech(格雷斯-奥泰.美国) 172.8. Restek(瑞斯泰克.美国) 172.9. Kromat.KB(科瑞迈.美国) 182.10. Sepax(赛分.美国) 18第3章 欧洲品牌液相色谱柱 193.1. Machery Nagel.Nucleodur(闪电.德国) 193.2. Merck(默克.德国) 193.3. Hamilton(哈美顿.瑞士) 203.3.1. Hamilton液相色谱柱 213.4. Kromasil.Eka(克罗马斯,作者暂定.瑞典) 22第4章 日本品牌液相色谱柱 234.1. CAPCELL PAK(资生堂.日本) 234.2. Shimadzu(岛津.日本) 244.3. Showa Denko.Shodex(昭和.日本) 254.4. TSKgel(东曹.日本) 254.5. YMC(山村化学.日本) 264.6. Nacalai Tesque.Cosmosil(纳采,作者暂定.日本) 274.7. Daicel(大赛璐.日本) 274.8. DAICEL历史介绍 284.9. DAICEL大赛璐(中国) 304.9.1. 大赛璐手性柱 31
选购液相色谱柱时,需要综合考虑分析物的性质、分离要求、样品基质、耐用性、品牌和成本等多个因素。? 首先,?分析物的性质?是选购液相色谱柱时需要考虑的重要因素。不同的化合物具有不同的极性、分子量等特性。对于极性较强的化合物,可能需要选择极性色谱柱,如氰基柱或氨基柱;而对于非极性化合物,则更适合使用反相色谱柱,如十八烷基硅烷键合硅胶柱(C18柱)?。 其次,?分离要求?也是选购时需要考虑的关键因素。如果需要对复杂混合物进行精细分离,可能需要选择粒径较小、柱效较高的色谱柱。较长的柱子通常能提供更好的分离度,但分析时间也会相应延长?。 此外,?样品基质?也是一个重要因素。如果样品中含有大量的杂质或干扰物,可能需要选择具有特定选择性或耐受性的色谱柱,以确保有效分离并减少干扰?。 最后,?耐用性、品牌和成本?也是选购时需要考虑的因素。优质的色谱柱应能在较长时间内保持良好的性能,经受多次使用和不同条件的考验。知名品牌通常在质量控制和技术支持方面更有保障,能为用户提供更可靠的产品和专业的建议。在满足分析要求的前提下,选择性价比高的色谱柱?。 综上所述,选购液相色谱柱需要综合考虑分析物性质、分离要求、样品基质、耐用性、品牌以及成本等多方面因素,从而确保高效液相色谱分析的成功进行和准确可靠的结果?。
[align=left]现代高效液相色谱中,分离效果好坏很大程度上取决于色谱填料的选择中。但是色谱填料的选责范围很宽,要做合适的选择,必须对此有一定的认识和了解。[/align][b]一. 硅胶基质填料[/b] 1, 1, 正相色谱正相色谱用的固定相通常为硅胶(Silica),以及其他具有极性官能团,如胺基团 (ZH[sub]2[/sub],APS)和氰基团(CN,CPS)的键合相填料。 由于硅胶表面的硅羟基(SiOH)或其他团的极性教强,因此,分离的次序是依据样品中的各组份的极性大小,即极性强落的组份最先被冲洗出色谱柱。正相色谱使用的流动相极性相对比固定相低,如:正乙烷(Hexane),氯(Chloroform) 二氯甲烷(Methylence Chloride)等.2反相色谱反相色谱填料常是以硅胶为基础,表面键合有极性相对教弱的官能团的键合相。反相色谱所使用的流动相极性教强,通常为水,缓冲液与甲醇,已腈等混合物。样品流出色谱柱的顺序是极性教强组合最先被冲出,而极性弱的组份会在色谱柱上有更强的保留。常用的反相填料有C18(ODS) C8(MOS)。C4(B)C[sub]6[/sub]H[sub]5[/sub](Phenyl)等。
气相色谱中常规使用的色谱柱分为极性如DB-1701、中等极性如DB-5、弱极性如DB-1等,那么液相色谱中对色谱柱是如何划分的呢?
每天用足够的时间来平衡色谱柱,您就会在处理问题方面获得最大的"补偿",而且您的色谱柱的寿命也会变得更长!------ 一定得做! 新的色谱柱在使用之前应该在您自己的液相色谱仪上进行性能测试,即使用色谱柱附带的检验报告上测试条件和样品来测定该色谱柱的柱效。并且,在以后的使用中,应时常对色谱柱进行测试。 卡套柱的安装(不加预柱) 1.将卡套架套入柱芯 2.将两片夹套片嵌入柱芯的凹槽,使柱芯高于夹套(见下图) 3.将已套到柱芯上的卡套架向上推,直至高过夹套片 4.将卡套帽和卡套架旋在一起,然后用手拧紧 5.然后依同样的顺序连接好柱子的另一端 6.连接到液相色谱仪,PEEK接头手拧即可;若为不锈钢接头应使用专用扳手 注意:使用卡套柱时,两端的卡套应时刻连接在柱芯上。不管您是平衡色谱柱或是清洗,任何时候都不能将卡套取下来,否则会造成填料的流失。 卡套柱的安装(加预柱) 1.将卡套架套入柱芯 2.将两片夹套片嵌入柱芯的凹槽,使夹套高于柱芯(见下图) 3.将已套到柱芯上的卡套架向上推,直至高过夹套片 4.将"子弹头"预柱放入卡套片内 5.将卡套帽和卡套架旋在一起,然后用手拧紧 6.然后依同样的顺序连接好柱子的另一端 7.连接到液相色谱仪,PEEK接头手拧即可;若为不锈钢接头应使用专用扳手 更换色谱柱滤网和玻璃棉过滤片(同时可以修补色谱柱) 注意:在取出反相柱芯的滤网和玻璃片之前,应该将色谱柱充分用水和甲醇/乙腈冲洗,而且修补工具的头部也应该蘸取少量的甲醇/乙腈,以避免在取出滤网和玻璃棉滤片时带出柱子内的填料。 1.将修补工具中的2套入柱芯的顶端 2.将修补工具中的3轻轻地旋入已套着2的柱芯中,并顺时针方向旋转到旋紧 3.一手握柱芯,另一只手轻轻地向外拉3,取出柱芯顶端的滤网 4.用一个小铲子轻轻地取出滤网下面的玻璃棉以及被污染的填料 5.将新的填料用甲醇润湿,然后填入挖去的部位,压平 6.照(下图)装上新的玻璃棉滤网,并用修补工具中的4将玻璃棉压入柱芯顶端 7.柱芯顶端套上2,然后参照(下图)将滤网放入 8.压紧,然后取下2,再用4将滤网的边缘压平 平衡色谱柱 反相色谱柱在经过出厂测试后是保存在乙腈/水中的。请一定确保您所使用的流动相和乙腈/水互溶。由于色谱柱在储存或运输过程中可能会干掉,因此在用流动相分析样品之前,应使用10-20倍柱体积的甲醇或乙腈平衡色谱柱;如果您所使用的流动相中含有缓冲盐,应注意用纯水"过渡"。 硅胶柱或极性色谱柱在经过出厂测试后是保存在正庚烷中的。如果该色谱柱需要使用含水的流动相,请在使用流动相之前用乙醇或异丙醇平衡 如何平衡色谱柱? 平衡过程中,将流速缓慢地提高 用流动相平衡色谱柱直到获得稳定的基线(缓冲盐或离子对试剂度如果较低,则需要较长的时间来平衡) 色谱柱的再生 进行色谱柱再生时,应使用一个谦价的泵,我们建议最好不使用您的高效液相色谱仪上的泵。 表1 建议用来冲洗的溶剂体积 色谱柱尺寸 柱体积 所用溶剂的体积 125-4 1.6ml 30ml 250-4 3.2ml 60ml 250-10 -20ml 400ml 请根据下表选择您的再生方法: 极性固定相(如Si,NH2*,DIOL基色谱填料)的再生: 正庚烷→氯仿→乙酸乙酯→丙酮→乙醇→水** 非极性固定相(如反相色谱填料RP-18,RP-8,CN等)的再生: 水→乙腈→氯仿(或异丙醇)→乙腈→水 0.05M稀硫酸可以用来清洗已污染的色谱柱 注意: 在对NH2改性的色谱柱进行再生时,由于NH2可能成铵根离子的形式存在,因此应该在水洗后用0.1M的氨水冲洗,然后再用水冲洗至碱溶液完全流出。 **如果简单的有机溶剂/水的处理不能够完全洗去硅胶表面吸附的杂质,用0.05M稀硫酸冲洗非常有效。 色谱柱的维护 1.使用预柱保护分析柱(硅胶在极性流动相/离子性流动相中有一定的溶解度) 2.大多数反相色谱柱的pH稳定范围是2-7.5,尽量不超过该色谱柱的pH范围 3.避免流动相组成及极性的剧烈变化 4.流动相使用前必须经脱气和过滤处理 5.如果使用极性或离子性的缓冲溶液作流动相,应在实验完毕柱子冲洗干净,并保存大乙腈中 6.压力升高是需要更换预柱的信号
[b]高效液相色谱柱的管理[/b]摘 要:介绍了影响色谱柱使用寿命的几个因素,探讨了色谱柱规范化管理和保养的经验。关键词:高效液相色谱 柱 管理 保养 高效液相色谱法是20世纪70年代急剧发展起来的一项高效、快速的分离、分析技术。液相色谱法是指流动相为液相的色谱技术,在经典的液相色谱法基础上,引入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法理论,在技术上采用高压泵、高效固定相和高灵敏度检测器,实现了分析速度快、分析效率高和操作自动化,它具有高压、高速、高效、高灵敏度等特点。它是用高压输液泵将具有不同极性的单一溶剂或不同比例的混合溶剂,缓冲液等流动相泵入装有固定相的色谱柱,经进样阀注入供试品,由流动相带入柱内,在柱内各成分被分离后依次进入检测器,色谱信号由记录仪、积分仪或色谱工作站记录。高效色谱柱是高效液相色谱的心脏,在高效液相色谱仪的使用中,保持色谱柱的柱效、容量和渗透特性,延长柱子的使用寿命非常重要。色谱柱使用时间后就会出现柱压升高、柱效降低、峰形畸变和分离度降低、保留时间改变等变化,如不采取措施,将会缩短色谱柱的使用寿命,影响工作效率,并造成一定的经济损失。因此,有必要加强和规范色谱柱的管理,从而延长色谱柱的使用寿命。本文从影响色谱柱使用寿命的几个因素出发,从管理的角度,探讨色谱柱的维护与保养。1 色谱柱的类型常用的色谱柱填充剂有硅胶和化学键合硅胶、离子交换树脂、凝胶或玻璃微球等填充剂。在化学键合硅胶中以十六烷基硅烷键合硅胶最常用,辛基硅烷键合硅胶次之,氰基或氨基键合硅胶也有使用。近年来,由于蛋白质等生物大分子物质分离提纯技术的飞速发展,离子交换色谱柱、凝胶色谱柱的应用也越来越广。2 影响色谱柱使用寿命的因素2.1 流动相在以水溶液为流动相时,水溶液中的微生物例如细菌容易生长,当用水溶液或有机酸缓冲液保护柱子时,一些霉菌可能在色谱柱中滋生,堵塞固定相颗粒间的空隙。由于湿法填充技术的问世,目前普遍使用的色谱柱填料直径一般都小于10um,流动相中的颗粒杂质很容易先沉积在柱头然后慢慢堵塞柱子。流动相的pH值对色谱柱也有影响,特别是对化学键合硅胶填料,水溶液的pH最适范围在2~7.5之间,当pH8时,硅胶会释出生成絮状物堵塞柱子,且难以复原,柱效很快降低,甚至完全失效。当在缓冲液中加入有机溶剂例如甲醇或乙腈时,盐类的溶解度下降,会析出盐沉淀,堵塞柱子。同时流动相中的有机溶剂和盐会腐蚀色谱柱头的筛板,产生柱头凹陷。流动相的极性对柱子也有一定影响,对于硅胶柱,甲醇、水、冰乙酸等极性较大物质会破坏填料,反之,对于化学键合硅胶,极性小的物质如正丁醇、二氯甲烷等也起同样的作用。碱性溶液会破坏阳离子交换树脂色谱柱,而酸性溶液容易损坏阴离子交换树脂柱。
以下是Agilent液相色谱柱的应用范围:正相吸附色谱极性:固定相 流动相固定相- 极性流动相(己烷,庚烷)- 非极性极性物质后出峰反相分配色谱极性:固定相 流动相固定相- 非极性流动相(甲,乙醇,乙腈,THF,二氯乙烷)- 极性非极性物质后出峰
对于LC-MS/MS色谱柱人们的惯性思维通常是由反相液相色谱柱开始研发, 产生这种惯性思维是因为常规高效液相色谱分析中C18等反相高效液相色谱柱占有统治地位,另一方面是色谱公司不懂LC-MS/MS分析误导用户的结果。这惯性思维是不正确的! LC-MS/MS分析的实用战略和HPLC有很大不同! LC-MS/MS分析的方法的选择性最重要! 色谱公司不能简单地将现成的反相液相色谱填料装成5cm x 2.1mm短柱充当LC-MS/MS柱使用, 但事实上几乎所有色谱公司都是这样做的。这样的反相液相色谱LC-MS/MS柱有三个明显的弱点:(1) 许多极性化合物难以保留,质谱灵敏度差。 许多重要的物质,如抗癌药物DTIC, 抗痛药物河豚毒素,污染物质三聚氰胺, 中草药中糖肽等非常极性, 在反相液相色谱柱上没有保留。还有许多的化合物比较极性, 使用少量的甲醇或乙腈就从反相液相色谱柱上洗脱。在药物代谢研究中, 观察到许多化合物自己疏水, 但代谢产物亲水的情况。甲醇或乙腈含量低, 离子化程度低, 质谱灵敏度差。所谓水相C18柱在LC-MS/MS分析中没有价值。(2) 用常规反相色谱填料装成2.1mm内径的色谱柱在LC-MS/MS和LC/MS应用中常陷入记忆效应(Carryover Effect)的“陷阱” LC-MS/MS和LC/MS应用中另一个重大问题是记忆效应(Carryover Effect)。记忆效应是指在进样后, 再进一针空白在同样的保留时间仍然观察到化合物峰。记忆效应的副作用是明显的: 它可能人为地增加下一样本的MRM信号, 影响定量分析的精密度和准确度。US FDA Bioanalytical Regulatory Guidances限制最高校准标准(highest calibration standard) 的记忆效应不能超过20 %最低校准标准(lowest calibration standard)MRM信号的20%。 由于大部分色谱公司都使用现成的反相液相色谱填料简单地装成5cm x 2.1mm短柱充当LC-MS/MS柱, 在许多情况下,使记忆效应强, 校准标准曲线范围必须人为缩短, 或不得已在进样后, 再进一针甚至两针空白最小化记忆效应, 然后进下一个样品。所有这些严重地降低了生产效率。(3) 峰形拖尾或扭曲 因为活性硅醇基无法完全封闭, 许多碱性化合物在几乎所有色谱公司的Cogent Diamond Hydride反相液相色谱柱上面有明显的峰形拖尾。这种峰形拖尾是记忆效应的一个重要的根源。另一方面,使用不正确方法过分封闭致使一些酸性和两性化合物分离效果不佳, 特别是出现峰失真和分裂现象。 专家认为LC-MS/MS色谱柱和色谱方法的第一选择是亲水色谱(HILIC或)! 亲水色谱使用乙腈作为弱溶剂和水为强溶剂, 彻底解决质谱灵敏度差, 记忆效应等问题。疏水化合物首先流出, 然后是亲水化合物。不仅彻底解决极性化合物难以保留的问题, 而且同时分析了疏水化合物, 也提高了疏水化合物质谱灵敏度。峰形拖尾问题也获得彻底解决。此外,乙腈提取液不需要蒸发和重新溶解,从而节省了大量的时间。另一方面, 反相LC-MS/MS色谱柱和色谱方法仍然重要, 不仅是一些重要的中性化合物如抗癌药物紫杉醇, 抗免疫器官植入药物FK 506和雷帕霉素(rapamycin), 降脂药等必须使用反相LC-MS/MS色谱柱和色谱方法, 还因为大多数客户习惯于反相LC-MS/MS色谱柱和色谱方法。即使这样反相液相色谱填料也必须通过处理才能装成5cm x 2.1mm短柱充当LC-MS/MS柱使用。
[color=#444444]如果遇到了大极性的物质,做液相的时候一般会考虑AQ柱或者HILIC模式的色谱柱,那您一般是如何选择的呢[/color]
现代高效液相色谱中,分离效果好坏很大程度上取决于色谱填料的选择。但是色谱填料的选择范围很宽,要做合适的选择,首先必须对此有一定的认识和了解。液相色谱仪填料可以是陶瓷性质的无机物基质,也可以是有机聚合物基质。液相色谱仪填料中的有机物基质主要是硅胶和氧化铝。无机物基质刚性大,在溶剂中不容易膨胀。液相色谱仪填料中有机聚合物基质主要有交联苯乙烯-二乙烯苯、聚甲基丙烯酸酯。有机聚合物基质刚性小、易压缩,溶剂或溶质容易渗入有机基质中,导致填料颗粒膨胀,结果减少传质,最终使柱效降低。以下鲁创分析仪器公司工程师简单介绍在液相色谱仪检测中应用最为广泛的三种基质的性质。 1)硅胶基质 硅胶基质是HPLC填料中最普遍的基质。除具有高强度外,还提供一个表面,可以通过成熟的硅烷化技术键合上各种配基,制成反相、离子交换、疏水作用、亲水作用或分子排阻色谱用填料。硅胶基质填料适用于广泛的极性和非极性溶剂。缺点是在碱性水溶性流动相中不稳定。通常,硅胶基质的填料推荐的常规分析pH范围为2~8。 2)氧化铝基质 氧化铝基质具有与硅胶相同的良好物理性质,也能耐较大的pH范围。它也是刚性的,不会在溶剂中收缩或膨胀。但与硅胶不同的是,氧化铝键合相在水性流动相中不稳定。不过现在已经出现了在水相中稳定的氧化铝键合相,并显示出优秀的pH稳定性。 3)聚合物基质 聚合物基质以高交联度的苯乙烯-二乙烯苯或聚甲基丙烯酸酯为基质的填料是用于普通压力下的HPLC,它们的压力限度比无机填料低。苯乙烯-二乙烯苯基质疏水性强。使用任何流动相,在整个pH范围内稳定,可以用NaOH或强碱来清洗色谱柱。甲基丙烯酸酯基质本质上比苯乙烯-二乙烯苯疏水性更强,但它可以通过适当的功能基修饰变成亲水性的。这种基质不如苯乙烯-二乙烯苯那样耐酸碱,但也可以承受在pH13下反复冲洗。 所有聚合物基质在流动相发生变化时都会出现膨胀或收缩。用于HPLC的高交联度聚合物填料,其膨胀和收缩要有限制。溶剂或小分子容易渗入聚合物基质中,因为小分子在聚合物基质中的传质比在陶瓷性基质中慢,所以造成小分子在这种基质中柱效低。对于大分子像蛋白质或合成的高聚物,聚合物基质的效能比得上陶瓷性基质。因此,聚合物基质广泛用于分离大分子物质。 液相色谱仪基质的选择大致遵循以下法则,硅胶基质的填料被用于大部分的HPLC分析,尤其是小分子量的被分析物,聚合物填料用于大分子量的被分析物质,主要用来制成分子排阻和离子交换柱。
[align=center][b]液相色谱柱的分类、选择及维护[/b][/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:管聪怡[/align][b]一.液相色谱柱的分类:(按色谱固定相基质分)1.硅胶基质:[/b]1.1反相色谱柱: 反相色谱填料常是以硅胶为基础,表面键合有极性相对较弱的官能团的键合相。反相色谱所使用的流动相极性较强,通常为水,缓冲液与甲醇,已腈等混合物。样品流出色谱柱的顺序是极性较强组合最先被冲出,而极性弱的组份会在色谱柱上有更强的保留。常用的反相填料有C18(ODS)、C8(MOS)、C4(B)、C6H5(Phenyl)等。1.2正相色谱: 正相色谱用的固定相通常为硅胶(Silica),以及其他具有极性官能团,如胺基团(NH2,APS)和氰基团(CN,CPS)的键合相填料。由于硅胶表面的硅羟基(SiOH)或其他团的极性较强,因此,分离的次序是依据样品中的各组份的极性大小,即极性强弱的组份最先被冲洗出色谱柱。正相色谱使用的流动相极性相对比固定相低,如:正乙烷(Hexane),氯仿(Chloroform),二氯甲烷(Methylene Chloride)等。1.3离子交换色谱柱:以磺化交联强阴/阳离子键合硅胶色谱柱,常用规格:强阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱(SAX),强阳离子交换色谱柱(SCX)[b]2.聚合物基质:[/b] 聚合物调料多为聚苯乙烯-二乙烯基苯或聚甲基丙酸酯等,其主要优点是在PH值为1~14均可使用。相对与硅胶基质的C18填料,这类填料具有更强的疏水性;大孔的聚合物填料对蛋白质等样品的分离非常有效。现在的聚合物填料的缺点是相对硅胶基质填料,色谱柱柱效较低。所有聚合物基质在流动相发生变化时都会出现膨胀或收缩。用于HPLC的高交联度聚合物填料,其膨胀和收缩要有限制。溶剂或小分子容易渗入聚合物基质中,因为小分子在聚合物基质中的传质比在陶瓷性基质中慢,所以造成小分子在这种基质中柱效低。对于大分子像蛋白质或合成的高聚物,聚合物基质的效能比得上陶瓷性基质。因此,聚合物基质广泛用于分离大分子物质。[b]3.其他无机填料:[/b] 其它HPLC的无机填料色谱柱也已经商品化。由于其特殊的性质,一般仅限于特殊的用途。如石墨化碳也用于正逐渐成为反相色谱填料。这种填料的分离不同与硅胶基质烷基键合相,石墨化碳的表面即是保留的基础,不再需其它的表面改性,该柱填料一般比烷基键合硅胶或多孔聚合物填料的保留能力更强,石墨化碳可用于分离某些几何导构体,又由于HPLC流动相中不会被溶解,这类柱可在任何PH与温度下使用。氧化铝也可用于HPLC,氧化铝微粒刚性强,可制成稳定的色谱柱柱床,其优点是可在PH高达12的流动相中使用。但由于氧化铝与碱性化合物作用也很强,应用范围受到一定的限制,所以未能广泛应用,新型氧化锆填料也可用于HPLC,商品化的仅有聚合物涂层的多孔氧化锆微球色谱柱,应用PH范围1~14,温度可达100℃。由于氧化锆填料几年才开始研究,加之面临的实验难度,其重要用途与优势尚在进行中。[b]二.色谱柱的选择[/b]液相色谱仪基质的选择大致遵循以下法则,硅胶基质的填料被用于大部分的HPLC分析,尤其是小分子量的被分析物,聚合物填料用于大分子量的被分析物质,主要用来制成分子排阻和离子交换柱。色谱柱在使用前,最好进行柱的性能测试,并将结果保存起来,作为今后评价柱性能变化的参考。在做柱性能测试时要按照色谱柱出厂报告中的条件进行(出厂测试所使用的条件是最佳条件),只有这样,测得的结果才有可比性。但要注意:柱性能可能由于所使用的样品、流动相、柱温等条件的差异而有所不同。三.[b]色谱柱的维护1. 色谱柱的平衡[/b] 反相色谱柱由工厂测试后是保存在乙腈/水中的。新柱应先使用10-20倍柱体积的甲醇或乙腈冲洗色谱柱。请一定确保您分析样品所使用的流动相和乙腈/水互溶。每天用足够的时间以流动相来平衡色谱柱,您就会在处理问题方面获得最大的"补偿",2. [b]色谱柱的再生[/b] 长期使用的色谱柱,往往柱效会下降(柱子的理论塔板数减低)。可以对色谱柱进行再生,在有条件的实验室应使用一个廉价的泵进行柱子的再生。建议用来冲洗柱子的溶剂体积[b]3. 色谱柱的维护[/b]a.使用预柱保护分析柱(硅胶在极性流动相/离子性流动相中有一定的溶解度)b.大多数反相色谱柱的pH稳定范围是2-7.5,尽量不超过该色谱柱的pH范围c.避免流动相组成及极性的剧烈变化d.流动相使用前必须经脱气和过滤处理e.如果使用极性或离子性的缓冲溶液作流动相,应在实验完毕柱子冲洗干净,并保存于甲醇或乙腈中f.氯化物的溶剂对其有一定的腐蚀性,故使用时要注意,柱及连接管内不能长时间存留此类溶剂,以避免腐蚀。
每天用足够的时间来平衡色谱柱,您就会在处理问题方面获得最大的"补偿",而且您的色谱柱的寿命也会变得更长!------ 一定得做! 新的色谱柱在使用之前应该在您自己的液相色谱仪上进行性能测试,即使用色谱柱附带的检验报告上测试条件和样品来测定该色谱柱的柱效。并且,在以后的使用中,应时常对色谱柱进行测试。 卡套柱的安装(不加预柱) 1.将卡套架套入柱芯 2.将两片夹套片嵌入柱芯的凹槽,使柱芯高于夹套(见下图)[img]http://ng1.17img.cn/bbsfiles/images/2005/02/200502021045_449_1630010_3.jpg[/img] 3.将已套到柱芯上的卡套架向上推,直至高过夹套片 4.将卡套帽和卡套架旋在一起,然后用手拧紧 5.然后依同样的顺序连接好柱子的另一端 6.连接到液相色谱仪,PEEK接头手拧即可;若为不锈钢接头应使用专用扳手 注意:使用卡套柱时,两端的卡套应时刻连接在柱芯上。不管您是平衡色谱柱或是清洗,任何时候都不能将卡套取下来,否则会造成填料的流失。 卡套柱的安装(加预柱) 1.将卡套架套入柱芯 2.将两片夹套片嵌入柱芯的凹槽,使夹套高于柱芯(见左图) 3.将已套到柱芯上的卡套架向上推,直至高过夹套片 4.将"子弹头"预柱放入卡套片内 5.将卡套帽和卡套架旋在一起,然后用手拧紧 6.然后依同样的顺序连接好柱子的另一端 7.连接到液相色谱仪,PEEK接头手拧即可;若为不锈钢接头应使用专用扳手 更换色谱柱滤网和玻璃棉过滤片(同时可以修补色谱柱) 注意:在取出反相柱芯的滤网和玻璃片之前,应该将色谱柱充分用水和甲醇/乙腈冲洗,而且修补工具的头部也应该蘸取少量的甲醇/乙腈,以避免在取出滤网和玻璃棉滤片时带出柱子内的填料。 1.将修补工具中的2套入柱芯的顶端 2.将修补工具中的3轻轻地旋入已套着2的柱芯中,并顺时针方向旋转到旋紧 3.一手握柱芯,另一只手轻轻地向外拉3,取出柱芯顶端的滤网 4.用一个小铲子轻轻地取出滤网下面的玻璃棉以及被污染的填料 5.将新的填料用甲醇润湿,然后填入挖去的部位,压平 6.照(左图)装上新的玻璃棉滤网,并用修补工具中的4将玻璃棉压入柱芯顶端 7.柱芯顶端套上2,然后参照(左图)将滤网放入 8.压紧,然后取下2,再用4将滤网的边缘压平 平衡色谱柱 反相色谱柱在经过出厂测试后是保存在乙腈/水中的。请一定确保您所使用的流动相和乙腈/水互溶。由于色谱柱在储存或运输过程中可能会干掉,因此在用流动相分析样品之前,应使用10-20倍柱体积的甲醇或乙腈平衡色谱柱;如果您所使用的流动相中含有缓冲盐,应注意用纯水"过渡"。 硅胶柱或极性色谱柱在经过出厂测试后是保存在正庚烷中的。如果该色谱柱需要使用含水的流动相,请在使用流动相之前用乙醇或异丙醇平衡 如何平衡色谱柱? 平衡过程中,将流速缓慢地提高 用流动相平衡色谱柱直到获得稳定的基线(缓冲盐或离子对试剂度如果较低,则需要较长的时间来平衡) 色谱柱的再生 进行色谱柱再生时,应使用一个谦价的泵,我们建议最好不使用您的高效液相色谱仪上的泵。 表1 建议用来冲洗的溶剂体积 色谱柱尺寸 柱体积 所用溶剂的体积 125-4 1.6ml 30ml 250-4 3.2ml 60ml 250-10 -20ml 400ml 请根据下表选择您的再生方法: 极性固定相(如Si,NH2*,DIOL基色谱填料)的再生: 正庚烷→氯仿→乙酸乙酯→丙酮→乙醇→水** 非极性固定相(如反相色谱填料RP-18,RP-8,CN等)的再生: 水→乙腈→氯仿(或异丙醇)→乙腈→水 0.05M稀硫酸可以用来清洗已污染的色谱柱 注意: 在对NH2改性的色谱柱进行再生时,由于NH2可能成铵根离子的形式存在,因此应该在水洗后用0.1M的氨水冲洗,然后再用水冲洗至碱溶液完全流出。 **如果简单的有机溶剂/水的处理不能够完全洗去硅胶表面吸附的杂质,用0.05M稀硫酸冲洗非常有效。 色谱柱的维护 1.使用预柱保护分析柱(硅胶在极性流动相/离子性流动相中有一定的溶解度) 2.大多数反相色谱柱的pH稳定范围是2-7.5,尽量不超过该色谱柱的pH范围 3.避免流动相组成及极性的剧烈变化 4.流动相使用前必须经脱气和过滤处理 5.如果使用极性或离子性的缓冲溶液作流动相,应在实验完毕柱子冲洗干净,并保存大乙腈中 6.压力升高是需要更换预柱的信号
高效液相色谱柱的选择一、硅胶基质填料 1、正相色谱 正相色谱用的固定相通常为硅胶(Silica)以及其他具有极性官能团胺基团,如(NH2,APS)和氰基团(CN,CPS)的键合相填料。由于硅胶表面的硅羟基(SiOH)或其他极性基团极性较强,因此,分离的次序是依据样品中各组分的极性大小,即极性较弱的组份最先被冲洗出色谱柱。正相色谱使用的流动相极性相对比固定相低,如正已烷(Hexane),氯仿(Chloroform),二氯甲烷(Methylene Chloride)等。2、反向色谱 反向色谱用的填料常是以硅胶为基质,表面键合有极性相对较弱官能团的键合相。反向色谱所使用的流动相极性较强,通常为水、缓冲液与甲醇、乙腈等的混合物。样品流出色谱柱的顺序是极性较强的组分最先被冲洗出,而极性弱的组分会在色谱柱上有更强的保留。常用的反向填料有:C18(ODS)、C8(MOS)、C4(Butyl)、C6H5(Phenyl)等。二、聚合物填料 聚合物填料多为聚苯乙烯—二乙烯基苯或聚甲基丙烯酸脂等,其重要优点是在PH值为1—14均可使用。相对于硅胶基质的C18填料,这类填料具有更强的疏水性;大孔的聚合物对蛋白质等样品的分离非常有效。现有的聚合物填料的缺点是相对硅胶基质填料,色谱柱柱效较低。三、其它无机填料 其它HPLC的无机填料色谱柱也已经商品化由于其特殊的性质,一般仅限于特殊的用途。如,石墨化碳黑正逐渐成为反向色谱柱填料。这种填料的分离不同于硅胶基质烷基键合相,石墨化碳的表面即是保留的基础,不再需其它的表面改性。该柱填料一般比烷基键合相硅胶或多孔聚合物填料的保留能力更强。石墨化碳可用于分离某些几何异构体,由于在HPLC流动相中不会被溶解,这类柱可在任何PH与温度下使用。氧化铝也可以用于HPLC。氧化铝微粒刚性强,可制成稳定的色谱柱柱床,其优点是可以在PH高达12的流动相中使用。但由于氧化铝与碱性化合物的作用也很强,应用范围受到一定限制,所以未能广泛应用。新型色谱氧化锆基质填料也可用于HPLC。商品化的只有聚合物涂层的多孔氧化锆微球色谱柱,应用PH1-14,温度可达100℃。由于氧化锆填料是最近几年才开始研究,加之面临的实验难度,其重要用途与优势尚在进行之中。怎样选择填料粒度 目前,商品化的色谱填料粒度从1um到超过30um均有销售,而目前分析分离主要用3和5um填料进行。填料的粒度主要影响填充柱的两个参数,即柱效和背压。粒度越小,柱压越大,柱压的增加限制了粒度小于3um的填料应用。在相同选择性条件下,提高柱效可提高分离度,但不是唯一的因素。如果固定相选择是正确,但是分离度不够,那么选用更小的粒度的填料是很有用的。3um填料填充柱的柱效比相同条件下的5um填料的柱效提高近30%;然而,3um的色谱柱的背压却是5um的2倍。与此同时,柱效提高意味着在相同条件下可以选用更短的色谱柱,即相同的塔板数或分离能力,但是柱长更短,以缩短分析时间。另外,可以采用低粘度的溶剂做流动相或增加色谱柱的使用温度,比如用乙腈代替甲醇,以降低色谱柱的压力。
液相色谱柱使用及保养 (转贴) 液相色谱仪由高压液体泵、检测器及液相色谱柱等三部分组成,其中液相色谱柱的正确安装和使用,是液相色谱工作的关键;也是液相色谱工作者获得正确可靠的实验数据的必经之路。一、液相色谱柱的安装: 1、液相色谱柱的结构: a、空柱由柱接头、柱管及滤片组装而成。 柱接头采用低死体积结构,柱接头是两端螺纹组件,一端是为7/16英寸外螺纹,另一端是3/16英寸的内螺纹(国内外已规范化)。7/16英寸外螺纹与1/4英寸柱管(Φ6.35mm)连接,中间放置压坏用于密封。3/16英寸的内螺纹与1/16英寸(Φ1.57mm)的连接管连接,中间也放置压环用于柱接头的密封。为了尽量减少柱外死体积,在安装色谱柱时,用Φ1.57mm连接管通过空心螺钉压环后要尽量插到底,然后再拧紧空心螺钉。压环被空心螺钉挤压变形后紧箍在连接管上(连接管通过压环后露出的管长度应严格控制在2.5mm长或其他固定尺寸)。 在两端柱接头内,柱管两端各放置一片不锈钢滤片(或滤网),用于封堵柱填料不被流动相冲出柱外而流失。空柱各组件均为316#不锈钢材质,能耐受一般的溶剂作用。但由于含氯化物的溶剂对其有一定的腐蚀性,故使用时要注意,柱及连接管内不能长时间存留此类溶剂,以避免腐蚀。 b、柱填料: 液相色谱柱的分离作用是在填料与流动相之间进行的,柱子的分类是依据填料类型而定。 正相柱:多以硅胶为柱填料。根据外型可分为无定型和球型两种,其颗粒直径在3—10 μm的范围内。另一类正相填料是硅胶表面键合—CN,-NH2等官能团即所谓的键合相硅胶。 反相柱:主要是以硅胶为基质,在其表面键合十八烷基官能团(ODS)的非极性填料。也有无定型和球型之分。 常用的其他的反相填料还有键合C8、C4、C2、苯基等,其颗粒粒径在3—10 μm之间。 2,色谱柱的安装: a、拆开柱包装盒,确认色谱柱的类型、尺寸、出厂日期以及柱内贮存的溶剂。 b、拧下柱两端接头的密封堵头放回包装盒供备用。 c、 按柱管上标示的流动相流向,将色谱柱的入口端通过连接管与进样阀出口相连接(如条件允许,建议在柱前使用保护柱);柱的出口与检测器连接。连接管是外径为1.57mm、内径为0.1-0.3mm的不锈钢管。连接管的两端均有空心螺钉及密封用压环。在接管时一定要设法降低柱外死体积。连接管通过空心螺钉、压环后尽量用力插到底,然后顺时针拧紧空心螺钉,直到拧不动为止,再用扳手继续顺时针拧1/4-1/2圈,切记不要用力过大。如色谱柱通过流动相加压后有漏液现象,请用扳手继续顺时针拧1/4圈,直至不漏液为止。二、液相色谱柱的使用: 色谱柱在使用前,最好进行柱的性能测试,并将结果保存起来,作为今后评价柱性能变化的参考。但要注意:柱性能可能由于所使用的样品、流动相、柱温等条件的差异而有所不同;另外,在做柱性能测试时是按照色谱柱出厂报告中的条件进行(出厂测试所使用的条件是最佳条件),只有这样,测得的结果才有可比性。 1、样品的前处理: a、最好使用流动相溶解样品。 b、使用予处理柱除去样品中的强极性或与柱填料产生不可逆吸附的杂质。 c、使用0.45μm的过滤膜过滤除去微粒杂质。 2、流动相的配制: 液相色谱是样品组分在柱填料与流动相之间质量交换而达到分离的目的,因此要求流动相具备以下的特点: a、流动相对样品具有一定的溶解能力,保证样品组分不会沉淀在柱中(或长时间保留在柱中)。 b、流动相具有一定惰性,与样品不产生化学反应(特殊情况除外)。 c、流动相的黏度要尽量小,以便在使用较长的分析柱时能得到好的分离效果;同时降低柱压降,延长液体泵的使用寿命(可运用提高温度的方法降低流动相的黏度)。 d、流动相的物化性质要与使用的检测器相适应。如使用UV检测器,最好使用对紫外吸收较低的溶剂配制。 e、流动相沸点不要太低,否则容易产生气泡,导致实验无法进行。 f、在流动相配制好后,一定要进行脱气。除去溶解在流动相中的微量气体既有利于检测,还可以防止流动相中的微量氧与样品发生作用。 3、流动相流速的选择: 因柱效是柱中流动相线性流速的函数,使用不同的流速可得到不同的柱效。对于一根特定的色谱柱,要追求最佳柱效,最好使用最佳流速。对内径为4.6mm的色谱柱,流速一般选择1ml/min,对于内径为4.0mm柱,流速0.8ml/min为佳。 当选用最佳流速时,分析时间可能延长。可采用改变流动相的洗涤强度的方法以缩短分析时间(如使用反相柱时,可适当增加甲醇或乙腈的含量)。 注意: a.由于甲醇廉价,对于反相柱推荐使用甲醇体系(必须使用乙腈的场合除外)。 b.对于正相柱推荐使用沸程为30-60℃的石油醚或提纯后的己烷作流动相,没有提纯的己烷不得使用。用水最好使用超纯水(电阻率大于18兆欧),去离子水及双蒸水中含有酚类杂质,有可能影响分析结果。 c.含水流动相最奸在实验前配制,尤其是夏天使用缓冲溶液作为流动相不要过夜。最好加入叠氮化钠,防止细菌生长。 d.流动相要求使用0.45 μm滤膜过滤,除去微粒杂质。 e.使用HPLC级溶剂配制流动相,使用合适的流动相可延长色谱柱的使用寿命,提高柱性能。 4、柱性能测试: 启动液相色谱仪:a、流动相流速设定为1ml/min。 b、UV检测器波长设定为254nm。 使用出厂测试时使用的流动相组成及测试样品。 记录并计算测试结果。*参考(标准JB5226-91)液相色谱仪测试用标准色谱柱
对于LC-MS/MS色谱柱人们的惯性思维通常是由反相液相色谱柱开始研发, 产生这种惯性思维是因为常规高效液相色谱分析中C18等反相高效液相色谱柱占有统治地位,另一方面是色谱公司不懂LC-MS/MS分析误导用户的结果。这惯性思维是不正确的! LC-MS/MS分析的实用战略和HPLC有很大不同! LC-MS/MS分析的方法的选择性最重要! 色谱公司不能简单地将现成的反相液相色谱填料装成5cm x 2.1mm短柱充当LC-MS/MS柱使用, 但事实上几乎所有色谱公司都是这样做的。这样的反相液相色谱LC-MS/MS柱有三个明显的弱点:(1) 许多极性化合物难以保留,质谱灵敏度差。 许多重要的物质,如抗癌药物DTIC, 抗痛药物河豚毒素,污染物质三聚氰胺, 中草药中糖肽等非常极性, 在反相液相色谱柱上没有保留。还有许多的化合物比较极性, 使用少量的甲醇或乙腈就从反相液相色谱柱上洗脱。在药物代谢研究中, 观察到许多化合物自己疏水, 但代谢产物亲水的情况。甲醇或乙腈含量低, 离子化程度低, 质谱灵敏度差。所谓水相C18柱在LC-MS/MS分析中没有价值。(2) 用常规反相色谱填料装成2.1mm内径的色谱柱在LC-MS/MS和LC/MS应用中常陷入记忆效应(Carryover Effect)的“陷阱” LC-MS/MS和LC/MS应用中另一个重大问题是记忆效应(Carryover Effect)。记忆效应是指在进样后, 再进一针空白在同样的保留时间仍然观察到化合物峰。记忆效应的副作用是明显的: 它可能人为地增加下一样本的MRM信号, 影响定量分析的精密度和准确度。US FDA Bioanalytical Regulatory Guidances限制最高校准标准(highest calibration standard) 的记忆效应不能超过20 %最低校准标准(lowest calibration standard)MRM信号的20%。 由于大部分色谱公司都使用现成的反相液相色谱填料简单地装成5cm x 2.1mm短柱充当LC-MS/MS柱, 在许多情况下,使记忆效应强, 校准标准曲线范围必须人为缩短, 或不得已在进样后, 再进一针甚至两针空白最小化记忆效应, 然后进下一个样品。所有这些严重地降低了生产效率。(3) 峰形拖尾或扭曲 因为活性硅醇基无法完全封闭, 许多碱性化合物在几乎所有色谱公司的反相液相色谱柱上面有明显的峰形拖尾。这种峰形拖尾是记忆效应的一个重要的根源。另一方面,使用不正确方法过分封闭致使一些酸性和两性化合物分离效果不佳, 特别是出现峰失真和分裂现象。 专家认为LC-MS/MS色谱柱和色谱方法的第一选择是亲水色谱(HILIC或Cogent Diamond Hydride)! 亲水色谱使用乙腈作为弱溶剂和水为强溶剂, 彻底解决质谱灵敏度差, 记忆效应等问题。疏水化合物首先流出, 然后是亲水化合物。不仅彻底解决极性化合物难以保留的问题, 而且同时分析了疏水化合物, 也提高了疏水化合物质谱灵敏度。峰形拖尾问题也获得彻底解决。此外,乙腈提取液不需要蒸发和重新溶解,从而节省了大量的时间。另一方面, 反相LC-MS/MS色谱柱和色谱方法仍然重要, 不仅是一些重要的中性化合物如抗癌药物紫杉醇, 抗免疫器官植入药物FK 506和雷帕霉素(rapamycin), 降脂药等必须使用反相LC-MS/MS色谱柱和色谱方法, 还因为大多数客户习惯于反相LC-MS/MS色谱柱和色谱方法。即使这样反相液相色谱填料也必须通过处理才能装成5cm x 2.1mm短柱充当LC-MS/MS柱使用。
高压液相色谱HPLC培训教程(一) I.概论一、液相色谱理论发展简况 色谱法的分离原理是:溶于流动相(mobile phase)中的各组分经过固定相时,由于与固定相(stationary phase)发生作用(吸附、分配、离子吸引、排阻、亲和)的大小、强弱不同,在固定相中滞留时间不同,从而先后从固定相中流出。又称为色层法、层析法。 色谱法最早是由俄国植物学家茨维特(Tswett)在1906年研究用碳酸钙分离植物色素时发现的,色谱法(Chromatography)因之得名。后来在此基础上发展出纸色谱法、薄层色谱法、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法、液相色谱法。 液相色谱法开始阶段是用大直径的玻璃管柱在室温和常压下用液位差输送流动相,称为经典液相色谱法,此方法柱效低、时间长(常有几个小时)。高效液相色谱法(High performance Liquid Chromatography,HPLC)是在经典液相色谱法的基础上,于60年代后期引入了[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]理论而迅速发展起来的。它与经典液相色谱法的区别是填料颗粒小而均匀,小颗粒具有高柱效,但会引起高阻力,需用高压输送流动相,故又称高压液相色谱法(High Pressure Liquid Chromatography,HPLC)。又因分析速度快而称为高速液相色谱法(High Speed Liquid Chromatography,HSLP)。也称现代液相色谱。二、HPLC的特点和优点HPLC有以下特点:高压-压力可达150~300Kg/cm2。色谱柱每米降压为75 Kg/cm2以上。高速-流速为0.1~10.0 ml/min。高效-可达5000塔板每米。在一根柱中同时分离成份可达100种。高灵敏度-紫外检测器灵敏度可达0.01ng。同时消耗样品少。HPLC与经典液相色谱相比有以下优点:速度快-通常分析一个样品在15~30 min,有些样品甚至在5 min内即可完成。分辨率高-可选择固定相和流动相以达到最佳分离效果。灵敏度高-紫外检测器可达0.01ng,荧光和电化学检测器可达0.1pg。柱子可反复使用-用一根色谱柱可分离不同的化合物。样品量少,容易回收-样品经过色谱柱后不被破坏,可以收集单一组分或做制备。三、色谱法分类 按两相的物理状态可分为:[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(GC)和液相色谱法(LC)。[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法适用于分离挥发性化合物。GC根据固定相不同又可分为气固色谱法(GSC)和气液色谱法(GLC),其中以GLC应用最广。液相色谱法适用于分离低挥发性或非挥发性、热稳定性差的物质。LC同样可分为液固色谱法(LSC)和液液色谱法(LLC)。此外还有超临界流体色谱法(SFC),它以超临界流体(界于气体和液体之间的一种物相)为流动相(常用CO2),因其扩散系数大,能很快达到平衡,故分析时间短,特别适用于手性化合物的拆分。 按原理分为吸附色谱法(AC)、分配色谱法(DC)、离子交换色谱法(IEC)、排阻色谱法(EC,又称分子筛、凝胶过滤(GFC)、凝胶渗透色谱法(GPC)和亲和色谱法,此外还有电泳。按操作形式可分为纸色谱法(PC)、薄层色谱法(TLC)、柱色谱法。 四、色谱分离原理 高效液相色谱法按分离机制的不同分为液固吸附色谱法、液液分配色谱法(正相与反相)、离子交换色谱法、离子对色谱法及分子排阻色谱法。1.液固色谱法 使用固体吸附剂,被分离组分在色谱柱上分离原理是根据固定相对组分吸附力大小不同而分离。分离过程是一个吸附-解吸附的平衡过程。常用的吸附剂为硅胶或氧化铝,粒度5~10μm。适用于分离分子量200~1000的组分,大多数用于非离子型化合物,离子型化合物易产生拖尾。常用于分离同分异构体。2.液液色谱法 使用将特定的液态物质涂于担体表面,或化学键合于担体表面而形成的固定相,分离原理是根据被分离的组分在流动相和固定相中溶解度不同而分离。分离过程是一个分配平衡过程。 涂布式固定相应具有良好的惰性;流动相必须预先用固定相饱和,以减少固定相从担体表面流失;温度的变化和不同批号流动相的区别常引起柱子的变化;另外在流动相中存在的固定相也使样品的分离和收集复杂化。由于涂布式固定相很难避免固定液流失,现在已很少采用。现在多采用的是化学键合固定相,如C18、C8、氨基柱、氰基柱和苯基柱。 液液色谱法按固定相和流动相的极性不同可分为正相色谱法(NPC)和反相色谱法(RPC)。 正相色谱法 采用极性固定相(如聚乙二醇、氨基与腈基键合相);流动相为相对非极性的疏水性溶剂(烷烃类如正已烷、环已烷),常加入乙醇、异丙醇、四氢呋喃、三氯甲烷等以调节组分的保留时间。常用于分离中等极性和极性较强的化合物(如酚类、胺类、羰基类及氨基酸类等)。 反相色谱法 一般用非极性固定相(如C18、C8);流动相为水或缓冲液,常加入甲醇、乙腈、异丙醇、丙酮、四氢呋喃等与水互溶的有机溶剂以调节保留时间。适用于分离非极性和极性较弱的化合物。RPC在现代液相色谱中应用最为广泛,据统计,它占整个HPLC应用的80%左右。 随着柱填料的快速发展,反相色谱法的应用范围逐渐扩大,现已应用于某些无机样品或易解离样品的分析。为控制样品在分析过程的解离,常用缓冲液控制流动相的pH值。但需要注意的是,C18和C8使用的pH值通常为2.5~7.5(2~8),太高的pH值会使硅胶溶解,太低的pH值会使键合的烷基脱落。有报告新商品柱可在pH 1.5~10范围操作。正相色谱法与反相色谱法比较表 正相色谱法 反相色谱法固定相极性 高~中 中~低流动相极性 低~中 中~高组分洗脱次序 极性小先洗出 极性大先洗出从上表可看出,当极性为中等时正相色谱法与反相色谱法没有明显的界线(如氨基键合固定相)。
液相色谱柱决定最终分离效果,所以在选择色谱柱时候有必要考虑清楚自己的需求。 首先液相色谱柱目前来说分为正反相色谱柱,正相有SI等,反相有C18等。正相主要分离极性物质,反相主要分离非极性物质,氨基柱等主要分离二者之间的。 明确了色谱柱大概功能之后,确认下自己样品信息,基本就有点眉目了,方向对了,剩下的事情就是细节了如:键合相、粒径、孔径、碳载量等 键合相:确定了正反相后基本就简单了,正相很简单,我们重点讨论下反相,C18主要分离非极性和弱极性物质,因为是键合硅胶,所以C18也分好几种有常规的如C18-A,耐纯水的OL Apple C18-AQ、耐酸碱的OL Apple C18-EX等,如果发现C18保留很弱,调整流动相也不行,这个时候可以考虑C8甚至C4等。 粒径:色谱法追求的是高效、高分辨、高速等。目前来说亚2um填料或者2UM核壳填料是很理想的模型,基本具备“三高”特征尤其是高速,线速度不在影响分离度,不过附带的缺点就是高压,要升级相应的硬件,成本高昂,需要谨慎考虑。 5um填料最普遍,目前来说完全可以胜任各种日常检测,即使有特殊要求,3um色谱填料基本上也能全覆盖,不过该模型下线速度和分离度是成反比的。 孔径:目前很多60~300A都有,甚至更高或者更低的。开孔的填料多了个类似分子筛功能,所以选择孔径一定要关注分子量,蛋白(分子量5000以上)一般都需要在160A以上,多肽(分子量上限在3000左右)在120A左右,一般快速柱孔径都很小,可以缩短样品路径。所以国际上还有无孔硅胶柱子,也很适合蛋白分离,彻底解决蛋白分子量大和太粘稠堵住孔径问题。 碳载量:快速柱碳载量很低,如A家等,省时间,省溶剂,但分析部分复杂样品如中药等有点力不从心,这个时候可以考虑英国OL Apple色谱柱,碳载量15~23%,碳载量数值就像河床的水草,越高代表越密集,保留样品能力越强,越有可能分离开难分离物质。 以上信息仅供参考,个人能力有限,欢迎大伙补充!
液相色谱工作中和色谱柱有关的故障及解决办法1.保留时间漂移A 温度变化 设定一个恒定的温度,而且当室温较所需温度低时要注意提高柱温的设定值。B 流动相的问题使用预混合则要注意每次配液的准确性、精密度与pH值的变化;流动相被污染或加入添加剂后可能对待测组分存在干扰。流动相的pH值和样品的pK值太接近,即便是使用有缓冲盐的流动相也会引起保留时间的波动,流动相的pH值比待分离组分的pK值至少相差2个pH单位2.异常的色谱峰A 出现一个或几个负峰 流动相吸收本底高;进样过程中进入空气;由于样品中的某个组分的紫外吸收低于流动相的紫外吸收。B 均为负峰信号电缆接反或检测器输出极性设置颠倒;光学装置尚未达到平衡。C 均为宽峰系统未达到平衡;溶解样品的溶剂极性在于流动相极性;色谱柱尺寸及类型选择不正确;色谱柱或保护柱被污染或柱效降低;由于温度变化所产生样品粘度过大;进样器故障或进样体积误差;检测器设置不正确,定量环体积不正确;检测池污染;检测器灯出现故障。D 出现双峰或肩峰进样量或样品浓度过高;溶解样品的溶剂极性较流动相极性强;保护柱或色谱柱污染或失效或堵塞;过滤器堵塞;分析柱“柱头塌陷”。E 拖尾峰检测器设置不正确;进样体积太大或样品浓度太高。较早流出的峰拖尾,柱外效应引起的(检查液相色谱系统的毛细连接、毛细管及检测池);较晚流出的峰拖尾,待分离化合物和固定相表面非特异性相互作用(在流动相中加入三乙胺或醋酸盐或者选择合适的固定相可以改善)F 出现平头峰出现鬼峰可能为上次样品的残余。在每次进完样后需要用充足的时间来平衡和清洗整个系统;样品中存在未知物,改进样品的预处理;流动相污染,更换新流动相,尽可能做到流动相现配现,隔夜的流动相应放入冰箱储存再次使用时要进行过滤,尽可能使用HPLC级试剂。贴心提示: ①保留时间没有规律的变化说明色谱柱没有充分平衡。随着色谱柱使用时间的增加,保留时间会前移,特别是当流动相的pH值为酸性时(pH≤2)。如果突然发生明显变化,一般由于系统的问题。②以上的问题只是工作中常见的部分问题,如有未提及的问题出现,请咨询您的供应商或厂家技术服务人员。③液相色谱故障排除时不应以问题的表征消失而告终,应该着重于在众多可能的因素中找出问题的根源、每次仅改变一个因素,系统地将问题定位,直至最终筛选出真正产生故障的因素④将换下来的有问题的部件扔掉,以免和其他好的混淆。保留的旧部件请用标签做好标记。⑤实验室应该具有优良的预防性的维护措施合严格周密的记录。对于常规分析,我们应该大致了解一根柱子/预柱可以进样多少针,这样可以将问题发生的频率最小化。
高效液相色谱(HPLC:High Performance Liquid Chromatography )是化学、生物化学与分子生物学、医药学、农业、环保、商检、药检、法检等学科领域与专业最为重要的分离分析技术,是分析化学家、生物化学家等用以解决他们面临的各种实际分离分析课题必不可缺少的工具。国际市场调查表明,高效液相色谱仪在分析仪器销售市场中占有最大的份额,增长速度最快。 高效液相色谱的优点是:检测的分辨率和灵敏度高,分析速度快,重复性好,定量精度高,应用范围广。适用于分析高沸点、大分子、强极性、热稳定性差的化合物。其缺点是:价格昂贵,要用各种填料柱,容量小,分析生物大分子和无机离子困难,流动相消耗大且有毒性的居多。目前的发展趋势是向生物化学和药物分析及制备型倾斜。7.1 基本原理 加样 流动相 固定相 流动相 A A B C B C B A 固定相 —— 柱内填料,流动相 —— 洗脱剂。HPLC是利用样品中的溶质在固定相和流动相之间分配系数的不同,进行连续的无数次的交换和分配而达到分离的过程。通常,按溶质(样品)在两相分离过程的物理化学性质可以作如下的分类:分配色谱:—— 分配系数亲和色谱:—— 亲和力吸附色谱:—— 吸附力离子交换色谱:—— 离子交换能力凝胶色谱(体积排阻色谱):—— 分子大小而引起的体积排阻分配色谱又可分为: