[color=#444444][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]6820型号,柱子是TD-5,主要分离俩个反应体系,一个是苯甲醛和丙二睛在甲苯中的 反应,另一个是苯甲醛和氰乙酸乙酯在甲苯中的反应,或者这俩种反应在水或者乙醇中的反应, 怎样建立方法 能将其分离开?谢谢了[/color]
目的:建立一个[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件同时分离测定环孢素A中乙醇及丙二醇的含量。方法:以GDX-101为固定相,柱长为2 m,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,氮气为载气,以二甲基亚砜为溶剂,以正丙醇为内标。结果:乙醇及丙二醇进样量分别在2.0~6.0 μg,1.0~3.0 μg,其峰面积与浓度呈良好的线性关系,加样回收率分别为99.9%(RSD<0.8%,n=5),101.4%(RSD<1.1%,n=5),精密度良好。结论:此[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件可同时测定环孢素A中乙醇及丙二醇的含量,方法简便准确。关键词 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 乙醇 丙二醇 环孢素A山地明(环孢素A)为诺华制药有限公司的产品,是一种免疫抑制剂,用于器官移植和骨髓移植中的抑制排斥现象以及自身免疫疾病。厂方质量标准中乙醇及丙二醇的含量采用石英毛细管柱测定,此种色谱柱在国内使用不普及,我们经多次试验,摸索出一较好的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件,适用于国内检测,即以GDX-101为固定相,柱长为2 m,采用氢离子火焰检测器,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,氮气为载气,以二甲基亚砜为溶剂,以正丙醇为内标,可同时分离测定环孢素A中乙醇及丙二醇的含量,改进后的方法,乙醇与正丙醇的分离度为3.1,丙二醇与正丙醇的分离度为5.0,符合中国药典1995年版中乙醇量度检查的分离度要求[1],操作简便,结果准确可靠。1 仪器与试药 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]:SP-6890 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱:玻璃柱,长2 m,固定相为GDX-101。 乙醇、异丙醇、丙二醇均为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]纯,二甲基亚砜为色谱纯。 样品:环孢素A胶囊(山地明),由诺华公司提供,批号为187MFD0797;241MFD0797;166MFD0797;483MFD0797;477MFD0797。 标准贮备液及内标贮备液:精密称取[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]级的乙醇及丙二醇2.50及1.25 g分置50 mL容量瓶中,加二甲基亚砜至刻度,摇匀,作为标准贮备液;精密量取正丙醇5.0 mL置50 mL量瓶中,加二甲基亚砜至刻度,摇匀,作为内标贮备液。2 试验方法与结果2.1 色谱条件 采用GDX-101为固定相,柱长为2 m,氮气为载气,采用氢离子火焰检测器,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,即初始为165 ℃,保持12 min,以40 ℃。min-1升至280 ℃,并保持20 min,检测器温度为280 ℃,进样量为2 μL。2.2 分离度试验 称取乙醇、丙二醇及正丙醇各50 mg置同一50 mL量瓶中,加二甲基亚砜至刻度,摇匀,进样2 μL,按上述色谱条件试验,记录色谱图,见图1-A,乙醇、丙二醇及正丙醇的保留时间分别为1.15,2.22,7.54 min,计算乙醇与正丙醇及丙二醇与正丙醇的分离度,其分离度分别为3.1和5.0。图1 分离度色谱(A)及样品测定(B)色谱图1.乙醇 2.正丙醇 3.丙二醇 4.二甲基亚砜2.3 线性范围及标准曲线 分别精密量取乙醇和丙二醇标准贮备液1.0,1.5,2.0,2.5,3.0 mL,分别置50 mL量瓶中,并分别加入内标贮备液1.0 mL,使乙醇终浓度为1.0,1.5,2.0,2.5,3.0 mg.mL-1,丙二醇的终浓度为0.5,0.75,1.0,1.25,1.5 mg.mL-1,分别进样2 μL,以乙醇及丙二醇的进样量为横坐标,以它们的峰面积与内标峰面积之比为纵坐标,分别进行线性回归,结果线性关系良好,乙醇、丙二醇回归方程分别为:A=8.935×103C+7.858×102 r=0.998 8A=8.086×103C-1.649×102 r=0.999 92.4 精密度试验 用乙醇与丙二醇浓度分别2.0及1.0 mg.mL-1的溶液,重复进样5次,结果乙醇与丙二醇的RSD分别为0.7%和1.0%,精密度良好。2.5 回收率试验 采用加样回收法,取已知乙醇与丙二醇含量的样品2粒,用二甲基亚砜溶解,置50 mL量瓶中,精密加入内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,精密量取此溶液4.0,4.5,5.0,5.5,6.0 mL,分别加入乙醇与丙二醇的浓度分别为2.0 mg.mL-1及1.0 mg.mL-1的标准溶液6.0,5.5,5.0,4.5,4.0 mL,混匀,量取混匀后的溶液2 μL,注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],测定这5份溶液的乙醇和丙二醇含量,计算回收率,乙醇的平均回收率为99.9%(RSD<0.8%,n=5),丙二醇的平均回收率为101.4%(RSD<1.1%,n=5)。2.6 样品的测定 取乙醇和丙二醇标准贮备液2.0 mL,内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,作为对照品溶液;取环孢素A胶囊2粒,置50 mL量瓶中,用二甲基亚砜溶解,精密加入内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,作为样品溶液;分别量取对照品溶液和样品溶液各2 μL,注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],按上述色谱条件测定,以内标法计算含量,即得;见图1-B。2.7 对比试验结果 取环孢素A样品5批,用改进后的方法测定样品中乙醇和丙二醇的含量,与厂方测定数据相比,结果基本吻合,见表1。表1 乙醇和丙二醇对比试验结果(%) 批号 本法结果 厂方测定数据 乙醇 丙二醇 乙醇 丙二醇 187MFD0797 101.0 106.3 100.5 105.0 241MFD0797 99.2 99.2 100.6 100.6 166MFD0797 101.7 102.7 101.3 103.0 483MFD0797 98.8 96.8 99.3 97.2 477MFD0797 99.1 98.1 98.9 97.7 3 讨论3.1 本法与原厂方方法相比,方法更为简便,条件普及,有利于对样品质量的控制。3.2 原厂方标准在测定乙醇含量时,以正丁醇为溶剂,由于正丁醇的保留时间与丙二醇过于接近,分离度达不到要求,本法采用二甲基亚砜为溶剂,不影响样品的溶解,同时使丙二醇与二甲基亚砜的分离度符合定量分析的要求。3.3 曾用固定相为GDX-401的[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]柱进行检测,乙醇与正丙醇得到完全分离,但丙二醇与溶剂峰重叠,分离度达不到要求。3.4 采用程序升温,可使溶剂出峰时间加快,缩短分析时间。王俊秋(北京市药品检验所 北京 100035)庞青云(北京市药品检验所 北京 100035)余立(北京市药品检验所 北京 100035)参考文献1,中国药典.1995.二部:附录44
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]是一种物理的分离方法。利用被测物质各组分在不同两相间分配系数(溶解度)的微小差异,当两相作相对运动时,这些物质在两相间进行反复多次的分配,使原来只有微小的性质差异产生很大的效果,而使不同组分得到分离。

[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离氧气、氮气、一氧化碳、二氧化碳、丙烯、丙烷,什么色谱柱能分离,或者用什么方法把他们分离定量。求大神帮忙,小女子不胜感激....
各位大侠好!今天在百度上搜到 采用气相色谱分离技术(无需“加液” )制氮:内容如下 这是一种新型的空气分离方法,它以压缩空气为原料,合成分子筛为吸附剂,采用气相色谱柱吸附流程,在常温压力下,利用空气中的氧和氮在分子筛中的扩散速度不同,把氧和氮加以分离,氮气的纯度和产气量可按客户需要调节。所产生气体流速稳定,氮气纯化彻底,产出的氮气纯度高,最高可得到99.9995%的纯氮,适用于各种气相色谱检测器。该系列高纯发生器只要一按开关,便可以源源不绝的生产出高质量和高纯度的氮气,运行稳定可靠,最重要的是它不需要任何化学消耗品。 操作方便,可24小时无人值守。且它可以在不需任何监管和最低保养的情况下无故障地运行。 其中有2个问题不明白1、合成分子筛为吸附剂,这是什么牌号的分子筛? 2、既然是通过分离技术,怎样确定在什么时间内取到比较纯的氮气?我对这个不了解,期待高手指教。
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离异丙醇和水用什么方法合适?GDX-301填充柱可不可以分离?
要正确地选择色谱分离方法,首先必须尽可能多的 了解样品的有关性质,其次必须熟悉各种色谱方法的主要特点及其应用范围。选择色谱分离方法的主要根据 是样品的相对分子质量的大小,在水中和有机溶剂中的溶解度,极性和稳定程度以及化学结构等物理、化学性质。一、相对分子质量对于相对分子质量较低(一般在200以下),挥发性比较好,加热又不易分解的样品,可以选择[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法进行分析。相对分子质量在200 ~ 2000的化合物,可用液固吸附、液-液分配和离子交换色谱法。相对分子质量高于2000,则可用空间排阻色谱法。二、溶解度水溶性样品最好用离子交换色谱法和液液分配色谱法;微溶于水,但在酸或碱存在下能很好电离的化合物,也可用离子交换色谱法;油溶性样品或相对非极性的混合物,可用液-固色谱法。三、化学结构若样品中包含离子型或可离子化的化合物,或者能与离子型化合物相互作用的化合物(例如配位体及有机螯合剂),可首先考虑用离子交换色谱,但空间排阻和液液分配色谱也都能顺利地应用于离子化合物;异构体的分离可用液固色谱法;具有不同官能团的化合物、同系物可用液液分配色谱法;对于高分子聚合物,可用空间排阻色谱法。
[align=center][b][size=24px]白酒分析气相色谱仪分离条件的选择[/size][/b][/align][size=18px] 气相色谱仪分析白酒时,除了选择适合的色谱柱和分析方法外,还要选择好分离的蕞佳操作条件,提高色谱柱的分离效能,增大分离度,获得好的分析结果。色谱技术人员根据实际经验总结出白酒分析气相色谱仪分离条件选择,供大家参考。1. 载气及流速、分流比的选择白酒的气相色谱分析,一般使用FID检测器,常用高纯N2做载气,H2做燃烧气,空气作助燃器。若使用一般填充色谱柱,内径在3~4mm,载气的流量在20~100m L/min。对于内径在0.25mm左右的毛细管色谱柱,载气流量在1~2m L/m in。流速太快会降低色谱柱的分离效能,一般高于蕞佳流速10%左右即可,既保证了色谱柱的分离效能,又能获得比较快的分析速度。H2的流速与载气N2流速相当(毛细管色谱柱载气流量+载气分流的流量),实验证明H2流量∶空气流量=1∶10时,FID检测器蕞灵敏。使用毛细管色谱柱时,分流比的选择直接影响到出峰的个数与分离效果。当分流比为30∶1时蕞为恰当,色谱柱分离效能较高,白酒微量成分分离效果好。载气中微量水分、氢气和空气中的微量杂质对色谱柱和检测器影响很大,严重时会使色谱柱失效,基线不稳,噪声增大,检测器灵敏度下降。所以在载气、H2、空气进入色谱仪之前,应当使用分子筛、硅胶等对气体进行净化处理。2. 色谱柱温的选择白酒中的大部分组分沸点都不高,但沸点范围较宽,为了使低沸点的组分有比较好的分离度,一般初始柱温在50℃。程序升温速度不宜过快,否则分离效果变差,程序升温速度太低,出峰时间长,峰形扁平。一般设定在1~8℃/m in,蕞佳程序升温速度在8℃/m in左右,以保证白酒中各组分在相应的温度下得到良好的分离。蕞终温度不能太高,一般不超过250℃,防止色谱柱温过高,引起固定液挥发流失,分离效能变差,出现基线漂移,或导致色谱柱失效。3. 气化室、检测器温度选择白酒的气相色谱分析中,气化室温度一般高于色谱柱温度50~60℃以上,一般控制在120~200℃,以保证进样时白酒试样中所有的组分都能瞬间变成气体。FID检测器的温度通常控制在150~250℃,避免水蒸汽在检测器中凝结,增大噪声而降低检测器的灵敏度,也可以避免出现检测器点火困难的问题。4. 进样量和进样速度的控制使用填充色谱柱时,柱容量比较大,进样量通常在1~5μL,使用10μL或5μL的微量注射器。采用毛细管色谱柱时,柱容量小,进样量通常在0.1~2μL。进样量低不利于使用低含量组分法进行检测,进样量过高则会导致部分组分峰发生重叠,分离不好。进样速度要求比较快,要求1 s内完成,以保证酒样瞬间气化。如果进样速度太慢,就会引起先插进去的针头部分的酒样先气化,导致色谱峰变宽或者异型,峰形不好,分析误差大的问题。每次进样时,应将微量注射器用被测酒样抽洗5次以上并排净气泡,保证待测试样浓度不发生变化,减少进样带来的误差。5. 其他注意事项为了尽可能地减少分析误差,保证分析结果的准确性,要定期老化色谱柱,在高于使用温度20℃,脱开检测器,通以载气10 h以上,让色谱柱中残留的高沸点组分流出,降低仪器噪声,减小高沸点残余物质的干扰。同时还要定期清理色谱柱头和衬管中积累的不挥发物,防止堵塞色谱柱。每进样50次左右就需更换气化室中的硅橡胶垫,保证气化室不漏气,避免出现色谱峰异常现象。在白酒的气相色谱仪分析中,适当地选择分析方法与测定条件,既可以提高色谱分析的分离效能与检测的灵敏度,又可以提高分析结果的准确度。这就需要我们在实际工作中不断探求与创新,找出每种酒样的蕞佳分析条件,做到准确而快速地分析白酒的微量成分,有效地指导白酒的生产、研发和质量监督,保障白酒的食品安全。[/size]
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]是一种物理的分离方法。利用被测物质各组分在不同两相间分配系数(溶解度)的微小差异,当两相作相对运动时,这些物质在两相间进行反复多次的分配,使原来只有微小的性质差异产生很大的效果,而使不同组分得到分离。
采用配备DB-FastFAME Intuvo [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]系统快速分离脂肪酸甲酯。脂肪酸甲酯 (FAME) 的分析可用于鉴定食品中的脂类组分,是食品分析中最重要的应用之一。采用本方法实现快速、良好的分离效果。对油类、脂肪和含脂食品的分析是政府实验室、质量控制 (QC) 实验室或合同研究组织 (CRO) 实验室的常见任务。测定食品中的总脂肪与反式脂肪含量时,对脂肪酸及其 FAME 衍生物的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]分析是脂肪表征的重要工具。在许多用于食品(如食用油)检测的法规方法中,测定脂肪酸组成时都要求使用涂覆氰丙基固定相的毛细管柱对特定的顺反脂肪酸异构体进行分离。此外,实现良好的 FAME 分离还需较长的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱(100 米)和较长的分析时间(超过 70 分钟)。然而,这种方法分析效率较低且分析成本较高。而采用氰丙基固定相的 DB-FastFAME Intuvo [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱,可实现 FAME 混合物的快速分离(包括分离一些关键顺反异构体),且能满足法规方法的要求。本文简述了采用 DB-FastFAME Intuvo [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱和[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]系统快速分析FAME 混标。[img]https://i5.antpedia.com/attachments/att/image/20200216/1581861033964746.png[/img]实验部分试剂与标准品FAME 36 组分混合物(部件号 5191-4276)、C4–C24 偶数碳饱和 FAME 混合物(部件号 5191-4278)和菜籽油 FAME混合物(部件号 5191-4277)均来自安捷伦科技公司。37 组分 FAME 混标(部件号 CDAA-252795-MIX-1 mL)购自上海安谱科学仪器有限公司。将 C4–C24 偶数碳饱和 FAME 混合物用己烷稀释至 500 μg/mL。菜籽油 FAME混合物为 100 mg 净混合物,用二氯甲烷稀释 20 倍。[img]https://i5.antpedia.com/attachments/att/image/20200216/1581861033868195.png[/img]仪器使用配备火焰离子化检测器 (FID) 的Intuvo 9000 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]进行分析。使用配备 5 μL 进样针(部件号 G4513-80213)和分流/不分流进样口的 Agilent 7693A 自动液体进样器进样。实验步骤将标准样品用与之相对应的方法进行进样分析,检测方法如表1-表5所示。[img]https://i5.antpedia.com/attachments/att/image/20200216/1581861033863172.png[/img]结果与讨论FAME 36 组分混标专门为模拟多种食品样品的脂肪酸组成而设计,可用于鉴定多种食品中的关键 FAME。该混标中包含 C4:0至 C24:1 范围的 FAME,包括多数重要的饱和、单不饱和及多不饱和 FAME。该混标不包含以前用作内标的一种 FAME,即二十三烷酸甲酯 (C23:0),。图 1所示为 FAME 36 组分混合物在 20 m ×0.18 mm、0.20 μm DB-FastFAME Intuvo[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱上的分离结果,图2所示为菜籽油按方法1进行分析的结果。该方法采用氦气作为载气,可在 5 分钟内实现所有化合物的分离,包括关键 AOAC 对,R s 1.5。采用这种方法获得了良好的峰形和分离度,且分析时间为 5 分钟。采用氢气作为载气,可在 4 分钟内完全分离 C4–C24 偶数碳饱和 FAME 混合物和 FAME 36 组分混合物(图 3 和图 4)。这表明使用该色谱柱可实现快速样品通量,且分离度不受影响。[img]https://i5.antpedia.com/attachments/att/image/20200216/1581861033504634.png[/img] 对于使用传统 37 组分 FAME 混标验证其FAME 方法的实验室,图 5 展示了在 Intuvo9000 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]上使用 20 m × 0.18 mm、0.20 μm DB-FastFAME 色谱柱得到的色谱图。该方法采用氦气作为载气,在 8 分钟内实现了所有化合物的完全分离。 与预期结果一样,采用氢气作为载气可加快分析速度,而分离度几乎相同。图 6所示的结果表明,采用氢气作为载气可在6.5 分钟的分析时间内实现 37 组分 FAME混标中所有化合物的完全分离。[img]https://i5.antpedia.com/attachments/att/image/20200216/1581861033301731.png[/img]结论DB-FastFAME Intuvo [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱可快速、出色地分离 FAME 混合物。实验表明,采用氦气作为载气时,DB-FastFAME Intuvo [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱可在 5 分钟内完全分离 FAME 36 组分混合物中的所有组分,包括关键 AOAC 对和关键顺反脂肪酸异构体。本实验也表明,此方法还能实现菜籽油的快速分析。采用氢气作为载气时,这种高效的 DB-FastFAME Intuvo[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱将运行时间缩短至 4 分钟以内,同时实现了所有化合物的基线分离。
[color=#444444]我现在用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离乙二醇与正丁醇(色谱柱:KB-5MS,柱温:90℃,进样口:250℃,检测器:250℃),两者能够分离,正丁醇的峰型还可以,但是乙二醇的峰拖尾很严重。。。。在不换色谱柱的条件下,有没有更好的方法,使得乙二醇的峰不拖尾。。。。请各位支招。。。谢谢了。。[/color]
[color=#444444]我现在用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离乙二醇与正丁醇(色谱柱:KB-5MS,柱温:90℃,进样口:250℃,检测器:250℃),两者能够分离,正丁醇的峰型还可以,但是乙二醇的峰拖尾很严重。。。。在不换色谱柱的条件下,有没有更好的方法,使得乙二醇的峰不拖尾。[/color]
小弟在此请教给位大虾FFAP毛细柱是否可以用来分离分析苯系物? 现有天美7890II型气相色谱仪(国产),无EPC控流,配有FID检测器,FFAP毛细柱。如果可以的话,能不能提供一些方法经验供小弟参考。 谢谢!
就GC色谱柱固定相的膜厚而言,其可能会以不同方式影响早期和之后洗脱峰的柱效,k'值5时反之亦然。但是,除非大幅度改变膜厚度(例如,从0.1mm改变为1mm),否则改变膜厚度的效果不会太剧烈。 这些值在等温分离中适用,而在梯度温度编程分离中则不同,但是趋势仍然适用。 综上所述的信息将使我们可以估计我们选择用于分析的色谱柱的预期塔板数,从而可以评估效率,因此,偏离这些预期值的任何重大偏差都可以视为值得研究与故障排除。 关于[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]效率的基本理论的最后一部分是所选载气的影响及其通过色谱柱的流速。从图3可以看出,各种载气在不同载气线速度下的效率最高(最低高度相当于理论塔板(HETP,H))。线速度是色谱柱内径和流速的函数。 我们之所以特别提到这一点,是因为有一些非常普遍的问题与无法通过仪器设置达到最佳效率有关。以下几点尤其值得注意: 需要检查所用色谱柱的线速度和所需的载气流速,以确保该组合产生最佳效率和最低的板高度(如图3中的蓝色区域所示)。氢气显示出约50 cm / sec的最佳线速度,氦气显示出30 cm / sec的最佳线速度,氮气显示出15cm / sec的最佳线速度。载气的线速度将通过数据采集系统或仪器前面板显示。 确保色谱柱尺寸在采集方法中设置正确(包括通过调整色谱柱长度进行的任何调整)。如果色谱柱尺寸不正确,则载气通过色谱柱的线速度将不正确,分离效率将受到影响。 当然,如果将不正确的色谱柱尺寸或载气设置到仪器中,我们可能会看到除了色谱效率降低之外,保留时间也会改变,这些变化将是一个很好的诊断线索。 除了这些方法上的考虑之外,还有哪些其他因素会导致分离效率降低?这个问题有很多答案,但是,我在下面概述了导致柱效率降低的一些常见问题。 1 柱安装问题: 确保正确准备(切割和清洁)GC色谱柱并以正确的方式将其安装到GC进样口和检测器中,这一点非常重要。色谱柱切割不良会导致样品入口内部分析物的转移变慢,如果该方法未建立热聚焦或溶剂聚焦过程,则可能导致峰变宽。通常,此问题还将伴随某种程度的峰分叉或拖尾。 色谱柱在进样口和检测器中的正确定位也至关重要。入口色谱柱的位置将再次使分析物最佳地转移到色谱柱中,当以分流模式操作入口时尤其重要。色谱柱在检测器中的位置将决定色谱柱出口与仪器内检测区域之间未清扫体积的量。这一点特别重要,因为载气是存在分散展宽,任何空隙体积都会对系统效率产生不利影响。 2 色谱柱污染和老化: 所有GC色谱柱都会老化,并且使用寿命有限。随着时间的流逝,色谱柱的入口端可能会被样品基质成分覆盖,固定相可能会被破坏,这通常会导致固定相在色谱柱下方“蠕变”,从而形成一个较厚的“气泡状”可降分离效率的固定相区域。样品遇到的色谱柱初始区域对于色谱质量至关重要,因此,我们必须确保该区域的相质量是原始的。通常,通过修整较短的色谱柱并重新安装可以解决此问题,并且可能需要一部分或更多的色谱柱修整才能恢复性能。始终修剪最少的量以恢复良好的性能,如果进行了重大修剪,请不要忘记调整仪器内的色谱柱长度,以确保保留时间重现性和正确的载气线速度。在载气供应管线中安装气阱总是一个很好的解决办法,以确保色谱柱(相)的寿命(最小的水分和氧气阱),并确保以正确的方式调节色谱柱。 适当的样品预处理对于色谱柱的使用寿命也很重要,在分析之前制备清洁的样品,会延长色谱柱的使用寿命,减少进样口维护操作。 3 样品引入条件: 影响分离效率的因素很多,都与将样品引入GC系统的方式直接相关。进样口衬管的清洁度和失活是主要考虑因素,在分流进样中,衬管中的任何活性部位的破坏可能会影响分析物向GC色谱柱顶部的转移,这在处理极性分析物时尤为明显。如果衬管清洁度不高或未显示出来,则衬管清洁度通常与峰拖尾有关仅出现轻微的活动迹象(失活涂层消失),然后可能会导致峰的总体变宽。确保衬管清洁,并在必要时定期更换衬管。 以下是重要的要点总结: 维持足够长的不分流时间,以将所有分析物转移至色谱柱,但也应足够短,以免溶剂从进样口缓慢流失,从而导致色谱破坏,柱箱的初始温度应至少比样品溶剂的沸点低10 ℃,固定相的极性应与样品溶剂的极性相匹配,反之,则应在进样口和分析柱之间留出至少1 m长的未涂层保留间隙。如果不满足,上述条件将导致分析物峰形展宽,这主要是由于分析物谱带从入口缓慢进入GC色谱柱时缺乏聚焦,因此效率会降低。 1 热点: 重要的是,在载气中通过系统的分析物必须以不间断的方式进行。因此,气流路径中任何比其周围环境凉爽的“斑点”都将破坏或减慢分析物通过色谱柱的通过,并有效地充当系统中死体积的区域。 如果消除了进样口和GC色谱柱之间的热滞后,通常在进样口上会出现冷点-杯内有滞后的小杯位于进样口下方是有原因的,因此不应将其移除。位于检测器单元下方的绝缘层也是如此,这也是为什么进入MS检测器的任何传输线也要分别加热的原因,应仔细检查传输线温度以确保其温度至少位于顶部温度与您的烤箱程序一致! 2 温度程序: 由于不当的温度程序将造成许多不良的分离。当考虑初始柱箱温度和分批进样的保持时间时,尤其如此。如前所述,程序升温的分离确实会产生更高效的峰,尤其是对于后来的洗脱组分,但是确保初始程序条件适合被测样品和分离的要求以及分离条件至关重要。样品引入方法,不分流或不分流进样。对于分流进样,通常的规则是我们不希望过慢的“分析物”穿过色谱柱的过程太快,因为会发生过量的样品分散。理想情况下,初始温度应比色谱图中第一种组分的洗脱温度低45℃左右,这可以通过筛选实验计算得出(典型值为50 ℃至色谱柱的梯度上限,每分钟10℃)。然而,作为初始保留时间,这实际上是一个反复试验的问题,从保留1分钟开始,然后提高或降低初始保留时间,以评估对选择性,效率和分离度的影响。 3 检测器采样率: 任何色谱系统中峰的正确“建模”将取决于跨峰捕获的数据点的数量。对于高效技术(例如毛细管[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]),必须特别注意检测器的采样频率,而质谱检测器尤其如此,质谱检测器的固有采样频率往往较低,尤其是在全扫描模式下。如果检测器仅捕获跨越峰的几个数据点,尤其是当峰顶点被检测器遗漏时,则它们看起来可能比其宽。请按照制造商的说明为使用中的检测器找到最佳采样频率。 无论如何,建议在新色谱柱保留常规方法的参考色谱图,该色谱图可用作评估柱效率随时间下降的幅度的参考。使用系统适应性测试(SST),也是明智的选择,以便在分析之前评估仪器的性能,并且柱效评估通常是SST的考察指标之一。 尽管柱效是毛细管[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法成功分离的关键驱动力,但从以上讨论中可以明显看出,在解决低柱效问题时要考虑许多因素。大多数问题是由仪器设置和GC色谱柱的老化引起的,因此对方法中的设定点进行故障排除以及色谱柱与进样口维护,是进行柱效诊断研究的考虑要点。
在测试中心液相色谱组呆了20多年,见过无数的客户,不同的客户对色谱的理解不一。很多人认为色谱就是打一针,出个谱图而已,容易的很,跟他们的科研档次无法比。觉得样品给你了,你必须做出来,而且很快得到其所需要的结果,全然不管你的仪器能否满足要求。做不好或者不想做,就会去告状,服务态度不好之类的。所以一旦征求意见,必然出现各种各样的服务问题。测试人员的地位在学校可见一斑。也有少数本身做液相色谱的,这些人沟通起来非常融洽,因为知道其实际做起来不容易,可惜这类的客户仅有百分之几。在色谱分析的三大分支中,我对液相、离子熟悉,对气相只是很了解,没动手做过。对于这三大类型,其实在实际中做的差别是很大的。先以我精通的离子色谱而言,我几乎涉及了所有的类型,离子色谱能否做关键在于设备,常规的很简单,特殊的全靠设备支撑,因为大部分离子色谱的分析都是优化的方法,固定的模式做起来并不难。但非常规的样品,则难度大大增加,即使同一个组分,由于基体差别,分析方案也是千差万别。也就是常规的很简单,特殊的则很难。现在厂家离子色谱方法开发就是一种特化的过程。离子色谱主要分析离子以及一些极性的化合物,表面上看应用范围比较窄,其实在很多领域有很好的应用,可以解决液相色谱无法解决的一些问题。对于气相色谱,复杂性比离子色谱要高,因为被测的有机化合物种类大大增加,但从气相的结构看,其载气的选择是非常有限的,主要靠色谱柱(极性,非极性,弱极性等),分离则依赖温度的程序升温,它真正的变化在色谱柱,在一般的分析中,大多变化在温度,柱子的变化并不多。因此对于气相色谱,基本就几根柱子。当然一些特别的检测则需要更高级特殊的装置,这跟离子色谱一样。由于受沸点的制约,气相色谱的应用受到很大的限制。而对于液相色谱,就我20年的经历,我认为其复杂性远远高于离子色谱和气相色谱。因为其变化比前二者更多,一是液相色谱分离有很多机理,每种机理都有对应的色谱柱类型,液相色谱的分离机理大约有十来个,很少有人会用过全部机理类型的色谱柱。虽然反相是最常见的分离手段,但由于反相的广泛使用,C18柱的变化类型极多差异很大,这不同C18柱之间的差异有时不亚于不同机理之间的差异。二是,液相色谱最大变化是流动相,不仅有机相类型有变,添加剂类型和浓度有变,不同pH差别很大,面对变化无穷的样品,这个流动相选择变化规律全靠长期的经验积累,很难用文字一言以蔽之。三是,液相色谱的检测器类型最多,离子色谱就三种,气相四五种,而液相色谱的检测器有十来种,相互之间差别极大,不同的检测器对色谱分离机理也有很大的选择性。因此要做好一张液相色谱图,很多情况下只能是你现有条件下的最佳分离,并不是这个化合物的最佳分析条件。对于特殊样品的分析,液相色谱更多的依赖于检测器和柱子的变化,同离子色谱不同。给你一个样品,用那类色谱(液相、气相还是离子),什么柱和条件,则完全依赖你的功底和阅历,当你拥有尽可能多的仪器装备,你才能充分发挥你的能力,依据化合物的特点,样品的特性,选择合适的仪器和配置,做出最佳的色谱图。
气相色谱法的分离原理
我想请教一下如何设置升温程序和载气流速以提高[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的分离度?我现在需要分离一个顺反异构体,设了好多方法都分离不好,需要您们的帮助!
RCONH22 确定初始操作条件主要包括进样口温度、检测器温度、色谱柱温度和载气流速。分流进样的进样量一般不超过2μL ,最好控制在 0 .5 μL 以下 ,进样量还和分流比有关 ,分流比大时 ,进样量可大一些 ;进样口温度应接近或高于样品中最重组分的沸点 ;对于一个未知的新样品, 可将进样口温度设置为 300 ℃;常用毛细管GC 所用柱内载气线流速为:氮气 20~40 cm/s。隔垫吹扫设定为 2 ~5 mL/min , 分流比依据样品情况(如待测组分浓度等)、进样量大小和分析要求来改变, 选择一个合适的折衷分流比,用分流比范围 20∶1 ~200∶1 ,待测组分浓度大或进样量大时, 分流比可相应增大,反之则减小,用大口径柱时分流比小一些,用微型柱做快速GC 时,分流比要求很大,流比小时, 分流歧视效应可能小,但初始谱带(主要是溶剂谱带)宽度大,分流比大时,初始谱带(主要是溶剂谱带)宽度小,但分流歧视效应可能大。检测器温度可参照色谱柱的最高温度设定,而不必优化。色谱柱温度,组成简单的样品最好用恒温分析;组成复杂的样品,常需要用程序升温分离;色谱柱的初始温度应接近样品中最轻组分的沸点, 最终温度取决于最重组分沸点;升温速率依样品的复杂程度而定,建议毛细管柱的尝试温度条件设置为OV -1或SE-54 柱 :从 50 ~280 ℃,升温速率 10 ℃/min ,V - 17(OV -1701)柱:从60 ~260 ℃, 升温速率 8 ℃/ min ,PEG -20M 柱:从60 ~200 ℃,升温速率 8 ℃/ min 。这是方法开发时的初始参考条件,具体工作中再根据样品的实际分离情况来优化设定。3 尝试性分析上述初始条件设定后,便可以进行样品的尝试性分析。一般先分离标准样品,然后分析实际样品。在此过程中,还要根据分离情况不断进行优化。GC的分离优化就是要在保证分离度和灵敏度的前提下,实现快速分析。在实际工作中,一般是首先满足分离度的要求,然后提高分析灵敏度,最后再考虑尽可能缩短分析时间。改变柱温和载气流速可改变分离度;内径越小,或者填料粒度越小,柱效越高;薄液膜色谱柱的柱效高于厚液膜柱;更换色谱柱可改变分离度;用化学作用如通过生化反应改变待测物结构;程序升温是GC分离复杂混合物的有效方法;进样量小一些、进样口温度高一些、载器气流速快一些、汽化室体积小一些,分流比大一些,对窄的初始谱带宽度有利。4 气相色谱定性与定量分析对于简单的样品,可通过标准物质对照来定性。对于复杂的样品, 则要通过保留指数定性和或GC/MS来定性。对于基层监测站,气相色谱定性分析最主要是依据保留值定性,即在相同的条件下,分别注入标准样品和实际样品,根据保留值确定色谱图上哪个峰是要分析的组分。但必须注意,在同一根色谱柱上,不同的化合物可能有相同的保留值,对未知样品的定性仅仅用一个保留值还不够。双柱或多柱保留指数定性是气相色谱定性分析较为可靠的方法,不同的化合物在不同色谱柱上具有相同保留值的几率要小的多。建议对复杂的样品采用双柱或多柱保留指数法定性。气相色谱定量方法包括面积百分比法、归一化法、外标法、内标法、标准加入法。基层监测站最常用的方法是外标法,只要用一系列浓度的标准样品做出工作曲线, 就可以在完全一致的条件下对未知样品进行定量

难分离物质最佳气相色谱分离条件的选择http://ng1.17img.cn/bbsfiles/images/2012/05/201205281617_368943_2019107_3.jpg
[align=center][b][size=24px]气相色谱仪分析的定性依据及定性方法[/size][/b][/align][color=#000000] [size=18px]气相色谱仪[/size][/color][size=18px]的色谱分析包括色谱定性分析和定量分析。今天为大家浅析气相色谱仪的定性分析依据和定性分析方法,仅供色谱工作者参考交流。 (一)气相色谱仪的定性分析依据:气相色谱主要功能不仅是将混合有机物中的各种成分分离开来,而且还要对结果进行定性及定量分析。所谓定性分析就是确定分离出的各组分是什么有机物质,而定量分析就是确定分离组分的量有多少。色谱在定性分析方面远不如其它的有机物结构鉴定技术,但在定量分析方面则远远优于其它的仪器方法。 有机物进入气相色谱后得到两个重要的测试数据:色谱峰保留值和面积,这样气相色谱可根据这两个数据进行定性定量分析。色谱峰保留值是定性分析的依据,而色谱峰面积则是定量分析的依据。 (二)气相色谱仪定性分析方法:气相色谱的定性分析方法主要有保留值定性法、化学[color=#000000]试剂[/color]定性法和检测器定性法。气相色谱的保留值有保留时间和保留体积两种,现在大多数情况下均用保留时间作为保留值。在相同的仪器操作条件和方法下,相同的有机物应有同样的保留时间,即在同一时间出峰。但必须注意:有同样保留时间的有机物并不一定相同。 气相色谱保留时间定性分析方法就是将有机样品组分的保留时间与已知有机物在相同的仪器和操作条件下保留时间相比较,如果两个数值相同或在实验和仪器容许的误差范围之内,就推定未知物组分可能是已知的比较有机物。但是,因为同一有机物在不同的色谱条件和仪器中保留时间有很大的差别,所以用保留时间值对色谱分离组分进行定性只能给初步的判断,绝对多数情况下还需要用其它方法作进一步的确认。一个最常用的确证方法是将可能的有机物加到有机样品中再进行一次气相色谱仪分析,如果有机样品中确含已知有机物的组分,则相应的色谱峰会增大。这样比较两次色谱图峰值的变化,就可以确定前期初步推断是否正确。[/size]
我[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分离度老是不好,能通过调节气体流速和温度或其他条件来提高分离度吗?具体可以调节哪些条件啊? 谢谢了啊
在实际工作中,当我们拿到一个样品,我们该怎样如何定性和定量,建立一套完整的分析方法是关键,下面介绍一些常规的步骤:1、样品的来源和预处理方法GC能直接分析的样品必须是气体或液体,固体样品在分析前应当溶解在适当的溶剂中,而且还要保证样品中不含GC不能分析的组分(如无机盐),可能会损坏色谱柱的组分。这样,我们在接到一个未知样品时,就必须了解的来源,从而估计样品可能含有的组分,以及样品的沸点范围。如能确认样品可直接分析。如果样品中有不能用GC直接分析的组分,或样品浓度太低,就必须进行必要的预处理,包括采用一些预分离手段,如各种萃取技术、浓缩和稀释方法、提纯方法等。2、确定仪器配置所谓仪器配置就是用于分析样品的方法采用什么进样装置、什么载气、什么色谱柱以及什么检测器。3、确定初始操作条件当样品准备好,且仪器配置确定之后,就可开始进行尝试性分离。这时要确定初始分离条件,主要包括进样量、进样口温度、检测器温度、色谱柱温度和载气流速。进样量要根据样品浓度、色谱柱容量和检测器灵敏度来确定。样品浓度不超过mg/mL时填充柱的进样量通常为1-5uL,而对于毛细管柱,若分流比为50:1时,进样量一般不超过2uL。进样口温度主要由样品的沸点范围决定,还要考虑色谱柱的使用温度。原则上讲,进样口温度高一些有利,一般要接近样品中沸点最高的组分的沸点,但要低于易分解温度。4、分离条件优化分离条件优化目的就是要在最短的分析时间内达到符合要求的分离结果。在改变柱温和载气流速也达不到基线分离的目的时,就应更换更长的色谱柱,甚至更换不同固定相的色谱柱,因为在GC中,色谱柱是分离成败的关键。5、定性鉴定所谓定性鉴定就是确定色谱峰的归属。对于简单的样品,可通过标准物质对照来定性。就是在相同的色谱条件下,分别注射标准样品和实际样品,根据保留值即可确定色谱图上哪个峰是要分析的组分。定性时必须注意,在同一色谱柱上,不同化合物可能有相同的保留值,所以,对未知样品的定性仅仅用一个保留数据是不够的,双柱或多柱保留指数定性是GC中较为可靠的方法,因为不同的化合物在不同的色谱柱上具有相同保留值的几率要小得多。6、定量分析要确定用什么定量方法来测定待测组分的含量。常用的色谱定量方法不外乎峰面积(峰高)百分比法、归一化法、内标法、外标法和标准加入法(又叫叠加法)。峰面积(峰高)百分比法最简单,但最不准确。只有样品由同系物组成、或者只是为了粗略地定量时该法才是可选择的。相比而言,内标法的定量精度最高,因为它是用相对于标准物(叫内标物)的响应值来定量的,而内标物要分别加到标准样品和未知样品中,这样就可抵消由于操作条件(包括进样量)的波动带来的误差。至于标准加入法,是在未知样品中定量加入待测物的标准品,然后根据峰面积(或峰高)的增加量来进行定量计算。其样品制备过程与内标法类似但计算原理则完全是来自外标法。标准加入法定量精度应该介于内标法和外标法之间。7、方法的验证所谓的方法验证,就是要证明所开发方法的实用性和可靠性。实用性一般指所用仪器配置是否全部可作为商品购得,样品处理方法是否简单易操作,分析时间是否合理,分析成本是否可被同行接受等。可靠性则包括定量的线性范围、检测限、方法回收率、重复性、重现性和准确度等。本文摘自《气相色谱方法及应用》
如题,GC分离效果关键影响因素到底是柱子还是其他色谱参数?比如程序升温。最近在做GC分析方法开发,但是发现柱子影响很大,一个色谱条件下这根柱子分离度很差,但是换了另外一根,分离度就立竿见影,极好。到底为啥?没去思考过,请教各位,帮忙分析一下喔,谢谢。
大家好,请教一个问题,实验室用的是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]填充柱,规格是TDX-01 2m*3mm,检测器是TCD,请问可以分离氕氘混合气体吗?氘气在色谱中会出峰吗?谢谢了。
第五课 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]-分离系统 色谱柱是色谱仪的分离系统。试样中各组分的分离在色谱 柱中进行,因此,色 谱柱是色谱仪的核心部分。色谱往 主要有两类:填充柱和毛细管柱,现分别叙述如下: 1.填充柱 填充柱由柱管和固定相组成,柱管材料为不锈钢或玻璃, 内径为2—4毫米,长为1—3米。往内装有固定相,固定相 又包括固体固定相和液体固定相两种。 2.毛细管往 毛细管柱又叫空心柱,空心柱分涂壁空心柱,多孔层空 心柱和涂载体空心柱。 涂壁空心柱是将固定液均匀地涂 在内径0.1—0.5毫米的毛钢管内壁而成。毛细管的材 料可以是不锈钢、玻璃或石英。这种色谱柱具有渗透性 好、传质阻力小等特点,因此柱子可以做得很长(一般 几十米,最长可到三百米)。和填充柱相比,其分离效率 高,分析速度快,样品用量小。其缺点是样品负荷量小, 因此经常需要采用分流技术。柱的制备方法也比较复杂; 多孔层空心柱是在毛细管内壁适当沉积上一层多孔性物 质,然后涂上固定液。这种柱容量比较大,渗透性好, 故有稳定、高效、决速等优点。
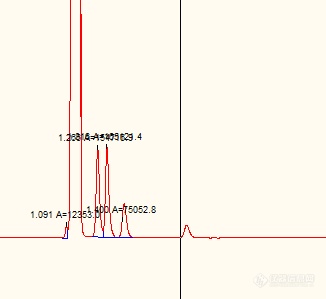
[color=#444444] 用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]GC-9160分离产物,产物为辛酸,辛醛,辛醇,庚烷,辛烷,辛酸辛酯等(大体上是这几种),色谱柱SE-54,程序升温,调了很多次条件,目前分离情况最好的是35℃保持2min,5℃/min升温到50℃,保持2min,再10℃/min升温到220℃,保持5min,分离出来的情况如左图,但是再次打色谱,相同的分离条件,还是这六种物质的混合物,就出现了右图的情况。[/color][color=#444444] 问题:怎样调检测器,进样器的温度?[/color][color=#444444] 换柱子怎么样?[/color][color=#444444][img=,361,339]https://ng1.17img.cn/bbsfiles/images/2019/07/201907101027248982_1504_1752329_3.png!w361x339.jpg[/img][img=,326,299]https://ng1.17img.cn/bbsfiles/images/2019/07/201907101027246261_6310_1752329_3.png!w326x299.jpg[/img][/color]
色谱柱温度,不仅影响色谱过程的热力学因素,也影响传质过程的动力学因素。柱温变化,不仅影响柱前端压力、载气流速等,更重要的是对物质的分离、分析结果带来影响。气相色谱中,根据升温方式,程序升温可分为线性程序升温和非线性程序升温,前者更普遍。线性程序升温,即随时间线性变化的升温方式,可分为一阶线性程序升温和N阶线性程序升温。对于每阶程序升温,都包含初温、程升速率、终温以及不同温度下的保持时间四个基本参数。 气相色谱恒温分析中,对化学性质相似的同类型的化合物,保留时间和沸点呈对数关系,随着保留时间增加,峰宽迅速增加,导致先流出峰相互叠加,后流出峰又因峰展宽,使检测灵敏度下降。因此一般通过柱温程序升温来解决这个问题。 那么,程序升温时,柱温N阶程序如何确定,是否N越大越好? 程序升温时,在最佳分离条件下,保留时间与沸点近似成线性关系,即随着柱温的升高,峰底宽基本不变或增加很小。程序升温中各组分均在最佳柱温下出峰,但并不是N越多越好。 气相色谱分析中,对于组分沸点范围窄、化学性质类似的样品,如同系物,可选用一阶升温;样品组分沸点范围宽、性质差异大的,应选择N阶程序升温。N应根据化合物的多少、需要达到的分离效果、仪器的条件等各方面来选择。 每阶程序升温中,设置初温、程升速率和终温这三个基本参数优化分离条件,要从分离效果和分析速度两方面考虑。 对于初温,一般比样品中沸点最低的组分沸点要低,可参考低沸点组分恒温分析时的温度。初温的选择,主要是依据低沸点组分,但要高于固定液的凝固温度。 升温速率的选择,在了解样品组分复杂程度的基础上,既要保证较小的保留时间,又要保证较大的分离度,一般在0-10℃/min之间。 终温的选择,主要根据固定相、样品组分的热稳定性和高沸点组分的沸点确定。同样的样品组分,流出时的柱温,在毛细管柱上的温度比填充柱低,毛细管柱上的温度一般比样品的沸点约低50℃。 此外,气相色谱中,柱温是影响化合物保留时间的重要因素。使用中,应注意柱温的选择,因为柱温关系到:① 色谱柱固定液的寿命。若柱温高于固定液的最高使用温度,则会造成固定液随载气流失,不但影响柱的寿命,而且固定液随载气进入检测器,将污染检测器,影响分析结果。② 分离效能和分析时间。若柱温过高了,会使各组分的分配系数K值变小,分离度减小;但柱温过低,传质速率显著降低,柱效能下降,而且会延长分析时间。③ 化合物保留时间。柱温越高,出峰越快,保留时间变小。柱温变化会造成保留时间的重现性不好,从而影响样品组分的定性结果。一般柱温变化1℃,组分的保留时间变化5%;如果柱温度变化5%,则组分的保留时间变化20%;④ 色谱峰峰形。柱温升高,正常情况下会导致半峰宽变窄,峰高变高,峰面积不变。但是组分峰高变高,以峰高进行定量时时分析结果可能产生变化;反之柱温降低,则相反。 而在色谱定性方法中,柱温变化对定性结果的影响如下:① 当采用绝对保留值定性时,其他色谱条件不变,柱温变化时,保留时间就会发生变化,这样就直接影响定性结果判断。② 当采用相对保留值α定性时,α只是柱温和固定液的函数,只与待测组分的热力学性质有关,消除了外界因素的影响,因此跟柱温变化关系不大,但是柱温变化影响判断结果。③ 当采用保留指数定性时,恒温分析,保留指数与保留时间有关,而柱温影响保留时间变化;程序升温分析,除了保留时间,保留指数还与保留温度有关。因此,这种定性方法易受柱温变化影响。④ 当采用纯样叠加法定性时,已知混合物中含某组分,将该组分的纯样加入,观察加入前后的响应信号变化。柱温变化,保留时间变化,但是加入前后的样品影响信号变化是一致的,因此柱温变化不影响采用这种方法定性的结果。 而在定量计算时,经常要用到校正因子,如重量校正因子,和组分的质量以及响应信号有关。柱温变化,峰高变化,峰面积不变,因此,在柱温变化不影响峰形正常的前提下,以峰高为响应信号的重量校正因子,受柱温影响,而以峰面积为响应信号的重量校正因子将不受影响。常见定量方法中,在柱温波动不影响出峰效果的前提下,对定量结果的影响如下:① 采用归一化法时,定量时需要各组分的校正因子,当以峰面积为响应信号时,定量结果不受影响,以峰高为响应信号则受影响。② 采用内标法时,需要计算定量校正因子,影响规律和①同。③ 采用外标法时,即标准曲线法,当以峰面积为响应信号时,不受影响,但是当以峰高为响应信号时,影响很大。 总之,柱温变化可能会导致定性、定量分析结果的变化。 既然柱温变化对分析结果有重要影响,那么选择合适的柱温以及对柱温进行控制就很重要了。 首先,应保证柱温不高于固定液的最高使用温度(即色谱柱的最高耐受温度),避免固定液流失而影响色谱柱柱效和使用寿命; 其次,选择合适的柱温,柱温的选择应使难分离的两组分达到预期的分离效果,峰形正常而分析时间又不长为宜,一般柱温应比试样中各组分的平均沸点低20-30℃,通过试验决定。对于沸点范围较宽的试样,应采用程序升温,按预定的加热速度随时间呈线性或非线性地增加温度。一般升温速度是呈线性的。 最后,特别是要保证仪器柱温控制的稳定性、均匀性,以及实际温度与预设温度之间的一致性。一般气相色谱仪柱温控温精度为±1℃,有些厂家的可达到±0.1℃。
建立方法过程中如何选择色谱柱?第一次建立方法时,应考虑色谱柱的下列性能参数,以便选出用于该分离试验的最佳色谱柱。 A .色谱柱固定相 B .内径 C .膜厚度 D .色谱柱长度A.色谱柱固定相气相色谱柱中,两种分析物由于其与固定相的相互作用不同而发生分离。因此,必须选定一个与样品特性相匹配的固定相。例如,如果组分足有不同的沸点(温度差大于2℃),推荐使用非极性色谱柱。如果组分之间的主要差异是极性不同,那么使用极性色谱柱较为理想。B.内径足内径的选择通常取决于仪器或检测方式。大多数现代化得气相色谱设备都与大部分色谱柱的尺寸相兼容。内径增大,色谱柱的样品容量增加,但分离度和灵敏度降低。反之,尺寸较小的色谱柱,其分离度和灵敏度也相应提高,但缺点是样品容量减少,所需样品量也增多。最好的方法是找一个已有的色谱方法,在此基础上进行优化。C.膜厚度膜厚增加,色谱柱的样品容量也增大,但洗脱峰的速度变慢。这有助于分析挥发性化合物,如风味物质。膜的厚度增加,色谱柱的过载风险减少,分离度随之提高。不过,膜的厚度增大,对于降解的敏感性也增大。相对来说,膜的厚度越大,相同组分的洗脱温度也越高。对于具有较高沸点,如甘油三酯或较大分子量的化合物,应使用较薄的膜进行分析,以提高分离度,避免增加不必要的分析时间。另一个要考虑的因素是相比率(b)。相比率用下面含有内径和膜厚度的公式进行计算: b= 内径/(4*膜厚度) 单位:μm相比率可用于两个方面:1.对量纲进行分类: a.对于挥发性样品b4002.要将一组分析数据从某个内径的色谱柱转移到另一个色谱柱而不改变方法,应选择与该色谱柱具有相似b值的色谱柱,这样二者也具有相似的保留性能。 膜厚度(μm) 0.1 0.25 0.5 1 1.8 3 0.1 250 100 50 25 14 8内径(mm) 0.25 625 250 125 63 35 21 0.32 800 320 160 80 44 27 0.53 1325 530 265 133 74 44 一般色谱柱的相比率(b)D.色谱柱长度能色谱柱的长度越长,柱效越高,分离度也越高,但二者并不成线性关系。分离度与色谱柱长度的平方根成正比,所以色谱柱长度增大二倍,平方根为1.414,分离度只能增加41.4%。不过,色谱柱长度增加,保留时间也会增大。色谱柱长度增大二倍,分析时间也增大二倍。一般来说,推荐使用最短的色谱柱进行分离试验。
高效色谱仪分离方法的选择原则:一、根据相对分子质量选择:1、相对分子质量很低的样品采用气相色谱。2、液液分配色谱、液固吸附色谱和离子交换色谱最适合分析相对分子质量为200~2000的样品。3、相对分子质量大于2000的样品,采用凝胶色谱为最优。二、根据溶解度选择:1、溶于水并能离解的样品,采用离子交换色谱。2、溶于烃类(如苯或异辛烷等)的样品,可采用液固吸附色谱。3、溶于CCl4的样品,多采用液液分配色谱和液固吸附色谱。4、既溶于水又溶于异丙醇的样品,常用水和异丙醇的混合液作液液分配色谱的流动相,以疏水性化合物作固定相。三、根据分子结构选择:1、酸、碱化合物采用离子交换色谱。2、脂肪族和芳香族采用液液分配色谱、液固吸附色谱。3、异构体采用液固吸附色谱。4、同系物不同官能团和强氢键化合物采用液液分配色谱。
气相色谱分离度不够怎么调整