要检测黄连中盐酸小檗碱的含量,高效液相用什么流动相
在反相色谱分析多肽含量时,流动相常用三氟乙酸,而不用磷酸、乙酸或分子量很小的甲酸呢?三氟乙酸起到了离子对试剂的作用了吗?
有一芳香酸和一芳香醛,HPLC分析过程中发现,流动相中有机相比例的改变得到的含量不一样有机相为乙腈和乙酸的水溶液附图,我觉得两个分离度都还可以,但是含量有差http://ng1.17img.cn/bbsfiles/images/2012/07/201207110836_376904_2355884_3.jpg这是乙腈比例为45的图,两个主峰含量为22.33&77.49http://ng1.17img.cn/bbsfiles/images/2012/07/201207110837_376905_2355884_3.jpg这是乙腈比例为40的图,两个主峰含量为20.19&79.67为啥含量会受流动相影响呢?请前辈们指导指导啊
用液相色谱-质谱对燕窝中唾液酸含量的检测,不知道对流动相的选择有什么要求?与液相色谱法检测选择的流动相有何不同?江湖救急,求各位大神各显神通帮帮忙。
液相色谱-串联质谱法检测食品中维生素D含量 如何用液相色谱-串联质谱法(LC-MS/MS)检测食品中的维生素D含量。这项技术可是现代食品分析中的佼佼者,能够帮助我们精准地掌握食品中的营养信息。 样品前处理 提取:首先,我们需要从食品样品中提取维生素D。这一步很关键,因为提取效率直接影响最终的检测结果。通常,我们会使用有机溶剂,比如乙腈或甲醇,来提取维生素D。 净化:提取后的样品往往含有很多杂质,这些杂质会影响检测结果。因此,我们需要对提取液进行净化处理。常用的净化方法有固相萃取(SPE)和液液萃取(LLE)。 浓缩:净化后的样品溶液需要进行浓缩,以提高维生素D的浓度。常用的浓缩方法有氮气吹干和旋转蒸发。 仪器操作 流动相选择:选择合适的流动相对分离效果至关重要。通常,我们会使用水和有机溶剂(如甲醇或乙腈)的混合物作为流动相,并根据需要添加少量酸或缓冲液。 色谱柱选择:选择适合的色谱柱也很关键。C18反相色谱柱是常用的选择,因为它对维生素D有很好的保留效果。 质谱条件:设置合适的质谱条件,包括离子源温度、喷雾电压、碰撞能量等。这些参数的优化可以大大提高检测灵敏度和特异性。 故障排除 峰形不好:如果发现峰形不好,可能是由于流动相比例不合适或色谱柱污染。尝试调整流动相比例或清洗色谱柱。 灵敏度低:如果灵敏度不够,可能是由于样品提取效率低或仪器参数设置不当。检查提取方法并优化仪器参数。 杂峰干扰:如果出现杂峰干扰,可能是由于样品净化不彻底或流动相选择不当。尝试改进净化方法或更换流动相。 仪器故障:遇到仪器故障时,首先要保持冷静,然后根据仪器的报错信息查找原因。必要时,可以联系仪器厂家进行维修。 总之,液相色谱-串联质谱法检测食品中维生素D含量是一项复杂但非常重要的技术。通过掌握这些操作要点和故障排除方法,我们可以更加准确、高效地完成检测任务。
用液相测物质的含量时,流动相应为盐的水溶液,但实际没加盐,测得液相值有影响吗?比如 药典中米非司酮的测量,,。。 要用到庚烷磺酸钠的水溶液。。。
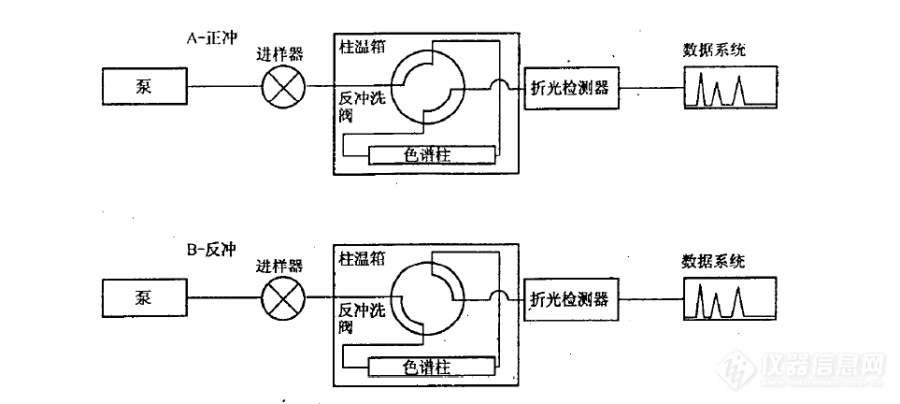
[align=center][font=宋体][size=14.0000pt]SH 0806-2008 [font=宋体]中间馏分芳烃含量的测定 分析方法的注意事项[/font][font=Calibri]----[/font][font=宋体]流动相[/font][/size][/font][/align][font=宋体][size=12.0000pt][font=宋体]概述:[/font]SH0806-2008[font=宋体]标准使用高效液相色谱方法测定柴油和馏程范围为[/font][font=Calibri]150-400[/font][font=宋体]℃的石油馏分中单环芳烃、双环芳烃、三环以上芳烃和多环芳烃含量。该分析方法虽然比较简单,但是分析条件的控制比较重要。[/font][/size][/font][font=宋体][size=12.0000pt]在实验操作中,尤其需要注意流动相的问题,流动相不良会造成保留时间漂移从而使得色谱柱切换时间选择发生困难。[/size][/font][align=center][font=宋体][size=12.0000pt][font=宋体]一[/font] [font=宋体]原理介绍[/font][/size][/font][/align][font=宋体][size=12.0000pt][font=宋体]系统结构原理如图[/font]1[font=宋体]所示,系统使用正庚烷做流动相,单输送泵、极性色谱柱(氨基或者氰基柱)、四通阀和示差检测器实现分离。[/font][/size][/font][font=宋体][size=12.0000pt][font=宋体]待机状态和进样状态下(即状态[/font]A[font=宋体]),流动相自右向左流过极性色谱柱,柴油中的烃类和芳烃类组分实现分离。理想情况下,单环芳烃、双环芳烃、多环芳烃依次在色谱柱出口流出,如图[/font][font=Calibri]2[/font][font=宋体]所示。[/font][/size][/font][font=Calibri][size=12.0000pt][img=,690,309]https://ng1.17img.cn/bbsfiles/images/2020/06/202006010841562718_6781_1604036_3.png!w690x309.jpg[/img] [/size][/font][align=center][font=宋体][size=9.0000pt][font=宋体]图[/font]1 SH 0806 [font=宋体]方法的硬件原理图[/font][/size][/font][/align][align=center][font=Calibri][size=12.0000pt][img=,690,348]https://ng1.17img.cn/bbsfiles/images/2020/06/202006010842112720_7230_1604036_3.png!w690x348.jpg[/img] [/size][/font][/align][align=center][font=宋体][size=9.0000pt][font=宋体]图[/font]2 [font=宋体]色谱柱内样品理想分离示意图[/font][/size][/font][/align][font=宋体][size=12.0000pt][font=宋体]当双环芳烃流出色谱柱后(色谱图中[/font]A[font=宋体]点位置,或称为切换点),四通阀旋转,系统状态变为反吹。色谱柱内流动相的方向变成自左至右,将三环以及三环以上的芳烃类物质反吹出色谱柱,在示差检测器上表现为单峰,如图[/font][font=Calibri]3[/font][font=宋体]所示。[/font][/size][/font][align=center][font=Calibri][size=12.0000pt][img=,690,351]https://ng1.17img.cn/bbsfiles/images/2020/06/202006010842234040_3244_1604036_3.png!w690x351.jpg[/img] [/size][/font][/align][align=center][font=宋体][size=9.0000pt][font=宋体]图[/font]3 [font=宋体]最终谱图[/font][/size][/font][/align][align=center][font=宋体][size=12.0000pt][font=宋体]二[/font] [font=宋体]分析注意要点[/font][/size][/font][/align][font=宋体][size=12.0000pt]首先要注意该方法的原理是比较理想化的,干扰因素也比较多。柴油中的单环芳烃、双环芳烃、多环芳烃是否可以清晰彻底的分离开,是难以保证的。况且柴油中的二烯烃、杂环类、酯类化合物等都会对分析结果带来影响。[/size][/font][font=宋体][size=12.0000pt]其次,色谱柱的选择十分重要,具体的选型需要咨询色谱柱厂家。[/size][/font][font=宋体][size=12.0000pt]再次,切换点的选择非常重要。[/size][/font][font=宋体][size=12.0000pt][font=宋体]样品组成可能比较复杂,[/font]A[font=宋体]点可以选择的时间窗口就会比较窄,需要多次重复实验寻找合适的切换点。[/font][/size][/font][font=宋体][size=12.0000pt]分析条件需要非常稳定,需要较为严格的控制流动相组成、泵输送流速以及色谱柱温度,以免影响保留的重复性。[/size][/font][align=center][font=宋体][size=12.0000pt][font=宋体]三[/font] [font=宋体]常见问题[/font]——流动相[/size][/font][/align][font=宋体][size=12.0000pt]保留时间的漂移是最为常见的问题。在进样系统性能测试标准样品时,芳烃的保留时间长时间的漂移,致使难以确定切换点。往往会耗费较多时间来平衡系统,等待保留时间稳定,从而降低分析效率。[/size][/font][font=宋体][size=12.0000pt]其本质的原因在于流动相的不稳定。[/size][/font][font=宋体][size=12.0000pt][font=宋体]笔者曾经在使用该系统时,长时间重新系统后,连续进样[/font]10[font=宋体]余次系统测试标样,发现芳烃的保留时间不断发生缩短,认为色谱柱未彻底平衡。[/font][/size][/font][font=宋体][size=12.0000pt][font=宋体]第二天更换了流动相(新换的流动相没有彻底封口放置在实验室[/font]10[font=宋体]小时),进样[/font][font=Calibri]3[/font][font=宋体]次,芳烃的保留时间较为稳定。[/font][/size][/font][font=宋体][size=12.0000pt]后来考虑了一下,原因应当为新换的正庚烷中水含量已经与空气中的水含量交换平衡,或者说水含量已经比较稳定,进而使得芳烃保留稳定。[/size][/font][align=center][font=宋体][size=12.0000pt][font=宋体]四[/font] [font=宋体]小结[/font][/size][/font][/align][font=宋体][size=12.0000pt]SH 0806-2008[font=宋体]系统分离原理属于正相液相色谱,我们知道正相[/font][font=Calibri]HPLC[/font][font=宋体]一般不太容易得到良好的保留时间重复性。原因是在正相[/font][font=Calibri]HPLC[/font][font=宋体]分析中,流动相中的微量水会显著的改变其极性。假设流动相原先的极性为[/font][font=Calibri]0.01[/font][font=宋体],吸收微量水之后极性变为[/font][font=Calibri]0.02[/font][font=宋体],看上去似乎变化不大,但其实极性增大了一倍。[/font][/size][/font][font=宋体][size=12.0000pt]尤其是使用硅胶色谱柱的场合,流动相与环境空气中的水蒸气发生交换,改变了极性,从而影响保留时间。在使用硅胶柱分析时,一般要避免使用彻底干燥的正己烷流动相,避免吸水造成保留不稳定,甚至需要特意在流动相中加入微量的水。[/size][/font]
请问质谱检测中 碳酸钠溶液能作为流动相吗?
本人新手,最近在做甘草苷的液相含量,可是用甲醇做流动相时,对照品峰型难看,像两个没分开的峰,使用乙腈时没有这个问题,请问为什么?非常感谢!
[table][tr][td] [align=center] [/align] [size=18px]在色谱分析过程中常常需要使用缓冲盐来调节流动相的pH 值,缓冲盐的不当使用对色谱柱可能造成柱压升高、柱效下降以及使化合物的保留时间发生变化等影响,缓冲盐使用不当对色谱柱的影响及解决办法。 缓冲盐是指对pH有缓冲能力的盐,能够让pH维持在一个恒定的数值。 何时应用缓冲盐 样品或样品中需研究的关键杂质有离子化倾向,其他特定少数情况另行叙述。存在较强离子化倾向的组分,其中一部分是分子状态,与反相色谱固定相结合的更好;另一部分是离子状态,更亲和于流动相。如不使用缓冲盐控制其电离状态,即分子状态和离子状态的比例,很容易出现峰拖尾分叉变形的情况。这种情况下一般就不应该使用水/有机相系统作为流动相,应选用缓冲盐/有机相系统。 常见的缓冲盐有哪些 缓冲盐类型的选择,主要取决于所需要的缓冲能力,在反向色谱中,流动相中水相的pH和离子强度在开发对条件微小变化不敏感的耐用方法中非常重要。对于离子型化合物,典型的样品的保留随pH改变而明显变化。通常在pH2到4条件下,保留时间对pH的微小改变稳定性最高。因此建议将这一pH范围作为大多数样品方法开发的起始pH,包括碱性化合物和一般的弱酸。缓冲盐溶液的pH值越接近其pka,缓冲能力越强。一般缓冲盐溶液的pH值应在其pka±1的范围内。 比起单纯的酸碱,盐类,特别是具有缓冲能力的盐类可以很好的控制流动相的pH值,根据不同缓冲盐中两种盐的配比,可以很容易的配置出一定pH的缓冲溶液。 1、甲酸盐通常在[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]中常用的甲酸盐都是甲酸铵,这类盐的溶解度好,完全兼容[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]的方法,对色谱柱的伤害也比较小,但是缺点是离子强度比较低,另外就是甲酸盐比较容易吸潮,称量的时候比较困难,在流动相里还可能挥发。与甲酸配合,可以得到甲酸-甲酸铵缓冲体系,大概缓冲能力在pH3~4.5的范围之内,只要调节两者浓度的比例即可。 2、乙酸盐常见为乙酸铵,在使用上,和甲酸盐十分类似,离子强度也不高,与乙酸配合的乙酸-乙酸铵缓冲体系pH的控制能力在pH4~5.5左右。 3、磷酸盐常用的是磷酸的钠盐和钾盐,二者对pH的控制能力十分接近,只是离子强度稍有差异,绝大多数情况下是可以互换使用的,磷酸由于是多元酸,能够形成一氢盐和二氢盐,所以使用磷酸缓冲体系调节pH也是组合比较多,跨度比较大的,并且可以提供较高的离子强度,可惜,磷酸盐流动相体系无法兼容质谱,并且对色谱柱损伤较大。以磷酸钠盐为例,可以有以下两种组合的缓冲体系:磷酸-磷酸二氢钠:pH可以达到1.2~3.1左右的范围磷酸二氢钠-磷酸氢二钠:pH可以达到6.5~8左右的范围 上述的缓冲对能调节的pH范围指的都是在保持缓冲能力的范围之内,如果仅仅是调节pH的话,范围还可以再扩展一些。 缓冲盐使用不对产生的影响 1、柱压升高原因:缓冲盐使用不当导致缓冲盐析出,堵塞塞板和键合相颗粒之间的孔隙,阻碍流动相传质,引起柱压升高 2、相同化合物的保留时间发生变化原因:如果没有冲洗干净就进行进样,色谱柱内含有的盐会使化合物的保留时间发生变化 3、柱效下降原因:有些缓冲盐会渗入到键合相的深处,损害硅胶基体,导致色谱柱键合相流失,柱床变松,柱效下降 ii)凝结在键合相表面,使C18碳链难以舒展,对物质的保留能力下降,导致柱效下降。因此用过缓冲盐后需要对色谱柱进行冲洗,水中缓冲盐浓度较大时应特别引起注意。 缓冲盐的正确使用方法 1、使用前的处理: 在使用缓冲盐作流动相之前需要用不含缓冲盐的流动相冲洗色谱柱,直至基线平稳。原则上,用于冲洗的流动相与分析时所用的流动相含水的比例相同(或含水更多),不同的只是用于冲洗用的流动相中不含缓冲盐。 理由:缓冲盐通常易溶于水,难溶于有机溶剂。用含缓冲盐的(特别是做流动相的水为饱和的缓冲盐溶液时)流动相进行分析时,如果分析前色谱柱中用于保存色谱柱的流动相中含水的比例相对较小,不先冲洗掉,接下来做样品的时候所用的流动相中如果有机溶剂含量大,而其比例中所含的水又不足以溶解该缓冲盐时,缓冲盐将会在色谱柱柱体上析出,沉积下来,这将可能导致上述对色谱柱的损害。 2、使用后的处理:用与分析时含水比例相同的流动相(与分析用流动相唯一的区别是,用于冲洗的流动 相不含缓冲盐)进行冲洗约30min,直至基线平稳。如果该色谱柱在接下来很长的一段时间内不使用,要长期保存,则需再加上一步,即用纯的有机溶剂冲洗一遍,直至基线平稳。 用与分析时含水比例相同的流动相(与分析用流动相唯一的区别是,用于冲洗的流动相不含缓冲盐)进行冲洗约30min,直至基线平稳。如果该色谱柱在接下来很长的一段时间内不使用,要长期保存,则需再加上一步,即用纯的有机溶剂冲洗一遍,直至基线平稳. 缓冲液可以提供离子平衡的反离子,并使流动相保持一定的离子强度和ph值,减少拖尾。 使用缓冲液要注意几点 1、避免使用盐酸盐,盐酸盐对钢质有腐蚀作用。2、缓冲液最好要现配现用,往往缓冲液是良好的菌类培养液,隔天或放置长时间实验时会有很多怪现象发生。 3、实验后不可用有机溶剂直接过度,有机溶剂会处使盐类析出,造成液路或色谱柱堵塞,可用95:5的水甲醇冲洗。 4、使用缓冲液要及时掌握ph范围,做到胸中有数。 5、清洗液路和柱子时,有温控可加热到30摄氏度易于冲洗。 6、长时间用缓冲溶液要注意观察接头处有无析出,若有白色盐类析出,可考虑一定周期用10%硝酸冲洗一下液路(拆下柱子,走30ml,再用5倍水冲洗)可以避免液路的堵塞。 7、选择缓冲液要用可靠的试剂,避免不纯的盐类造成不必要的麻烦。 如果流动相中有机溶剂的比例很高是不能用来冲洗缓冲盐的,是洗不出来的。通常C18柱先用5%~10%的甲醇冲洗,是可以把缓冲盐冲洗出来的,然后用纯的有机溶剂来保护柱子。最好的方法是使用与流动相相同浓度不含盐的流动相进行清洗。 但就是速度慢一些。用水是为了快速替换,一般在15分钟以内最好,且用0.8的流速较好. 如果用纯水冲,容易造成键合的碳链的流失,最好用5%~10%甲醇水溶液冲. 可以用纯水代替流动相中的缓冲液,有机相不变。这样冲洗柱子比较稳妥。 流动相流速的选择 因柱效是柱中流动相线性流速的函数,使用不同的流速可得到不同的柱效。对于一根特定的色谱柱,要追求最佳柱效,最好使用最佳流速。对内径为4.6mm的色谱柱,流速一般选择1ml/min,对于内径为4.0mm柱,流速0.8ml/min为佳。当选用最佳流速时,分析时间可能延长。可采用改变流动相的洗涤强度的方法以缩短分析时间(如使用反相柱时,可适当增加甲醇或乙腈的含量)。 注意: a.由于甲醇廉价,对于反相柱推荐使用甲醇体系(必须使用乙腈的场合除外)。 b.对于正相柱推荐使用沸程为30-60℃的石油醚或提纯后的己烷作流动相,没有提纯的己烷不得使用。用水最好使用超纯水(电阻率大于18兆欧),去离子水及双蒸水中含有酚类杂质,有可能影响分析结果。 c.含水流动相最*在实验前配制,尤其是夏天使用缓冲溶液作为流动相不要过夜。最好加入叠氮化钠,防止细菌生长。d.流动相要求使用0.45 μm滤膜过滤,除去微粒杂质。e.使用HPLC级溶剂配制流动相,使用合适的流动相可延长色谱柱的使用寿命,提高柱性能。 小结 正确使用缓冲盐很有必要,既可以防止缓冲盐析出,也可以达到提高色谱柱使用寿命的目的。我们不妨用一句话来总结它的使用方法:用前要过滤,用后需冲洗。[/size][/td][/tr][/table]
大家讲一讲含盐流动相损坏色谱柱原因
测定叶酸改性物B9-Vitapol含量的流动相是什么,急急急,在线等……
反相柱,甲醇和水为流动相,甲醇含量增加,压力增大[em09504][em09504],请问是哪有问题?
[b]Q:反相高效液相色谱法测定乐卡地平片的含量,流动相是?A:乙腈-0.01mmol/L乙酸铵溶液(含0.1%三乙胺,pH4.5,体积比65:35)===============================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:莫名其妙(注册ID:moyueqiu)lijing320323(注册ID:lijing320323)大川之子,纵横四海(注册ID:chuangu120)捌道巴拉巴巴巴(注册ID:v3082413)999youran(注册ID:999youran)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/12/201812131602322146_8508_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/12/201812131602349366_7616_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:102060化合物:乐卡地平色谱柱:[url=http://www.dikma.com.cn/product/details-227.html]Diamonsil C18 5μm 150 x 4.6mm[/url]色谱条件:色谱柱:Diamonsil C18 150×4.6 mm, 5μm (Cat#:99901)流动相:乙腈-0.01mmol/L乙酸铵溶液(含0.1%三乙胺,pH4.5,体积比65:35)流速:1.0mL/min进样量:20μL检测器:G1315B 二极管阵列检测器(DAD),356nm文章出处:天津药学 2006,,5(18):16-18关键字:高效液相色谱法,乐卡地平片,含量测定,HPLC,Diamonsil C18,钻石一代图谱:[b]摘要[/b]:目的:建立用高效液相色谱法测定乐卡地平片含量的方法.方法:采用色谱柱DismonsilTM钻石C18(150 mm×4.6 mm,5μm) 流动相为乙腈-0.01 mol/L乙酸铵溶液(含0.1%三乙胺,pH 4.5,体积比65∶35) 流速1.0 ml/min 检测波长为356 nm.结果:乐卡地平质量浓度在20~200μg/ml内,线性关系良好.结论:本方法快速灵敏、重现性好,测定结果准确可靠,可用于乐卡地平片的含量测定.[img=,319,504]http://www.dikma.com.cn/Public/Uploads/images/5-4(2).jpg[/img][img=,319,504]http://www.dikma.com.cn/Public/Uploads/images/5-4(1)(1).jpg[/img][url=http://www.dikma.com.cn/Doc/read/id/44]全文下载:反相高效液相色谱法测定乐卡地平片的含量[/url]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=152821]饲料中孔雀石绿和隐形孔雀石绿含量的液相色谱-串联质谱测定方法[/url]摘要建立了超高效液相色谱一串联四级杆质谱法测定饲料中孔雀石绿和隐性孔雀石绿的含量。用乙腈提取,提取液经蒸干浓缩后用中性氧化铝和阳离子交换固相萃取柱净化,使用u.PLC—MS/M进行检测。色谱条件:ACQUITY uPLC M BEH C】8柱(2.1 innl×100 rain i.d.,1.7 ),流动相乙腈0.1%甲酸溶液,梯度洗脱流速O.3 mL/min。采用电喷雾串联四极杆质谱检测。结果表明,孔雀石绿和隐性孔雀石绿的浓度为1~500 ng/mL时线形良好,在1~100 g/kg的添加水平条件下平均回收率为68.5% ~91.6% ,该方法的检测限为1.0/zg,/kg。
问题: 请问大家都用什么酸调节流动相的PH呀,一般都加多少含量或比例的酸呀,加完酸之后测得流动相PH大约是多少呢回复1: 乙酸,磷酸,一般习惯用酸度计调,数值要依据待测物的性质而定回复2: 看物质 吧,甲酸,乙酸,磷酸,高氯酸,硫酸,三氟乙酸。
张静等建立了液相色谱-三重四级杆质谱法(LC-MS-MS)快速测定化妆品中地氯雷他定等51种抗组胺类药物含量的方法。样品经10 mmol/L乙酸铵甲醇溶液超声提取后,经0.2 μm滤膜过滤后,以10 mmol/L乙酸铵水-甲醇作为流动相进行梯度洗脱,经Eclipse Plus C18色谱柱(100 mm×3.0 mm×1.8 μm)分离,采用电喷雾离子源在正、负离子 模式下进行多反应监测,外标法定量。结果表明,51种抗组胺类药物在2 ~ 50 ng/mL范围内线性关系良好(r0.999),检出限和定量限分别为0.15 μg/g和0.5 μg/g。对液态水基、乳液、膏霜、面膜、液态油基、凝胶、粉、蜡基8种不同化妆品基质在0.5、1.0、5.0 μg/g加标水平下的平均回收率为70.3% ~ 127.8%,相对标准偏差(RSD)小 于7.7%(n=6)。该方法前处理操作简便、快速、专属性强、灵敏度高、精密度、准确度均较好,可用于化妆品中51种抗组胺类药物含量的快速测定。 文章具体内容见附件
理论上[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]禁止使用任何不挥发性的缓冲盐,如果需要尽量使用诸如乙酸氨等挥发性盐,浓度不要超过20mmol/l。对于不挥发性的缓冲盐,如果你的仪器有吹扫捕集的话也可使用,但一定要小心。万不得已也不要用,首先有不挥发盐是得不到好的离子流的,其次盐留在质谱中很难除掉,除非停机清洗,不然一直会影响其他样品的分析。可以找质谱友好的条件来做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]联机,例如色谱条件为20mM磷酸盐的水/乙腈流动相,做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]联机的时候就可以用醋酸铵代替,然后用醋酸调节pH值与磷酸盐的一致即可。除了难挥发的盐,三乙胺、表面活性剂、还有高浓度(0.5%)的TFA,都对质谱不好,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]的流动相中应该避免。质谱的基线其实跟液相的紫外检测器和荧光检测器一样,基线高的原因不外乎内部和外部的原因。你选择的流动相在质谱的响应比较高,比如水相比较多的时候,噪音比较大些;还有如果盐含量比较大的时候,噪音更大些。检测器的灵敏度越高的时候,噪音应该越高。如果质谱的污染比较严重时,基线肯定比较高。比如离子阱检测器,用得久了,阱中的离子就会增多,一方面降低了质谱的灵敏度,另一方面增加了基线噪音。质谱的基线很多时候还跟你选择的离子宽度有关。比如你作选择离子扫描的时候,基线就低些。你作选择反应扫描的时候,离子宽度不要选得太宽,太宽噪音就高些。多级质谱一般做二级或三级质谱,基线噪音就低很多。
大家做含量时遇到过两个不同的色谱柱,检验出来的含量差很多的情况?我们做大豆磷脂的检验,用不同的色谱柱检验出来的结果差了4-5%,大家帮分析一下可能是什么原因引起的。(用的是同一个对照品和流动相。对照品也配了2遍了。)附:检验条件色谱条件与系统适应性试验 用硅胶为填充剂250mm×4.6mm×5μm,柱温为40℃;以甲醇:水:冰醋酸:三乙胺(85:15:0.45:0.05)为流动相A,以正己烷':异丙醇:流动相A(20:48:32)为流动相B;流速为每分钟1ml,按下表进行梯度洗脱;检测器为蒸发光散射检测器。标准曲线的制备 称取溶血磷脂酰胆碱对照品适量,精密称定,用三氯甲烷:甲醇(2:1)溶解,稀释制成每含磷脂酰胆碱20、60、100、200、300μg、精密量取上述对照溶液各20μl、注入液相色谱仪中,以浓度的对数值为横坐标,峰面积的对数值为纵坐标计算回归方程。
[color=#444444]对样品进行HPLC分析,除主峰(95%)外,还有两个杂质峰(2%、3%左右),流动相中有四丁基溴化铵做缓冲盐,想做[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url],确定主峰和杂质的结构,以便进一步进行工艺优化。[/color][color=#444444]但是,联系测试单位说,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]的流动相不能有缓冲盐,否则在质谱测试过程中缓冲盐会结晶析出,污染质谱,但我们尝试过不加缓冲盐进行液相色谱分析,三种组分完全分不开,现在不知道怎么解决,恳请大家不吝指教[/color]
我是新手,导师希望我用质谱来测定一下UDP-GlcNAc的含量,全称就是N-乙酰葡糖胺。我曾经用三乙胺醋酸作为流动相,用高效液相测定了含量,出峰时间在8分钟左右当直接标准品进样时,出峰比较快,很正常、但是当用三乙胺醋酸流动相时,标准品仍然用甲醇溶,却检测不到任何峰了这是怎么回事?我是一定要更改流动相了是吗?我查不到有关的流动相的资料,求各位专家大侠帮帮我,我该更换什么流动相比较合适?我换了流动相之后,样品仍然用纯甲醇溶解吗
[align=left][/align][align=left]在使用含盐流动相,尤其是高盐浓度或梯度条件进行液相分析时,稍不留神就会出现盐析的现象,会导致压力升高以及色谱峰裂峰等问题,不仅影响实验进度,还会影响色谱柱的使用寿命;如果处理不好,柱效下降甚至色谱柱报废都是有可能的。[/align][align=left]为了防止色谱柱被破坏,为了维护实验室的和平,今天YoYo就来介绍一下含盐流动相的使用攻略,快跟我往下看吧[/align][align=center][/align][align=center][/align][align=center] [/align][align=left][b][color=#0070c0]盐析的危害[/color][/b][/align][align=left]对于仪器的危害:系统堵塞,系统压力升高,泵压力波动增大,基线不平……[/align][align=left]对于色谱柱:柱压上升,峰形变差、裂峰,无法正常进行样品分析……[/align][align=left] [/align][align=left][/align][align=left][/align][align=left]因此,在使用含盐流动相时必须要特别注意以下几方面:[/align][align=left][/align][align=left][/align][align=left][b][color=#0070c0]1[/color][color=#0070c0]、色谱柱保存液[/color][/b][/align][align=left][b]1)未开封的新色谱柱[/b][/align][align=left] [/align][align=left]大阪曹達的新色谱柱,出厂保存液大多为100%乙腈(具体保存液种类请务必通过色谱柱盒内所附柱效报告单进行确认)。[/align][align=left]因此,为避免盐析,YoYo建议您按照以下步骤处理新色谱柱:[/align][align=left]①先使用与流动相组成比例相同但不含盐的溶液进行冲洗置换(避免使用纯水),时间建议1h以上[/align][align=left]②使用含盐流动相进行平衡[/align][align=left]③正常分析[/align][align=left][b] [/b][/align][align=left][b]2)已使用过的色谱柱[/b][/align][align=left] [/align][align=left]对于已开封使用过的色谱柱,需要了解使用履历,知晓前一次实验的条件、用完柱子后的最终保存液,判断是否需要再次进行保存液置换和过渡。[/align][align=left]建议用户建立实验室色谱柱管理表格,将色谱柱的使用履历(分析项目、流动相条件)、使用情况(柱压、用后柱效)进行记录,按照流程进行色谱柱的冲洗、保养和储存,方便对色谱柱进行管理。[/align][align=left] [/align][align=left][/align][align=left][/align][align=left][b][color=#0070c0]2、[/color][color=#0070c0]流动相的置换[/color][/b][/align][align=left][b] [/b][/align][align=left]在方法开发过程中,多数情况会涉及不同缓冲盐体系和不同有机相体系的各种尝试,那么在调整、更换流动相组成的过程中,请务必充分考虑到不同种类缓冲盐的溶解情况。[/align][align=left]一般情况下,盐的溶解能力:有机酸盐>无机酸盐[/align][align=left]最常用的磷酸缓冲盐中,溶解能力:铵盐>钾盐>钠盐[/align][align=left] [/align][align=left]若不确定所使用的缓冲盐和有机相之间的互溶情况,可按照不同比例将二者混合,静置30min,观察底部是否有沉淀或絮状物产生。[/align][align=left][b] [/b][/align][align=left][b][/b][/align][align=left][b][/b][/align][align=left][b][color=#0070c0]3[/color][color=#0070c0]、梯度条件[/color][/b][/align][align=left] [/align][align=left]当涉及缓冲盐-有机相梯度条件时,请确认缓冲盐在梯度条件中有机相最高点是否能够充分溶解。[/align][align=left]当然,不确定的时候也可以和上述方法一样,将缓冲盐和有机相按照梯度最高比例混合后静置,观察是否有沉淀产生。[/align][align=left][color=#0070c0] [/color][/align][align=left][color=#0070c0][/color][/align][align=left][color=#0070c0][/color][/align][align=left][b][color=#0070c0]4、[/color][color=#0070c0]色谱柱的保存[/color][/b][/align][align=left][b] [/b][/align][align=left]对于色谱柱使用时隔夜以及使用完后的保存,同样不能掉以轻心。[/align][align=left]当实验环境昼夜温差较大时,建议在夜间也要保持柱温(尽量使用柱温箱),并进行持续的小流速通液,以防止盐析;实验完毕后,使用不含盐的流动相(将缓冲盐相更换为纯水)对色谱柱和仪器进行冲洗置换,同样,在冲洗置换过程中不能使用纯水。[/align][align=left] [/align][align=left][/align][align=left][/align][align=left]希望今天的帖子能够帮到您,如果您有任何疑问欢迎留言![/align][align=center] [/align][align=center] [/align]
目的:建立盐酸舍曲林片含量及有关物质测定的高效液相色谱方法。方法:色谱柱为Diamonsil C18(4.6mm×200mm,5μm);流动相为甲醇-0.2%三乙胺溶液(用磷酸调到pH4.0)(60∶40),流速1.5mL/min;检测波长225nm。结果:进样量在2.49~19.94μg范围内,与峰面积线性关系良好,平均回收率为99.55%,RSD为0.60%(n=9)。结论:该方法简单、快速、准确,重现性及专属性好,可用于盐酸舍曲林片的质量控制。
各位老师们好,我接触[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]不久,而且之前一直做反相,最近同事有一个正相的方法想要让我试一下,流动相是正己烷+乙醇+乙酸乙酯(80:20:0.1),质谱是安捷伦的6465B,ESI源。我想请问一下,乙酸乙酯可以作为流动相进质谱吗?会有什么影响吗?比如说造成基线一直很高等等之类的,这个流动相会对仪器和我以后检查别的样品造成什么影响吗?谢谢各位老师啦!
最近做质谱发现流动相对质谱的结果有影响。比如之前用乙腈水做流动相,有一个化合物的分子离子峰就出不来,出的是一半分子量,但把乙腈换成甲醇就可以出。还有另一个化合物,同样用乙腈水体系,用20%乙腈起步的梯度,分子离子峰就出不来,出的都是碎片,但是换成60%乙腈起步的梯度,分子离子峰就出。都是同一样品前后进样,质谱条件参数都没变,为什么会这样?有没有高手能解释一下,谢谢。我猜测是不是质子性溶剂和非质子性溶剂的原因?
质谱电流高为什么样品或流动相不能加酸
[size=5]超临界流体色谱快速测定烟酰胺的含量[/size] 来源: 作者:郭亚东,马银海,张艳,彭永芳摘要:采用超临界流体色谱快速测定制剂中烟酰胺的含量.在CO2流动相中添加10%的甲醇,于填充柱上分离,检测波长为216nm,在测定范围内,浓度与其峰面积呈良好的线性关系(r=0.9998),峰面积的相对平均偏差(RSD)为1.39%,平均回收率97.3%~101.3%,4min即可完成分析.方法简便,样品前处理简单,可用于制剂中烟酰胺的快速分析。关键词:烟酰胺;超临界流体色谱;含量测定水溶性维生素对人们的生长发育和健康有着重要作用,人们除了从水果和蔬菜中摄取外,还从添加了维生素的食品和复合维生素制剂中补充人体的需要,有必要建立快速,稳定的分析方法用于其含量测定。对烟酰胺的含量测定方法主要是高效液相色谱法,该方法取得了较好的结果,但其分析时间长,样品前处理麻烦。此外,毛细管电泳,胶束电动毛细管电泳,气/质联用等方法也用于它的含量测定.本文探索了用超临界流体色谱测定维生素含量的方法,结果令人满意。1 仪器与试药超临界流体色谱仪:Gihon Model SF3系统(英国),对照品烟酰胺购自Lancaster化学公司(英国),甲醇为高效液相色谱纯,CO2为超临界流体色谱纯.2 实验方法及结果分析2.1 色谱条件色谱柱cyano(5μm,4.6×250mm),柱温50℃,紫外检测器配有高压检测池,其检测波长为216nm,进样装置带有l0μL进样阀的自动进样器,流动相压力20MPa,流动相流速为2.0mL/min。2.2 流动相对分离的影响只用CO2作流动相时,其保留时间太长,且色谱峰拖尾严重;当在流动相中加人10%的甲醇后,其峰形大为改善,保留时间缩短;当流动相流速改变时,保留时间会有小的改变,但对峰形几乎没有影响。2.3 线性关系考查将烟酰胺对照品取适量,精称后用甲醇稀释成5~50μg/mL的标准溶液,取6个不同浓度的对照品溶液按上述实验条件各进样三次,记录其色谱图,以对照品浓度(μg/mL)为横坐标,峰面积值为纵坐标,绘制标准曲线,得回归方程Y=一351.6+147.7X,R=0.9998,可见在所用浓度范围内具有良好的线性关系。2.4 精密度及稳定性试验测定该维生素日内和日间的峰面积,以考查分析方法的精密度和样品的稳定性,在上述实验条件下,连续进样8次,烟酰胺峰面积的相对标准偏差(RSD)为1.11%,放置1d后的RSD为1.39%,表现出良好的精密度和稳定性。2.5 回收率试验精密称取已知含量的同一样品三份,加人不同量的烟酰胺对照品,按样品测定项下的条件进样分析,计算其回收率,烟酰胺的回收率平均值±SD为98.3±1.28%。2.6 样品测定取昆明振华制药厂生产的复合维生素B(批号990701)5片,碾碎后用5mL甲醇溶解并超声提取20min,用0.45μm滤膜过滤,适当稀释后在上述色谱条件下进样分析,以峰面积按标准曲线法计算含量。3 讨论3.1 流动相选择当用CO2加10%甲醇作流动相时,烟酰胺的保留时间为3.7min。可以满足快速分析的要求,且色谱峰形得到改善。3.2 提取溶剂的选择比较了水、甲醇和乙醇作溶剂提取样品,结果以甲醇较好。样品用甲醇溶解并超声提取后,直接进样分析,不需要复杂的前处理.3.3 结果通过测定回收率,精密度并考查其线性关系,表明该方法可以于快速测定烟酰胺含量,能给出满意的结果.[参考文献][1] Hurtado S A,Nogues M T V,Pulido M I et a1.Determination of water—soluble vitamins in infant milk by HPLC[J].chromato A,1997,778:247.[2] Wills R B H,Shaw C G,Day W R.Analysis of water soluble vitamins by PHLC[J].Chromatogr Sci.,1977,15:62.
[align=left][/align][align=left]在使用含盐流动相,尤其是高盐浓度或梯度条件进行液相分析时,稍不留神就会出现盐析的现象,会导致压力升高以及色谱峰裂峰等问题,不仅影响实验进度,还会影响色谱柱的使用寿命;如果处理不好,柱效下降甚至色谱柱报废都是有可能的。[/align][align=left]为了防止色谱柱被破坏,为了维护实验室的和平,今天YoYo就来介绍一下含盐流动相的使用攻略,快跟我往下看吧[/align][align=center][/align][align=center] [/align][align=left][b][color=#0070c0]盐析的危害[/color][/b][/align][align=left]对于仪器的危害:系统堵塞,系统压力升高,泵压力波动增大,基线不平……[/align][align=left]对于色谱柱:柱压上升,峰形变差、裂峰,无法正常进行样品分析……[/align][align=left] [/align][align=left][/align][align=left][/align][align=left]因此,在使用含盐流动相时必须要特别注意以下几方面:[/align][align=left][/align][align=left][/align][align=left][b][color=#0070c0]1[/color][color=#0070c0]、色谱柱保存液[/color][/b][/align][align=left][b]1)未开封的新色谱柱[/b][/align][align=left] [/align][align=left]大阪曹達的新色谱柱,出厂保存液大多为100%乙腈(具体保存液种类请务必通过色谱柱盒内所附柱效报告单进行确认)。[/align][align=left]因此,为避免盐析,YoYo建议您按照以下步骤处理新色谱柱:[/align][align=left]①先使用与流动相组成比例相同但不含盐的溶液进行冲洗置换(避免使用纯水),时间建议1h以上[/align][align=left]②使用含盐流动相进行平衡[/align][align=left]③正常分析[/align][align=left][b] [/b][/align][align=left][b]2)已使用过的色谱柱[/b][/align][align=left] [/align][align=left]对于已开封使用过的色谱柱,需要了解使用履历,知晓前一次实验的条件、用完柱子后的最终保存液,判断是否需要再次进行保存液置换和过渡。[/align][align=left]建议用户建立实验室色谱柱管理表格,将色谱柱的使用履历(分析项目、流动相条件)、使用情况(柱压、用后柱效)进行记录,按照流程进行色谱柱的冲洗、保养和储存,方便对色谱柱进行管理。[/align][align=left] [/align][align=left][/align][align=left][/align][align=left][b][color=#0070c0]2、[/color][color=#0070c0]流动相的置换[/color][/b][/align][align=left][b] [/b][/align][align=left]在方法开发过程中,多数情况会涉及不同缓冲盐体系和不同有机相体系的各种尝试,那么在调整、更换流动相组成的过程中,请务必充分考虑到不同种类缓冲盐的溶解情况。[/align][align=left]一般情况下,盐的溶解能力:有机酸盐>无机酸盐[/align][align=left]最常用的磷酸缓冲盐中,溶解能力:铵盐>钾盐>钠盐[/align][align=left] [/align][align=left]若不确定所使用的缓冲盐和有机相之间的互溶情况,可按照不同比例将二者混合,静置30min,观察底部是否有沉淀或絮状物产生。[/align][align=left][b] [/b][/align][align=left][b][/b][/align][align=left][b][/b][/align][align=left][b][color=#0070c0]3[/color][color=#0070c0]、梯度条件[/color][/b][/align][align=left] [/align][align=left]当涉及缓冲盐-有机相梯度条件时,请确认缓冲盐在梯度条件中有机相最高点是否能够充分溶解。[/align][align=left]当然,不确定的时候也可以和上述方法一样,将缓冲盐和有机相按照梯度最高比例混合后静置,观察是否有沉淀产生。[/align][align=left][color=#0070c0] [/color][/align][align=left][color=#0070c0][/color][/align][align=left][color=#0070c0][/color][/align][align=left][b][color=#0070c0]4、[/color][color=#0070c0]色谱柱的保存[/color][/b][/align][align=left][b] [/b][/align][align=left]对于色谱柱使用时隔夜以及使用完后的保存,同样不能掉以轻心。[/align][align=left]当实验环境昼夜温差较大时,建议在夜间也要保持柱温(尽量使用柱温箱),并进行持续的小流速通液,以防止盐析;实验完毕后,使用不含盐的流动相(将缓冲盐相更换为纯水)对色谱柱和仪器进行冲洗置换,同样,在冲洗置换过程中不能使用纯水。[/align][align=left] [/align][align=left][/align][align=left][/align][align=left]希望今天的帖子能够帮到您,如果您有任何疑问欢迎留言![/align][align=center] [/align][align=center] [/align][color=#000000] [/color][color=#000000] [/color][color=#000000] [/color][align=left] [/align]
请问各位前辈,质谱分析流动相为什么要加乙酸?测一个中药里面的黄酮成分,流动相:0.05%乙酸-乙腈。
某项目流动相水相含0.15%辛烷硫酸钠,有机相为乙腈,样品中有一个未知峰,想做个质谱鉴定一下分子量,但是这个流动相含有离子对,而且这个物质若是流动相不添加离子对,根据之前分析方法开始时的结论,主峰与此杂质难以保留而且分不开,这种情况下,如何对这个样品做个液质?或者说如何将这个色谱条件转换为能做液质的条件?对于此类样品,若是将这个未知杂质在含离子对的条件下制备出来,是否有可能(其中的离子对试剂是否仍要除去)?