[url=http://www.f-lab.cn/microscopes-system/dplsm.html][b]差分偏光激光扫描显微镜[/b][/url]differential polarization laser-scanning microscope (DPLSM)具有[b]扫描光学显微镜[/b]和[b]分光偏振计[/b]的双重优点,可提供逐像素地实施的生物样本的各向异性数据,在记录生物组织图像强度的同时,能够实时地提供高精度的生物样品的各向异性组织的逐个像素的数据。差分偏光激光扫描显微镜采用模块化设计,可以直接安装到用户现有的激光扫描显微镜上,不用担心改变原来的光路和电子。我公司提供方便安装的差分偏光激光扫描显微镜DPLSM模块,可直接安装到激光扫描显微镜上,不需要改变电路和光路就可使用差分偏光激光扫描显微镜DPLSM功能。差分偏光激光扫描显微镜:[url]http://www.f-lab.cn/microscopes-system/dplsm.html[/url]
激光扫描共聚焦显微镜还能这么用! 众所周知,激光共聚焦显微镜主要的应用方向在观察活细胞结构及特定分子、离子的生物学变化,而在石笋这样的样品观察上使用激光扫描共聚焦显微镜,可以说脑洞大开了!让我们来看看原文,从Nikon A1激光扫描共聚焦显微镜使用者的角度看看,怎么把这个工具用活了! 激光扫描共聚焦显微镜在古气候纹层学的应用 第一作者:赵景耀 通讯作者:程 海 1984年第一台商业化的激光扫描共聚焦显微镜(Laser Scanning Confocal Microscope,简称 LSCM)出现,随之共聚焦显微镜技术成为了一个热点,并广泛应用在国内外生物和工业检测领域。现今,我们将LSCM首次应用于国内古气候纹层学研究。纹层学一直是古气候研究重要内容,特别是荧光微层在很多古气候载体中是重要的年代标尺和气候指标。2000年,Ribes等首次将LSCM应用于石笋荧光微层研究,发现LSCM分辨率可达1μm,因此,可适用于各种不同厚度的石笋年纹层;2008年,Orland等将LSCM与离子探针采样结合,首次发现了石笋δ18O的季节性信号,并表示以色列Soreq Cave单层δ18O季节波动可达2.15‰;2010年,Dasgupta等通过LSCM识别石笋纹层中的碎屑和粘土层,据此重建了美国明尼苏达州过去3000年极端暴雨事件,发现20世纪全球升温以来,其暴雨频率明显增加;2015年,Wendt利用LSCM,在巴西TBV Cave石笋纹层中发现了罕见的“双纹层”,且均出现在高生长速率的Heinrich事件期间,认为这与Heinrich期间,Intertropical Convergence Zone(ITCZ)南支南移所导致一年内存在2个雨季有关;2015年,Orland等再次将LSCM与离子探针技术应用于中国苦栗树洞石笋研究,发现全新世和B?lling-Aller?d暖期的夏季降水比例明显多于Younger Dryas时期。而目前,国内主要依赖于普通透射光和荧光显微镜,这一定程度上限制了国内古气候学研究。笔者在西安交通大学机械制造系统工程生物制造中心,利用购置的LSCM组件(图1a),观察石笋“年纹层”和砗磲“天纹层”,取得初步认识,以下分别就LSCM及其在古气候荧光微层方面的应用及注意事项作一简介。 图1 激光扫描共聚焦显微镜(LSCM)组件(a)及其原理(b) 1.倒置荧光显微镜(Inverted fluorescence microscope);2.荧光探测器(Flurescence detector);3.激光发生器(Laser generator);4.LSCM总控制器(Main controller);5.扫描头(Head of laser scanner);6.明场及电动载物台开关(Switch of bright-field microscopy and electric stage);7..荧光光源开关(Switch of fluorescent source);8.电动载物台(Electric stage);9.LSCM连接电脑(Computer and Monitor) LSCM以激光为点光源,由照明针孔与探测针孔对被探测点的共轭关系(图1b),实现对被探测点所在焦面的逐点激发,逐点扫描,该技术称为共聚焦。与普通荧光显微镜一次性照明整个视野不同,LSCM通过逐点扫描探测,呈现标本荧光层的2维或3维图像(图2),因此其对不同焦点和焦面的辨析能力,是普通荧光显微镜所不能达到的。其中,图2a中3D切片z轴步进间距(即焦面间距)为3μm,当前仪器上限25nm(仪器型号:Nikon A1)。在LSCM标本纹层成像过程中,放置于探测器前的探测针孔(Pinhole)(图1b)起着关键作用,有效地阻挡了不同焦点带来的杂散光,只有被探测点所发射的荧光透过Pinhole,到达探测器形成图像,这对图像对比度和分辨率有重要影响(图2)。而且LSCM采用光电倍增技术,可将微弱荧光信号进一步放大。综上,利用LSCM可以真正地实现10μm级荧光纹层的清晰辨别,其分辨率和辨识度是普通荧光显微镜所不能实现的,在此基础我们可以观察并辨别10μm左右石笋“年纹层”(图2d)和3~5μm级别砗磲“天纹层”(图2e)。 图2 石笋荧光层3D切片拟合(a)、石笋荧光“年纹层”(b、c和d)和砗磲荧光“天纹层”(e) 所有图像在1024扫描分辨率下,利用波长为488-nm的蓝色激光作为激发光源激发,然后用荧光滤光片滤选发射波长为505~539nm绿色发射光,最终被检测器探测并扫描成像;图片(a)由LSCM连续拍摄31层平行荧光焦面拟合而成,3μm/层;石笋样品(a)和(c)取自湖北省犀牛洞,(b)取自南京葫芦洞,(d)取自吉林省琉璃洞;(e)砗磲取自中国南沙群岛永暑礁 不同于普通光学显微镜,通过制作极薄的显微镜[url=http://www.gengxu.cn]滤光片[/url](≤1mm)实现对于杂散光或荧光焦面的控制。LSCM装配倒置荧光显微镜直接对古气候标本切面观察,源于LSCM对不同焦面荧光信号的精准解析和辨别能力,对于石笋和砗磲等古气候标本,无需制作显微镜薄片,只需将样品切面抛光磨平,即可实现对抛光表面荧光微层和透光微层定焦高分辨率扫描。LSCM极大地简化标本处理,不仅能够更好地节约和保护标本,且能和其他分析(如稳定同位素分析)在同一样品上进行,有利于精细对照,对于古气候研究有重要意义。例如,最近Li等在其他方法精确定年困难的情况下,利用LSCM方法精确确定了近百年石花洞的石笋样品年代序列;对著名的南京葫芦洞样品的初步工作显示,将能够重建上个冰期精细到年的时间序列及气候变化的变率(图2b),而又不破坏极其珍贵的样品。 但是由于LSCM以激光作为光源,在镜下观察过程中发现,根据物镜倍数(10×、20×、40×、60×和100×)不同,导致激光聚光强度不同,会出现不同程度的荧光猝灭,对于常用倍数10×和20×,荧光猝灭微弱,肉眼无法识别,可忽略。但是在60×油镜及以上倍数,荧光猝灭快速,因此在使用过程中,要注意调焦与拍摄时间的平衡。另外,计算机对焦过程是纳米级对焦,在标本前期处理过程中,保证样品观察面平整,是快捷对焦、自动扫描和拼接大图的工作基础。对于目前使用的型号Nikon A1,由于LSCM电动载物台承重和规格限制,以及明场聚光器位置限制(图1a),要求古气候标本观察面≤6cm×6cm,厚度≤5cm,但可根据需要选择不同型号的载物台。最后,由于各种LSCM在许多研究机构和医学院都具备,且使用费用不高,因此进行该研究不必购置新设备。
共焦显微镜因其高分辨率和能三维立体成像的优点被广泛应用在生物、医疗、半导体等方面。文章首先分析了影响共焦显微镜分辨率的因素,主要有光源、探测器孔径和杂散光等;并结合这些因素介绍了双光子共焦碌微镜、彩色共焦显微镜、荧光共焦显微镜、光纤共焦显微镜;然后从提高系统成像速度的方面介绍了波分复用共焦显微镜和频分复用共焦显微镜;最后分析了共焦显微镜的发展趋势。一、引言随着人们对于生物医学的研究,传统的光学显微镜已经无法满足研究的需要,人们需要可以实现三维成像的显微镜。1957年Marvin Minsky提出了共焦扫描显微镜的原理。1969年,耶鲁大学的Paul Davidovits和M.David Egger设计了第一台共焦显微镜,1987年第一台商业化共焦显微镜的问世,真正实现了三维立体成像。与普通光学显微镜相比,共焦显微镜具有极其明显的优点:能对物体的不同层面进行逐层扫描,从而获得大量的物体断层图像;可以利用计算机进行图像处理;具有较高的横向分辨率和纵向分辨率;对于透明和半透明物体,可以得到其内部的结构图像;还可以对活体细胞进行观察,获取活细胞内的信息,并对获得的信息进行定量分析。自共焦显微原理被提出以来,引起了研究者的广泛关注,提高显微系统的分辨率和改善系统的性能是研究者开发新型显微镜时考虑的主要因素。近几十年,国内外学者通过对共焦显微成像系统的三维点扩散函数、光学传递函数等方面的分析,得出影响显微系统分辨率的因素,主要包括系统的激励光源、探测器孔径、杂散光等。此外,共焦显微镜的成像速度也是决定系统性能的一个重要因素,专家们也一直在进行提高系统成像速度的研究。本文主要从提高显微系统分辨率和系统成像速度这两个方面来介绍共焦显微镜的发展情况。二、共焦扫描显微镜分辨率的提高光源、探测器孔径和杂散光等是影响共焦显微镜分辨率的几个主要因素,因此可以通过改善这些方面来提高显微系统的分辨率。1.光源显微镜的成像性质在很大程度上取决于所采用光源的相干性,有关研究表明,光源相干性好的系统其分辨率要比相干性差的系统要好,并且照明光源对分辨率的改变范围达到了26.4%。因此,选取适合的照明光源对提高显微系统的分辨率有很大帮助。常规的共焦扫描显微镜主要使用普通单色激光作为光源,随着技术的进步,目前已经出现了使用飞秒激光、超白激光、高斯光束作为光源的共焦显微镜,以提高系统性能,获得更高的分辨率。①飞秒激光为光源的双先子扫描共焦显微镜双光子扫描共焦显微镜通常使用近红外的飞秒激光作为激发光源,由于红外光具有较强的穿透性,它能探测到生物样品表面下更深层的荧光图像,并且生物组织对红外光吸收少,随着探测深度的增加衰减会变小,另一方面红外光的衍射低,光束的形状保持性好。2005年,Wild等人利用双光子扫描共焦显微技术实时观察和定量分析了PAHs在植物叶片表面和内部的光降解过程。后来又进一步研究了菲从空气到叶片的迁移过程、菲在叶片内部的运动及其分布情况等,该技术可观测PAHs在叶片内部的最大深度约为200μm。②白激光( supercontinuum laser)为光源的彩色共焦显微镜彩色共焦显微镜是利用光学系统的彩色像差,光源的不同光谱成分会聚焦到样品的不同深度,通过分析由样品反射的光谱能有效地获得样品的扫描深度。2004年,美国宾夕法尼亚州立大学的Zhiwen Liu课题小组使用光子晶体光纤产生的超连续谱白光作为彩色共焦显微镜的光源,这种超连续谱白光具有大的带宽,能够提高系统的扫描范围,能达到7μm扫描深度。另外超白激光有较高的空间相干性,无斑点噪声,能提高系统的信噪比和扫描速度。③使用高斯光束的荧光共焦显微镜荧光共焦显微镜是通过激光照射样品激发样品发出荧光,再通过探测器接受荧光对样品进行观察的共焦显微镜。华南农业大学的杨初平等人研究了不同光源孔径和束斑尺寸的高斯光束对荧光共焦显微镜分辨率的影响表明:与一定孔径尺寸的平行光束相比,采用高斯光束系统可以获得更好的分辨率。 2. 探测器孔径和杂散光共焦显微镜中探测器孔径能滤除部分杂散光,提高系统的分辨率和信噪比。根据相关文献对共焦扫描显微镜的三维光学传递函数与探测器孔径之间的依赖关系的研究,可以得到探测小孔直径为:d=β*1.22λ/NA,式中,β为物镜的放大率,λ为光的波长,NA为物镜的数值孔径。由该公式确定探测器小孔的直径,一方面满足了共焦扫描系统对探测器小孔直径的要求,从而保证高的横向和纵向分辨率,另一方面,又最大限度地使由试样中发射的荧光能量被探测器接收。为了更进一步提高系统分辨率,许多研究者对共焦显微镜中探测孔径进行了改进,例如使用单模光纤代替普通针孔孔径,还有双D型孔径等。① 使用单模光纤的光纤共焦显微镜在光纤共焦显微镜中用光纤分路器代替传统共焦显微镜中的光束分路器,并以单模光纤来代替光源和探测器的微米尺寸针孔孔径。使用单模光纤的优点在于:首先,在采用寻常针孔制作的共焦显微镜中,光源、针孔、探测器等有可能不在一条直线上从而会引起像差;但是在光纤作为针孔的共焦显微镜中,即使有的部件偏离直线时也不会引入像差。其次,使用单模光纤代替微型针孔,容易清除针孔的污染,而且不易受污染。第三,在使用光纤的系统中,可以自由移动显微镜部分而不必挪动探测器。2006年德克萨斯大学使用光纤共焦显微镜进行口腔病变检测,测得的系统横向和轴向分辨率分别为2. 1µm和10µm,成像速度为15帧/s,可观测范围为200µm×200µm。② 具有D型孔径的共焦显微镜近几年,具有对称D型光瞳的共焦显微成像技术引起广泛的关注,图1所示是该系统示意图。2006年美国东北大学的Peter J.Dwyer等人使用这种共焦显微镜进行了人体皮肤内部成像的实验,测得横向分辨率为1.7士0.1µm。2009年新加坡国立大学的Wei Gong等人采用傍轴近似方法理论分析了在共焦显微镜中使用双D型孔径对轴向分辨率的影响。分析表明在图1中的d值给定时,进入瞳孔的光信号强度l会随着探测器尺寸的增加而增加;但是在探测器尺寸给定时,光信号强度I会随着d的增加而单调递减。在使用有限大小的探测器时,改变d的大小,轴向分辨率可以得到改善。 http://www.biomart.cn//upload/userfiles/image/2011/11/1321512815.png 图1 双D型孔径共焦成像系统示意图在共焦成像光学系统中,到达像面的杂散光会在像面上产生附加的强度分布,从而进一步降低了像面的对比度,限制了系统分辨率的提高,因此在显微系统设计时,杂散光的影响也是不容忽视的。一般除了使用探测小孔来抑制杂散光,其他的一些设备例如可变瞳滤波器等对杂散光也有很好的过滤作用。最近以色列魏茨曼科学研究所的O.sipSchwartz and Dan Oron等人提出在系统中使用可变瞳滤波器,这个滤波器能够使多光子荧光共焦显微镜达到分辨率阿贝极限的非线性模拟,从而改善系统的分辨率。三、共焦扫描显微成像速度的提高共焦显微镜快速的成像速度为研究者观察生物细胞中快速动态反应提供了良好的条件。在共焦扫描显微成像系统中,传统的方法是通过改善扫描探测技术来提高成像速度。现有的扫描探测技术主要有Nipkow转盘法、狭缝共焦检测法、多光束的微光学器件检测法。这些方法可以改善扫描速度,但是与系统分辨率,视场之间都存在矛盾,因此又诞生了两种提高成像速度的新型显微镜:波分复用共焦显微镜和频分复用共焦显微镜。
激光共聚焦扫描显微镜简介一、 激光共聚焦显微镜的基本组成激光扫描共聚焦显微镜(laser scanning confocal microscope LSCM)是20世纪80年代发展起来的一项具有划时代意义的高科技新产品,是当今世界最先进的细胞生物学分析仪器。激光共聚焦显微镜利用激光作为光源,在传统光学显微镜基础上采用共轭聚焦的原理和装置,以及通过针孔的选择和PMT的收集,并带有一套对其所观察到的对象进行数字图像分析处理的系统软件。与传统光学显微镜相比,它具有更高的分辨率,实现多重荧光的同时观察并可形成清晰的三维图象等优点。所以它问世以来在生物学的研究领域中得到了广泛应用。激光共聚焦显微镜主要有四部分组成:1、显微镜光学系统。2、扫描装置。3、激光光源。4、检测系统。整套仪器由计算机控制,各部件之间的操作切换都可在计算机操作平台界面中方便灵活地进行。1.1 显微镜光学系统 显微镜是LSCM的主要组件,它关系到系统的成象质量。显微镜光路以无限远光学系统可方便地在其中插人光学选件而不影响成象质量和测量精度。物镜应选取大数值孔径平场复消色 差物镜,有利于荧光的采集和成象的清晰。物镜组的转换,滤色片组的选取,载物台的移动调节,焦平面的记忆锁定都应由计算机自动控制。1.2 扫描装置 LSCM使用的扫描装置在生物领域一般为镜扫描。由于转镜只需偏转很小角度就能涉及很大的扫描范围,图象采集速度大大提高,512×512画面每秒可达4帧以上,有利于那些寿命短的离子作荧光测定。扫描系统的工作程序由计算机自动控制。1.3 激光光源 LSCM使用的激光光源有单激光和多激光系统。多激光器系统在可见光范围使用多谱线氩离子激光器,发射波长为457nm、488nm和514nm的蓝绿光,氦氖绿激光器提供发射波长为543nm的绿光,氦氖红激光器发射波长为633nm的红光,新的405nm半导体激光器的出现可以提供近紫外谱线,但是小巧便宜而且维护简单。1.4 检测系统 LSCM为多通道荧光采集系统,一般有三个荧光通道和一个透射光通道,能升级到四个荧光通道,可对物体进行多谱线激光激发,样品发射荧光的探测器为感光灵敏度高的光电倍增管PMT,配有高速12位A/D转换器,可以做光子计数。PMT前设置针孔,由计算机软件调节针孔大小,光路中设有能自动切换的滤色片组,满足不同测量的需要,也有通过光栅或棱镜分光后进行光谱扫描功能的设置。二、激光共聚焦显微镜的特点以及在生物领域的应用传统光学显微镜相比,激光共聚焦显微镜具有更高的分辨率,实现多重荧光的同时观察并可形成清晰的三维图象等优点,在对生物样品的观察中,激光共聚焦显微镜有如下优越性:1、对活细胞和组织或细胞切片进行连续扫描,可获得精细的细胞骨架、染色体、细胞器和细胞膜系统的三维图像。2、 可以得到比普通荧光显微镜更高对比度、高解析度图象、同时具有高灵敏度、杰出样品保护。3、***图象的获得,如7 维图象(XYZaλIt): xyt 、xzt 和xt 扫描,时间序列扫描旋转扫描、区域扫描、光谱扫描、同时方便进行图像处理。 4、细胞内离子荧光标记,单标记或多标记,检测细胞内如PH和钠、钙、镁等离子浓度的比率测定及动态变化。5、荧光标记探头标记的活细胞或切片标本的活细胞生物物质,膜标记、免疫物质、免疫反应、受体或配体,核酸等观察;可以在同一张样品上进行同时多重物质标记,同时观察; 6、对细胞检测无损伤、精确、准确、可靠和优良重复性;数据图像可及时输出或长期储存。 由于共聚焦显微镜的以上优点,激光共聚焦显微镜在以下研究领域中应用较为广泛:1、细胞生物学:如:细胞结构、细胞骨架、细胞膜结构、流动性、受体、细胞器结构和分布变化、细胞凋亡机制;各种细胞器、结构性蛋白、DNA、RNA、酶和受体分子等细胞特异性结构的含量、组分及分布进行定量分析;DNA、RNA含量、利用特定的抗体对紫外线引起的DNA损伤进行观察和定量;分析正常细胞和癌细胞细胞骨架与核改变之间的关系;细胞黏附行为等 2、生物化学:如:酶、核酸、受体分析、荧光原位杂交、杂色体基因定位等,利用共聚焦技术可以取代传统的核酸印迹染交等技术,进行基因的表达检测,使基因的转录、翻译等检测变的更加简单、准确。3、药理学:如:药物对细胞的作用及其动力学;药物进入细胞的动态过程、定位分布及定量 4、生理学、发育生物学:如:膜受体、离子通道、离子含量、分布、动态;动物发育以及胚胎的形成,骨髓干细胞的分化行为;细胞膜电位的测量.荧光漂白恢复(FRAP)、荧光漂白丢失(FLIP)的测量等。 5、遗传学和组胚学:如:细胞生长、分化、成熟变化、细胞的三维结构、染色体分析、基因表达、基因诊断; 6、神经生物学:如:神经细胞结构、神经递质的成分、运输和传递; 7、微生物学和寄生虫学:如:细菌、寄生虫形态结构; 8、病理学及病理学临床应用:如:活检标本的快速诊断、肿瘤诊断、自身免疫性疾病的诊断; 9、免疫学、环境医学和营养学。如:免疫荧光标记(单标、双标或三标)的定位,细胞膜受体或抗原的分布,微丝、微管的分布、两种或三种蛋白的共存与共定位、蛋白与细胞器的共定位;对活细胞中的蛋白质进行准确定位及动态观察可实时原位跟踪特定蛋白在细胞生长、分裂、分化过程中的时空表达,荧光能量共转移(FRET)。
问题:Renishaw Raman显微系统用的激光器514 532 633 785nm具体是什么型号的?
在网站上看到的资料,不知道有没有人需要。可以浏览一下[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=27908]激光扫描共聚焦显微镜系统及其在细胞生物学中的应用[/url]
最近在了解高温观察用激光共焦扫描显微镜,看了很多有关采用CLSM观察的高温熔化、凝固和固态相变的观察,感觉很不错。但是我在论坛里看见采用激光扫描共焦显微镜拍摄的很多三维组织图像照片,这种激光共焦扫描显微镜和宝钢、首钢的那种高温观察用的激光扫描共焦显微镜是不是不一样啊??激光共焦扫描显微镜是不是也分好几种啊,请专家解惑,我刚刚接触,不是很了解。另外高温观察用激光共焦扫描显微镜大概多少钱啊,在哪里买呢,谢谢大家
共聚焦显微系统(LSCM)诞生至今,短短二十多年里,已经成为了科学研究的重要工具。在我国生命科学研究领域,也发挥着巨大的作用。如何更好利用激光共聚焦技术,推动生命科学研究,受到了学术界的广泛关注。 激光共聚焦显微镜作为光学显微镜的重大改进,与传统场式(widefield)照明显微镜相比有许多独特的优点, 它可以控制焦深、照明强度,降低非焦平面光线噪音干扰,从一定厚度标本中获取光学切片。可以在不改变普通荧光显微镜的制片方法的前提下,观察到非常清晰的高质量图像,并且通过共聚焦显微镜可以十分方便的观察活的细胞或组织。 它的诞生,大大提高了科学研究的效率。目前共聚焦显微镜在国内的应用已经相当广泛,在越来越多的国家级科研院所与高校实验室,都能看到科研工作者忙碌在共聚焦显微镜前的身影。以下为奥林巴斯品牌类显微镜:智能激光扫描共聚焦显微镜——FV10iFV1000MPE:只关注多光子荧光成像FluoView™ FV1000共聚焦显微镜DSU转盘扫描显微镜奥林巴斯FluoView™ FV300(已停产)大家了解多少?欢迎讨论用后感想。
摘要激光扫描共聚焦显微镜作为80年代发展起来的一种高精度分子细胞生物学分析仪器,具有组织细胞断层扫描、活细胞动态荧光监测、三维图像重建、共聚焦图像定量分析等先进功能,在近年的细胞凋亡这一研究热点中得到了大量创造性的应用。本文拟就对激光扫描共聚焦显微镜在凋亡的形态学、分子水平变化及重要生理过程三方面研究中的应用及其成果做一综述。细胞凋亡(apoptosis)是不同于细胞坏死的一种细胞主动死亡方式,并由特定的基因控制。凋亡细胞在形态上出现变圆皱缩、染色质浓缩边集、核碎裂、凋亡小体形成等变化,并最终由非炎症过程清除。由于细胞凋亡独特地影响着机体的细胞发育和代谢,在监测和清除肿瘤细胞与突变细胞等方面也可能发挥重要的作用,近年来受到了细胞生物学、分子生物学、免疫学等多学科的广泛关注。激光扫描共聚焦显微镜(laser scaing confocal microscopy, LSCM)是80年代发展起来的一种高精度分子细胞生物学分析仪器,辅以各类免疫荧光探针或荧光染料与被测物质特异性结合,不仅可观察固定的细胞组织切片,还可对活细胞的结构、分子和离子进行实时动态地观察和检测。在细胞凋亡的研究中,激光扫描共聚焦显微镜已被广泛地应用于形态学、分子水平监测及重要生理改变等各方面,其中不乏新颖之处,并获得了大量成果,以下将就此做一简单的介绍。激光扫描共聚焦显微镜与凋亡的形态学激光扫描共聚焦显微镜用点光源扫描标本的光学横断面,以代替普通光学显微镜所使用的场光源,并用探测针孔滤去离焦光线,所以消除了来自焦平面以外的衍射或散射光的干扰,可实现高清晰、高分辨率的组织细胞断层扫描。并且由于激光扫描共聚焦显微镜采用数字化成像,因而辅以一定的软件就能对图像进行定量分析及三维重建等操作。过去对细胞凋亡的形态学研究方法局限于活性细胞和组织切片染色、荧光镜观察,或者石蜡切片原位末端标记法。由于普通光镜的分辨率和清晰度有限,而电镜又显然不适合对凋亡这一复杂动态过程的监测,激光扫描共聚焦显微镜的应用使人们对细胞凋亡的形态学观察分析提高到了一个前所未有的新水平。细胞核核膜的破坏对于染色质聚集并形成凋亡小体起重要作用。lamin是构成核片层的蛋白质,位于核膜的内表面,由caase-6介导的lamin裂解可影响核膜的完整性。在McCall等的研究中,对果蝇卵子发生晚期的细胞凋亡现象进行了动态观察。以单抗mAb101标记其哺育细胞核内膜的laminDm0(哺乳类laminB的同源体),用激光扫描共聚焦显微镜加以观察。正常哺育细胞到11期时,染色的lamin呈弥散的雾状分布并围绕核周,而dcp-1GLC哺育细胞即使到了较晚的14期时,仍然显示界线明确的染色。可见dcp-1突变体在核lamin蛋白的酶切或解聚方面存在缺陷。细胞器Li 等在对C(6)-酰基鞘氨醇诱导胞内囊泡产生的研究中,在不产生中毒效应的情况下,加入10microM C(6)-酰基鞘氨醇以诱导鼠纤维母细胞(3T3-L1和3T3-F442A)凋亡。观察到囊泡的形成与C(6)-酰基鞘氨醇的诱导呈时间依从和剂量依从关系。大量小泡在其加入后8小时内出现,并且随时间而增大;大泡最终分布在核周,而小泡分布在细胞边缘。用抗-溶酶体膜蛋白抗体和共聚焦免疫荧光显微分析,证明增大的囊泡为晚期内吞体/溶酶体。另外,胞内的细胞器都有其适用的荧光探针,如高尔基复合体常用的探针有Dceramide、BODIPY ceramide等,内质网常用的有Dil、DiOC6等,经标记均可进行精细的观察。当然,激光扫描共聚焦显微镜在形态学中的优势更在于其对图像的三维重建功能,从而揭示过去只能在平面上显现的凋亡细胞在三维空间中的结构;而对细胞凋亡的动态过程,它可以用三维加时间的四维方式进行观察,来获取最逼真的形态学资料。凋亡过程中一些特征性的三维形态变化正期待着进一步具体的工作去发现。激光扫描共聚焦显微镜对凋亡细胞的分子水平监测随着分子生物学突飞猛进的发展,关于细胞凋亡分子机制的研究已有了很大的突破。细胞凋亡的信号传递途径及其调控涉及到大量的酶级联反应、生物大分子的空间转移等。而激光扫描共聚焦显微镜以其定性、定量、定时的优点,结合众多荧光探针的应用,成为了研究细胞凋亡分子水平变化的有力手段。DNA大分子DNA断裂以及染色质的异常凝聚,是细胞凋亡的关键,同时也是细胞核在细胞凋亡中具有标志性的变化。Columbara等报道将激光扫描共聚焦显微镜与原位TdT和Poll免疫荧光技术相结合,进而确定双链和单链DNA的断裂点。而在对细胞凋亡和细胞坏死区别的研究中,Kreel等在培养的K562细胞中加入放线菌素D以诱导凋亡,并对细胞的DNA片段进行了3’-末端标记。经激光扫描共聚焦显微镜观察发现K562细胞凋亡早期有大量DNA片段出现,且DNA片段弥散分布于除核仁外的细胞核区。伴随着凋亡的进展,细胞核内出现大量高标记密度的圆形小体。而采用NaN3或快速冻融法使细胞坏死,经激光扫描共聚焦显微镜观察证实,在坏死开始阶段并无DNA片段的出现,至少在坏死发生24小时后才有DNA片段产生。Caase家族Caases是一组高度保守的半胱氨酸蛋白酶,目前发现有11个成员。多数细胞凋亡是以Caase家族蛋白的激活并作用于其关键底物而实现的,而caases激活的关键又在于该家族蛋白间的级联反应,因此caases被认为是细胞凋亡的中心环节和执行者,成为研究的热点。Mandal等用激光扫描共聚焦显微镜对细胞凋亡中激活的caase-3的重分布进行了研究。用丁酸处理细胞后,观察到DNA-PKcs的裂解与caase-3的激活成正相关,而Bcl-2的过度表达则可抑制上述两个过程。同时还证明(1)激活后的caase-3重分布到核区,(2)裂解局部的DNA-PKcs和PARP(polyADP-ribosepolymerase,聚腺苷二磷酸核糖多聚酶),(3)裂解产物又被释放到核外的细胞液。caase-3的抑制物四肽DEVD-CHO又可抑制上述的三个连续的步骤。该研究提示:激活的caase-3在核内的重分布构成了丁酸所诱导的细胞凋亡中的一个重要凋亡信号。另外,在用激光扫描共聚焦显微镜对Q79诱导大鼠神经元凋亡的研究中,Sanchez等发现了Q79对caase-8的聚集和激活,而对caase-8的抑制则阻止了被诱导的细胞凋亡;加以Westernblot分析,还建立了caase-8的激活和某些神经退行性疾病(如舞蹈病)的联系。Grazyme丝氨酸蛋白酶grazyme为另一种重要的凋亡信号分子,对某些caase家族蛋白也有激活作用。Trapani等就证明了杀伤淋巴细胞利用穿孔素和grazymeB的协同作用来诱导靶细胞的凋亡,在其研究中通过激光扫描共聚焦显微镜观察到(1)50%细胞的胞核内快速聚集了以FITC荧光标记的grazymeB(最长7分钟,t1/2为2分钟),然后发生凋亡;(2)其它的细胞只有细胞液内有FITC-grazyme B的摄取,避免了凋亡。此间至少在13分钟后才有DNA碎片的出现,说明核内的grazyme B聚集出现在凋亡的执行阶段之前。并且通过对核内液的处理(加入70KDa FITC-dextran),间接观察到grazyme B的转移并非是因为核膜受caases的作用而破损,而是由于穿孔素的协同。其它以上的介绍显示,激光扫描共聚焦显微镜在检测活细胞酶活性动态变化方面有着突出的优势。实际上,对于细胞凋亡的分子机制这样一个极其复杂的课题,激光扫描共聚焦显微镜的应用远不只限于上述的几种离子和大分子,而是渗透到了大量的分枝课题中去。如在对重要的凋亡负调控蛋白Bcl-2的研究中,Beham等利用基因毒性损害(genotoxic damage)诱导细胞凋亡,并以Bcl-2蛋白抑制其凋亡过程。用激光扫描共聚焦显微镜和Immunoblotting观察显示,Bcl-2的作用在于阻止了诱导产生的p53蛋白向核内的转运。而Ohsawa等对独立于caase家族的另一种重要蛋白酶—组织蛋白酶进行了研究,用血清剥夺法诱导PC12细胞凋亡,并用激光扫描共聚焦显微镜监测了其精细超微结构改变过程和细胞内组织蛋白酶B和D的免疫活度的对比变化。又如,在人胰岛淀粉样多肽(hIA)的研究中,Hiddinga等用表达hIA的质粒转染COS-1细胞诱导凋亡,辅以免疫组化染色,用激光扫描共聚焦显微镜证明了hIA在细胞的内质网和高尔基复合体内呈簇状沉积,并与细胞
激光共聚焦显微镜系统的原理和应用激光扫描共聚焦显微镜是二十世纪80年代发展起来的一项具有划时代的高科技产品,它是在荧光显微镜成像基础上加装了激光扫描装置,利用计算机进行图像处理,把光学成像的分辨率提高了30%--40%,使用紫外或可见光激发荧光探针,从而得到细胞或组织内部微细结构的荧光图像,在亚细胞水平上观察诸如Ca2+ 、PH值,膜电位等生理信号及细胞形态的变化,成为形态学,分子生物学,神经科学,药理学,遗传学等领域中新一代强有力的研究工具。激光共聚焦成像系统能够用于观察各种染色、非染色和荧光标记的组织和细胞等,观察研究组织切片,细胞活体的生长发育特征,研究测定细胞内物质运输和能量转换。能够进行活体细胞中离子和PH值变化研究(RATIO),神经递质研究,微分干涉及荧光的断层扫描,多重荧光的断层扫描及重叠,荧光光谱分析荧光各项指标定量分析荧光样品的时间延迟扫描及动态构件组织与细胞的三维动态结构构件,荧光共振能量的转移的分析,荧光原位杂交研究(FISH),细胞骨架研究,基因定位研究,原位实时PCR产物分析,荧光漂白恢复研究(FRAP),胞间通讯研究,蛋白质间研究,膜电位与膜流动性等研究,完成图像分析和三维重建等分析。一.激光共聚焦显微镜系统应用领域:涉及医学、动植物科研、生物化学、细菌学、细胞生物学、组织胚胎、食品科学、遗传、药理、生理、光学、病理、植物学、神经科学、海洋生物学、材料学、电子科学、力学、石油地质学、矿产学。二.基本原理传统的光学显微镜使用的是场光源,标本上每一点的图像都会受到邻近点的衍射或散射光的干扰;激光扫描共聚焦显微镜利用激光束经照明针孔形成点光源对标本内焦平面的每一点扫描,标本上的被照射点,在探测针孔处成像,由探测针孔后的光点倍增管(PMT)或冷电耦器件(cCCD)逐点或逐线接收,迅速在计算机监视器屏幕上形成荧光图像。照明针孔与探测针孔相对于物镜焦平面是共轭的,焦平面上的点同时聚焦于照明针孔和发射针孔,焦平面以外的点不会在探测针孔处成像,这样得到的共聚焦图像是标本的光学横断面,克服了普通显微镜图像模糊的缺点。三.应用范围:细胞形态学分析(观察细胞或组织内部微细结构,如:细胞内线粒体、内质网、高尔基体、微管、微丝、细胞桥、染色体等亚细胞结构的形态特征;半定量免疫荧光分析);荧光原位杂交研究;基因定位研究及三维重建分析。1.细胞生物学:细胞结构、细胞骨架、细胞膜结构、流动性、受体、细胞器结构和分布变化2.生物化学:酶、核酸、FISH(荧光原位杂交)、受体分析3.药理学:药物对细胞的作用及其动力学4.生理学:膜受体、离子通道、细胞内离子含量、分布、动态5.神经生物学:神经细胞结构、神经递质的成分、运输和传递、递质受体、离子内外流、神经组织结构、细胞分布6.微生物学和寄生虫学:细菌、寄生虫形态结构7.病理学及临床应用:活检标本诊断、肿瘤诊断、自身免疫性疾病诊断、HIV等8.遗传学和组胚学:细胞生长、分化、成熟变化、细胞的三维结构、染色体分析、基因表达、基因诊断四.激光共聚焦显微镜在医学领域中的应用A.在细胞及分子生物学中的应用1. 细胞、组织的三维观察和定量测量2. 活细胞生理信号的动态监测3. 粘附细胞的分选4. 细胞激光显微外科和光陷阱功能5. 光漂白后的荧光恢复6. 在细胞凋亡研究中的应用B.在神经科学中的应用1. 定量荧光测定2. 细胞内离子的测定3. 神经细胞的形态观察C.在耳鼻喉科学中的应用1. 在内耳毛细胞亚细胞结构研究上的应用2. 激光扫描共聚焦显微镜的荧光测钙技术在内耳毛细胞研究中的应用3. 激光扫描共聚焦显微镜在内耳毛细胞离子通道研究上的应用4. 激光扫描共聚焦显微镜在嗅觉研究中的应用D.在肿瘤研究中的应用1. 定量免疫荧光测定2. 细胞内离子分析3. 图像分析:肿瘤细胞的二维图像分析4. 三维重建 E.激光扫描共聚焦显微镜在内分泌领域的应用1. 细胞内钙离子的测定2. 免疫荧光定位及免疫细胞化学研究3. 细胞形态学研究:利用激光扫描共聚焦显微镜 F.在血液病研究中的应用1. 在血细胞形态及功能研究方面的应用2. 在细胞凋亡研究中的应用 G.在眼科研究中的应用1. 利用激光扫描共聚焦显微镜观察组织、细胞结构2. 集合特殊的荧光染色在活体上观察角膜外伤修复中细胞移行及成纤维细胞的出现3. 利用激光扫描共聚焦显微镜观察视网膜中视神经细胞的分布以及神经原的树枝状形态4. 三维重建H. 激光扫描共聚焦显微镜在肾脏病中的应用可以系统观察正常人肾小球系膜细胞的断层扫描影像及三维立体影像水平,使图像更加清晰,从计算机分析系统可从外观到内在结构,从平面到立体,从静态到动态,从形态到功能几个方面对系膜细胞的认识得到提高。北京中科研域科技有限公司(蔡司显微镜代理商)地址:北京市朝阳区建国路15号院甲1号北岸1292,一号楼406室联系人:张辉13911188977 邮编:100024电话:010-57126588 传真:010-85376588E-mail:[email=zhs_8000@126.com][color=#0365bf]zhs_8000@126.com[/color][/email]
激光共聚焦显微镜系统的原理和应用激光扫描共聚焦显微镜是二十世纪80年代发展起来的一项具有划时代的高科技产品,它是在荧光显微镜成像基础上加装了激光扫描装置,利用计算机进行图像处理,把光学成像的分辨率提高了30%--40%,使用紫外或可见光激发荧光探针,从而得到细胞或组织内部微细结构的荧光图像,在亚细胞水平上观察诸如Ca2+ 、PH值,膜电位等生理信号及细胞形态的变化,成为形态学,分子生物学,神经科学,药理学,遗传学等领域中新一代强有力的研究工具。激光共聚焦成像系统能够用于观察各种染色、非染色和荧光标记的组织和细胞等,观察研究组织切片,细胞活体的生长发育特征,研究测定细胞内物质运输和能量转换。能够进行活体细胞中离子和PH值变化研究(RATIO),神经递质研究,微分干涉及荧光的断层扫描,多重荧光的断层扫描及重叠,荧光光谱分析荧光各项指标定量分析荧光样品的时间延迟扫描及动态构件组织与细胞的三维动态结构构件,荧光共振能量的转移的分析,荧光原位杂交研究(FISH),细胞骨架研究,基因定位研究,原位实时PCR产物分析,荧光漂白恢复研究(FRAP),胞间通讯研究,蛋白质间研究,膜电位与膜流动性等研究,完成图像分析和三维重建等分析。一.激光共聚焦显微镜系统应用领域:涉及医学、动植物科研、生物化学、细菌学、细胞生物学、组织胚胎、食品科学、遗传、药理、生理、光学、病理、植物学、神经科学、海洋生物学、材料学、电子科学、力学、石油地质学、矿产学。二.基本原理传统的光学显微镜使用的是场光源,标本上每一点的图像都会受到邻近点的衍射或散射光的干扰;激光扫描共聚焦显微镜利用激光束经照明针孔形成点光源对标本内焦平面的每一点扫描,标本上的被照射点,在探测针孔处成像,由探测针孔后的光点倍增管(PMT)或冷电耦器件(cCCD)逐点或逐线接收,迅速在计算机监视器屏幕上形成荧光图像。照明针孔与探测针孔相对于物镜焦平面是共轭的,焦平面上的点同时聚焦于照明针孔和发射针孔,焦平面以外的点不会在探测针孔处成像,这样得到的共聚焦图像是标本的光学横断面,克服了普通显微镜图像模糊的缺点。三.应用范围:细胞形态学分析(观察细胞或组织内部微细结构,如:细胞内线粒体、内质网、高尔基体、微管、微丝、细胞桥、染色体等亚细胞结构的形态特征;半定量免疫荧光分析);荧光原位杂交研究;基因定位研究及三维重建分析。1.细胞生物学:细胞结构、细胞骨架、细胞膜结构、流动性、受体、细胞器结构和分布变化2.生物化学:酶、核酸、FISH(荧光原位杂交)、受体分析3.药理学:药物对细胞的作用及其动力学4.生理学:膜受体、离子通道、细胞内离子含量、分布、动态5.神经生物学:神经细胞结构、神经递质的成分、运输和传递、递质受体、离子内外流、神经组织结构、细胞分布6.微生物学和寄生虫学:细菌、寄生虫形态结构7.病理学及临床应用:活检标本诊断、肿瘤诊断、自身免疫性疾病诊断、HIV等8.遗传学和组胚学:细胞生长、分化、成熟变化、细胞的三维结构、染色体分析、基因表达、基因诊断四.激光共聚焦显微镜在医学领域中的应用A.在细胞及分子生物学中的应用1.细胞、组织的三维观察和定量测量2.活细胞生理信号的动态监测3.粘附细胞的分选4.细胞激光显微外科和光陷阱功能5.光漂白后的荧光恢复6.在细胞凋亡研究中的应用B.在神经科学中的应用1.定量荧光测定2.细胞内离子的测定3.神经细胞的形态观察C.在耳鼻喉科学中的应用1.在内耳毛细胞亚细胞结构研究上的应用2.激光扫描共聚焦显微镜的荧光测钙技术在内耳毛细胞研究中的应用3.激光扫描共聚焦显微镜在内耳毛细胞离子通道研究上的应用4.激光扫描共聚焦显微镜在嗅觉研究中的应用D.在肿瘤研究中的应用1. 定量免疫荧光测定2. 细胞内离子分析3. 图像分析:肿瘤细胞的二维图像分析4. 三维重建 E.激光扫描共聚焦显微镜在内分泌领域的应用1. 细胞内钙离子的测定2. 免疫荧光定位及免疫细胞化学研究3. 细胞形态学研究:利用激光扫描共聚焦显微镜 F.在血液病研究中的应用1. 在血细胞形态及功能研究方面的应用2. 在细胞凋亡研究中的应用 G.在眼科研究中的应用1. 利用激光扫描共聚焦显微镜观察组织、细胞结构2. 集合特殊的荧光染色在活体上观察角膜外伤修复中细胞移行及成纤维细胞的出现3. 利用激光扫描共聚焦显微镜观察视网膜中视神经细胞的分布以及神经原的树枝状形态4. 三维重建H. 激光扫描共聚焦显微镜在肾脏病中的应用可以系统观察正常人肾小球系膜细胞的断层扫描影像及三维立体影像水平,使图像更加清晰,从计算机分析系统可从外观到内在结构,从平面到立体,从静态到动态,从形态到功能几个方面对系膜细胞的认识得到提高。
共焦激光扫瞄显微镜ZEISS所提供之英文数据,内容包含:1.影像构成原理2.电子信号处理[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=32959]共焦激光扫瞄显微镜[/url]
一、在细胞及分子生物学中的应用1. 细胞、组织的三维观察和定量测量 共聚焦显微镜的分辨率超过普通光学显微镜,染色过程简便,可以在活细胞上进行无创伤性的染色,最大程度地维持细胞的正常形态。多种自发性的荧光染料,已被广泛地用于诸如RNA、DNA细胞核、线粒体、内质网、肌动蛋白、细胞膜等结构的标记。运用免疫荧光技术,将不同波长的两三种荧光物质标记在内部不同结构的相应抗体上,以这几种荧光物质特定的光谱特性选择激发光和滤光片,则可以观察到细胞内部各结构间的毗邻关系。特别是在荧光着丝点易被遮盖(如荧光原位杂交实验)的情况下,这种三维图像的多角度观察提供了极大的优越性。细胞有丝分裂中细胞核内染色体数目(双倍体、多倍体)、形态和位置的变化,一直是细胞生物学肿瘤研究中的热点。着丝点是细胞核内的重要结构,被认为在有丝分裂中起重要的作用,应用共聚焦显微镜的定量测量技术,可以较精确地测定着丝点在不同分裂期的位置。共聚焦显微镜生成厚度小于0.2微米的依次相连的光学切片,即使较厚的组织的三维数据也可被计算机获取,运用适当的图像分析软件,可以测量并确定所观察结构的表面特征,体积等参数,为相互结合定量测量提供了新手段。2. 活细胞生理信号的动态监测:活细胞的功能监测在细胞生物学、神经生理学、药理学等领域都有重要意义。许多荧光染料可以聚集在细胞的特定结构,而对细胞的活性基本上不产生影响。可以利用这一特性来反映细胞受到刺激后形态或功能的改变。如亲脂性染料DiOC6(3)主要聚集在内质网,且对细胞的毒副作用极小。肌细胞中的肌浆网与ER有相同的属性,是胞内钙库,应用共聚焦显微镜,就可以动态观察肌细胞兴奋时SR的变化。许多参与神经元兴奋传导的离子如K+、Na+、Ca2+及H+、Cl-、Mg2+ 等,都有其自发性的荧光染料。Ca2+ 在细胞的兴奋、分化、死亡等过程中都起重要作用,是许多生理反应的胞内第二信使,是目前研究得最为充分的离子; 通过激光扫描共聚焦显微镜对胞内、核内钙转移的研究、对心肌细胞的钙变化研究、免疫细胞钙信号的研究、对Ca2+信号在凋亡细胞中作用的研究都取得了可喜的结果,而更多的研究则是将激光扫描共聚焦显微镜应用于神经生物学中对神经元Ca2+动态测量的研究。目前激光扫描共聚焦显微镜以其独特的优势成为钙研究中的重要手段之一。3. 粘附细胞的分选(adherent cell sorting) 对特异细胞的分选和克隆,是研究单个细胞或细胞系生物特性的先决条件。 将细胞贴壁培养在特制培养皿上,培养皿底部有一层特殊的膜,用高能量激光在欲选细胞四周切割成八角形几何形状,掀去培养皿底部的膜,非选择细胞则被去除。目前对粘附细胞分选方法多用于对杂交瘤和突变细胞的分选,也有用于对经转化的平滑肌细胞,卵巢癌细胞及人畸胎瘤干细胞等的分选和克隆,还可用于基因调控、基因治疗等研究。4. 细胞激光显微外科和光陷阱功能: 激光扫描共聚焦显微镜可将激光当作一把“光刀子”使用,完成诸如细胞膜瞬间穿孔,染色体切割,神经元突起切除等一系列细胞外科手术。光镊是利用激光的力学效应,将一个微米级大小的细胞或其它结构钳制于激光束的焦平面上,也称为光陷阱。光镊可以用来进行细胞融合(如卵细胞受精)、机械刺激或细胞骨架弹性测量等,特别是在测量植物细胞的细胞骨架时很有意义。5. 光漂白后的荧光恢复(FRAP): 细胞在相互接触后彼此间即有低阻抗的通道形成,以进行细胞间通讯;被经合成肽测试法证明只允许低于1.5KD分子通过的通道被称作缝隙连接。缝隙连接是存在于相邻细胞间的一类蛋白通道,普遍认为缝隙连接通过介导细胞间的信息传递,在诸如增殖、分化、代谢等过程中发挥极其重要作用。FRAP技术借助脉冲式激光照射细胞的某一区域,从而该区域荧光分子的光淬灭,该区域周围的未淬灭的荧光分子将以一定速率向受照区域扩散,而此扩散速率可通过低强度激光扫描探测。在研究细胞骨架构成、跨膜大分子迁移率、细胞膜流动性、胞间通讯等领域中有较大的意义。6. 在细胞凋亡研究中的应用细胞凋亡是由体内外因素触发细胞内预存的死亡程序而导致的细胞死亡过程,细胞凋亡作为生理性、主动性过程,能够确保正常发育、生长、维持内环境稳定,发挥积极的防御功能。用激光扫描共聚焦显微镜观察凋亡细胞,可见凋亡细胞体积变小,细胞质浓缩,细胞核变小,出现染色质沿核膜内侧排列的核边聚集现象。细胞凋亡的晚期,细胞核裂解为碎块,产生凋亡小体。细胞凋亡(Apoposis)是生物体内广泛存在的,由细胞特定基因控制,以细胞DNA 降解为特征的细胞自发过程,与机体中多种生理及病理过程密切相关。因而,对Apoposis 的研究现已成为研究细胞生物学研究的热点之一。而激光扫描共聚集显微镜结合众多荧光探针的应用,成为细胞Apoposis超微结构及分子水平变化的有力手段。二、在神经科学中的应用1. 定量荧光测定:对活细胞进行定量测定,具有很好的重复性,分析神经细胞和胶质细胞的某些物理及生物化学特性;监测抗原表达,细胞结合和杀伤等特征。在多发性硬化病人大脑活检标本上观察病变组织的微血管内皮细胞特异性地表达。2. 细胞内离子的测定:使用多种荧光探针,对神经细胞的Ca2+、PH及其它各种细胞内离子进行定量和动态分析。3. 神经细胞的形态学观察:激光扫描共聚焦显微镜使用模拟荧光处理,可将系列光学切片的数据合成三维图像,并可从任意角度观察。如Joshi等观察了细胞突触的骨架的三维图像。三维重建图像可使神经细胞及细胞器的形态学结构更加生动逼真。三、在耳鼻喉科学中的应用1. 在内耳毛细胞亚细胞结构研究上的应用:1993年Ikeda等应用激光扫描共聚焦显微镜研究内耳毛细胞的亚细胞结构,用Rhodamine 123染色,见线粒体分布于表皮板下和核下,加入1mmol/L三硝基酚使线粒体膜电位减小,荧光强度明显减弱。用DIOC6(3)染色,观察到内质网分布于表皮板下直至细胞核区域,呈网状、核下及侧膜下也有分布,胞质中则极少,探讨了蛋白激酶(PKC)在三磷酸肌醇/钙信号系统中的作用。2. 激光扫描共聚焦显微镜的荧光测钙技术在内耳毛细胞研究中的应用钙离子在细胞的生命活动中起着重要作用,它参与调节细胞功能,如肌肉收缩,细胞运动,递质合成与释放,信息传递,细胞换能等。激光扫描共聚焦显微镜的荧光测钙技术可探测到细胞内钙浓度的细微变化,当内耳毛细胞受到各种生理及病理因子刺激时,可用荧光测钙技术观察细胞内钙离子浓度的变化。为研究毛细胞的机能提供了新的手段。3. 激光扫描共聚焦显微镜在内耳毛细胞离子通道研究上的应用Issa等用膜片钳的全细胞记录法将Fluo-3已导入毛细胞,用激光扫描共聚焦显微镜观察,当毛细胞去极化时其底部侧膜上平均有18个亮点(钙内流所至),然后对同一毛细胞进行连续超薄切片电镜观察,证明这些亮点即为突触前活性区。4. 激光扫描共聚焦显微镜在嗅觉研究中的应用:Schild等用激光扫描共聚焦显微镜和钙荧光探针研究嗅觉感受器神经元的钙通道分布,以Fluo-3和Fura-red 染色后行双发射比例测量,测出其胞内游离钙呈不均匀分布,观察显示嗅觉感受器神经元的钙通道位于胞体部,与同一部位的钾通道一起构成适应性调节机制,而对树突尖端纤毛的钙依赖性换能过程无干扰。四、在肿瘤研究中的应用激光扫描共聚焦显微镜的出现,在一定程度上推动了肿瘤的研究进展。它为肿瘤细胞生物学、分子生物学、细胞通讯、细胞形态学研究、细胞的抗药物代谢、细胞膜及其受体等领域的研究,提供了有效手段。1. 定量免疫荧光测定:激光扫描共聚焦显微镜采用免疫荧光对肿瘤细胞的抗原表达、细胞结构特征、抗肿瘤药物的作用及机理等方面进行定量的观察和监测,为较理想的形态学观察方法。先采用荧光标记特异性抗原或抗体,使其与特异性抗体或抗原结合,再采用激光扫描共聚焦显微镜对其进行定性、定量和形态学分析。近年来报道较多的是P53肿瘤相关抗原等的定位、定性和定量分析。采用荧光标记某些蛋白分子,然后测定其平均荧光强度和积分荧光强度,从而对某些细胞结构蛋白分子进行定量分析。2. 细胞内离子分析激光扫描共聚焦显微镜可以准确地测定细胞内Ca2+ 、 K+ 、 Na+ 、 Mg2+ 、 pH等
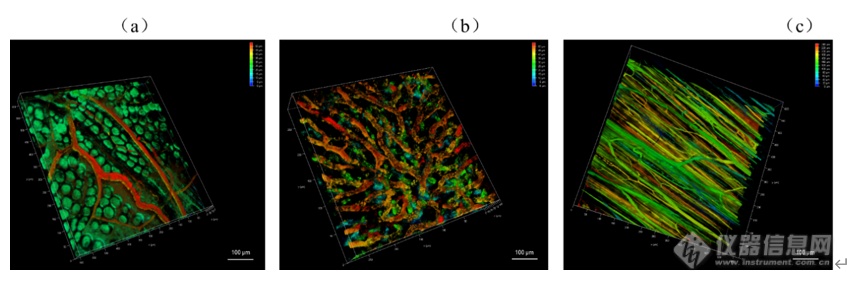
[align=center][b]双光子激光扫描显微镜的检测模式及其在生物医学领域的应用[/b][/align][align=center][font=宋体]刘皎[/font][sup]1[/sup],吴晶[sup]1[/sup][/align][align=center]1. [font=宋体]北京大学医药卫生分析中心,北京,[/font]100191[/align][b][font=黑体][[/font]摘要] [/b]双光子激光扫描显微镜(two-photon laser scan microscope, TPLSM[font=宋体])具有低光毒性、高时空分辨率、高信噪比等优点,结合了激光扫描共聚焦显微镜和双光子激发技术,广泛应用于脑科学、免疫学、肿瘤、胚胎发育等生物医学相关研究领域。本文结合作者所在的北京大学医药卫生分析中心共聚焦平台的工作经验,概述了[/font]TPLSM适用的样本、检测模式以及在生物医学领域的应用,以期为相关科研技术人员提供参考。[b][font=&][Abstract][/font] [/b]Two-photon laser scan microscopy (TPLSM) has the advantages of low phototoxicity, high spatial and temporal resolution, and high signal-to-noise ratio.TPLSM combines laser scanning confocal microscopy with two-photon excitationtechnology and it is widely used in brain science, immunology, tumor, embryodevelopment and other biomedical related research fields. Based on the author'swork experience in the confocal center of Peking University Medical and HealthAnalysis Center, this paper summarizes the applicable samples, detection modesand applications of TPLSM in the biomedical field, in order to provide referencefor related scientific researchers and technicians.[b][font=黑体][[/font]关键词] [/b]显微镜双光子,检测模式,应用[b]1 引言[/b]双光子激发技术的基本原理是在高光子密度情况下,荧光分子可同时吸收2个长波长光子,产生一个一半波长光子去激发荧光分子的相同效果。双光子激光扫描显微镜(two-photon laser scan microscope, TPLSM[font=宋体])在激光扫描共聚焦显微镜的基础上,以红外飞秒激光作为光源,长波长的近红外激光受散射影响小,易穿透标本,可深入组织内部非线性激发荧光,对细胞毒性小且具有高空间分辨率,适合生物样品的深层成像及活体样品的长时间观察成像[/font][1]。使用高能量锁模脉冲激光器,物镜焦点处的光子密度最高,在焦点平面上才有光漂白及光毒性,焦点外不损伤细胞。双光子效应只发生在焦点处,所以双光子显微镜无需共聚焦针孔,也能做到点激发点探测,提高了荧光检测效率[2]。[b][/b]双光子激光扫描显微镜显微镜可以通过XYZ,XYT,XYλ,XYZT,XYλT等多种模式实现多维成像,亦可进行更复杂实验的拍摄,比如二次谐波成像(Second Harmonic Generation Imaging,SHG[font=宋体])、双光子荧光寿命成像([/font]Two-photon Fluorescence Lifetime Imaging Microscopy, TP-FLIM[font=宋体])、荧光寿命[/font]-[font=宋体]荧光共振能量转移成像([/font]FluorescenceLifetime - Fluorescence Resonance Energy Transfer Imaging, FLIM-FRET[font=宋体])等实验以满足对样品的定性、定量、定位、共定位等多维度多功能的研究。[/font]TPLSM已成为生命科学各领域重要的研究工具,可在细胞及亚细胞水平对活体动物的神经细胞形态结构、离子浓度、细胞运动、分子相互作用等生理现象进行直接的长时间成像监测,还能进行光激活染及光损伤等光学操纵,广泛应用于脑科学、免疫学、肿瘤、胚胎发育等生物医学相关研究[3-5]。本文拟通过按TPLSM常见的检测模式分别阐述其在生物医学领域的应用,以其为相关科研技术人员提供参考。[b]2. TPLSM适用的样本[/b]TPLSM适用的样本非常广泛,从液体、固体等形式的材料或制剂、细菌、细胞、细胞团、类器官、组织切片、到各种模式动物(如线虫、果蝇、斑马鱼、小鼠、大鼠、兔、猴等)及其[font=宋体]脑、脊髓、肝脏、肺、皮肤等器官[/font],都可以通过搭载不同载物台进行测试。相对于传统激光扫描共聚焦显微镜200μm的成像深度极限,双光子显微镜成像深度可达800μm,如果是透明化样品可更厚。TPLSM尤其适合活体动物成像,且比小动物荧光成像有更高的分辨率和信噪比,一般TPLSM的XY轴分辨率为200 nm左右,Z轴分辨率为300 nm左右。[b]3. TPLSM的检测模式[/b]3.1 二维成像模式TPLSM可以实现点扫描、点探测,得到生物样品高反差、高分辨率、高灵敏度的二维图像,从而获得细胞/组织等光学切片的物理、生物化学特性及变化。也可以对所感兴趣的区域进行准确的定性、定量及定位分析。激光扫描显微镜的zoom功能,可以用来调节扫描区域的放大倍数。但受物镜分辨率的限制,一味的增大zoom值,不能得到相应的高清图像,需根据实际情况参考piexl size进行设定。TPLSM可以实现XY、XZ或XT的二维成像模式,XT线扫会在后文与XYT时间序列成像一起进行举例说明(图2b)。3.2 三维成像模式3.2.1 Z轴序列三维成像(XYZ)[align=left]TPLSM可沿Z轴方向通过电动载物台的连续扫描对样品进行无损伤的光学切片(XYZ),获得三维立体图像。同理,通过沿Y轴方向连续扫描,可获得连续的XZY图像。如图1所示TPLSM[font=宋体]可以顺利观察到可以观察到血管清晰形态结构:单个胚胎的胎盘微血管(图[/font]1a)、肝脏血窦微血管(图1b)和后肢微血管(图1c)[6]。[/align][align=center][img=,690,230]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151626576232_4807_3237657_3.png!w690x230.jpg[/img][/align][align=center]图1(a)胚胎胎盘微(b)肝脏血窦和(c)后肢的微血管三维成像[/align]3.2.2 时间序列扫描模式(XYT)[align=left]按照一定的时间间隔重复采集,则可实现对该样品的实时监测(XYT)。此类实验可观察组织区域内特异荧光探针标记的单个细胞或细胞内不同部位接受刺激后的整个变化过程。[font=宋体]如图[/font]2[font=宋体]([/font]a[font=宋体]),可以根据微血管[/font]XYT[font=宋体]序列扫描的成像结果中某一血细胞在前后两张图的位置移动和这两帧图的扫描时间间隔计算血流速度。若血流速度很快,[/font]XYT扫描不足以捕捉实际流速,可以使用XT线扫计算。如图2(b),微血管XT扫描图像中绿色荧光背景里的黑色线条代表单个血细胞的流动轨迹,每条线条的横坐标代表血细胞移动的距离(distance / μm[font=宋体]),纵坐标代表此段时间([/font]time/ ms[font=宋体]),根据这两个数据可以计算出单位时间内血细胞的流动速度([/font]μm / ms)[6]。[/align][align=center][img=,690,262]https://ng1.17img.cn/bbsfiles/images/2022/12/202212151627102569_8367_3237657_3.png!w690x262.jpg[/img] [/align][align=center]图2 微血管(a)XYT扫描结果和(b)XT一维扫描结果图像计算血流说明示意图[/align]3.2.3 光谱扫描模式(XYλ/XYΛ)通常配置有可调节接受范围的检测器的TPLSM,可以实现从400nm-800nm的发射波谱扫描。通过配置具有连续可调波长的双光子激光器,还可以实现750nm-1300nm激发波谱扫描。这对于开发研制特殊染料探针的课题来说是很方便、全面的检测功能。3.3四维成像模式(XYZT/XYλT/XYΛT)基于上述三维成像模式,结合时间序列扫描,可以实现TPLSM的四维成像。3.4二次谐波成像(SHG)SHG是一个二阶非线性过程,且一般为非共振过程,适合富含胶原纤维的样本成像,如角膜、鼠尾肌腱、皮肤等。生物组织产生的二次谐波最主要的转换源自胶原,不同生物组织中的二次谐波信号强弱与组织中的胶原含量密切相关,含胶原丰富的组织包括结缔组织和肌肉组织等二次谐波信号也比较强,另外还有一些能产生强二次谐波的生物结构是微管,如细胞分裂中纺锤体。对于具有中心对称性的生物结构,如果局部中心对称性的破坏也会产生二次谐波:在两中心对称介质的界面,不同物态分子的相互作用使局部微观场特性在交界面(如细胞膜)发生突变,从而产生界面二次谐波[7]。除了动物组织外,一些含有特殊分子结构的植物组织也能产生二次谐波。二次谐波显微成像具有高空间分辨率、深成像深度、低损伤、以及对结构对称性的高度敏感性的特点,如果能与其他成像技术结合,将成为生物样品研究的有力工具[8]。3.5双光子荧光寿命成像(TP-FLIM)[9]FLIM技术是研究细胞内生命活动状态的一种非常可靠的方法。荧光寿命是荧光团在返回基态之前处于激发态的平均时间,是荧光团的固有性质,因此其不受探针浓度、激发光强度和光漂白效应等因素影响,且能区分荧光光谱非常接近的不同荧光团,故具有非常好的特异性和很高的灵敏度。此外,由于荧光分子的荧光寿命能十分灵敏地反映激发态分子与周围微环境的相互作用及能量转移,因此FLIM技术常被用来实现对微环境中许多生化参数的定量测量,如细胞中折射率、黏度、温度、pH值的分布和动力学变化等,这在生物医学研究中具有非常重要的意义。目前FLIM技术在细胞生物学中一些重要科学问题的研究、临床医学上一些重大疾病的诊断与治疗研究以及纳米材料的生物医学应用研究等方面均有广泛应用,并取得了许多利用传统的研究手段无法获取的数据。FLIM检测需要脉冲激光,TPLSM带有的高能量锁模脉冲激光器可以满足激发要求。3.6荧光寿命-荧光共振能量转移成像(FLIM-FRET)[10]传统的FRET过程分析通常是基于荧光强度成像来实现,分析的结果容易受光谱串扰的影响。而将FLIM技术应用于FRET过程分析,利用FLIM技术可定量测量这一优势,可非常灵敏地反映供体荧光分子与受体荧光分子之间的能量转移过程。当受体分子与供体之间的距离10nm时,供体的能量转移到受体,受体从基态发生能量跃迁,从而影响供体的荧光寿命。与没有受体分子的时候相比,发生FRET的供体分子的荧光寿命降低。因此,FRET-FLIM联合能够实时监测生物细胞中蛋白质的动态变化,如蛋白质折叠、分子间(蛋白-蛋白,蛋白-核酸)相互作用和细胞间信号分子传递、分子运输以及病理学研究等。[b]4 结论和展望[/b]综上,TPLSM应用灵活,具备多种检测模式,适用于多种样本,亦可实现多种实验目的,如荧光的定量、定性、定位、共定位,动态荧光的测定等。一些特殊的实验模式,将TPLSM在生物医学领域的应用进一步扩大。通过结合其他技术(多手段联合拓展,如膜片钳、原子力显微镜、光电联用等),TPLSM必将成为助力生物医学领域研究的有力工具。双光子荧光成像由于具有天生的三维层析能力以及深穿透能力,在活体生物组织成像上广受欢迎。双光子显微镜镜下空间增大后,可广泛应用于猴、大小鼠、兔等较大的模式动物的活体成像。且可结合电生理技术、光遗传技术,广泛应用于麻醉、清醒或运行行为等生理状态下的动物脑科学神经相关研究,在单细胞、单树突精度上对神经元群体活动进行监控。如结合膜片钳技术,对活体脑组组急性切片神经元进行双光子深层成像[11];结合光遗传技术,实现视觉皮层同一神经元和神经元群体的稳定操控和长期多次重复记录[12];对在健身球上移动的头部固定小鼠小脑进行成像,探讨觉醒状态和运动行为对胶质网络中钙离子的激发的影响[13];结合多种疾病模型,探讨大脑皮层神经元及胶质细胞活性的改变及作用等[14]。随着多种双光子显微镜系统的出现,双光子显微镜成像技术将以其实时、无损地探测、诊断及检测能力,在生物医药及临床医学应用中发挥更大作用。[b]参考文献[/b][1] [font=宋体]李娟[/font],[font=宋体]张岚岚[/font],[font=宋体]吴珏珩[/font].[font=宋体]双光子显微镜的应用优势与维护要素[/font][J].[font=宋体]中国医学装备[/font],2021,18(12):158-163.[2] HendelT,Mank M, Schnell B,et al.Fluorescence changes of genetic calcium indicatorsand OGB1correlated with neural ac tivity and calcium in vivo and in vitro[J].JNeurosci, 2008,28(29):7399-7411.[3] DolginE.What leva lamps and vinaigrette can teach us about cellbiology[J].Nature,2018,555(7696):300-302.[4] Noguchi J,Nagaoka A, Watanabe S,et al.in vivo two-photon uncaging of glutamate revealingthe structure-function relatio nships of dendritic spines in the neocortex ofadult mice[J]. J Physiol,2011,589(Pt 10):2447-2457.[5] BishopD,Nikiél, Brinkoetter M,et al.Nearinfrared branding efficiently correlateslight and electron microscopy[J]. Nat Methods,2011,8(7):568-570.[6] [font=宋体]刘皎[/font],[font=宋体]丛馨[/font],[font=宋体]何其华[/font].[font=宋体]活体小鼠微血管血流倒置双光子激光扫描显微镜检测方法的建立[/font][J].解剖学报,2022,53(02):261-265.[7] [font=宋体]屈军乐[/font],[font=宋体]陈丹妮[/font],[font=宋体]杨建军[/font],[font=宋体]许改霞[/font],[font=宋体]林子扬[/font],[font=宋体]刘立新[/font],[font=宋体]牛憨笨[/font].[font=宋体]二次谐波成像及其在生物医学中的应用[/font][J].[font=宋体]深圳大学学报[/font],2006,(01):1-9.[8] [font=宋体]孙娅楠[/font],[font=宋体]赵静[/font],[font=宋体]李超华[/font],[font=宋体]等[/font].[font=宋体]二次谐波结合双光子荧光成像方法观察人源胶原蛋白透皮吸收情况[/font][J].激光生物学报,2017,26(1):24-29.[9] [font=宋体]刘雄波,林丹樱,吴茜茜,严伟,罗腾,杨志刚,屈军乐,荧光寿命显微成像技术及应用的最新研究进展。物理学报,[/font]2018,67(17):178701-1-178701-14[10] [font=宋体]罗淋淋,牛敬敬,莫蓓莘,林丹樱,刘琳,荧光共振能量转移[/font]-荧光寿命显微成像(FRET-FLIM[font=宋体])技术在生命科学研究中的应用进展。光谱学与光谱分析,[/font]2021,41(4):1023-1031[11] Isom-BatzG,Zimmem PE.Collagen injection for female urinary incontinence after urethralor periurethral surgery[J].J Unol,2009,181(2):701-704.[12] JuN,Jiang R,Mrcknik SL,et al.Long-term all-optical interrogation of corticalneurons in awake-behaving nonhuman prim ates[J].LOSBiology,2018,16(8):e2005839.[13]Nimmerjahn A,Mukamel EA, Schnitzer MJ.Motor behavior activates Bergmann glialnetworks[J].Neuron,2009,62(3):400-412.[23] Huang L, Lafaille JJ, YangG.LearningDependent dendritic spine plasticity is impaired in spontaneousautoimmune encep halomyelitis[J].Dev Neurobiol,2021,81(5):736-745.[14] Huang L,Lafaille JJ,Yang G.LearningDependent dendritic spine plasticity is impaired inspontaneous autoimmune encep halomyelitis[J].Dev Neurobiol, 2021,81(5):736-745.

提供照片出自OLYMPUS激光共聚焦扫描显微镜想了解本产品一切信息者可与本人联系:Olympus.zzq@126.com[img]http://ng1.17img.cn/bbsfiles/images/2006/06/200606021415_19451_1625155_3.jpg[/img]
[b][font='Microsoft YaHei', 宋体, sans-serif]【序号】:1[/font]【作者】:[/b][font=&][size=12px][color=#1c1d1e][b]周一览[/b][/color][/size][/font][font='Microsoft YaHei', 宋体, sans-serif][b][b][/b][/b][/font][font=&]【题名】:[/font][b][b][color=#333333][b][font=&][color=#032d2c][b]共聚焦激光扫描显微镜的研制[/b][/color][/font][/b][/color][/b][/b][font=&]【期刊】:[/font][font=Arial][font=&][size=12px]CNKI[/size][/font][/font][font='Microsoft YaHei', 宋体, sans-serif][color=#545454][b]【链接】:[url=https://link.springer.com/book/10.1007/978-0-387-45524-2]共聚焦激光扫描显微镜的研制 - 中国知网 (cnki.net)[/url][/b][/color][/font]
[b][font='Microsoft YaHei', 宋体, sans-serif]【序号】:1[/font]【作者】:[/b][font=&][size=12px][color=#1c1d1e][b][b]郑伟[/b][/b][/color][/size][/font][font='Microsoft YaHei', 宋体, sans-serif][b][b][/b][/b][/font][font=&]【题名】:[b][b]激光共焦扫描显微镜研究与软件研制[/b][/b][/font][font=&]【期刊】:[/font][font=Arial][font=&][size=12px]CNKI[/size][/font][/font][font='Microsoft YaHei', 宋体, sans-serif][color=#545454][b]【链接】:[url=https://kns.cnki.net/kcms/detail/detail.aspx?filename=1018798236.nh&dbcode=CMFD&dbname=CMFDTEMP&v=tp8D2bwk5nHWNaI8kWxjxAWIhbvBSi0KpipnvlBaa1QI0oJbPJNOQEe5HcciaOqv]激光共焦扫描显微镜研究与软件研制 - 中国知网 (cnki.net)[/url][/b][/color][/font]
激光共聚焦扫描显微镜是近代最先进的细胞生物医学分析手段之一。与传统荧光显微镜相比,共聚焦显微镜能得到更清晰的样品图像。它不仅可观察固定的细胞、组织切片,还可对活细胞的结构、分子、离子进行实时动态地观察
激光扫描共聚焦显微镜是近十年发展起来的医学图像分析仪器,与传统的光学显微镜相比,大大地提高了分辨率,能得到真正具有三维清晰度的原色图像。并可探测某些低对比度或弱荧光样品,通过目镜直接观察各种生物样品的弱自发荧光。能动态测量Ca2+ 、pH值,Na+、Mg2+等影响细胞代谢的各种生理指标,对细胞动力学研究有着重要的意义。同时激光扫描共聚显微镜可以处理活的标本,不会对标本造成物理化学特性的破坏,更接近细胞生活状态参数测定。可见激光扫描共聚焦显微镜是普遍显微镜上的质的飞跃,是电子显微镜的一个补充,现已广泛用于荧光定量测量,共焦图像分析,三维图像重建、活细胞动力学参数分析和胞间通讯研究等方面,在整个细胞生物学研究领域有着广阔的应用前景。1. 定量荧光测量ACAS可进行重复性极佳的低光探测及活细胞荧光定量分析。利用这一功能既可对单个细胞或细胞群的溶酶体,线粒体、DNA、RNA和受体分子含量、成份及分布进行定性及定量测定,还可测定诸如膜电位和配体结合等生化反应程度。此外,还适用于高灵敏度快速的免疫荧光测定,这种定量可以准确监测抗原表达,细胞结合和杀伤及定量的形态学特性,以揭示诸如肿瘤相关抗原表达的准确定位及定量信息。2. 定量共聚焦图像分析借助于ACAS激光共焦系统,可以获得生物样品高反差、高分辨率、高灵敏度的二维图像。可得到完整活的或固定的细胞及组织的系列及光切片,从而得到各层面的信息,三维重建后可以揭示亚细胞结构的空间关系。能测定细胞光学切片的物理、生物化学特性的变化,如DNA含量、RNA含量、分子扩散、胞内离子等,亦可以对这些动态变化进行准确的定性、定量、定时及定位分析。3. 三维重组分析生物结构ACAS使用SFP进行三维图像重组,SFP将各光学切片的数据组合成一个真实的三维图像,并可从任意角度观察,也可以借助改变照明角度来突出其特征,产生更生动逼真的三维效果。4. 动态荧光测定Ca2+、pH 及其它细胞内离子测定,利用ACAS能迅速对样品的点,线或二维图像扫描,测量单次、多次单色、双发射和三发射光比率,使用诸如Indo-1、BCECF 、Fluo-3等多种荧光探针对各种离子作定量分析。可以直接得到大分子的扩散速率,能定量测定细胞溶液中Ca2+对肿瘤启动因子、生长因子及各种激素等刺激的反应,以及使用双荧光探针Fluo-3和CNARF进行Ca2+和pH的同时测定。5. 荧光光漂白恢复(FRAP)——活细胞的动力学参数荧光光漂白恢复技术借助高强度脉冲式激光照射细胞某一区域,从而造成该区域荧光分子的光淬灭,该区域周围的非淬灭荧光分子将以一定速率向受照区域扩散,可通过低强度激光扫描探测此扩散速率。通过ACAS可直接测量分子扩散率、恢复速度,并由此而揭示细胞结构及相关的机制。6. 胞间通讯研究动物细胞中由缝隙连接介导的胞间通讯被认为在细胞增殖和分化中起非常重要的作用。ACAS可用于测定相邻植物和动物细胞之间细胞间通讯,测量由细胞缝隙连接介导的分子转移,研究肿瘤启动因子和生长因子对缝隙连接介导的胞间通讯的抑制作用,以及胞内Ca2+、PH和cAMP水平对缝隙连接的调节作用。7. 细胞膜流动性测定ACAS设计了专用的软件用于对细胞膜流动性进行定量和定性分析。荧光膜探针受到极化光线激发后,其发射光极性依赖于荧光分子的旋转,而这种有序的运动自由度依赖于荧光分子周围的膜流动性,因此极性测量间接反映细胞膜流动性。这种膜流动性测定在膜的磷脂酸组成分析、药物效应和作用位点,温度反应测定和物种比较等方面有重要作用。8. 笼锁-解笼锁测定许多重要的生活物质都有其笼锁化合物,在处于笼锁状态时,其功能被封闭,而一旦被特异波长的瞬间光照射后,光活化解笼锁,使其恢复原有活性和功能,在细胞的增值、分化等生物代谢过程中发挥功能。利用ACAS可以人为控制这种瞬间光的照射波长和时间,从而达到人为控制多种生物活性产物和其它化合物在生物代谢中发挥功能的时间和空间作用。9. 粘附细胞分选ACAS是目前唯一能对粘附细胞进行分离筛选的分析细胞学仪器,它对培养皿底的粘附细胞有两种分选方法: ① Coolie-CutterTM法,它是Meidian公司专利技术,首先将细胞贴壁培养在特制培养皿上,然后用高能量激光的欲选细胞四周切割成八角形几何形状,而非选择细胞则因在八角形之外而被去除,该分选方式特别适用于选择数量较少诸如突变细胞、转移细胞和杂交瘤细胞,即使百万分之一机率的也非常理想。 ② 激光消除法,该方法亦基于细胞形态及荧光特性,用高能量激光自动杀灭不需要的细胞,留下完整活细胞亚群继续培养,此方法特别适于对数量较多细胞的选择。10. 细胞激光显微外科及光陷阱技术借助ACAS可将激光当作“光子刀”使用,借此来完成诸如细胞膜瞬间穿孔、切除线粒体、溶酶体等细胞器、染色体切割、神经元突起切除等一系列细胞外科手术。通过ACAS光陷阱操作来移动细胞的微小颗粒和结构,该新技术广泛用于染色体、细胞器及细胞骨架的移动。
随着计算机技术和光电技术的飞跃发展,八十年代后期开始实际应用的激光共聚焦扫描显微镜(LSM),使人们在医学生物学上对活细胞的动态观察、细胞无损伤探测、免疫荧光标记和离子荧光探针的观察和研究上有了更加得心应手的手段和工具。随着计算机、光学显微镜、大数值孔径复消色差物镜、高分辨率分析显示、激光源、激光功率、高敏感度探测器、声光转换电子控制和各种荧光标记物的发展,使得LSM向更精、更快、多维和无损伤性分析的方向发展。
[b][font='Microsoft YaHei', 宋体, sans-serif]【序号】:1[/font]【作者】:[/b][font=&][size=12px][color=#1c1d1e][b][b]魏通达[/b][/b][/color][/size][/font][font='Microsoft YaHei', 宋体, sans-serif][b][b][/b][/b][/font][font=&]【题名】:[/font][b][b][color=#333333][b][font=&][color=#032d2c][b]共聚焦激光扫描光学显微成像关键技术研究[/b][/color][/font][/b][/color][/b][/b][font=&]【期刊】:[/font][font=Arial][font=&][size=12px]CNKI[/size][/font][/font][font='Microsoft YaHei', 宋体, sans-serif][color=#545454][b]【链接】:[url=https://link.springer.com/book/10.1007/978-0-387-45524-2]共聚焦激光扫描光学显微成像关键技术研究 - 中国知网 (cnki.net)[/url][/b][/color][/font]
扫描电镜可以改装成激光共聚焦显微镜吗?如何改装呢?谢谢

在蔡司的产品家族里面,扫描电镜SEM无疑是一颗璀璨的明珠。Zeiss扫描电镜向我们清晰的展示了万千样品的细微特征:http://ng1.17img.cn/bbsfiles/images/2016/12/201612200918_01_3005748_3.jpg而环绕在电镜周围的,则是为大家所熟知的一群“老朋友”:能谱、波谱、EBSD、阴极荧光谱仪等等。Zeiss电镜的朋友圈,随着科技的进步,向着更前沿的科研方向不断拓展延伸。在这个朋友圈中,最新闪亮登场的是WItec的激光拉曼(Raman)光谱仪。激光拉曼光谱仪在光谱仪的家族里也算是重器。对于大多数物质而言,在分子结构的分析方面,激光拉曼的作用,无可替代。http://ng1.17img.cn/bbsfiles/images/2016/12/201612200918_02_3005748_3.jpg那么扫描电镜与激光拉曼相结合,究竟能给我们带来那些新的发现呢?首先让我们领略一下Zeiss扫描电镜与激光拉曼联用系统的风采:图中主机为Zeiss Merlin扫描电镜,左侧为GatanMonoCL4阴极荧光光谱仪,中间黑色部分为激光拉曼的扫描电镜适配单元,右中下俩黑色部件:上方为激光拉曼的激光器部分(Laser source),下方为单色器(Monochromator)。http://ng1.17img.cn/bbsfiles/images/2016/12/201612200918_03_3005748_3.jpg接下来我们与您分享一下,扫描电镜与激光拉曼联用的一篇测试结果:样品为黄铁矿(Pyrite)和石英(Quartz)的伴生物。图一为Zeiss扫描电镜的样品拍摄结果: http://ng1.17img.cn/bbsfiles/images/2016/12/201612200919_01_3005748_3.jpg图一 Zeiss Merlin扫描电镜图像图二为WItec激光拉曼内置光学显微镜所拍摄的大致同一样品区域: http://ng1.17img.cn/bbsfiles/images/2016/12/201612200919_02_3005748_3.jpg图二大致同一区域的光学图像 图三为WItec激光拉曼在选定区域的图像分析结果:不同的颜色代表了不同的分子构成,给出了样品所包含的三种不同物质相的信息。http://ng1.17img.cn/bbsfiles/images/2016/12/201612200919_03_3005748_3.jpg图三 WItec激光拉曼的图像分析结果图四为WItec激光拉曼在选定区域的谱图分析结果: 红、蓝、绿三种颜色的谱图,与图像分析结果中相映的色彩区域一一对应,体现出三个不同相所包含物质成分及分子结构的信息。http://ng1.17img.cn/bbsfiles/images/2016/12/201612200919_04_3005748_3.jpg图四 WItec激光拉曼的谱图分析结果 图五为Zeiss扫描电镜与WItec激光拉曼的混合图像分析结果: http://ng1.17img.cn/bbsfiles/images/2016/12/201612200920_01_3005748_3.jpg图五 扫描电镜、激光拉曼的混合图像分析结果好了,转瞬之间我们就完成了,激光拉曼在亚微米尺度下的面扫描图像分析。这才是扫描电镜与激光拉曼联用的精华所在。扫描电镜告诉了我们:它看起来是个什么样子;而激光拉曼告诉了我们:它究竟是什么,它是如何构成的。Zeiss来自德国,WItec同样源于德国,这是科学仪器领域再完美不过的Couple了。最后,科学无国界,我们在此特别鸣谢韩国科学技术研究院,感谢KIST所提供的设备、测试结果及合作中的所有帮助。韩国科学技术研究院始建于1966年,从成立之日起,KIST就一直是带领韩国科学技术复兴和发展的领导性机构之一。致力于高新工业核心技术的研发,为韩国前沿性产业升级做出了杰出的贡献。此次购买蔡司扫描电镜激光拉曼联用系统主要用于石墨烯领域的研究。“知微行远,以科技探索世界”,欧波同将以更积极,更专业的态度,在科学仪器领域为各界工作者提供全方位的支持和帮助!

三维显微激光拉曼光谱仪三维显微激光拉曼光谱仪装置Nanofinder30 Nanofinder30 三维显微激光拉曼光谱仪装置是日本首创,世界最初的分析装置。它能在亚微米到纳米范围内,测定物质化学状态的三维图像。它由共焦激光显微镜,压电陶瓷平台(或电动扫描器)和光谱仪组成。并能自选追加原子力显微镜和近场表面增强拉曼测定的功能。 最新测量数据[ 变形Si的应力测定]PDF刊登 用二维的平面分析来评价变形Si。空间分辨率130nm, 变形率0.01%(0.1cm偏移)。 半导体/电子材料(异状物,应力,化学组成,物理结构)薄膜/保护膜(DLC,涂料,粘剂)/界面层,液晶内部构造结晶体(单壁碳纳米管,纳米晶体)光波导回路,玻璃,光学结晶等的折射率变化生物学(DNA, 蛋白质, 细胞 组织等) 以亚微米级分辨率和三维图像,能分析物质的化学结合状态空间分辨率200nm(三维共焦点模式),50nm(二维TERS模式)能同时测定光谱图像(拉曼/萤光/光致荧光PL),共焦显微镜图像,扫描探针显微镜图像(AFM/STM)和近场表面增强拉曼图像(SERS)能高速度,高灵敏度地测定样品(灵敏度:与原来之比10倍以上)不需要测定前样品处理,在空气中能进行非破坏测定全自动马达传动系统的作用,测定简单 共焦显微镜模式不能识别结晶缺陷,然而光致荧光(PL)模式却能清楚地测到结晶缺陷 共焦激光显微镜模式的形状测定 光谱窗 560 nm 用光致荧光(PL)模式测到的结晶缺陷的光谱图像(560nm的三维映像) 用AFM和共焦显微拉曼法同时测定CNT,能判定它的特性 (金属,半导体)和纯度。 同时测定单壁碳纳米管(CNT)的原子力显微镜(AFM) 形貌图像和拉曼光谱图像的例子 :拉曼光谱: 激光488nm,功率1.5mW,曝光时间2 sec,物镜100×Oil, NA=1.35, 积分时间100 sec (AFM和拉曼图像测定时) AFM形貌图像(右上)表示了单壁碳纳米管混合物的各种形状结构。图像中用数字1到8来表示其不同形状。数字1-6测得了拉曼光谱(上图所示),判定为半导体CNT。但7-8测不到拉曼光谱,所以不是半导体CNT,而可能是金属CNT(可用He-Ne激光633nm验证)。最上面表示了RBM(173cm-1), G-band(1593cm-1)及D-band(1351cm-1)的拉曼光谱图像 综合激光器和光谱分析系统的长处,坚固耐用的复合设计,卓越的仪器安定性,是纳米技术测定装置中的杰出产品。 ※日本纳米技术2004大奖“评价和测量部门”得奖. ※日本第16届中小企业优秀技术和新产品奖 “优良奖”得奖. 光学器件配置图Nanofinder30 [img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812071751_122565_1634361_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2008/12/200812071751_122566_1634361_3.jpg[/img][~122567~][~122568~]
[url=http://www.leica-microsystems.com/cn/%E4%BA%A7%E5%93%81/%E5%85%B1%E8%81%9A%E7%84%A6%E6%98%BE%E5%BE%AE%E9%95%9C/]激光共聚焦显微镜[/url]用于对样品(如贴片细胞)进行荧光成像,一般具有几条不同波长的激光作为激发光,研究人员可根据自身不同的实验需要来选择合适的激光进行荧光成像。共聚焦显微镜相对于传统的荧光显微镜具有极大的优势。首先,激光共聚焦显微镜具有极高的层切能力,可以对样品进行三维成像。与普通荧光显微镜不同,共聚焦显微镜可以对待观察样品的某一平面清晰成像,通过改变样品的垂直位置对样品的不同平面进行依次成像,还可对样品的特定平面进行实时动态成像。其次,共聚焦显微镜相对于传统的荧光显微镜具有极高的分辨率,基本达到了光学显微镜分辨率的理论极限。再次,由于激光共聚焦显微镜基于单点扫描的成像模式,因此可以在此基础上开发出其他传统荧光显微镜不能达成的技术,如荧光漂白恢复技术,荧光相关光谱技术等。共聚焦显微镜在生物学和化学领域具有极其广阔的应用,如对样品的荧光信号进行定性定量分析,对组织样品进行三维结构观察等。
用激光扫描共聚焦显微镜扫描出的图,就是只有绿黑两种颜色的图,如何用软件把它处理成表示亮度的曲线图啊,很多文献上看到了,不过不知道怎么弄,听说用matlab可以,还有人能帮帮忙,告诉我怎么样的步骤啊,matlab不会用啊谢谢,心里那个急啊,还望大家顶顶贴啊
[align=center][font='times new roman'][size=16px]激光扫描共聚焦显微镜的[/size][/font][font='times new roman'][size=16px]检测[/size][/font][font='times new roman'][size=16px]模式及其在生物医学领域的应用[/size][/font][/align][align=center][font='times new roman'][size=14px]吴晶[/size][/font][font='times new roman'][sup][size=14px]1[/size][/sup][/font][font='times new roman'][size=14px],刘皎[/size][/font][font='times new roman'][sup][size=14px]1[/size][/sup][/font][font='times new roman'][sup][size=14px], *[/size][/sup][/font][/align][align=center]1. [font='times new roman']北京大学医药卫生分析中心,北京,100191[/font][/align][font='times new roman'][/font][align=center][font='times new roman'][size=13px]* [/size][/font][font='times new roman']通讯作者[/font][/align][font='times new roman']摘要[/font][font='times new roman']由于激光扫描共聚焦显微镜(Confocal Laser Scanning Microscopy, CLSM)特有的分辨率和技术优势,使得其成为了生物学、医学及药学等领域重要的科研工具。本文结合[/font][font='times new roman']作[/font][font='times new roman']者所在的北京大学医药卫生分析中心共聚焦平台的工作经验,概述了CLSM适用的样本、[/font][font='times new roman']检测[/font][font='times new roman']模式以及在生物医学领域的应用,以期为相关科研技术人员提供参考。[/font][font='times new roman']A[/font][font='times new roman']bstract[/font][font='times new roman']Confocal Laser Scanning Microscopy (CLSM) has become an important scientific research tool in the fields of biology, medicine and pharmacy due to its unique resolution and technical advantages. Based on the author's work experience in the confocal [/font][font='times new roman']center[/font][font='times new roman'] of Peking University Medical and Health Analysis Center, this paper summarizes the applicable samples, detection modes and applications of CLSM in the biomedical field, in order to provide reference for related scientific researchers and technicians.[/font][font='times new roman']关键词[/font][font='times new roman']激光扫描共聚焦显微镜,[/font][font='times new roman']检测[/font][font='times new roman']模式,应用[/font][font='times new roman']1 引言[/font][font='times new roman']从17世纪世界上第一台原始的光学显微镜问世以来,光学显微镜在20世纪经历了快速发展时期[1]。但由于普通的光学显微镜受光波衍射效应的限制,分辨率已接近理论极限值。因此,为改善成像质量,提高图像清晰度,从而提高显微镜的成像分辨率,人们采用增加物象与背景的反差来实现此目的[2]。激光扫描共聚焦显微镜(Confocal Laser Scanning Microscopy, CLSM)的诞生,在一定程度上实现了这一目的。1984年,Bio-Rad公司首次推出世界第一台商品化的CLSM,从此CLSM迅速发展成为现代生物医学等领域科研的有力工具,广泛应用于细胞生物学、生理学、病理学、解剖学、胚胎学、免疫学和神经生物学等领域。[/font][font='times new roman']伴随着光学、计算机等技术的迅速发展,CLSM的分辨率甚至可以突破光学极限(0.2μm),达到0.05μm甚至0.02μm。与分辨率可以达到0.2nm的电子显微镜相比,CLSM的优势是既可以用于固定样品的拍摄,还可以用于活细胞实验,比如观察在特定刺激下细胞某个结构或者荧光强度的变化等。同时还可以通过XYZ[/font][font='times new roman'],[/font][font='times new roman']XYT[/font][font='times new roman'],[/font][font='times new roman']XYλ[/font][font='times new roman'],[/font][font='times new roman']XYZT[/font][font='times new roman'],[/font][font='times new roman']XYλT等多种模式实现多维成像,亦可进行更复杂实验的拍摄,比如荧光共振能量转移([/font][font='times new roman']Fluorescence Resonance Energy Transfer, [/font][font='times new roman']FRET),荧光漂白恢复([/font][font='times new roman']Fluorecence Recovery After Photobleaching, [/font][font='times new roman']FRAP),荧光寿命成像([/font][font='times new roman']Fluorescence Lifetime Imaging Microscopy, [/font][font='times new roman']FLIM)[/font][font='times new roman'],荧光相关光谱/荧光互相关光谱(Fluorescence Correlation/Co-Correlation Spectroscopy, [/font][font='times new roman']FCS[/font][font='times new roman']/FCCS)[/font][font='times new roman']等实验以满足对样品的定性、定量、定位、共定位等多维度多功能的研究。[/font][font='times new roman']本文拟通过按CLSM常见的[/font][font='times new roman']检测[/font][font='times new roman']模式分别阐述其在生物医学领域的应用,以其为相关科研技术人员提供参考。[/font]2. [font='times new roman']CLSM适用的样本[/font][font='times new roman']CLSM适用的样本非常广泛,从液体、固体等形式的材料或制剂、细菌、培养的粘附细胞、悬浮细胞、细胞团、类器官、各种染色、非染色荧光标记的组织或组织切片、到各种动物(如模式动物线虫、果蝇、斑马鱼、小鼠、大鼠等),都可以通过搭载不同载物台进行测试。所有的样品都可以通过匹配不同的器皿(包括共聚焦专用小皿、玻片、transwell小室、孔板等等)和固定器(比如不同热台、孔板支架等)放置到载物台上进行测试。[/font]3. [font='times new roman']CLSM的[/font][font='times new roman']检测[/font][font='times new roman']模式[/font]3.1 [font='times new roman']单一光切片模式(XY或XZ)[/font][font='times new roman']CLSM的最基本优势在于利用激光代替传统场光源,借助于激光扫描共聚焦显微镜的软件系统,CLSM可以实现点扫描、点探测,得到生物样品高反差、高分辨率、高灵敏度的二维图像,从而获得细胞/组织等光学切片的物理、生物化学特性及变化。也可以对所感兴趣的区域进行准确的定性、定量及定位分析。[/font][font='times new roman']CLSM特有的zoom功能,可以用来调节扫描区域的放大倍数。增加选定区域的zoom值,其图像会被放大。但zoom值会受吴晶分辨率的限制,一味的增大zoom值,不能得到相应的高清图像。因此,需根据实际情况参考piexl size进行设定。[/font]3.2 [font='times new roman']三维成像模式[/font]3.2.1 [font='times new roman']Z轴系列及三维成像模式,三维定位/图像重构[/font][font='times new roman']CLSM可对活的或固定的细胞及组织进行无损伤的系列光学切片,获得标本真正意义上的三维数据,这一功能被称为“细胞CT”:通过扫描振镜在X、Y方向的连续扫描,控制软件将扫描的像素点组成共聚焦图像,通过电动载物台沿Z轴方向的连续扫描,可获得样品不同层面连续的光切图像(xyz)。同理,通过沿Y轴方向连续扫描,可获得连续的xzy图像。再经计算机图像处理及三维重建软件,可产生生动逼真的动态效果。[/font]3.2.2 [font='times new roman']时间序列扫描模式(XYT)[/font][font='times new roman']共聚焦显微镜若按照一定的时间间隔、重复地采集样品内固定区域的荧光图像,并对其进行定位、定性及定量分析,则可实现对该样品的实时监测(XYT),此类实验可观察特异荧光探针标记的单个细胞不同部位或不同组织区域接受刺激后的整个变化过程,常用于对单个细胞内各种离子、膜电位、活性氧的比例及动态变化做实时定量分析,例如动态测定活细胞或组织内游离Ca[/font][font='times new roman'][sup][size=13px]2+[/size][/sup][/font][font='times new roman']、Mg[/font][font='times new roman'][sup][size=13px]2+[/size][/sup][/font][font='times new roman']、K[/font][font='times new roman'][sup][size=13px]+[/size][/sup][/font][font='times new roman']、Na[/font][font='times new roman'][sup][size=13px]+[/size][/sup][/font][font='times new roman']等离子的分布和浓度的变化、活细胞内H[/font][font='times new roman'][sup][size=13px]+[/size][/sup][/font][font='times new roman']浓度的变化、细胞/线粒体膜电位,自由基等。当Y方向上的扫描行数设为1时,便可进入特殊的XT模式,在这种扫描模式下得到的图像,可以用来计算血流速度等。[/font]3.2.3 [font='times new roman']光谱扫描模式(XYλ/XYΛ/XZλ)[/font][font='times new roman']通常配置有可调节接受范围的检测器[/font][font='times new roman']的CLSM[/font][font='times new roman'],可以实现从400nm-800nm的发射波谱扫描。通过配置具有连续可调波长的白激光,CLSM还可以实现激发波谱扫描。[/font][font='times new roman']3.3四维成像模式(XYZT/XYλT/XYΛT)[/font][font='times new roman']基于[/font][font='times new roman']上述[/font][font='times new roman']三维成像[/font][font='times new roman']模式[/font][font='times new roman'],结合时间序列扫描,可以实现CLSM的四维成像。[/font][font='times new roman']3.4反射光/透射光/微分干涉(DIC)成像模式[3-4][/font][font='times new roman']反射光成像主要是指光源发出的光到达样品后发生反射,检测器将此反射光信号转化为电信号进而生成样品表面的图像。利用反射光成像,能够更好的获得样品的表面纹理等信息,是对荧光图像信息的进一步补充。[/font][font='times new roman']透射光成像技术是通过光源发出的光到达样品后,透过样品的光进入检测器生成光信号,再由检测器转变为电信号所形成的图像信息。透射光成像通常能够更好的呈现目标的外轮廓信息,亦是对荧光图像信息的进一步补充。[/font][font='times new roman']很多CLSM配置有DIC模式。与其他成像技术相比,DIC成像技术通过对光路中梯度变化的呈现,实现“伪立体”效果,如在梯度比较小的区域中,相对比较扁平的上皮细胞亦可以较好的实现“立体”结构,同时,由于DIC成像技术不存在相差成像等技术中出现的光晕,还可以利用这个特点检测到细胞表面分布着的细菌,这是很多成像技术所观察不到的。因此DIC成像技术的主要优势在于不需要对相差环和聚光镜遮挡等因素进行考虑,可以直接实现高数值孔径的物镜观察,即可以提高轴向分辨率,这在对分辨率要求十分高的实验中具有重要的应用价值。[/font][font='times new roman']3.6 特殊[/font][font='times new roman']检测[/font][font='times new roman']模式[/font][font='times new roman']3.6.1 荧光漂白恢复(FRAP)[/font][font='times new roman'][5][/font][font='times new roman']FRAP技术由Axelrod等于20世纪70年代研发,指对细胞内的某一区域荧光漂白后,通过测定荧光分子的恢复速率,来研究活细胞中生物分子的动力学特征。[/font][font='times new roman']通过FRAP实验可以研究生物膜脂质分子的侧向扩散、细胞间的通讯、胞浆及细胞器内小分子物质转移性的观测、以及细胞骨架、核膜结构或大分子组装等。[/font][font='times new roman']3.6.2荧光能量共振转移(FRET)[/font][font='times new roman'][6][/font][font='times new roman']FRET是指两个荧光基团间能量通过偶极-偶极耦合作用以非辐射方式从供体传递给受体的现象。目前FRET技术可广泛用于单个固定细胞、亚细胞或活细胞原位生理环境下检测生物大分子的构象变化和分子间的直接相互作用,如检测配体-受体、蛋白分子共定位、转录机制、蛋白折叠以及蛋白质二聚化等,亦可用于检测酶活性变化、细胞凋亡以及膜蛋白的研究等。[/font][font='times new roman']在FRET体系中,常用的荧光能量供体、受体对主要有:CFP/YFP、BFP/RFP、CY3/CY5等。[/font][font='times new roman']进行FRET实验时,需要满足以下几个条件:① 所检测样品包含两个荧光分子,能量的提供者叫做供体,能量的接受者叫做受体;② 供体与受体的距离在[/font][font='times new roman']10[/font][font='times new roman']nm之间;③ 供体的发射波长与受体的激发波长一致。当供体的激发波长照射样品时,若没有FRET效应产生,只会检测到供体的发射光;反之,如果有FRET效应发生,则CLSM可检出供体发射的荧光减弱,而受体的发射光增强。[/font][font='times new roman']3.6.4 荧光寿命成像([/font][font='times new roman']FLIM[/font][font='times new roman'])[7][/font][font='times new roman']FLIM技术是研究细胞内生命活动状态的一种非常可靠的方法。荧光寿命是荧光团在返回基态之前处于激发态的平均时间,是荧光团的固有性质,因此其不受探针浓度、激发光强度和光漂白效应等因素影响,且能区分荧光光谱非常接近的不同荧光团,故具有非常好的特异性和很高的灵敏度。此外,由于荧光分子的荧光寿命能十分灵敏地反映激发态分子与周围微环境的相互作用及能量转移,因此FLIM技术常被用来实现对微环境中许多生化参数的定量测量,如细胞中折射率、黏度、温度、pH值的分布和动力学变化等,这在生物医学研究中具有非常重要的意义。目前FLIM技术在细胞生物学中一些重要科学问题的研究、临床医学上一些重大疾病的诊断与治疗研究以及纳米材料的生物医学应用研究等方面均有广泛应用,并取得了许多利用传统的研究手段无法获取的数据。[/font][font='times new roman']3.6.5 荧光共振能量转移-荧光寿命成像(FRET- [/font][font='times new roman']FLIM[/font][font='times new roman'])[8][/font][font='times new roman']FRET本身不是一种成像技术,而是一个物理过程。传统的FRET过程分析通常是基于荧光强度成像来实现,分析的结果容易受光谱串扰的影响。而将FLIM技术应用于FRET过程分析,利用FLIM技术可定量测量这一优势,可非常灵敏地反映供体荧光分子与受体荧光分子之间的能量转移过程。当受体分子与供体之间的距离10nm时,供体的能量转移到受体,受体从基态发生能量跃迁,从而影响供体的荧光寿命。与没有受体分子的时候相比,发生FRET的供体分子的荧光寿命降低。因此,FRET-FLIM联合能够实时监测生物细胞中蛋白质的动态变化,如蛋白质折叠、分子间(蛋白-蛋白,蛋白-核酸)相互作用和细胞间信号分子传递、分子运输以及病理学研究等。[/font][font='times new roman']3.6.3 荧光相关光谱/荧光互相关光谱([/font][font='times new roman']FCS[/font][font='times new roman']/FCCS)[9-12][/font][font='times new roman']FCS[/font][font='times new roman']和FCCS都是在涨落光谱技术的基础上衍生而来的,通过检测某一微小区域内荧光信号的瞬时涨落变化,分析分子的密度、扩散以及分子之间的相互作用,是一种新兴的单分子检测技术。由于FCS/FCCS的高灵敏性可以用来检测生物系统中发生的小概率时间,因此此技术主要用于分子之间相互作用、活细胞分析、核酸分析、蛋白质的寡聚化、蛋白质的动力学研究以及纳米制剂粒径测量等研究,在检测物质浓度、扩散速度、分子结合速率等方面体现出巨大的优越性,亦可用于肿瘤的早期诊断以及高通量药物筛选等。[/font][font='times new roman']FCS技术,即在CLSM焦点的微小测量区域内,通过对荧光强度随时间变化的自发性波动分析和其时间函数自相关的分析,并通过计算机统计与拟合运算,在活细胞内单分子水平给出分子的扩散系数、分子数目、分子浓度及分子之间结合与分离状态等动力学参数的检测方法。其实质是监测带有荧光基团的物质在激光作用体积内的扩散情况,可揭示异质群体中的每个个体,并对各自的亚群进行鉴定、分类、定量比较,亦可对复杂的生化反应提供详细、确定的动力学参数。[/font][font='times new roman']发明FCS的最初目的是在生物系统中研究非常稀的样本浓度的化学动力学特征。随着探测手段、自相关电子学等方面的技术进步,FCS在生物化学中的研究和应用越来越广泛,如经典的细胞膜中脂质扩散研究就是通过CLSM整合了FCS技术后所取得的巨大进展。[/font][font='times new roman']FCCS技术,确切来说是FCS技术的一种延伸应用。其既保持了FCS技术的灵敏性,又可以解决FCS对两种粒子的扩散速度要有明显不同的要求(至少相差2倍,即二者质量差相差8倍)。该技术在实验中通常将两种粒子用不同的荧光进行标记,荧光分子被激发后,产生两种互不干扰的荧光信号,分别被两个独立的检测器探测,然后将探测到的信息进行交叉函数分析。如果分子间存在相互作用,那么两种不同的荧光信号将同时经过检测通道,这时两个检测器就会产生同步的信号波动,从而产生互相关信号;而当单色荧光分子独立在微区域内运动时,则不会产生互相关信号。这样,相互作用的荧光分子和独立运动的荧光分子就被区分开来。由于FCCS技术直接反映分子间的相互作用,而不像FRET技术那样受分子扩散或聚集的影响,因此在生物分子互作、蛋白寡聚化、酶活性研究领域中有重要的应用前景。[/font][font='times new roman']4 结论和展望[/font][font='times new roman']综上,CLSM应用灵活,具备多种检测[/font][font='times new roman']模式,适用于多种样本,[/font][font='times new roman']亦可[/font][font='times new roman']实现多种实验目的,如荧光的定量、定性、定位、共定位,动态荧光的测定等[/font][font='times new roman']。一些特殊的实验模式,将CLSM在生物医学领域的应用进一步扩大。通过[/font][font='times new roman']结合其他[/font][font='times new roman']技术[/font][font='times new roman'](多手段联合拓展[/font][font='times new roman'],如膜片钳、原子力显微镜、光电联用等[/font][font='times new roman'])[/font][font='times new roman'],CLSM必将成为[/font][font='times new roman']助力生物医学领域研究[/font][font='times new roman']的有力工具[/font][font='times new roman']。[/font][font='times new roman']参考文献[/font]1. [font='times new roman']黄德娟,浅谈显微镜的发展史及其在生物学中的用途。赤峰教育学院学报,2000,2:51-52[/font]2. [font='times new roman']肖艳梅,付道林,李安生,激光扫描共聚焦显微镜(LSCM)及其生物学应用。激光生物学报,1999,8(4):305-311[/font]3. [font='times new roman']弓宇, 郭英玲, 张枫, 刘红旗, 基于反射光和透射光成像的图像识别方法比较。机电产品开发与创新,2013,26(3):7-9[/font]4. [font='times new roman']虞兆芳, DIC成像技术的优势。求知导刊,2016,2:53[/font]5. [font='times new roman']隋鑫,满奕,张越,林金星,荆艳萍,荧光漂白恢复技术及其在生物膜系统研究中的应用。电子显微学报,2017,36(6):601-609[/font]6. [font='times new roman']肖忠新,张进禄,荧光共振能量转移技术在激光共聚焦显微镜中的应用。中国医学装备,2014,8(11):73-75[/font]7. [font='times new roman']刘雄波,林丹樱,吴茜茜,严伟,罗腾,杨志刚,屈军乐,荧光寿命显微成像技术及应用的最新研究进展。物理学报,2018,67(17):178701-1-178701-14[/font]8. [font='times new roman']罗淋淋,牛敬敬,莫蓓莘,林丹樱,刘琳,荧光共振能量转移-荧光寿命显微成像(FRET-FLIM)技术在生命科学研究中的应用进展。光谱学与光谱分析,2021,41(4):1023-1031[/font]9. [font='times new roman']曲绍峰,林金星,李晓娟,FCS/FCCS技术及其在植物细胞生物学中的应用。电子显微学报,2014,33(5):461-468[/font]10. [font='times new roman']张普敦,任吉存,荧光相关光谱及其在单分子检测中的应用进展。分析化学,2005,33(6):875-880[/font]11. [font='times new roman']黄茹,周小明,荧光相关光谱在生物化学领域中的应用。激光生物学报,2013,22(4):289-293[/font]12. [font='times new roman']游俊,荧光相关光谱(FCS)在生物活细胞中的应用。湖北大学学报(自然科学版),2005,27(1):53-56[/font]
激光共聚焦显微镜系统(confocal system)的应用 1、细胞的三维重建:激光共聚焦显微镜能以0.1μm的步距沿轴向对细胞进行分层扫描,得到一组光学切片,经A/D转换后作为二维数组贮存。这些数组通过计算机进行不同的三维重建算法,可作单色或双色图像处理,组合成细胞真实的三维结构。旋转不同角度可观察各侧面的表面形态,也可从不同的断面观察细胞内部结构,测量细胞的长宽高、体积和断层面积等形态学参数。通过模拟荧光处理算法,可以产生在不同照明角度形成的阴影效果,突出立体感。通过角度旋转和细胞位置变化可产生三维动画效果。激光共聚焦显微镜的三维重建广泛用于各类细胞骨架和形态学分析、染色体分析、细胞程序化死亡的观察、细胞内细胞质和细胞器的结构变化的分析和探测等方面。 2、细胞定量荧光测定激光共聚焦显微镜以激光为光源,对细胞分层扫描,单独测定,经积分后能得到细胞荧光的准确定量,重复性极佳。它适于活细胞的定量分析,可测定细胞内溶酶体、线粒体、DNA含量、RNA含量、酶和结构性蛋白质等物质含量和分布,常用于原位分子杂交、肿瘤细胞识别、单个活细胞水平的DNA损伤及修复的定量分析。它适于快速高灵敏度测量,减少光猝灭的影响,在定量免疫荧光测定方面应用广泛,如作各种肿瘤组织切片抗原表达的定量分析,监测肿瘤相关抗原表达的定位定量信息,监测药物对肌体免疫功能的作用,监测自身免疫性疾病的多种抗原及药物对肌体免疫功能的作用,监测细胞结合和杀伤的形态特征并作定量分析等。细胞定量荧光测定可选用单荧光、双荧光方式,能自动测定细胞面积、平均荧光强度、积分荧光强度及形状因子等多种参数。 3、细胞内钙离子pH值和其它离子的动态分析通过一些专用荧光探针,可对细胞内钙离子、钠离子及pH值等作荧光标记,并对它们进行比率值和浓度梯度变化测定。由于细胞内钙离子为传递信息的第二信使,对细胞生长分化起着重要作用,通过单标记或双标记对细胞内钙离子和其它离子的荧光强度和分布精确测定,测定样品达到毫秒级的快速变化。借助光学切片功能可以测量样品深层的荧光分布以及细胞光学切片的生物化学特性的变化。通过不同时间段的检测可测定细胞内离子的扩散速率,了解它对肿瘤启动因子、生长因子等刺激的反应。细胞内离子测量广泛用于肿瘤研究、组织胚胎学、细胞生物学和药理学等领域。 4、细胞胞间通信和膜的流动性动物和植物细胞中缝隙连接介导的胞间通信在细胞增殖和分化中起着重要作用。通过测量细胞缝隙连接分子的转移,可以研究肿瘤启动因子和生长因子对缝隙连接介导的胞间通信的抑制作用及细胞内钙离子、pH值等对缝隙连接作用的影响,并监测环境毒素和药物在细胞增殖和分化中所起到的作用。选定经荧光染色后的细胞,借助于光漂白作用或光损伤作用使细胞部分或整体不发荧光,实时观察检测荧光的恢复过程,可直接反映细胞胞间通信结果。 细胞膜的流动性在进行膜的磷脂酸组成分析,药物作用点和药物作用效应,测定温度反应和物种比较方面有重要作用。细胞膜荧光探针受到极化光线激发后,发射光极性依赖于荧光分子的旋转,这种有序的运动自由度取决于荧光分子周围的膜流动性,所以极性测量能间接反映细胞膜的流动性。
[font=&]【题名】:显微系统(KEYENCE—基恩士)[/font] [font=&]【链接】: https://www.doc88.com/p-8969240676677.html?s=like&id=5[/font]

[align=center][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#373737]上世纪80年代,一台叫做[/color][/size][/font][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#78acfe][b]激光扫描共聚焦显微镜[/b][/color][/size][/font][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#373737]的仪器“横空出世”[/color][/size][/font][/align][align=center][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#373737]在随后短短三十余年的时间里[/color][/size][/font][/align][align=center][font=mp-quote, -apple-system-font, BlinkMacSystemFont, &][size=15px][color=#373737]这台仪器在生物、医学及工业检测领域得到广泛应用![/color][/size][/font][size=15px][color=#373737]有人用它观察活细胞形态结构[/color][/size][/align][align=center][size=15px][color=#373737]有人用它看到神经组织的细微病变[/color][/size][/align][align=center][size=15px][color=#373737]有人用它进行敏感精密光学部件的表面测量[/color][/size][/align][align=center][size=15px][color=#373737]最近发现[/color][/size][/align][align=center][size=15px][color=#373737]居然还有人用它进行[b]古气候纹层学研究[/b][/color][/size][size=15px][color=#373737](不明觉厉[img]https://simg.instrument.com.cn/bbs/images/brow/em17.gif[/img][/color][/size][size=15px][color=#373737]~)[/color][/size][/align][align=center][color=#78acfe][b][size=15px]慨叹用它的人脑洞之大,慨叹它如此年轻又如此多能[/size][/b][/color][/align][align=center][size=15px][color=#373737]随着新软件的不断开发及各个学科的不断发展和相互渗透,相信它还将会有更广阔的发展前景。[/color][/size][/align][align=center][size=15px][color=#373737]为了深入了解激光扫描共聚焦显微镜相关技术及市场情况,仪器信息网特组织[/color][/size][size=15px][color=#ff2941][b]“激光扫描共聚焦显微镜2019用户有奖调研”[/b][/color][/size][size=15px][color=#373737]活动。[/color][/size][/align][align=center][size=15px][color=#373737]活动截止日期:[/color][/size][color=#78acfe][b][size=15px]2019年12月15日[/size][/b][/color][/align][align=center][size=15px][color=#373737]活动对象:激光扫描共聚焦显微镜用户(或厂商专家)[/color][/size][/align][align=center][size=15px][color=#373737]参与方式:[/color][/size][size=15px]直接点击本链接或[/size][size=15px]扫[/size][size=15px]描下方二维码[/size][/align][align=center][size=15px][color=#78acfe][url=http://u0p0nhvtsktpnpd5.mikecrm.com/SkxnmHa][b]http://u0p0nhvtsktpnpd5.mikecrm.com/SkxnmHa[/b][/url][/color][/size][/align][align=center][color=#373737][img=,120,120]https://ng1.17img.cn/bbsfiles/images/2019/12/201912051626109208_2185_3471547_3.png!w690x690.jpg[/img][/color][/align][align=center][img]https://mmbiz.qpic.cn/mmbiz_gif/CTeU7IINFNTXkk1dh9NAIHZq4Zia840UJibtA1KpcSGThPiciacd0dmb2pKvBBT6j85ibMvTcrpqDKSlByD854LWYxw/640?wx_fmt=gif&tp=webp&wxfrom=5&wx_lazy=1[/img][size=15px][color=#373737]扫我扫我[/color][/size][img]https://mmbiz.qpic.cn/mmbiz_gif/CTeU7IINFNTXkk1dh9NAIHZq4Zia840UJibtA1KpcSGThPiciacd0dmb2pKvBBT6j85ibMvTcrpqDKSlByD854LWYxw/640?wx_fmt=gif&tp=webp&wxfrom=5&wx_lazy=1[/img][/align][align=center][color=#ff2941][b][size=15px]奖励方式:[/size][/b][/color][b][size=15px]第一重奖励[/size][/b][size=15px]:[/size][size=15px]活动期间,认真、如实填写完成调研问卷,即可[/size][size=15px][color=#ff2941][b]获20元[/b][/color][/size][size=15px]话费奖励。[/size][size=15px]共200份,先到先得[/size][/align][align=center][b][size=15px]第二重奖励[/size][/b][size=15px]:初步问卷有效[/size][size=15px],小编将致电进行友好愉快的电话调研,在电话调研后确定为有效问卷的情况下,将额外获得[/size][size=15px][color=#ff2941][b]50元话费[/b][/color][/size][size=15px]奖励[/size][/align][align=center][size=15px]注:[/size][size=15px]活动期间参与完成问卷,未被确认为有效问卷,但获得电话调研资格的用户,将在电话调研后确定为有效问卷的情况下,获得20元话费奖励。[/size][/align][align=center][size=15px](活动结束后统一发放)[/size][/align][align=center][size=15px]本次活动最终解释权归仪器信息网所有[/size][/align]