最近在使用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定乙醇含量,在采用外标法做标准曲线时遇到问题:相同浓度的乙醇标准样进样后得到峰面积却相差很大,我重复5次进0.2μl标准样时得到的峰面积为:8840,3904,8434,7563,14712,想请教下各位是什么原因!
想用气相色谱做乙醇气体含量,但是用什么对乙醇进行吸附比较好呢?计划的是吸附,脱附,然后直接测定,有没有大神提供个好的吸附乙醇方法?活性炭吸附可不可以?
[color=#444444]最近一直在纠结水中三氟乙醇含量的测定,听说可以用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]器,可是色谱柱,柱温气化室温度以及载气的流速我该怎么选择呢,我该根据什么选择呢,向大神求助[/color]
目的:建立一个[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件同时分离测定环孢素A中乙醇及丙二醇的含量。方法:以GDX-101为固定相,柱长为2 m,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,氮气为载气,以二甲基亚砜为溶剂,以正丙醇为内标。结果:乙醇及丙二醇进样量分别在2.0~6.0 μg,1.0~3.0 μg,其峰面积与浓度呈良好的线性关系,加样回收率分别为99.9%(RSD<0.8%,n=5),101.4%(RSD<1.1%,n=5),精密度良好。结论:此[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件可同时测定环孢素A中乙醇及丙二醇的含量,方法简便准确。关键词 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 乙醇 丙二醇 环孢素A山地明(环孢素A)为诺华制药有限公司的产品,是一种免疫抑制剂,用于器官移植和骨髓移植中的抑制排斥现象以及自身免疫疾病。厂方质量标准中乙醇及丙二醇的含量采用石英毛细管柱测定,此种色谱柱在国内使用不普及,我们经多次试验,摸索出一较好的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]条件,适用于国内检测,即以GDX-101为固定相,柱长为2 m,采用氢离子火焰检测器,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,氮气为载气,以二甲基亚砜为溶剂,以正丙醇为内标,可同时分离测定环孢素A中乙醇及丙二醇的含量,改进后的方法,乙醇与正丙醇的分离度为3.1,丙二醇与正丙醇的分离度为5.0,符合中国药典1995年版中乙醇量度检查的分离度要求[1],操作简便,结果准确可靠。1 仪器与试药 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]:SP-6890 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱:玻璃柱,长2 m,固定相为GDX-101。 乙醇、异丙醇、丙二醇均为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]纯,二甲基亚砜为色谱纯。 样品:环孢素A胶囊(山地明),由诺华公司提供,批号为187MFD0797;241MFD0797;166MFD0797;483MFD0797;477MFD0797。 标准贮备液及内标贮备液:精密称取[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]级的乙醇及丙二醇2.50及1.25 g分置50 mL容量瓶中,加二甲基亚砜至刻度,摇匀,作为标准贮备液;精密量取正丙醇5.0 mL置50 mL量瓶中,加二甲基亚砜至刻度,摇匀,作为内标贮备液。2 试验方法与结果2.1 色谱条件 采用GDX-101为固定相,柱长为2 m,氮气为载气,采用氢离子火焰检测器,进样口温度为210 ℃,检测器为280 ℃,柱温采用程序升温,即初始为165 ℃,保持12 min,以40 ℃。min-1升至280 ℃,并保持20 min,检测器温度为280 ℃,进样量为2 μL。2.2 分离度试验 称取乙醇、丙二醇及正丙醇各50 mg置同一50 mL量瓶中,加二甲基亚砜至刻度,摇匀,进样2 μL,按上述色谱条件试验,记录色谱图,见图1-A,乙醇、丙二醇及正丙醇的保留时间分别为1.15,2.22,7.54 min,计算乙醇与正丙醇及丙二醇与正丙醇的分离度,其分离度分别为3.1和5.0。图1 分离度色谱(A)及样品测定(B)色谱图1.乙醇 2.正丙醇 3.丙二醇 4.二甲基亚砜2.3 线性范围及标准曲线 分别精密量取乙醇和丙二醇标准贮备液1.0,1.5,2.0,2.5,3.0 mL,分别置50 mL量瓶中,并分别加入内标贮备液1.0 mL,使乙醇终浓度为1.0,1.5,2.0,2.5,3.0 mg.mL-1,丙二醇的终浓度为0.5,0.75,1.0,1.25,1.5 mg.mL-1,分别进样2 μL,以乙醇及丙二醇的进样量为横坐标,以它们的峰面积与内标峰面积之比为纵坐标,分别进行线性回归,结果线性关系良好,乙醇、丙二醇回归方程分别为:A=8.935×103C+7.858×102 r=0.998 8A=8.086×103C-1.649×102 r=0.999 92.4 精密度试验 用乙醇与丙二醇浓度分别2.0及1.0 mg.mL-1的溶液,重复进样5次,结果乙醇与丙二醇的RSD分别为0.7%和1.0%,精密度良好。2.5 回收率试验 采用加样回收法,取已知乙醇与丙二醇含量的样品2粒,用二甲基亚砜溶解,置50 mL量瓶中,精密加入内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,精密量取此溶液4.0,4.5,5.0,5.5,6.0 mL,分别加入乙醇与丙二醇的浓度分别为2.0 mg.mL-1及1.0 mg.mL-1的标准溶液6.0,5.5,5.0,4.5,4.0 mL,混匀,量取混匀后的溶液2 μL,注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],测定这5份溶液的乙醇和丙二醇含量,计算回收率,乙醇的平均回收率为99.9%(RSD<0.8%,n=5),丙二醇的平均回收率为101.4%(RSD<1.1%,n=5)。2.6 样品的测定 取乙醇和丙二醇标准贮备液2.0 mL,内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,作为对照品溶液;取环孢素A胶囊2粒,置50 mL量瓶中,用二甲基亚砜溶解,精密加入内标贮备液1.0 mL,并加二甲基亚砜至刻度,摇匀,作为样品溶液;分别量取对照品溶液和样品溶液各2 μL,注入[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],按上述色谱条件测定,以内标法计算含量,即得;见图1-B。2.7 对比试验结果 取环孢素A样品5批,用改进后的方法测定样品中乙醇和丙二醇的含量,与厂方测定数据相比,结果基本吻合,见表1。表1 乙醇和丙二醇对比试验结果(%) 批号 本法结果 厂方测定数据 乙醇 丙二醇 乙醇 丙二醇 187MFD0797 101.0 106.3 100.5 105.0 241MFD0797 99.2 99.2 100.6 100.6 166MFD0797 101.7 102.7 101.3 103.0 483MFD0797 98.8 96.8 99.3 97.2 477MFD0797 99.1 98.1 98.9 97.7 3 讨论3.1 本法与原厂方方法相比,方法更为简便,条件普及,有利于对样品质量的控制。3.2 原厂方标准在测定乙醇含量时,以正丁醇为溶剂,由于正丁醇的保留时间与丙二醇过于接近,分离度达不到要求,本法采用二甲基亚砜为溶剂,不影响样品的溶解,同时使丙二醇与二甲基亚砜的分离度符合定量分析的要求。3.3 曾用固定相为GDX-401的[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]柱进行检测,乙醇与正丙醇得到完全分离,但丙二醇与溶剂峰重叠,分离度达不到要求。3.4 采用程序升温,可使溶剂出峰时间加快,缩短分析时间。王俊秋(北京市药品检验所 北京 100035)庞青云(北京市药品检验所 北京 100035)余立(北京市药品检验所 北京 100035)参考文献1,中国药典.1995.二部:附录44
气相色谱法测定人体血液中乙醇含量的测量不确定度评定
[b][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定藿香正气水中的乙醇含量,Cs浓度怎么求?[/b]
最近在做柑橘皮水解发酵生产燃料乙醇实验,因为之前采用重铬酸钾分光光度计测定发酵液中乙醇含量时,由于发酵液中残留的未发酵完全的还原糖对实验结果的影响很大,导致最终结果误差太大,所以现在想采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法来测定。由于实验经费有限,实验室可用的色谱柱有:Porapak N、Porapak K、GDX-104、GDX-105、GDX-201、Chromosorb 105、Chromosorb 104。求色谱达人指点,看哪一种色谱柱可以用,本人将不胜感激!
[color=#444444]我想知道[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]如何测定回收液中乙醇和丙酮含量,我主要想用FID检测器,求各位大侠指点,如果有详细点的步骤最好了,我早上进样试了试貌似两个峰重合了。如果用内标法的话可以嘛?用什么做内标比较好,求具体过程[/color]
[color=#444444]无水乙醇的纯度在99.8%以上,可否用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]Porapak Q柱来定量检测水份含量?[/color]
[color=#444444]我最近做性能测试要测试醇水混合物以及酚水混合物各组分含量的确定,查看资料要用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定。以前没有接触过[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],假如我现在用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定乙醇与水混合物中乙醇和水的含量,应该选用哪种类型的柱子?如果我用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定苯酚和水混合物中苯酚和水的含量那应该用哪种柱子?这两种测试的柱子是不是可以通用?希望各位不吝赐教,在下感激不尽![/color]
[color=#444444]有谁做过试剂纯的乙醇中水含量的测定,我想通过[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]来标定出乙醇和水的含量,具体该怎么操作比较好啊!一般认为分析纯乙醇中水含量大约在0.23wt%左右吧。[/color]
准备增项乙醇含量的测定,消毒技术规范2002中的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,请问用什么型号的色谱柱
酒精中存乙醇含量怎样测定,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]能测吗?给一个测定方法.谢谢!!!
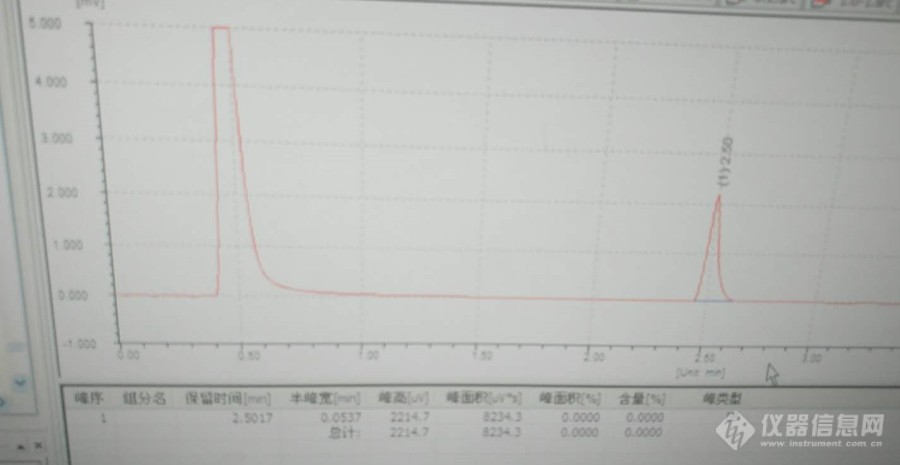
打算使用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]TCD测定发酵液中乙醇含量,最近几天在做时发现了很多问题,色谱柱:Porapak Q柱子,柱温:180℃,进样器温度180℃,载气:氩气,柱前压力0.08Mpa扫出的无水乙醇图谱如图1所示:去离子水谱图如图2所示:乙醇水溶液图谱如图3所示:现在的问题是:①水和乙醇出峰相邻,有重叠部分。而且如果乙醇水溶液中乙醇浓度很小,那么就不会出现乙醇峰,水峰会把乙醇峰给覆盖住;怎么避免这种情况出现,②峰出现拖尾,这个怎么办本人初次使用色谱,打听到本网站有很多能人,希望各位色谱达人指点,谢谢![img=,690,331]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101143506728_6036_1750127_3.png!w690x331.jpg[/img][img=,634,476]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101143533571_3070_1750127_3.png!w634x476.jpg[/img][img=,600,369]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101143557793_9866_1750127_3.png!w600x369.jpg[/img]
酒剂中甲醇乙醇含量测定,求自动进样的色谱条件、具体的温度设置
请问各位老师,请问化学试剂三乙醇胺的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法含量测定是用分流还是不分流的更好分析呢?我两种都试过,按照国标用异丙醇溶解后采取分流进样的方式,出峰很畸形,采用不分流进样也不理想,求各位大神,你们是怎样检测的呀?分享一下你们的检测条件呀!谢谢
用 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-900B (填充柱,手动进样)测定乙醇含量时候,保留时间有漂移,而且测出的乙醇含量误差较大,请教各位是怎么回事?
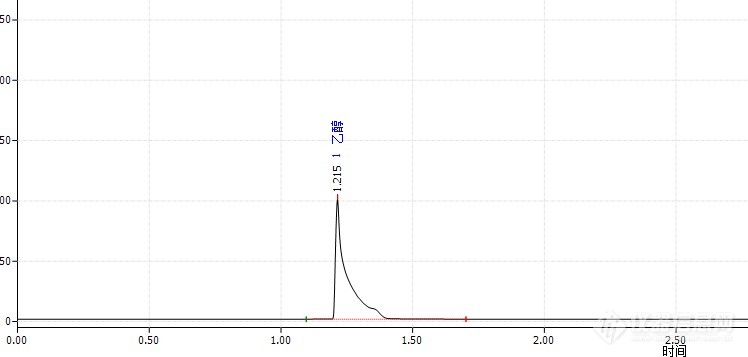
请问各位老师门,我要测75%酒精中的乙醇含量,用什么色谱柱好啊?我按照《消毒技术规范》中的方法,用纯水配制乙醇的标准曲线溶液,[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]进行分析,用过SE-30柱、WAX柱,但是拖尾严重,调大了分流比,效果依然不好。咨询了仪器工程师,工程师说用WAX的柱子,但是做出来峰型还是不好。请老师们给些建议。[img=,690,329]https://ng1.17img.cn/bbsfiles/images/2023/11/202311241526036605_3454_5105007_3.jpg!w690x329.jpg[/img]
采购的酒精,乙醇含量在95%以上(其余是水),没有气相色谱。能什么方法能快速检测?1.用酒精计可靠吗,?2.用密度瓶测密度,然后怎么换算成乙醇的含量呢,?3.其余的就不知了,
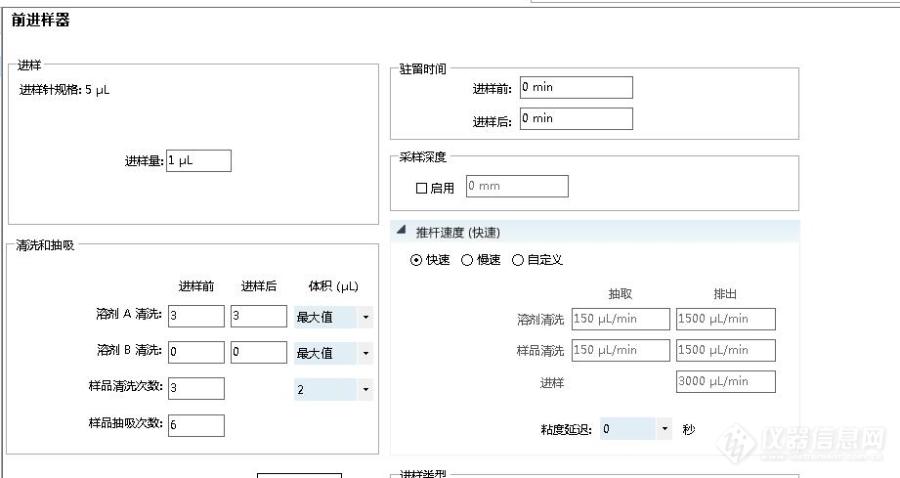
[align=center][b]水中微量甲基二乙醇胺含量测定方法研究[/b][/align][align=center]李久龙[/align][align=center](宁波中金石化有限公司,浙江,宁波,315200)[/align][b]摘要[/b]:目前分析水中甲基二乙醇胺含量的方法主要是使用电位电位滴定法或者色谱法进行测定,该方法主要是测量为百分含量的范围,是常量的测定方法;本次研究的是使用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定水中甲基二乙醇胺微量含量的检测,使用碱性专用色谱柱进行分离,氢火焰离子化检测器进行浓度测定,实现百万分之一(ppm级)微量含量的测定。[b]关键词:[/b]甲基二乙醇胺;微量;[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法甲基二乙醇胺是目前广泛应用于油田气和煤气、天然气的[url=https://baike.so.com/doc/5398730-5636161.html][color=windowtext]脱硫[/color][/url]净化、乳化剂和[url=https://baike.so.com/doc/4138139-4337808.html][color=windowtext]酸性气体[/color][/url]吸收剂、酸碱控制剂、[url=https://baike.so.com/doc/5923244-6136165.html][color=windowtext]聚氨酯泡沫[/color][/url]催化剂。我司使用甲基二乙醇胺作为脱硫剂,对含硫液化气等含硫物料进行脱硫,甲基二乙醇胺作为脱硫溶剂需要循环使用,在使用过程中需要监控甲基二乙醇胺溶液的浓度,避免浓度过低对脱硫效率产生影响,此种含量的测定方法使用的是电位滴定法进行测量。在使用过程中未避免甲基二乙醇胺泄露等情况发生,我们要监控与之接触的冷却水中甲基二乙醇胺含量,避免因甲基二乙醇胺泄露导致水质指标不合格,从而腐蚀设备。但是目前分析行业内没有一个成熟完整的方法可以准确的进行测量水中微量甲基二乙醇胺的含量。在此背景下我们摸索使用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定水中微量甲基二乙醇胺的浓度,取得了较好的效果。[b][b][color=windowtext]1 [/color][color=windowtext]行业标准SY/T 6537测定常量浓度的甲基二乙醇胺方法的介绍[/color]1.1滴定法简介[/b][/b]用盐酸标准溶液滴定,以测定溶液中的胺含量。称取一定量的样品,加入溴百里酚蓝指示液,用盐酸标准溶液滴定至试液由蓝色变为黄色,煮沸1-2min,冷却后再次滴定至黄色,计算得出胺含量浓度。[b][b]1.2色谱法简介[/b][/b]让样品气化后通过高分子多孔微球色谱柱进行分离,使用热导池检测器进行检测,用校正面积归一化法计算各组分的含量,TCD是通用型检测器,具有分析范围广的特点,但是该检测器的测量下限较高,最低能精确分析到0.01%的测量范围。[b][b]1.3方法讨论 [/b][/b]上述两种方法主要是测定常量的,不能分析微量含量的甲基二乙醇胺。滴定法的缺点在于滴定剂的浓度太低不好配置,且滴定法的终点判断、滴定速度的控制等需要经验丰富的分析工进行操作,整个分析的耗人工时长较长,不符合化工厂中控化验室的分析理念;色谱法均为分析简单、分析速度快等特点,是我们理想的分析手段。但是上述两种方法都只能分析常量范围内的甲基二乙醇胺的浓度,想要分析微量浓度的甲基二乙醇胺需要选择新的条件进行分析。[b][b][color=windowtext]2 [/color][color=windowtext]使用色谱法测定微量甲基二乙醇胺含量方法的探讨[/color]2.1检测器类型的选择[/b]首先甲基二乙醇胺属于有机物,可以在FID检测器上有响应,且FID检测器的测量下限可以准确测量到0.001%的低浓度范围,可以作为备选的一个检测器类型;第二个考虑的检测器考虑选用氮专用检测器,如NCD检测器,因为甲基二乙醇胺中用氮元素存在,所以可以使用NCD检测器进行检测,但是考虑到NCD的测量范围较小,只能测定0.1-1000ppm范围内的样品,如果我们样品中含量过大,会污染检测器,所以NCD检测器作为第二备选检测器;[b]2.2色谱柱的选择[/b]经过查找文献初步选定了三种色谱柱,分别为:CP-Sil 8 CB(30m*0.25mm*0.5um)、DB-Wax(60m*0.32mm*0.25um)、DB-1(30m*0.32*0.25um);经过分析测试,DB-1和CP-Sil 8 CB两根柱子的分离效果、响应值及基线平稳度较好,但是考虑到柱子的碱性耐受度,将CP-Sil 8 CB柱作为第一备选,DB-1柱子作为第二备选;3 实验部分[/b]仪器型号:Agilent 7890B12位自动进样器:7693A色谱柱型号:CP-Sil 8 CB For Amines 0.32mm*20m检测器条件: 检测器类型:FID 温度:300℃ 空气流量:300ml/min 氢气流量:30ml/min 氮气流量:25ml/min载气:氢气,压力 50kpa进样口:温度:270℃,分流进样,分流比:50:1柱箱:初始温度:150℃,保持:5min 升温速率:6℃/min,升到220℃,保持5min[b]3 实验部分3.1实验仪器及试剂[/b]实验仪器:Agilent 7890B;12位自动进样器:7693A,5ul自动进样针;500mg/L的甲基二乙醇胺标样,溶剂为纯水;100ml容量瓶若干、移液管若干;色谱柱型号:CP-Sil 8 CB[b]3.2试验条件[/b]检测器条件: 检测器类型:FID 温度:310℃ 空气流量:300ml/min 氢气流量:30ml/min 氮气流量:25ml/min载气:氮气,载气流速:2ml/min进样口:温度:280℃,分流进样,分流比:10:1柱箱:初始温度:100℃,保持:2min; 升温速率:5℃/min,升到220℃,保持2min; 升温速率:10℃/min,升到250℃,保持20min;3.2.1检测器设置[img=,690,432]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181638226950_5821_3389662_3.png!w690x432.jpg[/img]3.2.2自动进样器设置[img=,690,366]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181638325100_953_3389662_3.jpg!w690x366.jpg[/img]3.2.3进样口设置[img=,690,429]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181638121149_9928_3389662_3.jpg!w690x429.jpg[/img]3.2.4柱箱设置[img=,690,318]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181638435079_1244_3389662_3.jpg!w690x318.jpg[/img]3.2.5色谱柱及载气[img=,690,272]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181638571134_1565_3389662_3.jpg!w690x272.jpg[/img][b]3.3曲线的建立[/b]通过用纯水稀释500mg/L甲基二乙醇胺的标准溶液,分别得到0mg/L(纯水)、50mg/L、100mg/L、250mg/L及500mg/L的五种浓度的标准溶液。在色谱仪器上分别设置序列,每种浓度的样品做5次平行样,最终结果谱图如下: [img=,566,545]https://ng1.17img.cn/bbsfiles/images/2019/10/201910181636006532_2083_3389662_3.png!w566x545.jpg[/img]经曲线拟合,0-500mg/L的浓度范围内,线性率为0.99904,线性良好。[b]4 结果与讨论4.1 测量系统的重复性试验[/b]选取4个样品,由分三天进行测试,每个样品测量三次,测量结果如下,由分析结果来判定测量方法的重复性。[align=center]表1 重复性结果[/align] [table=549][tr][td] [align=center]样品名称[/align] [/td][td] [align=center]第一天平均结果[/align] [/td][td] [align=center]第二天平均结果[/align] [/td][td] [align=center]第三天平均结果[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]20.5[/align] [/td][td] [align=center]20.1[/align] [/td][td] [align=center]20.2[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]120.2[/align] [/td][td] [align=center]120.0[/align] [/td][td] [align=center]119.8[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]250.1[/align] [/td][td] [align=center]249.0[/align] [/td][td] [align=center]248.2[/align] [/td][/tr][tr][td] [align=center]D[/align] [/td][td] [align=center]100.5[/align] [/td][td] [align=center]99.8[/align] [/td][td] [align=center]99.4[/align] [/td][/tr][/table]由表1可知,四个样品三天测定的平均结果整天偏差均小于1%,说明本法的平行性和重复性都达到分析方法要求。[b]4.2 分析方法精度确定[/b]根据检测器的性质及分析是色谱的峰高确定,本方法测量的下限可以定为10mg/L,测量精度0.1mg/L。[b]5 实验结论[/b][color=#2B2B2B]本实验建立了采用FID检测器,使用耐碱性的色谱柱[/color]CP-Sil 8 CB,选用合适的分离条件,可以分析微量浓度的水中甲基二乙醇胺的含量。此方法填补了我们脱硫废水中微量甲基二乙醇胺含量分析的空白,可以作为我司中间控制数据出具,为生产工艺提供数据支持。[b]参考文献:[/b]黄代红,聂崇斌,马波,常宏岗,印境.SH/T 6537-2002 天然气净化厂气体及溶液分析方法,中国石油西南油气田分公司天然气研究院,2002.05.28曹磊,武杰.快速[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]实验条件优化与应用;第十五次全国色谱学术报告会文集(上册) 2005李莉萍,赵忠孝,朱正祥. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定脱碳液中MDEA和PIP含量,石油化工应用,2014.08
测定一种高粘多糖液体的乙醇含量,我们采用蒸馏法(FCC4规定);但是测定的结果总是高的离谱;规定500ppm, 我们的结果总是在2000左右。哪位高手可以解释一下。其他组分干扰,还是高温降解??采用GC-MS会不会解决?谢谢
我司客户要求提供甲基丙二酸二乙酯和丙二酸二乙酯产品中乙醇含量的具体数据,所以急需乙醇含量测定方法和参数。气相色谱条件1. 列的名称2. 列长度3. 柱内径4. 薄膜厚度5. 进样口温度(进口温度)6. 检测器温度7. 烘箱温度程序8. 载气流量9. 线速度10.分流比11.进样量顶空条件(如有需要)Thermostating时间Thermostation温度(顶空烤箱温度)循环温度(注射器,注射温度)传输线温度加压时间循环填充时间注射时间循环平衡时间矩阵沸点GC周期时间肯请各位高手不吝赐教,谢谢
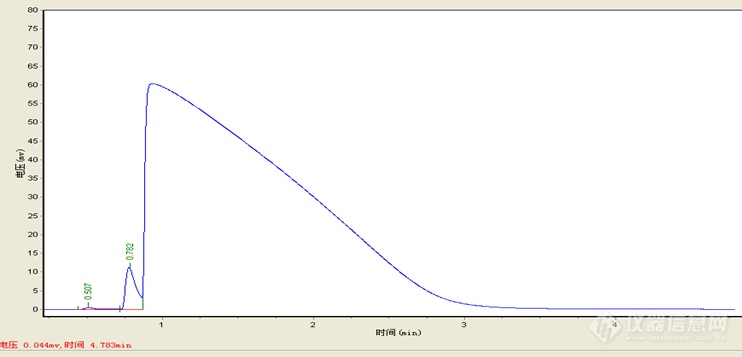
各位老师:有个问题想咨询一下大家。本单位顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url](福立9790)分析血液中乙醇含量,之前谱图一直是正常的,如下:[img=维修前空白样品谱图,第二个峰是内标叔丁醇峰,第一个峰不知道是什么峰?,690,355]http://ng1.17img.cn/bbsfiles/images/2018/05/201805041505395048_9291_3094479_3.jpg!w690x355.jpg[/img]后来因为柱温箱风机烧坏了,工程师维修之后第一个峰就时有时无,保留时间也不稳定了,问工程师,他也说不知道是什么情况[img]http://simg.instrument.com.cn/bbs/images/default/em09512.gif[/img]图如下:[img=0.5min左右的峰消失,图中第一个峰是乙醇峰,第二个是叔丁醇峰,690,352]http://ng1.17img.cn/bbsfiles/images/2018/05/201805041512328502_3862_3094479_3.jpg!w690x352.jpg[/img][img=维修前0.5min的峰跑到1min之后去了,690,381]http://ng1.17img.cn/bbsfiles/images/2018/05/201805041514177237_5181_3094479_3.jpg!w690x381.jpg[/img]
SF/XJD0107001-2010血液中乙醇的测定顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法GA/T 842-2019 《血液酒精含量的检验方法》想问下,这两个标准除了10年那个多了个单点法外,内标法上有什么区别吗?操作?仪器?含量计算?
气相色谱法测定工作场所空气中乙硫醇的含量?标准;GBT/160.49-2004 标准应进样多少才能出峰?
中药气雾剂中绿原酸含量及乙醇含量的测定概述 气雾剂系指将含药溶液或混悬液与适宜的抛射剂共同分装于具有特制阀门系统的耐压容器中,使用时借助抛射剂的压力将内容物成雾状喷出,患者主动吸入,发挥局部或全身治疗作用。 将中药做成气雾剂有效改变了中药制剂只能治疗慢性疾病的传统观点,具有剂量小、分布均匀、疗效确切、无毒副作用、使用方便等特点,患者于接受。目前,国际上气雾剂治疗急重症的药物已列入重要地位,国内临床上治疗重症的中药被列为重点研究方向,本实验将中药经提取后加工成气雾剂,喷雾后药物可直接进入肺泡,肺泡与肺泡之间有极丰富的毛细血管,并有很大的通透性,肺泡内的物质极易转移到血液中去,肺泡数目约3亿个,总面积可达50-100平方米,为物质的吸收提供了巨大的有效面积,肺部吸收速度很快,与静脉注射基本相同,并能有效的保持人体血液中的有效中药成分浓度,吸入时可减少胃肠道副作用,有速效的定位作用。试验目的 将本实验室制得的一批中药气雾剂进行质量研究,分别采用高效液相法和气相色谱法测定其中绿原酸的含量及乙醇含量实验步骤1.取出中药气雾剂,除去外包装气雾剂剩下装有药液的罐体,使用大头针钉入罐体顶部,按住后缓缓放去罐内的抛射剂(注意一定要缓慢否则容易导致药液跟着肆意喷出,影响下一步实验)。待抛射剂完全释放后,使用细口钳子将气雾剂罐顶拔出,移取其中的中药药液。如图为释放抛射剂的过程:http://ng1.17img.cn/bbsfiles/images/2013/11/201311251417_479124_2360169_3.jpg2. 绿原酸含量测定实验:供试品配制:每批样品分别移取药液1ml于100ml容量瓶中,以50%的乙醇溶液定容。以0.45微米的滤膜过滤至液相小瓶中。(如图:)http://ng1.17img.cn/bbsfiles/images/2013/11/201311251418_479125_2360169_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/11/201311251419_479127_2360169_3.jpg对照品配制:精密称定10mg绿原酸对照品(中国生物制品检定所,纯度92.5%),以50%乙醇溶液定容200ml容量瓶中,以0.45微米的滤膜过滤至液相小瓶中。(如图为称量对照品)http://ng1.17img.cn/bbsfiles/images/2013/11/201311251419_479128_2360169_3.jpg流动相配置:流动相比例为甲醇:水:冰乙酸 490:500:10 高效液相为安捷伦1100 色谱柱为菲罗门流速 1.0ml/min 柱温[color=
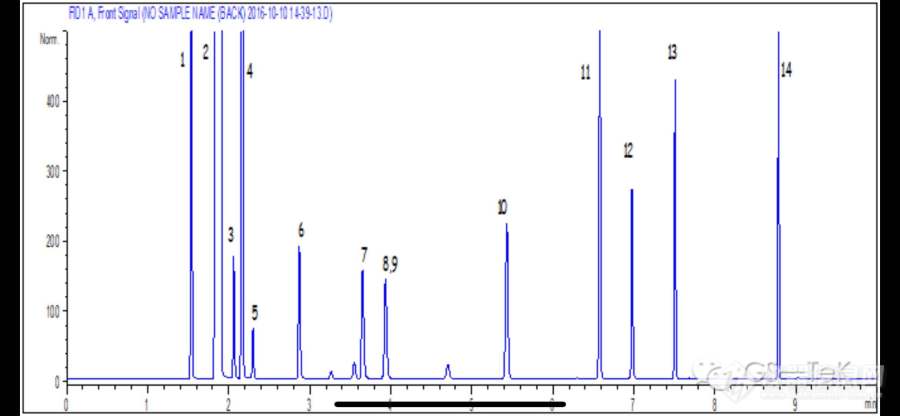
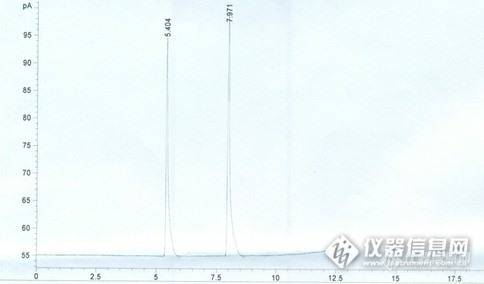
以下研究是美国[b][color=#ff0000]GS-Tek[/color][/b]公司提供。[font=SimSun][size=16px][color=#333333]变性燃料乙醇是以玉米等淀粉质原料,经发酵、蒸馏加工出乙醇,并进一步脱水,再加入适量变性剂[/color][/size][/font][font=Arial, sans-serif][size=16px][color=#333333]([/color][/size][/font][font=SimSun][size=16px][color=#333333]车用无铅汽油[/color][/size][/font][font=Arial, sans-serif][size=16px][color=#333333])[/color][/size][/font][font=SimSun][size=16px][color=#333333]变性的燃料乙醇。是由多种物质组成的,属于混合物,正是由于[/color][/size][/font][font=SimSun][size=16px]汽油是非常复杂的混合物,含有很多的低沸点的化合物可能和甲醇[/size][/font][size=16px],[/size][font=SimSun][size=16px]乙醇共同洗脱出来[/size][/font][font=SimSun][size=16px][color=#333333],[/color][/size][/font][font=SimSun][size=16px]所以常规[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱很难对甲醇和乙醇完全分离[/size][/font][font=SimSun][size=16px][color=#333333]。[/color][/size][/font][size=16px]GsBP-Bio-Ethanol[/size][font=SimSun][size=16px][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱是专门为快速、准确分析变性燃料中的甲醇和乙醇而制造生产,完全可以基线分离甲醇和乙醇以及其他的干扰物。大大缩短了分析时间,提高了实验效率而且符合[/size][/font][size=16px] ASTM D5501[/size][font=SimSun][size=16px]的要求。[/size][/font][font=SimSun]仪器[/font]:Agilent 7890 w/ FID[font=SimSun]色谱柱[/font]:[b][color=#ff0000]GsBP-Bio-Ethanol[/color] [/b] 30 mx 0.25 mm x 1.00 μm ([color=#ff0000][b]GS-Tek特殊[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱[/b][/color])[font=SimSun]货号[/font]:7625-3010-AlC3[font=SimSun]柱温[/font]:40 °C (5 min) 25 °C/min -300 °C (1min)[font=SimSun]载气[/font]:[font=SimSun]氢气[/font] 1.5 mL/min [font=SimSun]恒流模式[/font][font=SimSun]进样口[/font]:[font=SimSun]分流比[/font] 30:1 275 °C, 0.1 μL[font=SimSun]检测器[/font]:FID 325 °C[img]https://ng1.17img.cn/bbsfiles/images/2020/10/202010201049566994_5688_3276347_3.jpg!w690x318.jpg[/img][align=center][font=SimSun]图 1.[b] [/b][/font]GsBP-Bio-Ethanol[font=SimSun][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱的分析谱图[/font][/align][font=SimSun][size=16px]样品中含有汽油中的常见杂质,从图中可以看出,甲醇和乙醇与其他的潜在干扰物实现了很好的分离.[/size][/font][font=SimSun][size=15px]表1:化合物名称,保留时间和分离度的数据[/size][/font][table=648][tr][td=1,1,62][align=center][font=SimSun]序号[/font][/align][/td][td=1,1,362][align=center][font=SimSun]化合物[/font][/align][/td][td=1,1,133][align=center][font=SimSun]保留时间[/font](min)[/align][/td][td=1,1,91][align=center][font=SimSun]分离度[/font][/align][/td][/tr][tr][td=1,1,62][align=center]1[/align][/td][td=1,1,362][align=center]Methanol | [font=SimSun]甲醇[/font][/align][/td][td=1,1,133][align=center]1.536[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]2[/align][/td][td=1,1,362][align=center]Ethanol |[font=SimSun]乙醇[/font][/align][/td][td=1,1,133][align=center]1.907[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]3[/align][/td][td=1,1,362][align=center]Acetone | [font=SimSun]丙酮[/font][/align][/td][td=1,1,133][align=center]2.060[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]4[/align][/td][td=1,1,362][align=center]Isopropyl alcohol | [font=SimSun]异丙醇[/font][/align][/td][td=1,1,133][align=center]2.170[/align][/td][td=1,1,91][align=center]3.56[/align][/td][/tr][tr][td=1,1,62][align=center]5[/align][/td][td=1,1,362][align=center]Pentane | [font=SimSun]戊烷[/font][/align][/td][td=1,1,133][align=center]2.299[/align][/td][td=1,1,91][align=center]3.89[/align][/td][/tr][tr][td=1,1,62][align=center]6[/align][/td][td=1,1,362][align=center]n-Propanol | [font=SimSun]正丙醇[/font][/align][/td][td=1,1,133][align=center]2.870[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]7[/align][/td][td=1,1,362][align=center]2-Butanol | 2-[font=SimSun]丁醇[/font][/align][/td][td=1,1,133][align=center]3.651[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]8[/align][/td][td=1,1,362][align=center]Ethyl acetate | [font=SimSun]乙酸乙酯[/font][/align][/td][td=1,1,133][align=center]3.934[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]9[/align][/td][td=1,1,362][align=center]Hexane | [font=SimSun]正己烷[/font][/align][/td][td=1,1,133][align=center]3.934[/align][/td][td=1,1,91][align=center]0.00[/align][/td][/tr][tr][td=1,1,62][align=center]10[/align][/td][td=1,1,362][align=center]Benzene | [font=SimSun]苯[/font][/align][/td][td=1,1,133][align=center]5.432[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]11[/align][/td][td=1,1,362][align=center]Heptane | [font=SimSun]正庚烷[/font][/align][/td][td=1,1,133][align=center]6.579[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]12[/align][/td][td=1,1,362][align=center]Acetal | [font=SimSun]乙缩醛[/font][/align][/td][td=1,1,133][align=center]6.978[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]13[/align][/td][td=1,1,362][align=center]Toluene | [font=SimSun]甲苯[/font][/align][/td][td=1,1,133][align=center]7.509[/align][/td][td=1,1,91] [/td][/tr][tr][td=1,1,62][align=center]14[/align][/td][td=1,1,362][align=center]Xylene | [font=SimSun]二甲苯[/font][/align][/td][td=1,1,133][align=center]8.786[/align][/td][td=1,1,91] [/td][/tr][/table][size=16px] [/size][font=SimSun][size=16px]以上数据表明使用[/size][/font][size=16px]GsBP-Bio-Ethanol[/size][font=SimSun][size=16px][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱得到了良好的分辨率和峰型。对于乙酸乙酯和正己烷共同洗脱的现象,目前各个厂家仍然没有解决方案。如果样品中还有一些其他杂质,可以通过调整实验条件如柱温[/size][/font][size=16px],[/size][font=SimSun][size=16px]流速等来改善分离结果。[/size][/font][font=SimSun][size=16px][/size][/font][font=SimSun][size=16px][/size][/font]
心力丸是本所科研成果,药厂注册品种,国家中药保护品种,质量标准收载于卫生部中药成方制剂第十七册(WS3—B—3150—98)。本品具温阳益气、活血化瘀功能,用于心阳不振、气滞血瘀所致胸痹心痛、胸闷气短、心悸怔忡等证及冠心病、心绞痛。该制剂是由麝香、人参、附子、红花、人工牛黄、蟾酥等中药制成的浓缩丸,现国家规定处方中麝香以人工麝香等量替代使用,因此,人工麝香中主要有效成分麝香酮的含量[1],对控制该产品质量和保证临床用药安全有效具有重要意义。已有对六神丸等制剂中麝香酮进行测定的文献[2-5]报道。本文用[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法测定心力丸麝香酮的含量,方法简便、准确,可以有效控制该产品质量。1 仪器和试剂1.1 仪器岛津GC17A[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url],FID 检测器,N2000数据工作站(浙江智达) METTLER AE240电子分析天平 AS5150A超声波仪。1.2 试剂、试药麝香酮对照品(中国药品生物制品检定所,批号:071920006,含量测定用,质量分数99.8%) 心力丸(广东省药物研究所制药厂) 无水乙醇、乙醚等试剂均为分析纯 压缩空气、H2、N2均为高纯度的气体(广州气体厂,质量分数达99.9%以上)。2 方法与结果2.1 色谱条件毛细管柱:SPBTM1 FUSED SILICA Capillary Column(30 m×0.32 mm×1.0 μm) 柱温:200 ℃ 进样口温度:210 ℃ 检测器温度:225 ℃ 载气:N2 流速:2 mL/min 柱前压:80 kPa 空气:300 mL 氢气:30 mL 尾吹:30 mL 分流:50∶1 进样量:1 μL。在上述条件下,供试品溶液中麝香酮色谱峰能达到基线分离,供试品与邻峰的分离度大于2.0,峰形对称,人工麝香阴性供试品无干扰,方法具有专属性,按麝香酮计算理论塔板数不低于4 500。色谱图见图1-图3。图1 麝香酮对照品的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]图(M.麝香酮)(略)Figure 1 Gas chromatograms of muscone图2 心力丸供试品的[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]图(M.麝香酮)(略)Figure 2 Gas chromatograms of Xinli pills图3 人工麝香阴性[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]图(略)Figure 3 Gas chromatograms of negative sample2.2 线性关系考察精密称取麝香酮对照品0.151 94 g,置100 mL量瓶中,加无水乙醇使溶解并稀释至刻度,摇匀 再分别精密量取0.5、1、2、4、5、6、8、10 mL置10 mL量瓶中,加无水乙醇至刻度,摇匀,精密吸取1 μL进样,测定峰面积,以对照品质量浓度(ρ)为横坐标,峰面积(A)为纵坐标,求得回归方程为A=291382. 2ρ+18117.0,r=0.999 6,麝香酮线性范围为0.076~1.5 mgmL-1。2.3 供试品溶液制备取本品,研细,精密称取3.5 g,置具塞锥形瓶中,加入乙醚30 mL,密塞,冷浸12 h,滤过,残渣和具皿用少量乙醚洗涤数次,合并乙醚液,挥去乙醚,残渣加无水乙醇使溶解并定容至5 mL,摇匀,用0. 45 μm滤膜滤过,取续滤液,即得。2.4 测定方法精密吸取供试品溶液和对照品溶液1 μL,分别注入[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]中,记录色谱图,以外标法计算供试品中麝香酮含量。2.5 稳定性试验取同一供试品溶液制备后室温放置,分别在0、1、2、4、6、8、10 h进样测定,每次进样1 μL,测得麝香酮平均含量490.4 μg/g,RSD为0.29%。结果表明供试品在10 h内测定结果稳定。2.6 精密度试验取麝香酮对照品溶液(0.759 7 mg/mL)重复测定6次,测得麝香酮峰面积的RSD值为0.15%。2.7 重现性试验取同一批供试品,平行6次精密称取,按“2.3”项下方法制备供试品溶液,依“2.4”项测定,计算供试品中麝香酮含量,结果其RSD值为1.4%,表明方法重现性好。2.8 回收率试验精密称取已知含量的心力丸(麝香酮含量495. 0 μg/g)共9份,置具塞锥形瓶中 取高(1.5194 mg/mL)、中(0.759 7 mg/mL)、低(0.075 97 mg/mL)3个浓度的对照品溶液各3份,每份2 mL,置蒸发皿中,通风柜中挥干乙醇,残渣用适量乙醚溶解,移入称取有供试品的具塞锥形瓶,用乙醚洗涤具皿数次,将洗涤液并入锥形瓶,乙醚用量为30 mL,其余按“2.3”方法制备,按“2.4”方法测定,结果见表1。2.9 样品测定取本品6批,按“2.3”项下方法制备供试品溶液,按“2.4”法进行测定,结果见表2。表1 麝香酮回收率试验结果(略)Table 1 Recovery test of muscone表2 样品测定结果(略)Table 2 Assay test of samples3 讨论3.1 提取方法的选择分别考察了超声提取法和浸渍法,结果见表3。结果表明:用乙醚作溶剂的2种提取方法有偏差(相对偏差为3.1%),浸渍法提取比超声法提取损失少,或者说提取较完全 在产品含量测定时采用浸渍法提取,提取适宜时间为12 h 在生产过程中的产品质量检测则可采用超声提取方法。3.2 色谱柱的选择曾采用强极性毛细管柱(SHIMADZU CBP20睲25025)进行试验,结果麝香酮很难达基线分离,且被测组分峰有拖尾现象。表3 两种提取方法麝香酮含量测定结果(略)Table 3 Muscone contents from two batches of extractions【参考文献】[1] 唐洪梅,黄樱华,李得堂,等.[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法测定人工麝香中麝香酮的含量[J].中国实验方剂学杂志,2007,13(9):4-6.[2] 林巧玲,卓婷.[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法测定保婴散中麝香酮的含量[J].广东药学院学报, 2006,22(3):257-258.[3] 袁劲松,汤翠娥.[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法测定紫金胶囊中麝香酮含量[J].中国医院药学杂志, 2003,23(2):89-91.[4] 邹巧根,苏建俊.[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法测定麝香保心丸中麝香酮的含量[J].中国中药杂志, 1994,19(7):418-420.[5] 王强,毕开顺,陈金泉,等.六神丸中麝香酮含量的GC法测定[J].中国药科大学学报, 1995,25(6):87-89.
各位高人,乙醇中甲醇的含量测定,峰型不好,应该如何调整???我的色谱条件是,柱炉:130检测器:180进样器:180柱内流速25ml/min色谱柱:GDX-102但是峰型不好,怎么办啊[em0702]
气象色谱 用DMF作内标物,测回收乙醇里的薄荷醇含量!