《环境空气 苯系物的测定 固体吸附/热脱附-气相色谱 》 HJ 583-2010标准简介:为贯彻《中华人民共和国环境保护法》和《中华人民共和国大气污染防治法》,保护环境,保障人体健康,规范环境空气中苯系物的测定方法,制定本标准。本标准规定了测定环境空气及室内空气中苯、甲苯、乙苯、邻二甲苯。间二甲苯。对二甲苯、异丙苯和苯乙烯的固体吸附/热脱附——气相色谱法。本标准是对《空气质量 甲苯、二甲苯和苯乙烯的测定 气相色谱法》(GB/T 14677-93)的修订。本标准适用于环境环境空气及室内空气中苯、甲苯、乙苯、邻二甲苯。间二甲苯。对二甲苯、异丙苯和苯乙烯的测定。本标准也适用于常温下低浓度废气中苯系物的测定。(注:全文见资料库)
HJ 583-2010 环境空气 苯系物的测定 固体吸附热脱附-气相色谱法.pdf
在[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]中对分离起主要作用的是固定相,可分为固体固定相和液体固定相,分别对应气固色谱法和气液色谱法,前者主要用于气体和低沸点化合物的分离。固体固定相有两类,分别由无机材料(包括以其为基质用化学键合方法制备的键合固定相)和有机化合物聚合制成。固体固定相的保留和选择性取决于两个因素:①材料的化学结构(极性),即表面官能团的类型和数目,与分子间相瓦作用有关。②几何结构(孔结构和分布),也即比表面积。在使用固体固定相时,应注意三个方面:①使用前要进行活化,使用时要避免一些有反应性或腐蚀性的气体使之失活。②对组分吸附性太强时,会发生不可逆吸附。在某些情况下,在固体固定相表面上涂渍少量固定液,不仅可减少吸附,而且可改变选择性,改进特定组分的分离。③不同批次的产品色谱性能有差异(特别是无机材料制成的产品)。[b]无机吸附剂[/b]由无机材料制成的吸附剂,用于色谱法的有分子筛、硅胶、氧化铝和碳素。[b]1、分子筛[/b]分子筛是天然或人工合成的硅铝酸盐,化学组成是[M[sub]2[/sub]M']OAl[sub]2[/sub]O[sub]3[/sub]xSiO[sub]2[/sub]yH[sub]2[/sub]O,其中M为Na[sup]+[/sup]、K[sup]+[/sup]、Li[sup]+[/sup]等一价阳离子,M'是Ca[sup]2+[/sup]、Ba[sup]2+[/sup]、Sr[sup]2+[/sup]等二价阳离子,分子筛Na型与Ca型之分在于前者1/4~3/4的Na[sup]+[/sup]被Ca[sup]2+[/sup]置换:X、Y型之分是Al[sub]2[/sub]O[sub]3[/sub]与SiO[sub]2[/sub]的比例有不同,其中数字表明平均孔径的大小(单位为?,1?=0.1nm,下同)。[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]中最常用的分子筛为5A与13X型分子筛,前者由Ca-Al-Si的氧化物组成,有效孔径为5?:后者则由NA-AL-Si氧化物组成,有效孔径为10?。分子筛可能是吸附剂中极性最强的,因此CO[sub]2[/sub]、H[sub]2[/sub]O应从载气中除去。同时使用前要活化好,否则分离性能不好,柱中的水量将影响CO和CH[sub]4[/sub]的分离状况及流出次序。活化方法是在550℃活化2h(或在减压下于350℃活化2h;300℃活化4h;250℃活化12h)。分子筛因吸水而失活,在250℃通载气一夜可除去吸附水。分子筛受欢迎是由于它们分离O[sub]2[/sub]/N[sub]2[/sub]的独特能力,在通常的长度(1~2m)和正常的操作温度(室温~100℃)即可。它们也能用于分离H[sub]2[/sub]、CH[sub]4[/sub]、CO、NO和惰性气体He、Ne、Ar、Kr、Xe等。5A分子筛适于分离Ar与O[sub]2[/sub],13X分子筛则特别适于C[sub]6[/sub]~C[sub]11[/sub]烃的族分析。[b](二)硅胶[/b]硅胶由硅酸凝胶制成,化学成分是SiO[sub]2[/sub]nH[sub]2[/sub]O,分析C1~C4烷烃和SO[sub]2[/sub]、H[sub]2[/sub]S、COS、SF[sub]6[/sub]等气体硫化物。新购入的硅胶要用盐酸(1:1)浸泡2h,然后用水洗涤至无Clˉ。使用前于160℃左右活化2h。硅胶的缺点是分离性能不稳定,不同批次生产的性能不一样。硅胶曾用于分离CO[sub]2[/sub]和其他永久性气体,CO[sub]2[/sub]在C[sub]2[/sub]H[sub]6[/sub]后流出,因而在多柱系统中很有用。但是,现在这方面的应用大多数已由多孔聚合物代替。新一代硅胶基质的固定相如Spherosil和Porasil有较好的标准化的色谱性能,这些材料是多孔小球,无论是否涂固定液均可使用。Chromosil特别适于痕量硫化物的分析。[b](三)氧化铝[/b]氧化铝的化学组成是Al[sub]2[/sub]O[sub]3[/sub],其晶型有五种,[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法常用的为y型,其次为a型使用前要使用水、液体固定相或无机盐(如KCl或Na[sub]2[/sub]SO[sub]4[/sub])失活。氧化铝是轻烃分析的理想色谱柱,缺点是对极性化合物如醇、醛、酮等有很强的保留,即使在200℃,它们仍流不出来。因此,要防止高沸点化合物或极性不纯物进入柱子。即使用了KCl失活,H[sub]2[/sub]O和CO仍被Al[sub]2[/sub]O[sub]3[/sub]吸附导致保留时间减小。如果样品中水含量大于1μL/L,保留时间将减少,选择性发生变化。此时,柱子可在200℃以上活化15~30min再生柱子。第一次使用时需在450~1350℃活化2h。氧化铝具有中等吸附性,主要用于分离烃,它对不饱和烃异构体如C[sub]4[/sub]不饱和烃有独特的分离能力。经KCl改性的Al[sub]2[/sub]O[sub]3[/sub]PLOT柱稳定性大大提高,可进行C[sub]1[/sub]~C[sub]9[/sub]烃的分离分析。此外,Al[sub]2[/sub]O[sub]3[/sub]还能用于分离氢的自旋异构体。[b](四)碳素[/b]碳素的化学组成是碳,[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法使用的有活性炭、碳分子筛及石墨化炭黑。活性炭由果壳或木材烧制而成,结构为无定形碳(微晶碳),具高比表面积(800~1500m[sup]2[/sup]/g),用于分析永久性气体及C[sub]1[/sub]~C[sub]2[/sub]烃类。新购的活性炭要用等体积的苯冲洗3次,通空气吹干后,改用水蒸气于450℃活化2h,降温至150℃用空气再吹干。再生时可不用苯处理。活性炭由于宽的孔分布和组成差异,制备重复性差使得色谱性能难重复,其吸附性能强使分离的组分拖尾严重,不太适合做[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]固定相。活性炭由于其批与批之间再现性差,在色谱上使用有限。Kaiser利用聚偏二氯乙烯高温热解灼烧后得到的残留物,发展了一个类似于分子筛孔结构的碳材料,称为碳分子筛,比表面积一般在400~1200m/g。与活性炭相反,孔径分布较窄。活化方法为在180℃通氮气4h。它对分离气体和很短链化合物有用。一根单柱就能分离永久性气体和C[sub]1[/sub]~C[sub]3[/sub]烃。分离O[sub]2[/sub]、N[sub]2[/sub]、CO[sub]2[/sub]具独特能力,也能用于H[sub]2[/sub]O、SO[sub]2[/sub]、H[sub]2[/sub]S等气体的分析,特别适于分析在有机物之前流出的微量水。烃根据其不饱和程度分离,饱和烃后出峰。石墨化炭黑是炭黑在惰性气体中于2500~3000℃煅烧而成的结晶形碳,比表面积为5~260m[sup]2[/sup]/g活化方法与活性炭相同。表面几乎完全除去了不饱和键、弧电子对、自由基和离子。吸附主要由色散力引起,其大小很大程度上取决于吸附剂表面和被吸附分子间的距离。因此,石墨化炭黑尤其适合于分离几何结构和极化率上有差异的分子。如用Carbopack或F-SL可将8个C[sub]5[/sub]醇异构体分离开;用Carbograph ISC可把SF[sub]6[/sub]、SO[sub]2[/sub]、H[sub]2[/sub]S、COS、硫醇、二硫化合物很好地分离开。能使难分离化合物如间/对二甲酚、戊醇的所有八个异构体得以分离,同时对C[sub]1[/sub]~C[sub]10[/sub]范围的有机物如游离脂肪酸、醇、胺、烃等有杰出的分离能力,也能分离含硫小分子,许多在普通条件下易被吸附的痕量化合物可流出,出峰次序取决于几何结构和极化率。石墨化炭黑的缺点是机械强度较低。石墨化炭黑的吸附性能比活性炭小,最好在分析酸性物质时,用磷酸作削尾处理;分析碱性物质时,用碳酸钠处理。还可以用苦味酸、Carbowax1500、Carbowax 20ML改性。
气体样品中欲测组分的浓度往往很低,在进研色谱分析之前往往要进行富集。在直接采集欲测组分浓度很低的气体样品时,需要在现场采集体积很大的样品,回实验室进行富集,很不方便。为此研究了很多的气体样品的浓缩采集方法,主要有固体吸附法、溶液吸收法、低温浓缩(冰冻析出)法等等,下面先来介绍固体吸附法。 固体吸附法采样可有两种方式,一是将这些吸附材料制成吸附管,使用采样泵将空气样品以一己知的流量通过此吸附管,空气样品中挥发性有机污染物就被吸附管捕集浓缩,然后将吸附管加热解吸(或者通过溶剂解吸的方式,诸如二硫化碳、二氯甲烷等溶剂解吸)出这些被浓缩的挥发性有机污染物,通过色谱中的载气将它们送入色谱的分析测定系统中。此方法通常叫做吸附一热解吸(或者叫做吸附一溶剂解吸)方法。还有一种是将吸附材料制成带状的固体吸附采样器,通过扩散和渗透的方式将空气中挥发性有机污染物吸附浓缩(不是通过采样泵的动态采集方式),然后经热解吸或者溶剂解吸将浓缩的挥发性有机污染物提取出来,再送入色谱进行分析测定。此方法叫做扩散采样法或者叫做被动采样法。 固体吸附方法的核心材料是吸附剂,通常使用的吸附剂主要有活性炭、石墨化炭黑、多孔聚合物和多孔硅球等,其中活性炭和多孔聚合物在色谱分析样品制备中使用的最多。 吸附剂的物理特性参数主要有比表面积、孔径分布、极性、使用温度范围和组成结构等。人们经常根据这些参数选择合适的吸附剂并设计吸附浓缩的操作条件。 活性炭对大多数的有机物分子具有很好的吸附捕集特性,但是气体样品中的水分对活性炭的吸附干扰比较大,样品中的水分可能使活性炭采集的有机物成为不可逆吸附,并容易引起某些物质的降解,需要较高的热解吸温度(一般需要溶剂解吸)等都是它的缺点。 特别是使用活性炭采集和浓缩痕量物质时,这些缺点就更加突出,从而导致样品回收率低,也可能会伴随一些合成物质的产生。 活性炭可以制成条形或者带状的扩散型采样器,或者使用活性炭管直接扩散的方法采集空气样品(不是通过采样泵采集样品),同样可以获得较好的采集效率。活性炭管采集的样品也可以通过加热解吸的方式回收样品,同样可以得到较好的回收率。表1给出了美国 NIOSH 标准活性炭管采集湿空气中有机物的性能评价,表2给出了二硫化碳解吸活性炭管采集有机物的性能评价。[img=,690,1853]http://ng1.17img.cn/bbsfiles/images/2018/03/201803091611018433_3388_2384346_3.jpg!w690x1853.jpg[/img][img=,690,679]http://ng1.17img.cn/bbsfiles/images/2018/03/201803091611239574_4261_2384346_3.jpg!w690x679.jpg[/img] 由于石墨化炭黑具有较大的比表面积(100m[sup]2[/sup]/g),Carbotrap可以采集到许多C[sub]4[/sub]-C[sub]8[/sub]的有机化合物。而Carbotrap C(10 m[sup]2[/sup]/g)可以采集到更大的有机化合物。 Carbopack B和 c 分别与吸附材料Carbotrap和Carbotrap C 一样,只是在粒度上以60-80目取代了20-40目。石墨化炭黑可以被用来采集C[sub]4[/sub]-C[sub]10[/sub]的化合物,包括醇,游离酸,胺,酮,酚和烃类等化合物。表3给出了活性炭、石墨化炭黑和碳分子筛的物理特性参数。[img=,690,475]http://ng1.17img.cn/bbsfiles/images/2018/03/201803091612247593_5016_2384346_3.jpg!w690x475.jpg[/img] 碳分子筛被用来吸附和浓缩永久气体和较小的碳氢化合物。例如: Carbosieve S-Ⅲ特别适合于采集像C[sub]2[/sub]的烃类气体,而Carboxen 563和 564 适合于采集C[sub]2[/sub]-C[sub]5[/sub]的挥发性有机物 (Carboxen 564的吸附能力优于 Carboxen 563 ) ;Carboxen 569 具有最大的捕集有机物的能力和较低的水干扰特性。 目前,在色谱分析中最常用的多孔聚合物有Tenax , Chromosorb,Porapak,HayeSep,Amberlitresins,GDX,TDX等系列。 多孔聚合物材料采集和浓缩有机物的解吸方法常常使用热解吸的技术,热解吸的温度常在180-230℃。碳分子筛和石墨化炭黑的热稳定性较好,可使用较高的热解吸温度,在用于采集较小的和较大的有机物分子时,为了获得较好的解吸效率,常使用较高的热解吸温度:230-350℃ 。表4给出了常用多孔聚合物吸附材料(吸附痕量挥发性有机物用)的特性参数。[img=,690,1112]http://ng1.17img.cn/bbsfiles/images/2018/03/201803091612582374_9638_2384346_3.jpg!w690x1112.jpg[/img] 已有的实验和应用表明,选择合适的吸附材料是一件很难做好的事情,因为这取决于被收集样品的组成和它们的性质。虽然吸附剂对非挥发性物质具有很强的吸附性,但是它们的回收率仍然有限。另一方面,样品中挥发性物质还会通过吸附床而没有被吸附浓缩。此外,还必须避兔不重复的结果和样品被污染等现象发生。 XAD 树脂也是一种常用的吸附材料,有分析化学家采用玻璃纤维滤膜-XAD-2-活性炭串联方式进行挥发性有机物的吸附一溶剂解吸的回收率实验研究。研究结果(表5) 表明,样品湿度、采样流速或者有机滤膜颗粒物基木上不影响所研究的有机物的吸附浓度效率,此方式可应用于空气中挥发性有机污染物的采集和浓缩。[img=,690,1293]http://ng1.17img.cn/bbsfiles/images/2018/03/201803091613216123_5363_2384346_3.jpg!w690x1293.jpg[/img] 几种吸附材料的组合或者结合可以达到优点互补,可以采集到所有的目标化合物。例如: HayeSep D , Carboxen 1000和Carbosieve S-Ⅱ结合组成吸附管,在 25 ℃ 条件下,采集5L 空气样品,在 200 ℃ 热解吸可以测定出所有的目标化合物。多种吸附材料充填的采样管具有适用性,可以采集更宽范围的挥发性有机物。有报道,适中的吸附材料可保持低挥发性物质,而挥发性较大物质穿透后被捕集在较强吸附材料上。此系统避免了低挥发性物质在后级吸附材料上的不可逆吸附。Tenax TA和Carbosphere S(石墨化炭黑)结合可以采集空气中C[sub]2[/sub]-C[sub]8[/sub]碳氢和卤代烃化合物,低挥发性物质被吸附在肠Tenax TA上,挥发性较大物质被吸附在Carbosphere S(上。当只采集C[sub]2[/sub]-C[sub]8[/sub]碳氢化合物时,可以采用Tenax TA,Carbotrap,Carbosieve S-Ⅲ三种材料结合的采样管。此系统可以捕集城区空气中汽车尾气污染物和香烟雾。采用具有不同表面积的碳吸附材料(Carbotrap C,Carbotrap和Carbosieve S-Ⅲ)可以采集空气样品中非极性C[sub]4[/sub]-C[sub]14[/sub]的烃类化合物。 美国国家环保局标准分析方法(空气中有毒有机物的测定方法TO系列)中采用的吸附采样管的尺寸和材料主要有三种:玻璃采样管,13.5mm(i.d.)×100mm,内部填充约1.5g的Tenax 吸附材料:不锈钢采样管,12.7mm(i.d.)×100mm,内部填充约1.5g的Tenax吸符材料;组合式吸附剂管,分别依次填充Carbotrap C,Carbotrap和Carbosieve S-Ⅲ等吸附材料。当然,可根据自己实验室的状况和条件,自己设计和加工吸附剂采样管。吸附剂采样管的制备通常需要如下的步骤: 第一,将玻璃管或者不锈钢管放入盛有甲醇的烧杯中并超声10min后,使用新鲜甲醇冲洗这些空心管,再使用己烷超声10min,使用新鲜已烷冲洗这些空心管。然后,在 100 ℃ 条件下于真空(约8kPa )干燥箱中干燥 5h ,贮存在干燥器中备用。 第二,仔细检查空心管,特别是玻璃管,如果在空心管的端口出现损坏或者裂纹,应当将它们舍弃。 第三,使用镊子夹取石英棉将空心采样管的一端堵住并形成约10-50的石英棉塞,再用漏斗从此空心管的另一端填充吸附材料(Tenax) ,然后,夹取石英棉将空心采样 管的另一端堵住约10-50mm。石英棉和吸附材料的充填紧度要适中,不要太紧密。 第四,填充完毕的采样管使用之前,应当进行预处理。方法是:在高纯氮气或者氦气的流动下(10-30ml/min)于常温至少吹扫10min,然后升温到 250 ℃ 并保持 2-5h 。然后,采样管在高纯氮气或者氦气的流动下降到常温时,取下采样管并将管的两端密封好置于干燥器中备用。 第五,使用采样管采集样品之前,应当做一下采样管的空白实验,然后进行标准样品的采集实验。确定了样品回收率之后,将每一个采样管做好标记,说明此采样管的充填材料种类、处理日期、编号等。 通常,填充的吸附材料需要进行洗涤纯化,特别是那些比较脏的吸附剂。以Tenax 为例,首先依次使用甲醇和己烷将吸附材料进行索氏抽提 48h ,然后分别滤掉甲醇和己烷溶剂,将Tenax 转入石英盘中并置于通风厨中于常温下自然蒸发 30-60min ,再置入真空(约8kPa )干燥器中于 100 ℃ 干燥 3h 后降至常温,经过筛后备用。
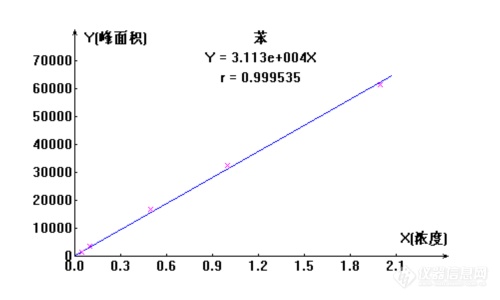
[align=center][b]挥发性有机物固体吸附热脱附[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]—质谱法[/b][/align][align=center]国联质检:高秋荣[/align]一、方法概述本方法使用无油采样器采集空气,是空气通过装有一种或者多种固体吸附剂的吸附管,然后将吸附管放入加热器中迅速加热,待分析的物质从吸附剂上被脱附后,由载气带入气象色谱的毛细柱中,经色谱分离后由质谱进行VOCs的定性定量分析。二、实验仪器1.吸附管三、试剂四、样品的采集采样时如果环境中尘,烟,气溶胶的含量很高,采样管入口端应接Tefion2-微孔过滤器或者连接一个金属管,管内塞一些干净的玻璃棉,街头使用聚四氟乙烯材料的短管。打开采样管两端的密封帽后,应马上采样,对于使用多层吸附剂的采样管,采样管气体入口段应为若吸附剂,出口端为强吸附剂。对于外径为6mm的采样管来说,最佳的采样流量为50ml/min,实际推荐采样流量为10~200ml/min,超过200ml/min或者低于10ml/min将产生较大的误差,采样所需时间应根据安全采样体积来确定,采集300ml的样品每个分析物质的检出限可达0.5ppb。对于大气环境的监测,典型的泵流量及采样时间: 1.用16ml/min的流量在1h采集960ml样品。 1.用67ml/min的流量在1h采集4020ml样品。 3.用40ml/min的流量在3h采集7200ml样品。 4.用10ml/min的流量在3h采集1800ml样品。 采集样品时,对同一批采样管需要设定两个实验室空白,既采样管老化后放在4度干净的环境中保存,在样品测定之前和样品测定之后分别测定一个实验室空白,每10个样品或一批样品低于10个样品时需要分析一个现场空白。 样品采集后,采集管应贮存在低于4度的干净环境中,在30d内分析完毕,采用多层吸附剂进行采样后,除非实现知道储存不对引起样品的明显缺失,否则应尽快进行分析。五、样品分析程序 1.标准物质的准备挥发性有机物的标准可以使用气体标准,也可以使用液体标准。(1)气体标准:使用高压管储存的气体标准,必须符合国家标准,使用国外的标准必须符合NIST/EPA认证的标准,并且样品必须在有限期内进行使用。稀释方法使用动态稀释法。(2)液体标准溶液:配置挥发性有机物的标准溶液,一般使用高纯度的甲醇为溶剂,配置液体标准时,分析物质的质量应与采样过程中进入采样管的量在同一个数量级上。(3)液体样品加到采样管的方法 将已老化的采样管作为色谱柱装到气象色谱的填充柱进样口上,调节载气的流量为100ml/min,对于挥发性低于正十二烷的物质,可以用5~10ul的微量进样器直接从为加热的进样口进样,对于挥发性高于正十二烷的物质,将进样口温度加热到50℃,以保证所有液体全部蒸发,这样后继续同载气,知道溶剂穿过吸附剂二分析的物质定量保留在吸附剂上,一般要5min,然后产下吸附管,立即盖上密封帽。如果溶剂不易从吸附剂上穿透,则应尽量减少液体的进样量,以减少溶剂对色谱的干扰。(3)热脱附进样器的操作热脱附进样器在工作之前首先核对系统是否漏气,然后根据仪器说明建立热托福条件,这些条件包括一级脱附温度,载气流速(一般在200~300℃脱附5~15min,载气流量为30~100ml/min)、二级脱附、一级脱附与二级脱附之间的分流比,二级脱附和毛细柱之间的分离比。 (4)色谱条件和质朴条件 可以根据需要选择内径0.25,0.32,0.53mm的30~50m的100%甲基聚硅氧烷毛细柱(DB-1)和5%苯基95%甲基聚硅氧烷毛细柱,所建立的色谱条件必须使本和四氯化碳达到基线分离。下面为DB-1 50m[img=,12,14]file:///C:\Users\ADMINI~1\AppData\Local\Temp\ksohtml\wps703.tmp.png[/img]0.32mm[img=,12,14]file:///C:\Users\ADMINI~1\AppData\Local\Temp\ksohtml\wps714.tmp.png[/img]1um毛细柱的色谱条件: 1.载气:99.999%的氮气,流速1~3ml/min:起始柱温30,保留时间两分钟,升温速度8℃/min,最后在200℃下所有峰出完为止。 2.质谱电子能量为70eV,质量范围为35~300amu,扫面时间每个峰至少扫面10此,每个扫描不超过1秒。 3.质谱的性能检查:通过4-溴氟苯进行核对,如果BFB调节的结果满足不了要求,必须对离子源等进行清洗和维护保养,以满足要求。 4.色谱柱条件:起始温度-50℃,保留2min,在200℃保留至所有化合物出峰完毕。六、标准曲线用标准气体向五个吸附管分别加入体积分数为10.100.1000ppb的标准,对标准液体分别加入1.0,1.0,5.0,1.0,2.0ul,在最佳条件下进行热脱附进样测定。有条件最好使用内标法,即向吸附管中加入含有甲苯-d8、全氟苯、全氟甲苯作为内标物的内标气体。[table][tr][td]管号[/td][td]1[/td][td]2[/td][td]3[/td][td]4[/td][td]5[/td][/tr][tr][td]标准(ppb)[/td][td]10[/td][td]100[/td][td]100[/td][td]1000[/td][td]1000[/td][/tr][tr][td] (ng)[/td][td]50[/td][td]100[/td][td]500[/td][td]1000[/td][td]2000[/td][/tr][/table][align=center]1.浓度为10ppm进样量5ul[/align][align=center]──────────────────────────[/align][align=center]序号 保留时间 名称 浓度 峰面积[/align][align=center]──────────────────────────[/align][align=center]1 5.053 苯 0.05 1375[/align][align=center]2 7.912 甲苯 0.05 1555[/align][align=center]3 9.427 乙酸丁酯 0.05 926[/align][align=center]4 11.318 乙苯 0.05 1610[/align][align=center]5 11.658 对间二甲苯 0.1 3230[/align][align=center]6 12.299 苯乙烯 0.05 2167[/align][align=center]7 12.488 邻二甲苯 0.05 1764[/align][align=center]8 20.626 正十一烷 0.05 1232[/align][align=center]──────────────────────────[/align][align=center]总计 0.45 13859[/align][align=center] [/align][align=center]2.浓度为100ppm 进样量 1ul[/align][align=center]──────────────────────────[/align][align=center]序号 保留时间 名称 浓度 峰面积[/align][align=center]──────────────────────────[/align][align=center]1 5.050 苯 0.1 3425[/align][align=center]2 7.914 甲苯 0.1 3348[/align][align=center]3 9.434 乙酸丁酯 0.1 1956[/align][align=center]4 11.328 乙苯 0.1 3582[/align][align=center]5 11.672 对间二甲苯 0.2 7295[/align][align=center]6 12.312 苯乙烯 0.1 3857[/align][align=center]7 12.500 邻二甲苯 0.1 4004[/align][align=center]8 20.647 正十一烷 0.1 2988[/align][align=center]──────────────────────────[/align][align=center]总计 0.9 30455[/align][align=center]3.浓度为100ppm进样量为5ul[/align][align=center]──────────────────────────[/align][align=center]序号 保留时间 名称 浓度 峰面积[/align][align=center]──────────────────────────[/align][align=center]1 5.050 苯 0.5 16483[/align][align=center]2 7.912 甲苯 0.5 17175[/align][align=center]3 9.425 乙酸丁酯 0.5 9315[/align][align=center]4 11.323 乙苯 0.5 16743[/align][align=center]5 11.672 对间二甲苯 1 34301[/align][align=center]6 12.307 苯乙烯 0.5 16697[/align][align=center]7 12.498 邻二甲苯 0.5 18471[/align][align=center]8 20.642 正十一烷 0.5 14581[/align][align=center]──────────────────────────[/align][align=center]总计 4.5 143766[/align][align=center]4.浓度为1000ppm 进样量为1ul[/align][align=center]──────────────────────────[/align][align=center]序号 保留时间 名称 浓度 峰面积[/align][align=center]──────────────────────────[/align][align=center]1 5.047 苯 1 32358[/align][align=center]2 7.905 甲苯 1 36502[/align][align=center]3 9.419 乙酸丁酯 1 21184[/align][align=center]4 11.317 乙苯 1 36881[/align][align=center]5 11.672 对间二甲苯 2 74231[/align][align=center]6 12.301 苯乙烯 1 37133[/align][align=center]7 12.491 邻二甲苯 1 40089[/align][align=center]8 20.633 正十一烷 1 27886[/align][align=center]──────────────────────────[/align][align=center]总计 9 306264[/align][align=center]5.浓度为1000ppm 进样量为2ul[/align][align=center]序号 保留时间 名称 浓度 峰面积[/align][align=center]──────────────────────────[/align][align=center]序号 保留时间 名称 浓度 峰面积[/align][align=center]──────────────────────────[/align][align=center]1 5.053 苯 2 61361[/align][align=center]2 7.920 甲苯 2 68554[/align][align=center]3 9.438 乙酸丁酯 2 39994[/align][align=center]4 11.340 乙苯 2 67930[/align][align=center]5 11.703 对间二甲苯 4 138949[/align][align=center]6 12.331 苯乙烯 2 69720[/align][align=center]7 12.523 邻二甲苯 2 74534[/align][align=center]8 20.671 正十一烷 2 52446[/align][align=center]──────────────────────────[/align][align=center]总计 18 573488[/align]校准曲线:[align=center][img=,500,300]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031106208710_507_2904018_3.png!w500x300.jpg[/img][/align][align=center][img=,452,272]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031106336666_2133_2904018_3.png!w452x272.jpg[/img][/align][align=center][img=,425,255]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031106486090_2963_2904018_3.png!w425x255.jpg[/img][/align][align=center][img=,460,276]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031108055626_8909_2904018_3.png!w460x276.jpg[/img][/align][align=center][img=,481,289]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031108216056_5338_2904018_3.png!w481x289.jpg[/img][/align][align=center][img=,500,300]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031108588186_2998_2904018_3.png!w500x300.jpg[/img][/align][align=center][img=,500,300]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031110003930_8576_2904018_3.png!w500x300.jpg[/img][/align][align=center][img=,500,300]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031109371760_1947_2904018_3.png!w500x300.jpg[/img][/align]七、样品的分析次序 对于挥发有机物GC-MS分析,样品的分析顺序为: 1.50ng 4-溴氟苯的调节仪器, 2.标准曲线,曲线个点相对的校正因子RSD[img=,14,16]file:///C:\Users\ADMINI~1\AppData\Local\Temp\ksohtml\wps74B.tmp.png[/img]25%,相对响应因子[img=,14,16]file:///C:\Users\ADMINI~1\AppData\Local\Temp\ksohtml\wps75C.tmp.png[/img]0.010. 3.空白的分析 4.样品的分析 5.中间浓度检验八、分析浓度的计算 (1)气体中化合物浓度的计算[align=center] [img=,49,41]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031111146350_1269_2904018_3.png!w49x41.jpg[/img][/align]式中:C——气体中分析物质的浓度,ug/m[sup]3[/sup][sup] [/sup]A——样品总分析物质的含量,ng Vs——标况下的采样总体积[align=center] [img=,155,44]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031111316840_1153_2904018_3.png!w155x44.jpg[/img][/align]式中:V——是及采样体积,L P——采样时的大气压,Kpa T——采样的温度,℃(2)使用内标进行定量时相对影响因子(RRF)的计算[align=center] [img=,155,44]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031111546770_5455_2904018_3.png!w155x44.jpg[/img][/align]式中:Is——目标化合物的峰面积; Cs——目标化合物的浓度,ug/ml; Iis——内标化合物的峰面积 Cis——内标化合物的浓度,ug/ml。(3)样品中分析物质浓度计算[align=center] [img=,135,48]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031112124036_2347_2904018_3.png!w135x48.jpg[/img][/align]九、精密度与准确度 对标准样品(浓度为1000±20ug/ml)进行6次测定,。结果测定如下:[align=center][img=,654,397]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031117417016_622_2904018_3.png!w654x397.jpg[/img][/align][align=center][img=,648,373]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031118069018_9576_2904018_3.png!w648x373.jpg[/img][/align][align=center][img=,659,359]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031118231506_4987_2904018_3.png!w659x359.jpg[/img][/align][align=center][img=,653,350]http://ng1.17img.cn/bbsfiles/images/2018/08/201808031118369756_5075_2904018_3.png!w653x350.jpg[/img][/align]十、总结 本方法的相对标准偏差为0.6%~1.4%,相对误差为0.3%~1.05%。满足方法的要求。通过对方法精密度和准确度的评价,本方法挥发性有机物数据准确,结果可信。 此方法的准确性好,测定结果真实可靠,可用于挥发性有机物的检测。
这是我总结的关于水中固体物质的术语和相应的测量,各位给指点下,看哪些理解有误,刚来学习,希望大家多多帮助。其中图件缺失,发在附件里了。3水中物质形态3.1 分类由于采用的标准不同,水中物质存在形态的类别有所不同。3.1.1从物质颗粒大小出发从水中物质存在的粒径大小的角度,水中物质可分为三类:1)悬浮物质:水中的悬浮物质是颗粒直径约在10-4mm(0.1μm)以上的颗粒。肉眼可见。这些微粒主要是由泥沙、沾土、原生动物、藻类、细菌、病毒、以及高分子有机物等组成,常常悬浮在水流之中,水产生的浑蚀现象,也都是由此类物质所造成。这些微粒很不稳定,可以通过沉淀和过滤而除去。水在静置的时候,重的微粒(主要是砂子和粘土一类的无机物质)会沉下来。轻的微粒(主要是动植物及其残骸的一类有机化合物)会浮于水面上,用过滤等分离方法可以除去。悬浮物是造成浊度、色度、气味的主要来源。它们在水中也不稳定,往往随着季节、地区的不同而变化。2)胶体物质:水中的胶体物质是指直径在10-4 ~10-6mm(0.001-0.1μm)之间的微粒。胶体是许多分子和离子集合物。天然水中的无机矿物质胶体主要是铁、铝和硅的化合物。水中的有机胶体物质主要是植物或动物的肢体腐烂和分解而生成的腐殖物。其中以湖泊水中的腐殖质含量最多,因此常常使水呈黄绿色或褐色。 由于胶体物质的微粒小,重量轻,单位体积所具有的表面积很大,故其表面具有较大的吸附能力,常常吸附着多量的离子而带电。同类胶体因带有同性的电荷而相互排斥,在水中不能相互粘合而处于稳定状态。所以,胶体颗粒不能藉重力自行沉降而去除,一般是在水中加入药剂破坏其稳定,使胶体颗粒增大而沉降予以去除。3)溶解物质:水的溶解物质是直径小于或等于10-6mm(0.001μm)的微小颗粒。主要是溶于水中的以低分子存在的溶解盐类的各种离子和气体。溶解物质可以用离子交换或除盐等方法予以去除。3.1.2从地球化学分析出发从水化学分析角度出发,水中物质分为两类:1)悬浮物质:粒径0.45μm的物质;2)溶解物质:粒径0.45μm的物质,包含有上一类的部分悬浮物质、全部胶体和溶解物质。即,在水化学中,0.45μm的滤膜时用来区分“dissolved”和“suspended”chemical constituents的标准。(注:微米:1μm=0.001mm。头发直径:75μm,肉眼可见最小黑点:40μm。)3.2测定项在水化学中,表示水中固体物质的指标较多,归纳起来有以下几种(参看:中華民國92 年10 月3 日環署檢字第0920072114 號公告):1)总固体重(TS):将搅拌均匀的水样在103~105℃下烘干至恒重,所得固体重量即为总固体重;2)悬浮固体重(SS):将搅拌均匀的水样以0.45μm的玻璃纤维滤片过滤,在103~105℃下将滤片烘干至恒重,所得固体重量即为悬浮固体重;3)总溶解固体重(DS):将总固体重减去悬浮固体重或将水样先经玻璃纤维滤片过滤后,其滤液在103~105℃下烘干至恒重,所得固体重量即为总溶解固体重。注意:在某些文献中,将直接测定的总溶解固体重称为溶解性固体,其重量加上重碳酸盐含量的一半(重碳酸盐在干燥时分解失去二氧化碳而转化为碳酸盐)才被认为溶解性总固体(参看:http://www.hygiene.cn.net/bzjyff/water/mwater9r.htm)。在此基础上,还可根据各固体种类的特性细分,见图2-1(此图出自何方?)。3.3取样采样时须使用抗酸性的玻璃瓶或塑料瓶,以免悬浮固体吸附于器壁上。分析前均应保存在4℃的暗处,以避免固体被微生物分解。采样后尽快检测,最长保存期限为7天。3.4测试原理总固体重、悬浮固体重和总溶解固体重的测试方法和步骤在文献中介绍较详细。主要是要注意恒重的定义,此处选择GB11901-89标准的规定,前后质量差≤0.2mg。如果考虑重碳酸盐的分解挥发,则溶解总固体的计算不能直接利用滤液烘干后前后质量的差来表示,而需将挥发跑掉的H2CO3增加进来,按下式计算(参看:饮用天然矿泉水检验方法1): ............................(1)式中: ρ──水样的溶解性总固体,mg/L;m1──蒸发皿质量,g;m2──蒸发皿和溶解性固体质量,g;V──水样体积,mL;ρ(HCO3-)──重碳酸盐的质量浓度,mg/L(必须先通过滴定求得)。当水样存在永久硬度时,构成永久硬度的钙、镁离子在蒸干时形成硫酸盐和氯化物,用105℃干燥法测定时,由于钙镁的硫酸盐所含结晶水不能去除完全,将使结果偏高;钙、镁的氯化物由于具有很强的吸湿性,对测量精度也将产生影响。向水样中预先加入适量的碳酸钠,使钙、镁离子在蒸干后形成碳酸盐,并在180℃干燥,将使上述影响得以消除(参看:http://www.hygiene.cn.net/bzjyff/water/mwater9r.htm。[em01] [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=18755]水中物质形态[/url]
[size=16px][font=arial][color=#222222]近日,中国[/color][/font][font=arial][color=#222222]科学院[/color][/font][font=arial][color=#222222]大连化学物理研究所研究员侯广进团队利用高压原位固体核磁共振(NMR)技术,揭示了部分还原氧化铈催化剂表面上非解离吸附活化双氢物种的独特化学状态。相关成果发表在《美国化学会志》上。 [/color][/font] 氢气在固体催化剂表面的吸附活化是合成氨、合成气转化、储氢等诸多能源化工过程的关键步骤,这引发了研究人员对于催化剂表面氢物种化学状态及催化功能的研究兴趣。然而,受限于表面氢物种环境敏感的特点及固体催化剂表面结构复杂性问题,对催化剂表面氢物种的实验观测存在挑战。因此,亟需发展对表面氢物种的原位、高分辨分析方法,以研究其吸附位点、电子与几何结构、与催化剂的相互作用及对催化反应的影响等重要科学问题。 固体核磁共振技术是高分辨研究催化剂表面吸附物种的重要谱学技术。然而,常规的非原位固体核磁共振方法难以研究表面氢物种在内的气氛敏感的活性物种的真实化学状态。侯广进团队前期克服技术挑战,开发出了高温高压原位固体核磁共振技术,该技术具有较宽的压力和温度操作窗口,并用于固、液、气等多相体系的原位固体核磁共振研究中,揭示了材料合成机制、气体吸附、主客体相互作用、催化反应路径及动力学等关键科学问题。 本工作中,研究人员利用高压原位固体核磁共振技术,研究了氧化铈催化剂表面氢物种的化学状态。团队通过引入HD气体,原位动态下采集二维J耦合2H-1H相关谱,发现并证明了部分还原氧化铈表面存在非解离吸附的双氢物种。团队进一步通过精准测量其J耦合常数及运动弛豫的NMR分析,确定了该双氢物种的活化吸附状态,揭示了HD分子吸附在催化剂表面,H-D键被活化拉长。随后,团队与西安交通大学常春然教授理论计算团队合作,结合不同还原程度的氧化铈吸附氢气的原位1H NMR观测及DFT计算结果,证实了该双氢物种的吸附状态,及其与氧化铈表面氧空位缺陷之间的关联。此外,研究人员借助乙烯加氢的探针反应,利用原位NMR技术观测到了该物种的催化转化过程。 该工作有助于加深对固体催化剂表面氢气吸附活化过程的认识,相关研究分析方法也有望拓展用于研究其它气体的吸附转化过程,从而指导相关催化剂和催化过程的精准设计。[/size]
在固体粉末需要回收的前提下,我想检测固体吸附的几种有机物的种类及其含量,本来我想用红外,但师兄说红外定性可以,定量不准。请问选择哪种仪器较好?固体粉末不易挥发,也难气化。
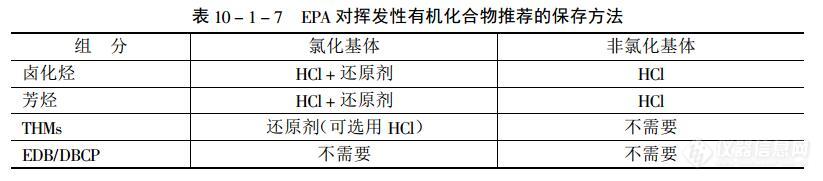
(一)液体样品的采集 液体样品主要是水样(包括环境水样、排放的废水水样及废水处理后的水样、饮用水水样、高纯水水样),饮料样品,油料样品(包括各种石油样品和植物油样品),各种溶剂样品等等,我们遇到最多的是水样。 液体样品的采集要求使用棕色的玻璃采样瓶,每次采集液体样品一定要完全充满采样瓶, 并使其刚刚溢出(根据需要采集的样品量选择采样瓶的大小),灌样品时不要产生气泡,然后使用聚四氟乙烯膜保护的瓶塞密封好采样瓶,密封好的瓶内也不要有气泡,并且在4摄氏度左右的低温箱中保存以备下一步制备色谱分析用的样品。釆集的液体样品的保存时间一般不超过5~6d。 从自来水龙头上取样时,要先打开水龙头放水,直到放出的水水温恒定后(通常需要10min)再取样。取样时调节水的流速为500ml/min,从水流中取双份样品。当从敞开的水体中取 样时,要将有代表性的样品灌到1L的大口瓶或烧杯中,然后再小心地从中取两份样品。 釆集液体样品的容器一般需要多次进行酸和碱溶液清洗,然后使用自来水和蒸馏水依次 进行冲洗,最后在烘箱中烘干备用。如果玻璃采样瓶比较脏,可先使用洗液清洗,除去容器内的脏物质后,再使用自来水和蒸馏水依次进行冲洗并在烘箱中烘干备用。 液体样品的采集也可釆用吸附剂吸附富集的方法釆集,特别是液体样品中欲测组分含量 很低时(如环境水样、废水处理后的水样、饮用水水样、高纯水水样等等)可用适当的吸附剂制成吸附柱,在采样现场让一定量的样品液体流过吸附柱,然后将吸附柱密封好,带回实验室,制备色谱分析用样品。 对于某些含有微生物的液体样品,如环境水样、废水水样、饮料样品一般都含有微生物,采集后,在现场要立即加入一些化学试剂,抑制微生物的生长,防止欲测组分被微生物的生长所破坏。① 对于含有可挥发性组分,但是不含有残留氯的水样和现场空白,可加HCl(每40ml加4 滴6mol/L HCl),以防止微生物降解和脱卤化氢。此时要注意HCl内可能含有痕量的有机溶剂,在使用前要检测一下沾污的可能性。② 对于含有残留氯的样品和现场空白在加入HCl同时还要加入还原剂。抗坏血酸(25mg/ 40ml)显然是最佳的选择,但是这一还原剂只适用于某些特殊的水样。硫代硫酸钠(3mg/40ml) 或者亚硫酸钠(3mg/40ml)也是适用的还原剂,但是加入到含HCl的水样时会生成S02,这可能 对某些填充柱的GC-MS分析造成干扰。表中给出了 EPA推荐的保存挥发性有机化合物所需加入的化学试剂。[img=,690,151]http://ng1.17img.cn/bbsfiles/images/2018/04/201804021452469430_1969_2384346_3.jpg!w690x151.jpg[/img] 所有情况都要作试剂空白,以保证没有干扰存在。在将样品瓶送到取样点之前或在采样之前就应将抗坏血酸或HCl加入。当两种保存剂都需要加时,在取样之前只加一种,以避免酸和还原剂之间的反应。然而,如果有证据可以表明酸和还原剂之间的反应不对分析或贮存产生影响时,两者就可以同时加入。 水样取好后要封紧样品瓶,此时TFE面应朝向水样。在取样后应将样品瓶颠倒几次,以便混合。收集水样后应立即将样品瓶冷却到4℃,并在此温度下放在没有有机溶剂蒸气的地方, 直到分析时取出。正常情况下,在釆样后14d内要分析全部样品。贮存时间多长合适,要根据样品的组成和基体决定,最好用数据来表明贮存时间多长最合适。③ 对于挥发性有机化合物和半挥发性有机化合物之外的其他有机化合物的水样,由于可以不考虑欲测有机污染物的挥发损失,仅考虑贮存期间的化学变化就可以了。不同类型的有机化合物可能发生的化学变化不同,其采样和贮存的方法也不尽相同,可分别酌情处理。(二)固体样品的采集 固体样品,诸如:合成树脂材料、各种食品、土壤等,一般使用玻璃样品瓶收集并密闭保存。如果能使用铝箔将上述样品瓶进行包装后贮存就更好了。收集固体样品的容器一般地都是一次性的,使用后就弃罝。 固体样品的均匀性较差,一般是取样时多取一些,然后再用缩分的方法采集所要用的样品。缩分可在采样现场进行,也可在实验室进行。原始样品的颗粒较细时,可直接进行缩分 原始样品的颗粒较粗时,需先将原始样品粉碎后进行缩分。采集固体样品时不能直接用手去拿样品,如必须用手拿样品时,要用戴了干净的白布手套 的手去拿。
红外分析中固体样品有哪些制样方法
[color=#444444][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中固定相的选择问题要求步骤尽可能详细,谢谢大家[/color][color=#444444]知道要用相似相容原理,但是不知道[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]所测的样品沸点的范围,不知道用气液气固怎么选择,不知道待测物的极性[/color]
请问一下,有没有人按HJ 734-2014 固定污染源废气 挥发性有机物的测定 固相吸附-热脱附/[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法 国标做过挥发性有机物啊
有哪位大佬有HJ 734-2014 固定污染源废气 挥发性有机物的测定 固相热脱吸附--附 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]质谱法 的编制说明吗? 求分享~~
求助标准:JG/T 5089-1997 油液中固体颗粒污染物的自动颗粒计数法谢谢!
求助:有谁知道可否用X荧光光谱在固体状态下测吸附材料中的S或N?谢谢!
采用什么方法可以分析固体(偏高岭土制成的固化体)对重金属的固化(或者吸附)作用
高效液相色谱法按组分在固定相和流动相两者间分离机理不同可分为,液固吸附色谱。液液分配色谱,化学键合相色谱法。离子交换色谱法,凝胶色谱法。我疑问的是,我们平时用的ODS-C18柱是固液吸附色谱柱吗???但是好像跟化学键合相色谱也相符合。毕竟色谱柱也是以硅胶为基质键合的C18填料柱。所以我们平时用的这个C18柱是哪一种呢?
adsorption,absorption,desorption单看这三个英文单词就知道这三种现象之前存在关联却又各不相同。吸附(sorption)描述的是吸收(absorption)和吸附(adsorption)的动作——脱附(desorption)是一种与吸附相反的动作。吸附和吸收是化学和生物学科当中一种非常重要的过程。因此当我们考虑分离方案的时候,尤其是在使用气相色谱法和液相色谱法时,我们有必要弄清楚这些过程并理解他们之间的差异。吸附和吸收的一个最主要区别在于,一个是表面处理而另一个是本体处理。吸附——发生在基质的表面。吸收——指的是一种物质进入到另一种物质的主体或者体积内部,比如说气体被液体所吸收。Adsorption吸附吸附是一种表面过程,表示气体或者液体在另外一种液体或者固体表面形成的积累现象。我们可以根据吸附质(化学物质所吸附的基质)和吸附剂分子之间的相互作用强度进一步解释何为吸附现象。物理吸附——物理吸附也称范德华吸附(Van der Waals),它是由吸附质和吸附剂分子间作用力所引起,此力也称作范德华力。化学吸附——化学吸附是吸附质分子与固体表面原子(或分子)发生电子的转移、交换或共有,形成吸附化学键的吸附。化学吸附过程所涉及的能量比物理吸附过程要多。这两种吸附作用的差异性主要体现在分子之间相互作用所产生的结合能大小的差异。Absorption吸收吸收是涉及固体、液体或气体的整体性质的现象。吸收所描述的是原子或者分子经由材料表面进入到材料体内的一种现象。和吸附现象类似的是,吸收也存在物理吸收和化学吸收两种情况。物理吸收——指的是溶解的气体与溶剂或溶剂中某种成分并不发生任何化学反应的吸收过程。此时,溶解了的气体所产生的平衡蒸汽压与溶质及溶剂的性质、体系的温度、压力和浓度有关。化学吸收——指的是当原子或者分子被吸收时所发生的化学反应。一个典型的例子就是当硫化氢从沼气流取出并转化成固体硫。Desorption解吸解吸是吸收的逆过程,又称气提或汽提,是将吸收的气体与吸收剂分开的操作。解吸是一种物质被另外一种物质释放的过程,或者也可以理解为一种物质从另外一种物质的表面或者穿过其表面而被释放出来的过程。当均衡情况发生改变时,解吸现象就会发生。想象一下,有一罐与周围环境相平衡的水,进入并离开这罐水的空气的量是相同的——水中氧气的浓度是恒定不变的。如果水温升高,水的平衡和溶解性发生变化,那么水中的氧气会被释放出来,因此水中氧气的含量降低。Adsorption and Desorption in Chromatography色谱法当中的吸附与解吸现象吸附和解吸是色谱法中的主要操作过程。通过待分离样本与固定相之间发生的吸附和解吸速率来实现样本的分离。如果色谱柱的条件有利于分子的吸附,那么分子就会附着在固定相上面,从而实现了与其他样本化学物质的分离。当色谱柱的条件有利于解吸,那么就会发生与吸附相反的现象——化学物质就会进入流动相当中。
请问专家,我用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定固体表面酸碱性(聚合物涂布在载体的表面做为固定相)AN(受电子数)和DN(给电子数)值,理论上讲,在进样量非常小时,保留时间与进样量是没有关系。当我用非极性溶剂作为探针分子,保留时间不随进样量变化,但是当我用极性溶剂做为探针注射入柱中,保留时间随着进样量的减少而变大,而我进的样足够小时,就会得到一个尾部拖得很长的峰,不能得到一个确定的保留时间,这样就没有办法计算出固体表面的AN和DN值。请问这是什么原因呢,是不是载体的吸附性造成的,载体硅烷化的效果不好?
各位不知道谁做过固体胶中苯,甲苯,二甲苯的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析,我想问下关于其前处理的问题,按照国标是用乙酸乙酯或NN-二甲基甲酰胺溶解,但我实际过程中无法用乙酸乙酯溶解固体胶,就算用NN-二甲基甲酰胺,也要在加热下才溶解,但一冷却发现有浑浊的东西,不知道哪位可以帮我想想办法?谢谢
[color=#444444]请问:我用的填充柱[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],FID检测器,固体固定相,如何才能测定其保留死时间呢,谢谢![/color]
蛋白质与色谱固定相之间的吸附为多位点吸附,什么叫多位点吸附?
重量法蒸汽吸附仪 产品简介重量法动态蒸汽吸附仪DVS系列在测量水和有机蒸汽在粉体表面吸附方面处于世界领先地位,它通过在一定相对湿度下气体通过样品后重量的变化来测定蒸汽吸附,比传统的干燥法测量更快,更节省时间。由于其独特的优势,DVS系列产品世界各地的实验室有广泛的应用,可用于研发部门以及质控部门确定产品结构、产品稳定性、吸湿性、包装和产品开发中固体材料存在的问题。结合了微天平、气体流动和蒸汽的测量技术的优势使用干燥的载气,通常为氮气,可以选择任何两个蒸汽源中的一个质量流量控制和独特的水和有机蒸汽浓度实时监控结合可以精确控制饱和干燥载气流量的比例整个体系的温度可以由选择,并且在闭合环条件下可以精确控制,以保证吸附质的蒸汽压恒定具有极其高的灵敏度和精确度,仅需少量的样品(通常1-30mg),因而可快速达到平衡全自动惰气吹扫装置和有机泄露检测器可在发生有机蒸气泄漏时关闭联锁装置,保证安全 DVS Advantage软件可程序控制仪器,用户界面友好,满足数据完整性和安全性的最高标准待测样品置于微量天平上,已知浓度的蒸汽通过样品,记录式微天平可以测量由蒸汽吸附或脱附引起的质量变化。这种动态流动环境易于快速研究吸附/脱附过程。如果进一步实验选择需要,样品可以首先预热,这样可以加速体相吸附或者无机氧化物干燥过程的分析循环时间。加热过程可独立进行或通过软件来控制升温速率。

[align=center][color=#333333]物理吸附法[/color][color=#333333]or BET[/color][color=#333333]法?[/color][/align][align=center][color=#333333]---[/color][color=#333333]浅析确定固体材料的比表面积、孔径分布等孔参数的实验方法的名称[/color][/align][align=center][color=#333333]丁延伟[/color][/align][align=center][color=#333333](中国科学技术大学理化科学实验中心,安徽省合肥市,[/color][color=#333333]230026[/color][color=#333333])[/color][/align][b][color=#333333]摘要:[/color][/b][color=#333333]气体吸附技术作为对固体材料的比表面积、孔径分布、孔隙度、表面性质等参数的分析的必备手段,在物理、化学、材料、生物、环境等学科中得到日益广泛的应用。[/color][color=#333333]BET[/color][color=#333333]法作为一种[/color][color=#333333]多分子层吸附理论,常用来计算固体材料的比表面积。[/color][color=#333333]本文介绍了物理吸附法和[/color][color=#333333]BET[/color][color=#333333]法的相关理论及应用,力图规范确定固体材料的比表面积、孔径分布等孔参数的实验方法的名称为物理吸附法。[/color][color=#333333] [/color][b][color=#333333]关键词:物理吸附,[/color][color=#333333]BET[/color][color=#333333]模型,比表面积[/color][/b][color=#333333] [/color][b][color=#333333]1. [/color][color=#333333]前言[/color][/b] 多孔材料由于其特殊的多孔性结构,使其具有高比表面积、高孔隙率、高透过性、高吸附性、可组装性等诸多优异的物理化学性能,因而在化工、生物医药、环保、功能材料等领域均有广泛应用[sup][/sup]。多孔材料的研究已成为当今材料科学研究领域的一大热点。多孔材料的研究离不开结构表征分析,多孔材料的孔隙结构特性主要包括孔径、孔径分布、孔形态、孔容积及孔通道特性等方面。多孔材料的孔隙结构是不规则的,孔穴尺寸在不同方向上存在着差异。多孔材料的这种各向异性状态,可以对其各项性能产生不同程度的影响[sup][/sup]。了解多孔材料的比表面积和孔隙形貌对研究其活性、吸附、催化、力学性能等都具有重要意义。多孔材料的表征方法很多,根据检测目的不同,一般可分为X射线小角度衍射法、气体吸附法、电子显微镜、压汞法、气泡法、离心力法、透过法、核磁共振法等。 气体吸附技术作为对固体材料的比表面积、孔径分布、孔隙度、表面性质等参数的分析的必备手段,在物理、化学、材料、生物、环境等学科中得到日益广泛的应用[sup][/sup]。气体吸附技术主要分为物理吸附和化学吸附两大类。通常使用物理吸附技术来确定固体材料的比表面积、孔径分布、孔隙度等信息[sup][/sup]。 然而,在许多已经公开发表的各种科研论文、专利等技术资料中通常对用来确定固体材料的比表面积、孔径分布等孔参数的实验方法的名称存在比较混乱的现象。例如,有些技术资料中称这种方法为BET法,而有的则称为比表面积测定法。本文试图从理论角度来规范这类方法的名称。[b]2.物理吸附相关理论[sup][/sup][/b] 通常将互不相混溶的两相接触所形成的过渡区域称为界面,吸附作用则发生在两相之间的界面上。吸附是物质(通常为固体物质)表面吸着周围介质(液体或气体)中的分子或离子现象,是一种传质过程。吸附质(adsorbate)通常定义为在界面上被吸附的物质,而吸附剂(adsorbent)则被定义为具备从[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]或者液相中吸附某些组分的能力的物质。吸附作用通常可以分为物理吸附与化学吸附。依靠分子间普遍存在的van der Waals力产生的吸附作用称为物理吸附,而由于吸附质分子与吸附剂发生化学作用产生的吸附称为化学吸附。 吸附质在吸附剂上的吸附量([i]x[/i])是绝对温度([i]T[/i])、气体压力([i]p[/i])或液体浓度([i]c[/i])和固体-气体之间的吸附作用势([i]E[/i])的函数,用式(1)表示。[img=,576,135]http://ng1.17img.cn/bbsfiles/images/2017/08/201708140959_01_2984502_3.jpg[/img] 对于给定的气-固体系,当温度[i]T[/i]保持恒定时,通常可认为吸附作用势[i]E[/i]保持不变。此时平衡吸附量[i]x[/i]只是压力[i]p[/i]的函数,该表达式得到的曲线通常称为吸附等温线(adsorptionisotherm)。同样的道理,当压力[i]p[/i]保持恒定时,吸附量[i]x[/i]与温度[i]T[/i]的关系曲线则称之为吸附等压线;当吸附量[i]x[/i]保持恒定不变时,[i]p[/i]与[i]T[/i]的关系则称为吸附等容线。[color=#333333] 物理吸附是由分子间的弱相互作用力所引起的吸附,由于该作用较弱,由此产生的吸附热较小,吸附和脱附速度也都较快。被吸附物质也较容易脱附下来,因此物理吸附是可逆的。例如分子筛对许多气体的吸附,被吸附的气体很容易解脱出来而不发生性质上的变化。[/color] 通常情况下,我们可以通过分析吸附体系的吸附等温线根据相关的理论模型来得到固体材料的比表面积、孔径分布、孔隙度、表面性质等参数。 实验上,利用专业的商品化的物理吸附仪或化学吸附仪,先将吸附剂在一定温度下以真空或吹扫气的形式对其进行彻底脱气,再在恒定温度下,控制吸附质与载气的分压,使吸附体系逐步达到平衡。这种通过控制吸附质分压与相应的平衡吸附量的关系所得到的实验曲线即为吸附等温线。 由于气体在固体表面的吸附状态多种多样,由此所得到的吸附等温线也不是一成不变的。2015年8月,国际化学领域最权威的国际纯粹与应用化学联合会(IUPAC)公布了最新的比表面积和孔参数分析的气体吸附分析规范[sup][/sup]。图1为物理吸附等温线的最新分类方法,实际由实验得到的各种吸附等温线大多是这六类等温线的不同组合。多年来,许多研究者对各类吸附等温线提出了许多吸附相互作用理论,并推导出了等温吸附公式,如Henry吸附式、Freundlich吸附式、Langmuir理论、BET吸附理论等,并依托于这些理论表征吸附剂的结构与成分,如比表面积、孔容积、孔径分布等,其研究深入到吸附作用的机理。[b]3. 气体吸附法测定比表面积与孔参数的基本原理[/b][color=#333333] 用于测量材料的物理吸附性质的仪器主要有容量法和重量法两种,其中以容量法更为常用。容量法测量物理吸附的仪器又分为流动法和静态法两种。本文主要介绍静态容量法仪器的工作原理及实验样品用量。[/color][color=#333333] 静态容量法由于待测样品是在固定容积的样品管中,吸附质相对动态法不流动。该方法测量是在等温(通常用液氮)条件下,向样品管内通入一定量的吸附质气体(通常为[/color][color=#333333]N[sub]2[/sub][/color][color=#333333]),通过控制样品管中的平衡压力直接测得吸附分压,由气体状态方程(通常为理想气体状态方程)得到该分压点的吸附量。测量过程中逐渐增加吸附质气体使吸附平衡压力逐渐变大,最终得到吸附等温线。通过逐渐吸附质气体被抽走来降低吸附平衡压力,得到脱附等温线(如图[/color][color=#333333]2[/color][color=#333333])。[/color][align=center][img=,494,383]http://ng1.17img.cn/bbsfiles/images/2017/08/201708141000_01_2984502_3.jpg[/img][/align][align=center][img=,494,383]http://ng1.17img.cn/bbsfiles/images/2017/08/201708141000_02_2984502_3.jpg[/img][/align][color=#333333] 根据所测得的吸附[/color][color=#333333]-[/color][color=#333333]脱附等温线可以判断吸附现象的本质,如属于分配(线性),还是吸附(非线性);测量吸附剂对特定吸附质的吸附容量;用于计算吸附剂的孔径、比表面、孔容积、孔形状等重要物理参数。[/color][color=#333333] 气体吸附法测定比表面积利用的是多层吸附的原理。其基本原理是测算出某种气体吸附质分子在固体表面形成完整单分子吸附层的吸附量,然后再乘以每个分子的覆盖面积即得到样品的总表面积。单位质量的吸附剂的总表面积([/color][color=#333333]m[sup]2[/sup]/g[/color][color=#333333])称为比表面积,它是表面积的常用表示方式。[/color][color=#333333]但是由于实际的固体表面并不是理想的二维平面,而是粗糙不平滑的。因此吸附法测得的表面积只是吸附质分子可以直接[/color][color=#333333]“[/color][color=#333333]接触[/color][color=#333333]”[/color][color=#333333]到的表面的面积,这一数值会因吸附质分子大小不同而发生变化。为了得到固体材料的真实有效的表面积,吸附质分子应该尽量小、接近球形而且对表面惰性。高纯氮气、氪气和氩气等气体都是适合的选择。其中,由于液态氮的价格便宜、容易高纯度获得,其在大多数表面上都可以形成典型的[/color][color=#333333] II[/color][color=#333333]、[/color][color=#333333]IV [/color][color=#333333]型吸附等温线,并且分子截面积已经得到了公认值,所以最为常用。气体吸附质分子在固体表面形成完整单分子吸附层的吸附量需要通过处理吸附等温线数据求出。[/color][color=#333333] 气体吸附法测定孔径分布利用的是毛细冷凝现象和体积等效交换原理,即将被测孔中充满的液氮量等效为孔的体积。[/color][color=#333333] 由于不同材料的孔结构大有不同,因此我们采用不同的数据处理方法与模型(如表[/color][color=#333333]1[/color][color=#333333])对不同情况下的孔结构进行具体处理[/color]。[align=center]表1 常用孔结构分析中的数据处理方法与模型[/align] [table][tr][td] [align=center]孔结构参数[/align] [/td][td] [align=center]数据处理方法或模型[/align] [/td][/tr][tr][td] [align=center]比表面[/align] [/td][td]BET, Langmiur(微孔), DR, BJT, DH[/td][/tr][tr][td] [align=center]中孔分布[/align] [/td][td]BJH, DH[/td][/tr][tr][td] [align=center]微孔分布[/align] [/td][td]DA(DR理论的扩展), HK, SF, MP[/td][/tr][tr][td] [align=center]微孔/中孔分布[/align] [/td][td]NLDFT[/td][/tr][tr][td] [align=center]微孔体积[/align] [/td][td]t-方法, DR(含平均孔宽,分子筛和活性炭等微孔表征)[/td][/tr][tr][td] [align=center]分形维数[/align] [/td][td]FHH, NK[/td][/tr][/table][b]4. BET理论[/b][color=#333333] BET[/color][color=#333333]理论是根据吸[/color]附等温线得到固体材料的比表面积的一种理论模型,最初是由三位美国学者S. Brunauer、P. Emmett和E. Teller于1938年提出的[url=https://baike.baidu.com/item/BET][color=black]BET[/color][/url]多分子层吸附理论,BET是三位科学家(Brunauer、Emmett和Teller)的首字母缩写。其数学表达式即BET方程。 推导BET方程所采用的模型主要做了以下基本假设:(1)吸附表面在能量上是均匀的,即各吸附位具有相同的能量;(2)被吸附分子间的作用力可略去不计;(3)固体吸附剂对吸附质气体的吸附可以是多层的,第一层未饱和吸附时就可由第二层、第三层等开始吸附,因此各吸附层之间存在着动态平衡;(4)自第二层开始[color=#333333]至第[/color][i][color=#333333]n[/color][/i][color=#333333]层([/color][i][color=#333333]n[/color][/i][color=#333333]→∞[/color][color=#333333]),各层的吸附热都等于吸附质的液化热。[/color][color=#333333] 我们可以通过热力学和动力学两种方法来推导[/color][color=#333333]BET[/color][color=#333333]方程,表达式如下:[/color][align=center][img=,675,272]http://ng1.17img.cn/bbsfiles/images/2017/08/201708141001_01_2984502_3.jpg[/img][/align][color=#333333] 由上式可见,当物理吸附的实验数据按[/color][color=#333333] [i]p[/i]/[i]v [/i]([i]p[/i][sub]0[/sub]-[i]p[/i])[/color][color=#333333]与[/color][i][color=#333333]p[/color][/i][color=#333333]/[i]p[/i][sub]0[/sub][/color][color=#333333]作图时应得到一条直线。直线的斜率[/color][i][color=#333333]m [/color][/i][color=#333333]= ([i]C[/i]-1)/([i]v[/i][sub]m[/sub][i]C)[/i],[/color][color=#333333]在纵轴上的截距为[/color][i][color=#333333]b[/color][/i][color=#333333]=1/([i]v[/i][sub]m[/sub][i]C)[/i][/color][color=#333333],所以以[/color][color=#333333]/V(P[sub]0[/sub]-P)[/color][color=#333333]对[/color][color=#333333]P/P[sub]0[/sub][/color][color=#333333]作图[/color][color=#333333],[/color][color=#333333]得一直线如图[/color][color=#333333]3[/color][color=#333333]所示。[/color][align=center][img=,534,396]http://ng1.17img.cn/bbsfiles/images/2017/08/201708141002_01_2984502_3.jpg[/img][/align][color=#333333] 根据直线的斜率和截距[/color][color=#333333],[/color][color=#333333]可求出形成单分子层的吸附量[/color][color=#333333]V[sub]m[/sub]=1/([/color][color=#333333]斜率[/color][color=#333333]+[/color][color=#333333]截距[/color][color=#333333])[/color][color=#333333]和常数[/color][color=#333333]C=[/color][color=#333333]斜率[/color][color=#333333]/[/color][color=#333333]截距[/color][color=#333333]+1[/color][color=#333333]。[/color][color=#333333] 根据[/color][i][color=#333333]V[/color][/i][sub][color=#333333]m[/color][/sub][color=#333333]由下式可以计算吸附剂的[/color][color=#333333]BET[/color][color=#333333]比表面积:[/color][img=,557,134]http://ng1.17img.cn/bbsfiles/images/2017/08/201708141002_02_2984502_3.jpg[/img][color=#333333] 需要指出,为满足以上假设[/color][color=#333333]BET[/color][color=#333333]方程的总有效区为相对压力在[/color][color=#333333]0.05~ 0.3[/color][color=#333333]之间。即便如此,[/color][color=#333333]BET[/color][color=#333333]方程还是不精确的,主要原因如下:([/color][color=#333333]1[/color][color=#333333])吸附剂表面吸附中心能量不均匀;([/color][color=#333333]2[/color][color=#333333])同一层中吸附质分子与相邻分子存在相互作用;([/color][color=#333333]3[/color][color=#333333])在大于[/color][color=#333333]1[/color][color=#333333]的多层吸附中,随吸附质远离吸附中心,相互之间作用力会减弱[/color][color=#333333]。[/color][b][color=#333333]5 [/color][color=#333333]结论[/color][/b] 测定多孔材料的孔结构,关键是通过正确的实验操作获得材料的吸附-脱附曲线,再利用合适的数据处理方法或模型获得相应的结构参数。通过以上分析我们可以清楚的看到,用来确定固体材料的比表面积、孔径分布等孔参数的实验方法的规范名称应为物理吸附法,由物理吸附法可以得到固体材料的比表面积、孔径分布、孔容积、分形维数、孔形状等更为丰富的信息,而BET法只是由吸附曲线中p/p[sub]0[/sub]在0.05-0.3之间的数据根据BET模型计算得到固体材料的BET比表面积。另外,BET法确定比表面积只是确定比表面积的其中一种方法。在实际工作中,我们不应该把这两种不同的方法混为一谈。[align=center]参考文献[/align]1. 徐如人,庞文琴,于吉红,等.分子筛与多孔材料化学.北京:科学出版社,2004:13.2. Stein, A. Wang, Z.Y. Fierke,M.A. Functionalization of porouscarbon materials with designed porearchitecture. Adv Mater, 2008, 20:1.3. Ajayan, V. Toshiyuki, M. Katsuhiko, A. New families of mesoporous materials, science and technology ofadvanced materials. Sci Techn Adv Mater, 2006, 10:1.4. Jianlin Shi*, “On thesynergetic catalytic effect of heterogeneous nanocomposite catalysts” , Chemical Reviews, 2013, 113 (3) 2139-21815. Stein, A. Wang, Z.Y. Fierke,M.A. Functionalization of porouscarbon materials with designed porearchitecture. Adv Mater, 2008, 20:1.6. Do D D, Adsorption analysis:equilibria and kinetics, Imperial College Press, 1998.7. Guiqing Lin, Huimin Ding,Daqiang Yuan, Baoshan Wang, and Cheng Wang, J. Am. Chem. Soc.2016, 138,3302-3305.8. Matthias Thommes, KatsumiKaneko, Alexander V. Neimark, James P. Olivier, Francisco Rodriguez-Reinoso, Jean Rouquerol and Kenneth S. W. Sing.Physisorption of gases, with special reference to the evaluation of surfacearea and pore size distribution (IUPAC Technical Report). Pure Appl. Chem.2015 87(9-10): 1051-10699. 甄开吉,王国甲,毕颖丽, 李荣生, 阚秋斌. 催化作用基础科学出版社,2005.
《环境空气 挥发性有机物的测定 吸附管采样热脱附/气相色谱-质谱法》(征求意见稿)大家看看,新标准有什么问题?
指直接装填到色谱柱中作为固定相的具有活性的多孔性固体物质。固体固定相大体可分为二类:第一类是吸附剂。如:分子筛、硅胶、活性炭、氧化铝等;第二类是高分子聚合物。如国内的GDX型高分子多孔微球,国外Porapak系列等;第三类是化学键合固定相。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中,通常是将固定液涂敷在载体表面上。采用化学键合固定相分析极性或非极性物质通常都能够得到对称峰,柱效很高,固定相的热稳定性也有所改善。
[size=5]超临界流体色谱法测定固体在二氧化碳中的溶解度[/size] 来源: 作者:赵锁奇,杨光华,王仁安摘要:开发了一种测定超临界二氧化碳中大分子溶质的溶解度的方法 这一方法将微型超临界流体萃取(Micro-SFE)直接与超临界色谱(SFC)相耦合.超临界流体色谱采用FID作为检测器,实验中两者具有阿一压力、温度及同样的CO流速。使用了模型溶质萘、联苯和菲来验证此方法,井得到了温度在308~330K.压力8.0~12.0MPa间溶质的等压溶解度曲线,实验结果与文献值相符,定量显示了在溶剂近临界区域固体/超临界流体二元系的相平衡特性 这一方法适用于重溶质在CO2中溶解度的测量。关键词:固体;溶解度;二氧化碳;超临界流体萃取;超临界流体色谱l 前 言近二十年不少研究者发表了相当数量的超临界流体中不同固体的平衡溶解度数据,常用模型化合物来考察温度、压力和超临界流体的密度对溶解度的影响.并用以建立超临界流体相平衡的理论。二氧化碳因其不可燃、无毒且价格低廉的特性成为最为常用的溶剂,而且二氧化碳有相对低的临界温度(31.2℃)和临界压力(72.9atm),显然有利于热敏性物质的分离。Francis测定过25℃下近临界二氧化碳中数百种溶质的溶解度.Tsekhanskaya等测定了超临界二氧化碳中固体萘的溶解度。McHugh发表了超临界CO2中萘和联苯的溶解度数据,Kurnik ,Schmitt和Reid则测定了包括CO2在内的超临界流体中数种有机化合物的溶解度数据。他们的工作中所用的仪器主要为中型的动态超临界流体萃取器。King,McHugh对超临界流体相平衡的静态和动态测定方法作了详细的评述。Bruno综述了溶质溶解度的四种测定方法,即动态流动法、静态(平衡)法、色谱溶解度法和光谱法。超临界流体色谱使用超临界流体作为流动相,起源于六十年代,自八十年代中期开始得到迅速发展,但主要是用于分析工作。八十年代超临界流体色谱开始用于测定热力学性质,如两相中溶质的偏摩尔体积和偏摩尔焓、固定相与流动相之间溶质的分配系数Staeh使用超临界流体萃取和薄层色谱来测定超临界流体中固体的溶解度,这对测定溶解度的压力闽值并获得密度变化对溶解度的影响的定性说明,无疑是有益的Saito和Skelton等报道了直接耦合的超临界流体萃取/超临界流体色谱,这一类系统使用紫外检测器,利用紫外吸收来测定复杂物质的溶解度,对无紫外吸收的溶质就显得无能为力了。Smith等将毛细管超临界流体色谱与质谱联合用于测定溶液中溶质的量,这种方法可以对宽范围的固体样品作出较快的测量,但难于用于液体样品。Battle等作了若干超临界流体色谱中溶质的保留机理的假设,以此为基础测定了固体芳烃的溶解度。相对于中型的超临界流体萃取来说,微型超临界流体萃取具有一定的优越性,如它便于建造和操作,所用样品量少.操作费用低,而且可以直接与分析仪器相衔接.如紫外、红外、核磁共振仪、质谱等.所用操作时间少。本文的目的是发展一种直接测定大分子固体或液体在超临界流体CO2中溶解度的新方法,该方法应较为简便地确定稀溶液范围内的定量结果。研究中建立了将超临界流体微萃取与超临界流体色谱系统直接连接到氢离子火焰检测器(FID)的实验装置,之所以选择氢离子火焰检测器是因为它是一种通用型宽线性范围的检测器,比起其它检测器.如TLC和紫外检测器,它有较高的灵敏度。实验选择了萘,联苯和菲作为模型化合物来验证方法的可靠性并研究这三种溶质-二氧化碳体系在超临界区的相平衡特征。
热解固体同时产生氨气、SO2、H2O、N2,我应该用那种吸附管啊?热解吸仪能用氢气做载气吗?吸附管都有什么种类啊?空白吸附管是什么啊?求大神解答啊
气体吸附法是测量材料比表面积和孔径分布的常用方法。其原理是依据气体在固体表面的吸附特征,在一定的压力下,被测样品表面在超低温下对气体分子可逆物理吸附作用,通过测定出一定压力下的平衡吸附量,利用理论模型求出被测样品的比表面积和孔径分布等与物理吸附有关的物理量。其中氮气低温吸附法是测量材料比表面积和孔径分布比较成熟而且广泛采用的方法。在液氮温度下,氮气在固体表面的吸附量取决于氮气的相对来说压力表(P/P0),P为氮气压力表,P0为液氮温度下氮气的饱和蒸气压,当P/P[0在0.05-0.35范围内时,吸附量与相对压力P/P0符合BET方程,这是氮吸附法测定比表面积的依据;当P/P0符合BET方程,这是氮吸附法测定比表面积的依据,当P/P0≥0.4时,由于产生毛细凝聚现象,氮气开始在微孔中凝聚,通过实验和理论分析,可以测定孔容-孔径分布(孔容随孔径的变化率)。 比表面积是多孔材料、超细粉体材料和催化剂的最重要物性之一。有两种常用的表示方法:一种是单位质量的固体所具有的表面积(m2/g),表示为 Sg=S/m 另一种方法是单位固体具有的表面积(m2/m3),表示为Sv=S/V式中:m-被测样品质量(g); V-被测样品体积(m2). 一般多用第一种方法来表示比表面积,计算比表面积的一般BET公式。假设Vd为吸附量(体积),Vm为单分子层的饱和吸附量,P/P0为N2的相对压力,C为第一层吸附热与凝聚热有关常数,P0为饱和蒸气压,W为样品质量,则BET公式为P/Vd(P0-P)=1/VmC+(C-1)/P/P0式中,P/P0一般选择相对压力在0.05-0.35范围内,仪器可以测得dV值。如果只需要的比表面积,就可以只选P/P0=0.05-0.35之间5点进行测量就可以了,也就是通常所说的五点法确定比表面积。
实验室测试苯,甲苯,二甲苯。MA证书写采用的标准是:1.热脱附进样吸附-气相色谱法《空气和废气监测分析方法》(第四版) 国家环保总局2003年第六篇第二章一(二) 2.环境空气 苯系物的测定 固体吸附热脱附气相色谱法 HJ 583-2010可这两个标准中都没有提到吸附管用的是活性炭。实验室人员说是参照其它实验室的方法。故:采用活性炭,不用标准中的TENAX的理由是什么?