推荐厂家
暂无
暂无
 金牌4年
金牌4年
 400-860-5168转4814
400-860-5168转4814
 留言咨询
留言咨询
 白金7年
白金7年
 400-803-1558
400-803-1558
 留言咨询
留言咨询
 钻石21年
钻石21年
 400-687-1226
400-687-1226
 留言咨询
留言咨询

 400-805-0826
400-805-0826
 留言咨询
留言咨询

 400-628-5299
400-628-5299
 留言咨询
留言咨询

 400-860-5168转2623
400-860-5168转2623
 留言咨询
留言咨询







[img=,500,95]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021007141220_851_981_3.jpg!w690x132.jpg[/img]1 普通共聚焦(左半部分)和STED超分辨(右半部分)检测DNA蛋白互作效果对比。(5nM TFAM 647N,恒力4pN)[b]STED 超分辨[/b]单分子水平定量分析DNA与蛋白的相互作用要求技术水平达到在复杂的生物微环境中保证超高的时间分辨率。这种体内复杂的生物学反应尤其常见于在体外模拟体内实验,比如高浓度的蛋白与不断变化的DNA相互作用。采用受激发射损耗显微技术(STED)能够实现快速对复杂的DNA进行高分辨的扫描。LUMICKS公司研发的SuperC-Trap™ 技术结合STED,能够实现高分辨率可视化的研究多蛋白结合的DNA反应动力学。Figure 1 显示实时观测荧光标记的高浓度(大约 5nM)TFAM转录因子与λ-DNA的相互作用。SuperC-Trap™ 采用光镊技术原位拉直DNA,然后结合STED技术高分辨率(≥50 nm)高频率(≤200 Hz)线性追踪TASM的动态变化。STED 能够实现对单个结合或非结合、寡聚化蛋白基团的实时追踪(Figure 1, 右半部份)。然而利用共聚焦显微镜却分辨不出来 (Figure 1,左半部分)。共聚焦的点状激发原理决定了其只能追踪分布密度比较高的蛋白分子的动态变化,却不能进行广角扫描。而且采用共聚焦技术位置比较相近的两种蛋白也很难被分辨。但是利用STED的受激发射损耗技术可突破衍射极限,可以轻易分辨两种相邻蛋白。[img=,500,111]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021023463820_3909_981_3.png!w690x154.jpg[/img]2 光镊技术(红色部分)结合共聚焦技术(绿色部分)模式图,多激发模式。[img=,500,103]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021024169794_3597_981_3.png!w690x143.jpg[/img]3 光镊技术(红色部分)结合STED超分辨技术(黄色部分)模式图,单激发模式。[img=,500,198]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021025123269_5345_981_3.png!w535x212.jpg[/img]4 共聚焦 (左) 和超分辨率显微镜STED (右)分辨率对比。647N-标记的结合DNA的限制性内切酶。5 共聚焦(蓝色)和超分辨率显微镜STED(红色)对两个相邻蛋白的分辨率对比。[b]SuperC-Trap[/b]共聚焦显微镜和超分辨显微镜的区别很明显。从Figure 4中可以看出超分辨显微镜能够清晰的将两种相邻蛋白分辨出来,而共聚焦的分辨率并不能达到。这种对比明显的说明了超分辨在精确定位上的优势。LUMICKS公司的SuperC-Trap不仅能够实现实时超分辨可视化的观察,而且还可以在亚pN水平、亚nm分辨率监测分子间的相互作用。结合我们的超稳定液流系统和独立的整合软件,使得整个实验在数分钟之内就能完成。
不知道论坛中有没申请山东省CMA 的xdjms?有个表中涉及到所用仪器的分辨力/率的问题。培训的老师讲是仪器设备的最小刻度值。我想跟大家讨论一下理化检测用的分析仪器的分辨率。在《质量专业综合知识》中有写明:对于数字式显示装置,其分辨力为末位数字的一个数码。我们的万分之一的电子天平,技术指标中的分辨力为:0.1mg,pH计技术指标的分辨力为:0.01(仪器显示到0.01)至此,我们可以认为仪器能读到的最小示值就是分辨力么?紫外,原子吸收,我们都是定波长看其吸光度,通过吸光度计算物质含量,那么仪器吸光度示值达到0.001,就认为分辨力为0.001么?懂仪器的可能知道对于光谱仪器来说,光谱带宽代表仪器的分辨力,我问过我们紫外的供应商,他说我可以直接写明光谱带宽是多少就行。此外,我们还有凯氏定氮仪,仪器显示的含氮量可以达到0.0001%,那它的分辨力就是0.0001%?还有滴定管,是不是分辨力为0.1mL?(还是因为它是带刻度的,为最小刻度值的一半?)现在我们的仪器大都是可以直接输出数据的吧?可以把它们称作数字式显示装置么?对于《质量专业综合知识》中有这样的说法:显示装置能有效辨别的最小的示值差,称为显示装置的分辨力,或简称为分辨力。它是指显示装置中对其最小示值的辨别能力。模拟式显示装置的分辨力,通常为标尺分度值的一半,即用肉眼可以分辨到一个分度值的1/2。数字式显示装置,其分辨力为末位的一个数码。对半数字式的显示装置,其分辨力为末位数字的一个分度。大家如何理解的?有论坛指出:“用标尺作为读数装置(包括带有光学机构的读数装置)的测量仪器分辨力,为标尺上任何两个相邻标记之间即最小分度值的一半。打个比方:指针式的百分表(0.01mm分度),分辨力为0.005mm数显式的百分表(0.01mm最末位),分辨力为0.01mm”我只想知道该填写什么样的数值,涉及到理论知识的最好大家可以举个例子。呵呵,有点长,希望我们可以讨论明白,谢谢了!
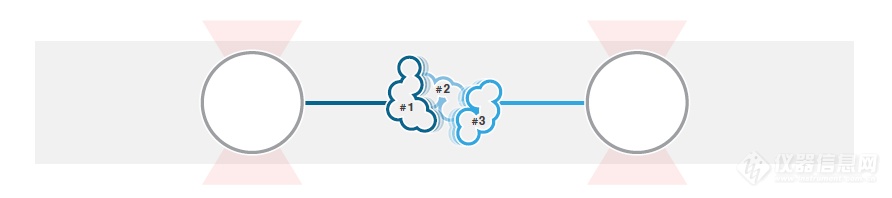
[b]研究多结构域蛋白阶段性去折叠[/b]很多生物大分子的功能与其构象和构象动力学密切相关,如蛋白质的生物功能需要其正确折叠成自然形态。错误折叠或者未折叠的蛋白会(部分)失活或者产生毒性,如错误折叠的蛋白与神经退行性疾病有关。研究蛋白如何正确折叠并改变构象以实现生物功能对理解其机制与疾病发生至关重要。单分子力谱(SMFS)是研究这些分子现象的理想工具,因为其具有独特的分离个体生物分子和实时观察构象变化及去折叠过程的功能。由于SMFS具有高敏感度和施加机械力的能力,可以直接操纵单个蛋白并通过测量其长度变化(亚nm级)观察构象改变。接下来我们使用LUMICKS开发的高分辨率光镊-荧光显微镜C-Trap演示了对钙调蛋白(CaM)的折叠过程的研究。[img=,500,110]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021105519876_1986_981_3.png!w690x153.jpg[/img][img=,218,200]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021106425366_604_981_3.png!w217x199.jpg[/img]1 多结构域蛋白的去折叠实验图解。具有3个结构域的蛋白通过DNA连接至两个被光所捕获的微球。2 通过改变光阱之间的距离可以对蛋白施力并检测断裂的发生。使用层流微流控和自动装载功能,N-端和C-端连接有DNA的单个CaM蛋白可被两个微球捕获(图1)。[img=,227,200]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021108116955_1942_981_3.png!w220x193.jpg[/img]3 10 mM Ca2+浓度下CaM的力-拉伸距离(蓝色)和力-收缩距离(红色)。拉伸与收缩的速度为100 nm/s。微球直径为1.0 μm,光阱的刚度为0.284 pN/nm。[img=,500,161]http://ng1.17img.cn/bbsfiles/images/2018/08/201808021108223351_3734_981_3.png!w638x206.jpg[/img]4 10 mM Ca2+浓度下CaM的多个状态下的动态平衡。图为50 kHz(灰色)和200 kHz(红色)下记录的数据。在右侧直方图中可以看到两个清晰的峰即表现为蛋白最常处于的两个状态。第一个实验,在10 mM Ca2+条件下对CaM的机械拉伸与收缩行为进行了记录。首先对100 nm/s的速度下的拉伸与收缩的相关数据进行了记录(图3)。随着施加的力增加,可观察到两个去折叠的阶段,表现为力的突然下降,与两个螺旋-环-螺旋结构域的去折叠相符合。由此可以得出结论,基于C-Trap设备的力和距离的高分辨率(100 Hz时误差在0.2 pN以下和0.5nm以下),去折叠的发生可以用力谱的力-距离曲线来确定。这种测量非常适合用于比较正常蛋白与发生了改变或损伤的蛋白的折叠的相关数据。接下来研究光阱位置固定时CaM的折叠、去折叠的动态平衡,对蛋白长度的变化进行测量并确定中间态的转变(图4)。对CaM分子施加7.5 pN的力,可以观察到三种状态之间的波动,反映了螺旋-环-螺旋亚结构域的折叠和去折叠,波动的数据图像与之前的研究1,2相符(图4)。仪器所获得的稳定的高质量数据为蛋白的折叠和去折叠之间的动态转变的检测提供了大量有效的信息。通过这种方法可以对不同状态的驻留时间和转变动力学进行测量。这些信息使得我们对特定蛋白的折叠、去折叠过程产生进一步的了解。对折叠和去折叠的动力学以及构象改变的研究表现了一种突破性的生物学和生物物理学研究方法。使用C-Trap光镊-荧光技术可以观察到折叠和去折叠现象还有动态平衡,使得科研人员可以研究去折叠的中间态并获得蛋白的结构与功能信息。对蛋白折叠和构象的进一步研究仰仗于C-Trap的高敏感度和多通道荧光单分子FRET功能,通过检测FRET效率信号与力的波动的变化来进一步检测蛋白构象,可以得到蛋白的机械性质与结构之间的关系。[b][/b]